Papiloma Invertido, importancia de la Tomografía Computarizada y Resonancia Magnética en el diagnóstico y extensión
Papiloma Invertido, importancia de la Tomografía Computarizada y Resonancia Magnética en el diagnóstico y extensión
Revista Ciencia Unemi, vol. 11, núm. 26, pp. 150-160, 2018
Universidad Estatal de Milagro

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.
Recepción: 02 Octubre 2017
Aprobación: 10 Febrero 2018
Resumen: Demostrar la importancia de la Tomografía computarizada (TC) y Resonancia Magnética (RM) en el diagnóstico, extensión y seguimiento de los pacientes con papiloma invertido (PI). Paciente femenino de 64 años, con antecedentes de sinusitis alérgica recurrente, que consulta por obstrucción nasal bilateral a predominio izquierdo, asociada a rinorrea purulenta y rinolalia de cinco meses de evolución. Se le realiza TC y RM de Macizo Cráneo facial (MCF). La TC demuestra formación de densidad de partes blandas ubicada en fosa nasal y seno maxilar derecho que se extiende hacia celdillas etmoidales bilaterales, seno frontal y seno esfenoidal derecho. La RM evidencia lesión expansiva sólida ubicada sobre seno maxilar derecho, que se extiende excavando la pared interna del mismo hacia fosa nasal homolateral. El PI es una neoplasia nasal que se caracteriza por su crecimiento invertido hacia el estroma. Es un tumor benigno que presenta una incidencia anual del 1 % promedio por cada 100.000 habitantes. La TC es el método imagenológico de elección para el diagnóstico de PI, siendo también útil en la valoración de la extensión en la fase preoperatoria. El diagnóstico de certeza lo determina la histopatología. La RM representa un método de gran utilidad en el seguimiento postoperatorio.
Palabras clave: Papiloma invertido, tomografía, resonancia, clasificación de Krouse.
Abstract: Demonstrating the importance of Computed Tomography (CT) and Magnetic Resonance (MRI) in the diagnosis, extension and follow-up of patients with inverted papilloma (IP) of a 64-year-old female patient with a history of recurrent allergic sinusitis who consults for bilateral nasal obstruction and left predominance associated with purulent rhinorrhea and rhinolalia of five months of evolution. CT and MRI of CranioFacial Massif (CFM) were performed. CT demonstrated soft tissue density formation located in the nasal fossa and right maxillary sinus extending to bilateral ethmoidal cells, frontal sinus and right sphenoid sinus. MRI showed solid expansive lesion located on the right maxillary sinus, extending through its inner wall to the homolateral nasal fossa. IP is a nasal neoplasm that is characterized by its inverse growth towards the stroma. It is a benign tumor that presents an annual incidence of 1% average per 100,000 inhabitants. CT is the imaging method of choice for the diagnosis of IP, and it is also useful in assessing extension in the preoperative phase. A thorough diagnosis is determined by histopathology. MRI represents a very useful method in postoperative follow-up.
Keywords: Inverted papilloma, tomography, resonance, Krouse classification.
I. INTRODUCCIÓN
El PI es una neoplasia nasal rara. “Es un tumor benigno del epitelio schneideriano de las vías aéreas superiores con una incidencia de 0,6/100.000 personas al año” (Di Pietrantonio, y otros, 2018), “que puede sufrir una transformación maligna a carcinoma epidermoide” (Uzun, Ozkanli, Kalcioglu, & Kokten, 2017).
Actualmente se determinó que corresponde a “una degeneración metaplásica severa de la mucosa que crece hacia el estroma subyacente, que resulta difícil de diferenciar del carcinoma escamoso de bajo grado” (Salazar Guilarte, Paredes Osado, Barberá, & Gras Albert, 2011); (Llorente Pendás, Suárez Fente, & Suárez Nieto, 2007) y no de un papiloma como tal.
Se ha categorizado en tres tipos: PI benigno, PI con displasia y/o carcinoma in situ, y PI con carcinoma de células escamosas. “El carcinoma escamoso sinonasal representa <1% de todas las neoplasias malignas, pero representa el 70% del cáncer nasosinusal. Hasta el 10% de los SCC están asociados con el papiloma invertido” (Lobo, y otros, 2017) .Su etiología es incierta, no obstante existe una fuerte asociación con el Virus del Papiloma Humano (VPH) 16 y 18 (Tejero Garcés, y otros, 2017). La probabilidad de trasformación maligna es muy alta (mayor al 70 %) (McKay, y otros, 2005).
“La desmogleina 3que está presente en 90% de los carcinomas escamoso celulares, también se ubica en determinadas áreas del PI (53%)” (Huang, y otros, 2010), por lo cual su hallazgo debe considerarse como factor de probabilidad de transformación (Burke Haywood, Fuller, Gerhard, Olobatuy, & Clark, 2017)maligna.
Su frecuencia es mayor en pacientes ancianos y predomina en varones (4:1). “El síntoma más común es la obstrucción nasal unilateral, también pueden presentarse síntomas como epistaxis, rinorrea, dolores o presiones faciales, cefaleas, anosmia, epifora, diplopía y otalgia” (Weissler, Montgomery, & Montgomery, 1986).
Al examen físico el PI se presenta como una lesión polipoidea unilateral blanquecina o transparente de aspecto edematoso y consistente.
La localización más frecuente es la fosa nasal en la zona del cornete medio (95%), con posibilidades de extensión a la coana (38%) y al Cavum (23%). La segunda es el seno maxilar con expansión a las celdillas etmoidales (57.1 %), también es frecuente la erosión ósea con destrucción de la pared medial del seno maxilar. El seno esfenoidal es una de las localizaciones menos frecuente (9,5%) (Bernardo, Hernández, Calvo, Llorente, & Gómez, 2001).
Ante la sospecha clínica de la presencia de un PI, es necesario complementar con estudio histopatológico, remitiendo un amplio fragmento de la pieza con el fin de descartar la presencia de focos de malignidad
El objetivo de este trabajo es demostrar que la Tomografía Computarizada (TC) y la Resonancia Magnética (RM), permiten realizar diagnóstico presuntivo del PI; valorar la extensión de la lesión antes de la cirugía, delimitar el tejido inflamatorio circundante mediante la captación de contraste y las secuencias correspondientes.
II. DESARROLLO
1. Materiales y métodos
-
- Se realizó un estudio de tipo descriptivo – bibliográfico con la revisión de artículos y publicaciones desde el 1990 hasta la fecha, tomando en consideración datos anatomopatológicos y clínicos con su respectiva estadificación según el clasificación propuesta por Krouse (2000).
- Se presenta el análisis descriptivo del caso, valorando una paciente femenina de 64 añoscon antecedentes de sinusitis alérgica recurrente, que consulta por episodios de obstrucción nasal bilateral a predominio izquierdo, asociado a rinorrea purulenta y rinolalia de cinco meses de evolución, presentando en la actualidad deformidad facial.
- Se le realiza TC y RM de MCF.
2. Discusión
El diagnóstico presuntivo del PI se basa en la anamnesis, la historia clínica, la edad del paciente, examen otorrinolaringológico, incluyendo endoscopia nasal.
Las características de la imagen tanto en la TC como la Resonancia Magnética (afectación ósea, morfología, localización) tienen vital importancia para la valoración del tamaño y la delimitación de la extensión de la lesión antes de la cirugía, diferenciándola del tejido inflamatorio circundante, mediante la captación del medio contrastado y la determinación del patrón típico columnar que es evidenciable en la RM potenciada en T2 o a través de los signos radiológicos osteolíticos que se aprecian en la TC, no obstante esta no es suficiente para confirmar el diagnóstico de PI, debido a que también puede manifestarse en hasta el 53% de pacientes con sinusopatia crónica (Ahumada, Cajade, Milá de la Roca, Santos, & Pereira, 2015).
El método imagenológico de elección en el diagnóstico del papiloma invertido es la TC, que permite documentar la presencia de erosión ósea que es altamente sugestiva de malignidad, así como otros signos típicos de papiloma como los focos de calcificación intratumorales o la hiperostosis focal del hueso adyacente, que sugiere el punto de origen del tumor (Buchwald, Nielsen, Ahlgren, Nielsen, & Tos, 1990).
El diagnóstico diferencial de papiloma invertido y otras masas de la fosa nasal es de difícil determinación, siendo necesaria las mediciones densitométricas tomográficas. Los valores densitométricos de la masa en las adquisiciones en nuestro paciente sin contraste se encuentran entre 55 - 60 UH y posterior a la infusión del contraste oscila entre 70 - 80 UH; el cornete medio presenta densidades entre 40 - 45 UH, mientras que las secreciones mucosas muestran valores entre 25 - 40 UH. Si bien estos realces no son específicos para realizar el diagnóstico de papiloma invertido, podrían ser de utilidad para la valoración de la extensión del mismo (Figura 1 – 2).
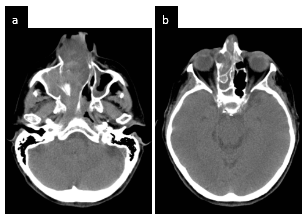
Figura 1
TC sin contraste endovenoso. Cortes axiales. Imagen con densidad de partes blandas con extensión a seno maxilar y celdillas etmoidales (a y b).
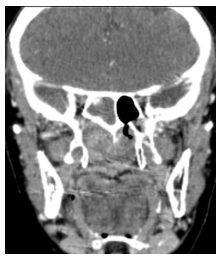
Figura 2
TC sin contraste endovenoso. Corte coronal. Extensión a hemiseno esfenoidal derecho.
Se considera que las estructuras óseas encontradas se deben a restos de celdillas etmoidales y cornetes embebidos en el seno de la masa tumoral. “La localización en zonas como el seno frontal, las celdillas etmoidales supraorbitarias o la región periorbitaria, contraindican la cirugía por vía endoscópica” (Bernardo, Hernández, Calvo, Llorente, & Gómez, 2001); (Aderito, Urdaneta Lafée, Abreu-Durán, & Rodríguez-Hernández, 2017).
La RM de alto campo es un método de vital importancia en el diagnóstico y seguimiento de estos tumores. Los estudios realizados con gadolinio presentan sensibilidad y especificidad del 100% en el diagnóstico de recidivas, diferenciándolas de tejidos fibroticos y de granulación. Un signo radiológico, evidenciado en RM, consiste en un patrón de disposición cerebriforme con los estudios potenciados en T2 y con gadolinio muy similar a la presentación histopatológica del PI.
El PET TC no es recomendable debido a que no distingue de de forma confiable el papiloma invertido del carcinoma.
Debido a la existencia de lesiones multifocales (4% de los casos), es conveniente siempre descartar la presencia de otras lesiones.
Existen diferentes sistemas de clasificación, que se basan en el volumen de la lesión y el origen de su pedículo. En algunos casos se ha buscado una clasificación que correlaciona la localización de la lesión con la planificación operatoria. Una de las más utilizadas es la descripta por Krouse.
| CLASIFICACIÓNDEKROUSE | |||
| Tipo 1 | Tipo 2 | Tipo3 | Tipo4 |
| Ubicación exclusiva en topografía de la cavidad nasal. | Compromiso de los sectores superior y medial de seno maxilar, celdillas etmoidales y/o complejo osteomeatal | Compromiso de los sectores lateral e inferior de seno maxilar, con eventual extensión a los senos esfenoidales o frontal | Infiltración extranasal o fuera de los senos paranasales con invasión de tejidos circundantes, o con transformación maligna agregada |
En la paciente de 64 años de edad, de este estudio, se puede decir que el estadio correspondiente es tipo 4 y los hallazgos radiológicos fueron:
En la Tomografía sin contraste del macizo cráneo facial se aprecia formación de densidad de partes blandas ubicada en fosa nasal y seno maxilar derecho con extensión a senos frontales y celdillas etmoidales, la formación hace protrusión hacia las coanas y Cavum con marcado realce postcontraste (Figura 3).
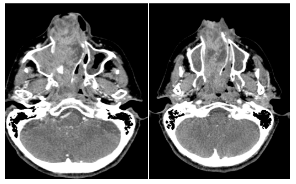
Figura 3
TC de MCF con contraste endovenoso. Cortes axiales.Protrusión hacia las coanas y Cavum con marcado realce postcontraste (a y b).
En la ventana ósea se destacan signos de marcada remodelación ósea predominantemente de los senos maxilar derecho y fosa nasal (Figura 4).
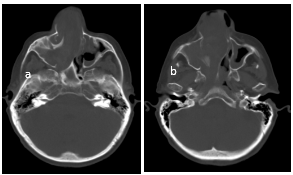
Figura 4
TC ventana ósea. Cortes axiales. Marcada remodelación ósea, predominantemente en fosa nasal y seno maxilar derecho (a y b).
Se considera que las estructuras óseas encontradas se deben a restos de celdillas etmoidales y cornetes embebidos en el seno de la masa tumoral. “La localización en zonas como el seno frontal, las celdillas etmoidales supraorbitarias o la región periorbitaria, contraindican la cirugía por vía endoscópica” (Bernardo, Hernández, Calvo, Llorente, & Gómez, 2001); (Aderito, Urdaneta Lafée, Abreu-Durán, & Rodríguez-Hernández, 2017).
En RM, secuencia en T1, la lesión se observa hipo-isointensa y se proyecta desde orificio nasal hasta Cavum y coana, con aspecto de lesión solida expansiva ubicada sobre seno maxilar derecho que se extiende alrededor de la pared interna del seno nasal hacia la fosa nasal homolateral y se proyecta hasta senos frontales y presenta erosión de la lámina papirácea (Figura 5 – 6 – 7).
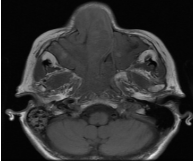
Figura 5
RMN de MCF. Secuencia T1 serie sin contraste endovenoso. Corte axial. Lesión expansiva sólida ubicada sobre seno maxilar derecho, que se extiende rodeando la pared interna del seno maxilar hacia fosa nasal homolateral.
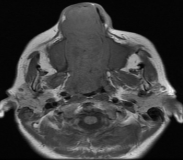
Figura 6
RMN de MCF. Secuencia T1 serie sin contraste endovenoso. Corte axial. La lesión se proyecta desde orificio nasal hasta Cavum y coanas.
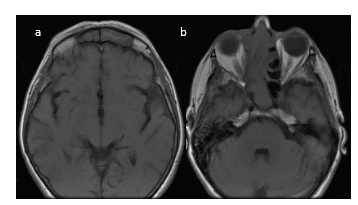
Figura 7.
RMN de MCF. Cortes axiales. Extensión hasta senos frontales y erosión de la lámina papirácea (a y b).
En secuencia T2 sin contraste, la lesión presenta áreas hiperintensas y de baja señal, determinando marcado desplazamiento del tabique nasal y oblitera trompa de Eustaquio derecha, con ocupación de celdillas mastoideas y oído medio homolaterales (Figura 8–9-10).
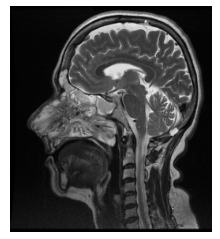
Figura 8
RMN de MCF. Secuencia T2 serie sin contraste endovenoso. Corte sagital. Extensión a senos paranasales, fosas nasales, Cavum y coanas.
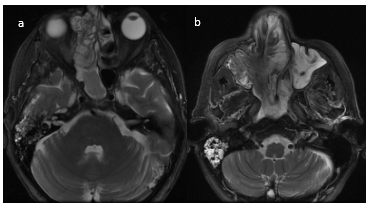
Figura 9
RMN de MCF. Secuencia T2 serie sin contraste endovenoso. Cortes axiales. Lesión de partes blandas, con áreas de señal hiperintensa y de baja señal. Determina marcado desplazamiento del tabique nasal, obliterando trompa de Eustaquio derecha, con ocupación de celdillas mastoideas y oído medio homolaterales.
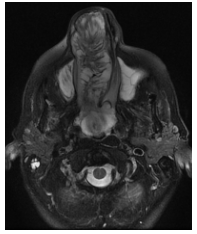
Figura 10
RMN de MCF. Secuencia T2 serie sin contraste endovenoso. Corte axial.
En RM con contraste la lesión presenta un realce intenso al gadolinio (Figura 11 – 12 – 13).
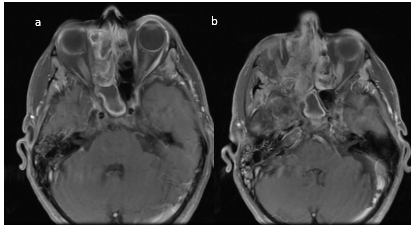
Figura 11.
RMN de MCF. Secuencia T1 serie con contraste endovenoso. Cortes axiales (a y b). Figura 12. RMN de MCF. Secuencia T1 serie con contraste endovenoso. Corte axial. Se observa realce postcontraste. Figura 13. RMN de MCF. Secuencia T1. Serie con contraste endovenoso. Cortes coronales (a y b). Importar tabla
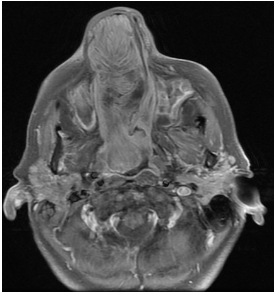
Figura 12.
RMN de MCF. Secuencia T1 serie con contraste endovenoso. Corte axial. Se observa realce postcontraste.
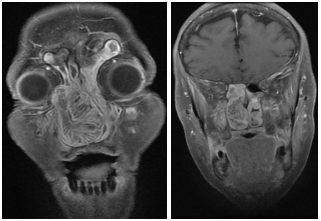
Figura 13.
RMN de MCF. Secuencia T1. Serie con contraste endovenoso. Cortes coronales (a y b).
III. CONCLUSIÓN
La TC preoperatoria es de vital utilidad para evaluar la extensión de las lesiones, no obstante el examen histopatológico es determinante en el diagnóstico de certeza del PI.
Existen elementos altamente sugestivos que en conjunto generan sospecha diagnostica de PI como lo son:
· La signo-sintomatología de insuficiencia ventilatoria secundaria a obstrucción nasal en un paciente adulto.
· Hallazgos tomográficos consistentes con formación de densidad de partes blandas, de localización unilateral, que ante la infusión de medio de contraste presenta moderado realce, ubicada en topografía del cornete medio.
· Que presente o no extensión al seno maxilar homolateral y muestre signos de remodelación ósea.
· Que mencionados hallazgos se asocien a lobulación de sus contornos.
Cabe recalcar que la valoración de la extensión de la lesión antes de la cirugía, a través de los métodos imagenológicos como la TC y RMN mediante la captación de contraste y las secuencias correspondientes, permiten determinar los límites de las estructuras anatómicas con tejido inflamatorio circundante, esta última no es suficiente para asegurar el diagnóstico de PI, porque puede estar presente hasta en 53% de pacientes con sinusitis crónica. El diagnóstico de certeza de papiloma invertido se obtiene mediante el estudio histopatológico.
La elevada frecuencia de recidivas, es un motivo por el cual se debería utilizar la TC como una técnica de gran importancia para valoración de la evolución, focalizando la evaluación del sitio original de ubicación del tumor primitivo previo a la extirpación del mismo con especial atención a la zona de la que se extirpó la lesión.
La RM de alto campo con gadolinio es una excelente alternativa en el diagnóstico de recidivas.
REFERENCIAS
Aderito, D. S.-F., Urdaneta Lafée, N., Abreu-Durán, P. A., & Rodríguez-Hernández, H. (Octubre de 2017). Tratamiento del papiloma oncocítico nasosinusal avanzado sin malignización asociada, con resección endoscópica y radioterapia en arcos de volumen modulado (RAVM). Reporte de un caso. Iatreia, 30(DOI 10.17533/udea.iatreia.v30n4a09.), 448-454.
Ahumada, A., Cajade, J., Milá de la Roca, A., Santos, S., & Pereira, F. (2015). Papilomas invertidos nasosinusales: Revisión retrospectiva de 10 años. REVISTA PORTUGUESA DE OTORRINOLARINGOLOGIA E CIRURGIA CÉRVICO-FACIAL, 53(4), 247 - 250.
Aribandi, M., McCoy, V. A., & Bazan, C. (2007). Imaging Features of Invasive and Noninvasive Fungal Sinusitis: A Review. RadioGraphics, 27, 1283-129.
Babbel, R., Harnsberger, H. R., Nelson, B., Sonkens, J., & Hunt, S. (1991). Optimization of techniques in screening CT of the sinuses. AJNR, 12, 849-54.
Bernardo, H., Hernández, L., Calvo, J., Llorente, J. L., & Gómez, J. L. (2001). Estudio por TC de los papilomas invertidos de la cavidad nasal y los senos paranasales. Radiología, 43(5), 237-241.
Bolivar Cuevas, S. A., Garcia Figueredo, D., Cuadrado Blazquez, M., Madureira Cordeiro, J. F., Tanasa, A., & Pruna Comella, X. (2014). Sociedad Española de Radiología Médica. Masas en senos paranasales: ¿Es esta lesion maligna?, 10.1594/seram2014/S-0298. España.
Buchwald, C., Nielsen, L. H., Ahlgren, P., Nielsen, P. L., & Tos, M. (1990). Radiological aspects of inverted papilloma. Eur J Radiology, 10, 481-90.
Burke Haywood, E., Fuller, C., G. W., Olobatuy, F., & Clark, D. W. (2017). Multifocal Sinonasal Inverted Papilloma with Middle Ear Involvement. Baylor University Medical Center Proceedings, 30(4 DOI: 10.1080/08998280.2017.11930228), 457-458.
Carta, F., Verillaud, B., & Herman, P. (2011). Role of endoscopic approach in the management of inverted papilloma. Curr Opin Otolaryngol Head Neck Surg, 19, 21 -4.
Dammann, F., Pereira, P., Laniado, M., Plinkert, P., Lowenheim, H., & Claussen, C. D. (1999). Inverted papilloma of the nasal cavity and the paranasal sinuses: using CT forprimary diagnosis and follow-up. AJR, 172, 543-548.
Di Pietrantonio, A., Asmus, H., Ingratta, C., Brennan, W., Schulz, J., & Carballo, L. (22 de Junio de 2018). Papiloma invertido sinunasal con invasión intracraneal: Reporte de caso y revisión bibliográfica. Surgical Neurology International, 9(doi:10.4103/sni.sni_370_1).
Díaz Molina, J. P., Llorente Pendás, J. L., Rodrigo Tapia, J. P., Álvarez Marcos, C., Obeso Agüera, S., & Suárez Nieto, C. (2009). Papilomas invertidos rinosinusales, Revisión de 61 casos. Acta Otorrinolaringol Esp, 60, 402 - 408.
Dragonetti, A., Gera, R., Sciuto, A., Scotti, A., Barbaro, E., & Minh, A. (2001). Sinonasal inverted papilloma: 84 patients treated by endoscopy and proposal for a new classification. Rhinology, 49, 207-213.
Gras Cabrerizo, J. R., Massegur Solench, H., Pujol Olmo, A., Montserrat Gili, J. R., Ademá Alcover, J. M., & Zarraonandia Andraca, I. (2011). Endoscopic medial maxillectomy with preservation of inferior turbinate: how do we do it? Eur Arch Otorhinolaryngoly, 268, 389–92.
Gras Cabrerizo, J. R., Montserrat Gili, J. R., Massegur Solench, H., León Vintró, X., De Juan, J., & Fabra Llopis, J. M. (2010). Management of sinonasal inverted papilomas and comparison of classification staging systems. Am J Rhinol Allergy, 24, 66–69.
Hähnel, Stefan, Birgit, E.-W., Tasman, A.-J., Forsting, M., & Jansen, O. (1 de January de 1999). Relative Value of MR Imaging as Compared with CT in the Diagnosis of Inflammatory Paranasal Sinus Disease. Radiology, 210(1), 171-176.
Harnsberger, Osborn, & Cols. (2011). Diagnostic and Surgical Imaging Anatomy. Amirsys.
Huang, C. C., Lee, T. J., Chang, P. H., Lee, Y. S., Chuang, C. C., & Jhang, Y. J. (2010). Desmoglein 3 is overexpressed in inverted papilloma and squamous cell carcinoma of sinonasal cavity. Laryngoscope, 120, 26-9.
Hyams, V. J. (1971). Papillomas of the nasal cavities and the paranasal sinuses: a clinicopathological study of 315 cases. Ann Otol Rhinol Laryngol, 80, 192-206.
Jaime Osorio, M., Lorena Aguayo, G., & Pilar Gajardo, O. (2013). Revisión de 25 casos de papiloma invertido en 8 años. Rev. Otorrinolaringol. Cir. Cabeza Cuello, 73, 146-150.
Karkos, P. D., Khoo, L. C., & Leong, S. C. (2009). Computed tomography and/or magnetic resonance imaging for preoperative planning for inverted nasal papilloma: review of evidence. J Laryngol Otol, 123, 705-709.
Kim, D. Y., Hong, S. L., Lee, C. H., Jin, H. R., Kang, J. M., Lee, B. J., . . . Cho, S. H. (2012). Inverted papilloma of the nasal cavity and paranasal sinuses: A Korean multicenter study. Laryngoscope, 487–494.
Krouse, J. H. (2000). Development of a staging system for inverted. Laryngoscope, 110, 965 - 968.
Lai, P. H., Yang, C. F., Pan, H. B., Wu, M. T., & Chu, S. T. (1999). Recurrent inverted papilloma: diagnosis with pharmacokin dynamic gadolinium-enhanced MR imaging. Am J Neuroradiol, 20, 1445-51.
Llorente Pendás, J. L., Suárez Fente, V., & Suárez Nieto, C. (2007). Papilomas invertidos nasosinusales. Acta Otorrinolaringología (págs. 78–83). España: 58.
Lobo, B. C., D'Anza, B., Farlow, J. L., Tang, D., Woodard, T. D., Ting, J. Y., & Sindwani, R. (Octubre de 2017). Outcomes of sinonasal squamous cell carcinoma with and without association of inverted papilloma: A multi-institutional analysis. American Journal of Rhinology & Allergy, 31(5 (https://doi.org/10.2500/ajra.2017.31.4470)), 305-309 (5).
McKay, S. P., Grégoire, L., Lonardo, F., Reidy, P., Mathog, R. H., & Lancaster, W. D. (August de 2005). Human papillomavirus (HPV) transcripts in malignant inverted papilloma are from integrated HPV DNA. Laryngoscope, 115(8), 1428-31.
Mena, F., Mena, C., & Quiroz, J. V. (2010). Cirugía en el papiloma invertido nasal. Rev. Otorrinolaringol. Cir. Cabeza Cuello, 70, 43-48.
Momeni Arash, K., Roberts, C. C., & Chew, F. S. (December de 2007). Imaging of Chronic and Exotic Sinonasal Disease: Review. American Journal of Roentgenology 189, no. 6_supplement, doi:10.2214/AJR.07.7031, S35-S45.
Ojiri, H., Ojita, M., Tada, S., & Fukuda, K. (2000). Potentially distinctive features of sinonasal inverted papilloma on MR imaging. AJR, 175, 465-8.
Salazar Guilarte, J. X., Paredes Osado, J. R., Barberá, J. M., & Gras Albert, J. R. (2011). Papilomas invertidos nasosinusales. Revisión de 10 años. Revista Española de Cirugía Oral y Maxilofacial, 138-141.
Sarmiento, D. H. (2004). axilectomía medial más etmoidectomía total endoscópica para el tratamiento del papiloma invertido nasosinusal. Revista de Otorrinolaringología Cirugía Cabeza Cuello, 64, 134-40.
Tejero Garcés, G., Alfaro, E., Queipo Gutiérrez, F. J., Vives Ricomà, E., Pérez Delgado, L., & Almajano Martínez, C. (2017). Relación entre el papiloma invertido nasosinusal y el virus del papiloma humano. ORL Aragón (Sociedad Aragonesa de Otorrinolaringología), 2(ISSN 1576-9127), 9-11.
Uzun, L., Ozkanli, S., Kalcioglu, M. T., & Kokten, N. (2017). Bilateral multifocal inverted papilloma with osseous. Brazilian Journal of Otorhinolaryngology(http://dx.doi.org/10.1016/j.bjorl.2016.06.012.), 3.
Weissler, M. C., Montgomery, M. M., & Montgomery, S. K. (1986). Inverted papilloma. Ann Otol Rhinol Laryngol, 95, 215-21.
Wood, J. W., & Casiano, R. R. (2012). Inverted papillomas and benign nonneoplastic lesions of the nasal cavity. Am J Rhinol Allergy, 26, 157–163.
Notas de autor
ejlucas2@hotmail.com