Toxoplasma gondii en mujeres embarazadas en la provincia de El Oro, 2014
Toxoplasma gondii en mujeres embarazadas en la provincia de El Oro, 2014
Revista Ciencia Unemi, vol. 9, núm. 21, pp. 135-141, 2016
Universidad Estatal de Milagro

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.
Recepción: 20 Agosto 2015
Aprobación: 25 Octubre 2016
Resumen: El objetivo de la presente investigación fue determinar los anticuerpos IgG- IgM de anti toxoplasma gondii en mujeres embarazadas, atendidas en una casa de salud privada, siendo el principal reservorio de esta infección el gato doméstico (Feliscatus), puede ocurrir en cualquier etapa del embarazo, es muy importante detectar en el primer trimestre para evitar trastornos del sistema nervioso central y retinocoroiditis. El método clínico que se utilizó para el diagnóstico de los anticuerpos IgG-IgM fue electroquimiolumisencia de alta sensibilidad, los resultados obtenidos de anticuerpos IgG contra T. gondii en embarazadas, fue 16% IgG-IgM seropositivo para anti T. gondii, en relación con las mujeres embarazadas con serología positiva para T. gondii decreció linealmente con la edad de la paciente, siendo el grupo de 20-25años el más afectado 40(12%) para IgG positivo y IgM 25(10%), lo que referencia acerca de la prevalencia del Toxoplasma gondii.
Palabras clave: anticuerpos IgG-IgM del toxoplasma gondii, toxoplasma gondii, Toxoplasmosis.
Abstract: The aim of this study was the determination of IgM antibodies IgG anti toxoplasma gondii in pregnant women, attended in a private health place, being the main reservoir of this infection the domestic cat (Felis catus), can occur at any stage of pregnancy, it is important to detect the first trimester of pregnancy to prevent disorders of the central nervous system and retinochoroiditis. The clinical method used was electroquimiolumisencia high sensitivity for the diagnosis of IgG - IgM antibodies, the results of IgG antibodies against T. gondii in pregnant women was 16% IgG anti-IgM seropositive for T. gondii, in relation of pregnant women with positive serology for T. gondii decreased linearly with the age of the patient, being the group most affected 20-25años 40 (12%) for IgG and IgM positive 25 (10%) giving reference on prevalence of Toxoplasma gondii.
Keywords: IgG- antibodies toxoplasma gondii, toxoplasma gondii, toxoplasmosis.
I. INTRODUCCIÓN
Las infecciones llamadas toxoplasmosis que se presentan en mujeres embarazadas son muy comunes en el primer trimestre de gestación, es la zoonosis más frecuente en los humanos, el agente causante es un protozoario conocido como Toxoplasma gondii, (Díaz, Zambrano, Chacón, Rocha, & Díaz, 2010), siendo el principal reservorio el gato doméstico (Feliscatus), la eliminación se da por medio de quistes en las heces, diseminando así la infección en el medio ambiente y propagándola (Hernández Cortázar, y otros, 2015) (Hernández, Acosta, Ortega, Guzmán, Aguilar & Jiménez, 2015). El parásito es un agente infeccioso causante del síndrome TORSCH (grupo de enfermedades que causan manifestaciones clínicas similares debido a infecciones por Toxoplasma gondii, virus de la rubéola, virus del herpes simplex, citomegalovirus y otros agentes infecciosos).
Este parásito intracelular móvil, gram negativo, sin hospedero específico (euríxeno) tiene forma arqueada, semilunar y carece de flagelos, pese a lo cual goza de autonomía de movimientos de rotación helicoidales, en los que participa toda la célula, gracias a las fibrillas dispuestas sobre su superficie. (Sánchez Artigas, y otros, 2012)
La transmisión congénita sucede en cualquier etapa de la gestación, sin embargo se enfocó durante el primer trimestre donde se producen los mayores efectos en el feto, los mecanismos de transmisión placentarios, después de la parasitemia, ocurren con una invasión de taquizoitos, donde la atraviesan fácilmente llegando a la circulación y tejidos fetales. (Castro, Góngora, & González, 2008) (Reyes, Guerrero, Arias, & Castro, 2001). Se considera de mucha importancia dar a conocer que el riesgo fetal aumenta conforme la duración del embarazo. La gravedad de la toxoplasmosis congénita dependerá a su vez de varios factores como son el número de parásitos que atraviesen la placenta, la inmadurez inmunológica del feto y la edad gestacional. (Restrepo Giraldo, 2008)
La infección congénita puede producir abortos, óbitos, así como alteraciones neurológicas (coriorretinitis, calcificaciones encefálicas, hidrocefalia, micro o macrocefalia y sistémicas (hepatoesplenomegalia, fiebre, ictericia). (Díaz, Zambrano, Chacón, Rocha, & Díaz, 2010)
La Asociación Española de Consumo Seguridad Alimentaria y Nutrición (AECOSAN), considerada a las mujeres embarazadas como un grupo poblacional vulnerable a este comportamiento, ya que la respuesta inmunológica de la placenta y su tropismo para virus y otros patógenos específicos, favorecen esta susceptibilidad a ciertas enfermedades infecciosas que, además, tienden a presentarse en forma de cuadros de mayor gravedad, esto se debe a ciertos cambios hormonales durante la gestación que parecen alterar diversos mecanismos de inmunidad celular, así como de la respuesta innata. (AECOSAN, 2014)
El impacto socioeconómico de los familiares de un niño con toxoplasmosis congénita es siempre muy fuerte. En la actualidad, con la posibilidad de hacer un diagnóstico seguro prenatal, tratamiento cuya eficacia es discutida, el daño referente en el área social y económica en el individuo que la padece es grande, también se afecta su círculo familiar e institucional, así como en la productividad del desarrollo social. Este trabajo puede ser un aporte para un mejor entendimiento de la problemática de salud, lo que permite diseñar y desarrollar programas médico-asistenciales y preventivos, adecuados a las necesidades y características de las poblaciones vulnerables.
Los resultados de las pruebas serológicas demuestran anticuerpos anti-toxoplasma gondii (AcTg) de las clases IgA e IgM, son considerados en el inicio de la primoinfección, permitiendo ser utilizados como marcadores que se relacionan con la fase aguda de la enfermedad. (García, 2015). El tiempo de la detección de estas inmunoglobulinas en suero depende de la sensibilidad del método de laboratorio empleado, con el mismo puede verificarse la primoinfección con la presencia de IgA en las primeras semanas y por la IgM hasta cerca de 6 meses de ocurrida la misma.
La IgG comienza a detectarse en bajas concentraciones cerca del mes del comienzo de la infección y su incremento es más lento que el de la IgA e IgM, pero alcanza valores superiores hasta pasados los 6 meses. (Barrera, y otros, 2002). Los anticuerpos IgG específicos, al parecer, se dirigen contra determinantes antigénicos proteicos de la superficie del taquizoito. Los isotipos predominantes de IgG son IgG1, seguido de IgG2 e IgG3 y su capacidad para la fijación de complemento, resulta en un mecanismo de resistencia a la infección, puesto que los taquizoitosopsonizados son susceptibles a la destrucción por la vía lisosomal en las células fagocíticas.
El parásito que ingresa al organismo es inmediatamente fagocitado por los monocitos, dentro de los cuales el protozoario se multiplica activamente, induce una respuesta inmune que se caracteriza por producción de citoquinas proinflamatorias, incluyendo interleuquina 12 (IL-12), interferón γ (IFN-γ) y factor de necrosis tumoral α (TNF-α), la cual obliga al parásito a formar quistes que permanecerán durante toda la vida del hospedero. (Reátegui & Vela G., 2009). Los anticuerpos del tipo IgG, IgM, IgA e IgE generados contra proteínas del Toxoplasma gondii pueden detectarse en las dos primeras semanas postinfección. (Giraldo Restrepo, 2008)
Los anticuerpos del tipo IgA en las superficies mucosas parecen conferir protección contra la reinfección; ésta puede producirse, pero aparentemente no causa enfermedad ni transmisión congénita del parásito. En el paciente inmunodeficiente la infección puede inducir la destrucción de los tejidos, causando neumonitis, miocarditis o encefalitis, entre otras enfermedades, y en los ojos, coriorretinitis aguda con inflamación grave y necrosis. (Berrueta Uribarren, 2016; Siacche, 2006)
La toxoplasmosis en el ser humano se presenta en todas las regiones del mundo, pero su prevalencia es mayor en las zonas tropicales. Es una zoonosis, y se la ha diagnosticado en más de 300 especies de mamíferos, incluyendo varias especies marinas, y en más de 30 aves domésticas y silvestres; en todas ellas se desarrolla el ciclo evolutivo asexual y son, por lo tanto, huéspedes intermediarios, que culmina con la formación de los quistes tisulares en diversos tejidos, en especial el muscular y el nervioso (Fernández, Acosta, & Montaño, 2011). En el gato doméstico ocurre el ciclo sexual o esporogónico y así son los únicos huéspedes definitivos; los ooquistes son el elemento final de esta reproducción que se eliminan en las heces del gato.
La toxoplasmosis es una de las infecciones más comunes del mundo, una vez infectado, incuba el parásito durante un periodo de entre 3 y 20 días. Después y durante sólo un periodo de 1 mes, libera los ooquistes en las heces, que son muy infecciosos. En algunas ocasiones las personas infectadas desarrollan síntomas similares a los de la influenza o a los de la mononucleosis infecciosa, como inflamación de las glándulas, cansancio, dolores musculares, malestar y fiebre. La toxoplasmosis se encuentra ampliamente distribuida en Latinoamérica con anticuerpos T. gondii (AcTg) detectables hasta en 65% de la población mundial. Se han descrito elevadas prevalencias. 10-30 % en América del Norte, T. gondii el 37,5% en Centroamérica, 33,9% en América del Sur. (Reátegui & Vela G., 2009) (Santiago, y otros, 2012) (Palmezano Díaz, Plazas Rey, & Rojas Carvajal, 2015).
La transmisión transplacentaria ocurre cuando la mujer se infecta con T. gondii, por primera y única vez durante el embarazo, cuando cruza la barrera placentaria; pudiendo tener consecuencias como aborto, mortinatos o partos prematuros y recién nacidos con coriorrenitis, hidrocefalia y retardo psicomotor.
Los estudios epidemiológicos realizados, demuestran la prevalencia de anticuerpo Anti- T. gondii en diversos grupos de población, reportándose las siguiente cifras globales: Oceanía 41.73%; Europa 31.76%; Asia 22.60%; África 19.07% y América del Sur, Chile, Brasil, Perú, Ecuador, 33.90%. América Central, Panamá, Costa Rica, Cuba con un 37.5% entre otros. (Espinoza Ortega & Espín Negrete, 2012).
II. DESARROLLO
1. Metodología
Técnica del Test para determinación los anticuerpos IgG - IgM. La investigación se desarrolló basado en un método explicativo básico, con un diseño experimental, el estudio se realizó a 250 mujeres embarazadas con una edad que oscilaba ente 15- 40 años, que cursaban en el primer trimestre de gestación, las mismas que asistieron a consulta ginecológica a una casa de salud privada, de diferentes partes de la provincia de El Oro, Ecuador. El proceso de análisis clínico es un método clínico cuantitativo. Se utilizó µL-capturado de muestra, las mismas que se colocaron en las cubetas enumeradas para cada una de ellas, con un tiempo estimado de duración total de 18 minutos, para la detección de anticuerpos anti-Toxo.
Procedimiento:
-
1 incubación: 10ul de muestra se pre-diluyen automáticamente con Elecsys Diluente Universal de 1:20. Se añade antígeno específico del T. gondii recombinado, marcado con un complejo de rutenio. Los anticuerpos IgM, IgG presentes en la muestra reaccionan al antígeno específico de T. gondii recombinantes, marcado con rutenio.
2 incubaciones. Se añade anticuerpos monoclonales biotinilados anti-IgM humano y micropartículas recubiertas de estreptavidina, un frasco de 6.5ml que equivale a 0.72 mg/mL. El complejo total se fija por interacción entre biotina y estreptavidina a la fase sólida. El tiempo estimado de duración de las 2 incubaciones es 10 minutos, a una temperatura de 20ºC-25 °C.
La mezcla de reacción se traslada a la célula de lectura donde, por magnetismo, las micro partículas se fijan a la superficie del electrodo. Los elementos no fijados se eliminan posteriormente con el reactivo ProCell. Al aplicar una corriente eléctrica definida se produce una reacción quimioluminiscente, cuya emisión de luz se rinde directamente con un fotomultiplicador.
El software Elecsys proporciona automáticamente los resultados, comparando la señal de electroquimiluminiscencia con el valor límite discriminatorio obtenido anteriormente por calibración de IgG, IgM anti T. (ROCHE, 2014)
2. Resultados
Mediante el análisis de inmunoglobulina se mide el nivel de inmunoglobulinas, o anticuerpos, en la sangre. En la Figura 1 se muestra los resultados de la determinación de serología IgG- IgM.
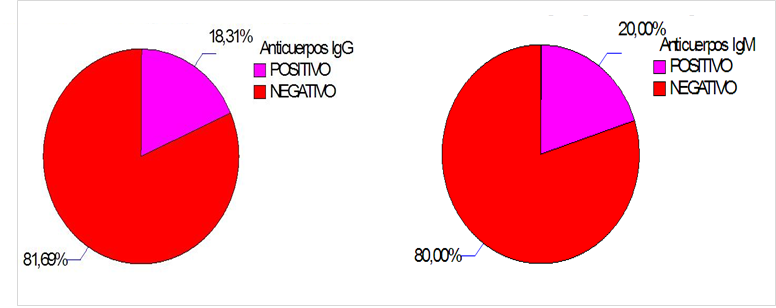
Figura 1.
Determinación de serología IgG- IgM contra Toxoplasma gondii
Fuente: Análisis de casos clínicos
En la población estudiada se evaluó los casos IgG-IgM negativos, encontrándose 203 (81,2%), pacientes positivos a T. gondii 40 (16%), 5 (2 %) IgG positivo y de IgM negativo. Así mismo, de 2 (0,8%) embarazadas se obtuvo datos IgG negativo y IgM positivo, en estos caso se considera como una infección aguda de toxoplasma gondii. Ver Figura 2.
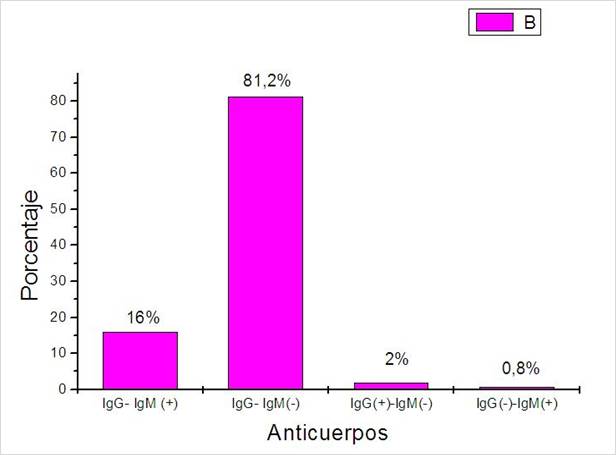
Figura 2.
Casos clínicos de anticuerpos IgG - IgM para el diagnóstico de toxoplasma gondii en mujeres embarazadas en el primer trimestre de gestación.
Fuente: Análisis de casos clínicos
En relación a la presencia de anticuerpos IgG -IgM contra T. gondii por grupo etáreo, se observó que la mayoría de casos se dio en el grupo comprendido entre 26-30 años con 50%, seguido de 21-26 años con 28% (Tabla 1). La proporción de embarazadas con serología positiva para Toxoplasma gondii decreció linealmente con la edad.
| 15-20 años | 21-25 años | 26-30 años | 31-35 años | 36-40 años | Total | Porcentaje | |
| IgG Positivo | 4 | 30 | 10 | 2 | 1 | 47 | 18,8 % |
| IgG Negativo | 16 | 40 | 115 | 18 | 14 | 203 | 81,2 % |
| IgM Positivo | 2 | 25 | 10 | 3 | - | 40 | 16 % |
| IgM Negativo | 18 | 45 | 115 | 17 | 15 | 210 | 84 % |
De los 250 casos clínicos para la determinación de IgG- IgM contra T. gondii, se observó 76% en mujeres pluriembarazadas, y 24% en mujeres primerizas. Ver Tabla 2.
| Mujeres embarazadas | Porcentaje | |
| Pluriembarazo | 190 | 76% |
| Primer embarazo | 60 | 24% |
De los 250 casos clínicos para anticuerpos IgG - IgM contra T. gondii, por procedencia se dieron, en la ciudad de Machala, casos clínicos negativos 100 (50%) en el diagnóstico de IgG-IgM anti toxoplasma, seguido por la ciudad de Pasaje con 82 (36,8%) para IgG- IgM anti toxoplasma. Ver Figura 3 y Tabla 3.
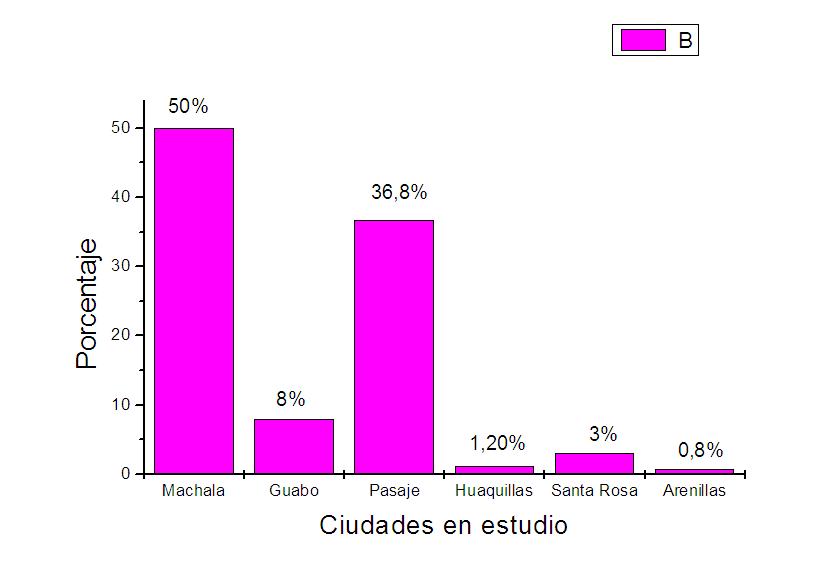
Figura 3.
Presencia de anticuerpos IgG-IgM contra T. gondii en mujeres embarazadas distribuidas por procedencia.
Fuente: Análisis de encuestas realizadas a los pacientes en estudio
| Residencias de las pacientes en estudio | Positivo | IgG Negativo | IgM Positivo | Negativo |
| Machala | 25 | 100 | 25 | 100 |
| Guabo | 3 | 17 | 2 | 18 |
| Pasaje | 10 | 82 | 9 | 83 |
| Huaquillas | - | 3 | - | 3 |
| Santa Rosa | 7 | 1 | 2 | 6 |
| Arenillas | 2 | - | 2 | - |
III. CONCLUSIONES
Para la determinación de anticuerpos IgG –IgM contra T. gondii en este estudio, se utilizó el método de Electroquimiolumisencia. De las 250 embarazadas estudiadas, 16% presentó anticuerpos IgG contra T. gondii y 81.2% no presentó, se pudo observar que 0.8% dio como resultado IgG (-) y IgM(+) que es el inicio de la infección de toxoplasmosis y para IgM positivo se obtuvo 16% y negativo 84%. La prevalencia de anticuerpos IgG -IgM contra T. gondii encontrada en el estudio100 (50%) para la ciudad de Machala, y la ciudad de Pasaje es de 82 (36.8%), permite inferir que Machala y Pasaje son ciudades endémicas importantes, probablemente por ser un país tropical. La evidencia de anticuerpos IgG -IgM contra T. gondii en embarazadas, en el 50% de casos estudiados se encontró en mujeres entre 26-31 años, período de mayor fertilidad y edades que se consideran las más favorables para la reproducción.
IV. REFERENCIAS
AECOSAN. (2014). Informe del Comité Científico de la Agencia Española de Consumo, Seguridad Alimentaria y Nutrición (AECOSAN) en relación con los riesgos microbiológicos asociados al consumo de determinados alimentos por mujeres embarazadas (versión resumen). España: AECOSAN-2014-001.
Barrera, A. M., Castiblanco, P., Gómez, J. E., López, M. C., Ruiz, A., Moncada, L., . . . Corredor, C. (2002). Toxoplasmosis Adquirida Durante el Embarazo. Revista Slud pública, 4(3), 286-293.
Berrueta Uribarren, T. (20 de junio de 2016). Toxoplasmosis. Obtenido de http://www.facmed.unam.mx/deptos/microbiologia/parasitologia/toxoplasmosis.html
Castro, A. T., Góngora, A., & González, M. E. (julio de 2008). Seroprevalencia de anticuerpos a toxoplasmosis gondii n mujeres embarazadas de Villavicencio Colombia. Orinoquia, 12(1), 91-100.
Díaz, L., Zambrano, B., Chacón, G., Rocha, A., & Díaz, S. (septiembre de 2010). Toxoplasmosis y embarazo. Revista de Obstetricia y Ginecología de Venezuela, 70(3), 190-205.
Díaz, L., Zambrano, B., Chacón, G., Rocha, A., & Díaz, S. (2010). Toxoplasmosis y embarazo. Revista de Obstetricia y Ginecologìa de Venezuela, 70(3), 190-205.
Díaz, L., Zambrano, B., Chacón, G., Rocha, A., & Díaz, S. (2010). Toxoplasmosis y embarazo. Revista de Ginecologìa y Obstetricia de Venezuela, 70(3), 190-205.
Dra. Rosa Flieller, D. M. (2013). Toxoplasmosis l embarazo. CATEDRA DE ENFERMEDADES INFECCIOSAS.
Espinoza Ortega, G., & Espín Negrete, L. (2012). Incidencia de toxoplasmosis en gatos mediante la prueba de hemoaglutinación. Ecuador: Tesis de Grado, Universidad Técnica de Cotopaxi.
Fernández, A., Gonzales, D., Toribio, V., & Zucco, A. G. (2014). Toxoplasma gondii. Microbiología clínica.
Fernández, T. R., Acosta, Y., & Montaño, M. A. (2011). Toxoplasmosis congénita: reporte de casos. Revista de Medicina FCM-UCSG, 17(3), 192-197.
FRENKEL. (1973). NEW KNOWLWDG OF TOXOPLASMA AND TOXOPLASMOSIS ADV. PARASITOL. En JOCOBS.
García, D. T. (2015). Toxoplasmosis congénita. SCIELO.
GIAL. (2003). MICROBIAL PATHOGENESIS AND THE EPITHELIAL CELL. Primera.
Giraldo Restrepo, M. (2008). Toxoplasmosis. Medicina & Laboratorio, 14(7-8), 359-375.
HENDRIX, C. (1999). Diagnóstico Parasitológico Veterinario. (ISBN: 0521443288 / 0 521 44328).
Hernández Cortázar, I., Acosta-Viana, K. Y., Ortega Pacheco, A., Guzmán Marín, E. d., Aguilar-Caballero, A. J., & Jiménez-Coello, M. (Marzo-April de 2015). Toxoplasmosis in Mexico: epidemiological situation in humans and animals. Revista do Instituto de Medicina Tropical de São Paulo, 57(2), 93-103.
Martin Hernández, I. (julio-septiembre de 2013). Toxoplasmosis congénita: una mirada al problema. BIOMED, 181-190.
Montoya, N. (2010). Principles and Practice of Infectious Diseases. Philadelphia: 7th ed.
Palmezano Díaz, J. M., Plazas Rey, L. K., & Rojas Carvajal, D. (enero-junio de 2015). Infeccion por Toxoplasma: panorama actual. Spei Domus , 11(22), 47-56.
Reátegui, C. B., & Vela G., L. (2009). Factores socioeconómicos-epidemiológicos y su relación con la seroprevalencia de toxoplasmosis en gestantes atendidas en los hospitales "Felipe Arriola" y "Cesar Garayar", Iquitos, Perú, 2009.
Restrepo Giraldo, M. L. (2008). Toxoplasmosis. Medicina y Laboratorio, 14(7 ), 359-375.
Reyes, C. M., Guerrero, M., Arias, M., & Castro, A. (2001). Transmisión de toxoplasma gondii en Costa Rica en concepto actualizado., (págs. 36-38). Costa Rica.
ROCHE. (2014). Life Needs Answers. España: Roche Diagnostic.
Sánchez Artigas, R., Góngora Amores, W., Goya Batista, Y., Miranda Cruz, A. C., Cubeñas Vega, G., & Pérez Martín, O. (marzo de 2012). Seroprevalencia de Toxoplasma gondii en donantes de sangre en la provincia de Guantánamo. Revista Cubana de Investigaciones Biomédicas , 31(1).
Sánchez, A. L.-J. (s.f.). TOXOPLASMOSIS Y EMBARAZO. TOXOPLASMOSIS Y EMBARAZO.
Sánchez, R., & Góngora, W. (2012). Aspectos básicos sobre la patogenia, respuesta inmune y bioseguridad en el trabajo con Toxoplasmosis gondii. Centro de Inmunología y Biopreparados, 1.
Santiago, B., Blazquez, D., Lopez, G., T., S., M., M., Alonso, T., & Moro, M. (2012). Perfil serologico en gestantes extranjeros frente a VIH, VHB, VHC, virus de rubeola, Toxoplasma gondii, Treponema pallidium y Trypanosoma cruzi. Enfermedades Infecciosas y Microbiologicas Clinicas, 64-69.
Siacche, H. O. (2006). Inmunología, diagnóstico e interpretación de pruebas de laboratorio. Colecciones Lecciones Universidad de Rosario