Artículos Científicos
Hidrólisis enzimática de polvillo de arroz para la producción de etanol de segunda generación
Hidrólisis enzimática de polvillo de arroz para la producción de etanol de segunda generación
Revista Ciencia Unemi, vol. 13, núm. 32, pp. 41-50, 2020
Universidad Estatal de Milagro

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.
Recepción: 16 Julio 2019
Aprobación: 27 Noviembre 2019
Resumen: El objetivo de la presente investigación fue hidrolizar el polvillo de arroz a azucares reductores y mediante fermentación alcohólica obtener bioetanol. Se prepararon nueve soluciones de polvillo de arroz molido (8 %, 13 % y 18 %) y agua purificada e inoculados con conidios de Trichoderma spp en concentraciones (0,2 g/L, 0,4 g/L y 0,6 g/L), los cuales se incubaron a 30°C por 144 horas. Mediante el método DNS (3, 5 ácido di nitrosalisilico), se cuantificó los azúcares reductores: tratamiento A: 4,32 ± 0,08%, B: 5,27 ± 0,07%, C: 5,10 ± 0,01%, D: 5,53 ± 0,12%, E: 8,24 ± 0,06%, F: 6,37 ± 0,07%, G: 5,13 ± 0,02%, H: 7,19 ± 0,26%, I: 9,69 ± 0,18% y el etanol mediante cromatografía de gases. El tratamiento que presentó mayor porcentaje de bioconversión fue el tratamiento I (18 % y 0,6 g/L de inóculo), donde la concentración de glucosa, fue 9,88%, y el rendimiento de etanol fue de 5° GL. En conclusión, es posible hidrolizar los carbohidratos totales presente en el polvillo de arroz en azucares reductores y posterior fermentación alcohólica.
Palabras clave: Azucares reductores, Bioconversión, Celulasas, Cromatografía de Gases, Saccharomyces cerevisiae, etanol.
Abstract: The objective of the present investigation was to hydrolyze the rice powder to reducing sugars and, through alcoholic fermentation, obtain bioethanol. Nine solutions of ground rice powder (8%, 13% and 18%) and purified water were prepared and inoculated with conidia of Trichoderma spp in concentrations (0.2 g / L, 0.4 g / L and 0.6 g). / L), which were incubated at 30 ° C for 144 hours. Using the DNA method (3, 5 di nitrosalisilic acid), the reducing sugars were quantified: treatment A: 4.32 ± 0.08%, B: 5.27 ± 0.07%, C: 5.10 ± 0, 01%, D: 5.53 ± 0.12%, E: 8.24 ± 0.06%, F: 6.37 ± 0.07%, G: 5.13 ± 0.02%, H: 7, 19 ± 0.26%, I: 9.69 ± 0.18% and ethanol by gas chromatography. The treatment with the highest percentage of bioconversion was treatment I (18% and 0.6 g / L inoculum), where the glucose concentration was 9.88%, and the ethanol yield was 5 ° GL. In conclusion it is possible to hydrolyze the total carbohydrates present in the rice powder bz reducing sugars and the subsequent alcoholic fermentation.
Keywords: Reducing Sugars, Bioconversion, Cellulases, Gas Chromatography, Saccharomyces cerevisiae, Ethanol.
I. INTRODUCCIÓN
En la naturaleza existen diversas fuentes de residuos y subproductos lignocelulósicos disponibles en abundancia, renovables y de bajo costo (Salanti, Zoia, Tolppa, & Orlandi, 2012). Los materiales lignocelulósicos se componen de polímeros de hidratos de carbón (almidones, celulosa, lignina y hemicelulosa) que contienen aproximadamente 68,4% de polisacáridos principalmente de pentosa y hexosa, las cuales se forman de cadenas lineales de β (1-4) de la D–glucopiranosa (Sofía & Paz, s. f.). Las diferentes propiedades físicas y químicas de la lignina pueden tener varios efectos sobre la hidrólisis enzimática de sustratos lignocelulósicos (Hongdan Zhang, Wu, & Xie, 2017). Los almidones, la celulosa y hemicelulosa están formada por monómeros de D-glucosa unidos por enlaces β-1,4, difíciles de hidrolizar a sus monómeros, debido a la presencia de la lignina y la cristalinidad altamente organizada de la celulosa(Salanti et al., 2012). La hemicelulosa es un heteropolímero de hidratos de carbono compuesto de varios azúcares diferentes, incluyendo azúcares de cinco y seis carbonos, y puede ser fácilmente descompuesta a sus monómeros. La estabilidad hidrolítica y la solidez estructural de la celulosa y hemicelulosa presentes en las plantas ha evolucionado para resistir a la degradación, esta robustez o dureza es atribuible a la reticulación entre los polímeros de hidratos de carbono y el polímero aromático (lignina) a través de los enlaces éster y éter. Estos enlaces éster y éter entre los azúcares oxidados, los ácidos urónicos, fenoles y fenilpropanoles, surgen como parte funcional de la lignina. El residuo digerido en el rumen de la paja de arroz contiene carbohidratos residuales altos, que lo convierte en una posible materia prima de etanol (Haibo Zhang et al., 2018). Una fuente renovable de biomasa es el polvillo de arroz, subproducto del pelado y pulido del grano de esta gramínea, el cual posee una composición de 68,44% de carbohidratos solubles y 11,51% de proteína (Salanti et al., 2012).
Para extraer los azúcares fermentables del polvillo de arroz, se requiere reducir el tamaño de partícula y someter a una hidrolisis enzimática para separar la celulosa, hemicelulosa y almidones de la lignina, porque la lignina posee un complejo sistema de uniones químicas difíciles de romper (Ren, Zhao, Chen, Guo, & Cao, 2015).
Los monosacáridos resultantes de la hidrolisis enzimatica de los carbohidratos presentes en el polvillo de arroz pueden ser fermentados a etanol, mientras que un alto porcentaje de pentosas en la hemicelulosa, tales como xilosa no son fáciles de fermentar por Saccharomyces cerevisiae(Ren et al., 2015).
Las barreras técnicas y las limitaciones fundamentales en los procesos de la despolimerización de azúcar han demostrado ser complejos y difíciles de superar(Jiang et al., 2016). La hidrólisis enzimática de celulosa , hemicelulosa y almidones se desarrolla mediante la intervención de múltiples enzimas celuliticas (Diego, 2015).
Las celulasas, hemicelulasas y amilasa son capaces de degradar los carbohidratos presentes en el polvillo de arroz en azúcares solubles que pueden ser fermentados para producir bioetanol. Actualmente, la sacarificación de residuos lignocelulósicos mediante hidrólisis enzimática produce bajos rendimientos, lo que dificulta el proceso de producción de bioetanol comercial (Greene, Himmel, Beckham, & Tan, 2015), el bioetanol es una fuente de energía renovable que puede reducir consumo de combustibles fósiles y contaminación ambiental(Shokrkar, Ebrahimi, & Zamani, 2018). Existen microorganismos como el Trichoderma spp que es un hongo con capacidad de producir grandes cantidades de enzimas celulíticas, cuya acción sinérgica puede sacarificar biomasa lignocelulósica en azucares solubles y fermentables (Seiboth, Verena, & Seibot, 2011). Trichoderma reesei Aq-5b y Trichoderma viride NSW-XM capaces de excretar enzimas degradantes de lignina y celulasa para crear un sistema de cultivo mixto para hidrolizar el polvillo de arroz (Wu et al., 2016). Las enzimas que produce este microorganismo se dividen en cuatro categorías en función de la acción catalítica de celulosa: exoglucanasas, endoglucanasas, beta-glucosidasas, y monooxigenasas. La sacarificación y fermentación simultáneas (SSF) es un proceso prometedor para la conversión de lignocelulósico materiales para biocombustibles. Sin embargo, los productos finales de fermentación podrían inhibir la sacarificación de los lignocelulósicos por las enzimas que degradan la celulosa (Nan et al., 2019).
Teniendo en cuenta toda esta evidencia científica y en búsqueda de una eficiente bioconversión de la biomasa lignocelulósica para la producción de etanol de segunda generación, el principal objetivo es estudiar:
La formación de sustancias inhibidoras y determinar su reducción mediante la aplicación de un pretratamiento eficaz; control de los parámetros fisicoquímicos del proceso de hidrólisis: temperatura, oxigenación, pH, agitación y concentración de nutrientes del medio de cultivo (Diego, 2015).
Los avances en biotecnología en las últimas décadas nos brindan herramientas necesarias para producir etanol a partir (Raele, Boaventura, Fischmann, & Sarturi, 2014) de la bioconversión de carbohidratos complejos a glucosa, fructosa, xilosa a partir de residuos agroindustriales mediante un proceso de hidrólisis enzimática. Este nuevo método de producción se lo denomina etanol de segunda generación(Raele et al., 2014). En las peladoras de arroz existentes en la provincia de El Oro, el polvillo de arroz no es utilizado adecuadamente con fines económicos, existiendo grandes volúmenes procedentes del proceso de pilado, lo que constituye una pérdida, ya que puede ser utilizado en: obtención de jarabes glucosados, preparación de medios de cultivos agrícolas, obtención de etanol, etc. Por lo tal el salvado de arroz es una materia prima prometedora para la producción de etanol, el arroz es un cultivo importante en países como China, India, Indonesia y Bangladesh; la producción de arroz en todo el mundo fue alrededor de 750 millones de toneladas en 2014 (Santos Michel et al., 2016).
La biomasa lignocelulósica es una materia prima abundante y una alternativa para portadores de energía a base de fósiles y productos químicos, prometedora para la producción de biocombustibles(Li et al., 2018). La lignocelulosa se compone de tres principales polímeros, a saber, celulosa, hemicelulosas y lignina, así como pequeñas cantidades de pectinas, extractos y proteínas(Kellock et al., 2019). La bioconversión de biomasa lignocelulósica en biocombustibles y productos bioquímicos que se refiere al pretratamiento, la hidrólisis enzimática y la fermentación ha ganado más y más atención debido a su reciclaje efectivamente sostenible de desechos lignocelulósicos, la reducción de emisión de CO2, bajo aporte de energía, impacto ambiental débilmente adverso, y producción de productos de alto valor agregado(Limayem & Ricke, 2012).
II. METODOLOGÍA
Población y muestra
La muestra objeto de estudio fue el polvillo de arroz clasificado mediante tamaño de partícula (315, 400 y 500 µm) de la variedad INIAP-14, semillas mejoradas por el Instituto Nacional de Investigaciones Agropecuarias de Ecuador. Las muestras fueron recogidas en el sector arrocero denominado “La Cuca”, perteneciente al cantón Arenillas, provincia de El Oro-Ecuador. Coordenadas: 3°33´ S 80°04”0; 3°33´ S 80°04” O.
Diseño del experimento
El proceso de hidrólisis enzimática del polvillo de arroz se lo realizó mediante la utilización de las enzimas producidas por Trichoderma spp (Rana, Eckard, Teller, & Ahring, 2014), la cual se realizó a temperatura constante de 30°C y oxigenación el medio de cultivo (aireación mecánica). Se estudió el efecto de la concentración de sustrato y la concentración inóculo sobre la concentración de azucares reductores obtenidos. Se desarrolló un experimento factorial:
El factor A: Efecto de la concentración de sustrato, tuvo tres concentraciones: 8, 13 y 18%.
Factor B: Efecto de la concentración de inóculo, a tres concentraciones: 0,2, 0,4 y 0,6 g/L. A continuación, se detalla la combinación factorial del experimento.
| Factor A: % sustrato | Factor B: [ g/L ]inóculo | ||
| I1 | I2 | I3 | |
| S1 | S1I1 | S1I2 | S1I3 |
| S2 | S2I1 | S2I2 | S2I3 |
| S3 | S3I1 | S3I2 | S3I3 |
Al realizar un diseño de experimentos factorial, se desarrollaron 9 experimentos, a los cuales se les monitoreo las condiciones del proceso como temperatura, pH y agitación del medio de cultivo.
Se utilizó conidios del hongo Trichoderma spp liofilizado de la marca comercial Trichoeb® 5 WP, producido por Ecuabiologica. La adaptación se realizó en un Erlenmeyer de 500 mL que contenía 200 mL de sustrato (polvillo de arroz y agua destilada). Una vez homogénea la mezcla, se inoculó 0,2, 0,4 y 0,6 g/L de conidios del hongo crecidas en una solución de CMC al 4 %.
A partir de los datos obtenidos se realizó un análisis de varianza de los datos utilizando el sofware Statgraphics Plus 5. Posteriormente se hizo la representación gráfica mediante el sofware Origin. 50.
Preparación del material lignocelulosico
Los residuos lignocelulósicos, después de ser recolectados y seleccionados son molidos mediante la utilización del Molino Fritsch-pulverisette 19, y luego clasificados por tamaño de partícula. Este proceso es fundamental para aumenta el área de ataque por el hongo y mejora la eficiencia de la hidrólisis(Sánchez Riaño, Gutiérrez Morales, Muñoz Hernández, & Rivera Barrero, 2010).
Esterilización del hidrolizado
El polvillo de arroz, mezclado con agua purificada en porcentaje de 8, 13 y 18% m/v fue sometida a esterilización industrial (121°C * 15 min), con la finalidad hidrolizar parcialmente los almidones, celulosa, hemicelulosa y eliminar microorganismos que puedan interferir en el proceso.
Hidrólisis enzimática (Carbohidratos - azucares fermentables).
Al medio de cultivo se le inoculo 0,2, 0,4 y 0,6 g/L, conidios del hongo Trichoderma spp de acuerdo al experimento que correspondía. La hidrólisis del polvillo de arroz se llevó a cabo en 144 horas, lo cual dependió de la concentración de inóculo adicionado al medio (Dwivedi, Alavalapati, & Lal, 2009).
Filtración y pasteurización del hidrolizado enzimático
Culminado el proceso de hidrolisis enzimática, al cabo de 144 horas, se filtró el hidrolizado para retirar los carbohidratos no hidrolizados y se detoxificó añadiendo 0,1 g/L de cloruro de calcio di hidratado (CaCl2*2H2O) y se procedió a pasteurizar (75°C * 15 min) el medio para eliminar la presencia del hongo y sus clasmidospora (Bonilla, Armijos, & Calderón, 2015).
Fermentación alcohólica.
Al hidrolizado pasteurizado se le inoculó 4 g/L de levadura Saccharomyces cerevisiae Hansen 1883 (NCYC 366), se obtuvo de la Colección Española de Cultivos Tipo (CECT) de la Universidad de Valencia y se dejó fermentar por 72 horas, tiempo necesario para la fermentación alcohólica de los azucares fermentables, presentes en el hidrolizado(Philippidis, Smith, & Wyman, 1993).
Control del proceso de hidrólisis enzimatica
Determinación de Azucares Reductores.
Mediante la utilización del método de ácido 3,5-dinitrosalicilico por espectrofotometría UV-Visible, se cuantifico los azucares reductores totales, utilizando como estándar glucosa anhidra (Vásquez, 2010) el cual se basa en la reducción del ácido 3-5 dinitrosalicilico a 2 amino 5 nitro salicílico por la acción de azucares reductores (ácido galacturonico), el cual forma un color naranja de intensidad proporcional a los grupos reductores que reacciona y que presenta una máxima absorción a una longitud de onda de 540 nm (Detns et al., s. f.). Para la calibración del espectrofotómetro se realizó una curva de calibración con soluciones de glucosa a cinco concentraciones diferentes (2, 4, 6, 8 y 10 g/L), calculándose la recta de mejor ajuste por el método de los cuadrados cuya ecuación es y = 0,1928 X – 0,020459, y el coeficiente de correlación de R2 = 0,9918.
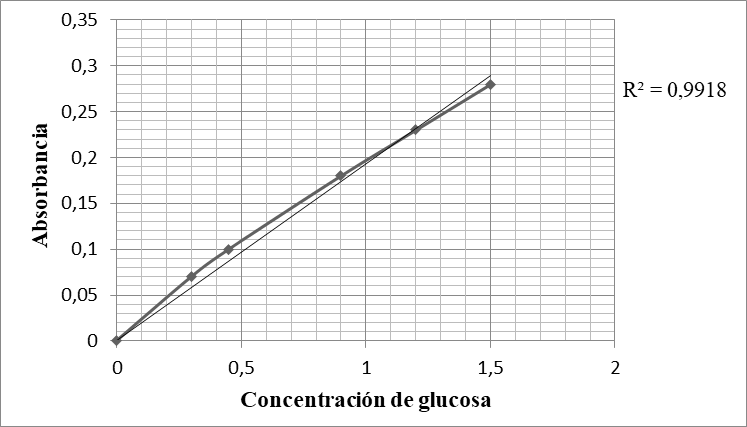
Figura 1.
Curva de calibración para azucares reductores.
Determinación de Etanol en el hidrolizado
Las concentraciones de etanol en el fermentado del hidrolizado se analizaron utilizando el Cromatógrafo de gases FULI 9790 II, con tiempo de retención de 1,300 min, respectivamente, utilizando una columna FULI Carbohydrates Ca, con agua como eluyente, a una temperatura de 90ºC, sobre un volumen de muestra de 10 μL, flujo de 0,5 mL/min, presión en la columna de 1,070 ± 0,10 (utilizar sistema internacional de medida kN, kPas, u otro) y sistema de detección de índice de refracción (De Queiroz et al., 2016).
III. RESULTADOS
Caracterización Química
Los resultados obtenidos en la caracterización química del polvillo de arroz utilizado como sustrato para la hidrólisis enzimática presento la siguiente composición
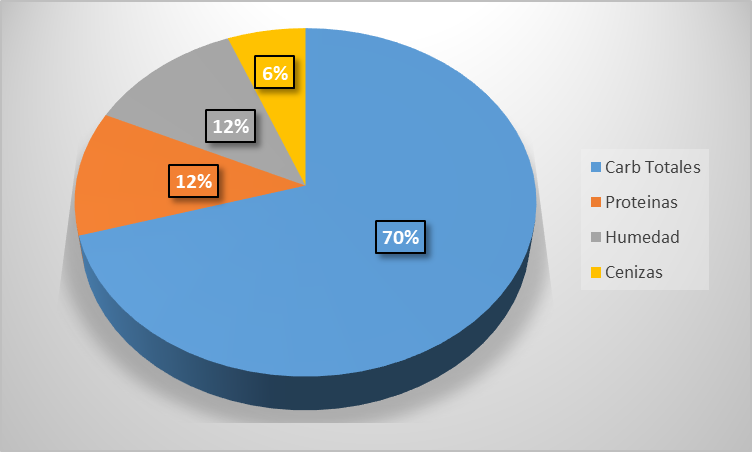
Figura 2
Composición polvillo de arroz.
El análisis del polvillo de arroz indica que existe un 70% de carbohidratos totales, los cuales están disponibles para bioconvertirse en azucares fermentables y posterior fermentación a etanol de segunda generación.
Determinación del pH de los experimentos, durante el tiempo de hidrólisis
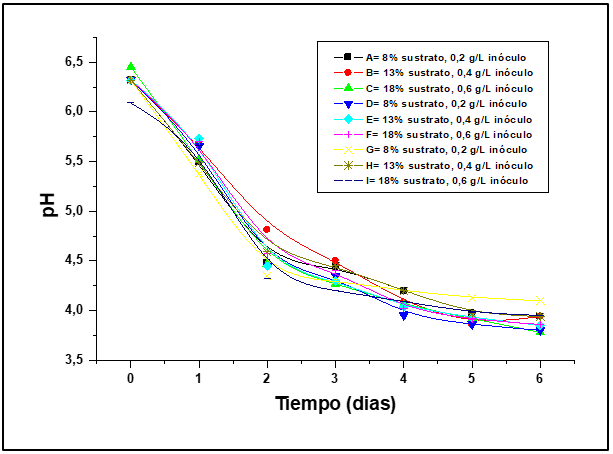
Figura 3
Determinación del pH de los 9 experimentos estudiados
La figura 3 muestra el descenso del pH durante el tiempo de hidrólisis del polvillo de arroz, el cual disminuye significativamente en los 9 tratamientos, en el mayor de los casos desde 6,32 –3,8 en el tratamiento D, estabilizándose después de 144 horas de hidrólisis en todos los tratamientos lo cual indica que el bioincremento micelial del hongo tiende a disminuir el pH del hidrolizado el cual se refleja en una desdoblación de azucares complejos en azucares simples como es la glucosa (Nitta et al., 2012).
Cuantificación de Glucosa en el Hidrolizado
En la hidrólisis enzimática se demuestra que la interacción entre la concentración de inóculo y concentración de sustrato tiene efecto significativo (p˂0,05) en la producción de glucosa tal como indica la tabla 2.
| Tratamientos | Media | Varianza | C. V. | N |
| A=15% sustrato, 0,2 g/L Inóculo | 4,32 | 0,08 | 1,85 | 3 |
| B=15% sustrato, 0,4 g/L Inóculo | 5,27 | 0,07 | 1,32 | 3 |
| C=15% sustrato, 0,6 g/L Inóculo | 5,10 | 0,01 | 0,19 | 3 |
| D=20% sustrato, 0,2 g/L Inóculo | 5,53 | 0,12 | 2,16 | 3 |
| E=20% sustrato, 0,4 g/L Inóculo | 8,24 | 0,06 | 0,72 | 3 |
| F=20% sustrato, 0,6 g/L Inóculo | 6,37 | 0,07 | 1,09 | 3 |
| G=25% sustrato, 0,2 g/L Inóculo | 5,13 | 0,02 | 0,38 | 3 |
| H=25% sustrato, 0,4 g/L Inóculo | 7,19 | 0,26 | 3,61 | 3 |
| I=25% sustrato, 0,6 g/L Inóculo | 9,69 | 0,18 | 1,85 | 3 |
| F = 91,08239 | ||||
| p = 5,66547E-13 | ||||
De acuerdo al análisis de varianza podemos ver que si existe diferencia estadísticamente significativa (p˂0,05) entre los 9 tratamientos estudiados, el tratamiento que produjo mayor concentración de azucares reductores fue el tratamiento I con 9,69%, cuya composición fue de 18 % de polvillo de arroz y 0,6 g/l de inóculo. Este hecho también se puede observar en la Figura 4, donde al aumentar la concentración de sustrato e inóculo se produce un incremento en la concentración de azucares reductores.
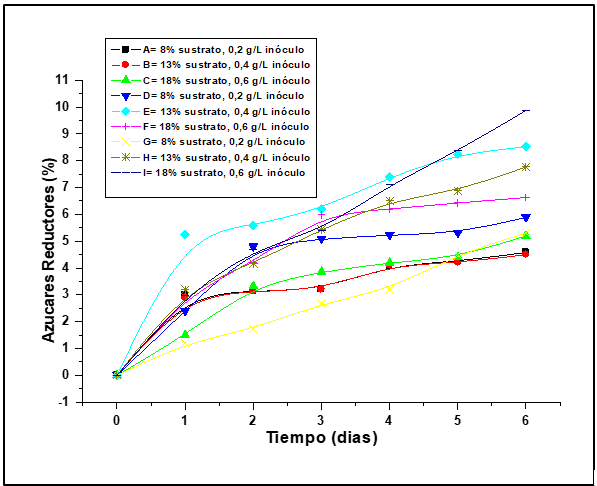
Figura 4
Incremento de la produción de azucares reductores en los 9 tratamientos
La Figura 4, muestra que existe interacción entre la concentración de sustrato e inóculo en la conversión de carbohidratos totales a azucares reductores, mayor cantidad de sustrato e inóculo mayor concentración de azucares, alcanzándose en el tratamiento I (18% sustrato, 0,6 g/L Inóculo) el 9,88% de AR. En la hidrólisis enzimática del polvillo de arroz utilizando el hongo Trichoderma spp, se obtuvo una concentración del 9,88% de AR, valores similares reportaron Saha et al. (2011), quienes consiguieron un contenido de glucosa del 9, 2% al hidrolizar paja de trigo(Chakraborty, Chowdhury, & Das Saha, 2011).
Determinación de etanol en las fermentaciones de los hidrolizados
La fermentación de los azúcares presentes en los hidrolizados de polvillo de arroz, es cercana al 100% en los 9 tratamientos estudiados, lo cual indica que el proceso de fermentación se desarrolló con eficiencia cercana al 100%.
La Figura 5 nos indica las concentraciones de etanol presentes en la fermentación de los hidrolizados de los 9 tratamientos (A, B, C, D, E, F, G, H e I).
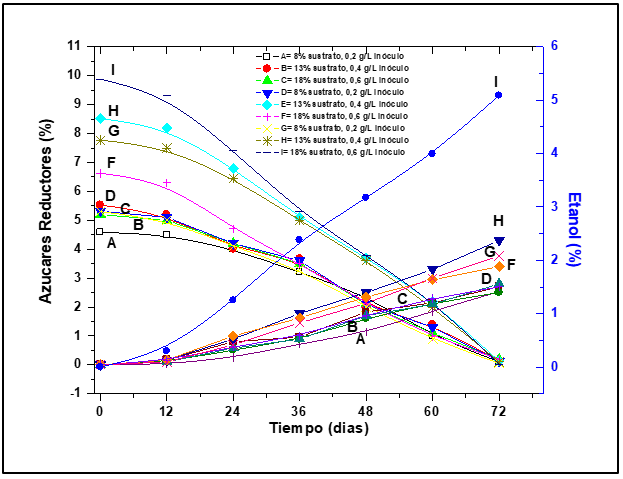
Figura 5
Concentración de azucares reductores VS concentración de etanol
La reducción de la concentración de azucares reductores en el proceso de fermentación es completa llegando a concentraciones residuales menores al 0,1 %, lo cual indica la conversión de los azucares reductores en etanol, alcanzándose concentraciones del 5 ,09 % en el tratamiento I (18 % de sustrato y 0,6 g/L de inóculo).
IV. CONCLUSIONES
La molienda aplicada al polvillo de arroz, redujo el tamaño de partícula (≤ 250 µm), aumento su densidad aparente, mejoro la solubilidad y aumento el área de ataque para el hongo, estudios similares en los que se realizaron pretratamientos como la molienda, se produjo una mejor solubilidad del polvillo con tamaño de partícula menor a 300 µm (Jamshidian, Golparvar, Naderi, & Darkhal, 2013).
El decrecimiento del pH en el medio de cultivo, brindó las condiciones óptimas de hidrólisis, ya que al aumentar el biocrecimiento miselar del hongo existió mayor actividad enzimática dando como resultado mayor concentración de azucares reductores (Singhania, 2011), el análisis de varianza aplicado al experimento indica que existe influencia directa en la concentración de inóculo y sustrato, a mayor concentración de sustrato e inóculo, se obtendrá mayor % de azucares reductores-etanol. La levadura (Saccharomyces cerevisiae) termoestable fue capaz de fermentar de manera eficiente todos los azucares reductores presentes en el hidrolizado a etanol, al inmovilizar la levadura que se produjo en el proceso de fermentación puede ser reutilizada con eficiencia cercana al 100%, reduciendo de esta manera los costos del proceso, reutilización similar proponen algunos investigadores (Cunha, Aguiar, Romaní, Oliveira, & Domingues, 2015).
Referencias
Bonilla, H. R., Armijos, H. A., & Calderón, B. L. (2015). Efecto de tres pre-tratamientos de cáscara de banano para la obtención de jarabe glucosado mediante hidrólisis enzimática. Avances en Química, 10(1), 79-82.
Chakraborty, S., Chowdhury, S., & Das Saha, P. (2011). Adsorption of Crystal Violet from aqueous solution onto NaOH-modified rice husk. Carbohydrate Polymers, 86(4), 1533-1541. https://doi.org/10.1016/j.carbpol.2011.06.058
Cunha, J. T., Aguiar, T. Q., Romaní, A., Oliveira, C., & Domingues, L. (2015). Contribution of PRS3, RPB4 and ZWF1 to the resistance of industrial Saccharomyces cerevisiae CCUG53310 and PE-2 strains to lignocellulosic hydrolysate-derived inhibitors. Bioresource Technology, 191, 7-16. https://doi.org/10.1016/j.biortech.2015.05.006
De Queiroz, D. P., Florentino, A. D. O., Bruno, J. C., Da Silva, J. H. D., Riul, A., & Giacometti, J. A. (2016). The use of an e-tongue for discriminating ethanol/water mixtures and determination of their water content. Sensors and Actuators, B: Chemical, 230, 566-570. https://doi.org/10.1016/j.snb.2016.02.080
Detns, R. C., Taken, S., Co, F. S., Smith, F., Co, C., & Titrim-, F. (s. f.). Use of DinitrosaIicyIic Acid Reagent for Determination of Reducing Sugar. Analytical Chemistry, (lll).
Diego, S. (2015). Application of the Direct Quadrature Method of Moments for the modelling of the enzymatic hydrolysis of cellulosic substrates. Chemical Engineering Science, 149, 1-20. https://doi.org/10.1016/j.ces.2016.04.029
Dwivedi, P., Alavalapati, J. R. R., & Lal, P. (2009). Cellulosic ethanol production in the United States: Conversion technologies, current production status, economics, and emerging developments. Energy for Sustainable Development, 13(3), 174-182. https://doi.org/10.1016/j.esd.2009.06.003
Greene, E. R., Himmel, M. E., Beckham, G. T., & Tan, Z. (2015). Glycosylation of Cellulases: Engineering Better Enzymes for Biofuels. Advances in Carbohydrate Chemistry and Biochemistry (1.a ed., Vol. 72). Elsevier Inc. https://doi.org/10.1016/bs.accb.2015.08.001
Jamshidian, P., Golparvar, A. R., Naderi, M. R., & Darkhal, H. (2013). Phenotypic correlations and path analysis between ear yield and other associated characters in corn hybrids ( Zea mays L .). International Journal of Farming and Allied Sciences, 2(S), 1273-1276.
Jiang, L., Zheng, A., Zhao, Z., He, F., Li, H., & Wu, N. (2016). The comparison of obtaining fermentable sugars from cellulose by enzymatic hydrolysis and fast pyrolysis. Bioresource Technology, 200, 8-13. https://doi.org/10.1016/j.biortech.2015.09.096
Kellock, M., Maaheimo, H., Marjamaa, K., Rahikainen, J., Zhang, H., Holopainen-Mantila, U., … Kruus, K. (2019). Effect of hydrothermal pretreatment severity on lignin inhibition in enzymatic hydrolysis. Bioresource Technology, 303-312. https://doi.org/10.1016/j.biortech.2019.02.051
Li, X., Li, M., Pu, Y., Ragauskas, A. J., Klett, A. S., Thies, M., & Zheng, Y. (2018). Inhibitory effects of lignin on enzymatic hydrolysis: The role of lignin chemistry and molecular weight. Renewable Energy, 123, 664-674. https://doi.org/10.1016/j.renene.2018.02.079
Limayem, A., & Ricke, S. C. (2012). Lignocellulosic biomass for bioethanol production: Current perspectives, potential issues and future prospects. Progress in Energy and Combustion Science, 38(4), 449-467. https://doi.org/10.1016/j.pecs.2012.03.002
Nan, Y., Yang, M., Xin, D., Li, K., Kuittinen, S., Pappinen, A., & Zhang, J. (2019). Acetone-butanol-ethanol solvents improved enzymatic hydrolysis of pretreated energy grass. Fuel, 245(February), 406-412. https://doi.org/10.1016/j.fuel.2019.02.043
Nitta, M., Furukawa, T., Shida, Y., Mori, K., Kuhara, S., Morikawa, Y., & Ogasawara, W. (2012). A new Zn(II) 2Cys 6-type transcription factor BglR regulates ??-glucosidase expression in Trichoderma reesei. Fungal Genetics and Biology, 49(5), 388-397. https://doi.org/10.1016/j.fgb.2012.02.009
Philippidis, G. P., Smith, T. K., & Wyman, C. E. (1993). Study of the enzymatic hydrolysis of cellulose for production of fuel ethanol by the simultaneous saccharification and fermentation process. Biotechnology and bioengineering, 41(9), 846-853. https://doi.org/10.1002/bit.260410903
Raele, R., Boaventura, J. M. G., Fischmann, A. A., & Sarturi, G. (2014). Scenarios for the second generation ethanol in Brazil. Technological Forecasting and Social Change, 87, 205-223. https://doi.org/10.1016/j.techfore.2013.12.010
Rana, V., Eckard, A. D., Teller, P., & Ahring, B. K. (2014). On-site enzymes produced from Trichoderma reesei RUT-C30 and Aspergillus saccharolyticus for hydrolysis of wet exploded corn stover and loblolly pine. Bioresource Technology, 154, 282-289. https://doi.org/10.1016/j.biortech.2013.12.059
Ren, N. Q., Zhao, L., Chen, C., Guo, W. Q., & Cao, G. L. (2015). A review on bioconversion of lignocellulosic biomass to H2: Key challenges and new insights. Bioresource Technology. https://doi.org/10.1016/j.biortech.2016.03.124
Salanti, A., Zoia, L., Tolppa, E. L., & Orlandi, M. (2012). Chromatographic detection of lignin-carbohydrate complexes in annual plants by derivatization in ionic liquid. Biomacromolecules, 13(2), 445-454. https://doi.org/10.1021/bm2014763
Sánchez Riaño, A. M., Gutiérrez Morales, A. I., Muñoz Hernández, J. A., & Rivera Barrero, C. A. (2010). Producción de bioetanol a partir de subproductos agroindustriales lignocelulósicos Bioethanol Production from agroindustrial lignocellulosic byproducts. Tumbaga, 5, 61-91.
Santos Michel, R. J., Canabarro, N. I., Alesio, C., Maleski, T., Laber, T., Sfalcin, P., … Mazutti, M. A. (2016). Enzymatic saccharification and fermentation of rice processing residue for ethanol production at constant temperature. Biosystems Engineering, 142, 110-116. https://doi.org/10.1016/j.biosystemseng.2015.12.013
Seiboth, B., Verena, C. I., & Seibot, S.-. (2011). Trichoderma reesei: A Fungal Enzyme Producer for Cellulosic Biofuels, Biofuel Production-Recent Developments and Prospects. Biotechnology for biofuels, 6(1), 127. https://doi.org/10.5772/959
Shokrkar, H., Ebrahimi, S., & Zamani, M. (2018). Enzymatic hydrolysis of microalgal cellulose for bioethanol production, modeling and sensitivity analysis. Fuel, 228(April 2017), 30-38. https://doi.org/10.1016/j.fuel.2018.04.143
Singhania, R. R. (2011). Production of celluloytic enzymes for the hydrolysis of lignocellulosic biomass. Biofuels, 177-201. https://doi.org/10.1016/B978-0-12-385099-7.00008-5
Sofía, Á., & Paz, P. (s. f.). Efecto de enzimas comerciales en la hidrólisis de residuos de cosecha de la caña de azúcar Pre-tratados con órgano-solvente.
Vásquez, M. (2010). Diseño del sistema de control para un biorreactor de tanque agitado, 14-16.
Wu, X., Zhang, J., Xu, E., Liu, Y., Cheng, Y., Addy, M., … Ruan, R. (2016). Microbial hydrolysis and fermentation of rice straw for ethanol production. Fuel, 180, 679-686. https://doi.org/10.1016/j.fuel.2016.04.087
Zhang, Haibo, Zhang, P., Ye, J., Wu, Y., Liu, J., Fang, W., … Zeng, G. (2018). Comparison of various pretreatments for ethanol production enhancement from solid residue after rumen fluid digestion of rice straw. Bioresource Technology, 247, 147-156. https://doi.org/10.1016/j.biortech.2017.09.065
Zhang, Hongdan, Wu, S., & Xie, J. (2017). Evaluation of the effects of isolated lignin on enzymatic hydrolysis of cellulose. Enzyme and Microbial Technology. https://doi.org/10.1016/j.enzmictec.2017.03.001