Artículos Científicos
Diagnóstico de la presencia de Badnavirus en las plantaciones bananeras de la Provincia de El Oro
Diagnóstico de la presencia de Badnavirus en las plantaciones bananeras de la Provincia de El Oro
Revista Ciencia Unemi, vol. 13, núm. 32, pp. 100-108, 2020
Universidad Estatal de Milagro

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.
Recepción: 08 Julio 2019
Aprobación: 30 Octubre 2019
Resumen: El Virus del rayado del Banano (BSV) perteneciente al Género Badnavirus, causa grandes pérdidas en el rendimiento productivo de las bananeras, es un agente infeccioso que se disemina por medio de la siembra de material infectado y a través de las cochinillas Pseudococcidae, es responsable de importantes pérdidas en la rentabilidad y un grave inconveniente en el mejoramiento genético de Musa sp. La ausencia de una técnica altamente sensible y específica para identificar las plantas afectadas, ha posibilitado que el virus del rayado del banano esté diseminándose en las plantaciones. Por lo tanto, para lograr una correcta identificación de las plantas afectadas por el Virus del Rayado del Banano, se planteó el siguiente objetivo: Diagnosticar la presencia de Badnavirus en las plantaciones bananeras de la provincia de El Oro. Los extractos totales de ácidos nucleicos de banano fueron obtenidos con CTAB al 2% con el cual se obtiene un ADN molde apropiado para el análisis de Reacción en cadena de la Polimerasa. Utilizando un par de primers que flanquean una región de 221 pb que corresponde al gen de la transcriptasa inversa y RNasa H del ORF 3 de los badnavirus. Con el uso de esta metodología fue posible determinar la existencia de este virus en el 89.36 % de las plantaciones evaluadas, en la Provincia de El Oro.
Palabras clave: Badnavirus, Diagnóstico, extracción de ADN, CTAB, PCR, primers.
Abstract: Banana Streak Virus (BSV), belonging to genus Badnavirus, causes great yield losses in banana. It is an infectious agent that spreads through the seeding of infected material and through mealybugs (Pseudococcidae). It is responsible for significant losses in profitability and a serious constraint in the genetic improvement of Musa sp. The absence of a highly sensitive and specific technique to identify the affected plants has enabled it to be disseminated in the plantations. Therefore, to achieve a correct identification of the plants affected by Badnavirus the following objective was proposed: Diagnose the presence of Badnavirus in the banana plantations of the province of El Oro. Total Nucleic Acid Extracts of banana were obtained with 2% CTAB with which a suitable template DNA was obtained for the analysis of the polymerase chain reaction. Using a pair of primers that flank a region of 221 bp that corresponds to the gene of the reverse transcriptase and RNase H of the ORF 3 of the badnaviruses. With the use of this methodology, it was possible to determine the existence of this virus in 89.36% of the plantations evaluated.
Keywords: Badnavirus, Diagnostic, DNA extraction, CTAB, PCR, primers.
I. INTRODUCCIÓN
El banano es un cultivo de gran importancia económica para nuestra provincia, ya que representa su principal actividad agrícola y es una importante fuente de ingreso económico para los pequeños y grandes productores, y la principal para las familias que trabajan en las fincas donde se produce.
En el Ecuador se cultivan alrededor de 200000 Ha de banano, el mismo que es atacado por una variedad de plagas y enfermedades, entre las cuales se encuentra la causada por el Virus del rayado del Banano, el cual es el virus de mayor importancia económica presente en las plantaciones de nuestro país.
La importancia de dar a conocer el peligro que representa este virus radica en que este es un virus que puede llegar a ocasionar la pérdida de la productividad del cultivo entre el 7 y el 90 % y se transmite primordialmente de forma vegetativa al 100 % de la progenie y por medio de las cochinillas, puesto que esta es la principal manera de propagación de banano y las cochinillas un insecto que se encuentra comúnmente en las bananeras lo convierte en una gran amenaza para industria bananera de nuestra provincia.
Para Kumar (2014) El Virus del rayado del banano es un Pararetrovirus perteneciente a Género Badnavirus de la Familia Caulimoviridae. Las partículas virales son baciliformes, de 120-150*30 nm de tamaño, poseen un ADN circular no covalentemente cerrado de doble cadena de aproximadamente 7.2 a 7.8 Kpb de longitud que usa una transcriptasa inversa codificada por el virus para replicarse,
Por otro lado King (2012) dice que el genoma contiene tres marcos de lectura abierta ORFs. La función de la proteína P1 es desconocida, P2 es la proteína asociada al virión y P3 es una poliproteina, con proteína de movimiento, proteína de cápside, proteasa apartica y transcriptasa inversa /Rnasa H1, es ese orden.
Mientras que Geering et al (2001) analizaron la distribución y estructura del ADN de BSV integrado en un rango de cultivares de Musa y sus resultados mostraron fuerte evidencia de que las secuencias integradas de BSV-OL están asociadas con el genoma B de las Musa cultivadas. Ellos no fueron capaces de detectar BSV-OL en un rango de cultivares del grupo AAA, así como en Calcuta 4.
El objetivo de este trabajo fue determinar la presencia de Badnavirus en las plantaciones bananeras de la provincia de El Oro.
II. MATERIALES Y MÉTODOS
Las muestras fueron recogidas en 47 fincas de los cantones Machala, Pasaje, El Guabo, Santa Rosa y Arenillas, donde se produce banano en la provincia de El Oro. Para el muestreo las fincas fueron clasificadas como Tecnificadas, Semitecnificadas y No Tecnificadas.
Las muestras de hojas fueron tomadas de plantas que mostraban síntomas de BSV, tal como los descritos por Diekmann y Putter (1996) y por Daniells et al. (1999). La muestra correspondió a una parte de la hoja que mostraba síntomas de rayado clorótico, de aproximadamente 30 x 40 cm.
Embalaje de la muestra.
Las muestras fueron envueltas en papel periódico humedecido y colocadas dentro de una funda plástica como lo recomendado por Thomas, Caruana y Jones (1994). Luego estas muestras fueron guardadas a –20oC y examinadas posteriormente.
EXTRACCIÓN DE ADN
Se
Se realizó la extracción de ADN con el método descrito por Zhang (1998) que se resume:
-
- Buffer CTAB (2 % CTAB, 20 mM EDTA, 100 mM Tris-HCl pH 8.0, 0.2 % mercaptoetanol).
- Se tomó aproximadamente 1 cm2 de tejido foliar y se lo introdujo en un microtubo de 1.5 mL.
- Se agregó N2 líquido hasta cubrir la muestra y se maceró directamente en el tubo hasta que se consumió el nitrógeno, en los casos que fue necesario se volvió a agregar nitrógeno a la muestra.
- Se agregó 800 uL oC a los tejidos macerados y se mezcló en un vortex.
- La mezcla entera fue mantenida a 60 oC por 20 min. Durante la incubación la mezcla fue puesta en el vortex varias veces.
- Después de la incubación se agregó 600 uLla mezcla cloroformo:alcohol isoamilico (24:1) helado, se agitó vigorosamente la mezcla en un vortex, y se centrifugó a 13000 rpm por 5 min.
- Se transfirió 400 uL isopropanol helado y se colocó la mezcla en hielo durante 10 min.
- Se centrifugó a velocidad máxima por 8 min y se descartó la fase acuosa.
- Se enjuagó el pellet con etanol al 80 %, se dejó secar al ambiente y luego se resuspendió en 50- 100 uL de agua ultrapura o en TE. Esta preparación fue usada para PCR.
REACCIÓN EN CADENA DE LA POLIMERASA (PCR).
niciadores basados sobre secuencias conservadas de la transcriptasa inversa de ScBV y BSV (Braithwaite, 1995)fueron utilizados
Iniciadores basados sobre secuencias conservadas de la transcriptasa inversa de ScBV y BSV (Braithwaite, 1995)fueron utilizados
Primer ScBV F5
5’ TCA AAG TTT GAT TTG AAG AGC GGG 3’
Primer ScBV R5
5’ CTC CGA GAA AAC CAA TAT GTC ATC 3’
La PCR fue realizada, de acuerdo a las indicaciones del autor Braithwaite (1995). El ADN más los iniciadores fueron hervidos por 5 min en un microtubo de 1.5 ml, en total 3 uL fueron colocados en cada tubo por muestra, y luego enfriados sobre hielo, en seguida se centrifugaron y 3 uL del volumen final fueron puestos en el tubo de PCR, el mix de PCR contenía 5 uL de Buffer (10 x), 8 uL del Cl2Mg (25 mM), 4 uL de dNTPs, 0,2 uL de Taq polimerasa, más la mezcla de los iniciadores y el ADN en un volumen final de 50 uL.
El programa de PCR utilizado fue el siguiente:
1 ciclo 94 0C por 7 min
3 ciclos 94 0C por 30 seg
50 0C por 30 seg
72 0C por 1 min
37 ciclos 94 0C por 30 seg
55 0C por 30 seg
72 0C por 1 min
1 ciclo 72 0C por 7 min
10 0C por
Los productos de la PCR fueron separados en un gel de agarosa de 1,5 % de concentración teñido con 0.8 uL de Bromuro de Etidio (15 mg/ml).
III. RESULTADOS Y DISCUSIÓN
Las muestras comprendieron los principales clones que son cultivados en la provincia, como son los del subgrupo Cavendish, entre ellos Cavendish gigante, Cavendish enano y Valery, en menor número Filipino y Grand nain, todos estos pertenecientes al grupo genómico AAA.
| Nivel de Tecnificación | Machala | Pasaje | El Guabo | Santa Rosa | Arenillas | Total |
| Tecnificadas | 4 | 7 | 6 | 1 | 1 | 19 |
| Semitecnificadas | 7 | 2 | 0 | 3 | 0 | 12 |
| No-tecificadas | 11 | 2 | 0 | 1 | 2 | 16 |
| Total | 22 | 11 | 6 | 5 | 3 | 47 |
Los síntomas observados en el muestreo oscilaron desde leves a severos con rayas cloróticas, vainas foliares exteriores partidas y distorsión general de la filotaxia siendo los vistos con mayor frecuencia, seguidos por rayado necrótico, rayas color marrón, hoja cigarro necrótica, líneas anchas de color amarillo a lo largo de la hoja, también se observó otros síntomas como rayado clorótico-necrótico, margen púrpura de las hojas, manchas color café en el peciolo, tejido necrótico en la sección transversal del pseudotallo, pecíolos partidos, hipertrofia de las nervaduras secundarias, racimo deforme y puntas de las hojas arrugadas.

Figura 1.
Síntomas característicos de las plantas muestreadas, en a se observa una alteración de la filotaxia, en b y en c un rayado clorótico discontinuo, las tres sobre una planta de Grand nain.
Extraccion de ADN
Con este protocolo se realizó la extracción de ADN de todas las muestras y se observó una cantidad y calidad de ADN apropiadas para el análisis por PCR como se muestra en las figuras 2. Los análisis de PCR fueron realizados a partir de las extracciones de ADN realizadas con este protocolo.
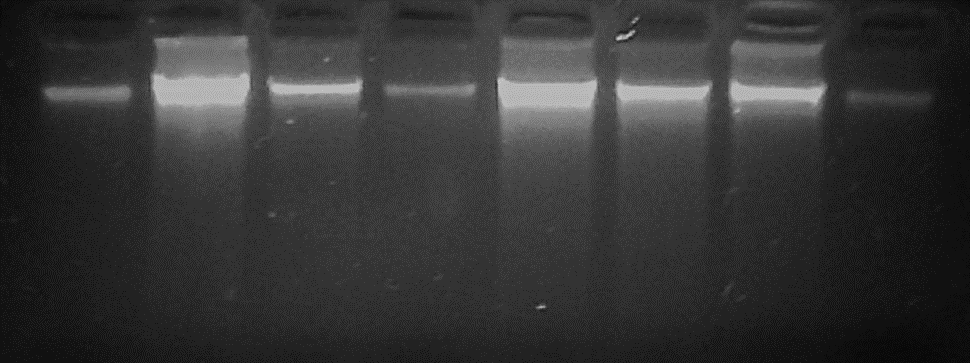
Figura 2
Migración de los extractos totales de ácidos nucleicos teñidos con bromuro de etidio (BE) de varias muestras de banano (Musa sapientum,) extraídos con el protocolo de Zhang (1998), sobre un gel de agarosa de 1.5 %, luego de un tratamiento con RNAsa.
PCR con los iniciadores de Braithwaite, ScBV F5 y ScBV R5, utilizando las recomendaciones delineadas por el mismo autor, luego de la extracción de ADN utilizando el protocolo de Zhang, dio como resultado la amplificación del fragmento de ADN esperado correspondiente al gen de la Transcriptasa inversa del ORF III del genoma del virus de 221 pb, como se muestra en la fig. 3
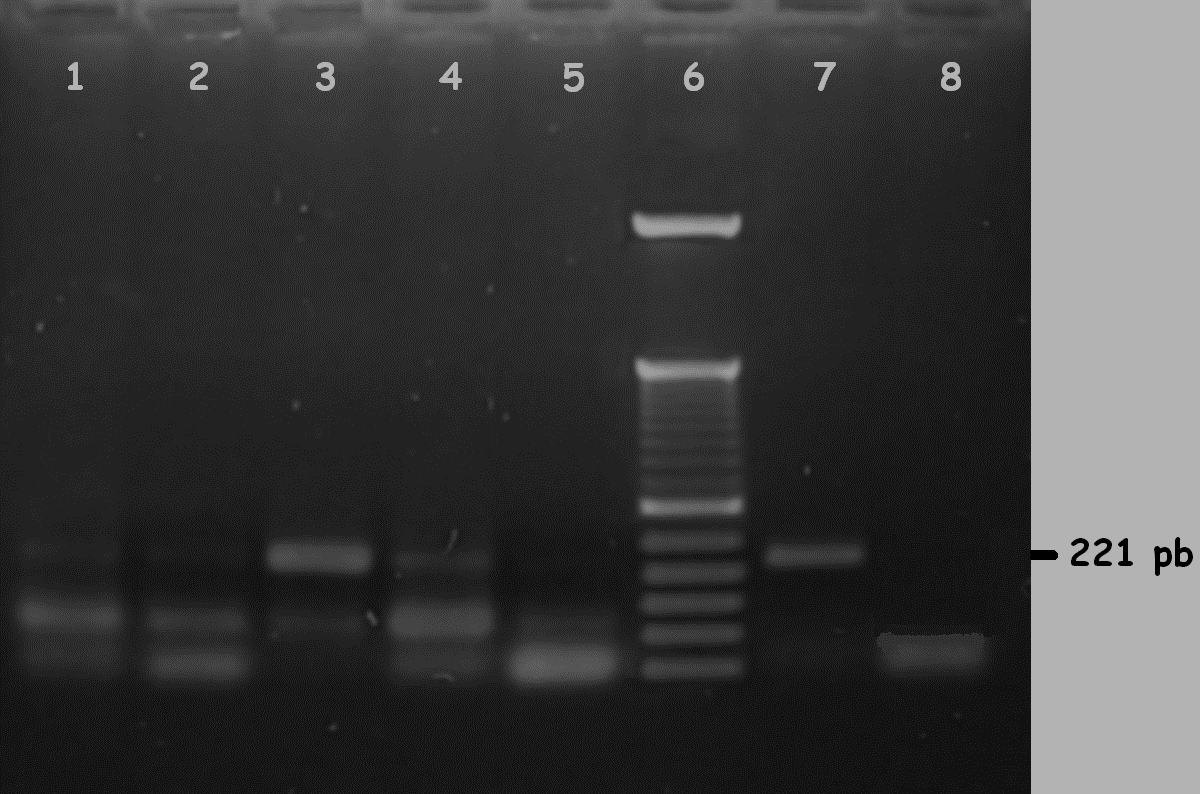
Figura 3
Foto de un gel de electroforesis de 1.5 % de agarosa en el que se muestra la migración de los amplicones de una PCR con los iniciadores ScBV F5 y ScBV R5, y el fragmento de amplificación esperado de 221 pares de bases de 5 muestras de Banano Musa sp AAA, pozos 1 a 5, 6) Marcador de peso molecular de 50 pb, 7) control positivo, 8) control negativo.
En resumen se pudo confirmar que de 103 muestras colectadas en el campo, correspondientes a plantas que mostraban síntomas de estar infectadas por BSV, solo 72 dieron resultados positivos a la infección por un Badnavirus (BSV o ScBV) lo cual representa el 69.9 % del total. De las 47 fincas visitadas en la zona bananera de la provincia de El Oro se encontró la presencia de Badnavirus en 42 de estas lo que representa el 89,36 % del número total de fincas, como se aprecia en el cuadro 2, de las cuales 19 eran tecnificadas, 12 semitecnificadas y 16 no tecnificadas.
| Número | Positivo | Negativo | |
| Fincas | 47 | 89,36% | 10,64% |
| Muestras | 103 | 69,90% | 30,10% |
En el cuadro 3 se ha resumido una lista de los síntomas encontrados con mayor frecuencia en las plantas que resultaron positivas a una infección por BSV luego de realizados los análisis de PCR.
| Síntoma | Frecuencia | ||
| Rayado clorótico | 56 | ||
| Distorsión general de la filotaxia | 28 | ||
| Vainas del pseudotallo partidas | 27 | ||
| Rayado color café del pseudopeciolo | 13 | ||
| Rayas color marrón | 13 | ||
| Rayado necrótico | 11 | ||
| Hoja cigarro necrótica | 6 | ||
| Hojas Arrugadas | 6 | ||
| Líneas amarillas anchas a lo largo de la nervadura central | 4 | ||
| Manchas necróticas | 3 | ||
| Tejido necrótico en la sección transversal | 3 | ||
| Rayado clorótico-necrótico | 2 | ||
En el presente estudio hemos diagnosticado la presencia de Badnavirus en las plantaciones bananeras de la provincia de El Oro, utilizando como método la reacción en cadena de la polimerasa (PCR por sus siglas en inglés) realizada a partir de extractos totales de ácidos nucleicos descrita por Ferreira (1998); Curtis (2001); Lodish, (2002) y Naidu (2000). También confirmamos reportes anteriores de la presencia de BSV en Ecuador, por medio de la Biología Molecular.
Los síntomas observados sobre las plantas muestreadas fueron muy variables como se puede observar en el cuadro 3, pero se enmarcaron dentro de los descritos por los autores citados Lockhart(1993); Lockhart (19959; Diekmann (1996); Daniells (1999); Jones (2000); Harper (2002).
Aunque existe evidencia de la presencia de sustancias inhibidoras de la PCR cuando esta se realiza a partir de purificaciones de ADN no apropiadas para este proceso Li(1994); Lockhart, (1995), en esta investigación hemos sido capaces de superar este inconveniente, y otro, que es la utilización de tediosos y largos procesos de purificación de ADN, con el uso del procedimiento de Zhang (1998). Lo primero es demostrado por la consistente amplificación del fragmento de ADN esperado y lo segundo por el corto tiempo utilizado en la extracción de ADN de cada muestra.
En tanto que la integración del genoma de BSV en el genoma de Musa ha sido publicada por Harper(1999); Ndowora (1999); Geering (2001), el hecho de que en este estudio utilizáramos iniciadores para ScBV y no para la cepa integrada, y no existan reportes de ScBV integrado en el genoma de Musa, más lo demostrado, de que la forma integrada completa está en el genoma B y este se encuentre ausente de los clones del subgrupo Cavendish, el cual es el que se cultiva en nuestra provincia, la no-amplificación del control negativo y la existencia de muestras negativas es evidencia de que no estamos amplificando secuencias integradas en el genoma A de Musa.
Ya que el origen de los bananos cultivados en El Oro es muy diverso, y la propagación clonal es un factor muy importante en la diseminación de la enfermedad, sumado a que es un cultivo que ha estado establecido durante más de 60 años, entonces, surge la posibilidad de que se encuentren numerosos aislados de BSV infectando banano y que al igual que en Uganda Harper, (1998) la variabilidad genética sea muy grande, lo cual impida que seamos capaces de detectar todos las cepas.
Por otro lado, ya ha sido mencionada la capacidad que tiene ScBV de infectar banano a través de las cochinillas Planococcus citri y Saccharicoccus sacchari (Diekmann et al 1996; Lockhart et al 1999; Lockhart, 1998), lo cual hay que tener muy en cuenta ya que a menudo se puede encontrar plantas de caña de azúcar (Saccharum officinarum) en los linderos y en pequeñas huertas dentro de las bananeras en El Oro, y el hecho de que se ha demostrado que está universalmente infectada con ScBV y es hospedera de la cochinilla rosada de la caña de azúcar (Saccharicoccus sacchari)(Jones et al 2000) la convierte en una potencial fuente de inóculo para banano, lo mismo ocurre con el plátano ya que este tiene integrado el genoma de BSV y bajo ciertas condiciones de stress este podría manifestarse, convirtiéndolo también en una fuente de inóculo.
Asimismo se ha indicado que las cochinillas vectores de Badnavirus incluyen especies de Pseudococcus, Planococcus, Planococcoides, Ferrisia, Saccharicoccus y Dysmicoccus (Lockhart, 1995) y de acuerdo al estudio realizado por Armijos y Silva (2004) especies de los géneros Dysmicoccus y Pseudococcus son encontradas en las bananeras del Ecuador, y con la observación hecha en nuestro País, de que estas son llevadas por hormigas (Jones et al 2000), aumenta el riesgo de un brote de BSV, entonces el verdadero rol que juegan las cochinillas y las hormigas en la diseminación de BSV en una plantación de Banano en el Ecuador debe ser establecido.
Para poder lograr un diagnóstico confiable de Badnavirus en las bananeras del Ecuador es necesario, como lo mencionado por Lockhart (1995), tener la capacidad de detectar todos los aislados existentes en el campo, y para llegar a hacerlo se necesita realizar una caracterización genómica de los aislados presentes en las plantaciones bananeras, para de esta forma poder tener un conocimiento de la variabilidad genética de BSV en el Ecuador y constatar si la variabilidad genética presente en Uganda ocurre también en otras partes..
IV. CONCLUSIONES
En base al análisis genético molecular realizado en este estudio se concluye que:
La enfermedad del rayado del banano, causada por un Badnavirus, se encuentra presente en las bananeras de la provincia de El Oro.
Y por lo tanto se recomienda:
-
- No cultivar caña de azúcar (Saccharum officinarum), junto con banano, ya que esta podría ser fuente de inóculo de ScBV.
- No cultivar plátano (Musa AAB), o algún otro híbrido con constitución genómica B, en estrecha proximidad con banano, ya que bajo ciertas condiciones de stress estas plantas podrían convertirse en fuente de inóculo de BSV.
- Eliminar aquellas plantas que muestren síntomas de estar infectadas con BSV, y las plantas sin síntomas que las rodean.
- En caso de realizar una plantación a partir de plantas obtenidas por cultivo de meristemas, estas deben estar certificadas como libres de enfermedades virales, de cualquier tipo que sean.
- Para la realización de las resiembras, se recomienda que el material a utilizarse sea obtenido de un lote que no haya manifestado síntomas de enfermedad por un lapso de al menos dos años.
- Hay que realizar un buen control de las poblaciones de cochinillas Homoptera: Pseudococcidae, ya que estas son el vector de la enfermedad.
V. REFERENCIAS BIBLIOGRÁFICAS
Agrios, G. (1998). Fitopatología. Mexico: Limusa.
Armijos, M. (2004). Ciclo de vida de los piojos harinosos (cochinillas harinosas) del Banano y plátano en el Ecuador. Guayaquil: inIAP-PROMSA.
Braithwaite, K. E. (1995). Detection of sugarcane bacilliform virus using the polymerase chain reaction. Plant Disease.
Caruana, m. L. (1998). Activities of CIRAD virus indexing centre. Montpellier: INIBAP.
Curtis, H. B. (2001). Biología (6 ed.). España: Medica Panamericana.
Dahal, G. O. (2000). Relationship between natural occurrence of banana streak virus and symptom expression, relative concentration of viral antigen, and yield characteristics of some micropropagated Musa spp. Plant Pathology., Vol. 49.
Dahal, G. P. (1998). Studies on a Nigerian isolateof banana streak badnavirus: Effect of intraplanr variation on virus accumulation and reliability of diagnosis by ELISA . Ann. Appl. Biol, Vol. 132.
Daniells, J. G. (2001). The effect of banana streak virus on the growth and yield of dessert bananas in tropical Australia. Ann. Appl. Biol., Vol. 139
Daniells, J. T. (1999). Banana streak disease. An ilustrated field guide. Australia: : Department of primary industries.
Diekmann, M. (1996). Technical guidelines for the safe movement of germplasm (2 ed.). Rome: IPGRI, Ed.
Dietzgen, R. T. (1999). PCR-based detection of viruses in banana and sugarcane. Current topics in Virology, Vol. 1.
Ferreira, M. (1998). Introducción al uso de marcadores moleculares en el análisis genético. Brasilia: EMBRAPA
Frison, E. S. (1998). The economic, social and nutritional importance of banana in the world. Cameroon.
Garcia, M. R. (2012). Viral Genomes - Molecular Structure, Diversity, Gene Expression Mechanisms and Host-Virus Interactions. . InTech.
Harper, G. H. (1998). Cloning and sequence analysis of banana Streak Virus DNA. . Virus Genes, Vol. 17.
Harper, G. H. (2002). Detection of banana streak virus in field samples from Uganda. . Ann. Appl. Biol., Vol. 141.
Harper, G. H. (2004). Banana streak virus is very diverse in Uganda . Virus Research, Vol. 100.
Harper, G. O.-H. (1999). Integration of Banana streask virus into the Musa genome: Molecular and citogenetic evidence. . Virology, Vol. 255.
Hernandez, P. A. (2011). Polymerase Chain Reaction:Types, Utilities and Limitations. intechopen, Ed.
Jones, D. (2000). Diseases of Banana, Abaca and Enset (Vols. Introduction toof Banana, Abaca and Enset. Worcestershire: C. publishing, Ed.
Jones, D. (2000). Diseases caused by viruses. Banana streak. Worcestershire: CABI publishing.
Khumallambam, D. K. (2013). An efficient protocol for total DNA extraction from the members of order Zingiberales- suitable for diverse PCR based downstream applications. Springer.
King, A. A. (2012). Virus taxonomy: Ninth report of the International Commitee on taxonomy of viruses. New York: Elsevier.
Kumar, L. S. (2014). Biology, Etiology, and Control of Virus Diseases of Banana and Plantain. . Elsevier.
Lassoudière. (1979).
Li, Q. C. (1994). A DNA extraction method for RAPD analysis from plants rich in soluble polysacharides. Plant Molecular Biology., Vol. 123.
Lockhart, B. (1993). Serological and genomic heterogeity of banana streak badnavirus: implications for virus detections in Musa germplasm. . Montpellier: CIRAD- FLHOR.
Lockhart, B. (1995). Banana streak badnavirus infection in Musa: Epidemiology, diagnosis and control. Taipei: F. a. Technology, Ed.
Lockhart, B. (1998). Management of viral sreak in banana and plantain: Understandong a new challenge. Davao: (INIBAP, Ed.
Lockhart, B. (1999). Badnaviruses.
Lodish, H. B. (2002). . (). Biología celular y molecular (4 ed.). España: Editorial Medica Panamericana.
Muylle, H. (1998). Development of techniques for the elimination of virus diseases from Musa:Progress Report. . Montpellier: INIBAP.
Naidu, R. H. (2000). Methods for the detection of plant virus diseases. Plant virology in sub-Saharan Africa.
Ndowora, T. D. (1999). Evidence that badnavirus infection in Musa can originate from integrated pararetroviral sequences. Virology, Vol. 255.
Pulimamidi, R. N. (2012). Gel-Electrophoresis and Its Applications. Hyderabad: Intechopen, Ed.
Zhang, Y. U. (1998). A small-scale procedure for extracting nucleic acids from woody plants infected with various phytopathogens for PCR assay. Journal of Virological Methods., Vol. 71.