SUPRESIÓN VIRAL DEL SILENCIAMIENTO POR RNA EN PLANTAS
VIRAL SUPPRESSION OF RNA SILENCING IN PLANTS
SUPRESIÓN VIRAL DEL SILENCIAMIENTO POR RNA EN PLANTAS
Revista Fitotecnia Mexicana, vol. 40, núm. 2, pp. 181-197, 2017
Sociedad Mexicana de Fitogenética, A.C.
Resumen: El silenciamiento por RNA en plantas es un mecanismo implicado en la regulación de la expresión génica que también funciona como defensa antiviral. El silenciamiento es inducido por la presencia de moléculas de RNA de doble hebra, que activa una cascada de procesos enzimáticos que resulta en la inhibición o supresión de moléculas de ácidos nucleicos a través de interacciones específicas. Para contrarrestar este mecanismo de defensa, los virus codifican en su genoma proteínas supresoras del silenciamiento que pueden interferir con cualquier etapa de la ruta. Estas proteínas supresoras del silenciamiento son muy diversas tanto en secuencia como en estructura y, han sido frecuentemente asociadas a interacciones de tipo sinérgico en infecciones mixtas. Aunque los detalles de los mecanismos moleculares de supresión se conocen en muy pocos casos, en general, los supresores virales contrarrestan el silenciamiento por RNA mediante su acción sobre moléculas de RNA relacionadas con la ruta o mediante interacción con los componentes proteicos de ésta. En este trabajo se hace una revisión sobre las diversas estrategias de supresión de silenciamiento viral descritas hasta el momento y su posible implicación en los procesos de patogénesis y sinergismo viral, dando prioridad a los virus con genoma de RNA por ser los mayoritarios entre los virus de plantas.
Palabras clave: Supresores virales del silenciamiento, virus de plantas, silenciamiento por RNA.
Abstract: RNA silencing in plants is a mechanism involved in the regulation of gene expression that also serves as antiviral defense. This process is induced by the presence of double-stranded RNA molecules that activate a cascade of enzymatic processes and results in the inhibition or suppression of nucleic acid molecules through specific interactions. To counteract this defense mechanism, viruses encode in their genome RNA silencing suppressor proteins that can interfere with any step of the RNA silencing pathway. These RNA silencing suppressor proteins are highly diverse in both sequence and structure and have often been linked to synergistic interactions in mixed infections. Although the details of the molecular mechanisms of suppression are completely known in very few cases, most viral suppressors counteract RNA silencing by acting on RNA molecules involved in the silencing pathway or by interacting with its protein components. This review discusses the different strategies of viral RNA silencing suppression currently known and their possible involvement in the pathogenesis and viral synergism processes primarily in RNA viruses, because they are the majority among plant viruses.
Keywords: Viral silencing suppressors, plant viruses, RNA silencing.
INTRODUCCIÓN
El silenciamiento por RNA es un sistema de regulación mediado por RNAs pequeños que causan la inhibición o supresión de moléculas de ácidos nucleicos a través de interacciones específicas. Este proceso está altamente conservado en organismos eucariotas, donde está presente en plantas, hongos y animales (Wang y Metzlaff, 2005).
Este fenómeno fue descubierto en plantas transgénicas de petunia (Petunia hybrida L.), donde la introducción de una copia foránea de un gen endógeno que se quería sobreexpresar resultó en la co-supresión de ambos, el transgén y el gen endógeno (Napoli et al., 1990; van der Krol et al., 1990). Posteriormente, en diferentes sistemas virales se demostró que, en contra del modelo propuesto, no era necesaria la expresión de proteínas virales para obtener resistencia frente al virus, sino que era suficiente con una secuencia viral no traducible (Lindbo y Dougherty 1992; van der Vlugt et al., 1992). La observación de que un transgén β-glucuronidasa (GUS) silenciado podía prevenir la acumulación viral de Potato virus X (PVX) portador de una secuencia GUS, indicaba que se trataba de un mecanismo de defensa antiviral específico de secuencia (English et al., 1996).
Otra evidencia que indicaba que se trataba de un mecanismo general de respuesta de la planta frente a la infección viral, fue el hallazgo de que en planta no sólo se encontrara resistencia frente a un virus inoculado inicialmente, sino también frente a otros virus que portaran secuencias homólogas (Ratcliff et al., 1997). El posterior descubrimiento de que los genomas virales codificaban proteínas supresoras de silenciamiento, capaces de bloquear o interferir con este proceso de silenciamiento por RNA, confirmó su implicación en defensa antiviral (Anandalakshmi et al., 1998; Kasschau y Carrington, 1998). La prueba inequívoca que explicaba la extrema especificidad de secuencia del proceso de silenciamiento por RNA fue el hallazgo de que en plantas que contenían un transgén silenciado, se acumularan RNAs pequeños de aproximadamente 24 nucleótidos (nt) de tamaño con secuencias idénticas a la del transgén (Hamilton y Baulcombe, 1999).
Para contrarrestar un mecanismo de defensa antiviral basado en el silenciamiento por RNA, los virus han evolucionado codificando una o varias proteínas supresoras de silenciamiento que bloquean distintos puntos de la cascada de silenciamiento antiviral (Anandalakshmi et al., 1998; Voinnet, 2005). Estas proteínas supresoras frecuentemente son multifuncionales, las cuales además de suprimir el silenciamiento antiviral, cumplen funciones indispensables para el ciclo vital del virus, como son: la proteína de cubierta, la proteína de movimiento, la replicasa, la proteasa, las proteínas implicadas en la transmisión viral y en la regulación de la transcripción (Csorba et al., 2009). Además, estos supresores frecuentemente están implicados en interacciones sinérgicas en infecciones mixtas, que pueden dar lugar a una acentuación de la sintomatología y en algunos casos a un aumento de los niveles de acumulación viral. La diversidad encontrada tanto a nivel estructural como funcional de estas proteínas, muestra la importancia de los estudios encaminados a conocer mejor el mecanismo de acción de estos supresores virales.
En este trabajo se ha llevado a cabo una revisión de los diversos mecanismos de supresión del silenciamiento antiviral en plantas de los supresores más representativos descritos hasta el momento, codificados por virus de ssRNA; así mismo, ya que estos supresores además de funcionar en defensa antiviral pueden interferir en procesos fisiológicos de la planta que dependen del silenciamiento por RNA, se ha abordado también el tema de su posible implicación en los procesos de patogénesis y sinergismo viral.
Mecanismos moleculares del silenciamiento por RNA en plantas
En plantas, el silenciamiento por RNA engloba una serie de procesos que pueden actuar a nivel transcripcional (transcriptional gene silencing, TGS) o post-transcripcional (post-transcriptional gene silencing, PTGS). Ambos procesos tienen en común el reconocimiento específico de secuencias de DNA o RNA por pequeñas moléculas de RNA. Este mecanismo está implicado en procesos tales como el mantenimiento de la integridad del genoma, la regulación de procesos del desarrollo y la defensa frente a ácidos nucleicos invasores, tales como transgenes, transposones y virus (Ruiz-Ferrer y Voinnet, 2009; Vaucheret, 2006; Voinnet, 2001).
El silenciamiento por RNA se induce por la presencia de moléculas de dsRNA que podrían derivar de la replicación viral, de repeticiones invertidas, de la transcripción convergente de transgenes y transposones, de loci endógenos con una alta estructura secundaria, o bien generarse por la acción de RNAs polimerasas dependientes de RNA (RDR) a partir de ssRNA. Estas moléculas son procesadas por RNasas de tipo III denominadas en plantas DCLs (Dicer-like), en pequeños RNAs (small RNAs, sRNAs) de doble hebra de entre 19 y 25 nt que presentan 2 o 3 nt protuberantes en el extremo 3' de ambas cadenas (Elbashir et al., 2001). DCL requiere de la acción de DRB (dsRNA binding protein), para que el procesamiento del dsRNA se produzca de un modo preciso y eficiente (Eamens et al., 2012a, b; Hiraguri et al., 2005). La metilación de los sRNAs generados mediada por la metiltransferasa HEN1 (Boutet et al., 2003), los protege de la degradación. Una de las hebras del sRNA es incorporada a un complejo de silenciamiento inducido por RNA (RNA induced-silencing complex, RISC) que contiene, entre otros componentes, una endonucleasa llamada Argonauta (AGO).
Una vez ensamblado, en el caso del PTGS (post-transcriptional gene silencing), este complejo es guiado por el sRNA hasta un mRNA diana de secuencia complementaria al que se une induciendo la inhibición de su traducción o su degradación. En el TGS (transcriptional gene silencing), este complejo es guiado hasta un DNA de secuencia complementaria al que se une e induce su metilación y el bloqueo de su transcripción. Existe un proceso de amplificación de la señal de silenciamiento mediado por RNA polimerasas dependientes de RNA (RDR), que resulta en la generación de nuevas moléculas de dsRNA que son procesadas en sRNAs secundarios (Figura 1).
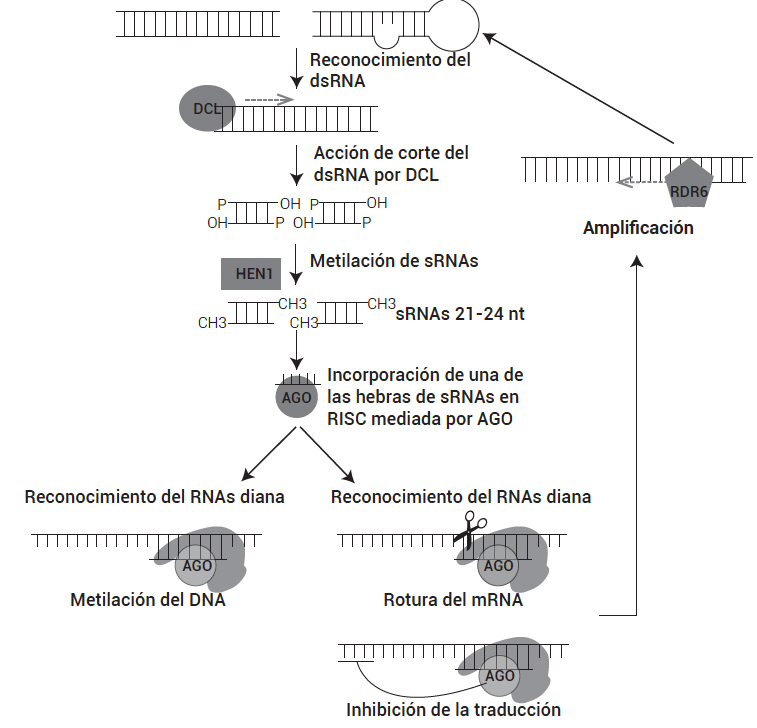
Figura 1
Ruta del silenciamiento por RNA en plantas
La molécula de dsRNA es reconocida y procesada por DCL, lo que genera dúplex de sRNAs que serán metilados por la acción de HEN1. Una de las hebras del sRNA es incorporada en el complejo RISC cuyo componente principal es AGO, y se lleva a cabo la degradación de los RNAs diana. Las RNA polimerasas dependientes de RNA (RDR) generan nuevas moléculas de dsRNA que serán nuevamente procesadas por DCL, dando lugar a la formación de sRNAs secundarios.
En plantas existen tres rutas básicas del silenciamiento por RNA: 1) la ruta de los microRNA (miRNA), 2) la ruta de degradación mediada por pequeños RNAs interferentes (small interfering RNAs, siRNAs), y 3) la ruta de metilación del DNA mediada por RNA (RNA-directed DNA methylation, RdDM). En la ruta de los miRNAs, la transcripción de los genes MIR da lugar a un miRNA primario, que forma una estructura secundaria parcialmente plegada, que es procesada por DCL1, una de las cuatro proteínas DCL de Arabidopsis thaliana, para dar lugar a una estructura precursora tipo horquilla de la que serán escindidos los dúplex de miRNA de 21 a 24 nt (Kim, 2005).
Otros factores, como la proteína de dedo de zinc SERRATE y las proteínas de unión a dsRNA DRB1 o HYL1, también están implicadas en la biogénesis de los miRNAs. Los miRNAs juegan un papel crítico en el control del desarrollo de la planta porque reprimen o controlan la expresión de genes reguladores tales como los factores de transcripción. Los miRNAs de planta tienen principalmente como diana las regiones codificantes de los mRNAs y, aunque funcionan predominantemente mediante la acción de corte del RNA, se ha visto que también pueden actuar mediante represión traduccional (Brodersen et al., 2008). En la ruta de degradación mediada por siRNAs, dsRNAs de tamaño largo endógenos o exógenos, o estructuras en horquilla son procesados por DCL4 y DCL2 en siRNAs de 21 y 22 nt, respectivamente. El dsRNA largo endógeno precursor de esos siRNAs es sintetizado por la RNA polimerasa dependiente de RNA 6 (RDR6), una de las seis RDRs de A. thaliana, usando ssRNA como molde. Los siRNAs endógenos conocidos como trans-acting siRNAs (tasiRNAs) juegan un papel muy importante durante el desarrollo de la planta y en las respuestas a estrés; sin embargo, parece que una de las funciones principales de esta ruta es la defensa antiviral de la planta (ver el siguiente apartado).
Por su parte, la ruta RdDM juega un importante papel en el silenciamiento de transposones y elementos de DNA repetitivos, lo que mantiene la estabilidad e integridad del genoma (Haag y Pikaard 2011; Matzke et al., 2009). Esta ruta también parece tener un papel importante en la defensa de la planta frente a virus de DNA. Los siRNAs de 24 nt implicados en esta ruta son procesados por DCL3 a partir del dsRNA sintetizado por la RNA polimerasa IV dependiente de DNA (Pol IV) y RDR2 (Henderson et al., 2006; Xie et al., 2004). Aunque los detalles moleculares de la RdDM no están del todo claros, como resultado de su actuación, se produce la metilación de novo del DNA por mediación de la DNA metiltransferasa DRM2 (Cao y Jacobsen, 2002; Henderson et al., 2010), con lo que se inhibe la transcripción.
En plantas, la activación del silenciamiento en una célula induce el silenciamiento de la misma secuencia en células adyacentes y en tejidos distales. Así, se han descrito tres tipos de movimiento de la señal de silenciamiento que ocasionarían un silenciamiento a corta distancia, un silenciamiento local extensivo y un silenciamiento sistémico (Kalantidis et al., 2008). El movimiento de la señal de silenciamiento a través de la planta presenta un patrón similar al del movimiento viral, que se mueve célula a célula a través de los plasmodesmos, y a larga distancia a través del floema desde tejidos fuente a tejidos de demanda (Voinnet, 2008). Aunque no se conoce la naturaleza exacta de la señal de silenciamiento, los datos disponibles indican que se trata de un ácido nucleico (Molnar et al., 2010), y se han propuesto posibles modelos de como ocurre el mismo. Así, mientras la proteína RDR6 parece jugar un papel crucial en la amplificación de la señal y su movimiento a largas distancias (Schwach et al., 2005), DCL4, en las células acompañantes, estaría implicada en la generación de sRNAs de 21 nt que son capaces de moverse de 10 a 15 células más allá del límite del floema (Dunoyer et al., 2005). Estudios recientes han demostrado que tanto siRNAs como miRNAs tienen la capacidad de moverse de una célula a otra y alcanzar el tejido vascular (Melnyk et al., 2011).
Silenciamiento por RNA como mecanismo de defensa antiviral en plantas
En plantas, el silenciamiento por RNA también funciona como mecanismo de defensa antiviral (Baulcombe, 2004; Burgyán y Havelda, 2011). Las infecciones virales en plantas están asociadas con la acumulación de siRNAs virales (viral small interfering RNAs, vsiRNAs) que pueden, a su vez, actuar silenciando el propio genoma viral. Por esta razón, los virus son tanto inductores como dianas del silenciamiento por RNA. Mientras que en virus de DNA los vsiRNAs podrían provenir de dsRNAs generados durante la transcripción bidireccional de sus genomas (Chellappan et al., 2004), en virus de RNA los vsiRNAs podrían generarse a partir de dsRNAs sintetizados durante el proceso de replicación viral. En este último caso se ha propuesto también que la presencia de regiones altamente estructuradas del genoma podría constituir una fuente de generación de vsiRNAs (Molnár et al., 2005); sin embargo, estudios recientes han mostrado que la mayor parte de los vsiRNAs se generarían por la acción de RDR celulares; por lo tanto, su biogénesis sería similar a la descrita para los siRNAs endógenos (Díaz-Pendón et al., 2007; Donaire et al., 2008; García-Ruiz et al., 2010; Qi et al., 2009; Wang et al., 2010).
En A. thaliana, las cuatro proteínas DCL identificadas están involucradas en la biogénesis de vsiRNAs. En el caso de virus RNA, el papel esencial en defensa antiviral lo tienen DCL4 y DCL2 (Ding y Voinnet, 2007) que generan vsiRNAs de 21 y 22 nt, respectivamente. De las dos, DCL4 parece tener un papel dominante, porque los vsRNAs de 21 nt son generalmente más abundantes que los de 22 nt. Esta predominancia de DCL4 sobre DCL2 podría también deberse a un efecto más potente en silenciamiento antiviral de los vsiRNAs de 21 nt con respecto a los de 22 (Wang et al., 2011). En el caso de DCL3, aunque hay indicaciones que sugieren que puede contribuir en defensa antiviral, especialmente si DCL4 es inactivada (Díaz-Pendón et al., 2007; Donaire et al., 2008; García-Ruiz et al., 2010; Qu et al., 2008), esta contribución parece no ser muy relevante (Deleris et al., 2006; García-Ruiz et al., 2010). También la contribución de DCL1 a la generación de vsiRNAs parece ser minoritaria (Deleris et al., 2006; Dunoyer et al., 2005; García-Ruiz et al., 2010). En el caso de virus con genoma de DNA, las cuatro proteínas DCL están implicadas en la biogénesis de vsiRNAs (Blevins et al., 2006).
Los vsiRNAs generados se asocian con el complejo antiviral RISC (RNA-induced silencing complex) del que AGO (proteína argonuta) forma parte, en el que se produce el reconocimiento de las dianas virales y su corte. De entre los 10 miembros de AGO identificadas en A. thaliana, AGO1 parece ser el más importante en defensa antiviral, aunque también se ha descrito la participación de AGO2, AGO3, AGO4, AGO5 y AGO7 (Brosseau y Moffett, 2015; Chiu et al., 2010; Jaubert et al., 2011; Morel et al., 2002; Qu et al., 2008). Se ha propuesto que AGO1 formaría parte de una primera línea de defensa antiviral, mientras que otras proteínas AGO actuarían en una segunda fase (Harvey et al., 2011; Qu et al., 2008).
De los vsiRNAs producidos durante el proceso de silenciamiento, sólo una pequeña fracción resulta de la acción de corte de DCL sobre la diana inicial. Existe un proceso de amplificación de la señal de silenciamiento mediado por RDR, que resulta en la generación de vsiRNAs secundarios (Voinnet, 2008). De las seis proteínas RDR identificadas en A. thaliana, RDR1, RDR2 y RDR6 parecen estar implicadas en respuesta antiviral (Dalmay et al., 2000; Díaz-Pendón et al., 2007; Donaire et al., 2008; García-Ruiz et al., 2010; Mourrain et al., 2000; Qu et al., 2008). Entre ellas, el papel de RDR6 es especialmente importante, pues se ha observado que una disminución en la actividad de esta enzima, hace que aumente la susceptibilidad a un gran número de virus (Mourrain et al., 2000;Qu et al., 2005; Schwach et al., 2005).
En plantas, el silenciamiento inducido en una célula puede moverse célula a célula y a largas distancias para alcanzar tejidos distales. De este modo, si la señal de silenciamiento se propaga de un modo más rápido del que lo hace el virus, los tejidos distales estarán alertados y de este modo tendrán la capacidad de resistir a la invasión viral (Ding y Voinnet, 2007). El silenciamiento sistémico, cuya amplificación está mediada por RDR6, juega un papel muy importante en defensa antiviral, porque previene la invasión viral del meristemo (Schwach et al., 2005). Esta exclusión del meristemo es especialmente importante en defensa antiviral, porque puede facilitar tanto la recuperación de la planta como prevenir la transmisión por semillas.
Supresión viral del silenciamiento
Para contrarrestar el silenciamiento por RNA, los virus han evolucionado codificando en su genoma proteínas supresoras del silenciamiento. El primer supresor de silenciamiento viral descrito fue la proteína HCPro de potyvirus (Anandalakshmi et al., 1998; Kasschau y Carrington, 1998). Desde entonces distintas aproximaciones han permitido identificar un gran número de supresores virales (http://www.revistafitotecniamexicana.org/documentos/40-2/7a-cuadro1.pdf). Así, se ha propuesto que los virus de plantas codifican en su genoma al menos un supresor del silenciamiento, aunque en algunos casos codifican más de uno como ocurre en los géneros Closterovirus, Crinivirus y Begomovirus (Csorba et al., 2015; Díaz-Pendón y Ding, 2008). Los supresores del silenciamiento, incluso dentro de la misma familia o grupo viral, son muy diversos tanto en secuencia como en estructura. Esta alta diversidad sugiere que han evolucionado de manera independiente y que son el resultado de procesos evolutivos recientes (Ding y Voinnet, 2007).
Muchas de estas proteínas supresoras son multifuncionales; es decir, además de cumplir con las funciones del ciclo viral, interfieren con la ruta de silenciamiento del hospedero (Voinnet, 2005), aunque también han sido descritas proteínas supresoras cuya única función es la supresión del silenciamiento. Los mecanismos de acción de los supresores son tan diversos que pueden interferir en cualquier etapa de la ruta de silenciamiento. Así mismo, cada vez existen más casos en que se describe que un mismo supresor viral es capaz de interferir en distintas etapas de la ruta de silenciamiento, lo que acentúa la efectividad de la supresión. Otra estrategia usada por los virus de plantas para suprimir de un modo más efectivo el silenciamiento por RNA es, como se ha comentado arriba, la producción de varias proteínas supresoras que podrían actuar en distintos puntos de la ruta de silenciamiento y complementarse entre sí.
Mecanismos moleculares de supresión del silenciamiento
Los detalles de los mecanismos moleculares subyacentes a la actividad específica de los supresores virales se conocen en pocos casos. En general, actúan sobre moléculas de RNA relacionadas con la ruta o interaccionan con los componentes proteicos de ésta ( http://www.revistafitotecniamexicana.org/documentos/40-2/7a-cuadro1.pdf).
Entre los distintos mecanismos de acción descritos para supresores virales de silenciamiento se encuentran:
Unión a dsRNA. Dado el papel clave que los dsRNAs juegan en la ruta de silenciamiento, se espera que cualquier mecanismo que impida su actuación, comprometa la efectividad de la misma. De este modo, uno de los mecanismos de acción más comunes de los supresores de silenciamiento es la unión a dsRNAs (Lakatos et al., 2006; Mérai et al., 2006). Depende de si se unen a dsRNAs de tamaño largo o de tamaño corto, se afectarán distintas etapas de la ruta; de este modo si el supresor se une a dsRNAs de tamaño largo, la enzima Dicer no podrá acceder a su sustrato y la digestión del mismo se verá afectada, mientras que la unión a dsRNAs pequeños (siRNAs) puede impedir que éstos se carguen al complejo RISC, y se inhiba por lo tanto esta etapa de la ruta.
Entre el grupo de supresores que se unen a dsRNAs de tamaño largo se encuentran la proteína P14 del aureusvirus (género Aureusvirus, familia Tombusviridae) Photos latent virus (PoLV), la proteína P38 del carmovirus (género Carmovirus, familia Tombusviridae) Turnip crinkle virus (TCV) (Mérai et al., 2006), y la proteína NSs del tospovirus (género Tospovirus, familia Bunyaviridae) Tomato spotted wilt virus (Schnettler et al., 2010). Estos supresores también son capaces de unir siRNAs, y representan la estrategia más común utilizada por las proteínas supresoras de silenciamiento de los virus de plantas (Chapman et al., 2004; Csorba et al., 2007; Goto et al., 2007; Kurihara et al., 2007; Martínez-Turiño y Hernández, 2009; Mérai et al., 2006; Schnettler et al., 2010). Entre las evidencias experimentales que apoyan que la unión a siRNAs interferiría con su carga en el complejo RISC, se encuentran las descritas para las proteínas p19 de tombusvirus (género Tombusvirus, familia Tombusviridae), p21 de closterovirus (género Closterovirus, familia Closteroviridae), NS3 de tenuivirus (género Tenuivirus), HCPro de potyvirus (género Potyvirus, familia Potyviridae) y p122 de tobamovirus (género Tobamovirus, familia Virgaviridae) (Csorba et al., 2007; Hemmes et al., 2007; Lakatos et al., 2006).
Como consecuencia de la unión del supresor a siRNAs, se interferiría en la metilación de los mismos por parte de la enzima HEN1, y afectaría así su estabilidad (Csorba et al., 2007; Lózsa et al., 2008; Vogler et al., 2007). Probablemente, el supresor mejor caracterizado entre los que unen siRNAs es la proteína p19 de tombusvirus (Silhavy et al., 2002). Estudios cristalográficos han mostrado que p19 forma un homodímero que selecciona específicamente siRNAs de 21 y 22 nt de tamaño (Vargason et al., 2003; Ye et al., 2003). El secuestro de siRNAs por parte de p19, bloquearía la formación de complejos RISC activos (Lakatos et al., 2006) e interferiría en el movimiento sistémico de la señal de silenciamiento (Molnar et al., 2010). Una estrategia totalmente distinta a la unión a siRNAs, aunque con el mismo resultado, es llevada a cabo por la proteína supresora RNasa III del crinivirus Sweet potato chlorotic stunt virus (SPCSV). Así, el corte de los siRNAs virales de 21 a 24 nt en productos de 14 nt mediado por la actividad endonucleasa de la proteína RNasa III, hace que éstos sean inactivos sin poder ser incorporados en el complejo RISC (Cuellar et al., 2009).
Interferencia con DCL. Los supresores virales que actúen directamente inhibiendo la maquinaria enzimática implicada en el procesamiento de dsRNAs, actuarán afectando la eficiencia de corte de DCL. Así, el factor DRB4 (dsRNA binding protein 4), que se requiere para el procesamiento de vsiRNAs mediado por DCL4, constituye la diana de varios supresores virales que se unen a él, y lo inhibirían. Como consecuencia de la interacción con este factor auxiliar de DCL4, se inhibe la formación de vsiRNAs de 21 nt (Deleris et al., 2006; Haas et al., 2008; Hiraguri et al., 2005; Qu et al., 2008; Shivaprasad et al., 2008). Otra estrategia que también resultaría en la interferencia de la acción de corte de DCL, es la utilizada por el dianthovirus (género Dianthovirus, familia Tombusviridae) Red clover necrotic mosaic virus (RCNMV). Así, la incorporación de DCL en el complejo de replicación de RCNMV conduciría a su inhibición (Takeda et al., 2005).
Interacción con proteínas AGO. El bloqueo de complejos RISC funcionales puede llevarse a cabo por medio de la unión directa a la unidad catalítica AGO (Zhang et al., 2006), su desestabilización o degradación (Baumberger et al., 2007; Bortolamiol et al., 2007; Pazhouhandeh et al., 2006). La primera proteína supresora en la que se describió la unión a AGO1 y AGO4 in vivo fue la proteína 2b del cucumovirus (género Cucumovirus, familia Bromoviridae) Cucumber mosaic virus (CMV) (González et al., 2010; Hamera et al., 2012; Zhang et al., 2006). Así, el que la interacción con AGO1 resulte en la inhibición de la actividad de corte de AGO1 (Zhang et al., 2006), sugiere que podría estar implicada en la prevención de la amplificación y dispersión de vsiRNAs (Goto et al., 2007; Zhang et al., 2006). Por su parte, la interacción con AGO4 que actúa uniendo siRNAs de 24 nt de origen endógeno que participan en RdDM, reduciría el acceso de los siRNAs a su diana endógena y modularía, de este modo, la transcripción de genes del hospedero en beneficio del virus (Hamera et al., 2012).
Por otra parte, la proteína supresora P0 de polerovirus (género Polerovirus, familia Luteoviridae), contiene un dominio tipo F-box, típico de factores celulares relacionados con la ubiquitinación y la degradación de proteínas, que tiene como diana AGO1 y cuyo papel sería promover su degradación (Baumberger et al., 2007; Bortolamiol et al., 2007; Csorba et al., 2010; Pazhouhandeh et al., 2006). En el caso del nepovirus (género Nepovirus, familia Secoviridae) Tomato ringspot virus (ToRSV), la proteína supresora CP se uniría a AGO1 para promover su degradación por autofagia (Karran y Sanfaçon, 2014) y como consecuencia suprimir su actividad inhibidora durante la traducción. Por su parte, la proteína p25 del potexvirus (género Potexvirus, familia Flexiviridae) PVX también interacciona físicamente con AGO (AGO1, 2, 3 y 4) y promueve su degradación a través de una ruta dependiente del proteosoma (Chiu et al., 2010). Estudios recientes han puesto de manifiesto la existencia de un nuevo tipo de interacción con AGO1 a través de repeticiones aminoacídicas del tipo GW/WG (glicina/triptófano). Este tipo de repeticiones son típicas de proteínas celulares que intervienen en el ensamblaje y funcionamiento de los complejos RISC (Karlowski et al., 2010), y los supresores que las contienen pueden interferir por competencia en la formación de novo de RISC o en su actividad (Azevedo et al., 2010; Giner et al., 2010).
Además de estos dos primeros casos descritos para la proteína p38 del carmovirus TCV y la proteína P1 del ipomovirus (género Ipomovirus, familia Potyviridae) Sweet potato mild mottle virus (SPMMV), se ha descrito que esta estrategia es utilizada también por la proteína p37 del carmovirus Pelargonium line pattern virus (PLPV). En este caso, se ha demostrado que estos dominios GW además de implicados en la unión a AGO1, también lo están en la unión a siRNAs, y ambas actividades son esenciales para que p37 pueda ejercer su actividad supresora (Pérez-Cañamás y Hernández, 2015). Resultados de este mismo trabajo también muestran que los dominios GW/WG de TCV p38, aparte de implicados en la interacción con AGO1, son necesarios para que se mantengan sus propiedades de unión tanto a siRNAs como a dsRNAs de tamaño largo. Estos resultados sugieren que ambas funciones podrían actuar de modo cooperativo; durante la interacción del supresor con AGO se incrementaría el secuestro de dúplex de siRNAs, e interferiría de este modo con la actividad de RISC.
Modulación de la homeostasis de AGO1. Aunque recientemente descrito, este mecanismo de acción basado en la modulación de la expresión génica del hospedero a nivel transcripcional, podría ser una estrategia ubicua en las interacciones virus-planta. AGO1, como se ha comentado anteriormente, es uno de los componentes más importantes de la ruta de silenciamiento implicado en defensa antiviral, cuya homeostasis depende de la expresión de miR168 (Rhoades et al., 2002). Resultados recientes muestran que durante la infección por tombusvirus se produce una inducción de la transcripción de AGO1 como parte del arsenal de respuestas antivirales de la planta. Para contrarrestar un mecanismo de defensa basado en AGO1, el supresor p19 promueve la inducción transcripcional de miR168, que resulta en la disminución de los niveles de expresión de AGO1 (Várallyay et al., 2010). Además de presentarse en la infección por tombusvirus, este fenómeno ha sido observado en el caso de otras infecciones virales (Du et al., 2011; Várallyay y Havelda, 2013).
Interferencia en la amplificación de siRNA secundarios. Las proteínas RDR del hospedero, en especial RDR1 y RDR6, están implicadas en la amplificación del silenciamiento y en la dispersión de la señal sistémica del mismo mediante la síntesis de vsiRNAs (Schwach et al., 2005); por lo tanto, la supresión de la actividad RDR puede constituir un punto clave dónde actuar para el supresor, porque al interferir en la amplificación del silenciamiento, la replicación y dispersión viral se verían favorecidas. Entre las proteínas supresoras que actúan en este punto se encuentra la proteína V2 del geminivirus (género Begomovirus, familia Geminiviridae) Tomato yellow leaf curl virus (TYLCV), que interacciona directamente con SGS3, el cofactor de RDR6, y bloquea de este modo la amplificación del silenciamiento (Glick et al., 2008). Estudios in vitro realizados con este mismo supresor han mostrado que V2 compite con SGS3 por dsRNAs que contengan extremos 5´ protuberantes, que podría constituir un intermediario de RDR6/SGS3 en la amplificación de vsiRNAs (Fukunaga y Doudna, 2009; Kumakura et al., 2009).
De igual modo, la proteína TGBp1 de potexvirus inhibe la síntesis de dsRNA dependiente de RDR6/SGS3 (Okano et al., 2014). También, el supresor βC1, codificado por el DNA satélite de Tomato yellow leaf curl China virus (TYLCCNV) interacciona con el supresor endógeno rgsCaM, una proteína celular relacionada con la calmodulina, en Nicotiana benthamiana, y reprime la expresión de RDR6 y por lo tanto la producción de siRNAs secundarios (Li et al., 2014). Ensayos de expresión transitoria en N. benthamiana mostraron que los supresores HCPro del potyvirus Sugarcane mosaic virus (SCMV) y 2b del cucumovirus Tomato aspermy virus (TAV), están implicados en la reducción de los niveles de acumulación de mRNA de RDR6 (Zhang et al., 2008). Del mismo modo, el supresor Pns10 del phytoreovirus (género Phytoreovirus, familia Reoviridae) Rice dwarf phytoreovirus (RDV) reduce los niveles de expresión de RDR6, y favorece la invasión viral de los ápices (Ren et al., 2010). También la proteína 2b de cucumovirus evita la dispersión de la señal de silenciamiento a larga distancia (Guo y Ding, 2002), al inhibir la producción de siRNAs secundarios (Wang et al., 2010). Es notorio por lo tanto que una actividad supresora centrada en RDR6 es una estrategia ampliamente utilizada por distintos virus que bloquea de un modo efectivo el silenciamiento antiviral.
Interacción con reguladores endógenos de la ruta de silenciamiento. Algunos supresores modulan una respuesta defensiva por parte de la planta basada en el silenciamiento por RNA, mediante su actuación sobre reguladores endógenos de la ruta de silenciamiento. Entre ellos se encuentra la proteína AL2 de geminivirus que inhibe a la enzima ADK (Adenosina kinasa) (Wang et al., 2003), implicada en procesos de metilación. Debido a que una parte de la respuesta defensiva contra estos virus implica la metilación de sus genomas, la inhibición de ADK, indirectamente, conseguiría bloquear el proceso de metilación (Wang et al., 2005). Debido a que para este grupo de virus de DNA es muy importante evitar la metilación de sus genomas, la interacción e inhibición de otra enzima implicada en el ciclo de metilación como SAHH (S-adenosil homocisteína hidrolasa), sería el factor endógeno sobre el que actuaría el supresor βC1 codificado por el DNA satélite de Tomato yellow leaf curl China virus (TYLCCNV) (Yang et al., 2011). De manera interesante, la proteína de geminivirus mencionada en primer lugar, AL2, también actúa induciendo la expresión e interacciona con la proteína celular rgs-CaM (Chung et al., 2014).
Otro ejemplo de factor endógeno que parece ser diana de diversos supresores no relacionados, es el factor transcripcional inducible por etileno (RAV2) (Endres et al., 2010). En el caso del Papaya ringspot virus (PRSV) la proteína supresora HCPro interacciona con calreticulina y modula de este modo la respuesta defensiva antiviral a través de la ruta de señalización del calcio (Shen et al., 2010b). Por su parte la proteína HCPro de los potyvirus Potato virus A (PVA), Potato virus Y (PVY) y Tobacco etch virus (TEV) interacciona con una proteína asociada al microtúbulo (HIP2), a través de su región altamente variable (HVR). Así, mientras que la reducción de HIP2 está asociada con una disminución de los niveles de acumulación viral, mutaciones en el dominio HVR de HCPro provocan una inducción sistémica mediada por etileno y ácido jasmónico de genes de defensa de la planta y necrosis (Haikonen et al., 2013a, b).
Supresores virales como determinantes de patogenicidad
Sinergismo viral
El que un virus sea capaz de replicarse en un hospedero, no necesariamente va unido al hecho de que sea patogénico. La patogénesis tiene lugar cuando una infección viral afecta a la fisiología del hospedero lo que causa alteraciones en el desarrollo y otras manifestaciones fenotípicas, que son consideradas como síntomas de la enfermedad (Culver y Padmanabhan, 2007; García y Pallás, 2015; Mandadi y Scholthof, 2013; Pallás y García, 2011). Como se ha visto, los virus, para infectar con éxito una planta, deben hacer frente a una repuesta defensiva basada en el silenciamiento por RNA, proceso que además de funcionar como defensa antiviral está implicado en la regulación de diversos procesos celulares. Para ello, la estrategia más comúnmente utilizada es la de codificar en su genoma proteínas supresoras del silenciamiento (Li y Ding, 2006). Estos supresores, además de funcionar en defensa antiviral, pueden interferir en procesos fisiológicos de la planta que dependen del silenciamiento por RNA, y esta interferencia contribuir a la patogénesis. Así, muchos supresores virales suelen ser considerados como los principales determinantes de patogenicidad tanto en infecciones simples como en infecciones mixtas sinérgicas.
Una de las rutas endógenas de silenciamiento por RNA en planta que más frecuentemente se ve afectada es la de los miRNAs. Como se ha visto, los miRNAs regulan negativamente importantes factores reguladores implicados en procesos de desarrollo, homeostasis de nutrientes y respuestas a estrés (Carrington y Ambrós, 2003; Pasquinelli y Ruvkun, 2002; Zhang et al., 2010). Es, por lo tanto, concebible que los supresores puedan ocasionar alteraciones en el desarrollo de procesos, tales como la división celular, la formación de hojas y el desarrollo de la flor, mediante la interferencia en la expresión y la función de los miRNAs, y que estas interferencias puedan resultar en el desarrollo de síntomas de enfermedad (Kasschau et al., 2003). De acuerdo con esto, plantas transgénicas que expresan proteínas supresoras de silenciamiento, a menudo muestran fenotipos similares a los síntomas virales (Chapman et al., 2004; Chellappan et al., 2005; Jay et al., 2011). Muchos de los supresores de silenciamiento que actúan secuestrando vsiRNAs, pueden interferir en estas rutas endógenas al inhibir su papel regulador. Como ejemplo se encuentra el caso del miRNA167 que resulta en la alteración de la regulación de su diana AUXIN RESPONSE FACTOR 8, y que parece ser especialmente relevante porque es el principal factor implicado en la alteración del desarrollo causada por al menos tres proteínas supresoras, HCpro de potyvirus, p19 de tombusvirus y p15 de pecluvirus (género Pecluvirus, familia Virgaviridae) (Jay et al., 2011).
También los genes R del tipo NBS-LRR están regulados negativamente por miRNAs para evitar que una expresión incontrolada dispare reacciones autoinmunes deletéreas. Es posible, por lo tanto, que la inactivación de esos miRNAs por los supresores resulte en un aumento de los niveles de expresión de los genes R lo que causaría síntomas de enfermedad como la necrosis letal (Shivaprasad et al., 2012; Wang et al., 2012b; Weber et al., 2004). La unión e inactivación de otros componentes de la ruta de silenciamiento como las proteínas AGO, estrategia comúnmente utilizada por las proteínas supresoras, puede también producir alteraciones en el desarrollo, como es el caso de la proteína 2b de CMV (Zhang et al., 2006) y de la proteína TGBp1 del carlavirus (género Carlavirus, familia Flexiviridae) Plantago asiatica mosaic virus (PlAMV) (Okano et al., 2014).
Es importante remarcar que los supresores pueden producir efectos patogénicos que no dependen directamente de su capacidad para suprimir el silenciamiento (Du et al., 2014). Como ejemplo se pueden citar, en el caso de geminivirus, el de la proteína supresora βC1 codificada por el DNA satélite asociado con TYLCCV, y el de la proteína C2 que actúan inhibiendo la ruta del ácido jasmónico (Lozano-Durán et al., 2011; Yang et al., 2008). Otros ejemplos de interacción de supresores con factores del hospedero que pueden tener un impacto en patogénesis viral son los propuestos para la interacción de la proteína supresora p6 del caulimovirus (género Caulimovirus, familia Caulimoviridae) Cauliflower mosaic virus (CaMV) con componentes implicados en la ruta de señalización del etileno (Geri et al., 2004), el de la interacción del supresor 2b de CMV con una catalasa del hospedero (Inaba et al., 2011) o el de la interacción del supresor HCpro de PVA con la proteína asociada al microtúbulo HIP2 (Haikonen et al., 2013b). También, una función incorrecta del proteosoma como consecuencia de la interacción con el supresor HCpro podría considerarse como otro factor que contribuye al incremento de la patogenicidad asociado a la actividad de una proteína supresora (Pacheco et al., 2012).
Dada la importancia de la supresión del silenciamiento por RNA para la supervivencia viral, es razonable considerar que los supresores virales podrían ser diana de mecanismos de defensa alternativos que podrían causar importantes síntomas de enfermedad (García y Pallás, 2015; Pallás y García, 2011; Wang et al., 2012b). De hecho, algunos supresores como la proteína p6 de CaMV en Nicotiana cleveladii, (Király et al., 1999), la proteína p19 de TBSV (Chu et al., 2000) y 2b de TAV (Li et al., 1999) en tabaco (Nicotiana tabacum), o la proteína CP de TCV en A. thaliana (Ren et al., 2000), han sido descritas como inductoras de respuestas necróticas locales o sistémicas similares a las mediadas por los genes R. También la proteína HCpro de TEV induce una débil respuesta específica que estimula la resistencia de la planta frente a diversos patógenos (Pruss et al., 2004). Aunque ninguna de estas respuestas es capaz de bloquear completamente la infección viral, son capaces de condicionar el desarrollo de síntomas.
Ya que diferentes supresores de silenciamiento actúan con mecanismos distintos que afectan a diversas etapas de la ruta de silenciamiento por RNA, no es sorprendente que en infecciones donde virus de diferentes familias se mezclan se produzca una acentuación de la sintomatología, lo que puede inducir mayores niveles de acumulación viral que en infecciones individuales. Este fenómeno es conocido como sinergismo viral. La mayoría de los estudios de sinergismo viral implican a un virus del género Potyvirus. Entre ellos, el caso mejor estudiado es el de la interacción PVX-PVY en Nicotiana tabacum, donde se produce tanto una acentuación de la sintomatología como un incremento en los niveles de acumulación de PVX (González-Jara et al., 2004; Pruss et al., 1997; Vance et al., 1991). El incremento en la patogenicidad observado cuando el supresor HCpro fue expresado a partir de un virus heterólogo, mostró que ésta era la secuencia implicada en la interacción sinérgica (Pruss et al., 1997); sin embargo, cuando el hospedero utilizado fue N. benthamiana no se observó un incremento en los niveles de acumulación de PVX en plantas co-infectadas con los potyvirus PVY, TEV o Plum Pox virus (PPV), a pesar de los severos síntomas observados, donde la aparición de lesiones necróticas sistémicas en hojas y tallos, conducía a la muerte de la planta (González-Jara et al., 2004, 2005).
En este sentido, se ha sugerido que el sinergismo entre PVX y potyvirus es dependiente del hospedero (González-Jara et al., 2004). De hecho, un estudio reciente en este mismo sistema ha propuesto el posible mecanismo implicado en esta interacción sinérgica. De este modo, se ha visto que la presencia del potyvirus, aunque no produce ningún efecto a nivel del RNA genómico de PVX, ayuda a la estabilización de los RNAs subgenómicos lo que permite que se alcance un nivel umbral de expresión de la proteína p25 de PVX, que sería de este modo reconocida por un posible gen R presente en N. benthamiana. Este reconocimiento es el que dispararía la respuesta que desencadenaría los síntomas observados de necrosis sistémica (Aguilar et al., 2015). De modo general, en las múltiples interacciones sinérgicas descritas en las que un potyvirus está implicado, los niveles de acumulación de potyvirus tales como PVY, TEV, Tobacco vein mottling virus (TVMV), Zuchini yellow mosaic virus (ZYMV), Pepper mottle virus (PepMoV) o Cowpea aphid-borne mosaic virus (CABMV), no se ven afectados, mientras que los del virus heterólogo aumentan (Fukuzawa et al., 2010; Murphy y Bowen, 2006; Pruss et al., 1997; Taiwo et al., 2007; Vance et al., 1995; Zeng et al., 2007).
La capacidad que tienen los virus de planta de causar infecciones sinérgicas en diferentes cultivos tiene implicaciones biológicas, epidemiológicas y económicas. El incremento de la multiplicación de uno o ambos virus implicados N. benthamiana, puede alterar la gama de hospederos o la tasa de transmisión por vectores (Elena, 2011), con las impredecibles consecuencias que ello ocasionaría. Como ejemplo se encuentra el caso de la ruptura de resistencia observada en plantas de tomate co-infectadas con ToCV y el tospovirus Tomato spotted wild virus (TSWV) (García-Cano et al., 2006), el de CMV en plantas de pepino (Cucumis sativus) co-infectadas con ZYMV (Wang et al., 2004) y el de un número de virus de batata (Ipomoea batatas L.) simultáneamente infectada con el crinivirus SPCSV (Karyeija et al., 2000; Mukasa et al., 2006; Untiveros et al., 2007). A pesar de las serias implicaciones biológicas y epidemiológicas que tienen estas interacciones sinérgicas, los mecanismos moleculares implicados en las mismas apenas se conocen.
Agradecimientos
Yazmín Landeo-Ríos fue beneficiaria de una beca predoctoral MAEC/AECID del Ministerio de Asuntos Exteriores y Cooperación de España. M. Carmen Cañizares fue beneficiaria de un contrato I3P (I3P-PC2004L) del CSIC (España) con la ayuda del Fondo Social Europeo (FSE). Este trabajo fue financiado por los proyectos AGL2010-22287-C02-01/AGR y AGL2013-48913-C2-1-R del Ministerio de Economía y Competitividad de España, co-financiado por el Fondo Europeo de Desarrollo Regional FEDER. Jesús Navas-Castillo y Enrique Moriones son miembros del Grupo de Investigación AGR-214, financiados parcialmente por la Consejería de Economía, Innovación y Ciencia, Junta de Andalucía, España, co-financiado por FEDER y FSE.
BIBLIOGRAFÍA
Aguilar E., D. Almendral, L. Allende, R. Pacheco, B. N. Chung, T. Canto and F. Tenllado (2015) The P25 protein of Potato virus X (PVX) is the main pathogenicity determinant responsible for systemic necrosis in PVX-associated synergisms. Journal of Virology 89:2090-2103.
Ahn J. W., C. J. Yin, J. R. Liu and W. J. Jeong (2010) Cucumber mosaic virus 2b protein inhibits RNA silencing pathways in green alga Chlamydomonas reinhardtii. Plant Cell Reports 29:967-975.
Anandalakshmi R., G. J. Pruss, X. Ge, R. Marathe, T. H. Smith and V. B. Vance (1998) A viral suppressor of gene silencing in plants. Proceedings of the Nacional Academy of Sciences of the United States of America 95:13079-13084.
Andika I. B., H. Kondo, M. Nishiguchi and T. Tamada (2012) The cysteine-rich proteins of Beet necrotic yellow vein virus and Tobacco rattle virus contribute to efficient suppression of silencing in roots. Journal of General Virology 93:1841-1850.
Angel C. A. and J. E. Schoelz (2013) A survey of resistance to Tomato bushy stunt virus in the genus Nicotiana reveals that the hypersensitive response is triggered by one of three different viral proteins. Molecular Plant-Microbe Interactions 26:240-248.
Asaoka R., H. Shimura, M. Arai and C. Masuta (2010) A progeny virus from a cucumovirus pseudorecombinat evolved to gain the ability to accumulate its RNA silencing suppressor leading to systemic infection in tobacco. Molecular Plant-Microbe Interactions 23:332-339.
Azevedo J., D. García, D. Pontier, S. Ohnesorge, S. García, L. Braun, M. Bergdoll, M. A. Hakimi, T. Lagrange and O. Voinnet (2010) Argonaute quenching and global changes in Dicer homeostasis caused by a pathogen-encoded GW repeat protein. Genes & Development 24:904-915.
Baulcombe D. (2004) RNA silencing in plants. Nature 431:356-363.
Baumberger N., C. H. Tsai, M. Lie, E. Havecker and D. Baulcombe (2007) The Polerovirus silencing suppressor P0 targets ARGONAUTE proteins for degradation. Current Biology 17:1609-1614.
Bayne E. H., D. V. Rakitina, S. Y. Morozov and D. Baulcombe (2005) Cell-to-cell movement of Potato petexvirus X is dependent on suppression of RNA silencing. The Plant Journal 44:471-482.
Blevins T., R. Rajeswaran, P. V. Shivaprasad, D. Beknazariants, A. Si-Ammour, H. S. Park, F. Vazquez, D. Robertson, F. Jr. Meins, T. Hohn and M. M. Pooggin (2006) Four plant Dicers mediate viral small RNA biogenesis and DNA virus induced silencing. Nucleic Acids Research 34:6233-6246.
Bortolamiol D., M. Pazhouhandeh, K. Marrocco, P. Genschik and V. Ziegler-Graff (2007) The Polerovirus F box protein P0 targets ARGONAUTE1 to suppress RNA silencing. Current Biology 17:1615-1621.
Boutet S., F. Vazquez, J. Liu, C. Beclin, M. Fagard, A. Gratias, J. B. Morel, P. Crete, X. Chen and H. Vaucheret (2003) Arabidopsis HEN1: a genetic link between endogenous miRNA controlling development and siRNA controlling transgene silencing and virus resistance. Current Biology 13:843-48.
Brodersen P., L. Sakvarelidze-Achard, M. Bruun-Rasmussen, P. Dunoyer, Y. Y. Yamamoto, L. Sieburth and O. Voinnet (2008) Widespread translation inhibition by plant miRNAs and siRNAs. Science 320:1185-1190.
Brosseau C. and P. Moffett (2015) Functional and genetic analysis identify a role for Arabidopsis ARGONAUTE5 in antiviral RNA silencing. The Plant Cell 27:1742-1754.
Burgyán J. and Z. Havelda (2011) Viral suppressors of RNA silencing. Trends in Plant Science 16:265-272.
Canto T., F. Cillo and P. Palukaitis (2002) Generation of siRNAs by T-DNA sequences does not require active transcription or homology to sequences in the plant. Molecular Plant-Microbe Interactions 15:1137-1146.
Cañizares M. C., R. Lozano-Durán, T. Canto, E. R. Bejarano, D. M. Bisaro, J. Navas-Castillo and E. Moriones (2013) Effects of the crinivirus coat protein-interacting plant protein SAHH on post-transcriptional RNA silencing and its suppression. Molecular Plant-Microbe Interactions 26:1004-1015.
Cañizares M. C., J. Navas-Castillo and E. Moriones (2008) Multiple suppressors of RNA silencing encoded by both genomic RNAs of the crinivirus, Tomato chlorosis virus.Virology 379:168-174.
Cañizares M. C., K. M. Taylor and G. P. Lomonossoff (2004) Surface-exposed C-terminal amino acids of the small coat protein of Cowpea mosaic virus are required for suppression of silencing. Journal of General Virology 85:3431-3435.
Cao X. and S. E. Jacobsen (2002) Role of the Arabidopsis DRM methyltransferases in de novo DNA methylation and gene silencing. Current Biology 12:1138-1144.
Carrington J. C. and V. Ambros (2003) Role of microRNAs in plant and animal development. Science 301:336-338.
Chapman E. J., A. I. Prokhnevsky, K. Gopinath, V. V. Dolja and J. C. Carrington (2004) Viral RNA silencing suppressors inhibit the microRNA pathway at an intermediate step. Genes & Development 18:1179-1186.
Chellappan P., R. Vanitharani and C. M. Fauquet (2004) Short interfering RNA accumulation correlates with host recovery in DNA virus-infected hosts, and gene silencing targets specific viral sequences. Journal of Virology 78:7465-7477.
Chellappan P., R. Vanitharani and C. M. Fauquet (2005) MicroRNA-binding viral protein interferes with Arabidopsis development. Proceedings of the Nacional Academy of Sciences of the United States of America 102:10381-10386.
Chen H. Y., J. Yang, C. Lin and Y. A. Yuan (2008) Structural basis for RNA-silencing suppression by Tomato aspermy virus protein 2b. The EMBO Reports 9:754-760.
Chen J., W. X. Li, D. Xie, J. R. Peng and S. W. Ding (2004) Viral virulence protein suppresses RNA silencing-mediated defense but upregulates the role of microRNA in host gene expression. The Plant Cell 16:1302-1313.
Cheng J., R. Koukiekolo, K. Kieliszkiewicz, S. M. Sagan and J. P. Pezacki (2009) Cysteine residues of Carnation italian ringspot virus p19 suppressor of RNA silencing maintain global structural integrity and stability for siRNA binding. Biochimica et Biophysica Acta 1794:1197-1203.
Cheng Y. Q., Z. M. Liu, J. Xu, T. Zhou, M. Wang, Y. T. Chen, H. F. Li and Z. F. Fan (2008) HC-Pro protein of Sugar cane mosaic virus interacts specifically with maize ferredoxin-5 in vitro and in planta. Journal of General Virology 89:2046-2054.
Chiba M., J. C. Reed, A. I. Prokhnevsky, E. J. Chapman, M. Mawassi, E. V. Koonin, J. C. Carrington and V. V. Dolja (2006) Diverse suppressors of RNA silencing enhance agroinfection by a viral replicon. Virology 346:7-14.
Chiba S., K. Hleibieh, A. Delbianco, E. Klein, C. Ratti, V. Ziegler-Graff, S. Bouzoubaa and D. Gilmer (2013) The benyvirus RNA silencing suppressor is essential for long distance movement, requires both zinc-finger and NoLS basic residues but not a nucleolar localization for its silencing suppression activity. Molecular Plant-Microbe Interactions 26:168-181.
Chiu M. H., I. H. Chen, D. C. Baulcombe and C. H. Tsai (2010) The silencing suppressor P25 of Potato virus X interacts with Argonaute1 and mediates its degradation though the proteasome pathway. Molecular Plant Pathology 11:641-649.
Chu M., B. Desvoyes, M. Turina, R. Noad and H. B. Scholthof (2000) Genetic dissection of Tomato bushy stunt virus p19-protein-mediated host-dependent symptom induction and systemic invasion. Virology 266:79-87.
Chung H. Y., G. Lacatus and G. Sunter (2014) Geminivirus AL2 protein induces expression of, and interacts with, a calmodulin-like gene, an endogenous regulator of gene silencing. Virology 460-461:108-118.
Csorba T., A. Bovi, T. Dalmay and J. Burgyán (2007) The p122 subunit of Tobacco mosaic virus replicase is a potent silencing suppressor and compromises both small interfering RNA- and microRNA-mediated pathways. Journal of Virology 81:11768-11780.
Csorba T., L. Kontra and J. Burgyán (2015) Viral silencing suppressors: tools forged to fine-tune host-pathogen coexistence. Virology 479-480:85-103.
Csorba T., R. Lózsa, G. Hutvágner and J. Burgyán (2010) Polerovirus protein P0 prevents the assembly of small RNA-containing RISC complexes and leads to degradation of ARGONAUTE1. The Plant Journal 62:463-472.
Csorba T., V. Pantaleo and J. Burgyán (2009) RNA silencing: an antiviral mechanism. Advances in Virus Research 75:35-71.
Cuellar W. J., J. F. Kreuze, M. L. Rajamäki, K. R. Cruzado, M. Untiveros and J. P. T. Valkonen (2009) Elimination of antiviral defense by viral RNase III. Proceedings of the Nacional Academy of Sciences of the United States of America 106:10354-10358.
Culver J. N. and M. S. Padmanabhan (2007) Virus-induced disease: altering host physiology one interaction at a time. Annual Review of Phytopathology 45:221-243.
Dalmay T., A. Hamilton, S. Rudd, S. Angell and D. Baulcombe (2000) An RNA-dependent RNA polymerase gene in Arabidopsis is required for posttranscriptional gene silencing mediated by a transgene but not by a virus. Cell 101:543-553.
Deleris A., J. Gallego-Bartolome, J. Bao, K. D. Kasschau, J. C. Carrington and O. Voinnet (2006) Hierarchical action and inhibition of plant Dicer-like proteins in antiviral defense. Science 313:68-71.
Delfosse V. C., Y. C. Agrofoglio, M. F. Casse, I. B. Kresic, H. E. Hopp, V. Ziegler-Graff and A. J. Distéfano (2014) The P0 protein encoded by Cotton leafroll dwarf virus (CLRDV) inhibits local but not systemic RNA silencing. Virus Research 180:70-75.
Deng X., J. Kelloniemi, T. Haikonen, A. L. Vuorinen, P. Elomaa, T. H. Teeri and J. P. Valkonen (2013) Modification of Tobacco rattle virus RNA1 to serve as a VIGS vector reveals that the 29K movement protein is an RNA silencing suppressor of the virus. Molecular Plant-Microbe Interactions 26:503-514.
Deng X. G., X. J. Peng, F. Zhu, Y. J. Chen, T. Zhu, S. B. Qin, D. H. Xi and H. H. Lin (2015) A critical domain of Sweet potato chlorotic fleck virus nucleotide-binding protein (NaBp) for RNA silencing suppression, nuclear localization and viral pathogenesis. Molecular Plant Pathology 16:365-375.
Díaz-Pendón J. A. and S. W. Ding (2008) Direct and indirect roles of viral suppressors of RNA silencing in pathogenesis. Annual Review of Phytopathology 46:303-326.
Díaz-Pendón J. A., F. Li, W. X. Li and S. W. Ding (2007) Suppression of antiviral silencing by Cucumber mosaic virus 2b protein in Arabidopsis is associated with drastically reduced accumulation of three classes of viral small interfering RNAs. The Plant Cell 19:2053-2063.
Ding S. W. and O. Voinnet (2007) Antiviral immunity directed by small RNAs. Cell 130:413-426.
Ding X. S., J. Liu, N. H. Cheng, A. Folimonov, Y. M. Hou, Y. Bao, C. Katagi, S. A. Carter and R. S. Nelson (2004) The Tobacco mosaic virus 126-kDa protein associated with virus replication and movement suppresses RNA silencing. Molecular Plant-Microbe Interactions 17:583-592.
Donaire L., D. Barajas, B. Martínez-García, L. Martínez-Priego, I. Pagán and C. Llave (2008) Structural and genetic requirements for the biogenesis of Tobacco rattle virus-derived small interfering RNAs. Journal of Virology 82:5167-5177.
Donze T., F. Qu, P. Twigg and T. J. Morris (2014) Turnip crinkle virus coat protein inhibits the basal immune response to virus invasion in Arabidopsis by binding to the NAC transcription factor TIP. Virology 449:207-214.
Du Z., D. Xiao, J. Wu, D. Jia, Z. Yuan, Y. Liu, L. Hu, Z. Han, T. Wei, Q. Lin, Z. Wu and L. Xie (2011) P2 of Rice stripe virus (RSV) interacts with OsSGS3 and is a silencing suppressor. Molecular Plant Pathology 12:808-814.
Du Z., A. Chen, W. Chen, Q. Liao, H. Zhang, Y. Bao, M. J. Roossinck and J. P. Carr (2014) Nuclear-cytoplasmic partitioning of Cucumber mosaic virus protein 2b determines the balance between its roles as a virulence determinant and an RNA-silencing suppressor. Journal of Virology 88:5228-5241.
Duan C. G., Y. Y. Fang, B. J. Zhou, J. H. Zhao, W. N. Hou, H. Zhu, S. W. Ding and H. S. Guo (2012) Suppression of Arabidopsis ARGONAUTE1-mediated slicing, transgene-induced RNA silencing, and DNA methylation by distinct domains of the Cucumber mosaic virus 2b protein. The Plant Cell 24:259-274.
Dunoyer P., C. Himber and O. Voinnet (2005) DICER-LIKE 4 is required for RNA interference and produces the 21-nucleotide small interfering RNA component of the plant cell-to-cell silencing signal. Nature Genetics 37:1356-1360.
Dunoyer P., C. H. Lecellier, E. A. Parizotto, C. Himber and O. Voinnet (2004) Probing the microRNA and small interfering RNA pathways with virus-encoded suppressors of RNA silencing. The Plant Cell 16:1235-1250.
Dunoyer P., S. Pfeffer, C. Fritsch, O. Hemmer, O. Voinnet and K. E. Richards (2002) Identification subcellular localization and some properties of a cysteine-rich suppressor of gene silencing encoded by Peanut clump virus. The Plant Journal 29:555-567.
Eamens A. L., K. W. Kim, S. J. Curtin and P. M. Waterhouse (2012a) DRB2 is required for microRNA biogenesis in Arabidopsis thaliana. PloS ONE 7:e35933.
Eamens A. L., K. W. Kim and P. M. Waterhouse (2012b) DRB2, DRB3 and DRB5 function in a non-canonical microRNA pathway in Arabidopsis thaliana. Plant Signaling & Behavior 7:1224-1229.
Elbashir S. M., W. Lendeckel and T. Tuschl (2001) RNA interference is mediated by 21- and 22-nucleotide RNAs. Genes & Development 15:188-200.
Elena S. F. (2011) Evolutionary constraints on emergence of plant RNA viruses. In: Recent Advances in Plant Virology. C. Caranta, M. A. Aranda, M. Tepfer, J. J. López-Moya (eds.). Caister Academic Press. Norfolk, UK. pp. 283-300.
Endres M. W., B. D. Gregory, Z. Gao, A. W. Foreman, S. Mlotshwa, X. Ge, G. J. Pruss, J. R. Ecker, L. H. Bowman and V. Vance (2010) Two plant viral suppressors of silencing require the ethylene-inducible host transcription factor RAV2 to block RNA silencing. PLoS Pathogens 6:e1000729.
English J. J., E. Mueller and D. Baulcombe (1996) Suppression of virus accumulation in transgenic plants exhibiting silencing of nuclear genes. The Plant Cell 8:179-188.
Feng L., C. G. Duan and H. S. Guo (2013) Inhibition of in vivo Slicer activity of Argonaute protein 1 by the viral 2b protein independent of its dsRNA-binding function. Molecular Plant Pathology 14:617-622.
Fernández-Calvino L., L. Martínez-Priego, E. Z. Szabó, I. Guzmán-Benito, I. González, T. Canto, L. Lakatos and C. Llave (2016) Tobacco rattle virus 16K silencing suppressor binds Argonaute 4 and inhibits formation of RNA silencing complexes. Journal of General Virology 97:246-257.
Fukunaga R. and J. A. Doudna (2009) dsRNA with 5´ overhangs contributes to endogenous and antiviral RNA silencing pathways in plants. The EMBO Journal 28:545-555.
Fukuzawa N., N. Itchoda, T. Ishihara, K. Goto, C. Masuta and T. Matsumura (2010) HC-Pro, a potyvirus RNA silencing suppressor, cancels cycling of Cucumber mosaic virus in Nicotiana benthamiana plants. Virus Genes 40:440-446.
Fusaro A. F., R. L. Correa, K. Nakasugi, C. Jackson, L. Kawchuk, M. F. S. Vaslin and P. M. Waterhouse (2012) The Enamovirus p0 protein is a silencing suppressor which inhibits local and systemic RNA silencing through AGO1 degradation. Virology 426:178-187.
García J. A. and V. Pallás (2015) Viral factors involved in plant pathogenesis. Current Opinion in Virology 11:21-30.
García-Cano E., R. O. Resende, R. Fernández-Muñoz and E. Moriones (2006) Synergistic interaction between Tomato chlorosis virus and Tomato spotted wilt virus results in breakdown of resistance in tomato. Phytopathology 96:1263-1269.
García-Ruiz H., A. Takeda, E. J. Chapman, C. M. Sullivan, N. Fahlgren, K. J. Brempelis and J. C. Carrington (2010) Arabidopsis RNA-dependent RNA polymerases and dicer-like proteins in antiviral defense and small interfering RNA biogenesis during Turnip mosaic virus infection. The Plant Cell 22:481-496.
Genovés A., J. A. Navarro and V. Pallás (2006) Functional analysis of the five Melon necrotic spot virus genome-encoded proteins. Journal of General Virology 87:2371-2380.
Genovés A., V. Pallás and J. A. Navarro (2011) Contribution of topology determinants of a viral movement protein to its membrane association, intracellular traffic, and viral cell-to-cell movement. Journal of Virology 85:7797-7809.
Geri C., A. J. Love, E. Cecchini, S. J. Barrett, J. Laird, S. N. Covey and J. J. Milner (2004) Arabidopsis mutants that suppress the phenotype induced by transgene-mediated expression of Cauliflower mosaic virus (CaMV) gene VI are less susceptible to CaMV-infection and show reduced ethylene sensitivity. Plant Molecular Biology 56:111-124.
Gillet F. X., D. I. Cattoni, S. Petiot-Bécard, F. Delalande, V. Poignavent, J. P. Brizard, Y. Bessin, A. Dorsselaer, N. Declerck, S. Sanglier-Cianférani, C. Brugidou and F. Vignols (2013) The RYMV-encoded viral suppressor of RNA silencing P1 is a zinc-binding protein with redox-dependent flexibility. Journal of Molecular Biology 425:2423-2435.
Giner A., L. Lakatos, M. García-Chapa, J. J. López-Moya and J. Burgyán (2010) Viral protein inhibits RISC activity by argonaute binding through conserved WG/GW motifs. PLoS Pathogens 6:e1000996.
Glick E., A. Zrachya, Y. Levy, A. Mett, D. Gidoni, E. Belausov, V. Citovsky and Y. Gafni (2008) Interaction with host SGS3 is required for suppression of RNA silencing by Tomato yellow leaf curl virus V2 protein. Proceedings of the Nacional Academy of Sciences of the United States of America 105:157-161.
González I., L. Martínez, D. V. Rakitina, M. G. Lewsey, F. A. Atencio, C. Llave, N. O. Kalinina, J. P. Carr, P. Palukaitis and T. Canto (2010) Cucumber mosaic virus 2b protein subcellular targets and interactions: their significance to RNA silencing suppressor activity. Molecular Plant-Microbe Interactions 23:294-303.
González I., D. Rakitina, M. Semashko, M. Taliansky, S. Praveen, P. Palukaitis, J. P. Carr, N. Kalinina and T. Canto (2012) RNA binding is more critical to the suppression of silencing function of Cucumber mosaic virus 2b protein than nuclear localization. RNA 18:771-782.
González-Jara P., F. A. Atencio, B. Martínez-García, D. Barajas, F. Tenllado and J. R. Díaz-Ruiz (2005) A single amino acid mutation in the Plum pox virus helper component-proteinase gene abolishes both synergistic and RNA silencing suppression activities. Phytopathology 95:894-901.
González-Jara P., F. Tenllado, B. Martínez-García, F. A. Atencio, D. Barajas, M. Vargas, J. Díaz-Ruiz and J. R. Díaz-Ruiz (2004) Host-dependent differences during synergistic infection by potyviruses with Potato virus X. Molecular Plant Pathology 5:29-35.
Goswami S., N. Sahana, V. Pandey, P. Doblas, R. K. Jain, P. Palukaitis, T. Canto and S. Praveen (2012) Interference in plant defense and development by non-structural protein NSs of Groundnut bud necrosis virus. Virus Research 163:368-373.
Goto K., T. Kobori, Y. Kosaka, T. Natsuaki and C. Masuta (2007) Characterization of silencing suppressor 2b of Cucumber mosaic virus based on examination of its small RNA-binding abilities. Plant & Cell Physiology 48:1050-1060.
Gouveia P., S. Dandlen, A. Costa, N. Marques and G. Nolasco (2012) Identification of an RNA silencing suppressor encoded by Grapevine leafroll-associated virus 3. European Journal of Plant Pathology 133:237-245.
Gouveia P. and G. Nolasco (2012) The p19.7 RNA silencing suppressor from Grapevine leafroll-associated virus 3 shows different levels of activity across phylogenetic groups. Virus Genes 45:333-339.
Guilley H., D. Bortolamiol, G. Jonard, S. Bouzoubaa and V. Ziegler-Graff (2009) Rapid screening of RNA silencing suppressors by using a recombinant virus derived from Beet necrotic yellow vein virus. Journal of General Virology 90:2536-2541.
Guo H. S. and S. W. Ding (2002) A viral protein inhibits the long range signaling activity of the gene silencing signal. The EMBO Journal 21:398-407.
Haag J. R. and C. S. Pikaard (2011) Multisubunit RNA polymerases IV and V: Purveyors of non-coding RNA for plant gene silencing. Nature Reviews Molecular Cell Biology 12:483-492.
Haas G., J. Azevedo, G. Moissiard, A. Geldreich, C. Himber, M. Bureau, T. Fukuhara, M. Keller and O. Voinnet (2008) Nuclear import of CaMV P6 is required for infection and suppression of the RNA silencing factor DRB4. The EMBO Journal 27:2102-2112.
Haikonen T., M. L. Rajamäki Y. P. Tian and J. P. T. Valkonen (2013a) Interaction of the microtubule-associated host protein HIP2 with viral helper component proteinase is important in infection with Potato virus A.Molecular Plant-Microbe Interactions 26:734-744.
Haikonen T., M. L. Rajamaki, Y. P. Tian and J. P. Valkonen (2013b) Mutation of a short variable region in HCpro protein of Potato virus A affects interactions with a microtubule-associated protein and induces necrotic responses in tobacco. Molecular Plant-Microbe Interactions 26:721-733.
Hamera S., X. Song, L. Su, X. Chen and R. Fang (2012) Cucumber mosaic virus suppressor 2b binds to AGO4-related small RNAs and impairs AGO4 activities. The Plant Journal 69:104-115.
Hamilton A. J. and D. C. Baulcombe (1999) A species of small antisense RNA in posttranscriptional gene silencing in plants. Science 286:950-952.
Hammond R. W. and J. Hammond (2013) Evaluating the silencing suppressor activity of proteins encoded by Maize rayado fino virus. In: APS-MSA Join Meeting. 10 - 14 August. Poster session: Molecular Plant-Microbe Interactions-Viruses. Austin, Texas. pp:623.
Han Y. H., H. Y. Xiang, Q. Wang, Y. Y. Li, W. Q. Wu, C. G. Han, D. W. Li and J. L. Yu (2010) Ring structure amino acids affect the suppressor activity of Melon aphid-borne yellows virus P0 protein. Virology 406:21-27.
Hao X., A. Lu, N. Sokal, B. Bhagwat, E. Leung, R. Mao, R. Reade, Y. Wu, D. Rochon and Y. Xiang (2011) Cucumber necrosis virus p20 is a viral suppressor of RNA silencing. Virus Research 155:423-432.
Harries P. A., K. Palanichelvam, S. Bhat and R. S. Nelson (2008)Tobacco mosaic virus 126-kDa protein increases the susceptibility of Nicotiana tabacum to other viruses and its dosage affects virus-induced gene silencing. Molecular Plant-Microbe Interactions 21:1539-1548.
Harvey J. J., M. G. Lewsey, K. Patel, J. Westwood, S. Heimstädt, J. P. Carr and D. C. Baulcombe (2011) An antiviral defense role of AGO2 in plants. PLoS ONE 6:e14639.
Havelda Z., C. Hornyik, A. Valoczi and J. Burgyán (2005) Defective interfering RNA hinders the activity of a tombusvirus-encoded posttranscriptional gene silencing suppressor. Journal of Virology 79:450-457.
Hemmes H., L. Lakatos, R. Goldbach, J. Burgyán and M. Prins (2007) The NS3 protein of Rice hoja blanca tenuivirus suppresses RNA silencing in plant and insect hosts by efficiently binding both siRNAs and miRNAs. RNA 13:1079-1089.
Hendelman A., M. Kravchik, R. Stav, M. Zik, N. Lugassi and T. Arazi (2013) The developmental outcomes of P0-mediated ARGONAUTE destabilization in tomato. Planta 237:363-377.
Henderson I. R., A. Deleris, W. Wong, X. Zhong, H. G. Chin, G. A. Horwitz, K. A. Kelly, S. Pradhan and S. E. Jacobsen (2010) The de novo cytosine methyltransferase DRM2 requires intact UBA domains and a catalytically mutated paralog DRM3 during RNA-directed DNA methylation in Arabidopsis thaliana. PLoS Genetics 6:e1001182.
Henderson I. R., X. Zhang, C. Lu, L. Johnson, B. C. Meyers, P. J. Green and S. E. Jacobsen (2006) Dissecting Arabidopsis thaliana DICER function in small RNA processing, gene silencing and DNA methylation patterning. Nature Genetics 38:721-725.
Hiraguri A., R. Itoh, N. Kondo, Y. Nomura, D. Aizawa, Y. Murai, H. Koiwa, M. Seki, K. Shinozaki and T. Fukuhara (2005) Specific interactions between dicer-like proteins and HYL1/DRB-family dsRNA-binding proteins in Arabidopsis thaliana. Plant Molecular Biology 57:173-188.
Hsieh Y. C., R. T. Omarov and H. B. Scholthof (2009) Diverse and newly recognized effects associated with short interfering RNA binding site modifications on the Tomato bushy stunt virus P19 silencing suppressor. Journal of Virology 83:2188-2200.
Hu Q., J. Hollunder, A. Niehl, C. J. Korner, D. Gereige, D. Windels, A. Arnold, M. Kuiper, F. Vazquez, M. Pooggin and M. Heinlein (2011) Specific impact of tobamovirus infection on the Arabidopsis small RNA profile. PloS ONE 6:e19549.
Inaba J., B. M. Kim, H. Shimura and C. Masuta (2011) Virus-induced necrosis is a consequence of direct protein-protein interaction between a viral RNA-silencing suppressor and a host catalase. Plant Physiology 156:2026-2036.
Jamous R. M., K. Boonrod, M. W. Fuellgrabe, M. S. Ali-Shtayeh, G. Krczal and M. Wassenegger (2011) The helper component-proteinase of the Zucchini yellow mosaic virus inhibits the Hua Enhancer 1 methyltransferase activity in vitro. Journal of General Virology 92:2222-2226.
Jaubert M., S. Bhattacharjee, A. F. S. Mello, K. L. Perry and P. Moffett (2011) ARGONAUTE2 mediates RNA-silencing antiviral defenses against Potato virus X in Arabidopsis.Plant Physiology 156:1556-1564.
Jay F., Y. Wang, A. Yu, L. Taconnat, S. Pelletier, V. Colot, J. P. Renou and O. Voinnet (2011) Misregulation of AUXIN RESPONSE FACTOR 8 underlies the developmental abnormalities caused by three distinct viral silencing suppressors in Arabidopsis. PLoS Pathogens 7:e1002035.
Jeong R. D., A. C. Chandra-Shekara, A. Kachroo, D. F. Klessig and P. Kachroo (2008) HRT-mediated hypersensitive response and resistance to Turnip crinkle virus in Arabidopsis does not require the function of TIP, the presumed guardee protein. Molecular Plant-Microbe Interactions 21:1316-1324.
Ji L. H. and S. W. Ding (2001) The suppressor of transgene RNA silencing encoded by Cucumber mosaic virus interferes with salicylic acid-mediated virus resistance. Molecular Plant-Microbe Interactions 14:715-724.
Jin H. and J. K. Zhu (2010) A viral suppressor protein inhibits host RNA silencing by hooking up with Argonautes. Genes & Development 24:853-856.
Jin Y., D. Ma, J. Dong, D. Li, C. Deng, J. Jin and T. Wang (2007) The HC-Pro protein of Potato virus Y interacts with NtMinD of tobacco. Molecular Plant-Microbe Interactions 20:1505-1511.
Kalantidis K., H. T. Schumacher, T. Alexiadis and J. M. Helm (2008) RNA silencing movement in plants. Biology of the Cell 100:13-26.
Karlowski W. M., A. Zielezinski, J. Carrere, D. Pontier, T. Lagrange and R. Cooke (2010) Genome-wide computational identification of WG/GW Argonaute-binding proteins in Arabidopsis. Nucleic Acids Research 38:4231-4245.
Karran R. A. and H. Sanfaçon (2014) Tomato ringstpot virus coat protein binds to ARGONAUTE 1 and suppresses the translation repression of a reporter gene. Molecular Plant-Microbe Interactions 27:933-943.
Karyeija R. F., J. F. Kreuze, R. W. Gibson and J. P. T. Valkonen (2000) Synergistic interactions of a potyvirus and a phloem-limited crinivirus in sweet potato plants. Virology 269:26-36.
Kasschau K. D. and J. C. Carrington (1998) A counter-defensive strategy of plant viruses: suppression of posttranscriptional gene silencing. Cell 95:461-470.
Kasschau K. D., Z. Xie, E. Allen, C. Llave, E. J. Chapman, K. A. Krizan and J. C. Carrington (2003) P1/HC-Pro, a viral suppressor of RNA silencing, interferes with Arabidopsis development and miRNA function. Developmental Cell 4:205-217.
Kataya A. R. A., M. N. S. Suliman, K. Kalantidis and I. C. Livieratos (2009) Cucurbit yellow stunting disorder virus p25 is a suppressor of post-transcriptional gene silencing. Virus Research 145:48-53.
Kim V. N. (2005) Small RNAs: classification, biogenesis, and function. Molecules and Cells 19:1-15.
Király L., A. B. Cole, J. E. Bourque and J. E. Schoelz (1999) Systemic cell death is elicited by the interaction of a single gene in Nicotiana clevelandii and gene VI of Cauliflower mosaic virus. Molecular Plant-Microbe Interactions 12:919-925.
Koukiekolo R., S. M. Sagan and J. P. Pezacki (2007) Effects of pH and salt concentration on the siRNA binding activity of the RNA silencing suppressor protein p19. FEBSLetters 581:3051-3056.
Kozlowska-Makulska A., H. Guilley, M. S. Szyndel, M. Beuve, O. Lemaire, E. Herrbach and S. Bouzoubaa (2010) P0 proteins of European beet-infecting poleroviruses display variable RNA silencing suppression activity. Journal of General Virology 91:1082-1091.
Kreuze J. F., E. I. Savenkov, W. Cuellar, X. Li and J. P. T. Valkonen (2005) Viral class 1 RNase III involved in suppression of RNA silencing. Journal of Virology 79:7227-7238.
Kubota K. and J. C. Ng (2016) Lettuce chlorosis virus p23 suppresses RNA silencing and induces local necrosis with increased severity at raised temperatures. Phytopathology 106:653-662 http://dx.doi.org.sci-hub.io/10.1094/PHYTO-09-15-0219-R
Kubota K., S. Tsuda, A. Tamai and T. Meshi (2003) Tomato mosaic virus replication protein suppressed virus-targeted posttranscriptional gene silencing. Journal of Virology 77:11016-11026.
Kumakura N., A. Takeda, Y. Fujioka, H. Motose, R. Takano and Y. Watanabe (2009) SGS3 and RDR6 interact and colocalize in cytoplasmic SGS3/RDR6-bodies. FEBS Letters 583:1261-1266.
Kurihara Y., N. Inaba, N. Kutsuna, A. Takeda, Y. Tagami and Y. Watanabe (2007) Binding of tobamovirus replication protein with small RNA duplexes. Journal of General Virology 88:2347-2352.
Lacombe S., M. Bangratz, F. Vignols and C. Brugidou (2010) The Rice yellow mottle virus P1 protein exhibits dual functions to suppress and activate gene silencing. The Plant Journal 61:371-382.
Lakatos L., T. Csorba, V. Pantaleo, E. J. Chapman, J. C. Carrington, Y. P. Liu, V. V. Dolja, L. Fernández C., J. J. López-Moya and J. Burgyán (2006) Small RNA binding is a common strategy to suppress RNA silencing by several viral suppressors. The EMBO Journal 25:2768-2780.
Landeo-Ríos Y., J. Navas-Castillo, E. Moriones and M. C. Cañizares (2016a) The p22 RNA silencing suppressor of the crinivirus Tomato chlorosis virus preferentially binds long dsRNAs preventing them from cleavage. Virology 488:129-136.
Landeo-Ríos Y., J. Navas-Castillo, E. Moriones and M. C. Cañizares (2016b) The p22 RNA silencing suppressor of the crinivirus Tomato chlorosis virus is dispensable for local viral replication but important for counteracting an antiviral RDR6-mediated response during systemic infection. Viruses 8:182. doi:10.3390/v8070182
Law S. M., B. W. Zhang and C. L. Brooks (2013) pH-sensitive residues in the P19 RNA silencing suppressor protein from Carnation italian ringspot virus affect siRNA binding stability. Protein Science 22:595-604.
Lewsey M., F. C. Robertson, T. Canto, P. Palukaitis and J. P. Carr (2007) Selective targeting of miRNA-regulated plant development by a viral counter-silencing protein. The Plant Journal 50:240-252.
Li F. and S. W. Ding (2006) Virus counterdefense: diverse strategies for evading the RNA-silencing immunity. Annual Review of Microbiology 60:503-531.
Li F., C. Huang, Z. Li and X. Zhou (2014) Suppression of RNA silencing by a plant DNA virus satellite requires a host calmodulin-like protein to repress RDR6 expression. PLoS Pathogens 10:e1003921.
Li H. W., A. P. Lucy, H. S. Guo, W. X. Li, L. H. Ji, S. M. Wong and S. W. Ding (1999) Strong host resistance targeted against a viral suppressor of the plant gene silencing defence mechanism. The EMBO Journal 18:2683-2691.
Lindbo J. A. and W. G. Dougherty (1992) Pathogen-derived resistance to a potyvirus: immune and resistant phenotypes in transgenic tobacco expressing altered forms of a potyvirus coat protein nucleotide sequence. Molecular Plant-Microbe Interactions 5:144-153.
Liu L., J. Grainger, M. C. Cañizares, S. M. Angell and G. P. Lomonossoff (2004) Cowpea mosaic virus RNA1 acts as an amplicon whose effects can be counteracted by a RNA-2-encoded suppressor of silencing. Virology 323:37-48.
Llave C., K. D. Kasschau and J. C. Carrington (2000) Virus-encoded suppressor of posttranscriptional gene silencing targets a maintenance step in the silencing pathway. Proceedings of the Nacional Academy of Sciences of the United States of America 97:13401-13406.
Lozano-Durán R., T. Rosas-Díaz, G. Gusmaroli, A. P. Luna, L. Taconnat, X. W. Deng and E. R. Bejarano (2011) Geminiviruses subvert ubiquitination by altering CSN-mediated derubylation of SCF E3 ligase complexes and inhibit jasmonate signaling in Arabidopsis thaliana. The Plant Cell 23:1014-1032.
Lózsa R., T. Csorba, L. Lakatos and J. Burgyán (2008) Inhibition of 3´ modification of small RNAs in virus-infected plants require spatial and temporal co-expression of small RNAs and viral silencing-suppressor proteins. Nucleic Acids Research 36:4099-4107.
Lu R., A. Folimonov, M. Shintaku, W. X. Li, B. W. Falk, W. O. Dawson and S. W. Ding (2004) Three distinct suppressors of RNA silencing encoded by a 20-kb viral RNA genome. Proceedings of the National Academy of Sciences of the United States of America 101:15742-15747.
Lukhovitskaya N. I., R. R. Vetukuri, I. Sama, S. Thaduri, A. G. Solovyev and E. I. Savenkov (2014) A viral transcription factor exhibits antiviral RNA silencing suppression activity independent of its nuclear localization. Journal of General Virology 95:2831-2837.
Mallory A. C., L. Ely, T. H. Smith, R. Marathe, R. Anandalakshmi, M. Fagard, H. Vaucheret, G. Pruss, L. Bowman and V. B. Vance (2001) HC-Pro suppression of transgene silencing eliminates the small RNAs but not transgene methylation or the mobile signal. The Plant Cell 13:571-583.
Mandadi K. K. and K. B. Scholthof (2013) Plant immune responses against viruses: how does a virus cause disease? The Plant Cell 25:1489-1505.
Mangwende T., M. L. Wang, W. Borth, J. Hu, P. H. Moore, T. E. Mirkov and H. H. Albert (2009) The P0 gene of Sugarcane yellow leaf virus encodes an RNA silencing suppressor with unique activities. Virology 384:38-50.
Martínez-Priego L., L. Donaire, D. Barajas and C. Llave (2008) Silencing suppressor activity of the Tobacco rattle virus-encoded 16-kDa protein and interference with endogenous small RNA-guided regulatory pathways. Virology 376:346-356.
Martínez-Turiño S. and C. Hernández (2009) Inhibition of RNA silencing by the coat protein of Pelargonium flower break virus: distinctions from closely related suppressors. Journal of General Virology 90:519-525.
Martín-Hernández A. M. and D. C. Baulcombe (2008) Tobacco rattle virus 16-kilodalton protein encodes a suppressor of RNA silencing that allows transient viral entry in meristems. Journal of Virology 82:4064-4071.
Mathioudakis M. M., L. Rodríguez-Moreno, R. N. Sempere, M. A. Aranda and I. Livieratos (2014) Multifaceted capsid proteins: multiple interactions suggest multiple roles for Pepino mosaic virus capsid protein. Molecular Plant-Microbe Interactions 27:1356-1369.
Mathioudakis M. M., R. S. L. Veiga, T. Canto, V. Medina, D. Mossialos, A. M. Makris and I. Livieratos (2013) Pepino mosaic virus triple gene block protein 1 (TGBp1) interacts with and increases tomato catalase 1 activity to enhance virus accumulation. Molecular Plant Pathology 14:589-601.
Matzke M., T. Kanno, L. Daxinger, B. Huettel and A. J. Matzke (2009) RNA-mediated chromatin-based silencing in plants. Current Opinion in Cell Biology 21:367-376.
Mbanzibwa D. R., Y. Tian, S. B. Mukasa and J. P. T. Valkonen (2009) Cassava Brown Streak Virus (Potyviridae) encodes a putative Maf/HAM1 pyrophosphatase implicated in reduction of mutations and a P1 proteinase that suppresses RNA silencing but contains no HC-Pro. Journal of Virology 83:6934-6940.
Melnyk C. W., A. Molnar and D. C. Baulcombe (2011) Intercellular and systemic movement of RNA silencing signals. The EMBO Journal 30:3553-3563.
Meng C., J. Chen, S. W. Ding, J. Peng and S. M. Wong (2008) Hibiscus chlorotic ringspot virus coat protein inhibits trans-acting small interfering RNA biogenesis in Arabidopsis. Journal of General Virology 89:2349-2358.
Meng C., J. Chen, J. Peng and S. M. Wong (2006) Host-induced avirulence of Hibiscus chlorotic ringspot virus mutants correlates with reduced gene-silencing suppression activity. Journal of General Virology 87:451-459.
Mérai Z, Z. Kerényi, S. Kertész, M. Magna, L. Lakatos and D. Silhavy (2006) Double-stranded RNA binding may be a general plant RNA viral strategy to suppress RNA silencing. Journal of Virology 80:5747-5756.
Mérai Z., Z. Kerényi, A. Molnár, E. Barta, A. Válóczi, G. Bisztray, Z. Havelda, J. Burgyán and D. Silhavy (2005) Aureusvirus P14 is an efficient RNA silencing suppressor that binds double-stranded RNAs without size specificity. Journal of Virology 79:7217-7226.
Mingot A., A. Valli, B. Rodamilans, D. San León, D. C. Baulcombe, J. A. García and J. J. López-Moya (2016) The P1N-PISPO trans-frame gene of Sweet potato feathery mottle Potyvirus is produced during virus infection and functions as RNA silencing suppressor. Journal of Virology 90:3543-3557.
Molnár A., T. Csorba, L. Lakatos, E. Várallyay, C. Lacomme and J. Burgyán (2005) Plant virus-derived small interfering RNAs originate predominantly from highly structured single-stranded viral RNAs. Journal of Virology 79:7812-7818.
Molnar A., C. W. Melnyk, A. Bassett, T. J. Hardcastle, R. Dunn and D. C. Baulcombe (2010) Small silencing RNAs in plants are mobile and direct epigenetic modification in recipient cells. Science 328:872-875.
Morel J. B., C. Godon, P. Mourrain, C. Béclin, S. Boutet, F. Feuerbach, F. Proux and H. Vaucheret (2002) Fertile hypomorphic ARGONAUTE (ago1) mutants impaired in post-transcriptional gene silencing and virus resistance. The Plant Cell 14:629-639.
Mourrain P., C. Béclin, T. Elmayan, F. Feuerbach, C. Godon, J. B. Morel, D. Jouette, A. M. Lacombe, S. Nikic, N. Picault, K. Rémoué, M. Sanial, T. A. Vo and H. Vaucheret (2000) Arabidopsis SGS2 and SGS3 genes are required for posttranscriptional gene silencing and natural virus resistance. Cell 101:533-542.
Mukasa S. B., P. R. Rubaihayo and J. P. T. Valkonen (2006) Interactions between a crinivirus, an ipomovirus and a potyvirus in co-infected sweet potato plants. Plant Pathology 55:458-467.
Murphy J. F. and K. L. Bowen (2006) Synergistic disease in pepper caused by the mixed infection of Cucumber mosaic virus and Pepper mottle virus. Phytopathology 96:240-247.
Napoli C., C. Lemieux and R. Jorgensen (1990) Introduction of a chimeric chalcone synthase gene into petunia results in reversible co-suppression of homologous genes in trans. The Plant Cell 2:279-289.
Nemes K., A. Gellért, E. Balázs and K. Salánki (2014) Alanine scanning of Cucumber mosaic virus (CMV) 2b protein identifies different positions for cell-to-cell movement and gene silencing suppressor activity. PloS ONE 9:e112095.
Netsu O., A. Hiraguri, T. Uehara-Ichiki, K. Komatsu and T. Sasaya (2015) Functional comparison of RNA silencing suppressor between the p5 protein of Rice grassy stunt virus and p3 protein of Rice stripe virus. Virus Research 203:10-19.
Okano Y., H. Senshu, M. Hashimoto, Y. Neriya, O. Netsu, N. Minato, T. Yoshida, K. Maejima, K. Oshima, K. Komatsu, Y. Yamaji and S. Namba (2014) In planta recognition of a double-stranded RNA synthesis protein complex by a potexviral RNA silencing suppressor. The Plant Cell 26:2168-2183.
Olspert A., K. Kamsol, C. Sarmiento, J. Gerassimenko and E. Truve (2014)Cocksfoot mottle virus coat protein is dispensable for the systemic infection. Virology Journal 11:19-29.
Olspert A., H. Paves, R. Toomela, T. Tamm and E. Truve (2010) Cocksfoot mottle sobemovirus coat protein contains two nuclear localization signals. Virus Genes 40:423-431.
Omarov R., K. Sparks, L. Smith, J. Zindovic and H. B. Scholthof (2006) Biological relevance of a stable biochemical interaction between the Tombusvirus-encoded P19 and short interfering RNAs. Journal of Virology 80:3000-3008.
Pacheco R., A. García-Marcos, A. Manzano, M. García de L., G. Camañes, P. García-Agustín, J. R. Díaz-Ruíz and F. Tenllado (2012) Comparative analysis of transcriptomic and hormonal responses to compatible and incompatible plant-virus interactions that lead to cell death. Molecular Plant-Microbe Interactions 25:709-723.
Pallás V. and J. A. García (2011) How do plant viruses induce disease? Interactions and interference with host components. Journal of General Virology 92:2691-2705.
Park J. W., S. Faure-Rabasse, M. A. Robinson, B. Desvoyes and H. B. Scholthof (2004) The multifunctional plant viral suppressor of gene silencing P19 interacts with itself and an RNA binding host protein. Virology 323:49-58.
Pasquinelli A. E. and G. Ruvkun (2002) Control of developmental timing by microRNAs and their targets. Annual Review of Cell and Developmental Biology 18:495-513.
Pazhouhandeh M., M. Dieterle, K. Marrocco, E. Lechner, B. Berry, V. Brault, O. Hemmer, T. Kretsch, K. E. Richards, P. Genschik and V. Ziegler-Graff (2006) F-box-like domain in the polerovirus protein P0 is required for silencing suppressor function. Proceedings of the Nacional Academy of Sciences of the United States of America 103:1994-1999.
Pérez-Cañamás M. and C. Hernández (2015) Key importance of small RNA binding for the activity of the glycine-tryptophan (GW) motif-containing viral suppressor of RNA silencing. The Journal of Biological Chemistry 290:3106-3120.
Powers J. G., T. L. Sit, C. Heinsohn, C. G. George, K. H. Kim and S. A. Lommel (2008) The Red clover necrotic mosaic virus RNA-2 encoded movement protein is a second suppressor of RNA silencing. Virology 381:277-286.
Pruss G., X. Ge, X. M. Shi, J. C. Carrington and V. B. Vance (1997) Plant viral synergism: the potyviral genome encodes a broad-range pathogenicity enhancer that transactivates replication of heterologous viruses. The Plant Cell 9:859-868.
Pruss G. J., C. B. Lawrence, T. Bass, Q. Q. Li, L. H. Bowman and V. Vance (2004) The potyviral suppressor of RNA silencing confers enhanced resistance to multiple pathogens. Virology 320:107-120.
Qi X., F. S. Bao and Z. Xie (2009) Small RNA deep sequencing reveals role for Arabidopsis thaliana RNA-dependent RNA polymerases in viral siRNA biogenesis. PLoS ONE 4:e4971.
Qu F., T. Ren and T. J. Morris (2003) The coat protein of Turnip crinkle virus suppresses posttranscriptional gene silencing at an early initiation step. Journal of Virology 77:511-522.
Qu F., X. Ye, G. Hou, S. Sato, T. E. Clemente and T. J. Morris (2005) RDR6 has a broad-spectrum but temperature-dependent antiviral defense role in Nicotiana benthamiana. Journal of Virology 79:15209-15217.
Qu F., X. Ye and T. J. Morris (2008) Arabidopsis DRB4, AG01, AG07, and RDR6 participate in a DCL4-initiated antiviral RNA silencing pathway negatively regulated by DCL1. Proceedings of the National Academy of Sciences of the United States of America 105:14732-14737.
Rahim M. D., I. B. Andika, C. Han, H. Kondo and T. Tamada (2007) RNA4-encoded p31 of Beet necrotic yellow vein virus is involved in efficient vector transmission, symptom severity and silencing suppression in roots. Journal of General Virology 88:1611-1619.
Rajamäki M. L., J. Streng and J. P. T. Valkonen (2014) Silencing suppressor protein VPg of a potyvirus interacts with the plant silencing-related protein SGS3. Molecular Plant-Microbe Interactions 27:1199-1210.
Rajamäki M. L. and J. P. T. Valkonen (2009) Control of nuclear and nucleolar localization of nuclear inclusion protein a of picorna-like Potato virus A in Nicotiana species. The Plant Cell 21:2485-2502.
Ratcliff F., B. D. Harrison and D. C. Baulcombe (1997) A similarity between viral defense and gene silencing in plants. Science 276:1558-1560.
Rawlings R. A., V. Krishnan and N. G. Walter (2011) Viral RNAi suppressor reversibly binds siRNA to outcompete dicer and RISC via multiple-turnover. Journal of Molecular Biology 408:262-276.
Reed J. C., K. D. Kasschau, A. I. Prokhnevsky, K. Gopinath, G. P. Pogue, J. C. Carrington and V. V. Dolja (2003) Suppressor of RNA silencing encoded by Beet yellows virus.Virology 306:203-209.
Ren B., Y. Guo, F. Gao, P. Zhou, F. Wu, Z. Meng, C. Wei and Y. Li (2010) Multiple functions of Rice dwarf phytoreovirus Pns10 in suppressing systemic RNA silencing. Journal of Virology 84:12914-12923.
Ren T., F. Qu and T. J. Morris (2000) HRT gene function requires interaction between a NAC protein and viral capsid protein to confer resistance to Turnip crinkle virus. The Plant Cell 12:1917-1925.
Rhoades M. W., B. J. Reinhart, L. P. Lim, C. B. Burge, B. Bartel and D. P. Bartel (2002) Prediction of plant microRNA targets. Cell 110:513-520.
Ronde D., A. Pasquier, S. Ying, P. Butterbach, D. Lohuis and R. Kormelink (2014) Analysis of Tomato spotted wilt virus NSs protein indicates the importance of the N-terminal domain for avirulence and RNA silencing suppression. Molecular Plant Pathology 15:185-195.
Ruiz-Ferrer V. and O. Voinnet (2009) Roles of plant small RNAs in biotic stress responses. Annual Review of Plant Biology 60:485-510.
Ruiz-Ruiz S., N. Soler, J. Sánchez-Navarro, C. Fagoaga, C. López, L. Navarro, P. Moreno, L. Peña and R. Flores (2013)Citrus tristeza virus p23: determinants for nucleolar localization and their influence on suppression of RNA silencing and pathogenesis. Molecular Plant-Microbe Interactions 26:306-318.
Sahana N., H. Kaur, R. K. Jain, P. Palukaitis, T. Canto and S. Praveen (2014) The asparagine residue in the FRNK box of potyviral helper-component protease is critical for its small RNA binding and subcellular localization. Journal of General Virology 95:1167-1177.
Sarmiento C., E. Gomez, M. Meier, T. A. Kavanagh and E. Truve (2007) Cocksfoot mottle virus P1 suppresses RNA silencing in Nicotiana benthamiana and Nicotiana tabacum. Virus Research 123:95-99.
Schnettler E., H. Hemmes, R. Huismann, R. Goldbach, M. Prins and R. Kormelink (2010) Diverging affinity of tospovirus RNA silencing suppressor proteins, NSs, for various RNA duplex molecules. Journal of Virology 84:11542-11554.
Schwach F., F. E. Vaistij, L. Jones and D. C. Baulcombe (2005) An RNA-dependent RNA polymerase prevents meristem invasion by Potato virus X and is required for the activity but not the production of a systemic silencing signal. Plant Physiology 138:1842-1852.
Senshu H., J. Ozeki, K. Komatsu, M. Hashimoto, K. Hatada, M. Aoyama, S. Kagiwada, Y. Yamaji and S. Namba (2009) Variability in the level of RNA silencing suppression caused by triple gene block protein 1 (TGBp1) from various potexviruses during infection. Journal of General Virology 90:1014-1024.
Senshu H., Y. Yamaji, N. Minato, T. Shiraishi, K. Maejima, M. Hashimoto, C. Miura, Y. Neriya and S. Namba (2011) A dual strategy for the suppression of host antiviral silencing: two distinct suppressors for viral replication and viral movement encoded by Potato virus M. Journal of Virology 85:10269-10278.
Shen M., Y. Xu, R. Jia, X. Zhou and K. Ye (2010a) Size-independent and noncooperative recognition of dsRNA by the Rice stripe virus RNA silencing suppressor NS3. Journal of Molecular Biology 404:665-679.
Shen W., P. Yan, L. Gao, X. Pan, J. Wu and P. Zhou (2010b) Helper component proteinase (HCPro) protein of Papaya ringspot virus interacts with papaya calreticulin. Molecular Plant Pathology 11:335-346.
Shiboleth Y. M., E. Haronsky, D. Leibman, T. Arazi, M. Wassenegger, S. A. Whitham, V. Gaba and A. Gal-On (2007) The conserved FRNK box in HC-Pro, a plant viral suppressor of gene silencing, is required for small RNA binding and mediates symptom development. Journal of Virology 81:13135-13148.
Shimura H., C. Masuta, N. Yoshida, K. Sueda and M. Suzuki (2013) The 2b protein of Asparagus virus 2 functions as an RNA silencing suppressor against systemic silencing to prove functional synteny with related cucumovirues. Virology 442:180-188.
Shivaprasad P. V., H. M. Chen, K. Patel, D. M. Bond, B. A. C. M. Santos and D. C. Baulcombe (2012) A microRNA superfamily regulates nucleotide binding site-leucine-rich repeats and other mRNAs. The Plant Cell 24:859-874.
Shivaprasad P. V., R. Rajeswaran, T. Blevins, J. Schoelz, F. Jr. Meins, T. Hohn and M. M. Pooggin (2008) The CaMV transactivator/viroplasmin interferes with RDR6-dependent trans-acting and secondary siRNA pathways in Arabidopsis. Nucleic Acids Research 36:5896-5909.
Silhavy D., A. Molnár, A. Lucioli, G. Szittya, C. Hornyik, M. Tavazza and J. Burgyán (2002) A viral protein suppresses RNA silencing and binds silencing-generated, 21- to 25-nucleotide double-stranded RNAs. The EMBO Journal 21:3070-3080.
Sun L., I. B. Andika, H. Kondo and J. Chen (2013a) Identification of the amino acid residues and domains in the cysteine-rich protein of Chinese wheat mosaic virus that are important for RNA silencing suppression and subcellular localization. Molecular Plant Pathology 14:265-278.
Sun L., I. B. Andika, J. Shen, D. Yang, C. Ratti and J. Chen (2013b) The CUG-initiated larger form coat protein of Chinese wheat mosaic virus binds to the cysteine-rich RNA silencing suppressor. Virus Research 177:66-74.
Szabó E. Z., M. Manczinger, A. Göblös, L. Kemény and L. Lakatos (2012) Switching on RNA silencing suppressor activity by restoring argonaute binding to a viral protein. Journal of Virology 86:8324-8327.
Taiwo M. A., K. T. Kareem, I. Y. Nsa and J. D’A. Hughes (2007) Cowpea viruses: effect of single and mixed infections on symptomatology and virus concentration. Virology Journal 4:95. doi: 10.1186/1743-422X-4-95
Takeda A., M. Tsukuda, H. Mizumoto, K. Okamoto, M. Kaido, K. Mise and T. Okuno (2005) A plant RNA virus suppresses RNA silencing through viral RNA replication. The EMBO Journal 24:3147-3157.
Tatineni S., F. Qu, R. Li, T. J. Morris and R. French (2012) Triticum mosaic poacevirus enlists P1 rather than HC-Pro to suppress RNA silencing-mediated host defense. Virology 433:104-115.
Te J., U. Melcher, A. Howard and J. Verchot-Lubicz (2005)Soilborne wheat mosaic virus (SBMV) 19K protein belongs to a class of cysteine rich proteins that suppress RNA silencing. Virology Journal 2:18.
Thomas C. L., V. Leh, C. Lederer and A. J. Maule (2003) Turnip crinkle virus coat protein mediates suppression of RNA silencing in Nicotiana benthamiana.Virology 306:33-41.
Torres-Barceló C., J. A. Darós and S. F. Elena (2010) HC-Pro hypo- and hypersuppressor mutants: differences in viral siRNA accumulation in vivo and siRNA binding activity in vitro. Archives of Virology 155:251-254.
Torres-Barceló C., S. Martín, J. A. Darós and S. F. Elena (2008) From hypo-to hypersuppression: effect of amino acid substitutions on the RNA-silencing suppressor activity of the tobacco etch potyvirus HC-Pro. Genetics 180:1039-1049.
Uhrig J. F., T. Canto, D. Marshall and S. A. MacFarlane (2004) Relocalization of nuclear ALY proteins to the cytoplasm by the Tomato bushy stunt virus P19 pathogenicity protein. Plant Physiology 135:2411-2423.
Untiveros M., S. Fuentes and L. F. Salazar (2007) Synergistic interaction of Sweet potato chlorotic stunt virus (Crinivirus) with carla-, cucumo-, ipomo-, and potyviruses infecting sweet potato. Plant Disease 91:669-676.
Untiveros M., A. Olspert, K. Artola, A. E. Firth, J. K. Kreuze and J. P. T. Valkonen (2016) A novel sweet potato potyvirus open reading frame (ORF) is expressed via polymerase slippage and suppresses RNA silencing. Molecular Plant Pathology 17:1111-1123 doi: 10.1111/mpp.12366
Valli A., G. Dujovny and J. A. García (2008) Protease activity, self-interaction, and small interfering RNA binding of the silencing suppressor P1b from Cucumber vein yellowing ipomovirus. Journal of Virology 82:974-986.
Valli A., A. M. Martín-Hernández, J. J. López-Moya and J. A. García (2006) RNA silencing suppression by a second copy of the P1 serine protease of Cucumber vein yellowing ipomovirus, a member of the family Potyviridae that lacks the cysteine protease HCPro. Journal of Virology 80:10055-10063.
Valli A., J. C. Oliveros, A. Molnár, D. Baulcombe and J. A. García (2011) The specific binding to 21-nt double-stranded RNAs is crucial for the anti-silencing activity of Cucumber vein yellowing virus P1b and perturbs endogenous small RNA populations. RNA 17:1148-1158.
van der Krol A. R., L. A. Mur, P. de Lange, A. G. M. Gerats, J. N. M. Mol and A. R. Stuitje (1990) Antisense chalcone synthase genes in petunia: visualization of variable of transgene expression. Molecular and General Genetics 220:204-212.
van der Vlugt R. A., R. K. Ruiter and R. Goldbach (1992) Evidence for sense RNA-mediated protection to PVYN in tobacco plants transformed with the viral coat protein cistron. Plant Molecular Biology 20:631-639.
Vance V. B. (1991) Replication of Potato virus X RNA is altered in coinfections with Potato virus Y. Virology 182:486-494.
Vance V. B., P. H. Berger, J. C. Carrington, A. G. Hunt and X. M. Shi (1995) 5´ proximal potyviral sequences mediate Potato virus X/potyviral synergistic disease in transgenic tobacco. Virology 206:583-590.
Várallyay E. and Z. Havelda (2013) Unrelated viral suppressors of RNA silencing mediate the control of ARGONAUTE1 level. Molecular Plant Pathology 14:567-575.
Várallyay E., E. Oláh and Z. Havelda (2014) Independent parallel functions of p19 plant viral suppressor of RNA silencing required for effective suppressor activity. Nucleic Acids Research 42:599-608.
Várallyay E., A. Válóczi, A. Ágyi, J. Burgyán and Z. Havelda (2010) Plant virus-mediated induction of miR168 is associated with repression of ARGONAUTE1 accumulation. The EMBO Journal 29:3507-3519.
Vargason J., G. Szittya, J. Burgyán and T. M. Tanaka-Hall (2003) Size selective recognition of siRNA by an RNA silencing suppressor. Cell 115:799-811.
Vaucheret H. (2006) Post-transcriptional small RNA pathways in plants: mechanisms and regulations. Genes & Development 20:759-771.
Vogler H., R. Akbergenov, P. V. Shivaprasad, V. Dang, M. Fasler, M. O. Kwon, S. Zhanybekova, T. Hohn and M. Heinlein (2007) Modification of small RNAs associated with suppression of RNA silencing by tobamovirus replicase protein. Journal of Virology 81:10379-10388.
Voinnet O. (2001) RNA silencing as a plant immune system against viruses. Trends in Genetics 17:449-459.
Voinnet O. (2005) Induction and suppression of RNA silencing: insights from viral infections. Nature Reviews Genetics 6:206-220.
Voinnet O. (2008) Use, tolerance and avoidance of amplified RNA silencing by plants. Trends in Plant Science 13:317-328.
Voinnet O., Y. M. Pinto and D. Baulcombe (1999) Suppression of gene silencing: a general strategy used by diverse DNA and RNA viruses of plants. Proceedings of the Nacional Academy of Sciences of the United States of America 96:14147-14152.
Wang H., K. J. Buckley, X. Yang, R. C. Buchmann and D. M. Bisaro (2005) Adenosine kinase inhibition and suppression of RNA silencing by geminivirus AL2 and L2 proteins. Journal of Virology 79:7410-7418.
Wang H., L. Hao, C. Y. Shung, G. Sunter and D. M. Bisaro (2003) Adenosine kinase is inactivated by geminivirus AL2 and L2 proteins. The Plant Cell 15:3020-3032.
Wang K. D., R. Empleo, T. T. Nguyen, P. Moffetta and M. A. Sacco (2015) Elicitation of hypersensitive responses in Nicotiana glutinosa by the suppressor of RNA silencing protein P0 from poleroviruses. Molecular Plant Pathology 16:435-448.
Wang L. Y., S. S. Lin, T. H. Hung, T. K. Li, N. C. Lin and T. L. Shen (2012a) Multiple domains of the Tobacco mosaic virus p126 protein can independently suppress local and systemic RNA silencing. Molecular Plant-Microbe Interactions 25:648-657.
Wang M. B., C. Masuta, N. A. Smith and H. Shimura (2012b) RNA silencing and plant viral diseases. Molecular Plant-Microbe Interactions 25:1275-1285.
Wang M. B. and M. Metzlaff (2005) RNA silencing and antiviral defense in plants. Current Opinion in Plant Biology 8:216-222.
Wang X. B., J. Jovel, P. Udomporn, Y. Wang, Q. Wu, W. X. Li, V. Gasciolli, H. Vaucheret and S. W. Ding (2011) The 21-nucleotide, but not 22-nucleotide, viral secondary small interfering RNAs direct potent antiviral defense by two cooperative argonautes in Arabidopsis thaliana. The Plant Cell 23:1625-1638.
Wang X. B., Q. Wu, T. Ito, F. Cillo, W. X. Li, X. Chen, J. L. Yu and S. W. Ding (2010) RNAi-mediated viral immunity requires amplification of virus-derived siRNAs in Arabidopsis thaliana. Proceedings of the Nacional Academy of Sciences of the United States of America 107:484-489.
Wang Y., K. C. Lee, V. Gaba, S. M. Wong, P. Palukaitis and A. Gal-On (2004) Breakage of resistance to Cucumber mosaic virus by co-infection with Zucchini yellow mosaic virus: enhancement of CMV accumulation independent of symptoms expression. Archives of Virology 149:379-396.
Weber H., S. Ohnesorge, M. V. Silber and A. J. P. Pfitzner (2004) The Tomato mosaic virus 30 kDa movement protein interacts differentially with the resistance genes Tm-2 and Tm-2². Archives of Virology 149:1499-1514.
Weinheimer I., K. Boonrod, M. Moser, M. Zwiebel, M. Füllgrabe, G. Krczal and M. Wassenegger (2010) Analysis of an autoproteolytic activity of Rice yellow mottle virus silencing suppressor P1. Biological Chemistry 391:271-281.
Weinheimer I., Y. Jiu , M. L. Rajamäki, O. Matilainen, J. Kallijärvi, W. J. Cuellar, R. Lu, M. Saarma, C. I. Holmberg, J. Jäntti and J. P. T. Valkonen (2015) Suppression of RNAi by dsRNA-degrading RNaseIII enzymes of viruses in animals and plants. PLoS Pathogens 11:e1004711.
Xia Z., Z. Zhu, J. Zhu and R. Zhou (2009) Recognition mechanism of siRNA by viral p19 suppressor of RNA silencing: a molecular dynamics study. Biophysical Journal Cell 96:1761-1769.
Xie Z., L. K. Johansen, A. M. Gustafson, K. D. Kasschau, A. D. Lellis, D. Zilberman, S. E. Jacobsen and J. C. Carrington (2004) Genetic and functional diversification of small RNA pathways in plants. PLoS Biology 2:0642-0652.
Xiong R., J. Wu, Y. Zhou and X. Zhou (2009) Characterization and subcellular localization of an RNA silencing suppressor encoded by rice stripe tenuivirus. Virology 387:29-40.
Yaegashi H., T. Takahashi, M. Isogai, T. Kobori, S. Ohki and N. Yoshikawa (2007) Apple chlorotic leaf spot virus 50 kDa movement protein acts as a suppressor of systemic silencing without interfering with local silencing in Nicotiana benthamiana. Journal of General Virology 88:316-324.
Yaegashi H., A. Tamura, M. Isogai and N. Yoshikawa (2008) Inhibition of long-distance movement of RNA silencing signals in Nicotiana benthamiana by Apple chlorotic leaf spot virus 50 kDa movement protein. Virology 382:199-206.
Yan F., Y. Lu, L. Lin, H. Zheng and J. Chen (2012) The ability of PVX p25 to form RL structures in plant cells is necessary for its function in movement, but not for its suppression of RNA silencing. PLoS ONE 7:e43242.
Yang J. Y., M. Iwasaki, C. Machida, Y. Machida, X. Zhou and N. H. Chua (2008) βC1, the pathogenicity factor of TYLCCNV, interacts with AS1 to alter leaf development and suppress selective jasmonic acid responses. Genes & Development 22:2564-2577.
Yang X., Y. Xie, P. Raja, S. Li, J. N. Wolf, Q. Shen, D. M. Bisaro and X. Zhou (2011) Suppression of methylation-mediated transcriptional gene silencing by βC1-SAHH protein interaction during geminivirus-betasatellite infection. PLoS Pathogens 7:e1002329.
Ye K., L. Malinina and D. J. Patel (2003) Recognition of small interfering RNA by a viral suppressor of RNA silencing. Nature 426:874-878.
Yelina N. E., E. I. Savenkov, A. G. Solovyev, S. Y. Morozov and J. P. Valkonen (2002) Long-distance movement, virulence, and RNA silencing suppression controlled by a single protein in hordei- and potyviruses: complementary functions between virus families. Journal of Virology 76:12981-12991.
Young B. A., D. C. Stenger, F. Qu, T. J. Morris, S. Tatineni and R. French (2012) Tritimovirus p1 functions as a suppressor of RNA silencing and enhancer of disease symptoms. Virus Research 163:672-677.
Yu B., E. J. Chapman, Z. Yang, J. C. Carrington and X. Chen (2006) Transgenically expressed viral RNA silencing suppressors interfere with microRNA methylation in Arabidopsis. FEBS Letters 580:3117-3120.
Zeng R., Q. Liao, J. Feng, D. Li and J. Chen (2007) Synergy between Cucumber mosaic virus and Zucchini yellow mosaic virus on Cucurbitaceae hosts tested byreal-time reverse transcription-polymerase chain reaction. Acta Biochimica et Biophysica Sinica 39:431-437.
Zhai Y., S. Bag, N. Mitter, M. Turina and H. R. Pappu (2014) Mutational analysis of two highly conserved motifs in the silencing suppressor encoded by Tomato spotted wilt virus (genus Tospovirus, family Bunyaviridae). Archives of Virology 159:1499-1504.
Zhang W., S. Gao, X. Zhou, J. Xia, P. Chellappan, X. Zhou, X. Zhang and H. Jin (2010) Multiple distinct small RNAs originated from the same microRNA precursors. Genome Biology 11:R81.
Zhang X., P. Du, L. Lu, Q. Xiao, W. Wang, X. Cao, B. Ren, C. Wei and Y. Li (2008) Contrasting effects on HCPro and 2b viral suppressors from Sugarcane mosaic virus and Tomato aspermy cucumovirus on the accumulation of siRNAs. Virology 374:351-360.
Zhang X., Y. R. Yuan, Y. Pei, S. S. Lin, T. Tuschl, D. J. Patel and N. H. Chua (2006) Cucumber mosaic virus-encoded 2b suppressor inhibits Arabidopsis Argonaute1 cleavage activity to counter plant defense. Genes & Development 20:3255-3268.
Zhang X., X. Zhang, J. Singh, D. Li and F. Qu (2012) Temperature-dependent survival of Turnip crinkle virus-infected Arabidopsis plants relies on an RNA silencing based defense that requires DCL2, AGO2 and HEN1. Journal of Virology 86:6847-6854.
Zhou Z. Sh., M. Dell’Orco, P. Saldarelli, C. Turturo, A. Minafra and G. P. Martelli (2006) Identification of an RNA silencing suppressor in the genome of Grapevine virus A. Journal of General Virology 87:2387-2395.
Zhu S., G. H. Lim, K. Yu, R. D. Jeong, A. Kachroo and P. Kachroo (2014) RNA silencing components mediate resistance signaling against Turnip crinkle virus. Plant Signal & Behaviour 9:e28435.
Zhu S., R. D. Jeong, G. H. Lim, K. Yu, C. Wang, A. C. Chandra-Shekara, D. Navarre, D. F. Klessig, A. Kachroo and P. Kachroo (2013) Double-stranded RNA-binding protein 4 is required for resistance signaling against viral and bacterial pathogens. Cell Reports 4:1168-1184.
Ziebell H., A. M. Murphy, S. C. Groen, T. Tungadi, J. H. Westwood, M. G. Lewsey, M. Moulin, A. Kleczkowski, A. G. Smith, M. Stevens, G. Powell and J. P. Carr (2011) Cucumber mosaic virus and its 2b RNA silencing suppressor modify plant-aphid interactions in tobacco. Scientific Reports 1:187.
Notas de autor
Autor para correspondencia (carmen.canizares@eelm.csic.es)