Artículos
Desarrollo de nanomaterial con carbón activado de vástago de banano
Nanomaterial development with activated carbon and banana stem
Desarrollo de nanomaterial con carbón activado de vástago de banano
Lámpsakos, núm. 22, pp. 37-47, 2019
Universidad Católica Luis Amigó
Recepción: 11 Febrero 2019
Aprobación: 28 Mayo 2019
Resumen:
En este trabajo se presenta el proceso de desarrollo de un material poroso a partir de carbón activado con ácido fosfórico, obtenido del vástago de banano criollo. La capacidad de adsorción es establecida mediante método estático, se evalúan 5 puntos en los cuales el carbón es sometido a diferentes porcentajes de humedad. Se hizo el análisis del área superficial (Sbet) del carbón obtenido y se establece su valor mediante el método B.E.T. El desarrollo de este nanomaterial amplía las posibilidades de investigación en campos como la refrigeración, en la que se usa como fuente de energía la radiación solar y en la electrónica se aprovecha la mayor área superficial de los carbones activados para construir súper condensadores, de manera que se coloca el carbón entre las placas paralelas, lo que hace que estos dispositivos presenten una capacitancia miles de veces mayor que la de los condensadores actuales de alta capacidad.
Palabras clave: Sorción, Carbón activado, Isotermas, Nanomateriales, Porosidad, Activación química, Área superficial, Impregnación, Precursor, Desorción.
Abstract:
His study presents the development process of a porous material from activated carbon with phosphoric acid obtained from local banana stem. The absorption capacity is set through the static method, 5 points in which carbon is submitted to different percentages of moisture are evaluated. The analysis of the surface area (Sbet) of the carbon obtained was made and its value is set through the B.E.T. method. The development of this nanomaterial wades enlarges the research possibilities in fields such as refrigeration, solar energy is used as a power supply. Electronics is the field in which the biggest surface area is used to make super condensers, in such way that the carbon is put between parallel plates. This way the devices show a capacitance level thousand times bigger than the one of the current high capacity condensers.
Keywords: Sorption, Activated carbon, Isotherms, Nanomaterials, Porosity, Chemical activation, Superficial area, Impregnation, Precursor, Desorption.
1. INTRODUCCIÓN
La utilización de materiales porosos es cada vez más frecuente dadas las múltiples posibilidades de aplicación que se extienden desde la purificación de gases y líquidos, hasta las más avanzadas en el ámbito tecnológico, como las aplicaciones en sistemas de refrigeración, tubos de calor y en supercapacitores para electricidad y electrónica.
Amplias zonas rurales de nuestro país y de los países latinoamericanos no disponen de energía eléctrica por las dificultades y costos asociados para el montaje de redes. La Unidad de Planeación Minero Energética (UPME) ha identificado en Colombia alrededor de 460,000 usuarios sin servicio de energía eléctrica, de los cuales alrededor de un 30% (aproximadamente 138,000) de ellos se encuentran en zonas no interconectadas [1]. En estos sitios, la refrigeración constituye una tecnología primordial para la preservación de productos agrícolas y alimenticios. Con este nuevo nano-material aplicado a sistemas de refrigeración que no requieran energía eléctrica para su funcionamiento se contribuiría a la competitividad de dichas zonas.
Se propone desarrollar un nuevo nanomaterial con las características adecuadas de adsorción y área superficial que permitan aplicaciones en refrigeración. Para alcanzar este objetivo, se usó como material básico adsorbente o precursor el vástago de banano criollo y como adsorbato, el vapor de agua. Se espera que la nueva pareja sólido-gas conformada por carbón activado-agua para ciclos de adsorción-desorción posibilite, a partir del modelo desarrollado, incrementar la capacidad de adsorción con respecto a la pareja carbón activado-metanol en un 10%, y se convierta en una alternativa tecnológica viable para el almacenamiento de energía térmica.
En este artículo se registra el proceso detallado para la obtención de carbón activado a partir del material poroso, así que se describe cada uno de los elementos y herramientas empleados; además, se expone el sistema a usar para la determinación experimental de la capacidad de adsorción y para la construcción de las isotermas. En la parte final se describen los resultados y se hace un análisis de cada uno, se expone un método de corrección para la isoterma obtenida y se calcula el COP para un sistema de refrigeración que use el carbón desarrollado. Por último, se presentan las conclusiones del trabajo realizado.
2. METODOLOGÍA
El carbón vegetal es el material de carbono más antiguo que se conoce y se obtiene a partir de la combustión incompleta de materias lignocelulósicas vegetales. Actualmente, los carbones activados se obtienen mediante un primer tratamiento térmico en atmósfera inerte de materiales con alto contenido en carbono, luego se someten a un proceso de gasificación parcial con vapor de agua, dióxido de carbono o a un tratamiento químico para modificar su porosidad. Las materias primas más utilizadas son de origen vegetal: madera, cáscaras y huesos, si bien se pueden utilizar coques de petróleo, carbones de bajo rango y turbas también [2].
El uso más habitual de estos materiales es como adsorbente para la purificación de productos en la industria farmacéutica, alimentaria, de agua potable y para producir diferencias de presión mediante ciclos de adsorción y desorción, por lo que sus propiedades más importantes son su porosidad y área superficial [2].
Para entender mejor el uso del carbón como adsorbente, es necesario explicar que la adsorción es el fenómeno físico por medio del cual las superficies sólidas atrapan moléculas de gas y permiten obtener información útil acerca del sólido adsorbente de la superficie específica, del volumen de poros o la distribución de tamaño de poro. Este fenómeno depende de diferentes variables experimentales como la temperatura, la presión y la naturaleza del adsorbente [3].
En este artículo, además de exponer el fenómeno de adsorción, también se hace la descripción de los elementos e insumos que intervienen en el desarrollo del material poroso, y se presenta el método usado para la obtención de las isotermas, el cual consta de 5 cajas plásticas herméticas, material transparente y unos 3000 cm3 de volumen dentro de los que se deben garantizar condiciones isotérmicas. Cada caja contiene una solución salina y muestras del carbón obtenido, es decir, que cada una actúa como un sistema independiente con una solución salina que garantiza humedad relativa diferente a la de las demás. Como resultado final se obtiene el carbón activado y se deja el sistema preparado para la construcción de las isotermas de adsorción.
Los ensayos que permitirán la obtención de las isotermas se realizarán con carbón activado químicamente mediante ácido fosfórico y como precursor, vástago de banano; se usará también un horno con atmósfera inerte que impida un proceso de combustión y evite la contaminación. Además, se empleará el vástago de banano criollo, dado que la literatura no reporta ningún desarrollo con este precursor y porque puede convertirse en una alternativa para resolver problemas medioambientales por la alta contaminación que representan sus desechos en las plazas de mercado.
El carbón activado es un material de carbón poroso, un carbonizado que se ha sometido a reacción con gases, a veces con la adición de productos químicos como el ZnCl2, durante (o después) el proceso de carbonización con el objeto de aumentar su porosidad [4].
Para la activación química se puede usar hidróxido de potasio (KOH) [5], ácido fosfórico (H3PO4), cloruro de zinc (ZnCl2) y carbonato de potasio (K2CO3). La activación con KOH requiere temperaturas por encima de 800°C, los otros 3 materiales requieren temperaturas alrededor de 500°C.
Materiales, reactivos y equipos
Reactivos. Se emplearon reactivos de grado analítico, es decir, con alta pureza. Se utilizó ácido fosfórico al 85% (H3PO4) y ácido clorhídrico (HCL).
Materiales. Como materia prima o precursor, se usó el vástago de banano criollo correspondiente a la variedad Gros Michel, con nombre científico: Musa Sapientum [6]. El nitrógeno (N2) se empleó como gas inerte para desplazar el oxígeno del horno y garantizar una atmósfera no reactiva.
Equipos. Se emplearon dos clases de hornos: horno de secado y horno vertical de carbonización y activación marca OVELMA, con resistencias eléctricas y alimentación de 110VAC, propiedad de la Universidad Pontificia Bolivariana de Medellín. El horno vertical es un cilindro de 25 cm de diámetro y 70 cm de largo, contiene un tubo central en acero dentro del cual se colocan pequeñas muestras del precursor a carbonizar, alcanza temperaturas hasta 1000°C. Ver Fig. 1. El horno de secado tiene convección forzada interna y temperatura máxima de 180°C, usado para extraer la humedad del precursor.

Fig. 1
Horno vertical para la carbonización. Propiedad de la Universidad Pontificia Bolivariana de Medellín
Con respecto al horno vertical de carbonización, el análisis de la Fig. 2 muestra el comportamiento de este cuando se programa para alcanzar 520°C.
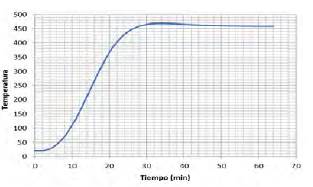
Fig. 2
Horno programado a 520°C. Llega hasta 470°C
Los primeros 4 minutos permanece a temperatura ambiente, después del minuto 8, la temperatura empieza a incrementarse de manera acelerada hasta el minuto 22. Entre el minuto 6 y el minuto 24 pasa de 40 a 430°C, a partir del minuto 24 la pendiente disminuye y alcanza finalmente una temperatura de 470°C. La curva muestra un comportamiento típico de este tipo de hornos en los que, durante la recta final, se llega a un estado de equilibrio de transferencia de calor entre el horno y el medio en el cual se encuentra. El horno llegó a la máxima temperatura 50°C por debajo de la temperatura máxima programada, esto puede presentarse debido al desgaste natural en un horno que tiene varios años de uso. Esta curva fue la utilizada para hacer el carbón activado con H3PO4. De acuerdo con [7], si la activación se hace con ácido fosfórico, la temperatura máxima es alrededor de 500°C.
Otros elementos y equipos. Balanza analítica marca Quirumed serie 5034. Capacidad: 120 g, sensibilidad: 0.0001 g, diámetro de plato: 90 mm, función de tara y calibración interna con urna de cristal. Un gotero, tres porta muestras, guantes plásticos y máscara, recipiente hermético para guardar el carbón activado, cilindro de N2 con 99.9% de pureza, rotámetro para gas N082-03 marca Aalborg. Flujo hasta 844 ml/min. Presión 14,7 Psia, longitud 10 pulg. Flotador de vidrio y tirillas para medir el PH.
Procedimiento para obtener el carbón activado con H3PO4
Esta es la prueba realizada para la obtención del carbón activado usando como precursor el vástago de banano criollo y como agente para la activación química, el H3PO4.
Paso a paso:
-
Lavar la muestra de vástago de banano con abundante agua para eliminar la suciedad que pudiera tener.
-
Cortar la muestra en trozos cúbicos con 3 mm de lado y luego secar a 80°C durante 22 horas.
-
Pesar 10g de la muestra seca.
-
Usar guantes y mascara de protección.
-
Medir 3,5 g de H3PO4 por cada gramo de muestra. Por lo tanto, se requieren 35 g de H3PO4.
-
A la cantidad de muestra, adicionarle gota a gota la solución acuosa de H3PO4 agitando de manera constante para lograr impregnación total del precursor.
-
Programar el horno de secado a 110°C (283K).
-
Llevar la muestra impregnada al horno de secado y dejarla allí por 4 horas. (La muestra impregnada tiene un peso total de 45g).
-
Sacar las muestras del horno y llevarlas al horno vertical.
-
Conectar cilindro de 5.6 m3 de N2 al medidor de flujo y este al horno vertical.
-
Programar un flujo de N2 de 100ml/min (100cm3/min) y esperar unos minutos para evacuar el aire del horno.
-
Programar el horno vertical para alcanzar una temperatura máxima de 450°C.
-
Mantener la temperatura máxima durante una hora.
-
Apagar el horno manteniendo el flujo de N2 hasta llegar a temperatura ambiente. (Después de secar los 45 g y someterlos al horno vertical, quedaron 21g de carbón activado sin lavar).
-
Retirar el carbón y lavarlo con agua caliente destilada hasta alcanzar un PH de 6 en el agua residual. (El PH de 6 se logra verificando continuamente el color que toman las tirillas hasta alcanzar el amarillo claro, como lo indican las instrucciones).
-
Secar el carbón a 110°C durante 12 horas.
Análisis detallado del procedimiento
Se sometieron 534 g de vástago de banano criollo al proceso de secado y se obtuvieron 36 g de muestra seca. Por lo tanto, la humedad del vástago es 93.3%. Para obtener 10 g de precursor seco se necesitan entonces 148,3 g de vástago.
La impregnación se hace con una relación 3.5:1, es decir, 3.5 g de ácido fosfórico por cada gramo de precursor seco. Se usan 10 g de precursor, por lo tanto, se requieren 35 g de ácido fosfórico. De los 10 g de precursor impregnados con 35 g de H3PO4, después del secado se obtienen 21 g de muestra impregnada seca. La muestra impregnada seca se lleva a la fase de pirolisis en el horno vertical y luego se lava. Después de 4 horas de lavado, se obtuvieron 3 g de carbón activado. Esto significa un rendimiento del 30% ya que la cantidad inicial de precursor seco fue de 10 g.
Obtención de las curvas isotermas. Para las isotermas se usaron 5 g de carbón activado dispuestos en un sistema estático. De los 5 g de carbón, 2,5 g se impregnaron nuevamente con cloruro de potasio (KCl) con el fin de aumentar la adsorción. El cloruro se preparó a 20% (200 g de KCl por 1l de solución). La impregnación se hizo con 1,25 ml de solución acuosa por 2,5 g de carbón activado (a razón aproximada en peso de 1/2). Los otros 2,5 g no se impregnaron. Esto se hace para determinar qué pasa en ambos casos. Algunos pasos del procedimiento anterior se hicieron con base en [8].
Sistema estático para la obtención de las isotermas de equilibrio. Una vez obtenido el carbón, es necesario realizar las pruebas respectivas para determinar la capacidad de adsorción y el área superficial. En la determinación de la capacidad de adsorción se usará agua en un sistema estático, como se explica en este numeral.
Funcionamiento del sistema estático. La actividad de agua en el carbón es equivalente a la humedad relativa del aire en equilibrio con el propio carbón [9]. Para obtener los datos de equilibrio, se utilizó el método estático con la ayuda de soluciones saturadas y se usaron 5 tipos de sales cuyas humedades relativas son reales y se muestran en la Tabla 1 [10].
| Sal usada en solución acuosa | % Humedad (Aw. actividad del agua) |
|---|---|
| Cloruro de Litio | 11,23 |
| Cloruro de calcio | 29,50 |
| Nitrato de sodio | 63 |
| Cloruro de sodio | 75,30 |
| Cloruro de potasio | 84,30 |
En las pruebas experimentales se utilizaron 5 cajas de plástico herméticas (una para cada solución salina) dispuestas en el interior de un sistema isotérmico que garantiza una temperatura constante de 22°C (ver Fig. 3). En cada una de las cajas de la Fig. 4 se dispusieron las muestras de carbón en dos recipientes como lo muestra la Fig. 5. El recipiente 1 contiene el carbón tal y como se obtuvo y el recipiente 2 contiene el carbón impregnado de cloruro de potasio.

Fig. 3
Sistema estático e isotérmico que contiene las cajas con las sales

Fig. 4
Cajas herméticas que contienen las sales y las muestras de carbón. Se usaron 5 de estas

Fig. 5
Tapa de una caja hermética con los recipientes para el carbón. Se usaron 2 de los 4 recipientes mostrados
Una vez dispuestas las muestras en los recipientes dentro de las cajas, se procede a pesar el carbón y el sistema que lo soporta usando una balanza analítica con una precisión de ± 0.001g. Los datos obtenidos se muestran en la Tabla 2.
| HUMEDAD | PESO DEL SISTEMA SIN CARBÓN (g) | PESO DEL CARBÓN SECO (g) | PESO DEL SISTEMA CON CARBÓN (medido) (g) | PESO DEL SISTEMA CON CARBÓN (calculado con la suma para verificar error) (g) | ||||||
|---|---|---|---|---|---|---|---|---|---|---|
| CAMARA HERMETICA | % HUMEDAD | RECIPIENTE 1 | RECIPIENTE 2 | RECIPIENTE 1 | RECIPIENTE 2 | RECIPIENTE 1 | RECIPIENTE 2 | RECIPIENTE 1 | RECIPIENTE 2 | |
| 1 | 11,23 | 3,342 | 3,292 | 0,312 | 0,315 | 3,654 | 3,608 | 3,654 | 3,607 | |
| 2 | 29,50 | 3,173 | 3,248 | 0,312 | 0,304 | 3,486 | 3,553 | 3,485 | 3,552 | |
| 3 | 63,00 | 3,203 | 3 256 | 0,308 | 0 308 | 3,512 | 3 566 | 3,511 | 3 564 | |
| 4 | 75,30 | 3,365 | 3,331 | 0,314 | 0,317 | 3,68 | 3,651 | 3,679 | 3,648 | |
| 5 | 84, 30 | 3,393 | 3,307 | 0,315 | 0,311 | 3,713 | 3,62 | 3,708 | 3,618 | |
La curva de adsorción se construye con los datos de la cantidad de agua adsorbida por cada muestra que se dispuso en las cámaras herméticas. Para esto se deja que el sistema llegue a un equilibrio, logrado después de varios días.
3. DESARROLLO
Con el fin de verificar el estado de equilibrio (adsorción máxima de agua de cada muestra) se hicieron las mediciones del sistema a los 7, 8 y 9 días con los resultados que se muestran en la Tabla 3.
| PESO DEL SISTEMA CON CARBÓN (medido 7 dias despues) (g) | PESO DEL SISTEMA CON CARBÓN (medido 8 dias despues) (g) | PESO DEL SISTEMA CON CARBÓN (medido 9 dias despues) (g) | |||
|---|---|---|---|---|---|
| RECIPIENTE 1 | RECIPIENTE 2 | RECIPIENTE 1 | RECIPIENTE 2 | RECIPIENTE 1 | RECIPIENTE 2 |
| 3,643 | 3,595 | 3,644 | 3,595 | 3,645 | 3,595 |
| 3,487 | 3,553 | 3,488 | 3,554 | 3,488 | 3,554 |
| 3,579 | 3,631 | 3,58 | 3,632 | 3,58 | 3,633 |
| 3,776 | 3,766 | 3,777 | 3,766 | 3,777 | 3,766 |
| 3,87 | 3,806 | 3,87 | 3,807 | 3,87 | 3,808 |
Con los datos de la Tabla 3, se puede evidenciar que durante los 3 días en los que se hicieron las mediciones, algunos valores no cambiaron y otros solo variaron en una milésima de gramo entre un día y otro. Lo anterior permite concluir que el sistema está en equilibrio y las muestras llegaron a su máxima adsorción en el día 9. Sin embargo, al comparar las medidas del sistema inicial con las obtenidas a los 9 días para el sistema en equilibrio, como lo muestra la Tabla 4, se encontró que para la cámara 1 con humedad del 11.23%, las muestras no habían adsorbido agua y, por el contrario, se había presentado desorción con salida de agua desde el carbón hacia el medio, se desorbieron 9 mg en el recipiente 1 (pasó de 3,654 g a 3,645 g) y 13 mg en el recipiente 2 (pasó de 3,608 g a 3,595 g). Era un resultado inesperado ya que se había asumido que las muestras dispuestas al inicio estaban totalmente secas. Los resultados de la segunda cámara muestran una variación muy pequeña: la muestra del recipiente 1 adsorbe 2 mg de H2O (pasó de 3,486 g a 3,488 g) y la muestra del recipiente 2 adsorbe 1 mg de H2O (pasó de 3,553 g a 3,554 g). Las otras 3 cámaras tuvieron una adsorción considerable. Ver datos en la Tabla 4.
| HUMEDAD | PESO DEL SISTEMA CON CARBÓN (medido) (g) | PESO DEL SISTEMA CON CARBÓN (medido 9 dias despues) (g) | DIFERENCIA DE PESOS (g) | ||||
|---|---|---|---|---|---|---|---|
| CAMARA HERMETIC A | % HUMEDAD | RECIPIENTE 1 | RECIPIENTE 2 | RECIPIENTE l | RECIPIENTE 2 | RECIPIENTE 1 | RECIPIENTE 2 |
| 1 | 11,23 | 3,6S4 | 3,608 | 3,645 | 3,595 | -0,009 | -0,013 |
| 2 | 29,50 | 3,486 | 3,553 | 3,488 | 3,554 | 0,002 | 0,001 |
| 3 | 63,00 | 3,512 | 3,566 | 3,58 | 3,633 | 0,068 | 0,067 |
| 4 | 75,30 | 3,68 | 3,651 | 3,777 | 3,766 | 0,097 | 0,115 |
| S | 84,30 | 3,713 | 3,62 | 3,87 | 3,808 | 0,157 | 0,188 |
La desorción que se presenta en la primera caja hermética indica que el carbón que se introdujo en los recipientes no estaba totalmente seco. La humedad ganada por el carbón antes de las pruebas pudo deberse a que se dejó de un día para otro en un frasco, cuyo volumen es muy superior a su contenido de carbón y adsorbió la humedad del espacio no ocupado. También se adquiere algo de humedad al manipular el carbón cuando se extrae del horno de secado.
La situación anterior se corrige con el siguiente procedimiento: se pesan las muestras de carbón húmedo que se extrae de las cajas, las muestras se secan durante 4 horas a 120°C; una vez secas, se pueden obtener los datos reales de adsorción para cada muestra.
En la Tabla 5 se describen los valores de las muestras húmedas retiradas de las cajas y de las muestras secas recién retiradas del horno. Con los datos obtenidos se calcula la cantidad real adsorbida. Las muestras de los recipientes marcados con el número 2, impregnadas con Cloruro de Potasio, mejoraron ligeramente la adsorción, como se puede evidenciar en la Tabla 5, para obtener mejores resultados se deberían aumentar la cantidad de agente impregnante, ya que la relación usada fue de 1/0.5, lo que significa que por cada gramo de carbón se usó medio gramo de agente. Las isotermas se construyen con los porcentajes adsorbidos (Nads) que se obtienen con la relación matemática ((muestra húmeda-muestra seca) / muestra seca) vs los porcentajes de humedad (Aw). Se construyeron 3 isotermas, una para cada recipiente y una para el promedio de las dos.
| DATOS CORREGIDOS | |||||||
|---|---|---|---|---|---|---|---|
| PESO DE CARBÓN CON AGUA (g) | PESO DEL CARBÓN SECO (g) | N ads (g-H2O/g-carbón) | |||||
| RECIPIENTE 1 | RECIPIENTE 2 | RECIPIENTE 1 | RECIPIENTE 2 | RECIPIENTE 1 | RECIPIENTE 2 | PROMEDIO | |
| 0,308 | 0,307 | 0,2885 | 0,2955 | 0,067590988 | 0,03891709 | 0,053254039 | |
| 0,308 | 0,305 | 0,2896 | 0,2875 | 0,063535912 | 0,060869565 | 0,062202738 | |
| 0,374 | 0,374 | 0,2987 | 0,2942 | 0,2520924 | 0,271244052 | 0,261668226 | |
| 0,407 | 0,433 | 0,3029 | 0,3095 | 0,343677781 | 0,399030695 | 0,371354238 | |
| 0,472 | 0,492 | 0,3104 | 0,3029 | 0,520618557 | 0,624298448 | 0,572458503 | |
Las isotermas se obtienen con los datos de la Tabla 5 y se observan en las Fig. 6, 7 y 8 donde Aw es la actividad del agua o porcentaje de humedad y el eje vertical muestra la cantidad agua adsorbida en gramos de H2O por cada gramo de carbón (Nads).
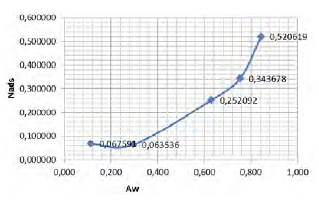
Fig. 6
Isoterma para los datos del recipiente 1
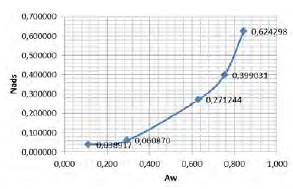
Fig. 7
Isoterma para los datos del recipiente 2
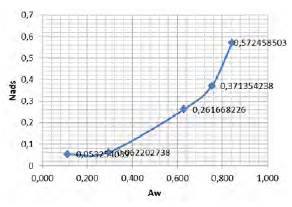
Fig. 8
Isoterma para los datos promedio del recipiente 1 y del recipiente 2
La Fig. 6 muestra una tendencia inicial de la curva hacia abajo debido a que el segundo valor de la cantidad de agua adsorbida (Nads) en la columna de recipiente 1, de la Tabla 5, es menor que el primer valor de la misma columna; este resultado no es normal ya que, a mayor porcentaje de humedad, mayor debe ser la cantidad adsorbida. El error pudo presentarse debido a que probablemente la segunda muestra no se secó lo suficiente o, al tratarse de cantidades tan pequeñas, se pudo cometer algún error en las medidas. Para valores de Aw por encima de 0,3, la curva tiende a aplanarse debido al espacio tan grande que hay entre el segundo y el tercer valor.
La Fig. 7 muestra una tendencia inicial de la curva a aplanarse debido a que el segundo valor de Nads en la columna de recipiente 2, de la Tabla 5, es ligeramente superior al primer valor de la misma columna; este resultado es normal porque a mayor porcentaje de humedad, mayor debe ser la cantidad adsorbida y así ocurre. Al igual que en la Fig. 6, después de un Aw de 0,3, la curva tiende a aplanarse.
La Fig. 8 corresponde a los datos promedio de la Tabla 5. Se puede observar, al igual que en la Fig. 7, una tendencia inicial de la curva a aplanarse debido a que el segundo valor de Nads en la columna promedio de la Tabla 5, es ligeramente superior al primer valor de la misma columna; este es un resultado esperado ya que a un mayor porcentaje de humedad, se presenta una mayor cantidad adsorbida y, de manera similar a los casos anteriores, la curva tiende a aplanarse después de un valor Aw de 0,3.
Como puede observarse en las Fig. 6 a 8, las curvas tienen una ligera tendencia hacia abajo o a aplanarse en la parte inicial y luego presentan un aplanamiento largo en la mitad del tramo, para después terminar las tres con unos valores elevados de adsorción en los puntos donde la actividad del agua está por encima de 0,7.
Área superficial
Para la determinación del área superficial se usó un equipo volumétrico Quanta Chrome Autosorb de propiedad de la Universidad Pontificia Bolivariana con las siguientes características básicas: determina área BET/mesoporosidad (P/Po> 1 x 10-3), trabaja con bajas presiones para Kriptón, determina microporosidad (P/Po < 1 x 10-4), habilidad para Quimisorción, reactor de1100°C.
Se hizo el análisis del área superficial (Sbet) del carbón obtenido y se establece que su valor es de 809,70 m2/g. El método B.E.T., desarrollado por Brunauer, Emmett y Teller [11], permite determinar la superficie de un sólido basándose en la adsorción de un gas inerte, generalmente N2, a baja temperatura. La idea central del método de BET es que al conocer la cantidad de gas adsorbido necesario para formar una monocapa y el área que ocupa una de estas moléculas adsorbidas, es posible estimar el área del sólido. El equipo usado también permitió establecer el tamaño de los poros y se obtuvo un ancho de 4,1703 Å, equivalente a 0.41703η,m lo que permite clasificar al material como microporoso.
4. CONCLUSIONES
Un buen carbón o ciertas zeolitas logran valores de adsorción del orden de 0,7 g de agua por gramo de carbón. Aquí se logra un valor de adsorción 0,57 g de agua por cada gramo de carbón para una actividad del agua del 84,3%. Se mencionó que en [12], lograron una capacidad de adsorción de 0,44 y 0,31 kg de H2O/ kg de adsorbente, lo que ratifica que el resultado obtenido es bueno a pesar de las limitaciones con las que se trabajaron.
El carbón obtenido tiene un tamaño irregular, pues se encuentran partículas de 2mm de diámetro y otras con características de polvo. El desempeño puede mejorar si se logra un carbón totalmente en polvo, ya que se aprovecha mucho mejor la superficie para la formación de poros en su interior. Queda como valor agregado de esta investigación lograr un carbón en polvo, para lo cual es necesario hacer un corte más fino al precursor antes de someterlo al proceso de impregnación y corregir irregularidades en el proceso de lavado.
Una segunda etapa de impregnación mejora la adsorción, como se pudo comprobar usando una cantidad modesta de cloruro de potasio para las muestras del recipiente 2 (fue solo de 0,5 g de cloruro por cada gramo de carbón). Se espera que aumentando la cantidad de agente impregnante, aumente la capacidad de adsorción.
El área superficial obtenida es muy superior a la de otros experimentos realizados con diferentes precursores. Algunos de esos experimentos entregaron las siguientes áreas: con Lignito 630 m2/g [7], con palosanto 520 m2/g, con Bambú 486 m2/g [14].
AGRADECIMIENTOS
Los autores desean expresar su agradecimiento al señor Farid Cortés de la Universidad Nacional de Colombia, sede Medellín, por su valioso aporte en el desarrollo de este trabajo y al personal de laboratorio de la Universidad Pontificia Bolivariana por permitir la realización de las pruebas, la obtención del carbón activado y por el uso de los equipos con los cuales se determinó el área superficial.
REFERENCIAS
[1] Ministerio de Minas y Energía. Decreto numero 1623, agosto 2015.
[2] C. Asimbay, N. Rosas, D. Endara, y V. H. Guerrero, "Obtención del Carbón Activado a partir de Residuos Linocelulósicos de Canelo, Laurel y Eucalipto", Revista Politécnica, vol. 36, no. 3, pp. 1-6, 2015. Disponible en: https://revistapolitecnica.epn.edu.ec/ojs2/index.php/revista_politecnica2/article/view/537
[3] R. Moliner, "Del carbón activado al grafeno: Evolución de los materiales de carbono". Bol. Grupo Español Carbón, número 41, 2016. Disponible en: www.gecarbon.com/boletines/articulos/Boletin-GEC_041_art1.pdf
[4] M. A. Álvarez Merino, F. Carrasco Marín, y F. J. Maldonado Hódar, Desarrollo y aplicaciones de materiales avanzados de carbón, Sevilla: Universidad Internacional de Andalucía, 2014.
[5] A. Sabrina, L. Galicia, E. Plaza, R. Atensio, A. Rodríguez, y E. González, "Carbón activado preparado a partir de carbón mineral bituminoso activado con hidróxido de potasio", Revista Técnica de la Facultad de Ingeniería, vol. 39, no. 2, pp. 63-71, 2016. Disponible en: https://produccioncientificaluz.org/index.php/tecnica/article/view/21324/21155
[6] L. Pari, and J. Umamaheswari, "Antihyperglycaemic activity of Musa sapientum flowers: effect on lipid peroxidation in alloxan diabetic rats", Phytotherapy Research, vol. 14, no. 2, 2000. Available: https://www.ncbi.nlm.nih.gov/pubmed/10685115
[7] M. A. Lillo-Ródenas, J. P. Marco-Lozar, D. Cazorla-Amorós, and A. Linares-Solano, "Activated carbons prepared by pirolysis of mixtures of carbon precursor/alkaline hidroxide", Journal of Analytical and Applied Pyrolysis, vol. 80, no. 1, pp. 166-174, 2007. doi: 10.1016/j.jaap.2007.01.014
[8] F. Suarez-García, A. Martínez-Alonso, J. M. D. Tascón, "Porous texture of activated carbons prepared by phosphoric acid activation of apple pulp", Carbon, vol. 39, no. 7, pp. 1111-1115, 2001. doi: 10.1016/S0008-6223(01)00053-7
[9] S. Lahsasni, M. Kouhila and M. Mahrouz, "Adsorption- Desorption Isotherms and Heat of Sorption of Prickly Pear Fruit (Opuntia ficus indica)", Energy Conversion and Management, vol. 45, no. 2, pp. 249-261, 2004. doi: 10.1016/S0196-8904(03)00133-X
[10] L. D. Fiorentin, B. T. Menon, S. T. D. de Barros, N. C. Pereira, O. C. da Lima, and A. N. Modenes, "Sorption isotherm of agricultural residue of orange bagasse", Revista Brasileira de Engenharia Agrícola e Ambiental, vol.14, no.6, pp. 653-659, 2010. Available: http://www.scielo.br/pdf/rbeaa/v14n6/a12v14n6.pdf
[11] M. A. Hernández, J. A. Velasco, F. Rojas, V. H. Lara, M. A. Salgado y V. Tamariz, "Evaluación de mesoporos y caracterización de arcillas del estado de puebla, México", Revista Internacional de Contaminación Ambiental, vol. 19, no. 4, pp. 183-190, 2003. Disponible en: https://www.revistascca.unam.mx/rica/index.php/rica/article/view/23591/22254
[12] C. Hai-jun, C. Quin, Y. Xiao-li, C. Xiu-jun, and Y. Hu-qing, "Attapulgite based composite adsorbent for cooling and air conditioning applications-I preparation and performance", in: The Fourth Pacific Basin Conference on Sorption Science and Technology, PRC, Tianjin, 2006.
[13] Q-S. Liu, T. Zheng, P. Wang, and L. Guo. "Preparation and characterization of activated carbon from bamboo by microwave-induced phosphoric acid activation". Industrial Crops and Products, vol. 31, no. 2, pp. 233-238, 2010. doi: 10.1016/j.ind-crop.2009.10.011.
Notas
Notas