Artigos Originais
Atividade antioxidante, teor de taninos, fenóis, ácido ascórbico e açúcares em Cereus fernambucensis
Antioxidant activity and content of tannins, phenols, ascorbic acid and sugar in Cereus fernambucensis
Atividade antioxidante, teor de taninos, fenóis, ácido ascórbico e açúcares em Cereus fernambucensis
Vértices (Campos dos Goitacazes), vol. 17, núm. 1, pp. 183-201, 2015
Instituto Federal de Educação, Ciência e Tecnologia Fluminense

Esta obra está bajo una Licencia Creative Commons Atribución 4.0 Internacional.
Recepción: 23 Julio 2013
Aprobación: 24 Noviembre 2014
Resumo: Cereus fernambucensis, conhecida popularmente como manacaru, é conhecida pelo sabor adocicado do seu fruto. Pesquisas clínicas mostram que os antioxidantes fenólicos de frutas, cereais e vegetais são os principais fatores que auxiliam para a redução da incidência de doenças, contribuindo para a saúde. Dessa forma, avaliaram-se os teores de taninos, fenóis totais, ácido ascórbico e açúcares no manacaru, levando-se em consideração a atividade antioxidante.
Palavras-chave: Cereus fernambucensis, Antioxidante, Fenóis, Taninos, Açúcares.
Abstract: Cereus fernambucensis, popularly known as manacaru, is known by the sweet taste of the fruit. Clinical research shows that phenolic antioxidants from fruits, grains and vegetables are the main factors that contribute to reducing the incidence of diseases, and contributing to health. Thus, we assessed the levels of tannins, total phenols, ascorbic acid and sugars in manacaru, taking into account the antioxidant activity.
Keywords: Cereus fernambucensis, Antioxidant, Phenols, Tannins, Sugars.
1 Introdução
A espécie Cereus fernambucensis, conhecida popularmente como manacaru (Figura 1), é largamente encontrada em restinga, floresta atlântica distribuída geograficamente em quase todo o território nacional (RN, PB, PE, AL, SE, BA, MG, ES e RJ). No Rio de Janeiro, essa espécie está localizada de acordo com a divisão dos seguintes blocos: Norte Fluminense, Região dos Lagos, Região Metropolitana e Sul Fluminense, e mais especificamente nas praias do complexo lagunar Grussaí-Iquipari em Campos dos Goytacazes – RJ. O manacaru é conhecido popularmente pelo sabor adocicado do seu fruto (ALMEIDA et al., 2011; CALVENTE et al. FREITAS; ANDREATA, 2005).

Figura 1
Fruto e flor de manacaru
Essa espécie pertence ao gênero Cereus (família Cactaceae) e está adaptada às condições de intenso xerofitismo, que é o estado dos vegetais que desenvolvem uma estrutura especial para se adaptar a condições extremas e caracterizam a paisagem vegetal das regiões mais secas da América Intertropical. As espécies dessa família são plantas suculentas com talos carnosos, roliços ou aplanados. Algumas variedades sem espinhos são usadas como forragem, e os frutos de algumas espécies constituem um agradável alimento (SILVA et al., 2009; GOLA, 1965).
Algumas espécies da família Cactaceae (Opuntia ficus indica Cactus pear, Opuntia monacantha Haw, O. albi-carpa, O. streptacantha) são utilizadas como alimentos, embora a produção seja ainda emergente no país, concentrando-se em São Paulo, na região de Valinhos e, de forma incipiente, nos estados de Pernambuco e Paraíba. Do total produzido em São Paulo, apenas uma pequena parte é destinada ao mercado interno, enquanto a maior parcela é exportada para a Europa e Estados Unidos, onde existe o hábito de consumo desses frutos, considerados exóticos (BAÑUELOS et al. 2012; YAHIA et al., 2011). A valorização dos frutos no mercado internacional abre perspectivas para as variedades locais, ainda não reconhecidas como frutícolas, tampouco apreciadas pela população urbana, em face do desconhecimento de suas potencialidades (ALVES et al., 2008).
Nesse sentido, estudos sobre a composição química e a digestibilidade do manacaru foram realizados por Araújo (2004). No entanto, poucos são os estudos encontrados na literatura sobre os frutos dessa planta, que apesar de serem encontrados em grandes quantidades de fevereiro a setembro, não são explorados comercialmente, ocorrendo seu desperdício, ou então sendo utilizados, quando muito, na elaboração de doces e geleias. Apesar de se encontrar em área de restinga, a possibilidade de produção de mudas abre uma alternativa para a recuperação das populações naturais de muitas dessas espécies, como o manacaru.
O Cereus fernambucensis é utilizado na medicina popular contra o vitiligo, que é uma doença autoimune caracterizada por zonas de despigmentação da pele, e também é usado na eliminação de cálculos renais. No entanto, pesquisas realizadas demonstram que essa espécie possui grande potencial antioxidante, além da inibição de óxido nítrico (NO) por macrófagos indicando também potencial anti-inflamatório (OLIVEIRA et al., 2009).
Como a oxidação é um evento metabólico que leva à geração da energia necessária para as atividades essenciais das células, o metabolismo do oxigênio nas células também leva à produção de radicais livres, os quais podem gerar graves danos (REIS et al., 2011). O estresse oxidativo tem sido relacionado ao desenvolvimento de várias doenças crônicas e degenerativas como, por exemplo, o câncer, as doenças cardíacas e as doenças degenerativas, assim como está envolvido no processo inflamatório e de envelhecimento (LOIZZO et al., 2012).
As pesquisas clínicas mostram que os antioxidantes fenólicos de frutas, cereais e vegetais são os principais fatores que contribuem para a redução da incidência de doenças crônicas e degenerativas encontradas em populações cujas dietas são altas na ingestão desses alimentos (LOIZZO et al., 2012). Assim, a ênfase em estudos por antioxidantes naturais tem crescido muito nos últimos anos (REIS, 2013).
Os antioxidantes são substâncias capazes de inibir ou retardar o processo de oxidação no meio em que estão inseridos. Os radicais livres podem ser neutralizados pelos antioxidantes naturais ou compartilhados indiretamente nos sistemas enzimáticos. Entre os antioxidantes mais comuns estão o ácido ascórbico, os compostos fenólicos, os taninos, o ácido úrico, os carotenoides, as betalaínas e os pigmentos (HASSANBAGLOU et al., 2012; REIS et al., 2013).
O ácido ascórbico (vitamina C) possui grande importância fisiológica, pois atua como antioxidante na reciclagem de tocoferóis, na produção e manutenção de colágeno e na redução do ferro-férrico no trato intestinal. Essas características fazem com que a vitamina C seja recomendada como suplementação alimentar. Além disso, é bastante utilizada na estabilização da cor e sabor de uma ampla variedade de frutas processadas na forma de sucos, polpas e outras bebidas (HASSANBAGLOU et al., 2012).
Os compostos fenólicos, por sua vez, compõem uma ampla classe de substâncias de origem natural cuja síntese não ocorre na espécie humana, e apresentam características anti-inflamatórias, anticarcinogênicas, antitrombóticas, antivirais, antimicrobianas, vasodilatadoras, imunomodulatórias e analgésicas (DEGÁSPARI et al., 2004). Existem cerca de cinco mil fenóis; entre eles destacam-se os ácidos fenólicos, fenóis simples, flavonoides, taninos, ligninas e tocoferóis, os quais possuem atividade antioxidante comprovada (REIS et al., 2011).
Os taninos são classificados em dois grupos principais, cujas estruturas são muito diferentes entre si, embora todos tenham em suas moléculas grupos poli-hidroxifenóis. Os pertencentes ao primeiro grupo são denominados taninos hidrolisáveis, que incluem os galotaninos e os elagitaninos, polímeros derivados dos ácidos gálico e elágico, como exemplificado na Figura 2 (DEGÁSPARI et al., 2004).
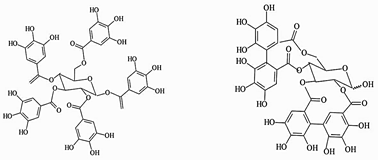
Figura 2
Estruturas de Taninos Hidrolisáveis Galotanino e Elagitanino
Os constituintes do segundo grupo são denominados de taninos condensados e são encontrados em maiores proporções e com maior importância nos alimentos. Exibem uma estrutura similar aos flavonoides, com coloração variando do vermelho ao marrom, conforme exemplificado na Figura 3. Em baixas concentrações em frutos, os taninos conferem-lhes características sensoriais desejáveis. Todavia em concentrações mais elevadas, conferem aos frutos e outros alimentos características adstringentes (DEGÁSPARI et al., 2004).
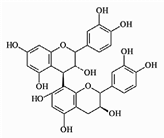
Figura 3
Estrutura de tanino condensado
Já os açúcares ou carboidratos são de grande abundância na natureza e atuam principalmente como fonte e reserva energética para o metabolismo, sendo necessários na alimentação. A classificação dos carboidratos reflete o fato de que todos se originam a partir da glicose, produzindo unidades mais simples e mais complexas. Os carboidratos simples mais encontrados nos alimentos são glicose, frutose, sacarose, lactose e, entre os complexos, o amido (CHITARRA, 2000). O termo “carboidrato” surgiu da crença de que os átomos de carbono estavam de alguma forma combinados com a água (hidratos de carbono) de acordo com a fórmula empírica dos açúcares mais simples: Cn(H20)n, apesar de essa definição não ser adequada para os oligo e polissacarídeos. Eles podem ser chamados, de uma maneira geral, de glicídios, amido ou açúcar (GHAZARIAN et al., 2011).
Esses compostos são formados por várias moléculas de monossacarídeos ligadas por meio de ligações hemiacetálicas ou ligações glicosídicas. Assim, as moléculas de monossacarídeos podem formar várias outras macromoléculas como os di-, tri, oligo- ou polissacarídeos. Os monossacarídeos são o tipo de carboidrato mais simples, sendo que os exemplos mais comuns são a glicose, a frutose e a galactose. Os dissacarídeos são compostos formados por duas moléculas de monossacarídeos como a maltose (glicose-glicose), a sacarose (glicose-frutose) e a lactose (glicose-galactose). Os oligossacarídeos são os compostos que resultam de 2 a 10 monossacarídeos. Já os polissacarídeos possuem mais de 10 monossacarídeos em sua estrutura, como por exemplo o amido e o glicogênio, que estão presentes respectivamente nas plantas e animais com a função de armazenamento de energia, além da celulose e da pectina, que são componentes da parede celular das plantas que lhes confere resistência (CHITARRA, 2000; GHAZARIAN et al., 2011).
Dessa forma, o presente trabalho objetiva avaliar a atividade antioxidante, os teores de taninos, fenóis totais, vitamina C e açúcares presentes em Cereus fernambucensis.
2 Materiais e métodos
2.1 Coleta do Material Vegetal
O material vegetal foi coletado no complexo lagunar Grussaí-Iquipari em Campos dos Goytacazes – RJ (entre as coordenadas 21°42’S e 21°48’S de latitude e 41°02’E e 41°03’W de longitude) nos períodos de frutificação, os quais correspondem aos meses de dezembro a fevereiro, em 2011. A exsicata foi depositada no Herbário da Universidade Estadual do Norte Fluminense Darcy Ribeiro (UENF).
2.2 Preparo do Extrato Aquoso e Frações
Para o preparo do extrato aquoso, os frutos de C. fernambucensis foram limpos, lavados com água destilada e tiveram suas partes (casca, semente e polpa) separadas. A casca foi separada da polpa e submetida à extração com água, originando o extrato (EMA), que foi preparado na proporção de 75% (m/v), em liquidificador comercial, sendo depois centrifugado e liofilizado. Uma parte do extrato foi submetida a uma precipitação com etanol (1:1) originando um sobrenadante (SM) e um precipitado (PM). Em seguida realizou-se uma extração líquido-líquido a partir do sobrenadante (SM), oriundo do extrato da casca dos frutos com solventes em ordem crescente de polaridade, originando as seguintes frações: hexano (FH), acetato de etila (FAcEt), butanol (FB) e resíduo (OLIVEIRA et al., 2009).
2.3 Preparo do Extrato Metanólico
Os frutos foram limpos e separaram-se as cascas das sementes. As cascas foram submetidas à extração exaustiva, por maceração estática com metanol. Esse extrato foi evaporado a 35 ºC em banho-maria ao abrigo da luz (OLIVEIRA, 2005).
2.4 Análise Antioxidante pelo Método do DPPH
O extrato aquoso (EMA) e as frações obtidas a partir do mesmo, a saber: sobrenadante, fração hexânica, fração acetato de etila e fração butanólica (SM, FH, FAcEt, FB) foram submetidas à avaliação quanto à atividade antioxidante pelo método fotocolorimétrico do radical livre estável 2,2-difenil-1-picril-hidrazil (DPPH – 0,1mM). Tal método consiste na adição de 1 mL do extrato em concentrações que variam de 0,1 - 1000 μg/mL, em 1 mL de uma solução metanólica de DPPH (0,1 mM), sendo a reação processada em 1h à temperatura ambiente. Imediatamente a absorção do DPPH foi verificada em 515 nm em um espectrofotômetro UV-Vis. A atividade sequestrante de radicais livres de cada amostra foi expressa pela relação da absorção de DPPH, baseada na solução de DPPH ausente do extrato (controle negativo) e uma solução de um padrão de substância aromática (controle positivo), o 2,6-di-(tert-butil)-4-metilfenol (BHT). Após, o percentual sequestrador (PS%) de radicais livres foi calculado (KOLEVA et al., 2002). A capacidade de sequestrar radicais livres foi expressa como percentual de inibição da oxidação do radical e foi calculada mediante a seguinte fórmula (YEN; DUH, 1994):
Onde ADPPH é a absorbância da solução de DPPH e AExtr é a absorbância da amostra em solução.
2.5 Determinação do Teor de Taninos Condensados
Na determinação de taninos condensados, o extrato aquoso e o extrato metanólico da casca do fruto de C. fernambucensis (500 mg) foram macerados com 4 porções de 5 ml de solução de acetona/água (7:3). As porções foram unidas em balão volumétrico e o volume completado para 25 mL. Prosseguindo, em 1 mL de amostra, adicionou-se uma solução de butanol (BuOH) em ácido clorídrico 5% (HCl) e aqueceu-se em banho-maria a 95 ºC por 2 horas. As amostras positivas desenvolveram coloração vermelha ou violeta e a absorbância das amostras foi feita a 540 nm após 5 a 10 minutos (MOREIRA, 2000), sendo os resultados expressos em percentagem. Utilizou-se na determinação uma curva padrão estabelecida com o tanino do quebracho, isolado a partir do extrato do quebracho, em diferentes concentrações (2 a 100 μg/mL) (QUEIROZ et al., 2002).
2.6 Determinação de Fenóis Totais
Para a determinação do teor de fenóis totais, extrato aquoso e o extrato metanólico da casca dos frutos de C. fernambucensis (500 mg) foram macerados com 4 porções de 5 ml de solução de acetona/ água (7:3). As porções foram unidas em balão volumétrico e o volume completado para 25 ml. Empregou-se o método de FolinDenis, o qual envolve a redução do reagente pelos compostos fenólicos das amostras com concomitante formação de um complexo azul (MOREIRA, 2000; SWAIN; HILLLS, 1959). Adicionou-se 0,5 mL do reagente de Folin-Denis em 0,5 mL da amostra e 3 mL de água destilada. Após 1 hora, 1 mL da solução de carbonato de cálcio (Na2CO3) saturada foi adicionada. A leitura foi realizada em espectrofotômetro a 760nm e os resultados foram expressos em mg/mL. A quantidade total de fenóis de cada extrato foi quantificada por meio de uma curva padrão preparada com ácido tânico.
2.7 Dosagem do Teor de vitamina C
Os teores de ácido L-ascórbico foram determinados por meio de titulação com 2,6 dicloroindofenol, substituindo o ácido metafosfórico por ácido oxálico 1%, conforme Cunniff (1998). Esse método baseia-se na redução do 2,6-dicloroindofenol (2,6D), de cor roxa, pelo ácido L-ascórbico em meio ácido, tornando-se incolor. O ponto final de titulação é verificado quando todo o ácido ascórbico presente foi oxidado e a solução 2,6D, não reduzida, confere coloração rosada à solução. O mesmo procedimento foi repetido para o ensaio em branco, substituindo a solução padrão de vitamina C por água destilada. O valor médio das titulações com solução padrão, subtraído do branco, foi o título da solução 2,6D. O resultado foi expresso em mg/100g de amostra para a fruta in natura e mg/100mL para os sucos (NOGUEIRA et al., 2002).
2.8 Dosagem do Teor de açúcar
A análise do teor de açúcar foi feita com 1g de casca e polpa fresca que passaram pelo processo de maceração em 10mL de água ultra pura, sendo centrifugada por 10 minutos, filtrada e injetada em cromatógrafo Shimadzu Class, modelo LC-l0, líquido com índice de refração usando coluna Phenomenex Rezex RCM (300 X 7,8 mm) mantida à temperatura de 60 ºC; volume de injeção de 20 μl; detector de índice de refração RI YL9170; fase móvel H.O e fluxo de 0,6 ml/min. Para a quantificação dos açúcares presentes foi realizada uma curva padrão em diferentes concentrações (área do pico X massa em mg) utilizando-se uma amostra pura de glicose e frutose.
2.9 Análise Estatística
Os experimentos foram feitos em triplicata (n = 3), sendo os resultados apresentados à média de três experimentos distintos.
2.10 Equipamentos e Reagentes
O espectrofotômetro de UV-VIS da marca Shimadzu Mini 1240 foi o equipamento usado para as análises de absorção. O Cromatógrafo Líquido de Alta Eficiência – CLAE, da marca Shimadzu Class, modelo LC-l0, com duas bombas LC10AT, acoplado ao detector por varredura de espectro na região do ultravioleta por arranjo de fotodiodos SPD-M10A e injetor Rheodyne 7725i com volume de injeção de 20 mL foi usado nos experimentos de separação cromatográfica.
Nas análises realizadas no CLAE foram utilizados reagentes de grau cromatográfico e, nas demais análises, reagentes P. A.
3 Resultados e discussão
3.1 Atividade Antioxidante
A capacidade de sequestrar radicais livres em relação ao radical estável 2,2-difenil1-picril hidrazil (DPPH) foi inicialmente escolhida por se tratar de uma metodologia simples, rápida e sensível (FROZZA et al., 2013). As substâncias antioxidantes presentes nos extratos reagem com o DPPH, que é um radical estável, e conv erte-o em 2,2-difenil1-picril hidrazina. O grau de descoloração indica o potencial antioxidante do extrato. As amostras foram avaliadas em concentrações de 1000 a 10 μg/ml, como mostra a Figura 4. Vale ressaltar que os testes foram realizados em triplicata e em três concentrações distintas, sendo apresentadas aqui as médias aritméticas e o desvio padrão. O padrão utilizado foi o BHT (Butil-hidroxi-tolueno), um antioxidante comercial de estrutura fenólica que é amplamente empregado na indústria alimentícia (HEIM, 2002).
Foi observada atividade antioxidante para EMA, SM e FB, nas três concentrações testadas (1000, 100 e 10 μg/mL), sendo que, na maior concentração (1000 μg/mL), essas três amostras apresentam atividade superior a 80%. O extrato aquoso (EMA) mostrou um potencial de sequestro de radicais livres superior a 80% em comparação com o padrão BHT na concentração mais alta.
Observando o resultado do sobrenadante (SM), pode-se observar que este exibiu resultados inferiores ao padrão BHT nas três concentrações avaliadas. Entretanto, na concentração mais alta, ultrapassou os 90% de sequestro de radicais livres e, na concentração de 10 μg/mL, exibiu uma atividade antioxidante superior às demais amostras analisadas nessa concentração.
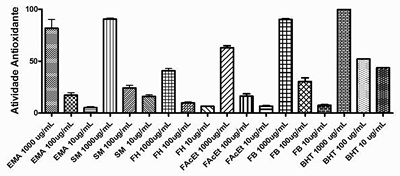
Figura 4
Atividade antioxidante das amostras, dos padrões fenólicos e do BHT (Média ± Desvio Padrão) (n=3)
Já a fração hexânica (FH) apresentou resultados pouco satisfatórios em relação ao padrão BHT e às outras amostras analisadas em todas as concentrações, visto que os resultados foram abaixo de 40% de atividade antioxidante, mesmo na maior concentração.
A fração acetato de etila (FAcEt), por sua vez, apresentou resultado inferior ao padrão e às demais amostras na concentração de 1000 μg/mL, exceto para a fração hexânica. Contudo, ainda observaram-se valores superiores a 60% de sequestro de radicais livres na maior concentração. Já na concentração de 100 μg/ml também obteve um percentual de sequestro inferior às demais amostras, porém significativo.
Quando a fração butanólica (FB) é comparada com o padrão BHT observa-se que essa fração possui 90% de percentual de sequestro de radicais livres na concentração de 1000 μg/mL. Já a concentração de 100 μg/mL, apresentou um percentual de atividade antioxidante superior às outras amostras avaliadas. A concentração de 10 μg/ mL não obteve resultados expressivos em comparação com o BHT, mas obteve resultado mediano em comparação com a maioria das amostras analisadas.
Quando comparada a fração butanólica (FB) com as demais amostras, observa-se que essa fração apresenta atividade antioxidante mais elevada nas três concentrações, podendo ser colocada em uma escala de sequestro de radicais livres: BM> SM> EM> FAE> HM.
Mediante tais resultados é possível constatar o potencial antioxidante exibido pelas amostras e também sua comparação com a atividade sequestrante de radicais livres com o padrão BHT. Segundo Ross e Kasum (2002), a capacidade antioxidante dos compostos fenólicos é determinada pela sua estrutura, especialmente com a facilidade com que um átomo de hidrogênio a partir de uma hidroxila do anel aromático pode ser doado a um radical livre.
Oliveira et al. (2009) corroboram esses resultados utilizando a mesma espécie em suas análises, o C. fernambucensis, sendo que foram avaliados o extrato aquoso, a fração e as subfrações das cascas dos frutos quanto ao perfil sequestrador de radicais livres frente ao radical livre estável DPPH, verificando-se para o extrato 90% de percentual de atividade antioxidante na concentração de 1000 μg/mL (%), para a fração hexânica 63 %, para a fração acetato de etila 80% e para a fração butanólica 80%.
Osorio-Esquivel et al. (2011) verificou no extrato metanólico do fruto da espécie Opuntia joconostle, pertencente ao gênero Opuntia, também inserido na família Cactaceae, cerca de 62% de sequestro de radicais pelo método de DPPH, a partir do endocarpo do fruto, sendo que para o pericarpo verificou-se cerca de 59% e para o mesocarpo, em torno de 42% de sequestro de radicais livres. Em comparação com os resultados neste trabalho que é a partir das cascas (pericarpo) de Opuntia jocnostle, notase que o sequestro de radicais livre pelo método de DPPH manteve entre 40 e 90% de ação antioxidante. Esses dados são muito semelhantes aos encontrados para o manacaru.
Hassanbaglou et al. (2012) analisaram quatro tipos de extratos preparados a partir das folhas da espécie vegetal Pereskia bleo (pertencente à família Cactaceae): extrato metanólico 27%; extrato hexânica 24%; extrato etanólico 54% e extrato em acetato de etila 16%. Entre esses, o extrato etanólico foi aquele que apresentou os melhores resultados, possivelmente porque é nesse extrato que encontra-se o maior número de moléculas polares.
Partindo do princípio de que a atividade antioxidante relaciona-se principalmente aos flavonoides, bem como aos ácidos fenólicos e aos taninos (ROESLER et al., 2007), avaliou-se também o teor desses últimos.
3.2 Determinação do Teor de Taninos
Os taninos são substâncias provenientes do metabolismo secundário de fontes vegetais e estão presentes na maioria das plantas. Todavia sua concentração nos tecidos vegetais pode variar, dependendo da idade, do tamanho da planta, da parte coletada, da época ou, ainda, do local de coleta (MONTEIRO et al., 2005).
A presença de taninos na composição química vegetal muitas vezes está relacionada à ação biológica descrita para uma espécie, sendo que a distribuição maciça de taninos está restrita a alguns táxons, o que faz com que a planta apresente uma grande produção de representantes dessa classe química em detrimento de outros metabólitos (LUNA, 2006).
A Tabela 1 mostra os teores de taninos condensados nas amostras analisadas.

Tabela 1
Dados obtidos da análise do teor de taninos condensados do extrato aquoso e metanólico das cascas do fruto de manacaru
De acordo com esses resultados pode-se observar que os teores de taninos condensados concentram-se no extrato aquoso, não sendo detectados teores de taninos hidrolisáveis.
A adstringência característica de frutos com alto teor de taninos é provocada pela propriedade que os taninos possuem de precipitar proteínas e, assim, quando em contato com as proteínas da saliva, formam um complexo insolúvel que popularmente se caracteriza pela sensação adstringente.
Diferentemente do obtido nesse estudo, Negesse, Makkar e Becker (2009), utilizando somente palmas (folhas) da Cactaceae da espécie Opuntia ficus-indica, observaram um teor de taninos totais de 21g/kg de tecido seco e, para taninos condensados, não obteve resultados significativos.
Sendo assim, os resultados obtidos nesse trabalho exibem um valor considerável no teor de taninos presentes no extrato aquoso do fruto de manacaru, Cereus fernambucensis, para membros de Cactaceae.
3.3 Determinação do Teor de Fenóis
O método de Folin-Denis permite quantificar flavonoides, antocianinas e compostos fenólicos presentes nas amostras (MOREIRA, 2000; OLIVEIRA, et al., 1994). A Tabela 2 demonstra a quantidade total de fenóis dos extratos aquoso e metanólico das cascas dos frutos de manacaru.

Tabela 2
Dados obtidos do teor de fenóis totais das cascas do fruto de manacaru
Os teores de fenóis totais foram detectados tanto no extrato aquoso quanto no extrato metanólico das cascas dos frutos de manacaru, sendo que se pode notar que há uma concentração maior dos teores de fenóis totais no extrato metanólico.
Há escassos dados na literatura a respeito da detecção de fenóis nessa espécie. Os que existem empregam a metodologia de Folin Ciocalteau e abrangem outras espécies pertencentes à mesma família. É necessário lembrar que existem diferentes formas de se expressar o teor de fenóis, conforme as diversas metodologias.
Segundo Santos-Zea, Errez-Uribe e Serna-Saldivar (2011), foi detectado para o extrato metanólico da espécie Opuntia ficus-indica a concentração de fenóis totais de 34,2g/mg de equivalentes de ácido gálico, por grama de amostra seca. Já Corral-Aguayo et al. (2008) relatou uma maior quantidade de fenóis totais para variedades do gênero Opuntia. Lee et al. (2011) relataram 41,40g/mg de equivalentes de ácido gálico, por grama de amostra seca, para a espécie Opuntia fícus-indica. Para a mesma espécie foi verificado 30,8g/mg de equivalentes de ácido gálico, por grama de amostra seca de fenóis totais, sendo que foi utilizada para esse estudo a metodologia de Folin Ciocalteu.
Herrera-Hernández et al. (2011), utilizando o método de Follin Ciocalteau para avaliação quanto ao teor de fenóis totais, observou em frutos verdes e maduros resultados diferentes para cada tipo de fruto. Para os frutos maduros foram verificados cerca de 45g/ mg de equivalentes de ácido gálico, por grama de amostra seca. Ehlenfeldt e Prior, (2001) obtiveram resultados de 7,3 g/mg de equivalentes de ácido gálico, por grama de amostra seca.
Os resultados apresentados por Necchi et al. (2012) indicam que o extrato de Nopalea cochenillifera (Cacataceae) apresenta um conteúdo de 29,62%, utilizando a metodologia de Folin Ciocalteu.
Yahia e Mondragon-Jacobo (2011) encontraram para várias espécies de Cactaceae teores diversos de fenóis totais: Oputia megacantha e Oputia robusta exibiram o maior teor de fenólicos totais, cerca de 130mg de ácido gálico/g, e o menor conteúdo fenólico foi encontrado em O. ficus-indica com apenas 10mg de ácido gálico/g.
Estudos apontam que a correlação entre a capacidade antioxidante e o teor de taninos e fenóis totais pode estar sujeita ao método selecionado e também às características hidrofóbicas ou hidrofílicas do sistema teste e dos antioxidantes avaliados (ROESLER et al., 2007). O método de Folin-Denis foi usado nesse estudo por ser um método amplamente aceito, bem como por tratar-se de uma metodologia rápida, simples, reprodutível e que independe da polaridade das amostras, dispensando seu tratamento prévio (REIS et al., 2013).
3.4 Determinação do Teor de Açúcares
Os açúcares são os principais sólidos solúveis presentes nas frutas. Entretanto outras substâncias solúveis também têm participação no teor de sólidos solúveis, como por exemplo os minerais solúveis, ácidos e álcoois. Nas frutas, os açúcares (frutose, glicose e sacarose) são os carboidratos predominantes. Alguns estudos demonstram haver aumento dos teores de açúcares durante o crescimento da fruta, enquanto em outros, não foi detectada alteração na concentração de açúcares durante o desenvolvimento da fruta (CHITARRA, 2000).
Para análise de açúcares redutores presentes na polpa e na casca do fruto de Cereus fernambucensis (manacaru), foram injetados dois padrões, a glicose e a frutose, com a finalidade de se quantificar esses açúcares nas frutas da espécie vegetal. Na Figura 5 encontram-se os cromatogramas da análise do teor de açúcares da polpa e da casca dos frutos de C. fernambucensis, nos quais é possível verificar os picos correspondentes tanto da glicose como da frutose.
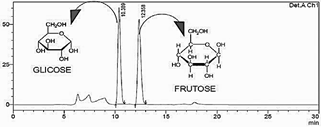
Figura 5
Cromatograma da polpa de manacaru para avaliação de açúcares
Também na Tabela 3 é possível ver a concentração dos açúcares. Dessa forma, a partir da curva padrão dos açúcares, foi possível quantificar esses dois açúcares presentes tanto na casca quanto na polpa do manacaru.

Tabela 3
Valores de glicose e frutose obtidos a partir da casca e da polpa do manacaru
De acordo com os resultados obtidos, pode-se observar que há uma maior concentração de ambos os açúcares (glicose e frutose) na polpa do fruto. Comparandose esses resultados com a literatura, observam-se valores inferiores para a casca e para a polpa (SAWAYA et al., 1983; PIMENTA, 1990). Oliveira et al. (2011) avaliaram os açúcares presentes no fruto do manacaru e verificaram a concentração de 7,3%. Em concordância, outros estudos revelam números que variam de 10,0 a 17,0% (MANICA, 2002; SEPULVEDA; SAENZ, 1990; SAWAYA et al., 1983; PIMENTA, 1990).
Silva et al. (2009) encontram os valores médios de açúcares a partir da polpa e da casca de frutos de manacaru. Comparando-se os resultados obtidos para a polpa e para a casca, constatou-se uma diferença percentual, a qual foi significativa, de modo que para a polpa se observa 5,76% e para a casca 1,53%. Tais dados mostram que os percentuais apresentados nesse trabalho são significativamente superiores tanto na casca quanto na polpa.
Os resultados obtidos por Oliveira et al. (2004) mediante a análise dos frutos do manacaru mostram um menor teor de açúcares redutores na polpa e maior na casca, cerca de 9,54 (% glicose). Esses dados corroboram os obtidos neste trabalho a partir de Cerus fernambucensis (manacaru).
3.5 Avaliação do Teor de Vitamina C
O efeito protetor de frutas e vegetais é geralmente atribuído a seus constituintes antioxidantes, que incluem a vitamina C (Figura 6), vitamina E (a-tocoferol), os carotenoides, glutationa, flavonoides e ácidos fenólicos, assim como outros compostos (YAHIA, 2010; SIES; STAHL, 1995).
A vitamina C é também responsável pelo sabor de determinadas variedades de frutas de alguns cactos. Os cactos, mais especificamente os frutos, são uma fonte de nutrientes e vitaminas (YAHIA, 2010).
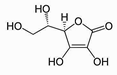
Figura 6
Estrutura química do ácido ascórbico vitamina C
Em espécie do gênero Opuntia, o conteúdo de vitaminas C altera de acordo com a variedade, o tipo de tecido e o estágio de maturação (MOUSSA-AYOUB et al., 2011).
A ingestão diária recomendada de vitamina C para adultos é de 60 mg/dia (PADH, 1994) e, por conseguinte, uma porção de 100 g da baga do cacto puro de manacaru pode contribuir com cerca de 51,9% a 95% da ingestão diária recomendada de vitamina C (GEBHARDT et al., 2008)
Como se pode observar na Tabela 4, foi possível obter para as cascas dos frutos de Cereus fernambucensis a concentração de 178mg/100g de amostra, já para a polpa dos frutos se verificam 22,94mg/100g de vitamina C.

Tabela 4
Teor de vitamina C (mg/100g) na casca e polpa de manacaru
De acordo com Joseph (2004), os cactos da espécie Opuntia lindheimeri, Opuntia stricta var. strictaem, espécies de Cactaceae, em relação ao conteúdo total de ácido ascórbico, variaram 10-111mg de peso/g das cascas dos frutos.
José et al. (2010) verificam que o teor de ácido ascórbico variou 14,5 a 23,3mg/100g para a polpa dos frutos de Cactaceae: a espécie Opuntia undulata apresentou 14,5mg/100g, a espécie Opuntia ficus-indica cerca de 18,5mg/100g e a espécie Opuntia stricta apresentou 23,3mg/100g de vitamina C. Tais resultados, quando comparados com os dados obtidos a partir da polpa dos frutos de Cereus fernambucensis, são inferiores, verificando-se que apenas a espécie Opuntia stricta corroborou os resultados aqui apresentados.
Herrera-Hernández et al. (2011), ao estudar outro membro da família Cactaceae, a espécie Myrtillocactus geometrizans, observaram valores bem altos de vitamina C (310380mg/kg, FW) para os frutos maduros.
Corral-Aguayo et al. (2008) verificou resultados semelhantes em seus experimentos quando comparados com base de peso fresco, nos quais se pode notar que o teor de vitamina C de cacto (311,4-582,4mg/kg) é maior do que na maioria das frutas comuns, tais como ameixa (95mg/kg), uva (108mg/kg), maçã (46mg/kg), pêssego (10mg/kg), banana (87mg/kg), amora (209mg/kg), e mirtilo (97mg/kg).
Yahia e Mondragon-Jacobo (2011) verificaram, em diferentes espécies de Cactaceae, o teor de vitamina C, sendo que o maior teor foi observado em Opuntia robusta, seguido por Opuntia streptacantha com 4000 e 2100mg/100g respectivamente. Um menor teor de ácido ascórbico foi observado em Opuntia ficus-indica e Opuntia Megacantha, com níveis variando entre 1200 e 1400mg/100g respectivamente.
Além disso, Oliveira et al. (1992), estudando os frutos de manacaru, obtiveram outros dados nutricionais, tais como: resultado de pH médio de 4,3; acidez total titulável de 0,13%; ºBrix de 11,8%; cerca de 8% de açúcares redutores; 0,26% de cinzas; e 91,17% de umidade. Aliado aos resultados do presente trabalho, pode-se inferir que os frutos, incluindo as cascas, apresentam características apropriadas ao processamento industrial na obtenção de doces e geleias, pois vários compostos nobres estão nessa parte da planta.
4 Conclusão
Este estudo relata a quantificação de taninos, fenóis totais, ácido ascórbico e açúcares, presentes nos frutos de manacaru, enfatizando a atividade antioxidante pelo método do DPPH, o qual é amplamente aceito e geralmente empregado na indústria alimentícia. Com base nos resultados obtidos, conclui-se que as amostras possuem boa capacidade de sequestrar radicais livres, ou seja, boa atividade antioxidante. Verificou-se que os teores de taninos condensados concentram-se no extrato aquoso, e foram detectados fenóis totais tanto no extrato aquoso quanto no extrato metanólico das cascas dos frutos de manacaru, podendo-se notar uma concentração dos teores de fenóis totais no extrato metanólico. Foi possível observar também que o teor de vitamina C do fruto de manacaru encontra-se mais concentrado na casca do que na polpa. Tal resultado é significativo, pois é um teor mais elevado em comparação ao encontrado em outras frutas comumente utilizadas no cotidiano como uva, ameixa, maça, pêssego e banana. Em relação aos teores de açúcares observou-se que estes se concentraram significativamente na polpa. Cabe ressaltar que, apesar da parte comestível se restringir à polpa, iniciativas de aproveitamento da casca devem ser iniciadas para estimular o seu consumo, a fim de que não se perca o valor nutricional encontrado nessa parte do fruto. Dessa forma, os resultados encontrados contribuem grandemente para o conhecimento a respeito dessa espécie, visto ser ela ainda muito pouco estudada. Um estudo químico e nutricional mais aprofundado certamente propiciará um estímulo à sua comercialização. Ressalta-se que a comercialização dessa espécie endêmica de restingas na região pode levar a um impacto ambiental por trânsito de pessoas e modificação na paisagem das restingas. Por esse motivo é imprescindível pensar realmente na exploração sustentável e no plantio comercial.
Agradecimentos
FAPERJ, UENF, CAPES e CNPq.
Referências
ALVES M. A. et al. Fruto de Palma [Opuntia Fícus-Indica (L) Miller, Cactaceae]: Morfologia, composicão química, fisiologia: índices de colheita e fisiologia póscolheita. Rev. Iber. Tecnología Postcosecha, v. 9, n. 1, p. 16-25, 2008.
ARAÚJO, L. F. Enriquecimento proteico do mandacaru sem espinhos (cereus jamacaru P.DC.) e da palma forrageira (opuntia fícus-indica mill) em meio semi-sólido por processo biotecnológico. 2004. 175 f. Tese. (Doutorado em Ciências Sociais)–Universidade Federal de Campina Grande, UFCG, Campina Grande, 2004.
BAÑUELOS, Gary S.; STUSHNOFF, Cecil; WALSE, Spencer S., ZUBER, Tatiana, YANG, Soo In; PICKERING, Ingrid J.; FREEMAN, John L. Biofortified, selenium enriched, fruit and cladode from three opuntia cactus pear cultivars grown on agricultural drainage sediment for use in nutraceutical foods, Food Chemistry, v. 135, p. 9-16, 2012.
BERNARDES, N. R.; PESSANHA, F. F.; OLIVEIRA, D. B. Alimentos funcionais: uma breve revisão. Ciência e Cultura – Revista Científica Multidisciplinar do Centro Universitário da FEB, v. 6, n. 2, p. 11-19, nov. 2010.
CALVENTE, A. M.; FREITAS, M. F.; ANDREATA, R. H. P. Listagem, distribuição geográfica e conservação das espécies de cactaceae no estado do Rio de Janeiro, Rodriguésia, v. 56, n. 87, p. 141-162, 2005.
CHITARRA, M. Processamento mínimo de frutos e hortaliças. Lavras: UFLA/FAEPE, 119 p, 2000.
CORRAL-AGUAYO, R. D. et al. Correlation between some nutritional components and the total antioxidant capacity measusured with six different assays in eight horticultural crops. Journal of Agricultural and Food Chemistry, v. 56, p. 10498-10504, 2008.
CUNNIFF, P. Official methods of analysis of AOAC International. Maryland: AOAC International, 1998. cap. 9. p. 33. 2 v.
DEGÁSPARI, C. H.; WASZCZYNSKYJ, N.; PRADO, M. R. M. Atividade antimicrobiana de Schinus terebinthfolius Raddi. Ciência Agroténica. v. 29, p. 617-622, 2005.
DEGÁSPARI, C.; WASZCZYNSKYJ, N. Propriedades antioxidantes de compostos fenólicos. Visão Acadêmica, Curitiba, v. 5, n. 2, p. 33-40, 2004.
EHLENFELDT, M. K.; PRIOR, R. L. Oxygen radical absorbance capacity (ORAC) and phenolic and anthocyanin concentrations in fruit and leaf tissues of highbush blueberry. Journal of Agricultural and Food Chemistry, v. 49, n.5, p. 2222–2227, 2001.
GEBHARDT, S. E. et al. USDA National Nutrient Database for Standard Reference, Release 21, 2008.
GOLA, G.; NEGRI, J; CAPALLETTI, C. Tratado de Botânica. 2. ed. Barcelona: Labor. 1965. 160 p.
HASSANBAGLOU, B. et al. Antioxidant activity of different extracts from leaves of Pereskia bleo (Cactaceae). Journal of Medicinal Plants Research, v. 6, n. 15, p. 29322937, 23 abr. 2012.
HEIM, K. E. Flavonoid antioxidants: chemistry, metabolism and structure-activity relationships. Journal Nutrition Biochemistry. v. 13, p. 572-584, 2002.
HERRERA-HERNÁNDEZ, M. G. Effects of maturity stage and storage on cactus berry (Myrtillocactus geometrizans) phenolics, vitamin C, betalains and their antioxidant properties. Food Chemistry, v.129, p.1744–1750, 2011.
JOSÉ, A. et al. Determination of antioxidant constituents in cactus pear fruits. Plant Foods Hum Nutr., v. 65, p. 253–259, 2010.
KOLEVA, I. I. et al. Screening of plant extracts for antioxidant activity: a comparative study on three testing methods. Phytochemical Analysis, v.13, p. 8-17, 2002.
LEE, J. C. et al. Antioxidant property of an ethanol extract of the stem of Opuntia ficus-indica var. Saboten. J. Agric. Food Chem., v. 50, p. 6490–6496, 2011.
LOIZZO, M. R. et al. Radical scavenging, antioxidant and metal chelating activities of Annona cherimola Mill. (cherimoya) peel and pulp in relation to their total phenolic and total flavonoid contents. Journal of Food Composition and Analysis, v. 25, p. 179-184, 2012.
LUNA, J. S. Estudo de plantas bioativas. 254 f., 2006. Tese. Recife, PE, Universidade Federal de Pernambuco. CCEN, 2006.
MANICA, I. Frutas nativas, silvestres e exóticas: técnicas de produção e mercado: feijão, figo da índia, fruta pão, jaca, lichia, mangaba. Porto Alegre: Cinco Continentes. 2002. 541 p.
MONTEIRO, J. M. et al. Taninos: uma abordagem da química à ecologia. Química Nova, v. 28, p. 892-896, 2005.
MOREIRA, D. L. Métodos de análise e dosagem de taninos condensados, taninos gálicos e fenóis totais. Rio de Janeiro, Apostila NPPN-UFRJ, 2000.
MOUSSA-AYOUB T. E. et al. Identification and quantification of flavonol aglycons in cactus pear (Opuntia ficus indica) fruit using a commercial pectinase and cellulase preparation. Food Chemistry, v. 124. p. 1177–1184, 2011.
NECCHI R. M. M. et al. In vitro antimicrobial activity, total polyphenols and flavonoids contents of Nopalea cochenillifera (L.) Salm-Dyck (Cactaceae). Research in Pharmacy, v. 2, n. 3, p. 01-07, 2012.
NEGESSE, T.; MAKKAR, H. P. S.; BECKER, K. Nutritive value of some nonconventional feed resources of Ethiopia determined by chemical analyses and an in vitro gas method. Animal Feed Science and Technology, v. 154, p. 204-217, 2009.
NOGUEIRA, R. J. M. C. et al. Efeito do estádio de maturação dos frutos nas características físico-químicas de acerola. Pesq. agropec. bras., Brasília, v. 37, n. 4, p. 463-470, 2002.
OLIVEIRA, M. R. T. et al. Caracterização física e físico-química dos frutos de palma (Opuntia monocantha How) e mandacaru (Cereus peruvianus, Mill). Agropecuária técnica, v. 13, 1992.
OLIVEIRA, E. A.; JUNQUEIRA, S. F.; MASCARENHAS, R. J. Caracterização físico-química e nutricional do fruto da palma (Opuntia Fícus Indica L. Mill) cultivada no Sertão do Submédio São Francisco. Holos, v. 3, n. 27, 2011.
OLIVEIRA, A. B.; MIGUEL, O. G. Atividade antibacteriana de Cereus jamacaru DC, Cactaceae, Revista Brasileira de Farmacognosia, v. 19, n. 2b, p. 561-564, abr./jun. 2009.
OLIVEIRA, D. B. et al. Extrato dos frutos de Cereus Fernambucensis: atividade antioxidante e inibição da produção de óxido nítrico (NO) por macrófagos. Interscienceplace, ano 2, n. 7, maio/jun., 2009.
OLIVEIRA, F. M. N. et al. Características físico-químicas da polpa e casca do fruto do mandacaru. In: CONGRESSO BRASILEIRO DE CIÊNCIA E TECNOLOGIA DE ALIMENTOS, 19., Recife, Anais... Recife: Centro de Convenções de Pernambuco, 2005.
OSORIO-ESQUIVEL, O. et al. Phenolics, betacyanins and antioxidant activity in Opuntia joconostle fruits. Food Research International, v. 44, p. 2160-2168, 2011.
PADH, H. Functional foods edited by Israel Goldberg. Chapman&Hill, 1994.
PIMIENTA, B. E. El nopal tunero. México: Univ. de Guadalajara, 1990.
QUEIROZ, C. R. A. A. et al. Caracterização dos Taninos da Aroeira-Preta (Myracrodruon urundeuva). Revista Árvore, v. 26, p. 485-492, 2002.
REIS, C. N. et al. Inibição da produção de óxido nítrico e efeito citotóxico de extrato aquoso de annona muricata L. Perspectivas Online, Ciências Biológicas e da Saúde, v. 1, n. 2, p. 1-8, 2011.
REIS, C. N. et al. Antioxidant activity and the content of tannins and phenolic fruit of Annona muricata L. Revista Vértices, Campos dos Goytacazes, RJ, v. 15, n. 3, p. 95112, set./dez. 2013.
ROESLER, R. et al. Atividade antioxidante de frutas do cerrado. Ciênc. Tecnol. Aliment., Campinas, v. 27, n. 1, p. 53-60, jan./mar. 2007.
ROSS, J. A.; KASUM, C. M. Dietary Flavonoids: Bioavailability, Metabolic Effects, and Safety. Annual Review of Nutrition. v. 22, p. 19-34, 2002.
SANTOS-ZEA, L.; ERREZ-URIBE, J. A. G.; SERNA-SALDIVAR, S. O. Comparative analyses of total phenols, antioxidant activity, and Flavonol Glycoside profile of Cladode Flours from different varieties of Opuntia spp. Journal of Agricultural and Food Chemistry, v. 59, p. 7054-7061, 2011.
SAWAYA, W. N.; KHALIL, J. K.; AL-HAMMAD, M. M. Nutririve value of prickli pear seeds, Opuntia ficus-indica, 1983.
SCHOFIELD, P.; MBUGUA, A. N.; PELL, A. N. Analysis of condensed tannins: a review. Animal Feed Science and Technology, v. 92, p. 21-40, 2001.
SEPÚLVEDA, E.; SÁENZ, C. Características químicas y físicas de pulpa de tuna (Opuntia fícus-indica L.). Revista de Agroquímica y Tecnología de Alimentos Valência, v. 30, n. 4, p. 551‐555, 1990.
SIES, H., STAHL, W. Vitamins E and C, b-carotene, and other carotenoids as antioxidants. American Journal of Clinical Nutrition, Bethesda, v.62, n.6, p.1315-1321, 1995.
SILVA, L.R.; ALVES, R.E. Caracterização físico-química de frutos de mandacaru. Rev. Acad., Ciênc. Agrár. Ambient., Curitiba, v.7, n.2, p.199-205, abr./jun. 2009.
SWAIN, T., HILLIS, W. E. The phenolics constituents of prumus domestica: the quantitative analysis of phenolic constituents. J Sci Food Agric. v. 10, p. 63-68, 1959.
YAHIA, E. M. The contribution of fruit and vegetable consumption to human health. Phytochemicals: Chemistry, nutritional and stability, p. 3−51, 2010.
YAHIA, E. M.; MONDRAGON-JACOBO, C. Nutritional components and anti-oxidant capacity of ten cultivars and lines of cactus pear fruit (Opuntia spp.). Food Research International, v. 44, p. 2311–2318, 2011.
YEN, G. C.; DUH, P. D. Scavenging effect of methanolic extracts of peanut hulls on freeradical and active-oxygen species. J. Agric. Food Chem., v. 42, n. 3, p. 629-632, 1994.
Notas de autor