Artículos originales
Prevalencia de colestasis intrahepática gestacional en embarazadas del Hospital de la Madre y el Niño de La Rioja, Argentina. Período: 2015 - 2019
Prevalence of Intrahepatic cholestasis of pregnancy (ICP) in pregnant women at the Hospital de la Madre y el Niño de La Rioja (La Rioja, Argentina). Period 2015 - 2019
Prevalencia de colestasis intrahepática gestacional en embarazadas del Hospital de la Madre y el Niño de La Rioja, Argentina. Período: 2015 - 2019
Bioquímica y Patología Clínica, vol. 88, núm. 2, pp. 20-27, 2024
Asociación Bioquímica Argentina
Resumen: La colestasis intrahepática gestacional (CIG) es una enfermedad hepática que se caracteriza por una conjunción clínica y bioquímica; se traduce en un incremento de los ácidos biliares de leve a moderada severidad, acompañado de prurito, generalmente, de inicio palmoplantar y predominio nocturno. La CIG aparece en el tercer trimestre del embarazo y desaparece luego del parto, mientras que su incidencia varía en diferentes áreas geográficas. Esta patología se asocia con riesgo elevado de morbimortalidad fetal. Objetivo: Determinar la prevalencia de CIG con diagnóstico clínico y bioquímico en embarazadas asistidas en el Hospital de la Madre y el Niño de la ciudad de La Rioja en el período 2015 - 2019 describiendo a las embarazadas con CIG según edad, localización geográfica, edad gestacional y tipo de parto. Asimismo, determinar los valores de referencia de ácidos biliares en embarazadas sanas en dicho nosocomio. Materiales y métodos: Se llevó a cabo un estudio con enfoque cuantitativo, descriptivo, observacional, retrospectivo, de corte transversal (2015-2019), proveniente de historias clínicas del Servicio de Obstetricia. El diseño se realizó teniendo en cuenta los casos de embarazadas con CIG y los controles que se establecieron: embarazadas sin CIG. Además, se utilizaron técnicas de estadística descriptiva. Resultados: La CIG tiene una prevalencia de 1,3 %, y la capital es la zona de mayor incidencia. Se presenta en el tercer trimestre de gestación y en mayores de 27 años con predominio de cesárea. Los ácidos biliares tienen un VR: 1,0-8,3 µmol/l. Conclusión: El laboratorio tiene un rol fundamental para el diagnóstico, el manejo adecuado y la prevención de complicaciones fetales.
Palabras clave: colestasis intrahepática gestacional, embarazadas, ácidos biliares, prurito.
Abstract: Intrahepatic cholestasis of pregnancy (ICP) is a liver disease characterized by a clinical and biochemical conjunction, in which there is an increase in bile acids of mild to moderate severity, accompanied by pruritus, generally with palmoplantar onset and predominantly at night. ICP appears in the third trimester of pregnancy and disappears after delivery, and its incidence varies in different geographical areas. This pathology is associated with a high risk of fetal morbidity and mortality. Objective: To determine the prevalence of ICP with a clinical and biochemical diagnosis in pregnant women assisted at the Hospital de la Madre y El Niño of the City of La Rioja, Argentina, in the period 2015-2019, by describing pregnant women with ICP according to age, geographic provenance, gestational age and type of delivery and by determining the reference values of bile acids in healthy pregnant women in the above-mentioned hospital. Materials and methods: Quantitative, descriptive, observational, retrospective cross-sectional approach (2015 - 2019) from medical records of the obstetrics service. The design was of cases (pregnant women with ICP) and controls (pregnant women without ICP). In addition, descriptive statistical techniques were used. Results: ICP showed a prevalence of 1.3 %, with La Rioja city being the area with the highest incidence. ICP occurred in the third trimester of pregnancy and in women over 27 years of age with a predominance of cesarean section. Bile acids had a RV: 1- 8.3 µmol/l. Conclusion: The laboratory has a fundamental role for the diagnosis, proper management and prevention of fetal complications caused by ICP.
Keywords: intrahepatic cholestasis of pregnancy, pregnant, bile acids, pruritus.
Introducción
En 2012, la Sociedad Española de Ginecología y Obstetricia (SEGO), en su actualización del protocolo de colestasis intrahepática gestacional (CIG), menciona que esta enfermedad es la hepatopatía más frecuente relacionada con la gestación y la 2ª causa de ictericia en el embarazo. Tiene una prevalencia de 0,7 % en los embarazos e incluye una variación geográfica amplia: se da en 1/300 a 1/2000 embarazos; en EEUU se observa en el 0,01 % a 0,02 % de embarazadas; en Chile, en 5 a 10 % de las gestantes (se incrementa en 20 % en partos gemelares). También se concluye que la enfermedad es más frecuente en pacientes con antecedentes de CIG, así como con ingesta de anticonceptivos hormonales.
En 2016, en el Consenso de la Federación Argentina de Sociedades de Ginecología y Obstetricia (FASGO) de CIG, se asevera que este trastorno hepático, que es más frecuente en la gestación, se genera por una alteración homeostática de los ácidos biliares, de manera tal que se traduce en un incremento de los mismos y presenta un cuadro clínico que se manifiesta por prurito, generalmente de inicio palmoplantar con predominio nocturno. Además, se hace hincapié en que los marcadores bioquímicos más precoces y sensibles son los ácidos biliares por lo que recomiendan un ayuno de 8 horas por lo menos para la toma de muestras de laboratorio. También se asevera que la aparición se da en el segundo trimestre tardío o tercer trimestre, y que se revierte el cuadro entre dos y ocho semanas después de culminar el embarazo. Asimismo, se menciona que la recurrencia es alta en los siguientes embarazos, con elevada morbimortalidad perinatal por las complicaciones del parto pretérmino y sufrimiento fetal.1,2,3,4,6
En cuanto a su etiología, es multifactorial y está influenciada por una combinación de factores genéticos, endócrinos y ambientales.2,3 Como criterios de diagnóstico se establecen los síndromes clínico y bioquímico:
Síndrome clínico: el síntoma principal es el prurito palmoplantar y/o prurito general. Generalmente, se presenta durante el último trimestre de gestación, en un 80 %, mientras que en el 1º y 2º trimestre se presenta en un 10 % y 25 %, respectivamente. Comienza generalmente en la región palmoplantar, con progresión central, generalizándose al resto del cuerpo; es de predominio nocturno, y puede provocar en la paciente excoriaciones que lleven a insomnio e irritabilidad. La ictericia se puede presentar en un 25 %, generalmente en la segunda semana posterior al cuadro pruriginoso; también pueden aparecer náuseas, vómitos, coluria, hipocolia y dolor en hipocondrio derecho. Culminada la gestación, el cuadro clínico se revierte de manera espontánea en un tiempo máximo de cuatro semanas.
Síndrome bioquímico: se produce una elevación de los ácidos biliares con o sin aumento de las enzimas hepáticas: glutámico oxalacetico transaminasa (GOT), piruvato glutamato transaminasa (GPT), fosfatasa alcalina (FAL), gamma-glutamiltransferasa (GGT) y bilirrubina. La actividad de protrombina, <70 % por malabsorción de vitamina K, es poco frecuente.
Los ácidos biliares en suero son el marcador más sensible y precoz para el diagnóstico de colestasis intrahepática de la gestación.1,3 El rango de referencia depende de la técnica utilizada para analizarlos. La mayoría de los estudios utiliza un límite superior normal de 10 μmol/L para un análisis enzimático de ácidos biliares séricos totales.
Los niveles de transaminasa pueden estar elevados 2 a 10 veces sobre el valor normal, a menudo antes de la elevación de ácidos biliares. La GPT es más sensible que la GOT en el diagnóstico de la colestasis intrahepática del embarazo.2 Debido a que la placenta produce grandes cantidades de FAL durante el embarazo, generalmente, no es útil en el diagnóstico de colestasis intrahepática de la gestación. La gamma glutamiltransferasa (GGT) puede estar elevada, pero, comúnmente, es normal. Las enzimas hepáticas en el diagnóstico de colestasis intrahepática de la gestación se normalizan 2 a 8 semanas después del parto. La mayoría de las complicaciones ocurren cuando los niveles de ácido biliar exceden 40 μmol/L.3,5,7,8
Si la medición de ácidos biliares séricos no está disponible, el Real Colegio de Obstetras y Ginecólogos del Reino Unido recomienda que se diagnostiquen como colestasis intrahepática de la gestación los casos de mujeres con prurito típico y pruebas de función hepática anormales, ya habiéndose descartado otros diagnósticos diferenciales como diagnostico probable de CIG (PCIG). Hasta tanto se realice la determinación de AB sérico, la paciente será guiada y tratada como CIG.2 En general, la mayoría de las pruebas hepáticas permanecen en el rango normal durante el embarazo, excepto las producidas por la placenta (fosfatasa alcalina, alfafetoproteína).
Se ha establecido una clasificación según niveles de riesgo para CIG, para un mejor manejo y tratamiento de esta patología, teniendo en cuenta: niveles bioquímicos (perfil hepático junto con AB), criterios clínicos, antecedentes relevantes como CIG en embarazos previos, antecedentes familiares de CIG, fetos muertos con o sin diagnóstico preciso de CIG.
-
Leve: los ácidos biliares de 10,0 a 19,9 μmol/L y el perfil hepático se encuentran dentro de parámetros normales.
-
Moderado: los ácidos biliares se encuentran entre 20,0 y 39,9 μmol/L, y/o el perfil hepático se halla incrementado, pero no más del doble.
-
Alto: los ácidos biliares están por encima de 40 μmol/L y/o el perfil hepático es más del doble y/o no hay respuesta al tratamiento médico.
El propósito final de esta investigación es aportar información para mejorar la atención sanitaria que reciben las pacientes embarazadas con CIG que asisten al HMyN, por lo que se hace necesario determinar la prevalencia de casos según los valores de referencia de los ácidos biliares séricos como también, describir otras características de las pacientes, motivo por el cual se establecieron los siguientes objetivos:determinar la prevalencia de CIG con diagnóstico clínico y bioquímico en embarazadas asistidas en el Hospital de la Madre y el Niño de la ciudad de La Rioja en el período 2015-2019 describiendo a las embarazadas con CIG según edad, localización geográfica, edad gestacional y tipo de parto. Asimismo, determinar los valores de referencia de los ácidos biliares en embarazadas sanas en dicho nosocomio. La importancia del diagnóstico radica en prevenir las complicaciones de la madre y del feto de forma precoz y evitar efectos perjudiciales para ellos.9,10,11
Materiales y métodos
Se realizó un estudio cuantitativo, descriptivo, de tipo observacional, con información retrospectiva, proveniente de historias clínicas del Servicio de Obstetricia e información del laboratorio bioquímico central del Hospital de la Madre y el Niño (HMyN), El estudio, de corte transversal, abarcó el período de 2015 a 2019. Se hizo un diseño retrospectivo de casos de embarazadas con CIG y controles sin CIG. .
El recorte que se realiza en la población de estudio corresponde al conjunto de todas las mujeres embarazadas asistidas por primera vez en el Servicio de Obstetricia del HMyN de la ciudad de La Rioja en el período antes mencionado e incluye muestras de pacientes embarazadas con diagnostico CIG según síndromes clínicos y bioquímicos.
Criterios de inclusión: pacientes registradas en el Hospital de la Madre y el Niño que contaran con historia clínica en el período 2015-2019; mujeres embarazadas cuyos partos fueron atendidos en el HMyN durante el período 2015-2019; pacientes que tuvieran resultados de perfil hepático, tiempo de protrombina y/o ácidos biliares como parte de los exámenes de laboratorio; pacientes que presentaran prurito de inicio palmoplantar con predominio nocturno y /o general; gestantes y recién nacidos cuyas historias clínicas contaran con los datos del estudio.
La base de datos se construyó con la recolección de información obtenida por las historias clínicas de las pacientes a partir de los objetivos de estudio. Para ello, se solicitó al director del Hospital, como así también al área correspondiente, su autorización para el acceso a las historias clínicas de las pacientes que ingresaron a dicho nosocomio durante el período del estudio.
La recopilación de datos se llevó a cabo mediante la revisión de historias clínicas de pacientes que cumplían con los criterios de inclusión, transcribiendo los datos de estudio a una base de datos elaborada en Excel: “Registro de datos”.
Mediante el registro disponible de las historias clínicas de las pacientes con CIG y los registros de laboratorio, se establecieron las siguientes variables.
Edad (en años cumplidos): 14-19, 20-24, 25-29, 30-34, 35-40, 41-45.
Localidad: de residencia del paciente (capital - interior)
Prurito generalizado: sí/no
Prurito palmoplantar: sí/no
Edad gestacional: según los siguientes grupos: 20-25 / 26-30 /31-35 /más de 35.
Tipo de parto (posterior al diagnóstico de CIG): normal o cesárea.
Nacido vivo: sí/no.
CIG (según diagnóstico, que se realiza por la información de la historia clínica, que incluye síndromes clínicos, prurito palmoplantar de predominio nocturno, con la progresión de la enfermedad y la ausencia de tratamiento): sí/no
Acido biliar: valor cuantitativo
CIG según proveedor: presencia de CIG: sí/no
Niveles de riesgo de CIG: alto, moderado y leve.
Hepatograma (bilirrubina, FAL, GGT, GOT, GPT): valor cuantitativo
CIG (según el valor de referencia calculado por HMyN): sí/no.
Coagulación (TP, KPPT): valor cuantitativo
Medición de variables
Los criterios diagnóstico considerados fueron: criterios clínicos con la aparición de prurito palmoplantar de predominio nocturno, sin lesiones y prurito generalizado; criterio de normalidad bioquímica, que se estableció por medio de las determinaciones de los siguientes metabolitos teniendo en cuenta sus valores de referencias (Tabla I): GOT, GPT, GGT, FAL, bilirrubina, TP y ácidos biliares, que fueron evaluados en muestras de sangre obtenidas de todas las pacientes por punciones venosas teniendo en cuenta su parte preanalítica y, luego, analizadas con sus respectivos métodos usando equipamiento y reactivos Wiener: Cm 250 Wiener y Col 4 Wiener.
Tanto la enzima GOT como la GPT fueron determinadas a 37°C mediante el método UV optimizado (IFCC, International of Clinical Chemistry and Laboratory Medicine) a 340 nm, mientras que, en la determinación de la fosfatasa alcalina (FAL), se utilizó el método cinético optimizado (DGKC y SSCC) a 405 nm, y el método (Szasz modificado), para la determinación de gamma glutamil transpeptidasa (GGT. La bilirrubina (total y directa) reacciona específicamente con el ácido sulfanílico diazotado produciendo un pigmento color rojo - violáceo (azobilirrubina), que se mide fotocolorimétricamente a 530 nm. Si bien la bilirrubina conjugada (directa) reacciona directamente con el diazorreactivo, la bilirrubina no conjugada (indirecta) requiere la presencia de un desarrollador acuoso (Reactivo A) que posibilite su reacción. De tal forma, para que reaccione la bilirrubina total (conjugada y no conjugada) presente en la muestra, debe agregarse benzoato de cafeína al medio de reacción. Para el estudio del tiempo de protrombina, que analiza la vía extrínseca de la coagulación, determinación y/o deficiencia de factores y vitamina k, se utilizó tromboplastina cálcica en una etapa.
Todas las técnicas usadas fueron evaluadas con precisión y exactitud por sus respectivos calibradores y controles de calidad Standatrol SE, como así también, por su control externo ProgBA. Para los analitos, se tuvieron en cuenta los valores de referencia que se presentan en la Tabla I.
Los ácidos biliares, que constituyen el marcador más sensible y precoz, se determinaron por método enzimático colorimétrico a 540 nm mediante la reacción del azul de tetrazolio marca Randox, UK, con coeficiente de variación 1,2 %. La performance analítica fue evaluada según control de calidad interno, calibradores comerciales Randox. Luego, para los pacientes con CIG, se categorizaron los niveles de riesgo:
-
Alto: ≥40 µmol/L
Moderado: 21 hasta 39,9 µmol/L
Bajo: 10 µmol/L hasta 20,9 (8,10).
| Analitos | Intervalos de referencia |
| Ácido biliar | Menor de 10 µmol/L * |
| GGT | 7 – 32 * |
| GOT | 10 – 32* |
| GPT | 10 – 31* |
| FAL | 64 – 300 * |
| Bilirrubina total | Menor de 1,0* |
| TP | 70 % a 100 % |
| Resultado | FAL | GPT | GOT | GGT | Bilirrubina total | TP |
| Normales | 8,7 % | 29,8 % | 45,3 % | 31,0 % | 56,5 % | 96,9 % |
| Patológicos | 79,8 % | 64,6 % | 49,7 % | 44,7 % | 16,8 % | 0 % |
| S/D | 12,4 % | 5,6 % | 5,0 % | 24,3 % | 26,7 % | 3,1 % |
| Total con CIG (n=161) | 100 % | 100 % | 100 % | 100 % | 100 % | 100 % |
Análisis de datos
Se utilizaron técnicas de estadística descriptiva: tablas de frecuencias, contingencia, cálculo de indicadores descriptivos y elaboración de gráficos. El diagnóstico habitual de CIG, en el HMyN, se realiza mediante manifestaciones clínicas y de laboratorio por lo cual los positivos fueron considerados verdaderos positivos (VP) y, en el caso contrario, verdaderos negativos (VN).
Luego, el análisis con las manifestaciones clínicas de prurito palmoplantar y generalizado se realizó mediante el cálculo de la sensibilidad y la especificidad.
La sensibilidad es la capacidad del factor de diagnosticar los positivos y la especificidad es la capacidad de diagnosticar los negativos:
El cálculo de sensibilidad y especificidad se realiza para dos factores clínicos, el prurito palmoplantar y generalizado y para el factor de referencia del HMyN de ácido biliar. Estos indicadores permiten valorar el único factor utilizado para diagnosticar CIG. Por lo tanto, valores altos de especificidad indican una alta capacidad del factor clínico de detectar positivos. En general, estos valores se expresan en porcentajes.
Para la determinación de valores de referencia del HMyN de ácido biliar en embarazadas sanas, se estudió la distribución y se eliminaron valores outliers y, dado que la distribución es asimétrica, se calcularon el P5 y el P95.
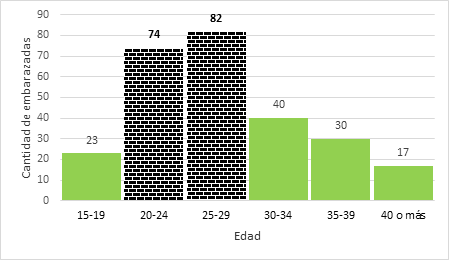
Figura 1.
Edad de las embarazadas en la muestra general.
Resultados
Se trabajó con una muestra de 266 pacientes embarazadas entre 15 y 45 años, con edad promedio de 27,5 años ± 6,5 años. En la Figura 1, se observa mayor cantidad de pacientes en el grupo de 20 a 30 años, por lo tanto, las 156 (74 + 82) representan el 58,6 % de las pacientes analizadas.
El 66,2 % (n = 176) tenía como localidad de origen o procedencia la ciudad capital, mientras que el resto, el 33,8 %, pertenecía a zonas del interior de la provincia. El rango de las semanas de gestación variaba entre 18 y 41 y solo un 1,9 % (n = 5) tuvo nacimiento con muerte fetal.
La prevalencia se calcula como el total de embarazadas diagnosticadas positivamente con CIG, según clínica y laboratorio, dividido el total de mujeres embarazadas asistidas por primera vez (N = 11981) en el período 2015 - 2019 en el HMyN.
De la muestra de 266 pacientes, se obtuvo un n = 161 positivos de CIG, por lo tanto, la prevalencia de CIG es de 1,3 %.
Las pacientes diagnosticadas con CIG positivamente (n = 161) poseen una edad que varía entre 18 y 40 años, con un promedio de 27,4 ± 6,4 años. El 62,1 % (n = 100) reside en la ciudad capital de La Rioja y el restante 37,9 % (n = 61), en diversas localidades de la provincia. Estos valores son muy cercanos a la muestra general.
Por otro lado, las semanas de gestación varían entre 18 y 40, con un promedio de 34,9 ± 3,7 semanas.
En relación con el tipo de parto, el 79,5 % (n = 128) tuvo nacimientos vía cesárea y el resto, parto normal. En cuanto al ácido biliar (n = 115), en la Figura 2, se observa una distribución asimétrica, con mayor frecuencia de valores que superan los 18 µmol/L. Asimismo, se detectan valores menores de 10 µmol/L, correspondientes a pacientes diagnosticadas con signos clínicos. En los 161 casos (n = 46), no se realizó el análisis de ácido biliar por falta de reactivo por lo cual se los tomó como diagnóstico probable de CIG (PCIG).
Por otro lado, los registros de laboratorio presentaron valores anormales, principalmente en FAL, GPT, GOT, GGT y bilirrubina Total. No se presentaron valores anormales en TP, tal como se muestra en la Tabla II. La GPT exhibe un valor de 64,6 %, que es más sensible que la GOT en el diagnóstico de la CIG. Si bien obtuvimos un 79,8 % de FAL, sabemos que es un valor sin significancia clínica en la CIG debido a que la placenta produce grandes cantidades de FAL durante el embarazo y, por eso, generalmente, no es útil en el diagnóstico de CIG.
En embarazadas con ácido biliar igual o superior a 10 µmol/L, se calculó el nivel de riesgo y se registraron un 37,5 % de nivel leve, un 35,9 % de nivel moderado y un 26,6 % de nivel alto.
En el diagnóstico de estas embarazadas, los signos clínicos ocupan un papel fundamental, ya que, de los 161 casos, 126 presentaron al menos algún prurito (78 %).
Relación de CIG con prurito palmoplantar y generalizado
La relación entre la presencia de CIG y la manifestación clínica de prurito palmoplantar se presenta en la Tabla III. En la misma, se advierte que el 75,8 % de los positivos diagnosticados con factores clínicos poseen la presencia de prurito palmoplantar. Por lo tanto, la sensibilidad del prurito palmoplantar es del 75,8 % y la especificidad, del 68,2 %.
Además, se detectó una relación entre el diagnóstico de CIG con el factor prurito palmoplantar (Chi = 44,5; p<0,001). Luego, se analizó la relación entre la presencia de CIG y la manifestación clínica de prurito generalizado. Estos resultados se presentan en la Tabla IV. En la misma, se advierte que el 61,9 % de los positivos diagnosticados con factores clínicos posee la presencia de prurito generalizado, por lo tanto, la sensibilidad es del 61,9 %. El 63,9 % de los negativos no presenta la manifestación de prurito generalizado, por lo tanto, la especificidad es del 64,0 %. Luego, se detectó una relación entre el diagnóstico de CIG con el factor prurito generalizado (Chi = 14,8; p<0,001).
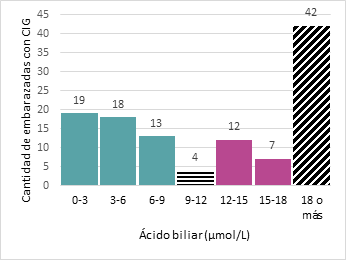
Figura 2.
Valores de ácido biliar en embarazadas con colestasis intrahepática gestacional.
CIG, colestasis intrahepática gestacional.
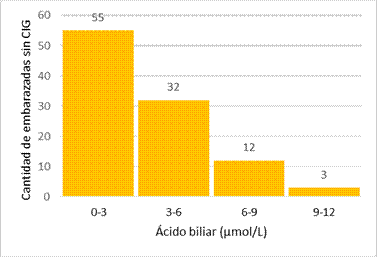
Figura 3.
Cantidad de embarazadas sin colestasis intrahepática gestacional en HMyN según valores de ácido biliar.
| Diagnóstico CIG | Prurito palmoplantar | Total | ||
| No | Sí | |||
| No (Controles) | N | 60 | 28 | 88 |
| % | 68,2 | 31,8 | 100,0 | |
| Sí (Casos) | N | 37 | 116 | 153 |
| % | 24,2 | 75,8 | 100,0 | |
| Total | N | 197 | 144 | 241 |
| % | 40,2 | 59,8 | 100,0 | |
| Diagnóstico CIG | Prurito generalizado | Total | ||
| No | Sí | |||
| No (Controles) | N | 55 | 31 | 97 |
| % | 64,0 | 36,0 | 100,0 | |
| Sí (Casos) | N | 59 | 96 | 150 |
| % | 38,1 | 61,9 | 100,0 | |
| Total | N | 114 | 127 | 241 |
| % | 47,3 | 52,7 | 100,0 | |
Determinación de valores de ácidos biliares en embarazadas del HMyN
Del total de la muestra de 266 embarazadas se registró el valor de ácido biliar en 217. En la Tabla V, se presentan los valores que describen la presencia de ácido biliar: mínimo y máximo, media, mediana y percentiles. Se incluye la medida de variabilidad del rango intercuartílico, sugerida para medir la variación en distribuciones asimétricas, a partir de la cual se advierte que la variabilidad es mayor en el grupo de las embarazadas con CIG.
En la población de embarazadas sanas, se determinan los valores de referencia, que surgen de los registros del HMyN. La distribución del ácido biliar es asimétrica, según se observa en la Figura 3, por lo cual se calculó el P5 y P95 a fin de determinar los valores de referencia para el 90 % central.
Mediante el análisis de outliers o valores extremos de los registros de ácido biliar en embarazadas sanas, se calculó el valor límite de 9,25 µmol/L, a partir del cual se descartan valores, por lo que se censuraron 3 registros. Luego, con un n = 99 de casos, se calcularon valores de referencia P5 y P95 para el 90 % central de las embarazadas sanas. Los valores de referencia para embarazadas sanas del HMyN son los que se presentan en la Tabla VI. Para el percentil del 90 % central de embarazadas, los valores son de 1 - 8,3 µmol/L. De esta manera, en el HMyN se determinaron valores de referencia de ácido biliar en embarazadas sanas entre 1 y 8,3 µmol/L.
Relación del diagnóstico de CIG (clínica y laboratorio) con el diagnóstico de CIG según determinaciones de ácido biliar
Según el rango de ácido biliar provisto por el proveedor (RANDOX), es posible determinar la presencia de CIG en las embarazadas. Luego, si el ácido biliar alcanza o supera los 10 µmol/L, se determina que una paciente tiene CIG.
Las determinaciones de ácido biliar no fueron realizadas a la totalidad de pacientes debido al faltante de reactivos. De la muestra de 266 embarazadas, tal como se indicó en el punto anterior, se registró el ácido biliar de 217. Sobre este grupo de embarazadas, se estudió el porcentaje de diagnosticadas por la clínica/laboratorio y el porcentaje de diagnosticadas solo por el valor de referencia del proveedor (≥10 µmol/L). En la muestra total de embarazadas, se registra un 53 % diagnosticado con CIG mediante clínica y laboratorio (115/217). Sin embargo, el diagnóstico del registro del ácido biliar solamente es de 29,5 %. En la Tabla VII, se relacionan estos resultados y se señala que 115 embarazadas fueron diagnosticadas con CIG según clínica/laboratorio y, de esas, solamente 64 presentaron ácido biliar ≥10 µmol/L (sensibilidad del 55,7 %).
| Colestasis intrahepática gestacional | ||
| No (Controles) | Sí (Casos) | |
| N | 102 | 115 |
| Sin registro de ácido biliar | 3 | 46 |
| Mínimo | 0,4 | 0,9 |
| Máximo | 9,8 | 161,0 |
| Media | 3,6 | 21,9 |
| DS | 2,3 | 28,4 |
| P5 | 1,0 | 2,0 |
| P95 | 8,5 | 67,7 |
Relación del diagnóstico de CIG clínico con el diagnóstico de CIG según valores de referencia de ácido biliar del HMyN
Si se toman los valores de referencia del HMyN, el porcentaje de embarazadas que se detectan como positivas según el ácido biliar es de 33,6 %, un porcentaje mayor que el correspondiente al valor habitual, que es 29,5 %. Existen 73 embarazadas que podrían ser diagnosticadas con CIG considerando solamente el valor de referencia del HMyN y 144 embarazadas que no serían diagnosticadas con este valor.
Por otro lado, el diagnóstico correspondiente al valor de referencia del HMyN (Tabla VIII) indica que se logra detectar el 93,1 % de negativos (especificidad) y el 57,4 % de positivos (sensibilidad). Estos valores propios de referencia poseen mayor sensibilidad que el valor de referencia del proveedor.
| Indicador | Valor |
| N | 99 |
| Mínimo | 0,4 |
| Máximo | 8,6 |
| Media | 3,5 |
| P50 | 2,8 |
| P5 | 1,0 |
| P95 | 8,3 |
| Diagnóstico de colestasis intrahepática gestacional | Colestasis intrahepática gestacional según valor de referencia de ácido biliar del proveedor | Total | ||
| No (< 10 µmol/L) | Si (≥10 µmol/L) | |||
| No (Controles) | N | 102 | 0 | 102 |
| % | 100,0 | 0,0 | 100,0 | |
| Si (Casos) | N | 51 | 64 | 115 |
| % | 44,3 | 55,7 | 100,0 | |
| Total | N | 153 | 64 | 217 |
| % | 70,5 | 29,5 | 100,0 | |
| Diagnóstico de colestasis intrahepática gestacional | Colestasis intrahepática gestacional según ácido biliar HMyN | Total | |||
| No (< 8,3 µmol/L) | Sí (≥8,3 µmol/L) | ||||
| No (Controles) | N | 95 | 7 | 102 | |
| % | 93,1 | 6,9 | 100,0 | ||
| Sí (Casos) | N | 49 | 66 | 115 | |
| % | 42,6 | 57,4 | 100,0 | ||
| Total | N | 144 | 73 | 217 | |
| % | 66,4 | 33,6 | 100,0 | ||
Discusión
Dentro de las enfermedades hepáticas de la gestación, la colestasis intrahepática gestacional es la patología más frecuente y puede generar severas complicaciones feto/neonatales, por lo cual la detección oportuna es importante para el Hospital de la Madre y el Niño de la provincia de La Rioja.
En el trabajo, se incluyeron 266 pacientes embarazadas, que fueron diagnosticadas con CIG según síndromes clínicos y bioquímicos y que asistieron por primera vez al Servicio de Obstetricia del Hospital de la Madre y el Niño de la ciudad de La Rioja durante el período 2015 - 2019.
La prevalencia de CIG es de 1,3 % en embarazadas del HMyN de la ciudad de La Rioja, capital de la provincia, donde se da la mayor incidencia. La mayoría de embarazadas diagnosticadas se encuentran en el tercer trimestre de gestación y son, principalmente, mayores de 27 años.
La edad gestacional promedio de las embarazadas diagnosticadas con CIG fue de 35 semanas. Por otro lado, la mayoría de las embarazadas han tenido partos por medio de cesárea.
Existe una relación entre el diagnóstico CIG mediante la clínica y el laboratorio y la presencia de prurito palmoplantar y generalizado, ya que el 78 % presentó alguno de estos signos. En particular, el 75,8 % posee la manifestación de prurito palmoplantar y el 61,9 %, del generalizado, por lo que la sensibilidad (capacidad de detectar verdaderos positivos) es mayor en el palmoplantar. Toda mujer que presente prurito requiere estudios de laboratorio complementarios, ya que la CIG se basa en la presencia de prurito asociada a concentraciones elevadas de ácidos biliares séricos, y hepatograma.
En relación con los analitos estudiados en este trabajo, más del 44 % de las embarazadas presenta alteraciones de FAL, GPT, GOT y GGT. Para BT, un 26,7 % y para TP, un 3,1 % de alteraciones, lo que indica que estos últimos tienen escaso valor diagnóstico.
Mediante los niveles de ácido biliar y según las especificaciones del proveedor, se observó un 62,5 % de pacientes con un riesgo alto o moderado, hecho que evidencia la necesidad de realizar análisis de AB. Estos resultados concuerdan con la bibliografía consultada en este estudio, en la cual se considera que la alteración de los AB y enzimas hepáticas en suero materno son buenos predictores de la mayoría de las complicaciones que se presentan asociadas a la CIG, y que los AB constituyen el marcador más sensible y precoz de la enfermedad.
Se determinaron los valores de referencia propios para el HMyN mediante el percentil central del 90%, y se obtuvieron como resultado valores entre 1 y 8,3 µmol/L; este último es inferior al sugerido por el proveedor. Lo expuesto implica que con estos valores de referencia se podrían detectar más embarazadas con CIG. Este valor de referencia presenta para el diagnóstico CIG una sensibilidad (posibilidad de diagnosticar verdaderos positivos) de 57,4 % y una especificidad (posibilidad de diagnosticar verdaderos negativos) de 93,1%, indicadores más favorables al diagnóstico que el utilizado hasta el momento.
La CIG es una patología que se presenta con una prevalencia del 1,3 % en el Hospital de la Madre y el Niño de la cuidad de La Rioja, y la capital de la provincia es la zona con mayor incidencia. La más grande cantidad de embarazadas diagnosticadas se encuentra en tercer trimestre de gestación y las pacientes son, principalmente, mayores de 27 años.
El laboratorio fue fundamental para el diagnóstico de la patología, ya que los ácidos biliares, los primeros en aumentar acompañados por la alteración de las enzimas hepáticas, se mostraron más alterados y este hecho permitió que más de la mitad de las pacientes pudieran ser diagnosticadas.
El laboratorio conjuntamente con la clínica, que en el HMyN tiene un papel fundamental para el diagnóstico, contribuye al diagnóstico oportuno, el manejo adecuado y la prevención de complicaciones fetales. A partir de estos resultados, quedarán abiertos otros interrogantes, que podrán ser abordados para mejorar la atención en el área química del Laboratorio del HMyN.
Referencias bibliografías
1. M. García, A. García, C. Pérez, J. Grande, J.M. Hernández, P. de la Fuente. Federación Argentina de Sociedades de Ginecología y Obstetricia. Colestasis Intrahepática Gestacional (CIG). Colestasis intrahepática del embarazo: diagnóstico y manejoIntrahepatic cholestasis of pregnancy. Diagnosis and managementDisponible en: http://www.fasgo.org.ar/archivos/consensos/Consenso_de_obstetricia. 2009 DOI: 10.1016/s0304-5013(05)72380-3
2. Šimják P, Pařízek A, Vítek L, Černý A, Adamcová K, Koucký M, et al. Fetal complications due to intrahepatic cholestasis of pregnancy. J Perinat Med. 2015;43(2):133–9. DOI: 10.1515/jpm-2014-0089
3. Marschall HU. Management of intrahepatic cholestasis of pregnancy. Expert Review of Gastroenterology & Hepatology. 2015;9(10):1273-9 DOI: 10.1586/17474124.2015.1083857
4. Hosein Dalili,Firouzeh Nili,Mahdi Sheikh ,Amir Kamal Hardani,Mamak Shariat,Fatemeh Nayeri, et al. Comparison of the Four Proposed Apgar Scoring Systems in the Assessment of Birth Asphyxia and Adverse Early Neurologic. Plos One. 2015;10(3). DOI: 10.1371/journal.pone.0122116
5. Diken Z, Usta IM, Nassar AH. A clinical approach to intrahepatic cholestasis of pregnancy. Am J Perinatol. 2014;31(1):1-8. DOI: 10.1055/s-0033-1333673
6. Shemer W, Thorsell E, Marschall M, Kaijser HU. Risks of emergency cesarean section and fetal asphyxia after induction of labor in intrahepatic cholestasis of pregnancy: A hospital-based retrospective cohort study. Sexual / Reproductive Healthcare. 2013 Mar;4(1):17-22. DOI: 10.1016/j.srhc.2012.11.005
7. Monte MJ, Marin JJG, Antelo A, Vazquez-Tato J. Bile acids: chemistry, physiology, and pathophysiology. World J Gastroenterol. 2009;15(7):804-16. DOI: 10.3748/wjg.15.804
8. Geenes V, Chambers J, Khurana R, Shemer EW, Sia W, Mandair D, et al. Rifampicin in the treatment of severe intrahepatic cholestasis of pregnancy. Eur J Obstet Gynecol Reprod Biol. 2015;189:59-63. DOI: 10.1016/j.ejogrb.2015.03.020
9. Floreani A, Gervasi MT. New insights on intrahepatic cholestasis of pregnancy. Clin Liver Dis. 2016;20(1):177-89. DOI: 10.1016/j.cld.2015.08.010
10. Gabzdyl E, Schlaeger J. Intrahepatic Cholestasis of Pregnancy. A critical Clinical Review. The Journal of Perinatal & Neonatal Nursing. 2014;29(1):41-50. DOI: 10.1097/JPN.0000000000000077
13. Sebiha O, Yasin C, Orhan VO, Sule Y. Review of a challenging clinical issue: Intrahepatic cholestasis of pregnancy. World Journal of Gatroenterology. 2015;21(23):7134-41. DOI: 10.3748/wjg.v21.i23.7134
Notas de autor
soniateranlopez@hotmail.com
Información adicional
redalyc-journal-id: 651

