Artículos originales
Verificación e implementación de los métodos de β-hidroxibutirato y ácidos grasos libres no esterificados en un equipo automatizado
Verification and implementation of the β-hydroxybutyrate and non-esterified free fatty acid methods in automated equipment
Verificación e implementación de los métodos de β-hidroxibutirato y ácidos grasos libres no esterificados en un equipo automatizado
Bioquímica y Patología Clínica, vol. 89, núm. 1, pp. 60-65, 2025
Asociación Bioquímica Argentina
Resumen: Introducción: El β-hidroxibutirato (βOH) y los ácidos grasos libres no esterificados (NEFA) son medidos para el estudio de las enfermedades metabólicas e hipoglucemias. Además, la medición de βOH en suero es útil para hiperglucemias y control de dietas cetogénicas. La verificación debe confirmar que se ha cumplido el desempeño declarado por el fabricante. Objetivo: Verificar los métodos cuantitativos de NEFA y βOH. Materiales y métodos: Se utlizaron la guías del CLSI EP15-A3 y EP6-A y el autoanalizador de Roche/Cobas 501. Resultados: Se observó lo siguiente: a) Condiciones de repetibilidad NEFA: nivel 1 (N1): coeficiente de variación 0,60% y nivel 2 (N2): 0,62%. N1 βOH: 1,54% y N2 0,56%; b) Precisión intermedia NEFA: 2,51% N1 y 1,62% N2 y 1,62% N1 y 0,78% N2 para βOH; c) Veracidad NEFA: 0,7 mmol/L N1 y 1,6 mmol/L N2, rangos de verificación 0,55-0,66 mmol/L y 1,38-1,53 mmol/L; βOH 0,3 mmol/L N1 y 2,9 mmol/L N2, rangos de verificación 0,294-0,325 mmol/L y 2,793-2,942 mmol/L. El sesgo de la estimación de la veracidad fue de 11,85% y 11,98% para NEFA y de 4,83% y 1,92% para βOH; d) Linealidad: hasta 2,4 mmol/L NEFA y hasta 3,23 mmol/l βOH. Conclusiones: Se logró verificar la precisión intermedia y en condiciones de repetibilidad para ambos analitos, la veracidad desde el punto de vista clínico, aunque no estadístico, para NEFA y la veracidad clínica y estadística para βOH. Para el NEFA, se verificó la linealidad estadística y clínica y para el βOH, la linealidad clínica.
Palabras clave: verificación de métodos, β-hidroxibutirato, ácidos grasos libres no esterificados, especificaciones técnicas.
Abstract: Introduction: β-Hydroxybutyrate (βOH) and non-esterified free fatty acids (NEFA) are measured for the study of metabolic diseases and hypoglycemia, and βOH, in addition, for hyperglycemia and control in ketogenic diets. Verification should confirm that the performance declared by the manufacturer has been met. Objective: To verify the NEFA and βOH methods. Materials and methods: The CLSI guidelines EP15-A3 and EP6-A were followed. The Roche/Cobas 501 autoanalyzer was used. Results: NEFA repeatability conditions were as follows: level 1 (N1) coefficient of variation 0.60% and level 2 (N2) 0.62%. N1 βOH 1.54% and N2 0.56%. Intermediate precision: 2.51% N1 and 1.62% N2 for NEFA and 1.62% N1 and 0.78% N2 for βOH. Veracity: 0.7 mmol/L N1 and 1.6 mmol/L N2, verification ranges 0.55-0.66 mmol/L and 1.38-1.53 mmol/L for NEFA; 0.3 mmol/L N1 and 2.9 mmol/L N2, verification ranges 0.294-0.325 mmol/L and 2.793-2.942 mmol/L for βOH. The veracity estimation bias was 11.85% and 11.98% for NEFA and 4.83% and 1.92% for βOH. Linearity was up to 2.4 mmol/L for NEFA and up to 3.23 mmol/l for βOH. Conclusions: It was possible to verify precision under repeatability and intermediate conditions for both analytes, veracity from a clinical point of view, although not statistical for NEFA, and clinical and statistical veracity for βOH. Statistical and clinical linearity was verified for NEFA and clinical linearity for βOH.
Keywords: method verification, β-hydroxybutyrate, non-esterified free fatty acids, technical specifications.
Introducción
Los cuerpos cetónicos son pequeñas moléculas sintetizadas principalmente en el hígado a partir de ácidos grasos que circulan por el torrente sanguíneo durante el ayuno, el ejercicio prolongado y cuando se restringen los carbohidratos. Estos son tomados por tejidos que necesitan energía, convertidos primero en acetil-CoA y luego, en ATP. Durante la cetosis, se forman y utilizan tres cuerpos cetónicos principales para obtener energía: acetona, acetoacetato y β-hidroxibutirato (βOH), el cuerpo cetónico más abundante en los mamíferos.1,2
La presencia y el grado de cetosis pueden ser determinados midiendo los niveles sanguíneos de βOH. Además, su determinación es útil para el control en dietas cetogénicas. Dicha dieta constituye el tratamiento no farmacológico de eficacia probada más utilizado en la última década para el manejo de la epilepsia refractaria en la población pediátrica. Consiste en un plan alimenticio rico en grasas, adecuado en proteínas y bajo en hidratos de carbono (HC), diseñado para producir cetosis e imitar los cambios metabólicos que ocurren durante el ayuno.3,4,5
Los ácidos grasos no esterificados (NEFA) son medidos en el laboratorio para el estudio de enfermedades metabólicas e hipoglucemias y se utilizan para evaluar la síntesis de estos ácidos en diferentes situaciones de ayuno. En el laboratorio del estudio, al formar parte de un hospital pediátrico de alta complejidad, estas determinaciones son solicitadas de forma habitual.
La norma IRAM-ISO 15189:2023 establece que los procedimientos analíticos validados por el fabricante, utilizados sin modificaciones, deben estar sujetos a la verificación independiente por parte del laboratorio antes de ser introducidos en el uso rutinario. En la misma norma, se establece que el laboratorio debe disponer de un procedimiento para verificar que puede realizar correctamente los métodos de análisis antes de comenzar a utilizarlos, asegurando que se puede alcanzar el desempeño requerido, según lo declarado por el fabricante o el método. El Clinical Laboratory Standard Institute (CLSI) provee guías de verificación con protocolos accesibles al laboratorio de rutina. La CLSI EP15-A3 está diseñada para la verificación de precisión y veracidad de un método que previamente fue validado por el fabricante, mientras que la CLSI EP6-A se utiliza para verificar linealidad. La implementación de ambas le permite al laboratorio, mediante el aporte de evidencia objetiva (en forma de características de desempeño), demostrar que se ha cumplido con los requisitos especificados por el fabricante para el procedimiento analítico y así habilitar su uso en la práctica diaria.6,7
Los reactivos disponibles que se comercializan actualmente para ambos analitos son para uso manual, con la posibilidad de adaptación a la automatización, lo que genera, por un lado, mayor demanda de personal, de tiempo y de costos, y, por otro, una mayor probabilidad de error a la hora de realizar la determinación debido a la variación intra e interoperador de la técnica. Es por eso que se planteó como objetivo realizar la verificación de la precisión, veracidad y linealidad de los métodos de medición de NEFA y βOH de acuerdo con especificaciones internacionales de guías publicadas por el CLSI, en un equipo automatizado de química clínica de un hospital pediátrico de alta complejidad para su posterior implementación en la rutina asistencial.
Materiales y métodos
Se realizó un estudio experimental, transversal y prospectivo.
Autoanalizador y reactivos
Se utilizó el autoanalizador de Química Clínica Roche/Cobas 6000 501. Los reactivos usados fueron de RANDOX-CROMOION® para NEFA (lote: 575736, vencimiento:28/8/2023) y STANBIO Laboratory para βOH (lote: 170558, vencimiento: 31/5/2023). Ambos son métodos cuantitativos y colorimétricos. Para realizar la verificación de la veracidad y precisión de los métodos, se utilizaron muestras del control de calidad externo de RIQAS de dos niveles diferentes (bajo o nivel 1 y alto o nivel 2). Para la linealidad, se utilizaron muestras de pacientes de concentración elevada: 2,4 mmol/L para NEFA y 3,23 mmol/L para βOH.
Procedimientos de verificación
Se utilizaron las guías del CLSI: la EP15-A3, para verificación de precisión intermedia (intralaboratorio) y repetibilidad (intracorrida), medidas como coeficiente de variación (CV), y para evaluar veracidad, medida en términos del sesgo o error sistemático. Se realizaron mediciones por quintuplicado durante cinco días consecutivos de los dos materiales de control externo de RIQAS.8 Las muestras seleccionadas tienen concentraciones que representan niveles de decisión médica, para βOH: 0,3 mmol/L (nivel 1) y 2,9 mmol/L (nivel 2), siendo el intervalo de referencia utilizado en nuestro laboratorio 0,03–0,3 mmol/L, y para NEFA: 0,7 mmol/L (nivel 1) y 1,6 mmol/L (nivel 2), siendo el intervalo de referencia utilizado en nuestro laboratorio 0,1–0,9 mmol/L. Ambos intervalos de referencia son los reportados en la bibliografía.
Se usaron las mismas muestras para precisión y veracidad utilizando los mismos resultados obtenidos en el protocolo de precisión para el protocolo de veracidad.
Para ninguno de los dos mensurandos, existen valores de variabilidad biológica como especificación analítica, es por eso que se seleccionó como requisito de calidad para NEFA el estado del arte: 29%, calculado a partir de 3 por el CV% del grupo interlaboratorio obtenido del reporte RIQAS del grupo que realiza la técnica colorimétrica de punto final. Por otro lado, para βOH, utilizamos como especificación analítica el criterio de aceptación RIQAS: 10,7% (conformado por las desviaciones diana de evaluación del rendimiento de RIQAS, reportado en los informes del control de calidad externo de RIQAS).
Se utilizó la guía CLSI EP6-A para verificar la linealidad. Para realizar el ensayo de linealidad, se prepararon una serie de diluciones a partir de una muestra de suero con concentración elevada. Para NEFA, la linealidad declarada por el fabricante es de 0,072 a 2,4 mmol/l, por lo que se eligió una muestra de 2,4 mmol/L. Para βOH, la linealidad declarada por el fabricante es de 0,0 a 8,0 mmol/L, y la muestra seleccionada fue de 3,23 debido a que es la concentración más alta con la que contamos, dado que no disponemos de muestras de pacientes ni RIQAS ni control comercial de un nivel semejante a 8,0 mmol/L.9 Con esa muestra de máxima concentración y una muestra de concentración “cero” (solución fisiológica), se realizaron tres diluciones (25%, 50% y 75%) con valores intermedios equidistantes; cada punto se valoró por triplicado. Para considerar la recta estadísticamente lineal, tiene que darse una ecuación de orden 1, donde el error de no linealidad es cero. En caso de que no sea estadísticamente lineal en el rango evaluado (ecuación de orden 2,3 y 4), se evalúa que sea clínicamente lineal. El error de no linealidad que se mida tiene que ser siempre menor del 50% del requisito de la calidad. Si el error de no linealidad es menor del 50% del requisito de la calidad, podemos decir que el método es clínicamente lineal, a pesar de no ser estadísticamente lineal.
Análisis de los datos
Para realizar el procesamiento estadístico de los datos, se utilizó una planilla de cálculo de Excel® diseñada para la verificación de los analitos acreditados por nuestro laboratorio por la norma IRAM ISO 15189:2023, disponible en el sistema documental de nuestro laboratorio QBnet, donde se evalúan outliers utilizando el método de Grubbs, precisión intracorrida e intralaboratorio y veracidad.
Outliers: se obtuvieron los límites de Grubbs como: media +/- G(crítico)*SD de los 25 datos. Se verificó que todos los valores arrojados en las corridas se encontraran dentro del intervalo hallado. El valor G(crítico) se obtiene de tabla teniendo en cuenta el N= número de corridas x número de repeticiones. Para N=25, G(crítico)=3,135.
Precisión:se compararon los CV% obtenidos en condiciones de repetibilidad y en condiciones de precisión intermedia con los CV% declarados por el fabricante para precisión. Si los CV% hallados eran menores que los del fabricante, la precisión era aceptada. Los CV% propios se obtuvieron realizando el análisis de varianza (ANOVA), un método de prueba de igualdad de tres o más medias poblacionales, por medio del análisis de las varianzas muestrales.
Veracidad: se estimó el sesgo relativo de la media obtenida por nuestro laboratorio con respecto al valor asignado a los materiales con concentración conocida; la media obtenida de los 25 resultados fue enfrentada al valor asignado del material seleccionado calculando el sesgo. Las muestras seleccionadas cuentan con una estimación de su valor asignado con un error aceptable. En primer lugar, se evaluó el sesgo estimado desde un punto de vista estadístico. Para ello, se calcularon los límites inferior y superior del intervalo de verificación del valor evaluado; si el valor de media obtenida estaba contenido dentro de estos límites la veracidad, se consideraba aceptada. Luego, se evaluó la consistencia de los datos para estudiar el sesgo desde un punto de vista clínico considerando el requisito de la calidad seleccionado para el procedimiento de medida de acuerdo con su uso previsto. Se utilizó como criterio de aceptación el error sistemático (es decir, el 50% de los requisitos de calidad definidos).
Linealidad: se utilizó el programa LINCHECKER con el que se obtuvieron las gráficas, la ecuación de la curva y el error de no linealidad. El estudio fue realizado cumpliendo con las normas éticas de la institución y de acuerdo con recomendaciones nacionales e internacionales (Declaración de Helsinki). No se consideró necesaria la aprobación del Comité de Docencia e Investigación, ya que forma parte de los procesos propios de nuestro laboratorio de análisis clínicos.
Resultados
Outliers
No se hallaron outliers en ninguno de los dos niveles de cada analito evaluado, ya que todas las repeticiones entraron en los límites definidos por el test de Grubbs. Para el nivel 1 de βOH, la media fue de 0,29 mmol/L, con un límite superior de 0,31 mmol/L y un inferior de 0,28 mmol/L. Para el nivel 2, la media fue de 2,92 mmol/L, con un límite superior de 2,99 mmol/L y un inferior de 2,85 mmol/L. Para el nivel 1 de NEFA, la media fue de 0,69 mmol/L, con un límite superior de 0,74 mmol/L y un inferior de 0,64 mmol/L. Para el nivel 2, la media fue de 1,64 mmol/L, con un límite superior de 1,71 mmol/L y un inferior de 1,56 mmol/L.
Precisión
Los resultados de CV% obtenidos fueron menores que lo especificado por el fabricante, por lo que se dio como aceptada la verificación realizada en los parámetros de precisión intracorrida e intralaboratorio para ambos analitos (Tabla I).
| Nivel | CV en condiciones de repetibilidad (%) | CV en condiciones de repetibilidad del fabricante (%) | CV en condiciones de precisión intermedia (%) | CV en condicio-nes de precisión intermedia del fabricante (%) | Aceptado? |
| NEFA | |||||
| 1 | 0,60 | 4,81 | 2,51 | 4,32 | Sí |
| 2 | 0,62 | 4,74 | 1,62 | 4,51 | Sí |
| βOH | |||||
| 1 | 1,54 | 1,70 | 1,62 | 5,20 | Sí |
| 2 | 0,56 | 1,40 | 0,78 | 1,70 | Sí |
Veracidad
Para NEFA, el sesgo entre laboratorio y la muestra de concentración conocida fueron rechazados estadísticamente en ambos niveles, por lo que se verificó que el sesgo hallado no sea clínicamente significativo. Para el caso de βOH, el sesgo fue aceptado estadísticamente y clínicamente para los dos niveles. Se logró realizar la verificación de la veracidad para ambos analitos (Tabla II y Tabla III).
| Nivel | Media (mmol/L) | Intervalo de verificación (mmol/L) | Aceptado |
| NEFA | |||
| 1 | 0,7 | 0,55-0,66 | No |
| 2 | 1,6 | 1,38-1,53 | No |
| βOH | |||
| 1 | 0,3 | 0,29-0,33 | Sí |
| 2 | 2,9 | 2,79-2,94 | Sí |
| Nivel | Sesgo (%) | Error sistemático aceptado (%) | Aceptado |
| NEFA | |||
| 1 | 11,85 | 14,5 | Sí |
| 2 | 11,98 | 14,5 | Sí |
| βOH | |||
| 1 | 4,83 | 5,35 | Sí |
| 2 | 1,92 | 5,35 | Sí |
Linealidad
En la Figura 1, se muestran los resultados de la linealidad para NEFA y, en la Figura 2, para βOH. Para NEFA, obtuvimos una línea recta (orden 1), lo que quiere decir que el método es estadísticamente lineal. Por ende, un método estadísticamente lineal siempre es clínicamente lineal, porque el error de linealidad es cero. Por otro lado, para βOH obtuvimos una recta de orden 3, por lo que no podemos decir que es estadísticamente lineal. Sin embargo, el error de no linealidad es de 3,54%, menor del 50% del requisito de calidad definido: 5,35%, por lo que es clínicamente lineal.
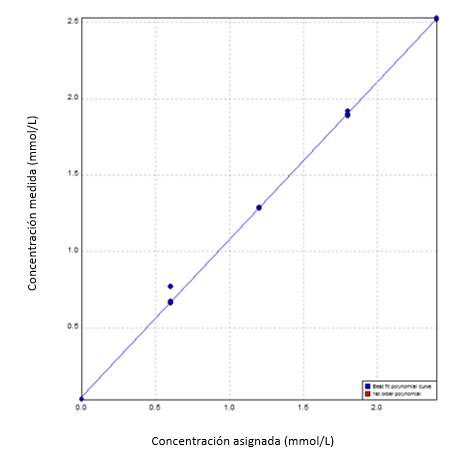
Figura 1.
Linealidad NEFA: concentración medida contra concentración asignada
Ecuación de la recta: y=0,04933 + 1,033 x
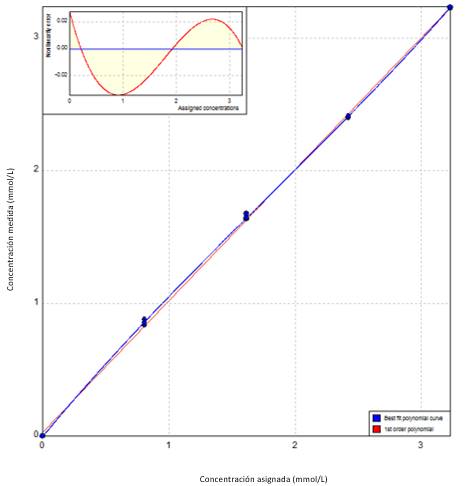
Figura 2.
Linealidad βOH: concentración medida contra concentración asignada
Ecuación que mejor se adapta: y= 0,0004143 + 1,145 x - 0,1122 x2 + 0,02084 x3
Discusión
La implementación de una nueva técnica en el laboratorio requiere la realización de la verificación, dado que es, además, requisito de la norma IRAM ISO 15189:2023 para la acreditación de un laboratorio. Los ensayos de verificación desempeñan un papel fundamental en la mejora constante de la actividad realizada en el laboratorio garantizando el cumplimiento de los estándares internacionales de calidad y las exigencias de los organismos de acreditación. Además, contribuyen a fortalecer la confiabilidad de los informes generados por los laboratorios de análisis clínico.
La verificación nos permitió la evaluación global de los resultados desde un punto de vista clínico además de estadístico, dado que una ventaja del protocolo EP15-A3 respecto de la versión A2 es que considera el requisito de la calidad para la evaluación global de los resultados.10,11
Se verificó la precisión intermedia y en condiciones de repetibilidad para ambos métodos de ambos analitos, ya que los CV% obtenidos para los dos niveles de control fueron menores que los CV% declarados por el fabricante.
La veracidad tanto estadística como clínicamente para βOH fue verificada. Si bien para NEFA la verificación de la veracidad no fue aceptada estadísticamente, sí lo fue clínicamente.
En cuanto a la linealidad, para NEFA, verificamos estadística y clínicamente la linealidad reportada por el fabricante, que alcanza hasta 2,4 mmol/L. Para βOH, aunque no disponemos de una muestra con una concentración tan alta como la declarada por el fabricante (8,0 mmol/L), pudimos confirmar la linealidad clínicamente hasta 3,23 mmol/L. Como proyecto de mejora, nos proponemos reevaluar la linealidad hasta el nivel máximo de 8,0 mmol/L si en el futuro disponemos de una muestra con una concentración cercana a este valor.
Tras evaluar todos los resultados obtenidos, nuestro laboratorio dio por verificados ambos métodos, y los implementó en el equipo automatizado de forma rutinaria.
Nuestro hospital realiza alrededor de 460 determinaciones de βOH y 220 de NEFA al año, por lo que automatizar los métodos de ambos analitos nos permite mejorar los tiempos de respuesta y atención de los pacientes optimizando los recursos, disminuyendo la demanda de personal, costos y tiempo. Además, al automatizar las metodologías, disminuimos el error que es inherente a la realización de las técnicas manuales (intra e interoperador) generando mayor confiabilidad y exactitud en los resultados y optimizando la etapa analítica.
La verificación de las especificaciones de desempeño declaradas por el fabricante para precisión y estimación del sesgo según los lineamientos generales de la guía CLSI EP 15 A3 de la CLSI, y la de la linealidad, según la guía EP6-A de ambos mensurandos representó el primer paso en la incorporación de estos a la rutina asistencial del laboratorio mediante equipos automatizados. El siguiente paso consiste en verificar los intervalos de referencia. Sin embargo, dada la naturaleza pediátrica del hospital, esta verificación presenta desafíos cuando se intenta realizar mediante el método directo. Para llevar a cabo la verificación de intervalos de referencia utilizando el método indirecto, se requiere un tamaño muestral mayor del que actualmente se dispone, por lo que se continuará utilizando el rango de referencia de bibliografía consensuado con los servicios médicos.
Referencia bibliográficas
1. Paoli A. Ketogenic Diet for Obesity: Friend or Foe? Int. J. Environ. Res. Public Health. 2014;11:2092–2107, https://doi.org/10.3390/ ijerph110202092
2. Newman JC, Verdin E. β -Hydroybutyrate: A Signaling Metabolite. Annu Rev Nutr. 2017; 37: 51–76, https://doi.org/10.1146/annurev-nutr-071816-064916
3. Albertia MJ, Agustinhob A, Argumedoc L, Armenob M, Blanco V, Bouquet S, et al. Recomendaciones para el manejo clínico pediátrico de la dieta cetogénica en el tratamiento de la epilepsia refractaria. Arch. argent. Pediatr. 2016;114(1):56-63, http://dx.doi.org/10.5546/aap.2016.56
4. Freeman JM, Kossoff EH, Hartman AL. The ketogenic diet: one de-cade later. Pediatrics 2007;119(3):535-43, https://doi.org/10.1542/ peds.2006-2447
5. Neal EG, Chaffe H, Schwartz RH, Lawson MS, et al. The ketogenic diet for the treatment of childhood epilepsy: a randomised controlled trial. Lancet Neurol 2008;7(6):500-6, https://doi.org/10.1016/s1474- 4422(08)70092-9
6. Guglielmone R, de Elías R, Kiener O, Collino C, Barzón S. Verificación de métodos en un laboratorio acreditado y planificación del control de ca-lidad interno. Acta bioquím. clín. latinoam. 2011 Jun [citado 2024 Ago 05],45(2): 335-347. Disponible en: http://www.scielo.org.ar/scielo.php?script=sci_arttext&pid=S0325-29572011000200012&lng=es.
7. IRAM-ISO 15189.Laboratorios de análisis clínicos Requisitos para la calidad y la competencia. Tercera edición, 2014.
8. EP15-A3 User Verification of Precision and Estimation of Bias; Approved Guideline —Third Edition (2014).
9. EP06-A Evaluation of the Linearity of Quantitative Measurement Proce-dures: A Statistical Approach; Approved Guideline (2003).
10. Abdel Ghafar M, El-Masry M. Verification of Quantitative Analytical Methods in Medical Laboratories. J Med Biochem. 2021;40(3):225–236, https://doi.org/10.5937/jomb0-24764
11. EP15-A2 User Verification of Performance for precision and trueness. Approved Guideline—Second Edition (2005)
Notas de autor
aldibariandaran@gmail.com
Información adicional
redalyc-journal-id: 651

