Artículos originales
DOI: https://doi.org/10.62073/n539ct33
Resumen: Introducción: La enfermedad por arañazo de gato es causada por la bacteria Bartonella henselae. Afecta principalmente a niños y suele manifestarse con adenopatías regionales autolimitadas. El método de diagnóstico consiste en la detección de inmunoglobulinas específicas por inmunofluorescencia indirecta. Quienes cursan la enfermedad habitualmente tienen títulos de IgG iguales o mayores de 1/256. Objetivos: Determinar la prevalencia de anticuerpos IgG e IgM anti - Bartonella henselae en pacientes que reúnen criterios epidemiológicos y/o clínicos, a la vez que correlacionar los datos epidemiológicos con los resultados de serología y estudiar diagnósticos diferenciales. Materiales y métodos: Se realizó un estudio retrospectivo, descriptivo y observacional de pacientes con sospecha de enfermedad por arañazo de gato en el período de marzo de 2016 a febrero de 2022. Se utilizó un kit comercial de inmunofluorescencia. Se analizaron las siguientes variables: edad, sexo, presencia de fiebre, contacto con gatos, edad de las mascotas, comienzo de los síntomas, presencia de adenopatías y su localización, tratamiento antibiótico al inicio y luego del resultado, otras pruebas serológicas. Resultados: Se procesaron 424 muestras de suero. Cursaba infección reciente el 43,8 %, con predominio masculino (58,2 %) y mediana de edad 7 años. El 94,6 % tenía adenopatías, la mayoría cervicales; 98,9 % tuvo contacto con gatos; 81,2 % recibió tratamiento empírico, principalmente, trimetoprima-sulfametoxazol. Se ajustó el esquema antibiótico a azitromicina en 76,4 %. Conclusiones: Debido a la elevada prevalencia en nuestra población, es importante realizar la medición de anticuerpos específicos para Bartonella henselae a fin de efectuar un diagnóstico diferencial oportuno en pacientes con adenopatías.
Palabras clave: enfermedad por arañazo de gato, Bartonella henselae, inmunofluorescencia indirecta, adenopatías.
Keywords: cat scratch disease, Bartonella henselae, indirect immunofluorescence, lymphadenopathy
Introducción
Bartonella henselae es el agente etiológico de la enfermedad por arañazo de gato (EAG). Se trata de un bacilo Gram negativo, pequeño, pleomórfico, del género Bartonella, con tropismo por glóbulos rojos. La enfermedad, en general, se presenta como una linfadenopatía regional autolimitada y afecta principalmente a los niños.
El reservorio natural de la bacteria es animal, principalmente, el gato, pero también se ha encontrado en el perro doméstico. La transmisión entre los gatos es a través de las pulgas (Ctenocephalides felis) y, en humanos, probablemente, a través de las heces de las pulgas luego del contacto con las mascotas1,2. Más del 90 % de los casos clínicos ocurre en personas que han estado en contacto con gatos, más a menudo gatos menores de un año, y la mayoría refiere haber sido arañada, mordida o lamida.
La presentación clínica típica comienza con la aparición de una pápula de color rojizo en el sitio de la lesión (arañazo o mordedura) que precede una a dos semanas la aparición de la adenitis regional. En pacientes inmunocompetentes, se trata de un cuadro de evolución subaguda, acompañado de otros síntomas inespecíficos, como fiebre, malestar, fatiga, sudores nocturnos y compromiso del estado general. Con menos frecuencia, puede acompañarse de dolor abdominal y hallazgos ecográficos como microabscesos hepatoesplénicos3,4,5. Las linfadenopatías cervical y axilar son las formas más comunes. Se han descrito presentaciones atípicas de la EAG; la más frecuente es el síndrome oculoglandular de Parinaud. En una minoría de casos, incluidos los huéspedes inmunodeprimidos, B. henselae puede causar infecciones sistémicas graves, como osteomielitis, endocarditis, angiomatosis bacilar o peliosis hepática. La linfadenopatía indolora prolongada puede simular neoplasias malignas y tuberculosis6,7,8.
Como B. henselae es una bacteria de difícil cultivo, se requiere el uso de exámenes serológicos para la detección de inmunoglobulinas específicas. El método más recomendado es la inmunofluorescencia indirecta (IFI), que permite dosar anticuerpos IgG e IgM con buena sensibilidad y especificidad. Los pacientes con la enfermedad, tanto adultos como niños y adolescentes, habitualmente tienen títulos de IgG iguales o mayores de 1:256. Títulos menores de 1:256 podrían representar una infección antigua o hallarse en el comienzo o final de la enfermedad9,10. En caso de sospecha de infección reciente, se recomienda repetir la prueba de 10 a 14 días después en busca de seroconversión o un aumento de los títulos. Una IgM positiva es indicativa de infección aguda, pero si es negativa, no descarta la enfermedad. En los casos en que no pueda estudiarse una segunda muestra, resulta de utilidad el dosaje de IgM11.
Existen otros métodos basados en tinciones específicas, como es la tinción de Warthin-Starry, o también, métodos moleculares, como la identificación del genoma de la B. henselae mediante PCR en muestras de biopsias de ganglios o piel. La principal desventaja de estos métodos es que se utilizan muestras invasivas12,13. La mayoría de los pacientes inmunocompetentes con un cuadro clínico de EAG experimenta resolución gradual de los síntomas y no suele ser necesario, según la mayoría de los autores, el empleo de antimicrobianos. En los casos en que se requiera tratamiento antibiótico, se recomienda azitromicina 500 mg por vía oral una vez al día durante 5 días14. En caso de pacientes intolerantes o alérgicos a azitromicina, se recomienda el uso de claritromicina, rifampicina o ciprofloxacina.
La bacteria B. henselae se encuentra ampliamente distribuida en todo el mundo, pero los estudios seroepidemiológicos en poblaciones humanas han mostrado resultados diversos. En Argentina, existen pocos trabajos publicados que estudian la enfermedad por arañazo de gato15,16.
El laboratorio participa de un programa de control de calidad externo, organizado por el Hospital Garrahan, que se inició en el año 2020 en busca de mejorar la calidad del diagnóstico y evaluar el nivel de concordancia entre los resultados de los distintos laboratorios participantes.
El objetivo de este trabajo fue determinar la prevalencia de anticuerpos IgG y/o IgM anti- Bartonella henselae en muestras de pacientes atendidos en el Hospital Nacional Profesor Alejandro Posadas que reunían criterios epidemiológicos y/o clínicos de enfermedad por arañazo de gato, a la vez que correlacionar datos epidemiológicos con los resultados serológicos y estudiar diagnósticos diferenciales.
Materiales y métodos
Se realizó un estudio retrospectivo, descriptivo, observacional de pacientes que consultaron por sospecha de EAG en el período de marzo de 2016 a febrero de 2022 en el Hospital Nacional Profesor Alejandro Posadas. Se incluyeron pacientes pediátricos y adultos, tanto de servicios externos como de internación, con edades entre 2 meses y 71 años. A cada paciente, se le tomó una muestra de sangre que fue remitida al laboratorio de Microbiología Molecular junto con la planilla epidemiológica completada por el médico. Se recolectaron los datos clínicos y epidemiológicos de las respectivas planillas y de las historias clínicas. Los pacientes fueron seleccionados según los siguientes criterios: 1- presencia de adenopatías regionales, 2- contactos con gatos y/o perros, 3- fiebre de origen desconocido.
Se determinó la presencia de anticuerpos séricos IgM e IgG específicos anti-Bartonella henselae por técnica de inmunofluorescencia indirecta (IFI), utilizando un kit comercial de Focus Diagnostic (Cypress, CA, USA) y siguiendo las instrucciones del fabricante (Figura 1). La sensibilidad esperada del ensayo es de 88 - 95 %. La unión del anticuerpo del paciente con el antígeno bacteriano se visualizó bajo microscopio de fluorescencia (Leica TM 750) con la aparición de fluorescencia verde manzana brillante sobre los bacilos fijados en el portaobjetos (Figura 2). Para dosaje de anticuerpos IgG, los sueros se procesaron en dilución basal de 1:64 y, a los sueros positivos, se les realizaron diluciones al medio hasta determinar sus títulos. En cada ensayo, se usó un control negativo y uno positivo. Se consideró infección reciente la detección de títulos IgM ≥ 1:20 y/o IgG ≥ 1:2569,10, y los pacientes que cumplían esa condición fueron incluidos en el grupo EAG. Los pacientes con serologías negativas para IgM y títulos de IgG menores de 1/256 se incluyeron en el grupo No-EAG. Algunos pacientes con serologías negativas para IgM y títulos de IgG menores de 1/256 también fueron incluidos en el grupo EAG por criterio médico. Los sueros con interferencias que dificultaban la observación del patrón específico de B. henselae se excluyeron del análisis de los resultados.
Se analizaron las siguientes variables: edad, sexo, presencia de fiebre, contacto con mascotas (gato/perro), edad de las mascotas (considerando cachorro al animal con edad menor de 1 año), comienzo de los síntomas, presencia de adenopatías y su localización, tratamiento antibiótico en el momento de la toma de muestra, rotación en el esquema antibiótico posterior al resultado serológico. Se registraron, además, pruebas serológicas para CMV, EBV y toxoplasmosis.
Análisis estadístico: se realizó un análisis según tipo de variables; con las variables continuas, se usaron medidas de tendencia central como la mediana y rango intercuartil, y con las variables discretas, medidas de frecuencia. Se aplicó un análisis estadístico comparativo mediante la U de Mann - Whitney con las variables continuas y chi cuadrado con las variables discretas, usando el programa InfoStat. Se consideró una diferencia estadísticamente significativa con p<0.05.
El protocolo del estudio fue aprobado por el Comité de Ética del Hospital Profesor Alejandro Posadas.
Resultados
Se procesaron 420 muestras de suero de pacientes, 75 de adultos y 345 de pacientes pediátricos. Se detectaron anticuerpos anti-Bartonella henselae (títulos ≥ 1/64) en 232 pacientes (55,2 %). Dentro del grupo EAG, se agruparon 184 pacientes; el 43,8 % incluía 12 pacientes que tenían criterio médico y títulos de IgG entre 1/64 y 1/128. Dentro del grupo No – EAG, se agruparon 236 pacientes (56,2 %). En el grupo EAG. el 38,7 % (29/75) eran adultos y 44,6% (154/345), niños. Ninguna muestra tuvo IgG negativa e IgM positiva; 3 pacientes presentaron títulos de IgG < 1/256 e IgM positiva (Figura 3).
Variables
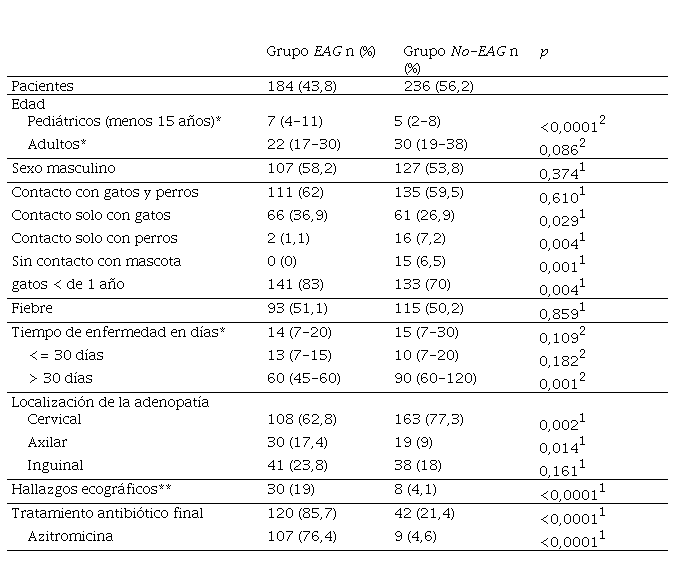
El sexo mostró predominio masculino en ambas poblaciones. La distribución del sexo y edad en los dos grupos se detalla en la Tabla I.
Presencia de adenopatías y su localización: El 91,2 % (383/420) de las solicitudes registraron la presencia de adenopatías en una o más localizaciones, el 7,4 % no tenía adenopatías y, en el 1,4 % de los casos, no se registró el dato. En el grupo EAG, 174 (94,6 %) pacientes presentaron adenopatías cuya localización más frecuente fue la cervical y, en 7 pacientes, estaba comprometido más de un sitio anatómico. La localización de estas se muestra en la Tabla I. No presentaron adenopatías 10 pacientes del grupo EAG; los mismos presentaron microabscesos hepáticos/esplénicos (3), síndrome febril prolongado (1), eritema nodoso (1), edema de papila (1), dolor abdominal (1), sin datos (3).
Tiempo transcurrido desde el inicio de los síntomas hasta la toma de muestra: En el grupo EAG, el 91,1 % (163/179) de los pacientes tenía un tiempo de evolución menor o igual a 30 días con una mediana de 13 días y, en el grupo No-EAG, el 77,2% (179/232) y la mediana fueron de 10 días. Por otro lado, aquellos pacientes que presentaron tiempo de evolución mayor de 30 días fueron 16 (8,9 %) del grupo EAG con una mediana de 60 días y 53 (22,8 %) en el grupo No-EAG con una mediana de 90 días.
Nexo Epidemiológico: El 96,3 % (393/408) de los pacientes estudiados manifestó haber tenido contacto con gatos y/o perros: 91,9 % (375/408), con gatos y 66,2 % (264/399), con perros. Se documentaron lesiones causadas por los gatos en 7 casos (6 del grupo EAG). Tuvieron contacto solo con perros 18 pacientes. En el 79,5 % (291/366) de los casos, se trataba de mascotas menores de 1 año (Tabla I).
Tratamiento antibiótico previo al diagnóstico: El 75,8 % (311/410) de los pacientes estudiados había recibido un esquema de tratamiento empírico previo a la toma de la muestra que incluía uno o más antibióticos. Los más utilizados fueron: trimetoprima-sulfametoxazol (57 %), betalactámico orales (46 %), clindamicina (16 %) y azitromicina (5 %). Del grupo de pacientes con EAG, el 81 % (145/179) tenía registro de haber recibido tratamiento antibiótico previo, y los esquemas reportados fueron similares en la población total.
Tratamiento antibiótico pos diagnóstico: En 120 pacientes del grupo EAG, se registró la utilización de algún antibiótico; en 25 de ellos, se indicó inicio de tratamiento antibiótico, en 82 se indicó una rotación del esquema antibiótico inicial y en 13 no hubo modificaciones. La azitromicina fue el principal antibiótico de elección (Tabla I).
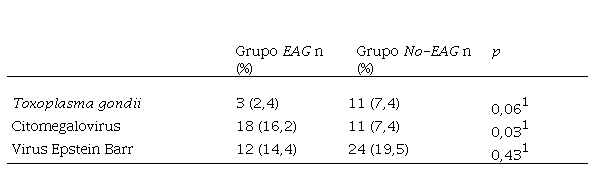
Otros estudios serológicos registrados: En 71 % del total de los pacientes, se registraron estudios serológicos para otras infecciones, de las cuales las más destacadas fueron el virus de Epstein-Barr (EBV), el citomegalovirus (CMV) y la toxoplasmosis (Tabla II). Además, un 25 % tuvo registros de estudios serológicos para sífilis y virus de inmunodeficiencia humana (HIV), de los cuales se obtuvieron 1 resultado positivo para HIV y 1 resultado positivo para sífilis, ambos, en pacientes adultos.
Otros diagnósticos registrados: En el 18,1 % de los pacientes, hubo registro de diagnósticos diferenciales distintos a la EAG. Entre las más frecuentes, destacamos: 12 faringitis estreptocócicas (una en el grupo EAG), 6 linfomas, 6 tuberculosis (una en el grupo EAG), 5 infecciones estafilocócicas, 2 toxocariosis, 1 brucelosis, 1 infección por COVID.
Discusión
Se detectó una alta prevalencia de anticuerpos anti- Bartonella henselae, tanto en niños como en adultos, en los pacientes estudiados por sospecha de enfermedad por arañazo de gato. En nuestro país, Armitano y col., en un estudio publicado en 2017 y utilizando el mismo kit diagnóstico, detectaron una seroprevalencia muy similar a la nuestra en pacientes pediátricos con sospecha clínica de la enfermedad (52 %). La mediana de edad de su población estudiada fue de 5 años, con predominio del sexo femenino de 54 %15. Nuestra población pediátrica tenía una mediana de 6 años y predominio del sexo masculino (54 %).
En relación con trabajos de otros países, en Perú, se reportó una muy elevada prevalencia en niños con adenitis regional (81,1 %) y una mediana de edad de 7 años17. En Croacia, se dio una seroprevalencia de 35,8 % tanto en niños como adultos con linfoadenopatías18. En Polonia, un estudio mostró una seropositividad de B. henselae de 57 % en pacientes con linfoadenopatías19.
Si bien las adenopatías cervicales fueron las más frecuentes, son las de localización axilar las que tienen una diferencia significativa con el grupo No-EAG. También presenta diferencia significativa el hallazgo ecográfico de microabscesos en hígado y bazo. Es importante tener en cuenta que no siempre la manifestación de esta enfermedad es con aparición de adenopatías, sino que puede manifestarse con dolor abdominal, síndrome febril prolongado, eritema nodoso y edema de papila.
Se documentó fiebre en la mitad de los casos de EAG, sin una diferencia con el grupo No-EAG, por lo que se considera un signo inespecífico.
En escasas oportunidades, pudo documentarse la presencia de arañazo u otras lesiones en los pacientes que acudieron a la consulta, no obstante, el contacto con gatos cachorros es el nexo epidemiológico fundamental y mostró una diferencia estadísticamente significativa con respecto al contacto con perros y gatos adultos.
En el grupo EAG, es más frecuente la consulta temprana con lo cual las presentaciones de más de 30 días dan indicio de otras patologías, como en el caso del grupo No-EAG, que, en su mayoría, son patologías de origen no infeccioso y sin una presentación aguda.
La detección de anticuerpos IgM es indicio de infección reciente y, en nuestro trabajo, aportó al diagnóstico de EAG en los casos en que el título de la IgG era menor de 1/256, sin embargo, hay reportes en los que sólo es positiva la IgM15. Además, todos los casos con títulos menores que el punto de corte e IgM negativa no fueron estudiados con una segunda muestra, como es indicado para detectar aumento de título, lo cual es una debilidad de nuestro estudio. En esos casos, el criterio clínico definió el diagnóstico.
Se pudo constatar un uso importante de antibioticoterapia. Esto se debe a la recomendación de cubrir con betalactámicos las infecciones bacterianas ante adenomegalias sin foco primario. En el grupo EAG, donde se constató un ajuste terapéutico posterior al resultado de la serología, se pudo observar que el antibiótico más usado fue la azitromicina y luego, la trimetoprima-sulfametoxazol. En este sentido, el tratamiento recomendado para la EAG, si bien está discutido y basado en una evidencia no conclusiva, es azitromicina como antibiótico principal (vía oral por 5 días en linfadenitis) y como alternativa, azitromicina más rifampicina en caso de EAG atípica o trimetoprima sulfametoxazol, coincidiendo con lo hallado en nuestro trabajo.
Conclusiones
Con base en los resultados encontrados, se concluye que las adenopatías regionales de comienzo agudo, especialmente en la población de niños que presenten además el antecedente epidemiológico de contactos con gatos pequeños, deben ser estudiadas para la búsqueda de EAG. La confirmación rápida y confiable de EAG puede evitar procedimientos de diagnóstico innecesarios, costosos e invasivos. Por lo tanto, es importante un diagnóstico preciso y oportuno20 para ajustar el tratamiento, realizar un diagnóstico diferencial y para determinar presencia de coinfecciones21.
Conflicto de intereses
Los autores declaran no poseer conflictos de interés.
Referencias bibliográficas
1. Reynolds MG, Holman RC, Curns AT, O'Reilly M, McQuiston JH, Steiner CA. Epidemiology of cat-scratch disease hospitalizations among children in the United States. Pediatr Infect Dis J 2005;24(8):700-4, https://doi.org/10.1097/01.inf.0000172185.01939.fc
2. Cheslock ME, Embers ME. Human Bartonellosis: An Underappreciated Public Health Problem? Trop Med Infect Dis 2019;4(2):69, https://doi.org/10.3390/tropicalmed4020069
3. Dunn MW, Berkowitz FE, Miller JJ, Snitzer JA. Hepatosplenic cat-scratch disease and abdominal pain. Pediatr Infect Dis J. 1997;16(3):269-72, https://doi.org/10.1097/00006454-199703000-00003
4. Del Pozo AA, Angulo-Cruzado M, Amenero-Vega R, Álvarez-Lulichac A, Fernández-Cosavalente H, Barboza-Meca J, et al. Hepatosplenic abscesses in an immunocompetent child with cat-scratch disease from Peru. Ann Clin Microbiol Antimicrob. 2019;18(1):23, https://doi.org/10.1186/s12941-019-0322-0
5. Luciano A, Rossi F, Bolognani M, Trabucchi C. Microascessi epatici e splenici nella malattia da graffio di gatto. Caso clinico [Hepatic and splenic micro-abscess in cat scratch disease. Report of a case]. Pediatr Med Chir. 1999;21(2):89-91. PMID: 10570789
6. Carithers HA. Cat-scratch disease. An overview based on a study of 1,200 patients. Am J Dis Child 1985;139:1124–33, https://doi.org/10.1001/archpedi.1985.02140130062031
7. Margileth AM. Cat scratch disease. Adv Pediatr Infect Dis 1993; 8:1–21.
8. Spickler, AR. 2012. Cat Scratch Disease and Other Zoonotic Bartonella Infections. Disponible en: https://www.cfsph.iastate.edu/diseaseinfo/factsheets/
9. Eymin LG, Zapata PA, Andrade AM, Aizman SA, Rojas O , Rabagliati BR. Enfermedad por arañazo de gato: Características clínicas y de laboratorio en pacientes adultos hospitalizados por fiebre o adenopatías. Rev. méd. Chile 2006;134(10):1243-1248. Disponible en: https://www.scielo.cl/scielo.php?script=sci_arttext&pid=S0034-98872006001000005
10. Ferrés M, Abarca K, Prado P, Montecinos L, Navarrete M, Vial P. Prevalencia de anticuerpos contra Bartonella henselae en niños, en adolescentes y en una población de riesgo ocupacional en Chile. Rev. méd. Chile 2006;134(7):863-867. Disponible en: https://www.scielo.cl/scielo.php?script=sci_arttext&pid=S0034-98872006000700009
11. Abarca K, Winter M, Marsac D, Palma C, Contreras AM, Ferrés M. Exactitud y utilidad diagnóstica de la IgM en infecciones por Bartonella henselae. Rev. chil. infectol. 2013; 30(2):125-128, https://doi.org/10.4067/s0716-10182013000200001
12. Lamps LW, Scott MA. Cat-scratch disease: historic, clinical, and pathologic perspectives. Am J Clin Pathol 2004;121 Suppl 1: S71-80, https://doi.org/10.1309/jc8ym53l4e0l6pt5
13. Sulaiman ZI, Samra H, Askar G. Cat Scratch Disease: An Unusual Case of Right Inguinal Lymphadenitis Due to Bartonella henselae. Cureus. 2023 Aug 28;15(8):e44280, https://doi.org/10.7759/cureus.44280
14. David H Spach, MD; Sheldon L Kaplan, MD.Treatment of cat scratch disease. Uptodate 2011.
15. Armitano R, Lisa A, Martínez C, Cipolla L, Lachini R, Prieto M. Bartonella henselae: evidencia serológica en pacientes pediátricos con sospecha clínica de enfermedad por arañazo de gato. Rev Argent Microbiol. 2018; 50(4):365-368, https://doi.org/10.1016/j.ram.2017.10.004
16. Deregibus MI, Bagnara EI, Buchovsky A. Enfermedad por arañazo de gato: experiencia en un hospital pediátrico de tercer nivel. Arch Argent Pediatr. 2023;121(1):e202202592, https://doi.org/10.5546/aap.2022-02592.eng
17. Miranda-Choque E, Candela-Herrera J, Díaz-Pereda J, Fernández-Vega A, Kolevic-Roca L, Patiño-Gabriel L, et al. Bartonella henselae en niños con adenitis regional atendidos en un hospital nacional del Perú, 2012. Rev Peru Med Exp Salud Publica 2014; 31(2):274-7, http://www.scielo.org.pe/scielo.php?script=sci_arttext&pid=S1726-46342014000200012
18. Vilibic-Cavlek T, Karlovic-Martinkovic D, Ljubin-Sternak S, Tabain I, Persic Z, Mlinaric-Galinovic G. High prevalence of Bartonella henselae and Bartonella quintana antibodies in Croatian patients presenting with lymphadenopathy . Pol J Microbiol. 2012; 61(4):315-7. PMID: 23484416
19. Podsiadły E, Sokołowska E, Tylewska-Wierzbanowska S. Seroprevalence of Bartonella henselae and Bartonella quintana infections in Poland in 1998-2001. Przegl Epidemiol 2002;56 (3): 399-407. PMID: 12608089
20. Metzkor-Cotter E, Kletter Y, Avidor B, Varon M, Golan Y, Ephros M, et al. Long-Term Serological Analysis and Clinical Follow-Up of Patients with Cat Scratch Disease. Clin Infect Dis 2003; 37: 1149–54, https://doi.org/10.1086/378738
21. Baranowski K, Huang B. Cat Scratch Disease. [Updated 2020 Jun 23]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2020. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK482139/
Notas de autor
amagda66@yahoo.com.ar
Información adicional
redalyc-journal-id: 651