Resumen: Los tipos de HPV de alto riesgo (VPH-AR) más comúnmente aceptados en todo el mundo son el 16 y el 18, implicados en el 70% de las lesiones cervicales. La implementación del tamizaje desde los años 70 ha reducido la prevalencia de esta patología. Sin embargo, en los países subdesarrollados, aún existen muchos problemas para poner en funcionamiento el tamizaje correcto en toda la población. Objetivos: Describir la distribución de los genotipos de VPH a partir de muestras exo/endocervicales desde 2010 hasta 2020, y analizar la correlación citológica entre las diferentes patologías ginecológicas. Materiales y métodos: Se analizaron 316 frotis. La citología se realizó según Bethesda 2010. Se llevó a cabo la genotipificación del VPH, y se obtuvieron los siguientes resultados: alto riesgo (AR): 117; bajo riesgo (BR): 76; detectables: 47; indetectable: 44; posible alto riesgo: 26; desconocido: 6. Respecto de la distribución, se detectaron: VPH 16 (34), 6(28), 11(21), 58(20), 53(17), 33(12), 66(11), 31(11), 54(7), 61-62-81 (6). 160 de 316 tenían citodiagnóstico: 31 tenían VPH-BR y 34, VPH-AR sin lesión visible; 23 inflamatorias tenían VPH-BR (12) y VPH-AR (11); 46 LSIL (lesión escamosa intraepitelial de bajo grado), con 21 BR, y 25 AR; 11 HSIL (lesión escamosa de alto grado) con 7 HR; 14 ASCUS (significado indeterminado) con 7 HR; Conclusión: Se encontró mayor prevalencia de VPH-AR, con predominio de 16, 58, 33, 66, 31, 45 y 56. El VPH 18 no presentó una frecuencia elevada. Las muestras citológicas sin lesiones visibles, inflamatorias, con LSIL y VPH-AR son las que merecen seguimiento, y la citología es importante aquí debido a las limitaciones de la sola información del genotipo.
Palabras clave: vph, citología, lsil, hsil, carcinoma de cuello uterino, genotipificación.
Abstract: Background: The most widely recognized high-risk HPV types (HR-HPV) are 16 and 18, which are involved in 70% of cervical lesions. The prevalence of this pathology has been reduced thanks to the implementation of screening since the 1970s. However, in underdeveloped countries, there are still many problems to implement the correct screening in the whole population. Objectives: To describe the prevalence of HPV genotypes from 315 cervical smears collected from 2010 to 2020, and to analyze the cytological correlation between the different pathologies. Materials and methods: Cytology was performed according to Bethesda 2010. HPV genotyping was performed. Results: Genotyping: High risk (HR): 117; Low risk (LR): 76; Detectable: 47; Undetectable: 44; Possible high risk: 26; Unknown: 6. Prevalence: HPV 16 (34), 6 (28), 11 (21), 58 (20), 53 (17), 33 (12), 66 (11), 31 (11), 54 (7), and 61-62-81 (6). A total of 160 of 316 could be diagnosed: 31 had HR-HPV and 34 had HR-HPV without visible lesion; 23 inflammatory had HR-HPV 12 and HR-HPV 11; 46 had low-grade squamous intraepithelial lesion (LSIL), with 21 LR, and 25 HR; 11 had high-grade squamous lesion (HSIL), with 7 HR; 14 had undetermined significance (ASCUS) with 7 HR. Conclusion: Higher prevalence of HR-HPV was observed, with predominance of HPV 16, 58, 33, 66, 31, 45 and 56. HPV 18 did not present high frequency. Cytological specimens without visible lesions, inflammatory, LSIL, and HR-HPV warrant follow-up, and cytology is important because of the limitations of genotypic information alone.
Keywords: hpv, dytology, lsil, hsil, cervical cancer, genotyping.
Artículos originales
Distribución de genotipos de virus de papiloma humano en muestras citológicas: seguimiento de 10 años en la ciudad de Mar del Plata, Argentina.
Distribution of human papillomavirus genotypes in cytological samples: 10-year follow-up in the city of Mar del Plata, Argentina.
La infección cervical por papilomavirus (VPH) es una de las enfermedades de transmisión sexual más frecuentes en todo el mundo. La mayoría de las mujeres se infectan poco después de iniciar la actividad sexual. El pico de prevalencia se da en mujeres menores de 25 años, y las infecciones por VPH, a esta edad, suelen ser transitorias, pero hay un segundo pico en mujeres, a los 40 años, que coincide con la edad de mayor incidencia de cáncer de cuello uterino1.
Se ha demostrado que la infección por virus del papiloma humano de alto riesgo (VPH-AR) está relacionada con el desarrollo de cáncer de cuello uterino, y la persistencia del virus en las lesiones intraepiteliales de cuello uterino (LEI) es la base para la aplicación de las pruebas de VPH para el cribado y manejo de las pacientes. Existen mecanismos conocidos para la progresión de lesión benigna a carcinomas; el más famoso es el aumento de las proteínas E6 y E7, pero también hay más, relacionados con las interacciones de estas dos oncoproteínas con la transición epitelio-mesénquima y la activación de vías de señalización supervivientes2,3,4. La mayoría de las infecciones por VPHAR se resuelven espontáneamente y no progresan hacia el desarrollo de displasia o cáncer. Los tipos clásicos de VPH-AR son el VPH-16 y el VPH-18, pero, recientemente, se han identificado muchos otros tipos de VPH-AR en SIL o cáncer de cuello uterino.
Las respuestas inmunitarias celulares del huésped parecen ser la causa de la regresión espontánea de las lesiones cervicales. En los seres humanos, la mayoría de las lesiones desaparecen entre 6 y 12 meses después de su identificación5.
Los viriones del VPH se producen en las capas diferenciadas del epitelio escamoso. En la mayoría de los casos, el virus permanece episomal, y los viriones se liberan cuando las capas externas se descaman. En un pequeño número de casos, los tipos de alto riesgo del VPH (VPHAR) se integran en el ADN celular y producen una infección persistente. Cuando el VPH se encuentra en su estado episomal, la proteína E2 suprime la expresión de las oncoproteínas, E6 y E76. Se ha encontrado E2 en células endocervicales normales en biopsias en las que posteriormente se detectó el genoma del VPH 16. Estos hallazgos concuerdan con los informes que sugieren que E2 es importante durante las primeras etapas de la carcinogénesis del cuello uterino y que su desaparición se corresponde con la aparición de E7 7. Si bien las guías de la OMS recomiendan el tamizaje primario (test de VPH) como la mejor estrategia, no debe descartarse la utilización de la citología para el seguimiento de las pacientes portadoras de VPH-AR en países en vías de desarrollo, teniendo en cuenta el costo de los métodos moleculares. Esto es posible porque la transición de lesiones escamosas de bajo grado (LSIL), que ya se ha dicho revierte en la mayoría de las mujeres, a lesiones escamosas de alto grado (HSIL) es detectable cuando los frotis se tiñen con el método de Papanicolaou y presentan características celulares que permiten diferenciar unas de otras. Además, la evolución a HSIL puede tardar años, más aún cuando existe la posibilidad de evolucionar al carcinoma cervical, que puede aparecer más de una década después desde la presentación de LSIL8,9.
Conocer el genotipo del VPH podría ser una herramienta útil para comprender también la correlación entre su prevalencia y las diferentes lesiones. Los VPH-AR más comúnmente aceptados en todo el mundo son el 16 y el 18, implicados en el 70% de las lesiones cervicales; el otro 30% incluye otros VPH-AR como el 31, 33, 35, 45, 51, 52, 56, 58, 59, 66 y 68, mientras que los VPH-AR más comunes son el 6 y el 1110.
Cerca del 80% del cáncer cervicouterino mundial ocurre en países en vías de desarrollo. La implementación del tamizaje citológico y colposcópico desde principios de los años 70 ha reducido la prevalencia de esta patología debido al reconocimiento de lesiones preneoplásicas11. Sin embargo, en los países subdesarrollados y en vías de desarrollo, todavía existen muchos problemas para implementar el correcto cribado en toda la población, y esto se debe a muchas razones: la principal es la distribución de los centros médicos y la posibilidad de asistir a uno.
Una de las características más importantes en el cribado es la forma correcta de obtener los frotis, y, para ello, es obligatorio encontrar células metaplásicas, y/o células endocervicales. Estas son el control de calidad para una buena práctica12. Un frotis satisfactorio es obligatorio, y el pronóstico se basa no solo en eso, sino también en la experiencia del citólogo, el genotipo, los factores de riesgo e incluso en predictores más avanzados como la técnica AgNOR13.
En Argentina, la vacuna preventiva contra el VPH está implementada desde 2011 para todas las niñas de 11 años e incluye los cuatro genotipos: 6, 11, 16 y 18. La prevalencia de VPH reportada en nuestro país muestra resultados similares para el genotipo 16, que es el más frecuente, pero los que le siguen son el 58, 18, 31, 33 y 35, en diferentes proporciones14,15,16. Debido a la gran extensión de nuestro territorio, es necesario establecer la variación de genotipos por provincias o incluso ciudades17.
Los objetivos de este estudio fueron describir la distribución de los genotipos del virus de papiloma humano a partir de muestras exo/endocervicales, desde el año 2010 hasta 2020, y analizar la correlación citológica entre las diferentes patologías premalignas y malignas ginecológicas y sus implicaciones clínicas.
Se incluyeron
Se incluyeron muestras de pacientes que asistieron a controles ginecológicos regulares, que contaban con el estudio citológico realizado dentro de las tres semanas previas a la toma de muestra, y que dieron su consentimiento voluntario por escrito para participar en este estudio. Las muestras debían ser de suficiente calidad como para permitir la genotipificación de HPV, es decir, que se hubiera verificado una correcta extracción de ADN. Se excluyeron las muestras que no cumplían con lo mencionado previamente.
Las muestras eran de pacientes de la ciudad de Mar del Plata y fueron tomadas por personal técnico especializado en Fares Taie Biotecnología. El motivo de consulta era la prescripción médica para tipificación de virus de papiloma humano. Se recibieron un total de 316 muestras en un período de 10 años.
El procedimiento de citología vaginal se realizó según lo descrito previamente por nuestros grupos; surge de las conclusiones de Bethesda y de numerosos papers donde se emplean los algoritmos de seguimiento de las pacientes. Incluye la presencia de células endocervicales y/o metaplásicas escamosas para una evaluación satisfactoria, y se excluyeron las muestras que presentaban cuellos uterinos con sangrado profuso12 ,18.
El ADN se extrajo de muestras clínicas cervicovaginales utilizando el kit comercial DNA High Pure PCR Template preparation Kit (Roche), siguiendo las instrucciones del fabricante.
Todas las amplificaciones de ADN por qPCR se realizaron en un termociclador Rotor Gene (Qiagen, Hilden, Alemania) utilizando Eva Green ® como colorante fluorescente intercalante (KAPA HRM QUICK; Biosystems, Woburn, MA).
Para corroborar una correcta extracción del ADN, se amplificó el gen actina beta con los siguientes cebadores: fw 5'-TGCGTGACATTAAGGAGAAG-3' y actina beta rv 5'-GCTCGTAGCTCTTCTCCA-3', que amplifica un fragmento de 99 pb de actina beta humana19.
Los genotipos del VPH se determinaron mediante pPCR utilizando los sistemas de cebadores MY09/MY11 y GP5+/GP6+20.
Los productos de amplificación se sembraron en un gel de agarosa al 2%, y se purificaron con el AccuPrep ®PCR/ Gel Purification Kit. La reacción de Sanger se llevó a cabo utilizando el kit BigDye® Terminator v3.1 Cycle Sequencing, y la purificación de la misma PCR se realizó con el kit ZR-96 DNA Sequencing Clean-up Kit ™ (ZYMO RESEARCH) e inyección en el analizador genético Applied Biosystems 3500.
Los electroferogramas obtenidos se analizaron para determinar el genotipo de cada muestra. Las similitudes de secuencias se determinaron mediante la herramienta Basic Local Alignment Search Tool (BLAST) (https://blast.ncbi.nlm.nih.gov/Blast.cgi) del National Center for Biotechnology Information (NCBI).
Los posibles resultados de los estudios moleculares son: DETECTABLE, cuando se detecta ADN del virus y se identifica el genotipo; DETECTABLE NO GENOTIPIFICABLE, en los casos en los que el ADN viral es detectado, aunque su carga es muy baja o no es posible determinar el genotipo por secuenciación a causa de una posible coinfección y, por último, NO DETECTABLE, en los casos en los cuales no se encuentra ADN viral en la muestra.
Los datos recolectados se presentaron como variables categóricas, como la presencia o ausencia de diferentes genotipos de HPV, y se expresaron en frecuencias y porcentajes. Las variables continuas, como la edad de las pacientes, se agruparon en rangos.
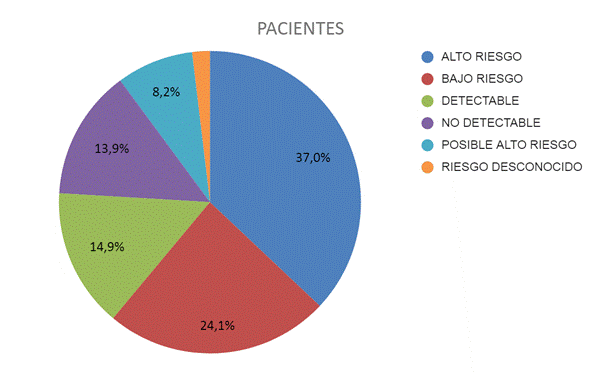
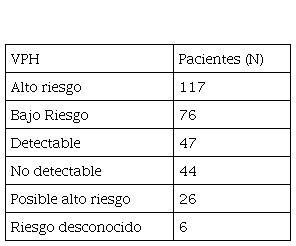
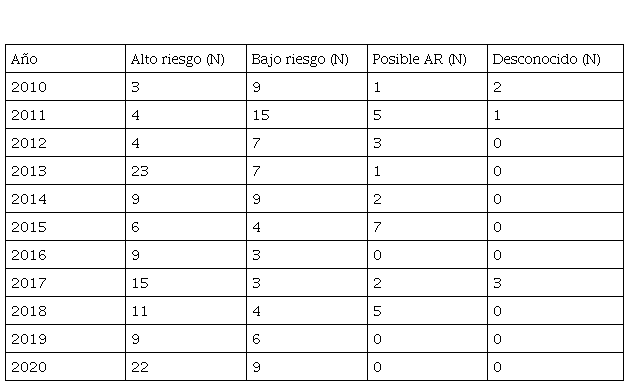
Se analizó a todas las pacientes, y las distribuciones se resumen en la Tabla 1 y la Figura 1. Es importante mencionar la gran cantidad de alto riesgo, en comparación con el resto, e incluso hay que tener en cuenta los 26 casos incluidos en el grupo de "posible alto riesgo". Esto se analiza también en el apartado citológico, que se puede representar por lesión.
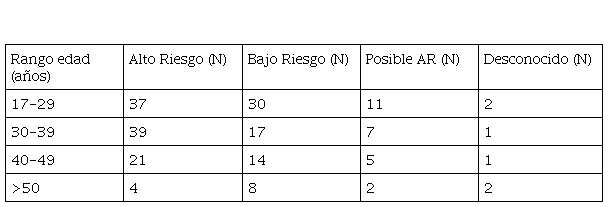
Como se mostró anteriormente, la Figura 1 indica el porcentaje de cada grupo. Sabemos que la mayor frecuencia de cáncer de cuello uterino se sitúa en torno a los 30 años, por lo que las mujeres se agruparon por edades en la Tabla 2 y la Figura 2.
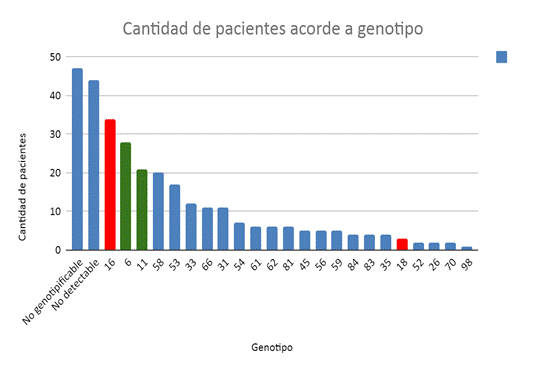
Una de las características más importantes de la infección por VPH es la prevalencia de los genotipos que se pueden encontrar en un determinado país, y la correlación entre sí es de alto o bajo riesgo. Si distribuimos el número de pacientes portadoras de un mismo genotipo, podemos ver la frecuencia de cada uno en la Figura 2. La primera figura muestra la distribución de VPH-AR, y la Figura 2, la distribución en nuestra ciudad, que es importante comparar directamente con otras ciudades e incluso países. La mayoría son "no genotipables" (lo mismo que DETECTABLE en la Figura 1) y "no detectables", y aun así, sigue habiendo más casos de VPH-AR, de los que el VPH 16 es el más frecuente.
Para la evaluación de la distribución por riesgo, considerando todo el período, encontramos un mayor predominio de los genotipos de alto riesgo entre los años 2010 y 2020, como se muestra en la Tabla 3.
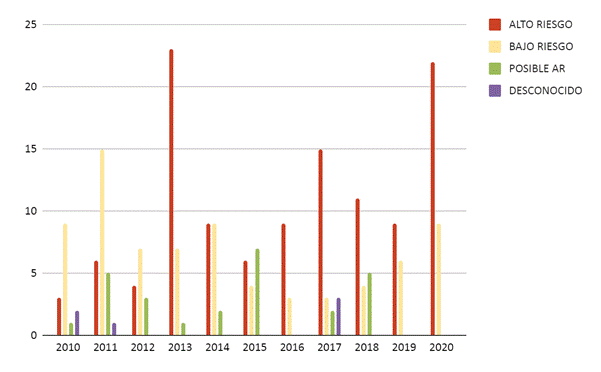
En la Figura 3, podemos ver la frecuencia por año, con un claro predominio del alto riesgo a través del tiempo, y esto es una consideración porque es el mismo lapso en que se implementó la vacuna.
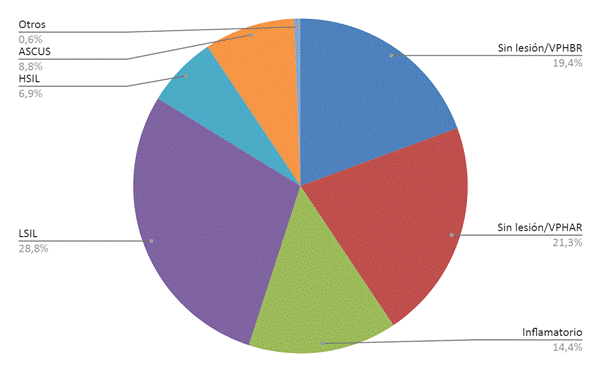
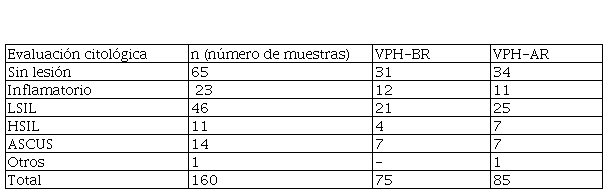
Un total de 160 frotis pudieron ser diagnosticados por citología. Con una clasificación según sus cambios morfológicos, se han distribuido en 7 grupos, como muestran la Figura 4 y la Tabla 4:
1- Frotis sin lesión, portadores de VPH de bajo riesgo: 31 casos. 31 de las pacientes sin lesión cervical y con prueba de Papanicolaou normal estaban infectadas por VPH de bajo riesgo. Este grupo de pacientes se denomina portadoras sanas, y requieren un seguimiento en 3 años.
2- Frotis sin lesión, portadores de VPH de alto riesgo: 34 casos. 34 pacientes, que representan el 21% de todos los frotis, no tienen lesión y tienen un VPH de alto riesgo. Este grupo debe tener un seguimiento estricto cuando se realiza el cribado, con un control de 12 meses18.
3- Frotis con lesiones inflamatorias: 23 casos: a) VPH de bajo riesgo: 12 casos; b) VPH de alto riesgo: 11 casos (un VPH 53). Este grupo representa el 15%. Casi la mitad de las pacientes son portadoras de un VPH de alto riesgo. Aunque todas ellas no presentan alteraciones virales anormales, estas 11 mujeres, según el resultado de la tipificación, deberían ser controladas mediante citología y colposcopía.
4- LSIL: 46: a) VPH de bajo riesgo: 21 casos; b) VPH de alto riesgo: 25 casos. Este porcentaje es del 31,5% (46/146). El 53% de los LSIL son portadores de un VPH de alto riesgo; este es el caso más frecuente en el que las pacientes pueden evolucionar a HSIL. Alrededor del 12% de los LSIL globales evoluciona a HSIL si no hay tratamiento, y se recomienda el control citológico/colposcópico y/o la biopsia21. El 47% restante nunca evolucionará a una patología peor, y casi todos ellos se eliminarán mediante inmunología celular.
5- HSIL: 11: a) VPH de bajo riesgo: 4 casos; b) VPH de alto riesgo: 7 casos. Este grupo representa casi el 6,4%. Del total de pacientes con HSIL, el 36% tiene un VPH de bajo riesgo; esta lesión no está asociada al virus de bajo riesgo, por lo que es obligatorio confirmar, ya que podría tratarse de otro tipo de lesión o de una coinfección con un genotipo de alto riesgo.
El grupo más peligroso está representado por el 64% de las mujeres con HSIL y VPH de alto riesgo. Podría tratarse de dos subclasificaciones de la neoplasia intraepitelial cervical, CIN, según Richard: la menos grave, llamada CIN2, y la peor, CIN3, o carcinoma in situ. Ambas tienen integración viral del genoma (y la mitad de las CIN2 progresa a CIN3), y una gran tendencia a culminar en carcinoma invasivo. Los tratamientos son la biopsia, el LEEP y la conización.
6- ASCUS: 14: a) VPH de bajo riesgo: 7 casos; b) VPH de alto riesgo: 7 casos. ASCUS (Atypical squamous cells of undetermined significance) tiene más posibilidades de ser reactivo que neoplásico. Este es un significado dudoso en citología. En nuestro trabajo, tenemos la misma proporción de VPH de bajo y alto riesgo. Según las recomendaciones del consenso de Bethesda, estas pacientes deben someterse a una biopsia para definir el tipo de lesión que presentan y el tratamiento posterior.
7- Otros: 1: Hubo un caso de carcinoma vulvar in situ. Este frotis tenía un VPH 58, que es un VPH de alto riesgo. Se trata de una lesión muy infrecuente, más aún en una mujer de 23 años, que requiere una intervención quirúrgica.
La infección por el VPH y el elevado número de cánceres de cuello uterino siguen siendo un problema sanitario. El manejo de esta patología ha mejorado desde la implantación del cribado citológico, pero, en determinados países una distribución no equitativa de la atención médica hace que la aparición de HSIL o incluso de carcinomas cervicales sea muy frecuente, a pesar de todo el conocimiento que hay sobre este tema.
Tras una evaluación de un período de 10 años, comprobamos que la mayoría de las pacientes que presentaban una colposcopía o una colpocitología anormales llegaban a nuestro laboratorio y se sometían a un estudio genotípico. El primer resultado importante fue la mayor prevalencia de VPH-AR, en general22, una condición obligatoria para el desarrollo del cáncer, pero no la única. Esta clase de pacientes son las que necesitan un seguimiento anual23.
Dividido por rango de edad, también encontramos que el VPH-AR es prevalente en todas las mujeres, excepto en las mayores de 50 años, lo cual también concuerda con la bibliografía. Mientras el carcinoma cervical es un cáncer de pacientes jóvenes, el carcinoma endometrial es más común en mujeres menopáusicas24.
Como se muestra en la Tabla 3, la mayoría de las pacientes tuvieron un resultado detectable no genotipificable, lo que significa que, con este método, no se identificó ningún genotipo debido a la baja concentración de VPH en las muestras o a la coinfección. Es posible que, en algunas de las pacientes en las que se identificó el genotipo, hubiera coinfección, pero la metodología de secuenciación Sanger, en estos casos, brinda información del genotipo mayoritario. El resultado no detectable se debe a que no hay ADN, y esto es posible porque algunas de nuestras pacientes estaban en un control postratamiento o eran sospechosas de infección.
Si bien la metodología empleada presenta sus limitaciones, permite el estudio de la presencia de todos los genotipos de HPV existentes y no de una cantidad acotada, como otros métodos comerciales disponibles.
De los que resultaron positivos, el pico de distribución está dado por el VPH 16, que también es conocido mundialmente por ser responsable, junto con el VPH 18, del 70% de las lesiones cervicales. Sin embargo, en nuestro orden de frecuencia, encontramos que, en Mar del Plata, Argentina, el VPH 16 es seguido por VPHA-R como el 58, 33, 66, 31, 45 y 56. Si bien estos virus presentes en lesiones premalignas de cuello uterino no son los que se detectan mayoritariamente en el cáncer de cuello uterino, su presencia no puede ser subestimada25,26,27.
Desde 2013, hay una mayoría permanente de VPH-AR, por lo tanto, debe ser considerado con cautela si hay un factor que lo está aumentando en esta población y que debe ser estudiado. Una consideración en sí misma es la vacunación, donde podría haber un desplazamiento de genotipos, puesto que disminuyen los incluidos en la vacuna y aumentan los de la minoría local. Esto debe investigarse más a fondo.
Existen 8 probables/posibles VPH-AR, que son los genotipos 26, 53, 66, 67, 68, 70, 73 y 8228. En nuestra muestra, estos representan un 8,2%, lo que podría aumentar aún más la prevalencia de la cantidad total de VPH-AR reales. Debido a la falta de datos sobre su capacidad de transformación y relativa baja frecuencia global, solo los incluimos en el análisis epidemiológico. pero no, en el citológico. Es importante tener en cuenta este punto, porque, en un futuro próximo, esta característica podría implicar un valor relativamente más alto de VPH-AR.
Una de las características más importantes fue el estudio citológico. Aquellas mujeres de las que pudimos recoger toda la información, la historia clínica, la citología y el genotipo, fueron incluidas en el análisis, y alcanzaron un total de 160.
Los grupos 2, 3.B y 4.B, son los que necesitan un seguimiento estrecho por ser portadores de VPH-AR, y, en esos casos, la citología es muy importante por las limitaciones de la información del genotipo únicamente. Cualquiera de ellos, si tiene factores de riesgo, puede evolucionar a HSIL o carcinoma.
El grupo 5.B tiene grandes posibilidades de progresar a carcinoma por lo que es obligatorio tratar a esas pacientes inmediatamente.
Existe una distribución relativamente alta de pacientes ASCUS, portadoras en la misma proporción de VPH-AR y VPH-BR. De acuerdo con las indicaciones médicas, todas deben ser biopsiadas, pero hay más posibilidades de que progresen a HSIL aquellas que tienen VPH-AR por encima del VPH-BR.
En este estudio, tuvimos un frotis extraño, un carcinoma vulvar, portador de un VPH-AR. El capítulo relacionado con este carcinoma y otros, como el anal, el de pene e incluso el de endocérvix, deben investigarse más a fondo, pero su relación con distintos VPH es cada vez más clara.
En conclusión, este es el primer análisis epidemiológico realizado en la ciudad de Mar del Plata que podría ser utilizado para futuras investigaciones y programas nacionales de planificación de la vacunación. No obstante, debemos destacar la importancia de realizar la genotipificación y el estudio citológico en forma conjunta como métodos complementarios a favor de la evolución del paciente.
redalyc-journal-id: 651
fer.rguerra@gmail.com







