Artículos originales
Epidemiología molecular del virus del papiloma humano en el tamizaje del cáncer cervicouterino en Córdoba, Argentina
Human Papillomavirus Molecular Epidemiology in Cervical Cancer Screening in Córdoba, Argentina
Epidemiología molecular del virus del papiloma humano en el tamizaje del cáncer cervicouterino en Córdoba, Argentina
Bioquímica y Patología Clínica, vol. 89, núm. 3, pp. 46-51, 2025
Asociación Bioquímica Argentina
Resumen: Introducción: Las pruebas moleculares, seguidas de citología en mujeres positivas para HPV, proporcionan un aumento significativo de la sensibilidad y especificidad en la detección temprana de la neoplasia cervical. Objetivos: a) Evaluar los resultados de la prueba cobas ® 4800 HPV (Roche), introducida como estrategia de detección primaria del cáncer cervicouterino en los algoritmos locales, y b) Caracterizar la distribución de genotipos empleando técnicas de secuenciación masiva. Materiales y métodos: Se tamizaron 3685 mujeres, de entre 30 y 64 años, con patología cervical desconocida. Se recolectaron muestras para pruebas de HPV y de citología, como prueba de triage. Las muestras positivas para HPV fueron analizadas por secuenciación masiva. Resultados: La positividad global para HPV de alto riesgo fue del 12,6% (464/3685). Dentro de las muestras positivas, los HPV 16 y 18 estuvieron presentes, en infección simple o combinada, en el 20,7% (96/434) y el 13,8% (64/434) de los casos, respectivamente, mientras que, en el 72,8% (338/464) de los casos, se identificaron exclusivamente otros genotipos de HPV de alto riesgo, distintos del HPV 16 y 18. Conclusiones : El ensayo comercial utilizado permitió la genotipificación parcial, lo que posibilitó la estratificación del riesgo y priorizó la toma de decisiones clínicas en mujeres positivas para HPV 16 y 18. La implementación de rutina de la genotipificación ampliada mediante secuenciación masiva permitirá afrontar nuevos desafíos en el abordaje de la epidemiología molecular del HPV.
Palabras clave: papillomaviridae, virus del papiloma humano, epidemiología molecular, tamizaje, cáncer cervicouterino.
Abstract: Introduction: Molecular assays followed by cytology in Human Papillomavirus (HPV)-positive women provide a significant increase in sensitivity and specificity in the early detection of cervical neoplasia. Objectives: a) to evaluate the results of the "Cobas 4800 HPV Test" (Roche), introduced as a primary screening strategy for cervical cancer into the local algorithms; and b) to characterize the distribution of genotypes using massive sequencing techniques. Materials and Methods: A total of 3685 women between 30 and 64 years of age with unknown cervical pathology were screened. Samples were collected for HPV testing and cytology as a triage test. HPV-positive samples were further analyzed by massive parallel sequencing. Results: The overall positivity for high-risk HPV was 12.6% (464/3685). Among the positive samples, HPV 16 and 18 were present in simple or combined infections in 20.7% (96/434) and 13.8% (64/434) of the cases, respectively, whereas exclusively high-risk HPV genotypes other than HPV 16 and 18 were present in 72.8% (338/464) of the cases. Conclusions: The commercial assay used allowed partial genotyping, particularly enabling risk stratification and prioritizing clinical decision making in women positive for HPV 16 and 18. The routine implementation of extended genotyping through massive sequencing will allow facing new challenges in addressing the molecular epidemiology of HPV.
Keywords: papillomaviridae, human oapillomavirus, molecular epidemiology, screening, cervical cancer.
Introducción
La infección persistente por el virus del papiloma humano (HPV, por sus siglas en inglés) es un requisito necesario, pero no suficiente, para el desarrollo del cáncer cervical (CC)1. Por este motivo, solo una pequeña proporción de mujeres infectadas desarrolla lesiones premalignas, conocidas como neoplasia intraepitelial cervical de grado 3 (NIC3) y adenocarcinoma in situ, las cuales, con el tiempo, pueden progresar a cáncer.
Hasta la fecha, se han descrito más de 200 genotipos de HPV2 , de los cuales más de 40 infectan el tracto anogenital y aerodigestivo. Catorce de estos están asociados con un mayor riesgo de desarrollar CC y son considerados HPV de alto riesgo oncogénico (HPV-AR)3. Los genotipos 16, 18, 31, 33, 35, 45, 52 y 58 están presentes en el 90% de los casos de CC, siendo los genotipos 16 y 18 responsables del 70% de los tumores4.
Mundialmente, se estima que en 2022 aproximadamente 662000 mujeres fueron diagnosticadas con CC y, de estas, 348000 fallecieron por esta causa5. En Argentina, alrededor de 4600 nuevos casos de CC son diagnosticados cada año, y casi la mitad de las mujeres muere a causa de la enfermedad. El 82% de estas muertes ocurre en mujeres mayores de 40 años6.
En la provincia de Córdoba, la tasa de mortalidad está por debajo de la media nacional7. Sin embargo, podría existir un subregistro de casos, especialmente en poblaciones vulnerables, ya que un estudio reciente identifica el CC como el cáncer más prevalente en mujeres adolescentes y adultas jóvenes de la provincia de Córdoba8.
La evidencia actual indica que el tamizaje del CC utilizando ensayos que detectan el material genético del HPV es más efectivo que el uso de métodos basados en citología9. Si bien existen numerosos métodos moleculares para la detección del virus, es fundamental que los mismos estén validados clínicamente para detectar infecciones virales asociadas al riesgo de desarrollar NIC de grado 2 o superior (NIC2+). La mayoría de los métodos comerciales disponibles para genotipificar el HPV están basados en hibridación, RFLP o PCR en tiempo real10. Las pruebas moleculares, seguidas de citología en mujeres positivas para el virus, proporcionan un aumento significativo de la sensibilidad y de la especificidad clínicas en la detección temprana de la neoplasia cervical.
Las técnicas de secuenciación de nueva generación (NGS, por sus siglas en inglés) existen desde hace varias décadas, pero, recién en los últimos años, comenzaron a cambiar el potencial diagnóstico de los laboratorios de microbiología clínica y salud pública11. Estas metodologías, altamente sensibles, posibilitan la detección de genotipos del HPV presentes en un bajo número de copias, y la caracterización de infecciones múltiples. Además, permiten la identificación de nuevos genotipos y determinar si el virus se ha integrado al genoma celular, un evento genético clave en el desarrollo y la progresión a CC12. A pesar de todas estas ventajas, las técnicas de NGS aún no se implementan rutinariamente en el entorno clínico debido a la falta de estandarización, directrices de calidad y costos más elevados13.
Argentina cuenta con el Programa Nacional de Prevención de Cáncer Cervicouterino (PNPCC)14, cuyo objetivo principal es reducir la incidencia y mortalidad debida a este tipo de neoplasia. Para ello, diseña, implementa y evalúa estrategias para fortalecer los programas de prevención provinciales. En la provincia de Córdoba, el Programa Provincial de Prevención de Cáncer de Cuello Uterino en Atención primaria (PPCCUAPS) cuenta con una prueba comercial de HPV validada para el tamizaje desde el año 201715. Si bien esta prueba se implementó hace varios años, se dispone de escasos datos poblacionales sobre los genotipos circulantes en el ámbito local. Conocer a fondo la epidemiología molecular del HPV en la era vacunal aportará información para la toma de decisiones sanitarias. La vigilancia epidemiológica impactará en el desarrollo de nuevas fórmulas vacunales y la adecuación de las pruebas de HPV utilizadas en el tamizaje para optimizar su desempeño. Asimismo, podría contribuir en el nivel individual a una mejor estratificación del riesgo de desarrollar CC y a la toma de decisiones terapéuticas, una vez establecida su sensibilidad clínica.
En este sentido, el objetivo del estudio fue proporcionar información actualizada sobre la epidemiología molecular del HPV en mujeres tamizadas en el contexto del programa de prevención de CC de la provincia de Córdoba.
Materiales y métodos
Población de estudio
Se realizó un estudio transversal, observacional y retrospectivo en el cual se evaluaron muestras de cepillados cervicouterinos, recolectadas en la ciudad de Córdoba en el período de mayo 2021 - mayo 2022, en el marco del PPCCUAPS.
Según el algoritmo utilizado, a las mujeres con una prueba de HPV positiva, se les ofreció acceder a una evaluación adicional. Dicho triage incluyó: citología cervical, colposcopía y, eventualmente, la toma de una muestra de biopsia para confirmación diagnóstica. Los resultados de citología se clasificaron según el sistema Bethesda 200116y las histologías, según la nomenclatura de LAST17.
Los criterios de inclusión del programa de tamizaje fueron: no estar gestando, no haberse sometido a histerectomía total, no presentar citología anormal previa y el cumplimiento de las condiciones de preparación previa de las pacientes para la toma de muestra adecuada.
Las participantes prestaron su consentimiento para la realización de los estudios ginecológicos que forman parte de sus controles de rutina.
Las mujeres participantes se clasificaron en siete grupos etarios: 30-34 años, 35-39 años, 40-44 años, 45-49 años, 50-54 años, 55-59 años y 60-64 años, para el análisis de la positividad de HPV-AR y la distribución de genotipos.
Detección del HPV
La detección y genotipificación del HPV se realizó con la prueba cobas® HPV (Roche Diagnostics, GmbH, Mannheim, Alemania) siguiendo estrictamente las indicaciones del fabricante. La misma detecta y tipifica los HPV-AR mediante PCR en tiempo real, discriminando los genotipos HPV-16, HPV-18 de manera individual y, en forma agrupada, otros 12 genotipos de alto riesgo (HPV-Ot: 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 66, y 68).
NGS y análisis bioinformático
Para la genotipificación extendida, se amplificó un fragmento de 450 pares de bases de la región L1 del genoma del HPV utilizando el juego de primers PGMY18. La preparación de librerías se realizó mediante un protocolo adaptado con el kit COVIDSeq (Illumina, USA) utilizando los reactivos de preparación de librerías, a partir del paso de tagmentación. La secuenciación se realizó en la plataforma MiSeq (Illumina, USA) mediante secuenciación de extremos emparejados (2x 150 nucleótidos) y fragmentos con un tamaño promedio de 350 nucleótidos.
Las lecturas obtenidas se alinearon contra los genomas de referencia obtenidos de la base de datos PaVE19. Se utilizaron únicamente los genomas correspondientes a genotipos del HPV que tienen tropismo por tejidos de origen humano (Tabla 1). La alineación se realizó con BWA20 y se empleó la herramienta SAMtools21 para el filtrado y el mapeo. Se excluyeron las lecturas que no mapearon contra ninguna de las referencias y aquellas con una calidad de mapeo menor de Q30.
| Genotipo | Diagnóstico citológico | ||||||
| AG-NOS | ASC-H | ASC-US | HSIL | LSIL | NILM | Total | |
| HPV-16 | 0 | 0 | 0 | 11 | 0 | 10 | 21 |
| HPV-18 | 0 | 1 | 0 | 0 | 1 | 2 | 4 |
| HPV-Ot | 2 | 5 | 8 | 6 | 14 | 95 | 130 |
| HPV-16 + HPV-Ot | 0 | 1 | 0 | 3 | 3 | 4 | 11 |
| HPV-18 + HPV-Ot | 0 | 0 | 0 | 1 | 0 | 5 | 6 |
| HPV-16 + HPV-18 + HPV-Ot | 0 | 0 | 0 | 0 | 2 | 0 | 2 |
| Total | 2 | 7 | 8 | 21 | 20 | 116 | 174 |
Análisis estadístico
Se realizó un análisis descriptivo y exploratorio de los datos para calcular las frecuencias de las variables de interés. Los análisis estadísticos se realizaron utilizando el software Infostat versión 202022, aplicando la prueba de chi cuadrado. La significancia estadística se estableció en p<0,05.
Consideraciones éticas
El estudio se realizó de acuerdo con los lineamientos de la Declaración de Helsinki de la Asociación Médica Mundial y siguiendo las normas éticas locales específicas, establecidas por el Ministerio de Salud de la provincia de Córdoba, Argentina.
Resultados
Características de la población en estudio
Se estudió un total de 3685 muestras de cepillados cervicouterinos, correspondientes a mujeres entre 30 y 64 años [edad media: 46 (± 8) años]. La positividad global del HPV fue del 12,6% (464/3685) (IC95: 11,3 a 13,4). La mayor tasa de positividad para HPV se registró en el grupo etario de 30-34 años, con tendencia a la baja en los rangos etarios siguientes, y se observó un incremento a partir del grupo etario de 50-54 años (Figura 1).
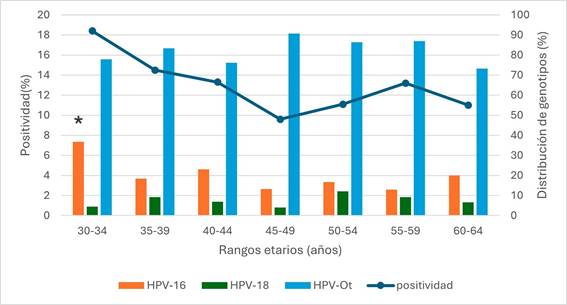
Figura 1.
Rango etario vs. positividad y distribución de genotipos
La línea azul muestra la variación en la positividad a lo largo de los grupos etarios. Las barras muestran la proporción relativa de genotipos encontrada en cada grupo etario; *p<0,05.
Distribución de genotipos
El 13,6% (63/464) de los casos fue positivo para HPV-16; el 3,7% (17/464), para HPV-18 y el 72,8% (338/464), para el grupo HPV-Ot. En el 9,9% (46/464) de los casos restantes, se detectaron las siguientes combinaciones: 63,0% (29/46) HPV-16 + HPV-Ot; 28,3% (13/46) HPV-18 + HPV-Ot; 6,5% (3/46) HPV-16 + HPV-18 + HPV-Ot); 2,2% (1/46) HPV-16 + HPV-18. La distribución de genotipos por grupo etario sigue la misma tendencia que la distribución global: el grupo HPV-Ot es el más abundante, seguido del HPV-16 y, por último, el HPV-18. En el grupo etario de 30-34 años, la proporción de genotipo HPV-16 es significativamente mayor en comparación con el resto de los grupos etarios (p<0.05). En este mismo rango etario, aproximadamente un 40% de los casos corresponde a los dos genotipos de mayor poder oncogénico, HPV-16 y HPV-18 (Figura 1).
Datos citohistológicos
Del total de participantes con prueba de HPV positiva, el 37,5% (174/464) respondió a la convocatoria para la evaluación adicional o triage concurriendo a la toma de muestra para la realización de estudios de citología y colposcopía. En las citologías patológicas (HSIL) se encontró un 60% (15/25) de casos asociados a la presencia de genotipos HPV 16 y/o HPV-18, mientras que un 40% (10/25) de los casos estuvo asociado a la presencia de HPV-Ot. En las citologías normales (NILM), se encontró un 16,8% (21/125) de casos asociados a la presencia de genotipos HPV 16 y/o HPV-18, mientras que un 83,2 % (104/125) de los casos estuvo asociado a la presencia de HPV-Ot (Tabla I). En pacientes con citología anormal (ASCUS≥), se confirmaron por histología 11 casos de CIN3+ (Figura 2). En estas lesiones, el HPV-16 estuvo presente en el 54,5% (6/11) de los casos; el HPV-18, en el 18,2% (2/11) de los casos; HPV-16 + HPV-Ot, en 2 casos (18,2%) y, en un caso (9,1%), se detectó HPV-Ot.

Figura 2.
Flujograma para el tamizaje de cáncer cervical con prueba HPV Cobas®.
NGS
El 12,3 % (57/464) de las muestras positivas para HPV se secuenció por NGS. Mediante secuenciación masiva, se identificaron 26 genotipos diferentes, en su mayoría genotipos de alto riesgo. Un 53,8 % (14/26) de los genotipos encontrados no estaba incluido en la prueba cobas® HPV. Los 10 genotipos principales detectados, en orden descendente de frecuencia relativa, fueron los siguientes: 16 (36,8%), 51 (17,5%), 45 (14,0%), 18 (12,3%), 39 (12,3%), 59 (10,5%), 66 (10,5%), 68 (7,0%), 52 (5,3%) y 58 (5,3%).
El 43,9% (25/57) de las muestras estudiadas por NGS correspondió a infecciones múltiples, y se identificaron hasta 5 genotipos en cada muestra (Figura 2). En las cinco muestras con diagnóstico de CIN3+ confirmado por histología, se identificó el genotipo HPV-16 como infección simple en el 80% de los casos, mientras que un caso correspondió a una coinfección en la cual se encontró el genotipo de bajo riesgo oncogénico HPV-82, además del HPV-16.
Discusión
Los resultados de este trabajo muestran que la positividad global de la infección por HPV hallada en la población estudiada fue del 12,6%, similar a la obtenida en un estudio previo realizado en Jujuy, Argentina23. La mayor positividad se observó en mujeres jóvenes, con una disminución de esta a medida que aumenta la edad hasta el rango de 50-54 años. Esto se condice con lo reportado por otros estudios donde la positividad más alta de infección por HPV se registra a edades tempranas, luego de la primoinfección, y disminuye con la edad24,25,26. Por otro lado, se registró un incremento en la positividad de infección por HPV en el grupo etario de 55-59 años. Este fenómeno también ha sido analizado por otros autores27,28,29 y, en efecto, en un metaanálisis sobre la prevalencia del HPV en el ámbito mundial en un millón de mujeres, se describió a partir de los 55 años en África y América27. Algunas mujeres, a partir de los 55 años de edad, pueden modificar su sistema inmune por procesos de inmunosenescencia, lo que las hace más propensas a infecciones virales. Asimismo, pueden haber estado en contacto con el virus a edades más tempranas y así, desarrollar posteriormente estas infecciones latentes.
La distribución global de genotipos fue similar a la reportada por otros autores que también utilizaron el test de HPV cobas® como prueba primaria de tamizaje30,31, siendo el grupo HPV-Ot el más prevalente, seguido por el HPV-16 y, por último, el HPV-18. En el grupo etario 30-34 años, la proporción de casos de HPV-16 fue significativamente mayor que en el resto de los grupos etarios. En conjunto, los casos de HPV-16 más los de HPV-18, correspondientes a los genotipos de mayor riesgo oncogénico, representan más de un 40% de las infecciones en este grupo etario, hecho que señala el valor de la estratificación de riesgo y la priorización de la toma de decisiones clínicas.
Este estudio aporta valiosos datos locales sobre la epidemiología molecular del HPV en el contexto de un programa de tamizaje. Con respecto a la correlación con la citología, de acuerdo con lo esperado, los genotipos de alto riesgo oncogénico HPV-16 y HPV-18 se encontraron en alta proporción en las lesiones HSIL (60%) en comparación con las citologías normales, donde la proporción es más baja (16,8%), y predominaron los genotipos HPV-Ot.
Se ha reportado que la adherencia al triage es baja en países de ingresos medios32. Según nuestros resultados, menos del 40% del total de mujeres con una prueba de HPV positiva regresó para la realización de citología y colposcopía. En ese sentido, Paolino y col. han propuesto una estrategia para mejorar la adherencia al triage mediante la nueva citación de la paciente a través de mensajes de texto33, que podría ser aplicable en nuestro entorno.
En la población en estudio, se encontraron 11 casos de CIN 3+ correspondientes a un 2,3% del total de muestras positivas para HPV. Sin embargo, dada la recaptación incompleta de las pacientes positivas para HPV, no es posible estimar una tasa de detección de la patología.
En las muestras estudiadas por NGS, se detectaron 26 genotipos del HPV. Los mismos correspondieron mayoritariamente a genotipos de alto riesgo oncogénico. Estos hallazgos reflejan la variedad de genotipos circulantes en el ámbito local en la población tamizada. Una ventaja significativa de NGS fue su potencial para caracterizar infecciones múltiples, así como también, el descubrimiento de otros genotipos no incluidos en el ensayo de cobas®. Aunque el rol de las infecciones múltiples en la progresión de la enfermedad está aún en discusión, algunos autores proponen que interacciones cooperativas o competitivas entre ciertos genotipos podrían aumentar el riesgo de desarrollar CC34. Si bien el número de muestras secuenciadas asociadas a casos en los que se confirmaron alteraciones histológicas compatibles con CIN3+ fue bajo, el genotipo HPV-16 estuvo presente en todas las muestras, principalmente como infección simple. Esto concuerda con un estudio previo realizado en nuestro país donde las lesiones histológicas de alto grado mostraron una diversidad genotípica significativamente menor en comparación con las lesiones de bajo grado, que mostraron una mayor abundancia de genotipos35.
La secuenciación permitió obtener datos cualitativos sobre la variedad de los genotipos circulantes en la población estudiada. Sin embargo, debido al bajo número de muestras secuenciadas por NGS (una de las limitaciones principales de este trabajo), no es posible calcular las prevalencias de los diferentes genotipos localmente.
A futuro, la utilización de NGS, de reciente incorporación en el sistema público de salud de la provincia de Córdoba, permitirá el conocimiento más detallado de la distribución de genotipos circulantes, al proporcionar información para la toma de decisiones de política sanitaria relevantes para el ajuste de programas de vacunación y tamizaje.
Agradecimientos
Al Programa de Promoción de la Investigación en Cáncer del Ministerio de Salud de la Nación, a través del Instituto Nacional del Cáncer (INC) de Argentina, por la Beca de Investigación en Cáncer 2022 otorgada a Franco Cippitelli.
Referencias Bibliográficas
1. Walboomers JMM, Jacobs M V, Manos MM, Bosch FX, Kummer JA, Shah K V, et al. Human papillomavirus is a necessary cause of invasive cervical cancer worldwide. J Pathol. 1999;189(1):12-9, https://doi.org/10.1002/(sici)1096-9896(199909)189:1%3C12::aid-path431%3E3.0.co;2-f
2. HPV reference clones – International Human Papillomavirus Reference Center [Internet]. Disponible en: https://www.hpvcenter.se/human_reference_clones/
3. Burd EM. Human Papillomavirus and Cervical Cancer. Clin Microbiol Rev. 2003;16(1):1-17, https://doi.org/10.1128/CMR.16.1.1-17.2003
4. de Sanjose S, Quint WG, Alemany L, Geraets DT, Klaustermeier JE, Lloveras B, Tous S, Felix A, Bravo LE, Iljazovic E. Retrospective International Survey and HPV Time Trends Study Group. Lancet Oncol. 2010;11(11):1048-56. Lancet Oncol. julio de 2010;11:1048-56. Disponible en: https://doi.org/10.1016/s1470-2045(10)70230-8
5. Cancer today [Internet]. Disponible en: https://gco.iarc.fr/today/en/dataviz/tables?mode=cancer&sexes=2&group_populations=1&multiple_populations=1&types=1
6. Arrosi S, Laudi R. Guía programática abreviada para el tamizaje de cáncer cervicouterino. Programa Nacional de Prevención de Cáncer Cervicouterino [Internet]. 2014 ene [citado 17 de julio de 2024]. Disponible en: https://www.fmed.uba.ar/sites/default/files/2018-02/8.pdf
7. Mortalidad por cáncer cervicouterino [Internet]. Argentina.gob.ar. 2021. Disponible en: https://www.argentina.gob.ar/salud/instituto-nacional-del-cancer/estadisticas/mortalidad-ccu
8. Allais MPB, Dutari P, Llanos RB, Ferreira G, Nicolas G, Musso V. Distribución de la patología oncológica en pacientes adolescentes y adultos jóvenes en la provincia de Córdoba, Argentina. Oncología Clínica. 2023;28(2), https://doi.org/10.56969/oc.v28i2.144
9. Ronco G, Dillner J, Elfström KM, Tunesi S, Snijders PJF, Arbyn M, et al. Efficacy of HPV-based screening for prevention of invasive cervical cancer: Follow-up of four European randomised controlled trials. The Lancet. 2014;383(9916):524-32, https://doi.org/10.1016/s0140-6736(13)62218-7
10. Siqueira JD, Alves BM, Castelo Branco ABC, Duque KCD, Bustamante-Teixeira MT, Soares EA, et al. Comparison of four different human papillomavirus genotyping methods in cervical samples: Addressing method-specific advantages and limitations. Heliyon. 2024;10:e25474, https://doi.org/10.1016/j.heliyon.2024.e25474
11. Hilt EE, Ferrieri P. Next Generation and Other Sequencing Technologies in Diagnostic Microbiology and Infectious Diseases. Genes (Basel). 2022;13(9):1566, https://doi.org/10.3390/genes13091566
12. Hu Z, Ma D. The precision prevention and therapy of HPV-related cervical cancer: new concepts and clinical implications. Cancer Med, 2018;7(10):5217-36, https://doi.org/10.1002/cam4.1501
13. Sara L, Mühr A, Guerendiain D, Cuschieri K, Sundström K, Yeager M. Human Papillomavirus Detection by Whole-Genome Next-Generation Sequencing: Importance of Validation and Quality Assurance Procedures. Viruses. 2021;13(7):1323, https://doi.org/10.3390/v13071323
14. Programa Nacional de Prevención de Cáncer Cervicouterino [Internet]. Argentina.gob.ar. 2019. Disponible en: https://www.argentina.gob.ar/salud/instituto-nacional-del-cancer/institucional/pnpcc
15. Diaz Vilches V. VPH y cáncer de cuello de útero: prevención y detección precoz [Internet]. Web de Noticias - Gobierno de Córdoba. 2023. Disponible en: https://prensa.cba.gov.ar/salud-2/vph-y-cancer-de-cuello-de-utero-prevencion-y-deteccion-precoz/
16. Solomon D, Davey D, Kurman R, Moriarty A, O’Connor D, Prey M, et al. The 2001 Bethesda SystemTerminology for Reporting Results of Cervical Cytology. JAMA. 2002;287(16):2114-9, https://doi.org/10.1001/jama.287.16.2114
17. Darragh TM, Colgan TJ, Thomas Cox J, Heller DS, Henry MR, Luff RD, et al. The lower anogenital squamous terminology standardization project for HPV-associated lesions: Background and consensus recommendations from the college of American pathologists and the American society for colposcopy and cervical pathology. Int J Gynecol Pathol 2013;32(1):76-115, https://doi.org/10.1097/pgp.0b013e31826916c7
18. Coutlée F, Gravitt P, Kornegay J, Hankins C, Richardson H, Lapointe N, et al. Use of PGMY Primers in L1 Consensus PCR Improves Detection of Human Papillomavirus DNA in Genital Samples. J Clin Microbiol. 2002;40(3):902-7, https://doi.org/10.1128/jcm.40.3.902-907.2002
19. PaVE [Internet]. Disponible en: https://pave.niaid.nih.gov/search/search_database
20. Li H. Aligning sequence reads, clone sequences and assembly contigs with BWA-MEM [Internet]. arXiv; 2013. Disponible en: http://arxiv.org/abs/1303.3997
21. Danecek P, Bonfield JK, Liddle J, Marshall J, Ohan V, Pollard MO, et al. Twelve years of SAMtools and BCFtools. Gigascience. 2021;10(2): giab008, https://doi.org/10.1093/gigascience/giab008
22. Infostat - Software estadístico [Internet]. Disponible en: https://www.infostat.com.ar/
23. Arrossi S, Thouyaret L, Laudi R, Marín O, Ramírez J, Paolino M, et al. Implementation of HPV-testing for cervical cancer screening in programmatic contexts: The Jujuy demonstration project in Argentina. Int J Cancer. 2015;137(7):1709-18, https://doi.org/10.1002/ijc.29530
24. Yan X, Shen L, Xiao Y, Wang Q, Li F, Qian Y. Prevalence, characteristics, and distribution of HPV genotypes in women from Zhejiang Province, 2016–2020. Virol J. 2021;18:208, https://doi.org/10.1186/s12985-021-01676-z
25. Winer RL, Hughes JP, Feng Q, Stern JE, Xi LF, Koutsky LA. Incident Detection of High-Risk Human Papillomavirus Infections in a Cohort of High-Risk Women Aged 25–65 Years. J Infect Dis. 2016;214(5):665-75, https://doi.org/10.1093/infdis/jiw074
26. Gravitt PE, Winer RL, Mcbride AA, Munger K. Natural History of HPV Infection across the Lifespan: Role of Viral Latency. Viruses. 2017;9(10):267, https://doi.org/10.3390/v9100267
27. Bruni L, Diaz M, Castellsagué X, Ferrer E, Bosch FX, De Sanjosé S. Cervical Human Papillomavirus Prevalence in 5 Continents: Meta-Analysis of 1 Million Women with Normal Cytological Findings. J Infect Dis. 2010;202(12):1789-99, https://dx.doi.org/10.1086/657321
28. Smith JS, Melendy A, Rana RK, Pimenta JM. Age-Specific Prevalence of Infection with Human Papillomavirus in Females: A Global Review. J Adolesc Health. 2008;43(4):S5.e1-S5.e62, https://doi.org/10.1016/j.jadohealth.2008.07.009
29. de Sanjosé S, Diaz M, Castellsagué X, Clifford G, Bruni L, Muñoz N, et al. Worldwide prevalence and genotype distribution of cervical human papillomavirus DNA in women with normal cytology: a meta-analysis. Lancet Infect Dis. 2007;7(7):453-9, https://doi.org/10.1016/s1473-3099(07)70158-5
30. Bobadilla ML, Villagra V, Zorrilla ME, Olmedo G, Riveros MC, Franco F, et al. Detección y tipificación del Virus Papiloma Humano en el marco del tamizaje virológico para la detección de lesiones del cuello uterino en Asunción, Paraguay. Memorias del Instituto de Investigaciones en Ciencias de la Salud 2019;17(1):6-15, https://doi.org/10.18004/Mem.iics/1812-9528/2019.017(01)06-015
31. Fleider LA, Tinnirello MA, Cherey FG, García MG, Cardinal LH, Kamermann FG, et al. High sensitivity and specificity rates of cobas® HPV test as a primary screening test for cervical intraepithelial lesions in a real-world setting. 2023. PLoS ONE 18(2): e0279728, https://doi.org/10.1371/journal.pone.0279728
32. Paolino M, Gago J, Le Pera A, Cinto O, Thouyaret L, Arrossi S. ecancer 2020;14:1138, https://doi.org/10.3332/ecancer.2020.1138
33. Paolino M, Sánchez Antelo V, Kohler RE, Viswanath K, Arrossi S. Implementation of an mHealth intervention to increase adherence to triage among HPV positive women with HPV—self-collection (ATICA study): post-implementation evaluation from the women’s perspective. BMC Womens Health 2023; 23:1-12, https://doi.org/10.1186/s12905-023-02475-0
34. Senapati R, Nayak B, Kumar Kar S, Dwibedi B. HPV genotypes co-infections associated with cervical carcinoma: Special focus on phylogenetically related and non-vaccine targeted genotypes. PLoS ONE. 2017;12(11):e01878442017, https://doi.org/10.1371/journal.pone.0187844
35. Alejandro Basiletti JI, Valls J, Poklé povich TI, Dolores Fellner M, Rol M, Alonso R, et al. Human papillomavirus genotyping using next generation sequencing (NGS) in cervical lesions: Genotypes by histologic grade and their relative proportion in multiple infections. PLoS One. 2022;17(11):e0278117, https://doi.org/10.1371/journal.pone.0278117.g001
Notas
Notas de autor
silviakademian@gmail.com
Información adicional
redalyc-journal-id: 651

