Resumen: Las nuevas tecnologías computacionales y los avances en ingeniería han permitido desarrollar biomodelos numéricos para la simulación de sistemas biológicos (huesos). Estos modelos matemáticos permitirán realizar estudios más detallados para diagnosticar a tiempo afecciones (osteoporosis). La biomecánica se encarga de la descripción y estudio de los componentes mecánicos; además de encargarse del estudio, análisis y descripción de los movimientos del cuerpo humano. Con el diseño de biomodelos numéricos que tengan características que se asemejen a la estructura real del hueso y el uso de elementos finitos, los resultados serán muy cercanos a las condiciones reales del cuerpo humano. El análisis numérico utilizado para simular condiciones específicas es de gran ayuda para determinar tratamientos médicos o sustituir elementos biológicos por prótesis.
Palabras clave: biomodelos, osteoporosis, biomecánica, ingeniería, porosidad.
Abstract: New computational technologies and advances in engineering have allowed the development of numerical bio-models for the simulation of biological systems (bones). These numerical models will allow for more detailed studies for timely diagnoses of conditions (osteoporosis). Biomechanics is responsible for the description of the structural components of the human body. With the design of numerical biomodels that have characteristics that resemble the real structure of bone and the use of finite elements, results will be very close to actual conditions in the human body. The numerical analysis used to simulate specific conditions is of great help to determine medical treatments or to replace biological elements with prosthesis.
Keywords: biomodels, osteoporosis, biomechanics, engineering, porosity.
INGENIERÍAS Y TECNOLOGÍAS
Obtención de biomodelos personalizados para el análisis mecánico estructural de hueso trabecular con y sin porosidad
Obtaining personalized biomodels of trabecular bone with and without porosity to its mechanical analysis and comparative results
Recepción: 29 Marzo 2023
Aprobación: 21 Febrero 2024
Publicación: 31 Mayo 2024
La tecnología, especialmente la ingeniería, ha desarrollado importantes avances científicos para estudiar con precisión enfermedades y afecciones que alteran el cuerpo humano. Estos avances se basan principalmente en la realización de evaluaciones específicas en zonas donde el ojo humano no puede llegar. Desde hace algunas décadas existe un problema de salud relacionado con las fracturas de diferentes elementos biológicos (huesos) debido a diversos agentes y condiciones externas (ya sea por accidentes que agrietan el hueso o por osteoporosis; debido a la porosidad en el interior del hueso). Este problema genera la necesidad de realizar o establecer diversos métodos de predicción de fracturas (aplicados individualmente y/o a toda la población). Sin embargo, la predicción de fracturas es un reto para la ciencia biomecánica (Marquet Rivera et al., 2018).
Los avances tecnológicos aumentan día a día la esperanza de vida de las personas con afecciones que se traducen en complicaciones para realizar sus actividades cotidianas y que ponen en riesgo su calidad de vida. El ritmo acelerado de vida, tanto cultural como tecnológico, lleva a un aumento acelerado de enfermedades y dolencias, que afectan principalmente las capacidades físico-motoras de los individuos (Marquet-Rivera et al., 2021b) y los lleva a un estado de postración. La osteoporosis, por ejemplo, representa un problema de salud, especialmente en las personas mayores (el riesgo de fractura aumenta considerablemente). En la actualidad no existen métodos adecuados de predicción de fracturas, por tal motivo el objetivo del presente trabajo de investigación consiste en el diseño y creación de un biomodelo de sistema biológico (hueso) para su análisis mediante una evaluación numérica mecánica-estructural de los padecimientos que se puedan presentar en pacientes con porosidades, principalmente padecimientos de osteoporosis, con la finalidad de apoyar a los cuerpos médicos a tomar decisiones oportunas para su diagnóstico oportuno y posible rehabilitación.
Una herramienta muy útil para la prevención es el análisis de sistemas biológicos mediante simulaciones numéricas utilizando el método de los elementos finitos (MEF) (Ramos Botello, Estrada Cingualbres, & Bosch Cabrera, 2013), un método especialmente avanzado en el campo de la biomecánica, que supone una importante contribución a la división de ortopedia y traumatología por lo que con el apoyo de dicha tecnología se pretende obtener resultados favorables que contribuyan en el alcance del objetivo planteado y con ello también una contribución al conocimiento y a la sociedad en general.
La fisiología de los huesos representa la principal herramienta para la medicina; ya que con ella se ha logrado explicar el comportamiento de tejidos, células y órganos. Por otro lado, la física y la ingeniería han estado en constante contacto con la medicina, donde su principal objetivo es el desarrollo de mejores tratamientos y una mejor comprensión de las patologías. La ingeniería mecánica y la mecánica clásica, en particular, han desarrollado vínculos muy estrechos para estudiar el comportamiento de materiales que simulan huesos, diseñar nuevos materiales sustitutivos y desarrollar una nueva rama del conocimiento (la biomecánica). La función principal de la biomecánica es la aplicación de metodologías, filosofías y conocimientos de ingeniería orientados a la aplicación en medicina (Marquet Rivera et al., 2018).
En la actualidad, las innovaciones tecnológicas y la aplicación de la ingeniería (para desarrollar análisis del comportamiento del cuerpo humano, sus diferentes características y elementos mecánicos) han permitido explotar enormemente su potencial. Ello les permite disponer de mejores herramientas de análisis para sus estudios. El crecimiento exponencial de las tecnologías computacionales permite la creación de biomodelos de partes específicas del cuerpo humano para elaborar diversos estudios mecánicos, médicos y estadísticos. Un biomodelo se considera una interpretación matemática del comportamiento mecánico y biológico de un componente, cuerpo o sistema. La función de estos modelos es aclarar la importancia de los factores que intervienen en los diferentes procesos, ya sean mecánicos o biológicos, para luego simularlos y predecir una posible respuesta (Marquet-Rivera et al., 2021a).
Existen diversos métodos para poder llevar a cabo exámenes diagnósticos en los pacientes, una vez obtenidas las imágenes del interior del cuerpo, con la finalidad de poder brindar el mejor tratamiento y preservar una buena calidad de vida; algunos métodos utilizados en la práctica clínica son la obtención de imágenes para su análisis textural DEXA (DXA), las tomografías computarizadas cualitativas (QTC) y el análisis de modelos de huesos mediante el método de elementos finitos. Actualmente sólo se puede diagnosticar la osteoporosis mediante DXA; sin embargo, estudios realizados demuestran que el análisis textural mediante DXA aporta escasa información con respecto a análisis densitométricos, por lo que se deben de combinar diversas variables para obtener mejores resultados (Caeiro Rey et al., 2007). Por tal motivo, mediante investigaciones de simulación de sistemas biológicos como la realizada en este trabajo se pretende ampliar la gama de posibilidades en cuanto a técnicas de evaluación y diagnóstico de padecimientos, siendo mucho menos invasiva en los pacientes y tomando como base las soluciones que arroja el método de elementos finitos.
Los avances en la tecnología digital permiten obtener imágenes del interior del cuerpo para su análisis. Tal es el caso de las imágenes obtenidas por tomografía computarizada (TC), cuyo formato estándar es conocido como DICOM (Digital Imaging and Communications in Medicine), que permite la conectividad de dispositivos para su análisis en sistemas médicos (Serna Serna, Trujillo Lemus, & Rivera Piedrahita, 2010). Un posible inconveniente que se presenta en la obtención de las TC en los pacientes es de tipo económico, ya que cada estudio de laboratorio ronda entre los 1,200 y 2,000 pesos; lo cual en ocasiones impide que todos los pacientes que no tienen acceso a algún tipo de seguro médico puedan acceder a ellas; sin embargo, hoy día existen también diversos programas sociales que ayudan a las personas de bajos recursos para que puedan tener acceso a este y otros tipos de estudios de análisis que ayuden a su estado de salud. El análisis de los sistemas biológicos puede realizarse de diversas formas, todas las cuales requieren la ayuda de programas informáticos. Para la obtención de biomodelos de hueso trabecular se siguen los siguientes pasos (Hernández-Vázquez et al., 2020):
1.- Obtención de la tomografía computarizada
2.- Procesamiento de la imagen en formato DICOM mediante programas informáticos
3.- Exportación de ficheros con extensión *.STL
4.- Importación del modelo en un programa CAD para generar un sólido
5.- Importación del modelo en un programa de Elementos Finitos (ANSyS) para verificar que se pueden examinar sus condiciones mecánicas
6.- Obtención de resultados
Como antesala para realizar el modelo de cadera para su análisis numérico, consiste en la adquisición de una tomografía computarizada (TC) de cadera, de manera tal que dicha imagen sea muy precisa y que permita de buena forma realizar el estudio en cuestión.
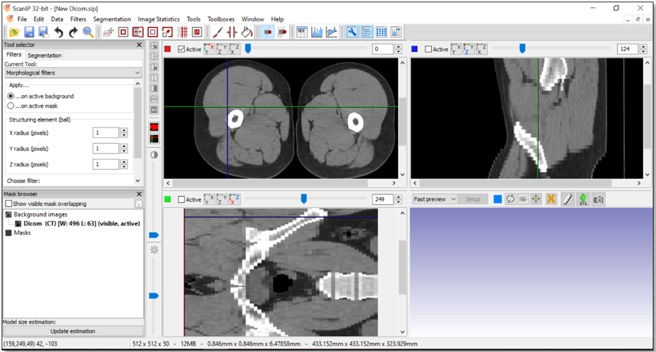
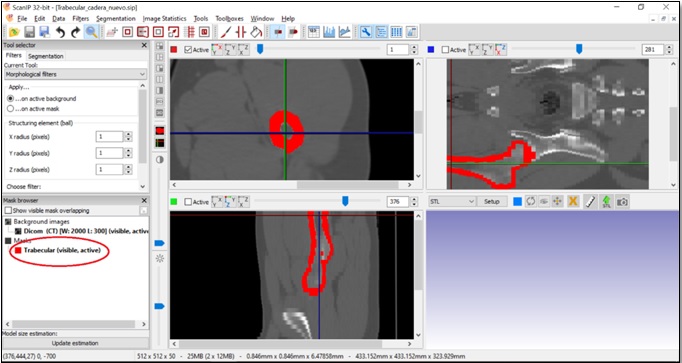
Para este trabajo se inicia por procesar las imágenes en formato estándar DICOM en el programa computacional ScanIp, implementando máscaras que se asemejen lo mejor posible a la geometría del hueso (figura 1). Dentro del programa computacional ScanIp se van seleccionado las máscaras que irán desarrollando el modelo del hueso con el cual se trabajará en análisis mecánico (figura 2).
Una vez que el programa del método de los elementos finitos puede utilizar el biomodelo para realizar la evaluación numérica procede a aplicar las propiedades mecánicas de los materiales, los agentes externos que afectan al sistema y las restricciones de movimiento implicadas. Las condiciones de linealidad (tensión frente a deformación) se modifican considerando que las propiedades mecánicas de los componentes utilizados son capaces de deformarse más allá de su límite elástico. La continuidad en la aplicación de la fuerza se interrumpe al generar una geometría de forma muy compleja y considerar la interacción de dos o más materiales (por ejemplo, hueso cortical y hueso trabecular). La isotropía se modifica al considerar un material ortotrópico; sin embargo, introducir un cambio en la homogeneidad del modelo es un proceso muy complejo. Es necesario modificar la geometría del modelo de forma microestructural introduciendo una serie de poros diversos que tienen tamaños y formas diferentes. Además, hay un gran número de ellos y están situados de forma aleatoria dentro del modelo. Esta operación representa un gran número de recursos computacionales y de tiempo invertido.
Para generar el modelo con porosidad, se importa el modelo en el software CAD para introducir pequeñas esferas mediante operaciones lineales que representan las porosidades (uso de software computacional Solidworks). Una vez adherido el poro al sistema biológico, se puede modificar su tamaño para simular el daño osteoporótico. La generación de modelos computacionales de sistemas biológicos es compleja y tiene ciertas limitaciones. Sin embargo, para obtener resultados precisos, el modelo final debe ser lo más parecido posible a la anatomía y fisiología del hueso. Los avances en imagen han permitido la generación de modelos 3D de órganos, tejidos y huesos a partir de tomografía computarizada (TC), garantizando que el modelo final tenga una estructura similar al sistema biológico (Hernández-Vázquez et al., 2020). Así como la aplicación de programas de métodos de elementos finitos permiten realizar análisis más complejos (Urriolagoitia Sosa, 2005).
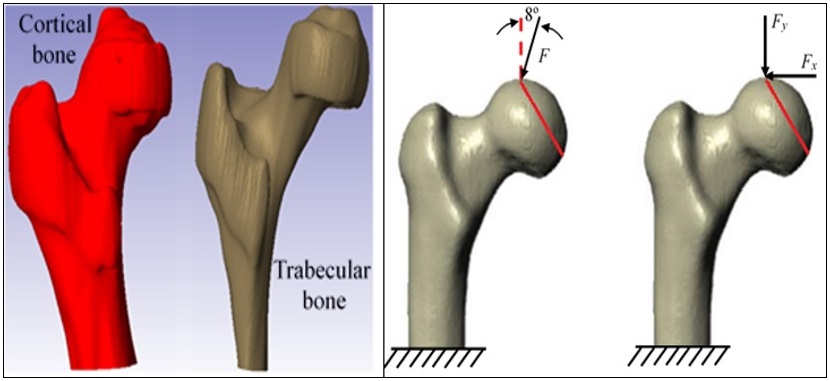
Se presentan dos casos de estudio; primero el biomodelo sin consideración porosa y el segundo, considerando porosidad en la trabécula ósea (figura 3). La porosidad se induce mediante el software Solidworks (figura 4), en donde se generan las porosidades mediante operaciones matriciales; la finalidad de inducir las porosidades en un hueso de paciente sano es para lograr una simulación que logre llevar a cabo análisis mecánicos de condiciones reales, para que más adelante en trabajos posteriores hacer una comparación de resultados con modelos de pacientes con padecimientos reales. Estos modelos serán sometidos a agentes externos (fuerzas) donde el programa resolverá la discretización correspondiente y los resultados que se analizarán según sus condiciones mecánicas; estas condiciones mecánicas están consideradas en este estudio para una persona sana, por tanto, las propiedades mecánicas del hueso también están consideradas para una persona sana; para estudios de investigación posteriores se pretende utilizar propiedades mecánicas del hueso con padecimiento de osteoporosis.
Destaca que el modelo de hueso de cadera corresponde a un hombre adulto masculino sano con una masa corporal de 86 kg, que se encuentra de forma bípeda (es decir, de pie) por lo que dicha masa se reparte en ambas extremidades quedando de 43 kg por lado. Por tanto, se introduce una fuerza de 419.9 N en la parte superior de la cabeza acetabular en la dirección del eje Z del componente. También se añaden condiciones de contorno colocándolas en la parte inferior del hueso (Ux= 0, Uy= 0, Uz= 0, Rotx= 0, Roty= 0, Rotz= 0) para mantener fija la parte inferior del modelo.

Las propiedades tomadas para el estudio en el biomodelo de este trabajo de investigación son de tipo ortotrópicas y fueron seleccionadas por las razones siguientes: a) todos los módulos ortogonales caen dentro del rango de 0 a 4.74 GPa que comúnmente son reportados en la literatura; b) las relaciones entre los módulos de Young direccionales muestran una relación similar donde E1/E2 y E1/E3 son aproximadamente iguales a 2.0 y donde E3/E2 es aproximadamente 0.7 para el tejido esponjoso y c) el módulo de Young medio es de 1.0 GPa indicado en la literatura; por tal motivo, las propiedades mecánicas aplicadas al hueso trabecular (tabla 1) se han tomado de diversas investigaciones disponibles en la literatura (Krone & Schuster, 2006). La densidad para el hueso trabecular se fijó en 1,400 kg/m3.

El modelo (figura 5 y figura 6) se resuelve y los resultados se presentan a continuación:
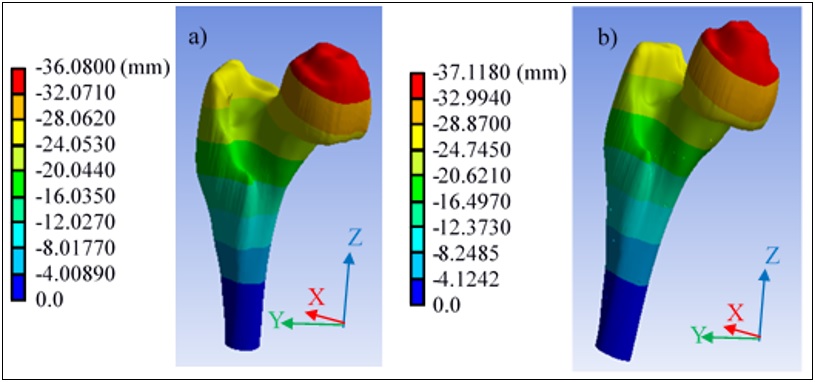
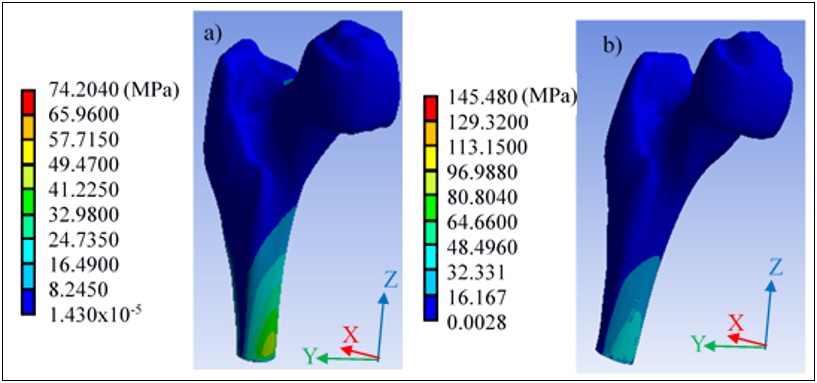
En el presente trabajo de investigación los análisis correspondientes sólo se llevaron a cabo en el hueso trabecular por ser la parte del hueso que presenta mayor cantidad de porosidades (característica propia del tipo de hueso); sin embargo, se pretende que en futuras investigaciones se realicen los mismo análisis pero en el hueso en conjunto tomando en cuenta el hueso cortical; esto con la finalidad de visualizar el comportamiento del biomodelo en situaciones o servicios en un contexto real; es decir, en donde se pueda simular cuando la persona corre, salta o carga un peso extra. Cabe señalar que los resultados obtenidos se realizaron para probar que el modelo desarrollado soporta los análisis mecánicos por medio de elementos finitos; el biomodelo trabajado corresponde a una persona adulta de 40 años de edad sana y con un peso de 86 kg, por lo que no contamos con un parámetro de referencia para comparar con un paciente con algún tipo de padecimiento como lo es osteoporosis; sin embargo, mediante el presente estudio se pretende abrir una puerta para futuros análisis comparativos y en donde se pueda prevenir una fractura o falla en el hueso de pacientes reales.
En el análisis realizado, se destaca la diferencia de resultados entre los modelos con y sin porosidad, demostrando que el desplazamiento en el hueso que no tiene poros presentes es menor que en el que tiene porosidad. La tensión de Von-Mises también crece en el modelo que presenta poros (el valor máximo es casi el doble que en el modelo que no presenta porosidad). Sin embargo, aunque la porosidad tiene un gran efecto en el análisis, hay que realizar trabajos futuros para introducir una mayor porosidad o un mayor número de poros en las zonas del hueso donde la osteoporosis provoca un desgaste importante del sistema biológico y, por tanto, puede causar una posible fractura, con el objetivo principal de prevenir el dolor del paciente e iniciar un posible tratamiento especializado. Además, podría proporcionar una mayor variedad de situaciones futuras para las evaluaciones mediante la alternancia de condiciones.
redalyc-journal-id: 674
Los autores agradecen al Instituto Politécnico Nacional y al Consejo Nacional de Ciencia y Tecnología el apoyo financiero prestado para el desarrollo de esta investigación.
artursc4@hotmail.com






