Artículo científico
Recepción: 19 Febrero 2020
Aprobación: 04 Mayo 2020
Resumen: El objetivo fue optimizar la aplicación del proceso Fenton para degradar las aguas residuales del camal municipal de Chota–Perú, que contienen alta carga orgánica y son un peligro constante de contaminación de cuerpos de agua y suelo. Los parámetros evaluados fueron: DBO5, DQO, alcalinidad, dureza, pH, conductividad, sólidos totales, turbidez, temperatura, potencial óxido-reducción (ORP) y oxígeno disuelto (OD). Se utilizó un sistema de jarras con agitación a 30 rpm para tratar las muestras y diferentes concentraciones de FeSO4 y H2O2 y pH de acuerdo al diseño Box–Behnken y cálculo de sus valores mediante la metodología de superficies de respuesta con el software Statgraphics 5.1 plus. El tiempo de reacción más adecuado se calculó en 18 minutos y las concentraciones de FeSO4, H2O2 y pH se estimaron en 2110,55 mg/L, 1092,67 mg/L y 3,22 respectivamente. Se observó una mejora del indicador de biodegradabilidad a un valor de 0,5 y una remoción de la DQO alrededor del 79,9 %. El proceso Fenton resulta ser una alternativa eficaz para el tratamiento de aguas residuales de camales y puede ser aplicado como pre-tratamiento.
Palabras clave: proceso Fenton, agua residual, sustancia recalcitrante.
Abstract: The objective was to evaluate the application of the Fenton process to degrade the wastewater of the municipal slaughterhouse of Chota–Peru, which contains high organic load and are a constant danger of contamination of bodies of water and soil. The parameters evaluated were: Biochemical Oxygen Demand (BOD5), Chemical Oxygen Demand (COD), alkalinity, hardness, pH, conductivity, total solids, turbidity, temperature, oxidation-reduction potential (ORP) and dissolved oxygen (DO). A jar system with agitation at 30 r.p.m was used to treat the samples and different concentrations of FeSO4, H2O2 and pH according to the Box–Behnken design and calculating their values using the response surface methodology with Statgraphics 5.1 plus software. The most suitable reaction time was calculated at 18 minutes and concentrations of FeSO4, H2O2 and pH were estimated at 2110,55 mg/L, 1092,67 mg/L and 3,22 respectively. An improvement of the biodegradability indicator was observed at a value of 0,5 and a removal of the COD at around 79,9 %. The Fenton process turns out to be an effective alternative for the treatment of slaughterhouse wastewater and can be applied as a pre-treatment.
Keywords: Fenton process, residual water, recalcitrant substance.
1. Introducción
Las aguas residuales del camal municipal de Chota–Perú son fluidos que se generan durante las operaciones de estabulación y faenado de los animales de beneficio tales como vacunos, porcinos y ovinos y de toda actividad de limpieza y desinfección que se ejecute dentro de las instalaciones del camal. Una vez transportados los animales descansan dentro de los corrales y antes de ser sacrificados son bañados para quitarles del cuerpo el polvo y las excretas, luego del sacrificio, la sangre, desechos de limpieza de vísceras y sustancias provenientes de la mucosa generan aguas residuales con altos índices de carga orgánica [1] y que son descargadas directamente sobre cuerpos de agua y suelo, lo que genera la aparición de vectores de infección, impacto visual negativo, malos olores [2][3] y un desbalance en el nivel de amortiguamiento natural de las aguas de la quebrada Colpamayo–Chota, lo que pone en riesgo la salud de las familias asentadas en las cercanías del camal y de aquellas que hagan uso del agua en su recorrido ya que la exposición a la contaminación es continua alterando seriamente a los ecosistemas [4].
El grado de contaminación de las aguas residuales de camales depende del tipo de animal sacrificado, grado de procesado y protocolos de limpieza [5], sin embargo; la alta concentración de materia orgánica tanto disuelta como en suspensión se debe principalmente a la presencia de aminas, proteínas, sustancias volátiles, ácidos orgánicos, pelos, grasas y material lignocelulósico [6], pero el desangrado es uno de los factores más críticos que contribuye a la contaminación de las aguas residuales de un camal por el alto poder contaminante de la sangre que fácilmente contribuye a rebasar los límites máximos permisibles establecidos en la normativa [7], así también; la presencia de grasas y aceites es de importancia en especial la fracción suspendida [5] ya que el exceso constituye un gran problema para tratamientos biológicos.
En tal sentido los procesos avanzados de oxidación (POA) han despertado interés en la actualidad por su versatilidad y eficacia para el tratamiento de aguas residuales [8][9], ya que los métodos de tratamiento convencionales tienen limitaciones frente a contaminantes recalcitrantes que los hacen lentos e ineficaces y pueden generar productos intermedios con mayor toxicidad [10]. El proceso Fenton constituye un POA que se ha probado en diversos tipos de aguas contaminadas tales como de la industria química [11], termoeléctrica [12],cosmética [13], agroquímica [14], textil [15], petroquímica [9], alimentaria [16] y en lixiviados de rellenos sanitarios [17], donde el mecanismo de reacción se ha estudiado con detenimiento y propuesto por varios investigadores, siendo los iones Fe+2 el catalizador y peróxido de hidrógeno el agente oxidante que en medio ácido generan radicales hidroxilos (OH•), donde el pH, temperatura, dosificación de reactivos y cantidad de constituyentes orgánicos e inorgánicos determinan la eficiencia total de la reacción [18][19]. En esencia los radicales OH• son en extremo altamente reactivos y no selectivos con un potencial de oxidación de 2,8 V [20] capaz de abrir anillos de compuestos aromáticos, fenoles, nitrofenoles, aminas, aminas aromáticas, etc. [21] con altas velocidades de reacción provocando grandes cambios estructurales en los contaminantes hacia la degradación parcial (sustancias más facilmente biodegrables) o total (mineralización) permitiendo su posterior descarga sobre cuerpos de agua o suelo. El proceso Fenton puede estudiarse de acuerdo a las reacciones planteadas en la Tabla 1 cuyo fin es obtener radicales OH• pero de manera controlada ya que estos pueden generar reacciones competitivas y de autoreacción, sin embargo; su efectividad está comprobada y la viabilidad depende de la optimización en la adición de los reactivos, tiempo de contacto y de las características fisicoquímicas finales del agua tratada y en función a ello puede utilizarse como pre o post tratamiento [22].
En el Perú se han reportado estudios en el tratamiento de agua residuales de camales mediante tratamiento químico cal–sulfato de aluminio [24] y flotación por aire disuelto [6], sin embargo con respecto a la aplicación de proceso Fenton para este tipo de aguas residuales no han sido reportados.
Las aguas residuales de camal municipal de Chota–Perú no reciben ningún tipo de tratamiento y son vertidos directamente a las aguas de la quebrada Colpamayo lo que resulta un atentado al ambiente y a las personas que habitan en las cercanías, por tal motivo el objetivo del presente trabajo fue encontrar el pH y la dosis óptima de adición del reactivo de Fenton para lograr la máxima remoción de la DQO en las aguas residuales del camal.
2. Metodología
2.1. Toma de muestras de aguas residuales del camal
Las muestras fueron recolectadas del punto de descarga de aguas residuales del camal municipal Chota, ubicado en la zona urbana de la provincia de Chota–Perú. Se midió la temperatura in situ y las muestras se tomaron al azar en horario de faena de camal durante una hora en intervalos de 10 minutos entre muestreo y muestreo, luego se homogenizaron para obtener un volumen de 25 litros. Enseguida las muestras fueron colocadas en un depósito hermético y se transportaron en condiciones de oscuridad a la brevedad hacia el Laboratorio de Aguas Residuales de la Universidad Nacional Autónoma de Chota.
2.2. Acondicionamiento y análisis de muestras
Las muestras de aguas residuales del camal fueron filtradas utilizando papel filtro 125 mm de diámetro (Whatman) con la finalidad de eliminar el exceso de material lignocelulósico y restos de vísceras. Se efectuaron pruebas de caracterización inicial y final de acuerdo a las técnicas propuestas en el Standard Methods (APHA-AWWA-WPCF, 1992) y se calculó la demanda química de oxígeno (DQO) mediante oxidación con K2Cr2O7 a reflujo cerrado a través de viales para análisis de DQO (Merck), que fueron luego colocados en un termorreactor (Velp Scientifica) a 150 °C durante 2 horas, después de enfriarse se tomaron las lecturas de absorbancia en un espectrofotómetro UV-Vis(PG instrument T80+) a 620 nm (L.D.2 mg O2/L).Para la demanda biológica de oxígeno (DBO5) se utilizaron botellas oxi-top (Velp Scientifica) donde las muestras se incubaron a 20 °C con agitación, en condiciones de oscuridad durante 5 días. La alcalinidad, dureza, conductividad, sólidos totales, turbidez, potencial oxido-reducción (ORP), oxígeno disuelto (OD) y pH se midieron con un equipo multiparamétrico (Hanna Instruments). La aplicación del proceso Fenton se realizó en un equipo de prueba de jarras con agitación (Velp Scientífica) a 30 rpm y temperatura ambiente.
2.3. Plan experimental para aplicación del proceso Fenton
La Tabla 2 muestra los códigos y niveles de análisis usados para la optimización del proceso Fenton, se evaluaron las interacciones de tres variables independientes del proceso: FeSO4, H2O2 y pH de acuerdo al diseño de experimentos Box–Behnken [25], obteniendo como variable de respuesta la remoción de contaminantes de las aguas residuales expresado como DQO. Varios autores establecen que el pH ideal para el proceso Fenton es 3 [26][27][28], sin embargo; otros trabajos también reportan que puede ser efectivo a pHs próximos a 2,5 y 4 con buenos resultados [29][30][31][32], en base a las evidencias revisadas se optó por evaluar el rango de pHs establecido en la Tabla 2 para las aguas residuales estudiadas y encontrar el pH más adecuado para el proceso.
Código y niveles del Diseño Box–Behnken para aplicación del proceso Fenton

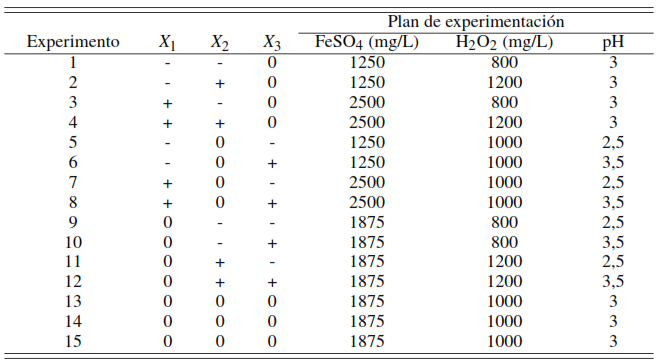
La Tabla 3 resume el desarrollo del plan experimental que se llevó a cabo de acuerdo al diseño seleccionado, se efectuaron 15 experimentos iniciales con dos réplicas obteniéndose en total 45 ensayos, las dosificaciones de reactivo, pHs y su respuesta en remoción de DQO son alimentados al software Statgraphics 5.1 Plus para la estimación de los valores más adecuados de los factores aplicando la metodología de superficie de respuesta y la contrastación de medias se efectuó mediante la diferencia mínima significativa con un α = 0, 05.
Plan experimental Box–Behnken para la aplicación del proceso Fenton
2.4. Estimación del tiempo de contacto de la reacción de Fenton
Se tomaron dos muestras de 500 mL de agua residual y se ajustó el pH a 3 con ácido sulfúrico concentrado (96,6 % p/p, ACS Fermont), a una muestra se adicionó los valores para el máximo nivel y a la otra los valores para el mínimo nivel de FeSO4 7 H2O (99 % p/p, Merck) y H2O2 (30 % v/v, Merck) (Tabla 2). Primero se adicionó el FeSO4 7 H2O homogenizando en un equipo de prueba de jarras durante 3 minutos a 50 rpm para facilitar su disolución, enseguida se agregó el H2O2 manteniendo agitación constante a 30 rpm y cada 5 minutos durante una hora se tomaron 10 mL del agua residual tratada, se neutralizó con NaOH (98,8 % p/p, Loba Chemie) para promover la sedimentación de los contaminantes y del hierro, luego se adicionó óxido de manganeso [33] para descomponer el H2O2 remanente y se procedió a filtrar, del filtrado se tomaron 2 mL y se agregó en un vial de análisis de DQO, se agitó y se colocó en el termorreactor. Luego de la digestión se dejó enfriar y se efectuaron las lecturas de absorbancia en el espectrofotómetro, cuyos valores obtenidos permiten calcular la equivalencia en porcentaje de remoción de la DQO. La remoción de la DQOTOTAL se calculó con la ecuación (17):
 (17)
(17)donde:
DQOi: representa la DQO inicial,
DQOr : representa la DQO remanente.
3. Resultados y discusión
3.1. Caracterización fisicoquímica inicial de las aguas residuales del camal
La Tabla 4 muestra la caracterización inicial de las aguas residuales del camal municipal de Chota, se observa que los valores de DQO y DBO5 se encuentran muy por encima de lo que establece la normativa peruana para aguas residuales. El índice de biodegradabilidad (DBO5/DQO) es de 0,4 que es un indicativo de aguas residuales parcialmente biodegradables [34] por lo que es muy probable la presencia de moléculas orgánicas recalcitrantes provenientes de los mismos residuos, esto es debido a las grandes cantidades de sangre, materia fecal, grasas, proteínas e insumos de limpieza y desinfección [6] que no lo hacen factible para una oxidación biológica efectiva. El valor de pH indica que las aguas residuales son ligeramente alcalinas, valores similares fueron reportados [6][24], así mismo se observa que el ORP adquiere valores negativos lo que indica que las aguas residuales tienen características de un entorno reductor, con una considerable disminución de la cantidad de OD y consiguiente reducción de iones y moléculas lo que se traduce en el alto valor de la DQO.
Composición fisicoquímica inicial de las aguas residuales del camal municipal de Chota
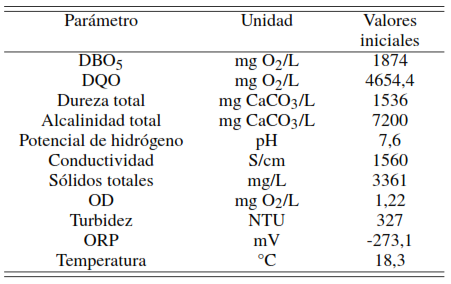
El valor medido para la dureza hace referencia a un tipo de agua residual muy dura lo que hace suponer altas concentraciones de calcio y magnesio, esto es debido a que en la ciudad de Chota se utiliza agua entubada sin tratamiento de potabilización, la que tiene alto contenido de sales y que sumada a los desechos de faenado provocan que tal valor se incremente. En cuanto a la alcalinidad su valor hace suponer altas concentraciones de carbonato, bicarbonato, ácido silícico, fosfatos y otros ácidos de carácter débil, sin embargo; por el valor de pH 7,6 se puede inferir que la especie química de mayor dominancia son los iones bicarbonatos. La turbidez tiende a un valor moderado, valores cercanos fueron reportados [5] y es un indicador de la cantidad de materia ionizable en especial impurezas solubles y esto guarda relación directa con el alto valor de sólidos totales disueltos, la que se debe principalmente a la abundancia de materia fecal, lignocelulósica y sangre que son vertidos sin ningún tratamiento aunque puede tratarse como material sedimentable.
3.2. Tiempo de reacción del proceso Fenton
La Figura 1 muestra que el tiempo de reacción más adecuado para llevar a cabo el proceso Fenton es de 18 minutos, en los primeros minutos se observó que el porcentaje de la remoción de DQO no es tan atractiva para ambas curvas, puesto que la reacción en cadena hacia la generación de radicales OH• está en progreso para las condiciones establecidas, sin embargo; a partir de los 5 minutos hasta los 15 minutos el porcentaje de remoción de la DQO alcanza su máximo comportamiento exponencial lo que probablemente se relaciona con la mayor presencia de radicales OH• en la muestra tratada. A partir del minuto 18 no se apreció un cambio significante en la remoción de la DQO y la curva adopta un comportamiento asintótico. Entre los 30 a 35 minutos se observó una ligera disminución en la remoción de la DQO, esto se debe posiblemente a la generación de productos intermedios de la reacción y que pueden ser mas recalcitrantes que los iniciales. La revisión de antecedentes reportan tiempos muy próximos al calculado con gran efectividad [35], como también tan cortos como 1 minuto [14] y prolongados como 100 minutos [36], sin embargo; ello depende de la naturaleza química del agua a tratar y de las características finales deseadas, pero hay que tener en consideración que tiempos prolongados de tratamiento puede hacer inviable el proceso.
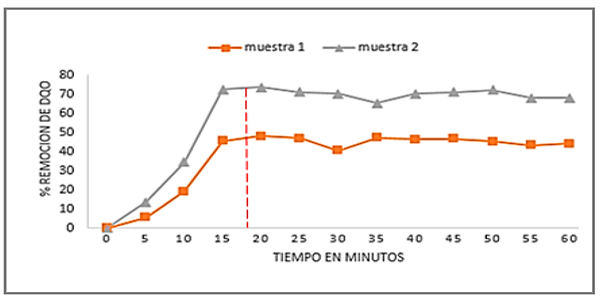
Figura 1
Tiempo de contacto estimado del reactivo de Fenton a pH ajustado a 3 sobre las aguas residuales del camal de Chota
3.3. Estimación de los factores del proceso Fenton
En la Figura 2 se observan los porcentajes promedio de remoción de la DQO de las aguas residuales del camal siguiendo el plan experimental de Box–Behnken. Los experimentos 4, 8, 10, 12, 13, 14 y 15 alcanzaron remociones por encima del 70 % de la DQO, ello corresponde a un pH que está en el rango de 3 a 3,5, las máximas remociones se alcanzaron a un pH muy próximo a 3, confirmándose lo predicho en la literatura, y de acuerdo a ello el pH estimado como el más adecuado para las aguas residuales estudiadas fue de 3,22 (Tabla 5). Los experimentos 5, 7, 9 y 11 presentaron bajas remociones a un pH 2,5 debido a que en condiciones muy ácidas se puede favorecer la formación de iones [Fe(H2O)6]+2[37], el cual a su vez reacciona lentamente con el H2O2 haciéndose lenta la generación de radicales OH•. Por otro lado, un incremento del pH por encima de 4 conduce a la precipitación del Fe bajo la forma de Fe(OH)3 e inhibe la regeneración del Fe+2 (ecuación (4)) y volver a empezar el proceso de oxidación (ecuación (1)), sin embargo; dicha posibilidad de recuperación del Fe+2 es bastante lenta y puede generar radicales OH2• que son también especies oxidantes pero no tan potentes como el radical OH•, pero dicho radical puede ser perjudicial para la oxidación Fenton ya que éste puede interactuar con el Fe+2 (ecuación (3)), H2O2 (ecuación (7)) y radicales OH• (ecuación (10)) generando reacciones improductivas. Valores de pH por debajo de 2,5 no favorecen la oxidación Fenton, esto es debido a que el peróxido de hidrógeno se estabiliza mejor a tales condiciones en iones (H3O2)+2 inhibiendo también la regeneración del Fe+2 (ecuación (12)).
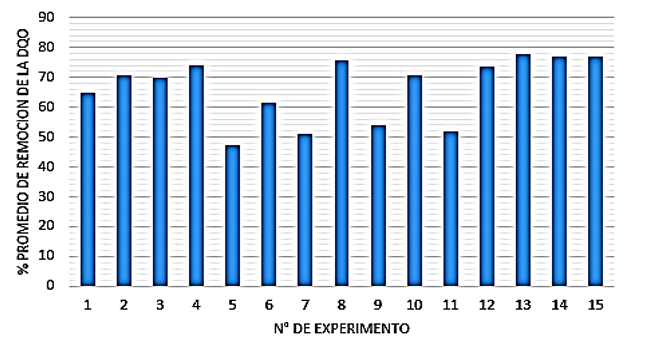
Figura 2
Porcentajes de remoción de la DQO en aguas residuales del camal municipal de Chota
*El orden de los experimentos está de acuerdo a la Tabla 3 en dosificación de reactivos y pH
Estimación de los factores del proceso Fenton para la máxima remoción de la DQO en aguas residuales del camal de Chota

Los porcentajes de las remociones de la DQO para cada ensayo fueron alimentados al software Statgraphics 5.1 plus de acuerdo al diseño propuesto, obteniéndose una superficie tridimensional con punto loma (Figura 3) que se ajusta a un modelo de segundo orden y propone un punto de optimización de las variables del proceso Fenton sobre las aguas del camal para la mayor remoción posible de la DQO.
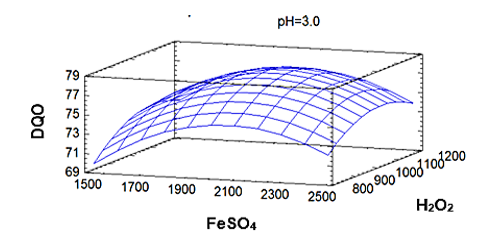
Figura 3
Superficie de respuesta estimada a pH ajustado a 3 para la remoción de la DQO de las aguas residuales del camal municipal de Chota
La Figura 4 muestra la proyección bidimensional de la superficie de respuesta estimada, donde cada contorno de las elipses formadas indica una infinidad de posibilidades de combinación de FeSO4, H2O2 y pH para la remoción de la DQO. El punto más adecuado del proceso Fenton se sitúa dentro de la elipse pequeña siendo los valores estimados los que se indican en la Tabla 5. Tales concentraciones garantizan la generación eficiente de radicales OH• para la degradación máxima de los contaminantes, pero ello implica tener en observancia las reacciones improductivas, el efecto de barrido de los radicales OH• y la regeneración del Fe+3 a Fe+2 que en efecto es muy lenta y provocaría que la reacción se detenga ante la ausencia de Fe+2. Existen reportes de la utilización de FeSO4 en el orden de 500 mg/L a 3300 mg/L y de H2O2 150 mg/L a 6000 mg/L [36][37] cuyos valores radican en el grado de complejidad de las sustancias a tratar, situándose dentro de éstas las aguas residuales del camal de Chota.
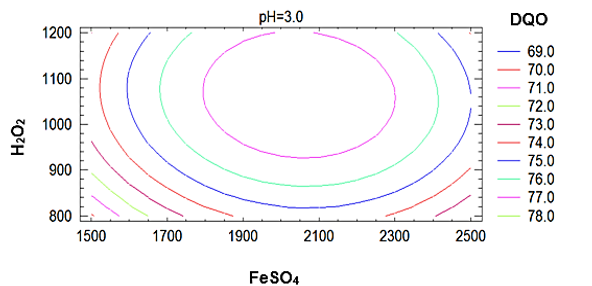
Figura 4
Contornos de superficie de respuesta estimada a pH ajustado a 3 para la remoción de la DQO de las aguas residuales del camal municipal de Chota
La Figura 5 muestra los efectos e interacciones de las variables del proceso Fenton estudiado, cada barra que traspase la línea indicada expresa que es estadísticamente significativo a un 95 % de confianza.
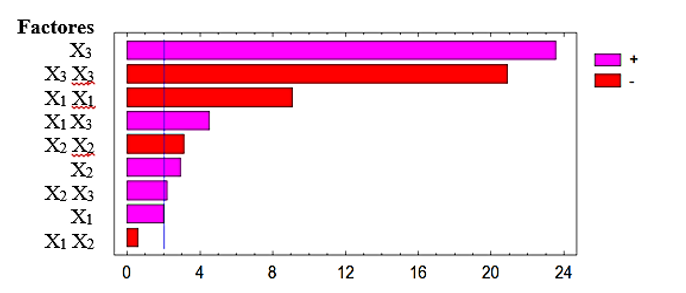
Figura 5
Diagrama de Pareto de los efectos e interacciones de los factores para la remoción de la DQO en aguas residuales del camal municipal de Chota
Se observan siete efectos que tienen influencia sobre la remoción de la DQO, el estadístico R2 ajustado fue de 96,4 % proponiendo que el pH es de gran importancia en el proceso seguido por el FeSO4, H2O2, interacciones y efectos cuadráticos.
La Figura 6 muestra el comportamiento de los efectos estandarizados y corrobora lo observado en el diagrama de Pareto, la región por debajo de la línea estandarizada indica las interacciones de los factores con coeficientes negativos y por encima de la línea las interacciones con coeficientes positivos.
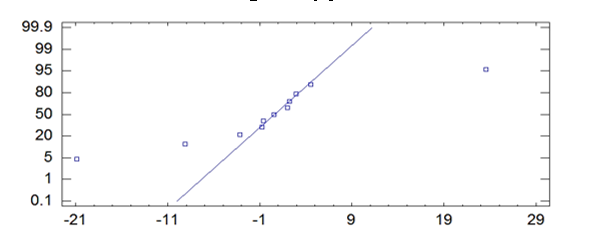
Figura 6
Probabilidad normal para la remoción de la DQO en aguas residuales del camal municipal de Chota
Las interacciones que más se alejan de la línea son más significativos, por tanto se observan tres efectos que marcan distancia de la línea arriba y que corresponden al pH, FeSO4 y H2O2, esto quiere decir que un aumento en sus niveles de dosificación conlleva a un aumento en la remoción de la DQO, por el contrario para el efecto negativo debajo de la línea un aumento se traduce en una disminución de la remoción de DQO (ecuación (18)). Los factores e interacciones que se encuentran sobre la línea no tienen un efecto de gran significancia puesto que corresponden a un estimado de los errores de los efectos.
La ecuación de regresión al modelo ajustado que expresa mejor la remoción de la DQO es (ecuación (18)):
 (18)
(18)El modelo matemático tiene una desviación normal para los residuos de 2,03 lo que hace suponer que los datos no están muy dispersos y el error absoluto de la media es de 1,41 que es un valor pequeño lo que representa que el error de pronóstico es aceptable.
4. Aplicación del proceso Fenton con los factores optimizados
En la Tabla 6 se observa una mejoría en los parámetros analizados en las muestras de aguas residuales tratadas, se alcanzó una remoción máxima experimental para la DQO del 79,9 % muy próximo al valor estimado (Tabla 5). El valor de la DBO se redujo en un 75 % y el índice de biodegradabilidad (IB) alcanzó un valor de 0,5 lo que supone una agua residual más fácilmente biodegradable. La acidificación de las muestras y posterior neutralización favoreció la reducción de la dureza en 81 %, alcalinidad en 96 % esto es debido al cambio de pH que promovió la formación de flóculos y precipitación de la materia orgánica coloidal arrastrando a su paso iones y moléculas, mejorando a su vez la turbiedad de la solución por la gran cantidad de sólidos totales removidos (88 %).
Composición Fisicoquímica después de la aplicación del proceso Fenton de las aguas residuales del camal de Chota
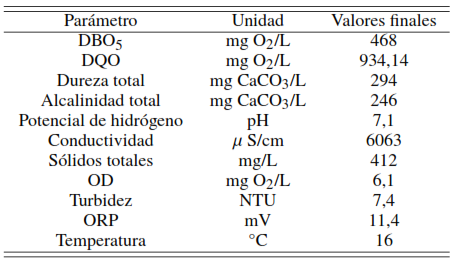
El incremento de la conductividad se debe a la adición de las sales ferrosas y sales formadas por la neutralización de las muestras tratadas a pesar de ser removidas mediante la generación de lodos es probable aun la presencia de sus iones. El ORP alcanzó valores positivos lo que indica que el agua tratada se encuentra en un entorno oxidante, es decir; la disminución considerable de la DQO en el agua residual después del tratamiento permite observar una mejora sustancial del OD.
Tras la aplicación del proceso Fenton el IB solo mejoró un 20 % , por ello cabe la posibilidad que durante la oxidación se hayan formado compuestos orgánicos de cadena corta con características recalcitrantes, sin embargo un tratamiento biológico posterior puede eventualmente dar solución a este inconveniente.
5. Conclusiones
Las aguas residuales de camales fueron tratadas mediante el proceso Fenton siguiendo el diseño Box–Benhken. El tiempo de reacción más adecuado se calculó en 18 minutos y fue necesario aplicar un tratamiento primario de desbaste a las aguas. La aplicación de la metodología de superficie de respuesta calculó una dosificación de 2110,55 mg/L de FeSO4, 1092,67 mg/L de H2O2 y un pH de 3,22, con ello se alcanzó una remoción máxima experimental de la DQO en 79,9 %. El análisis estadístico señala al pH como el factor de gran importancia en el proceso. Se notó una mejoría en el índice de biodegradabilidad (IB=0,5) en el agua residual tratada así como en todos sus parámetros estudiados. Por tanto la aplicación del proceso Fenton sobre aguas residuales de camales resulta efectivo.
Agradecimientos
Los autores agradecen a la Universidad Nacional Autónoma de Chota por el apoyo a través del I concurso de financiamiento de trabajos de investigación científica y tecnológica para docentes con recursos del canon.
7. Referencias
[1]D. Muñoz, “Sistema de tratamiento de aguas residuales de matadero: Para una población menor de 2000 habitantes,” Facultad de Ciencias Agropecuarias, vol. 3, no. 1, pp. 87–98, 2005.
[2]Y. Solarte, M. Peña, y C. Madera, “Transmisión de protozoarios patógenos a través del agua para consumo humano,” Colombia Médica, vol. 37, no. 1, pp. 75–82, 2006.
[3]A. Rajab, M. Salim, J. Sohaili, A. Anuar, Salmiati, and S. Lakkaboyana, “Performance of integrated anaerobic/aerobic sequencing batch reactor treating poultry slaugtherhouse wastewater,” Chemical Engineering Journal, vol. 313, pp. 967–974, 2017.
[4]V. Lahera, “Infraestructura sustentable: Las plantas de tratamiento de aguas residuales,” Quivera, vol. 12, no. 2, pp. 58–69, 2010.
[5]L. Becerra, M. Horna, y K. Barrionuevo, “Nivel de contaminación en los efluentes provenientes de camales de la región de la Libertad,” Revista del cuerpo médico del Hospital Nacional Almanzor Aguinaga Asenjo, vol. 7, no. 3, pp. 23–26, 2014.
[6]G. Salas y C. Condorhuamán, “Tratamiento de las aguas residuales de un centro de beneficio o matadero de ganado,” Revista Peruana de Química e Ingeniería Química, 2008.
[7]D. Borja, K. Salazar, y H. Brito, “Cuantificación de efluentes de aguas residuales del camal frigorífico Riobamba,” Ciencia Digital, vol. 3, no. 2, pp. 783–794, 2019.
[8] J. Sanz, J. Lombrana, y A. De Luis, “Estado del arte en la oxidación avanzada a efluentes industriales: nuevos dessarrollos futuras tendencias,” Afinidad–Barcelona, vol. 70, no. 561, pp. 25–33, 2013.
[9] O. Pourehie and J. Saien, “Homogeneous solar Fenton and alternative processes in a pilot-scale rotatable reactor for the treatment of petroleum refinery wastewater,” Process Safety and Enviromental Protection, vol. 135, pp. 236–243, 2020.
[10] G. Salas, “Tratamiento por oxidación avanzada (reacción Fenton) de aguas residuales de la industria textil,” Revista Peruana de Química e Ingeniería Química, vol. 13, no. 1, pp. 30–38, 2010.
[11] C. Kantar, O. Oral, O. Urken, N. Ayman, and S. Keskin, “Oxidative degradation of Chlorophenolic compounds with pyrite-Fenton process,” Envorimental Pollution, vol. 247, pp. 349–362, 2019.
[12] M. Taco y E. Mayorga, “Aplicación del proceso Fenton en la disminución de la materia orgánica en aguas residuales de la industria termoelectrica,” Química Central, vol. 3, no. 1, pp. 25–30, 2013.
[13] P. Bautista, A. Mohedano, M. Gilarranz, J. Casas, and J. Rodriguez, “Application of Fenton oxidation to cosmetic wastewater treatment,” Journal of Hazardous Materials, vol. 143, pp. 128–134, 2007.
[14] H. Zhao and C. Kong, “Elimination of pyraclostrobin by simultaneous microbial degradation coupled with the Fenton process in microbial fuel cells and the microbial community,” Bioresource Technology, vol. 258, pp. 227–233, 2018.
[15] Y. Quin, S. Luo, S. Geng, W. Jiao, and Y. Liu, “Degradation and mineralization of aniline by O3/Fenton process enhanced using high-gravity technology,” Chinese Journal of Chemical Engineering, vol. 26, no. 7, pp. 1444–1450, 2018.
[16] H. Lin, N. Oturan, J. Wu, H. Zhang, and M. Oturan, “Cold incineration of sucralose in aqueous solution by electro-Fenton process,” Separation and Purification Technology, vol. 173, pp. 218–225, 2017.
[17] J. Nercolini, D. Hoefling, V. Trevisan, and E. Eskoronsky, “Application of the Fenton and Fenton-Like processes in the landfill leachate tertiary treatment,” Journal of Environmental Chemical Engineering, vol. 7, no. 5, pp. 1–8, 2019.
[18] S. Sun, X. Zeng, C. Li, and A. Lemley, “Enhanced heterogeneous and homogeneous Fenton-like degradation of carbamazepine by nano-Fe3O4/H2O2 with nitrilotriacetic acid,” Chemical Engineering Journal, vol. 244, pp. 44–49, 2014.
[19] E. Neyens and J. Baeyens, “A review of classic Fenton´s peroxidation as an advanced oxidation technique,” Journal of Hazardous Materials, pp. 33–50, 2003.
[20] D. Al-Zubaidi and K. Pak, “Degradation parachlorophenol in syntetic wastewater using Batch Electro-Fenton process,” Materials today: Proceedings, vol. 20, pp. 414–419, 2020.
[21] M. Nalinrut, W. Chen, J. Anotai, and L. Ming-Chun, “Factors affecting degradation of o - toluidine by Fenton process,” Sustainable Enviroment Research, vol. 21, no. 2, pp. 101–107, 2011.
[22] A. Trovó, T. Silva, O. Gomes, A. Machado, W. Borge, P. Muller, and D. Daniel, “Degradation of caffeine by photo-Fenton process: Optimization of treatment conditions using experimental desing,” Chemosphere, vol. 90, pp. 170–175, 2013.
[23] W. Gernjak, S. Malato, M. Maldonado, and M. Fuerhacker, Solar photo-Fenton treatment of EU priority Substances- process parameters and control strategies. Madrid: Ed. Ciemat, 2006.
[24] G. Quille y T. Donaires, “Tratamiento de efluentes líquidos y sólidos del camal municipal de Ilave,” Revista Investigaciones Altoandinas, vol. 15, no. 1, pp. 65–72, 2013.
[25] C. Montgomery, Diseño y análisis de experimentos, 2nd ed. Limusa Wiley S.A. de C.V., 2004.
[26] P. Nakhate, H. Patil, and K. Marathe, “Intensification of landfill leachate treatment by advanced Fenton process using classical and statistical approach,” Chemical Engineering and Processing - Process Intensification, vol. 133, pp. 148–159, 2018.
[27] D. Gümüs and F. Akbal, “Comparison of Fenton and electro-Fenton processes for oxidation of phenol,” Process Safety and Enviromental Protection, vol. 103 parte A, pp. 252–258, 2016.
[28] S. Giray, M. Hakan, S. Akarsu, C. Ayhan, and M. Dolaz, “Comparison of classic Fenton with ultrasound Fenton processes on industrial textile wastewater,” Sustainable Enviroment Research, vol. 28, no. 4, pp. 165–170, 2018.
[29] J. Xu, Y. Long, D. Shen, H. Feng, and T. Chen, “Optimization of Fenton treatment process for degradation of refractory organics in pre-coagulated leachate membrane concentrates,” Journal of Hazardous Materials, vol. 323, pp. 674–680, 2016.
[30] N. Cintra, L. Barroso, G. Goncalves, S. Fleury, M. Soares, G. Rodríguez, and R. Neves, “Removal of azo dye using Fenton and Fenton-like processes: Evaluation of process factors by Box–Behnken design and ecotoxicity tests,” Chemico- Biological Interactions, vol. 291, pp. 47–54, 2018.
[31] D. Hermosilla, M. Cortijo, and C. Pao, “Optimizing the treatment of landfill leachate by conventional Fenton and photo-Fenton processes,” Science of the Total Enviroment, vol. 407, pp. 3473–3481, 2009.
[32] P. Castro y J. Duran, “Degradación y decoloración de agua contaminada con colorantes textiles mediante procesos de oxidación avanzada,” Tecnología en Marcha, vol. 27, no. 2, pp. 40–50, 2014.
[33] W. Zhang, H. Wang, and F. Wang, “Promotion of H2O2 descomposition activity over β-MnO2 nanorod catalysts,” Colloids and Surfaces A: Physicochemical and Engineering Aspects, vol. 304, pp. 60–66, 2007.
[34] J. Blanco, “Degradación de un efluente textil real mediante procesos Fenton y foto-Fenton,” Tesis de Master, Universidad Politécnica de Catalunya, España, 2009.
[35] L. Cabrera, S. Caldas, S. Rodrigues, A. Bianchini, F. Duarte, and E. Primel, “Degradation of herbicide diuron in water employing the Fe0/H2O2 system,” Journal of the Brazilian Chemical Society, vol. 21, no. 12, pp. 2347–2352, 2010.
[36] P. Ghosh, A. Samanta, and S. Ray, “COD reduction of petrochemical industry wastewater using Fenton´s oxidation,” The Canadian Journal of chemical Enginnering, vol. 88, no. 6, pp. 1021–1026, 2010.
[37] H. Ibarra, I. Drobosz, y M. Á. Gómez, “Optimización Multiobjetivo del proceso Fenton en el Tratamiento de Aguas Residuales provenientes de la Producción de Café Soluble,” Información Tecnológica, vol. 29, no. 5, pp. 111–122, 2018.
Notas de autor
wuriarte@unach.edu.pe
Enlace alternativo
http://servicio.bc.uc.edu.ve/ingenieria/revista/v27n2/art04.pdf (pdf)

