Revisión de Tema

Esta obra está bajo una Licencia Creative Commons Atribución 4.0 Internacional.
Recepción: 14 Agosto 2020
Aprobación: 23 Junio 2022
DOI: https://doi.org/10.29375/01237047.3966
Resumen: Introducción. La Organización Mundial de la Salud (OMS) estima que más del 40% de las mujeres embarazadas a nivel mundial tienen anemia, y la mitad de estas padecen deficiencia de hierro. La prevalencia en América Latina es del 40% y en Colombia del 44.7%. Fisiológicamente en el embarazo se produce una mal llamada “anemia dilucional”, existen condiciones en la embarazada que la predisponen a tener una anemia patológica. Esta última es causada principalmente por un déficit de hierro, de allí la importancia de diagnosticar a tiempo esta entidad e iniciar el manejo. La administración de hierro es la base del tratamiento de la anemia por deficiencia de hierro. Puede ser administrado por vía oral, la cual es la preferida en la mayoría de las pacientes; sin embargo, cuando este no es posible administrarlo, es esencial recurrir al hierro parenteral. No obstante, el hierro parenteral es poco usado como primera línea en el manejo de la anemia gestacional. El presente artículo tiene como objetivo realizar una revisión que permita identificar la terapia con hierro parenteral como una alternativa eficaz de manejo para la anemia gestacional, teniendo en cuenta las características farmacológicas, la administración y el uso entre las diferentes moléculas disponibles en Colombia. Metodología. Corresponde a un estudio de revisión de literatura en bases de datos y bibliotecas electrónicas, los criterios que se tuvieron en cuenta fueron textos publicados entre 1996 y 2020, en español e inglés. Se obtuvo un resultado de 95 artículos, de los cuales se seleccionaron 49. Las palabras clave para su búsqueda fueron fisiología, hierro parenteral, anemia gestacional, déficit de hierro, complicaciones del embarazo, compuestos de hierro, farmacocinética, diagnóstico y tratamiento. División de temas tratados. Fisiología; ayudas diagnósticas; características farmacológicas del hierro parenteral; ventajas, indicaciones y contraindicaciones del hierro parenteral; efectos secundarios y forma de aplicación. Conclusiones. El hierro parenteral es un tratamiento seguro y eficaz para manejar la anemia en el embarazo, se debe tener en cuenta las indicaciones y la farmacología de las moléculas para elegir la más adecuada. Además, repone más rápidamente las reservas de hierro y los niveles de hemoglobina.
Palabras clave: Anemia, Deficiencias de Hierro, Complicaciones del Embarazo, Fenómenos Fisiológicos Nutricionales Maternos, Compuestos de Hierro, Farmacocinética.
Abstract: Introduction. The World Health Organization (WHO) estimates that more than 40% of pregnant women worldwide have anemia, and that half of them suffer from iron deficiency. The prevalence of this in Latin America is 40%, and in Colombia, 44.7%. Physiologically, a problem called “dilutional anemia” occurs during pregnancy. There are conditions in pregnant women that predispose them to suffering from pathological anemia. The latter is mainly caused by iron deficiency, hence the importance of diagnosing this entity on time and starting treatment. Iron administration is the basis of treatment of anemia caused by iron deficiency. It can be administered orally, which is the preferred option in the majority of patients. However, when this is not possible, parenteral iron must be used. However, parenteral iron is rarely used as the first line of treatment of gestational anemia. The objective of this article is to carry out a review that allows for the identification of therapy with parenteral iron as an efficient alternative for the treatment for gestational anemia, considering the pharmacological characteristics, administration, and use among the different molecules available in Colombia. Methodology. We carried out a search in databases and electronic libraries. The criteria considered were texts published between 1996 and 2020 in Spanish and English. 95 articles were obtained, of which 49 were selected. The keywords for their search were physiology, parenteral iron, gestational anemia, iron deficit, pregnancy complications, iron compounds, pharmacokinetics, diagnosis, and treatment. Division of Covered Topics. Physiology; diagnostic aids; pharmacological characteristics of parenteral iron; advantages, indications, and contraindications of parenteral iron; secondary effects and application method. Conclusions. Parenteral iron is a safe and efficient treatment to handle anemia during pregnancy. The indications and pharmacology of the molecules must be considered to choose the most appropriate option. In addition, it replaces iron reserves and hemoglobin levels more quickly.
Keywords: Anemia, Iron Deficiencies, Pregnancy Complications, Maternal Nutritional Physiological Phenomena, Iron Compounds, Pharmacokinetics.
Resumo: Introdução. A Organização Mundial de Saúde (OMS) estima que mais de 40% das mulheres grávidas em todo o mundo são anêmicas, e metade delas sofre de deficiência de ferro. A prevalência na América Latina é de 40% e na Colômbia de 44.7%. Fisiologicamente na gravidez ocorre a chamada “anemia dilucional”, e existem condições na gestante que a predispõem a ter uma anemia patológica. Esta última é causada principalmente por deficiência de ferro, daí a importância de diagnosticar esta entidade a tempo e iniciar o manejo. A administração de ferro é a base do tratamento da anemia por deficiência de ferro. Pode ser administrado por via oral, o que é preferido pela maioria das pacientes; porém, quando não for possível administrá-lo dessa forma, é imprescindível recorrer ao ferro parenteral. No entanto, o ferro parenteral é raramente usado como primeira linha no manejo da anemia gestacional. O objetivo deste artigo é realizar uma revisão que permita identificar a terapia com ferro parenteral como uma alternativa eficaz de tratamento da anemia gestacional, levando em consideração as características farmacológicas, administração e uso entre as diferentes moléculas disponíveis na Colômbia. Metodologia. Foi realizada uma busca em bases de dados e bibliotecas eletrônicas, os critérios levados em consideração foram textos publicados entre 1996 e 2020, em espanhol e inglês. Foi obtido um total de 95 artigos, dos quais 49 foram selecionados. As palavras-chave para a busca foram fisiologia, ferro parenteral, anemia gestacional, deficiência de ferro, complicações na gravidez, compostos de ferro, farmacocinética, diagnóstico e tratamento. Divisão dos temas abordados. Fisiologia; auxiliares de diagnóstico; características farmacológicas do ferro parenteral; vantagens, indicações e contraindicações do ferro parenteral; efeitos colaterais e método de aplicação. Conclusões. O ferro parenteral é um tratamento seguro e eficaz para o manejo da anemia na gravidez, as indicações e farmacologia das moléculas devem ser levadas em consideração a fim de escolher a mais adequada. Além disso, reabastece mais rapidamente as reservas de ferro e os níveis de hemoglobina
Palavras-chave: Anemia, Deficiências de Ferro, Complicações na Gravidez, Fenômenos Fisiológicos da Nutrição Materna, Compostos de Ferro, Farmacocinética.
Introducción
Según la Organización Mundial de la Salud (OMS) y el American College of Obstetricians (ACOG), la anemia en el embarazo se define como un valor de hemoglobina por debajo de 11 g/dl (en primero y tercer semestre), 10.5 g/dl (en segundo semestre) y/o valor de hematocrito inferior al 33% (en primer y tercer trimestre) y 32% (segundo trimestre) (1).
Existe asociación entre la anemia en el embarazo y la morbilidad materna y perinatal (2); globalmente, el 20% de la mortalidad materna es por causas indirectas como la anemia (3), adicionalmente, la OMS estima que más del 40% de las embarazadas en el mundo tienen anemia, el 50% de la cifra se da debido a deficiencia de hierro, esta causa es más común en países en vía de desarrollo debido a la malnutrición en estos países (4). A nivel mundial, el 52% de las embarazadas en países subdesarrollados tienen anemia, en comparación con el 20% de países industrializados. Los lugares con prevalencias más altas son India (88%), África (50%), América Latina (40%), y el Caribe (30%) (5); en el continente americano la prevalencia se encuentra alrededor del 60%; sin embargo, varía de un país a otro, dependiendo de los factores de riesgo, como la malnutrición, malaria etc. (6). En Colombia, el valor es de 44.7% de la población gestante (7). La anemia se presenta mayormente en la zona rural y en estratos 1 y 2 del Sistema de Identificación de Potenciales Beneficiarios de Programas Sociales (SISBEN). Las regiones con más afectación son la zona pacífica, la oriental y el atlántico (8).
En Colombia se recomienda el uso de suplemento de hierro más ácido fólico en todas las embarazadas, excepto cuando cuentan con valores de hemoglobina superiores a 14g/dL, ya que se considera que la mujer que maneja estos valores tiene buenas reservas de hierro (9).
Los factores de riesgo de la anemia por deficiencia de hierro en el embarazo son ser donante de sangre, ser vegetariano, tener una dieta pobre en hierro, embarazo múltiple, dieta rica en fósforo, enfermedades gastrointestinales malabsortivas, enfermedades tropicales, bajo nivel socioeconómico e inadecuados controles prenatales (10). La anemia genera complicaciones maternas y fetales, como infecciones urinarias, retraso en el crecimiento intrauterino, bajo peso al nacer, preeclampsia, parto prematuro, ruptura prematura de membranas, aborto espontáneo, entre otras (11). En la Tabla 1 se especifican los efectos de la anemia en el embarazo y el neonato.
Para el diagnóstico de la anemia gestacional se necesita un cuadro hemático con el fin de documentar los niveles de hemoglobina, el volumen corpuscular medio y la concentración media de hemoglobina. Adicionalmente, la determinación del nivel de ferritina sérica es suficiente para el diagnóstico de anemia por deficiencia de hierro. Un valor de < 30 µg/L es evidencia de reservas de hierro agotadas y anemia por deficiencia de hierro. Para niveles de ferritina sérica normales y/o elevados, se deben investigar otras causas posibles (p. ej., hemoglobinopatías como β-talasemia, anemia de células falciformes, anemia por infección, anemia hemorrágica, etc.) (12).
El ACOG recomienda el consumo de 60mg/día de hierro ferroso elemental. A pesar de que el hierro oral juega un papel vital en el tratamiento de la anemia en gestantes, su absorción se ve afectada por ciertos alimentos o fármacos. Además, su consumo oral causa efectos gastrointestinales, lo que limita la adherencia y control del índice eritrocitario. Debido a esto y a la prevalencia de la anemia, es importante conocer el debido uso de la terapia parenteral con hierro. El objetivo central de esta revisión es dar a conocer la terapia con hierro parenteral como una alternativa eficaz de manejo para la anemia en el embarazo, teniendo en cuenta las características farmacológicas, posología y disponibilidad.
Tabla 1.Efectos de la anemia durante el embarazo, en la madre y sus hijos.
Efectos de la anemia durante el embarazo en la madre y sus hijos

Fuente: elaborado por los autores (40-43).
Metodología
Corresponde a un estudio de revisión en bases de datos y bibliotecas electrónicas, tales como: PubMed, LILACS, UpToDate, Ovid, ELSEVIER, SciELO y ClinicalKey, con una ventana de tiempo personalizado entre 1996 y 2020, en inglés y español. Se usaron las palabras claves: fisiología; hierro parenteral, anemia gestacional, déficit de hierro, complicaciones del embarazo, compuestos de hierro, farmacocinética, diagnóstico, y tratamiento. Se obtuvo un resultado de 95 artículos, posteriormente se realizó un resumen analítico, se seleccionaron 49 artículos.
División de temas tratados
Fisiología
Los cambios hematológicos generados en el embarazo ocasionan el aumento del volumen plasmático de manera exponencial de acuerdo a las edades gestacionales; esta expansión comienza desde la sexta semana de gestación y continúa hasta alcanzar su máximo valor de aproximadamente el 40%-50% a la semana 24 de gestación, para luego estabilizarse o disminuir ligeramente al final del embarazo (13,14). La masa de eritrocitos aumenta levemente en el embarazo como resultado de niveles altos de eritropoyetina en respuesta a la progesterona circulante y al lactógeno placentario (15). El aumento marcado del volumen plasmático provoca una disminución significativa del hematocrito y la hemoglobina (Hb), lo cual se hace más evidente desde el segundo trimestre hasta finalizar la gestación.
Durante el embarazo, las mujeres cursan con una mayor demanda de niveles séricos de hierro debido al aumento en la eritropoyesis por la acción de la progesterona y el lactógeno Carboximaltosa férrica tienen un alto peso molecular, por lo tanto, suministran el hierro a la transferrina de forma regulada. Por lo que son clínicamente bien tolerados, incluso a dosis altas. Los complejos tipo II, como el hierro sacarosa, liberan grandes cantidades de hierro débilmente unido en la sangre; a pesar de su menor peso molecular y estabilidad, estos siguen siendo adecuados para la aplicación intravenosa. Sin embargo, las dosis únicas máximas son significativamente más bajas y los tiempos de administración son drásticamente más largos (21) (Tabla 2).
Tabla 2.Diferencias farmacológicas entre el hierro sacarosa, la carboximaltosa férrica y el hierro dextrano.
Diferencias farmacológicas entre el hierro sacarosa la carboximaltosa férrica y el hierro dextrano
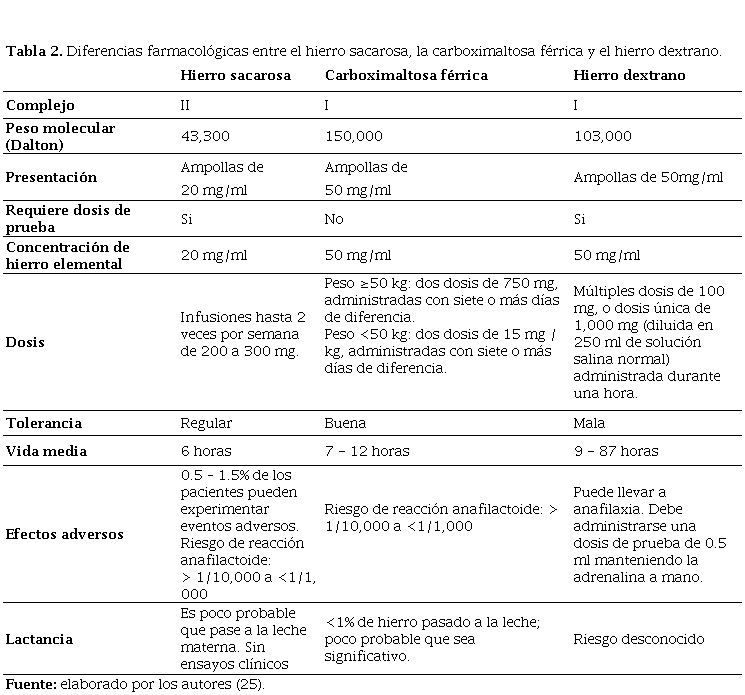
Fuente: elaborado por los autores (25).
Ventajas, indicaciones y contraindicaciones del hierro parenteral
El tratamiento con hierro parenteral está indicado a partir del segundo trimestre del embarazo en pacientes con baja adherencia al tratamiento oral, cuando no hay tolerancia al hierro oral, en casos de malabsorción comprobada y en aquellas que tienen anemia severa y se requiere de una recuperación rápida de la hemoglobina (22).
Una ventaja del hierro parenteral es la rápida reposición de las reservas de hierro, mientras que utilizar la terapia oral puede llevar meses. Un metaanálisis realizado por Burwick et al. (23) en el año 2018, tenía como objetivo evaluar los beneficios del hierro intravenoso en el embarazo, incluyeron once ensayos clínicos aleatorizados que compararon el hierro intravenoso con el oral para el tratamiento de la anemia por deficiencia de hierro en el embarazo; las mujeres embarazadas que recibieron hierro intravenoso, en comparación con el hierro oral, tuvieron los siguientes beneficios: alcanzaron el objetivo de hemoglobina con mayor frecuencia, razón de probabilidades (OR) agrupada de 2.66 (intervalo de confianza [IC] del 95%: 1.71-4.5), p < 0.001; aumento del nivel de hemoglobina después de 4 semanas, diferencia de medias ponderada agrupada de 0.84 g/dl (IC del 95%: 0.59 a 1.09), p < 0.001; disminución de las reacciones adversas, OR combinado 0.35 (IC del 95%: 0.18-0.67), p = 0.001]. Se concluyó que el hierro parenteral fue más eficaz, alcanzó más rápidamente los niveles normales de hemoglobina y reportó menos efectos adversos comparado con el tratamiento oral.
Breyman et al. (24) realizaron un ensayo clínico aleatorizado, publicado en el año 2017, con el objetivo de comparar la eficacia y seguridad de la carboximaltosa férrica intravenosa con el sulfato ferroso oral de primera línea en mujeres embarazadas con anemia por deficiencia de hierro, los objetivos secundarios tuvieron en cuenta la seguridad y la calidad de vida. Incluyeron 252 mujeres entre 16 y 33 semanas gestacionales. Se encontró que los niveles de hemoglobina mejoraron a tasas comparables en ambos tratamientos; sin embargo, significativamente más mujeres lograron la corrección de la anemia con carboximaltosa férrica frente al sulfato ferroso [Hb ≥11.0 g/ dL; 84% frente a 70%; razón de probabilidades (OR): 2.06, intervalo de confianza (IC) del 95%: 1.07, 3.97; p= 0.031] y dentro de un marco de tiempo más corto (mediana de 3.4 frente a 4.3 semanas). El tratamiento con carboximaltosa férrica mejoró significativamente la vitalidad (p= 0.025) y el funcionamiento social (p= 0.049) antes del parto. Los eventos adversos relacionados con el tratamiento fueron experimentados por 14 (11% con carboximaltosa férrica) y 19 (15% con sulfato ferroso) mujeres, con tasas marcadamente más altas de trastornos gastrointestinales informados con sulfato ferroso (16 mujeres) que con carboximaltosa férrica (3 mujeres). Se concluye que la carboximaltosa férrica intravenosa mejora la anemia en embarazadas en un tiempo más corto en comparación con el sulfato ferroso oral, además el tratamiento parenteral mejoró la calidad de vida, funcionamiento social y no se reportaron efectos adversos en el recién nacido.
Se ha encontrado que el hierro sacarosa tiene pocas propiedades alergénicas, baja incidencia de efectos adversos severos como reacciones anafilácticas, tiene un buen perfil de seguridad para las embarazadas con una frecuencia de efectos adversos del 0.36%. Adicional a esto, tiene una alta disponibilidad para la eritropoyesis, poca excreción renal (<5%) y baja acumulación tisular y toxicidad (25).
Se ha encontrado que las mujeres embarazadas que recibieron hierro parenteral en comparación con las que se les administró hierro por vía oral, alcanzaron la hemoglobina (Hb) objetivo con más frecuencia, tuvieron un aumento de la Hb después de 4 semanas y reportaron menos efectos secundarios [OR 0.35, IC 95%: 0.23–0.53, p < 0.001] como la anafilaxia, o el colapso circulatorio (22). Sumado a esto, se ha demostrado que el hierro parenteral tiene beneficios a largo plazo, prolongando el periodo de lactancia materna [p = 0.04], un mejor estado general con menos cansancio [p = 0.005] y menos depresión postnatal [p = 0.003] en comparación con las mujeres que recibieron hierro oral (26).
Teniendo en cuenta las contraindicaciones para el uso del hierro parenteral, se recomienda que los pacientes con múltiples alergias medicamentosas reciban una dosis de glucocorticoide antes de la infusión de hierro para reducir la probabilidad de que ocurran reacciones alérgicas (27,28). La administración de hierro parenteral se debe evitar en pacientes con menos de 12 semanas de gestación, ya que no hay ensayos que confirmen su seguridad en el primer trimestre, además, debe hacerse solo en sitios con personal entrenado y equipados con elementos de reanimación. Todo el personal debe recibir capacitación actualizada en el manejo de infusiones de hierro intravenoso y sus potenciales reacciones adversas. Se debe proporcionar información al paciente sobre el riesgo de una reacción adversa antes de administrar el hierro parenteral. Se deben verificar los factores de riesgo del paciente para una reacción de hipersensibilidad, como lo son el haber tenido una reacción previa a hierro intravenoso, historia de múltiples alergias, asma severa y enfermedad respiratoria, cardiaca o enfermedad hepática descompensada. También se debe monitorizar durante la infusión el estado general del paciente, su presión arterial, frecuencia cardiaca y frecuencia respiratoria (29,30).
Efectos secundarios
El uso de hierro parenteral se ha visto asociado con muy pocos efectos secundarios al compararse con el hierro oral. Las estadísticas muestran que un 26% de pacientes que recibieron hierro parenteral experimentaban efectos secundarios; sin embargo, la mayoría de estos eran leves y autolimitados. Únicamente un 3% de los pacientes presentan efectos adversos más severos, entre los cuales solo un 0.1% a 0.6% desarrollan una anafilaxia que compromete la vida de la paciente (31) (Tabla 3).
Tabla 3. Efectos adversos según fármacos intravenosos (IV).
Efectos adversos según fármacos intravenosos IV
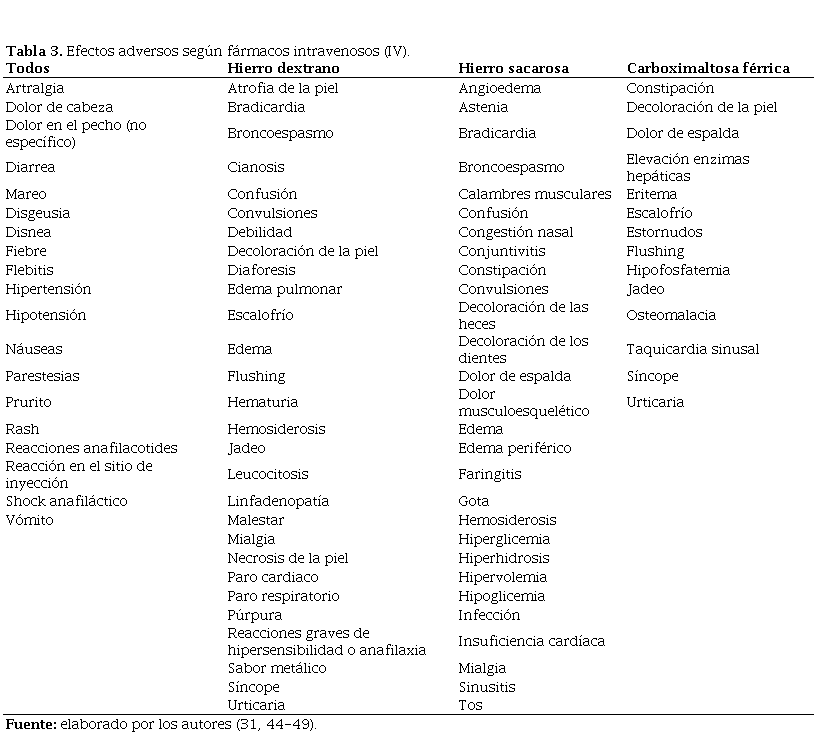
Fuente: elaborado por los autores (31,44-49).
Forma de aplicación
La administración de hierro parenteral debe hacerse bajo estricta monitorización de la paciente. La dosis de hierro administrada va a depender del objetivo del tratamiento: reponer las reservas de hierro y/o tratar la anemia. Cualquiera de los dos objetivos mencionados tendrá en cuenta el peso de la paciente, el nivel actual de hemoglobina y la cantidad de hierro elemental por mililitro del producto escogido para la aplicación. La dosis y la administración dependen de la preparación escogida para el tratamiento.
Existen dos métodos para determinar la dosis que debe ser administrada a cada paciente teniendo en cuenta las características mencionadas con anterioridad: la fórmula de Ganzoni y el método simplificado (32).
Fórmula de Ganzoni
Déficit total de hierro/dosis acumulativa de hierro (mg) = peso corporal* (Kg) x (Hb objetivo - Hb actual en g/dL) x 0.24** + depósito de hierro (mg)***
*En pacientes con sobrepeso debe usarse el peso ideal. Si son pacientes con bajo peso, usar el peso actual.
**El factor 0.24 proviene de = 0.0034 x 0.07 x 1,000.
Donde el contenido de hierro en Hb = 0.34%. Volumen sanguíneo = 7% del peso corporal, y 1,000 es la conversión de g a mg.
***Depósito de hierro: <35 Kg de peso corporal: depósito de hierro = 15 mg/Kg peso corporal. ≥35 kg de peso corporal: depósito de hierro = 500 mg (32).
Método simplificado
La siguiente tabla puede ser utilizada para estimar la cantidad acumulativa de hierro requerida para suplir las reservas corporales de hierro para los pacientes con un peso corporal ≥ 35 kg (Tabla 4).
Tabla 4. Cantidad acumulativa de hierro requerida para suplir las reservas corporales de hierro para los pacientes con un peso corporal ≥ 35 kg.
Cantidad acumulativa de hierro requerida para suplir las reservas corporales de hierro para los pacientes con un peso corporal ≥ 35 kg
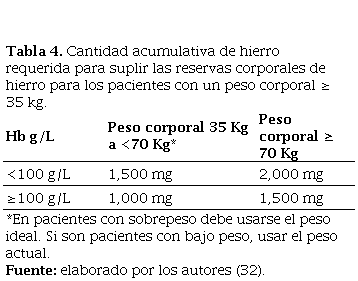
Fuente: elaborado por los autores (32).
Este método debe usarse con precaución debido a que es basado en un solo ensayo clínico multicéntrico, realizado por Rayko Evstatiev, et al., en adultos con enfermedad inflamatoria intestinal con un promedio de hemoglobina de 104 g/L y un peso corporal ≥ 35 kg (33).
Después de calcular las necesidades de la paciente, hay que tener en cuenta las formas de aplicación de cada producto:
● Hierro dextrano (de bajo peso molecular)
Puede administrarse de dos formas: la primera, múltiples dosis de 2 ml lo que equivale a 100 mg de hierro elemental.
Y la segunda, una dosis única de infusión de 1,000 mg en 250 ml de SSN durante una hora. Esta última ha mostrado ser segura y efectiva en diferentes escenarios de sangrado uterino excesivo, embarazo, postparto y otras (34–36). Requiere una dosis de prueba de 0.5 ml que correspondería a 25 mg.
● Hierro sacarosa
Puede administrarse hasta 2 veces por semana en dosis de 200 a 300 mg, con una dosis única máxima de 200 mg. El tiempo de perfusión debe ser de 100 mg en 15 min, y de 200 mg en 30 min (37). Requiere una dosis de prueba de 25 mg en 15 min.
● Carboximaltosa férrica
Si el peso de la paciente es ≥50 kg se administran dos dosis de 750 mg, aplicadas con siete o más días de diferencia. Si el peso de la paciente es <50 Kg se disponen dos dosis de 15 mg/Kg, administradas igualmente con los siete días de diferencia. Es importante resaltar que la dosis única máxima es de 1,000 mg o 15 mg/Kg. El tiempo de perfusión debe ser de 200 mg en bolo, y 1,000 mg en 15 min. No requiere de una dosis de prueba (37).
Para pacientes con asma o más de una reacción alérgica a algún medicamento, es decir, pacientes que se encuentran con un riesgo mayor de tener una reacción adversa a la administración de hierro intravenoso, se recomienda administrar 125 mg de metilprednisolona y un antihistaminérgico H2 por vía intravenosa antes de iniciar la administración intravenosa del producto escogido. En pacientes con historia de artritis inflamatoria se recomienda la administración de metilprednisolona 125 mg intravenoso y la prescripción de un curso corto de prednisona (1 mg/kg al día vía oral por 4 días) (38).
Antes de iniciar la infusión deberá informarse del procedimiento y su duración a la paciente y aclarar las dudas que tenga al respecto. Debe vigilarse por lo menos durante 30 minutos después de la administración, teniendo en cuenta los efectos secundarios que dependen de la cantidad de hierro soluble en el tracto gastrointestinal como cefalea, urticaria, prurito, dolor torácico, náuseas, vómito, diarrea, epigastralgia y edema periférico (37).
Para evidenciar mejoría en los valores de hemoglobina es necesario solicitar un cuadro hemático 2 semanas después de aplicada la última dosis del hierro total calculado. La ferritina generalmente se normaliza inmediatamente después de administrar la terapia, por ende, no es necesario hacerle seguimiento a este parámetro.
Con respecto a los costos de cada fármaco se encontró que 100 mg de hierro sacarosa I.V (Venofer®, Vifor) fue de 219 euros o 916,077 pesos colombianos (COP), y 437 euros o 1,827,971 COP para 1,000 mg de carboximaltosa IV (Ferinject®, Vifor). Además, se debe tener en cuenta el valor agregado de utensilios utilizados, el cual fue calculado en 1.3 euros o 54,379 COP por infusión (39).
Conclusión
El hierro parenteral es una alternativa segura y eficaz en el tratamiento de la anemia durante la gestación cuando no es posible administrarlo de forma oral o cuando se requiere de una recuperación rápida de la hemoglobina. Este repone más rápidamente las reservas de hierro y los niveles de hemoglobina; presenta menos efectos adversos tanto para la madre como para el recién nacido; mejora la calidad de vida y el funcionamiento social; prolonga el tiempo de lactancia materna y disminuye la depresión postnatal. Hay 3 tipos de moléculas disponibles en Colombia: el hierro sacarosa, la carboximaltosa férrica y el hierro dextrano. Todas con la misma eficacia, pero con diferente farmacocinética, por lo tanto, la dosis, la tolerabilidad y la vigilancia son diferentes en cada una, a partir de este principio se puede escoger la ideal para cada paciente.
Agradecimientos
Se agradece a las personas participantes en el estudio.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Financiación
Para la realización de este estudio no existió ningún tipo de financiación externa a los autores.
Referencias
1. American College of Obstetricians and Gynecologists. ACOG Practice Bulletin No. 95: Anemia in Pregnancy. Obstet Gynecol [Internet]. 2008;112(1):201-7. doi: https://doi.org/10.1097/AOG.0b013e3181809c0d
2. Smith C, Teng F, Branch E, Chu S, Joseph KS. Maternal and Perinatal Morbidity and Mortality Associated With Anemia in Pregnancy. Obstet Gynecol [Internet]. 2019;134(6):1234-44. doi: https://doi.org/10.1097/AOG.0000000000003557
3. World Health Organization. Maternal health. [Internet] Ginebra: WHO; 2022 [citado 29 de junio de 2022]. Recuperado a partir de: https://www.who.int/health-topics/maternal-health#tab=tab_1
4. World Health Organization. Antenatal iron supplementation. [Internet]. Ginebra: WHO; 2022 [citado 29 de junio de 2022]. Recuperado a partir de: https://www.who.int/data/nutrition/nlis/info/antenatal-iron-supplementation
5. Lee AI, Okam MM. Anemia in pregnancy. Hematol Oncol Clin N Am [Internet]. 2011;25(2):241-59. doi: https://doi.org/10.1016/j.hoc.2011.02.001
6. Becerra C, Gonzáles GF, Villena A, de la Cruz D, Florián A. Prevalencia de anemia en gestantes, Hospital Regional de Pucallpa, Perú. Rev Panam Salud Pública [Internet]. 1998;3(5):285-92. doi: https://doi.org/10.1590/S1020-49891998000500001
7. Rincón-Pabón D, Urazán-Hernández Y, González-Santamaría J. Prevalencia y factores sociodemográficos asociados a anemia ferropénica en mujeres gestantes de Colombia (análisis secundario de la ENSIN 2010). Nutr Hosp [Internet]. 2019;36(1):87-95. doi: https://doi.org/10.20960/nh.1895
8. Instituto Colombiano de Bienestar Familiar. ENSIN: Encuesta Nacional de Situación Nutricional [Internet]. ICBF. [citado 2 de enero de 2021]. Recuperado a partir de: https://www.icbf.gov.co/bienestar/nutricion/encuesta-nacional-situacion-nutricional
9. Gómez-Sánchez PI, Arévalo-Rodríguez I, Rubio-Romero JA, Amaya-Guío J, Osorio-Castaño JH, Buitrago-Gutiérrez G, et al. Guías de Práctica Clínica para la prevención, detección temprana y tratamiento de las complicaciones del embarazo, parto o puerperio: introducción y metodología. Rev Colomb Obstet Ginecol [Internet]. 2013;64(3):234-4. doi: https://doi.org/10.18597/rcog.105
10. Espitia-De La Hoz F, Orozco-Santiago L. Anemia en el embarazo, un problema de salud que puede prevenirse. Médicas UIS [Internet]. 2013;26(3):45-50. Recuperado a partir de: https://revistas.uis.edu.co/index.php/revistamedicasuis/article/view/3920
11. Vilalba-Cerquera YF, Vanegas-Torres SV, Pérez ML, Peralta MM, Rivera JD, Galindo JD, et al. Caracterización de la población con anemia en el embarazo y su asociación con la morbimortalidad perinatal. Rev Méd de Risaralda [Internet]. 2019;25(1):30-39. doi: https://doi.org/10.22517/253 95203.18441
12. Breymann C, Honegger C, Hösli I, Surbek D. Diagnosis and treatment of iron-deficiency anaemia in pregnancy and postpartum. Arch Gynecol Obstet [Internet]. 2017;296:1229-1234. doi: https://doi.org/10.1007/s00404-017-4526-2
13. de Haas S, Ghossein-Doha C, van-Kuijk SMJ, van- Drongelen J, Spaanderman MEA. Physiological adaptation of maternal plasma volume during pregnancy: a systematic review and meta- analysis. Ultrasound Obstet Gynecol [Internet]. 2017;49(2):177-87. doi: https://doi.org/10.1002/uog.17360
14. Vricella LK. Emerging understanding and measurement of plasma volume expansion in pregnancy. Am J Clin Nutr [Internet]. 2017;106(6):1620S-1625S. doi: https://doi.org/10.3945/ajcn.117.155903
15. Sun D, McLeod A, Gandhi S, Malinowski AK, Shehata N. Anemia in Pregnancy: A Pragmatic Approach. Obstet Gynecol Surv [Internet]. 2017;72(12):730-7. doi: https://doi.org/10.1097/OGX.0000000000000510
16. Means RT. Iron Deficiency and Iron Deficiency Anemia: Implications and Impact in Pregnancy, Fetal Development, and Early Childhood Parameters. Nutrients [Internet]. 2020;12(2):447. doi: https://doi.org/10.3390/nu12020447
17. Milman N. Prepartum anaemia: prevention and treatment. Ann Hematol [Internet]. 2008;87(12):949- 59. doi: https://doi.org/10.1007/s00277-008-0518-4
18. Kalaimani-Rabindrakumar MS, Pujitha- Wickramasinghe V, Gooneratne L, Arambepola C, Senanayake H, Thoradeniya T. The role of haematological indices in predicting early iron deficiency among pregnant women in an urban area of Sri Lanka. BMC Hematol [Internet]. 2018;18-37. doi: https://doi.org/10.1186/s12878-018-0131-2
19. Milman N. Fisiopatología e impacto de la deficiencia de hierro y la anemia en las mujeres gestantes y en los recién nacidos/infantes. Rev Perú Ginecol Obstet [Internet]. 2012;58:293-312. doi: https://doi.org/10.31403/rpgo.v58i47
20. Auerbach M, Adamson JW. How we diagnose and treat iron deficiency anemia. Am J Hematol [Internet]. 2016;91:31-8. doi: https://doi.org/10.1002/ajh.24201
21. Geisser P, Burckhardt S. The pharmacokinetics and pharmacodynamics of iron preparations. Pharmaceutics [Internet]. 2011;3(1):12-33. doi: https://doi.org/10.3390/pharmaceutics3010012
22. Pavord S, Daru J, Prasannan N, Robinson S, Stanworth S, Girling J, et al. UK guidelines on the management of iron deficiency in pregnancy. Br J Haematol [Internet]. 2020;188:819-30. doi: https://doi.org/10.1111/bjh.16221
23. Govindappagari S, Burwick RM. Treatment of Iron Deficiency Anemia in Pregnancy with Intravenous versus Oral Iron: Systematic Review and Meta- Analysis. Am J Perinatol [Internet]. 2019;36(4):366-76. doi: https://doi.org/10.1055/s-0038-1668555
24. Breymann C, Milman N, Mezzacasa A, Bernard R, Dudenhausen J. Ferric carboxymaltose vs. oral iron in the treatment of pregnant women with iron deficiency anemia: an international, open-label, randomized controlled trial (FER-ASAP). J Perinat Med [Internet]. 2017;45(4):443-53. doi: https://doi.org/10.1515/jpm-2016-0050
25. Breymann C. Iron Deficiency and Anaemia in Pregnancy: Modern Aspects of Diagnosis and Therapy. Blood Cells Mol Dis [Internet]. 2002;29(3):506-16. doi: https://doi.org/10.1006/bcmd.2002.0597
26. KhalafallahAA, DennisAE. Iron deficiency anaemia in pregnancy and postpartum: pathophysiology and effect of oral versus intravenous iron therapy. J Pregnancy [Internet]. 2012;630519. doi: https://doi.org/10.1155/2012/630519
27. Auerbach M, Landy HJ. Anemia in pregnancy. UpToDate. [Internet]. Recuperado a partir de: https://www.uptodate.com/contents/anemia-in-pregnancy?search=ANEMIA%20IN%20PREGNANCY&source=search_result&selectedTitle=1~150&usa getype=default&display_rank=1
28. Camaschella C. Iron-deficiency anemia. N Engl J Med [Internet]. 2015;372(19):1832-43. doi: https://doi.org/10.1056/NEJMra1401038
29. Rampton D, Folkersen J, Fishbane S, Hedenus M, Howaldt S, Locatelli F, et al. Hypersensitivity reactions to intravenous iron: guidance for risk minimization and management. Haematologica [Internet]. 2014;99(11):1671-6. doi: https://doi.org/10.3324/haematol.2014.111492
30. Taylor S, Rampton D. Treatment of iron deficiency anemia: practical considerations. Pol Arch Med Wewn [Internet]. 2015;125(6):452-60. doi: https://doi.org/10.20452/pamw.2888
31. Burns DL, Pomposelli JJ. Toxicity of parenteral iron dextran therapy. Kidney Int Suppl [Internet]. 1999;55(69):S119-24. doi: https://doi.org/10.1046/j.1523-1755.1999.055suppl.69119.x
32. National Blood Authority. Iron product choice and dose calculation guide for adults [Internet]. Australia; 2022. [citado 30 de junio de 2022]. Recuperado a partir de: https://www.blood.gov.au/iron-product-choice-and-dose-calculation-guide-adults
33. Evstatiev R, Marteau P, Iqbal T, Khalif IL, Stein J, Bokemeyer B, et al. FERGIcor, a Randomized Controlled Trial on ferric carboxymaltose for Iron Deficiency Anemia in Inflammatory Bowel Disease. Gastroenterology [Internet]. 2011;141(3):846-853.e1-2. doi: https://doi.org/10.1053/j.gastro.2011.06.005
34. Auerbach M, Pappadakis JA, Bahrain H, Auerbach SA, Ballard H, Dahl NV. Safety and efficacy of rapidly administered (one hour) one gram of low molecular weight iron dextran (INFeD) for the treatment of iron deficient anemia. Am J Hematol [Internet]. 2011;86(10):860-2. doi: https://doi.org/10.1002/ajh.22153
35. Auerbach M, Winchester J, Wahab A, Richards K, McGinley M, Hall F, et al. A randomized trial of three iron dextran infusion methods for anemia in EPO-treated dialysis patients. Am J Kidney Dis [Internet]. 1998;31(1):81-6. doi: https://doi.org/10.1053/ajkd.1998.v31.pm9428456
36. Ondo WG. Intravenous iron dextran for severe refractory restless legs syndrome. Sleep Med. 2010;11(5):494-6. doi: https://doi.org/10.1016/j.sleep.2009.12.002
37. Álvarez Vega DM, Espinosa LA. Guía de práctica clínica (gpc): manejo de anemia en el embarazo y el puerperio en el Hospital Local del Norte – E.S.E. ISABU. 2018.
38. Auerbach M, Chaudhry M, Goldman H, Ballard H. Value of methylprednisolone in prevention of the arthralgia-myalgia syndrome associated with the total dose infusion of iron dextran: a double blind randomized trial. J Lab Clin Med [Internet]. 1998;131(3):257-60. doi: https://doi.org/10.1016/s0022-2143(98)90098-1
39. Bager P, Dahlerup JF. The health care cost of intravenous iron treatment in IBD patients depends on the economic evaluation perspective. J Crohns Colitis [Internet]. 2010;4(4):427-30. doi: https://doi.org/10.1016/j.crohns.2010.01.007
40. Wiegersma AM, Dalman C, Lee BK, Karlsson H, Gardner RM. Association of Prenatal Maternal Anemia With Neurodevelopmental Disorders. JAMA Psychiatry [Internet]. 2019;76(12):1294-304. doi: https://doi.org/10.1001/jamapsychiatry.2019.2309
41. Meinzen-Derr JK, Guerrero ML, Altaye M, Ortega-Gallegos H, Ruiz-Palacios GM, Morrow AL. Risk of infant anemia is associated with exclusive breast-feeding and maternal anemia in a Mexican cohort. J Nutr [Internet]. 2006;136(2):452-8. doi: https://doi.org/10.1093/jn/136.2.452
42. Henly SJ, Anderson CM, Avery MD, Hills-Bonuyk SG, Potter S, Duckett LJ. Anemia and Insufficient Milk in First-Time Mothers. Birth [Internet]. 1995;22(2):87-92. doi: https://doi.org/10.1111/ j.1523-536x.1995.tb00565.x
43. Beard JL, Hendricks MK, Perez EM, Murray-Kolb LE, Berg A, Vernon-Feagans L, et al. Maternal iron deficiency anemia affects postpartum emotions and cognition. J Nutr [Internet]. 2005;135(2):267-72. doi: https://doi.org/10.1093/jn/135.2.267
44. Radhika AG, Sharma AK, Perumal V, Sinha A, Sriganesh V, Kulshreshtha V, et al. Parenteral Versus Oral Iron for Treatment of Iron Deficiency Anaemia During Pregnancy and post-partum: A Systematic Review. J Obstet Gynaecol India [Internet]. 2019;69:13-24. doi: https://doi.org/10.1007/s13224-018-1191-8
45. Neogi SB, Devasenapathy N, Singh R, Bhushan H, Shah D, Divakar H, et al. Safety and effectiveness of intravenous iron sucrose versus standard oral iron therapy in pregnant women with moderate-to-severe anaemia in India: a multicentre, open-label, phase 3, randomised, controlled trial. Lancet Glob Health [Internet]. 2019;7(12):e1706-16. doi: https://doi.org/10.1016/S2214-109X(19)30427-9
46. Gilmartin CE, Hoang T, Cutts BA, Leung L. Retrospective cohort study comparing the adverse reactions and efficacy of intravenous iron polymaltose with ferric carboxymaltose for iron deficiency anemia. Int J Gynaecol Obstet [Internet]. 2018;141(3):315-20. doi: https://doi.org/10.1002/ijgo.12476
47. Cançado RD, Novis-de Figueiredo PO, Olivato MCA, Chiattone CS. Efficacy and safety of intravenous iron sucrose in treating adults with iron deficiency anemia. Rev Bras Hematol Hemoter [Internet]. 2011;33(6):439-43. doi: https://doi.org/10.5581/1516-8484.20110119
48. Zoller H, Schaefer B, Glodny B. Iron-induced hypophosphatemia: an emerging complication. Curr Opin Nephrol Hypertens [Internet]. 2017;26(4):266-75. doi: https://doi.org/10.1097/MNH.0000000000000329
49. Huang LL, Lee D, Troster SM, Kent AB, Roberts MA, Macdougall IC, et al. A controlled study of the effects of ferric carboxymaltose on bone and haematinic biomarkers in chronic kidney disease and pregnancy. Nephrol Dial Transplant [Internet]. 2018;33:1628-35. doi: https://doi.org/10.1093/ndt/gfx310
Notas de autor
Andrea Valentina López Acevedo. Universidad Autónoma de Bucaramanga. Calle 100 #36-39, casa 98, CP 680003. Bucaramanga, Santander, Colombia. Email. alopez426@unab.edu.co.
Información adicional
¿Qué se sabe del tema?: • La anemia en el embarazo es un factor que se debe tener en cuenta dado que somos una región con factor de riesgo para la misma, su elevada frecuencia y las complicaciones que puede llegar a generar en el binomio madre-hijo. • Para el correcto diagnóstico, contamos con cuadro hemático o niveles de ferritina (por déficit de hierro). • Las opciones terapéuticas para tratar esta patología son la terapia oral, como primera línea de tratamiento, sin embargo, presenta algunas limitaciones, por lo que conocer las aplicaciones del hierro parenteral son de gran ayuda para tratar de manera adecuada a los pacientes.
¿Qué aporta de nuevo?: • Se expone desde diferentes puntos de vista la temática de la anemia gestacional (Fisiológico, patológico, farmacológico, etc.), para que se pueda alcanzar un mayor entendimiento del tema tratado y como esta se desarrolla. • Se dieron a conocer cuáles eran las opciones y beneficios que trae el tratamiento con hierro parenteral, abriendo un abanico de posibilidades al momento de poder tratar esta patología tan frecuente, dando claridad sobre sus indicaciones y contraindicaciones. • Iniciar la infusión y aclarar las dudas al paciente no deben olvidarse previo al uso de esta terapia ya que son requisitos fundamentales para su correcta realización.
Cómo citar.: Ortiz-Serrano R, Leal-Bernal J, López-Acevedo AV, Martínez-Maldonado EG, Mejía-Rodríguez PA. Beneficios del uso del hierro parenteral como alternativa eficaz en el manejo de la anemia gestacional en Colombia. MedUNAB [Internet]. 2022;25(2):279-289. DOI: https://doi.org/10.29375/01237047.3966
Enlace alternativo
https://revistas.unab.edu.co/index.php/medunab/article/view/3966/3646 (xml)
https://revistas.unab.edu.co/index.php/medunab/article/view/3966/3634 (pdf)
https://revistas.unab.edu.co/index.php/medunab/article/view/3966 (html)
