Artículos

Recepción: 19 Marzo 2025
Aprobación: 20 Junio 2025
Publicación: 25 Noviembre 2025
Resumen: Las actividades mineras y la ganadería en el cantón Yacuambi alteran las condiciones ecológicas de cuerpos hídricos, especialmente de ríos y fuentes abastecedoras de agua para consumo humano. En este trabajo de investigación se evaluó la calidad del agua aplicando métodos basados en bioindicadores, específicamente fitoplancton, como mecanismo que complementa la evaluación fisicoquímica. El fitoplancton desempeña un papel importante en la estructura y producción primaria de los ecosistemas acuáticos, de manera que, estudiar su composición y estructura es un indicador biológico de la calidad del agua. In situ, se tomaron muestras de agua para el análisis fisicoquímico (pH, oxígeno disuelto, conductividad, sólidos totales disueltos, temperatura, nitratos y fosfatos) y biológico (diatomeas). A nivel de laboratorio se realizó microscopía y cuantificación de células fitoplanctónicas que permitió aplicar un índice para determinar la calidad del agua. La aplicación del Índice Diatomológico General (IDG) reveló diferencias significativas en la calidad del agua (p < 0.05) entre la quebrada Santa Inés y los ríos Yacuambi y El Salado. En cuanto a la abundancia se registraron individuos de los géneros Microspora, Ulothrix, Navicula, Gomphonema y Ulnaria. La temperatura, oxígeno disuelto y conductividad fueron las variables que más se diferenciaron entre los ríos estudiados (p < 0.05). Un análisis multivariado mostró la conformación de grupos específicos para cada uno de los ríos estudiados, grupos que incluyeron organismos fitoplanctónicos indicadores de una buena o mala calidad de agua y aspectos fisicoquímicos que, explicaron en todos los casos, al menos un 69 % de la variabilidad de la información contenida en la base de datos.
Palabras clave: diatomeas, bioindicadores, Índice Diatomológico General, calidad de agua.
Abstract: Mining and livestock activities in the Yacuambi canton significantly alter the ecological conditions of aquatic bodies, particularly rivers and water sources used for human consumption. This study evaluated water quality using methods based on bioindicators, specifically phytoplankton, as a complementary approach to physicochemical assessments. Phytoplankton play a crucial role in the structure and primary production of aquatic ecosystems; therefore, analyzing their composition and structure serves as a biological indicator of water quality. In situ water samples were collected for both physicochemical analysis (pH, dissolved oxygen, conductivity, total dissolved solids, temperature, nitrates, and phosphates) and biological analysis (diatoms). In the laboratory, microscopy and quantification of phytoplanktonic cells were conducted, enabling the application of an index to determine water quality. The application of the General Diatom Index (GDI) revealed significant differences in water quality (p < 0.05) among the Santa Inés stream and the Yacuambi and El Salado rivers. In terms of abundance, individuals from the genera Microspora, Ulothrix, Navicula, Gomphonema, and Ulnaria were recorded. Temperature, dissolved oxygen, and conductivity were the variables that most differentiated the studied rivers (p < 0.05). Multivariate analysis revealed the formation of specific groups for each river, including phytoplankton organisms that serve as indicators of water quality and physicochemical variables, which together explained at least 69 % of the data variability in all cases.
Keywords: Diatom, bioindicators, General Diatomological Index, water quality.
INTRODUCCIÓN
En los países en vías de desarrollo, la contaminación del agua constituye uno de los principales problemas que afectan a los ecosistemas acuáticos. El vertido de desechos mineros, domésticos, industriales y de otras fuentes, sin un tratamiento adecuado, altera significativamente la calidad del agua, la cual, en muchos casos, se puede utilizar para la ganadería, la agricultura e incluso el consumo humano [1].
Actualmente, la evaluación de la calidad del agua se realiza mediante mediciones de parámetros fisicoquímicos, que requieren equipos especializados capaces de detectar componentes orgánicos e inorgánicos que deterioran la calidad del agua. Sin embargo, los resultados obtenidos solo reflejan la condición del momento de la toma de la muestra [2].
Ante estas limitaciones, es necesario el empleo de organismos vivos como bioindicadores para determinar el estado ecológico de los cuerpos de agua. Entre los más utilizados se encuentran los peces, macroinvertebrados y el fitoplancton [3]. En zonas influenciadas por minería, las altas concentraciones de metales pesados en el agua generan efectos negativos en la morfología de las diatomeas, lo cual genera deformaciones en el frústulo. Además, provocan la desaparición de diatomeas sensibles a la contaminación, las cuales son reemplazadas por taxones más tolerantes [4].
El fitoplancton, al igual que los macroinvertebrados, son ampliamente empleados en la evaluación de la calidad del agua, ya que ambos constituyen componentes clave de la biodiversidad acuática. Estos bioindicadores ofrecen información tanto de las condiciones pasadas como de las condiciones actuales de la calidad del agua. El análisis de su estructura permite identificar la presencia de individuos tolerantes o sensibles a la contaminación [5].
El fitoplancton desempeña un rol central en la estructura y funcionamiento de ecosistemas de agua dulce, ya que tanto las algas como las cianobacterias son componentes clave de la producción primaria [6]. En este sentido, las algas se han destacado como bioindicadores de la calidad del agua a nivel de poblaciones y comunidades, debido a su alto grado de sensibilidad a los contaminantes ambientales y a sus ciclos de vida cortos, lo que permite determinar en el corto plazo el estado ecológico de un cuerpo de agua [7].
La composición y la diversidad de estos organismos son el resultado de la interacción entre sus rasgos biológicos y diversos factores ambientales como la disponibilidad de nutrientes, la materia orgánica, el sedimento y la composición química del agua [8, 9]. Por ello, se han planteado diferentes índices para determinar la calidad del agua, entre los cuales destaca el Índice Diatómico General (IDG), el cual enfoca su análisis en los niveles de polución, la abundancia y la capacidad de adaptación presentados por las comunidades de diatomeas (Bacillariophyta) [10].
En el cantón Yacuambi, provincia de Zamora Chinchipe, el 43,76 % de su territorio se encuentra concesionado para actividades mineras, siendo el oro el principal recurso no renovable presente en el subsuelo. Actualmente, este mineral es extraído por lugareños del territorio bajo prácticas artesanales de explotación sin la presencia de ninguna medida al menos para mitigar en parte los graves daños que producen a los ecosistemas acuáticos [11].
En los últimos cinco años, la actividad minera en Yacuambi ha generado el deterioro de las condiciones ecológicas de importantes cuerpos hídricos, generando riesgos para la salud humana, así como para las comunidades acuáticas y el funcionamiento ecosistémico. Además, esta situación ha provocado polarizaciones importantes entre grupos sociales, generando conflictos socioambientales que agravan más la problemática alrededor de la minería. Ante esta realidad, este trabajo de investigación evaluó la calidad del agua aplicando métodos basados en bioindicadores como un mecanismo complementario a la evaluación fisicoquímica. Este enfoque busca generar información científica que permita evidenciar ante los actores sociales, políticos y el sector privado las consecuencias de la minería sobre las condiciones de calidad del agua de importantes cuerpos hídricos de Yacuambi. Particularmente, este trabajo de investigación implementa una metodología innovadora que permite evaluar la calidad de agua usando organismos fotosintéticos (diatomeas) como bioindicadores, complementando así la evaluación basada en información fisicoquímica que comúnmente se lleva a cabo en estudios de calidad de agua.
MATERIALES Y MÉTODOS
La parroquia 28 de Mayo, ubicada en el cantón Yacuambi (Fig. 1), limita al norte con las provincias de Azuay y Morona Santiago; al sur, con el cantón Zamora; al este, con el cantón Yantzaza y la provincia de Morona Santiago; y al oeste, con las provincias de Loja y Azuay [12].
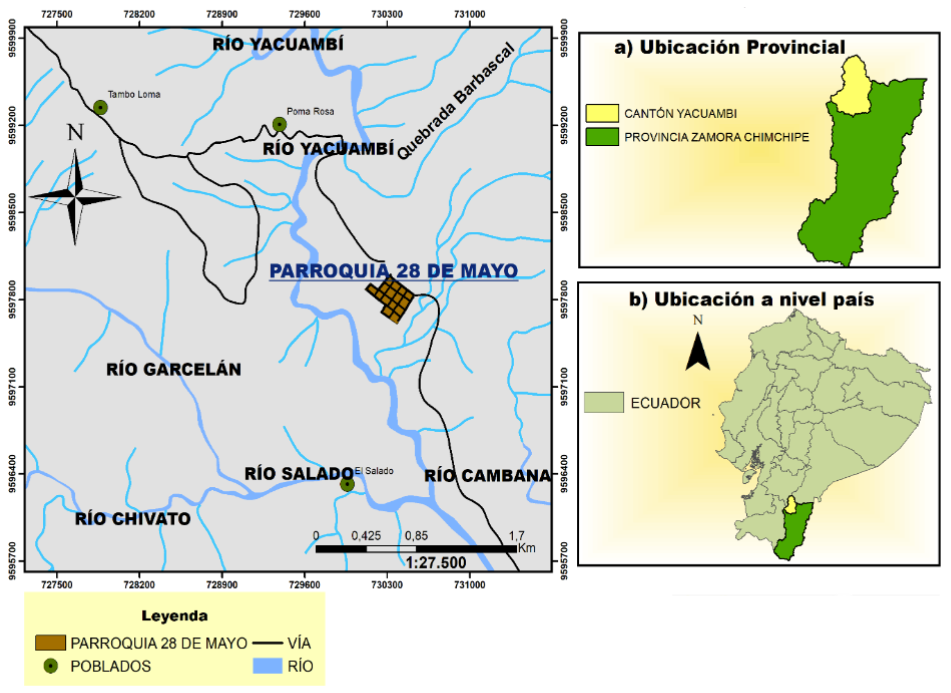
Figura 1. Ubicación de la parroquia 28 de mayo, cantón Yacuambi. Elaboración propia
El monitoreo de la calidad del agua se realizó en tres sistemas hídricos: la quebrada Santa Inés, el río Yacuambi y el río El Salado (Fig. 2). La quebrada Santa Inés abastece agua para la zona urbana de la parroquia 28 de Mayo y presenta importantes indicios de alteración por el avance de la frontera ganadera. Por su parte, en los ríos Yacuambi y el Salado, se desarrollan actividades mineras artesanales no regularizadas.
En el caso de los ríos El Salado y Yacuambi la definición de puntos de muestreo tuvo como referencia zonas intervenidas por minería. Para ambos casos se determinó una distancia longitudinal de un kilómetro siguiendo el cauce de los ríos. La distancia entre los puntos estudiados fue de 200 metros (5 puntos por cada río).
Para la quebrada Santa Inés, los puntos de estudio se establecieron desde la zona de recarga hídrica hasta la zona de captación, definiendo cinco puntos de muestreo cada 150 metros. Además, en los puntos de monitoreo de la quebrada Santa Inés, el río Yacuambi y el río El Salado, se aplicó el Índice de Calidad de Bosque de Ribera (QBR), mismo que evalúa la vegetación ribereña, considerando 4 aspectos: grado de cobertura de la cubierta vegetal, estructura de la vegetación, calidad de la cubierta vegetal y grado de naturalidad del canal fluvial, cada uno con valores del 1 a 25 [13], el resultado es la suma de todos los bloques (Tabla 1).
Tabla 1. Categorías Índice de Calidad de Bosque de Ribera [14]

Fuente: Copyright # 2002 John Wiley & Sons, Ltd.
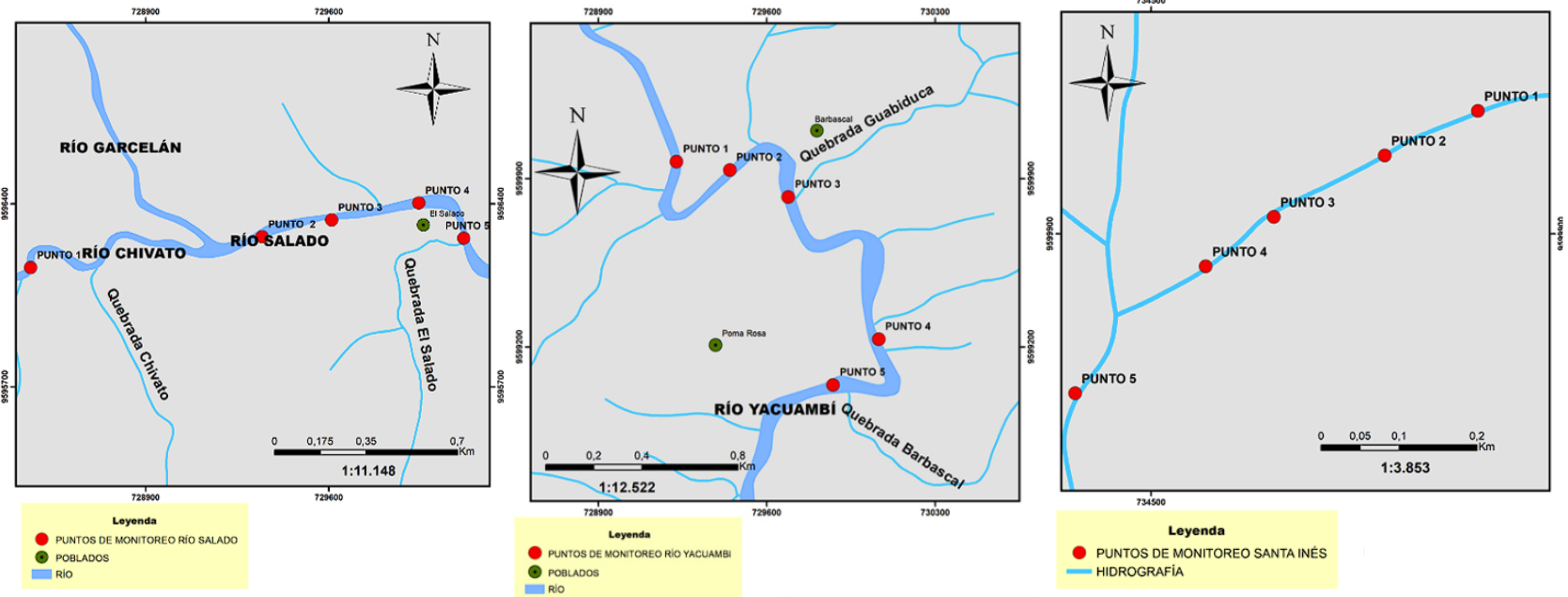
Figura 2. Cuerpos hídricos monitoreados en la parroquia 28 de Mayo, cantón Yacuambi. Elaboración propia.
Se utilizó una sonda multiparamétrica modelo Hanna HI9819 para registrar, en cada punto de muestreo definido para los tres ríos, las lecturas de oxígeno disuelto, temperatura, pH, sólidos totales disueltos y conductividad eléctrica. Además, en Santa Inés y en El Salado se tomaron muestras de agua para el análisis de nutrientes como fosfatos (método por ácido ascórbico) y nitratos (método por reducción con cadmio), los mismos que se realizaron en el laboratorio certificado de la Universidad Técnica Particular de Loja (UTPL).
Para estudiar las diatomeas epilíticas, las muestras fueron recogidas de sustratos naturales, preferentemente rocas de 10 a 20 cm de diámetro, sumergidas en agua a una profundidad de 10 a 20 cm, en lugares con luz solar y que presenten un biofilm parduzco en la superficie, condición que caracteriza la colonización de algas diatomeas en el sustrato. Para retirar las diatomeas del sustrato, se usó un cepillo de dientes para raspar la superficie colonizada en 5 rocas. Una vez finalizado el raspado, se transfirió la muestra del recipiente a un frasco de plástico de 100 ml que fue etiquetado con cinta adhesiva. Luego, se añadió solución de Lugol (1 %) a las muestras para su conservación [15].
Las muestras biológicas fueron trasladadas en cadena de frío y almacenadas en el Laboratorio de Ecología Acuática de la Universidad Técnica Particular de Loja (UTPL) donde se realizó la microscopía. Para la identificación y conteo celular, las muestras fueron transferidas a tubos falcon de 50 ml y decantadas por un periodo de 12 horas. Durante este tiempo, el material que contiene las comunidades de diatomeas se sedimenta al fondo del tubo.
Posteriormente, se extrajo una alícuota de 1 ml de muestra, la cual se depositó en una cámara de recuento Sedgewick Rafter. El conteo celular se realizó de acuerdo a Guzman y Leiva [16], utilizando un microscopio ZEIZZ Axiolab 5. Inicialmente, se realizó un barrido preliminar con un aumento de 10X para verificar la abundancia de individuos y determinar si la población es densa. El conteo de los individuos se realizó con un aumento de 10X en 30 campos de visión, siguiendo la metodología de McAlice [17], quien demostró que un recuento de 30 cuadrantes en una cámara de recuento Sedgewick Rafter permite identificar entre el 90 % y el 95 % de las especies presentes en la muestra. Finalmente, los especímenes observados fueron registrados en una matriz, junto con su respectiva abundancia en cada uno de los 30 campos de visión.
La identificación taxonómica se realizó mediante microfotografías utilizando el microscopio ZEIZZ Axiolab 5. Para ello, se colocó una gota de la muestra sedimentada en un portaobjetos para observar y fotografiar especímenes con un aumento de 40X. La identificación de los organismos se realizó hasta nivel de género [18].
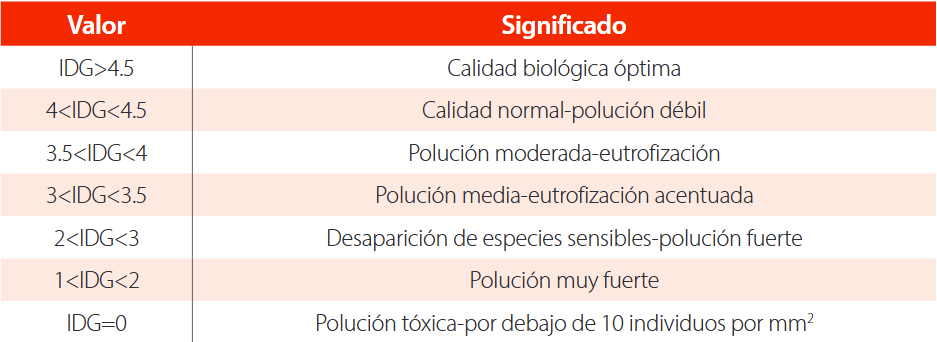
Además, se obtuvieron los siguientes índices biológicos: diversidad de Shannon-Weinner, equitatividad y riqueza. La determinación de la riqueza se basó en el conteo del número de géneros presentes en cada río. Para determinar la calidad del agua se aplicó el Índice Diatómico General (IDG) (Ecuación 1), que considera la variabilidad y sensibilidad de géneros de diatomeas, y que responden a cambios de la calidad del agua [10]. Los resultados del índice fueron comparados de acuerdo a los niveles de calidad de la Tabla 2.
Donde:
Aj: abundancia relativa, es decir la cantidad de géneros en relación a la muestra.
Vj: variabilidad del género o amplitud ecológica, donde: 1 (ubicua) a 3 (característica).
Sj: sensibilidad a la contaminación, donde: 1 (resistente) a 5 (sensible).
Tabla 2. Categorías de calidad de agua para el índice diatómico general (Rumeau y Coste, 1988)
Para el análisis estadístico, se empleó estadística descriptiva para resumir las condiciones fisicoquímicas de los cuerpos de agua. Las variables continuas se describieron mediante promedios y desviación estándar. Para comparar los parámetros fisicoquímicos entre los tres ríos, se aplicó la prueba no paramétrica Kruskal-Wallis cuando los datos no tuvieron una distribución normal. Adicionalmente, se realizó un análisis de componentes principales (ACP) para observar las tendencias de variación individual de los ríos estudiados y reconocer eventualmente los agrupamientos particulares. Los datos completos fueron exportados a una hoja de cálculo de Microsoft Excel 2016 para su limpieza y codificación, y posteriormente transferidos al programa R, versión 4.2.3, para el análisis estadístico subsiguiente.
RESULTADOS
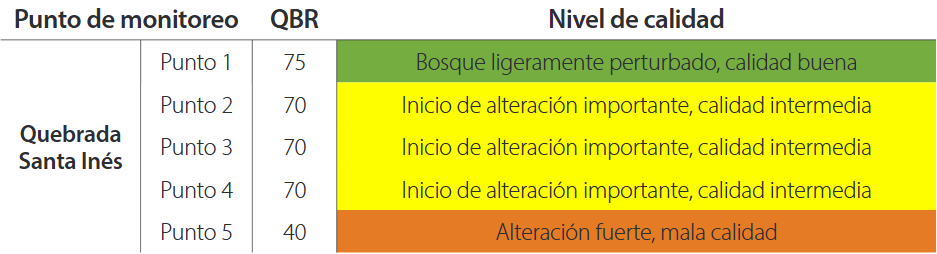
En la quebrada Santa Inés, según lo indicado en la Tabla 3, la calidad del bosque de ribera en la mayor parte de los puntos de monitoreo presenta indicios de una alteración importante, por lo tanto, la calidad de bosque de ribera se clasifica como intermedia.
Tabla 3. Índice de calidad de bosque de ribera de la quebrada Santa Inés, cantón Yacuambi
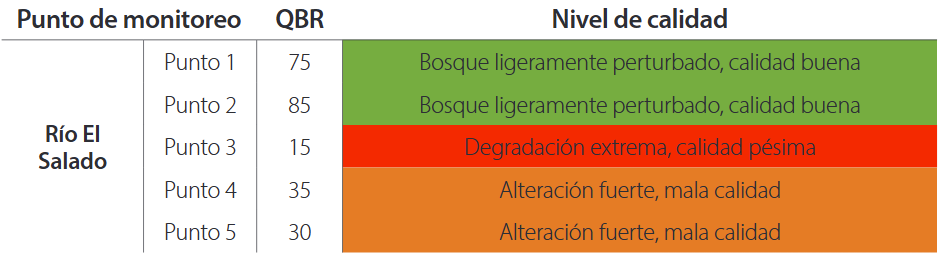
En el río Salado, según lo indicado en la Tabla 4, en la mayor parte de los sitios evaluados la calidad del bosque de ribera oscila entre un estado de bosque ligeramente perturbado y uno de alteración fuerte; sin embargo, en el punto 3 se observa una degradación extrema de la cobertura ribereña.
Tabla 4. Índice de calidad de bosque de ribera del río El Salado, cantón Yacuambi
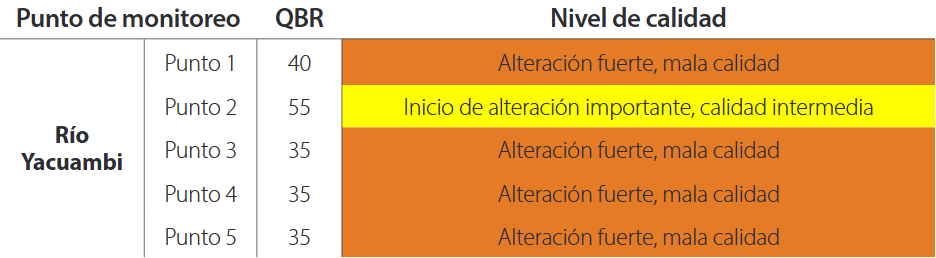
La aplicación del Índice de Calidad del Bosque de Ribera (QBR) mostró que, según la Tabla 5, en el río Yacuambi la mayor parte de los sitios monitoreados presenta una alteración fuerte; por lo tanto, existe una mala calidad de ribera
Tabla 5. Índice de calidad de bosque de ribera del río Yacuambi, cantón Yacuambi
En la Tabla 6 se indican los valores promedio de las variables fisicoquímicas de los lugares estudiados. La quebrada Santa Inés presentó la mayor concentración de fosfatos y nitratos. El pH en las tres zonas de estudio fue ácido y la mayor acidez se presentó en el río Yacuambi. La mayor concentración de oxígeno disuelto se registró en la quebrada Santa Inés y la menor en el río El Salado. La quebrada Santa Inés presentó el valor más alto de conductividad y concentración de Sólidos Totales Disueltos (STD). Con respecto a la temperatura, el río Yacuambi y El Salado presentaron los valores más altos.
Tabla 6. Promedios y desviación estándar de parámetros fisicoquímicos de las zonas de estudio en el cantón Yacuambi
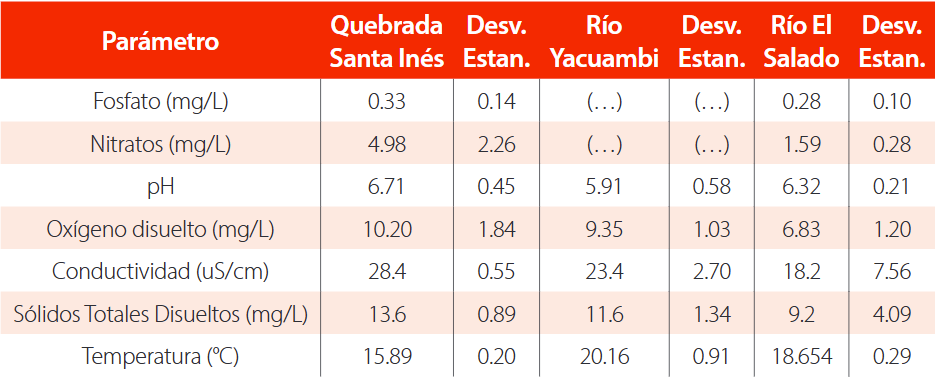
(…): Valor no registrado
Desv. Estan.: desviación estándar
De acuerdo a la Figura 3, la mayor diversidad de comunidades de diatomeas se reportó en la quebrada Santa Inés (H’=2.21) y en el río El Salado (H’=2.14), mientras que la menor se observó en el río Yacuambi (H’=1.92). La equitatividad fue mayor en el río El Salado (E=0.83) y en el río Yacuambi (E=0.83), y menor en la quebrada Santa Inés (E=0.80). Con respecto a la riqueza, obtuvo su mayor valor en la quebrada Santa Inés (16 géneros) y en el río El Salado (13 géneros), mientras que el valor más bajo se registró en el río Yacuambi (10 géneros).
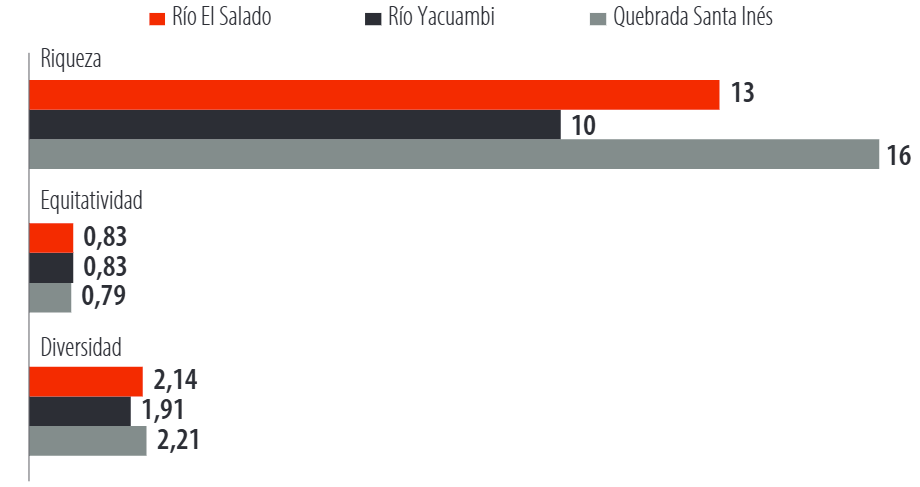
Figura 3. Índices biológicos de diversidad, equitatividad y riqueza de la quebrada Santa Inés, río Yacuambi y río el Salado, cantón Yacuambi
En la quebrada Santa Inés Gomphonema lagenula fue la más abundante. Otros taxones con importantes abundancias fueron: Gomphonema y Rhoicosphenia curvata (Fig. 4).
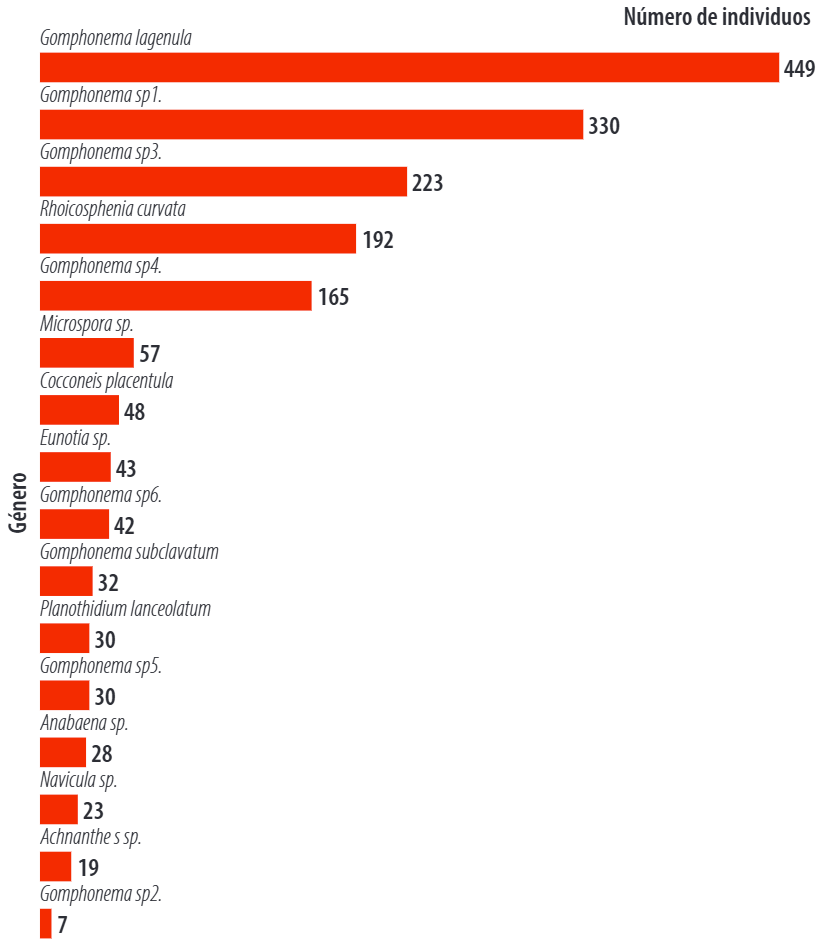
Figura 4. Abundancia de comunidades fotosintéticas en la quebrada Santa Inés, cantón Yacuambi
En el río Yacuambi (Fig. 5), la mayor abundancia correspondió al género Navicula. Taxones como Gomphonema, Psammothidium, Encyonema y Ulnaria también presentaron abundancias importantes.
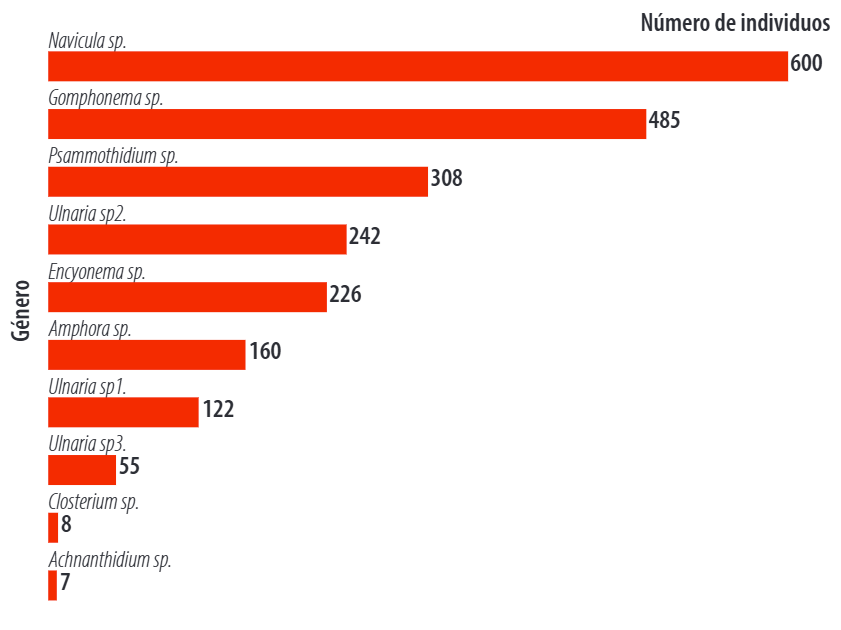
Figura 5. Abundancia de comunidades fotosintéticas río Yacuambi, cantón Yacuambi
En el río El Salado (Fig. 6), la mayor abundancia correspondió a los géneros Microspora sp. y Ulothrix sp.
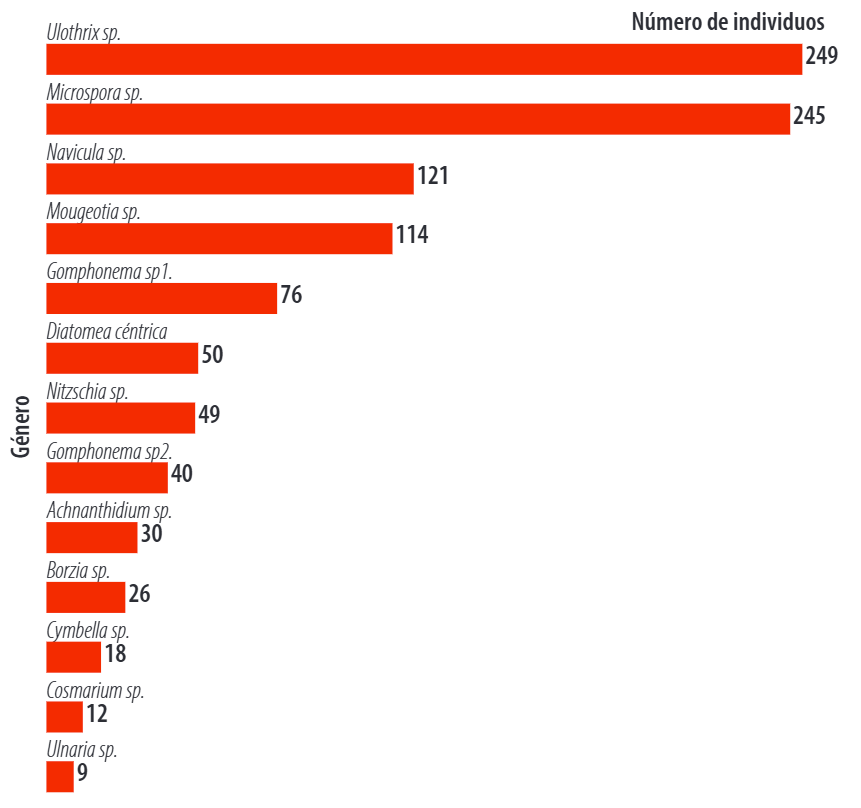
Figura 6. Abundancia de comunidades fotosintéticas río El Salado, cantón Yacuambi
La aplicación del Índice Diatómico General (IDG) reportó que, en la quebrada Santa Inés (Fig. 7), la calidad del agua se encuentra en una polución media con una eutrofización acentuada en la mayoría de los puntos monitoreados, a excepción del punto 5, sitio donde no se evidenció presencia de actividades ganaderas.
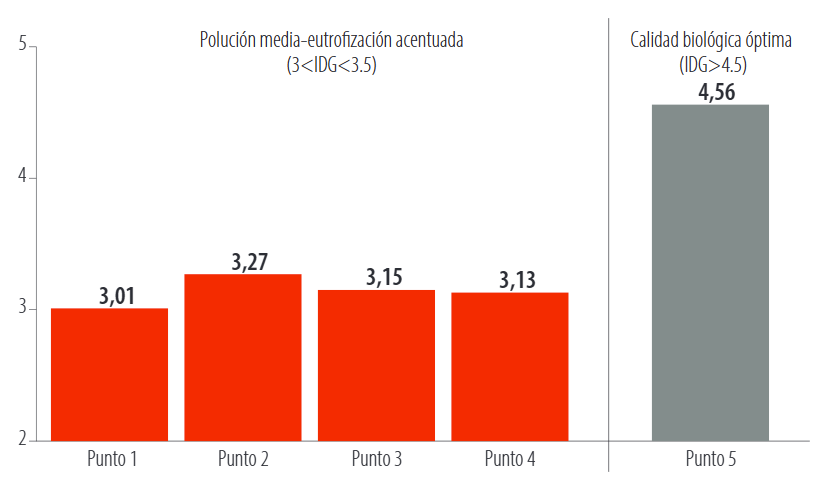
Figura 7. Índice Diatómico General quebrada Santa Inés, cantón Yacuambi
La calidad del río Yacuambi (Fig. 8), de acuerdo al IDG, se encuentra en una polución media con una eutrofización acentuada.
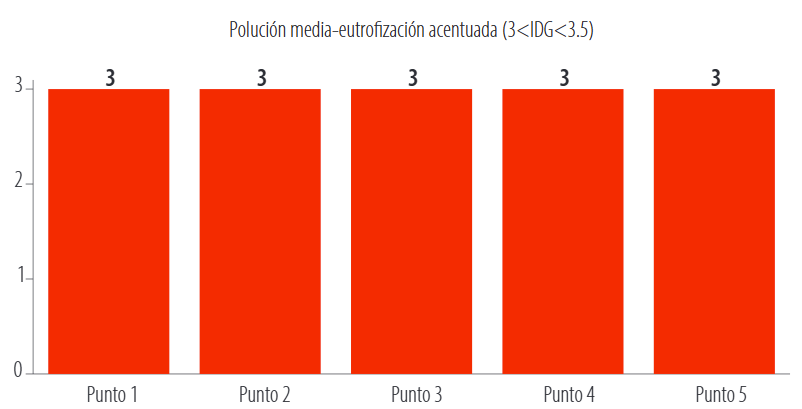
Figura 8. Índice Diatómico General río Yacuambi, cantón Yacuambi
Con respecto al río El Salado (Fig. 9), la calidad del agua se encuentra entre una polución intermedia a fuerte. Los puntos que presentan fuerte polución, están ubicados en un área de mayor intervención minera, actividad que gravemente ha alterado el ecosistema.
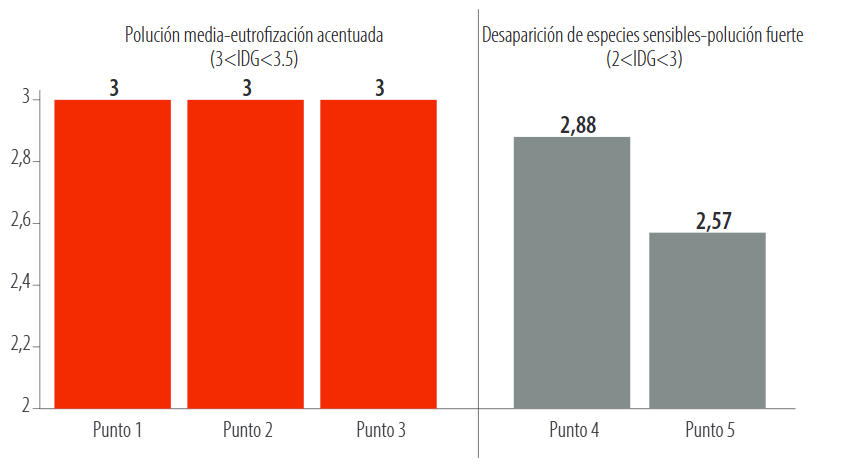
Figura 9. Índice Diatómico General río El Salado, cantón Yacuambi
En el análisis de los valores promedios de variables fisicoquímicas, se encontró una diferencia estadísticamente significativa en los niveles de temperatura (p<0.05) entre las tres zonas de estudio. El río Yacuambi registró la temperatura más alta, seguido del río El Salado y la quebrada Santa Inés (Fig. 10).
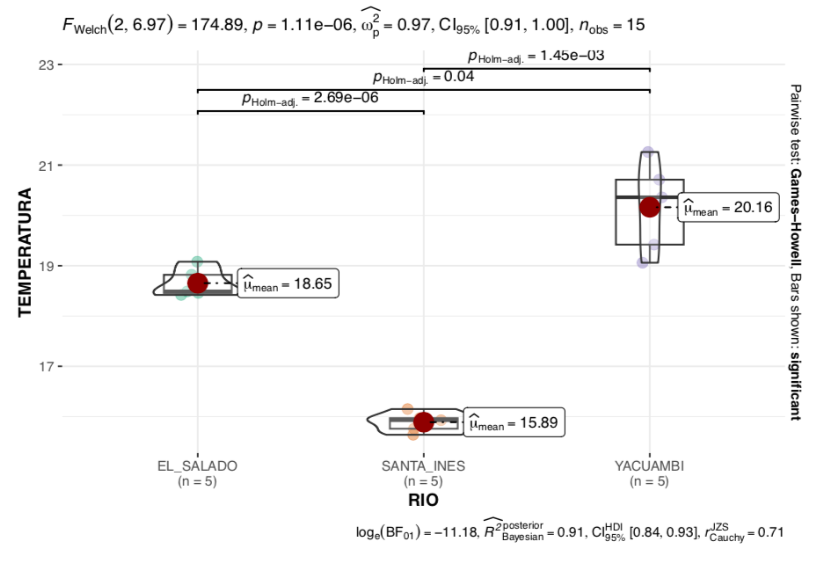
Figura 10. ANOVA paramétrico de la temperatura en la quebrada Santa Inés, río Yacuambi y río el Salado, cantón Yacuambi
En cuanto al oxígeno disuelto (Fig. 11), se encontraron diferencias estadísticamente significativas en las tres zonas de estudio (p < 0.05). La quebrada Santa Inés presentó la mayor concentración a diferencia del resto de zonas estudiadas.
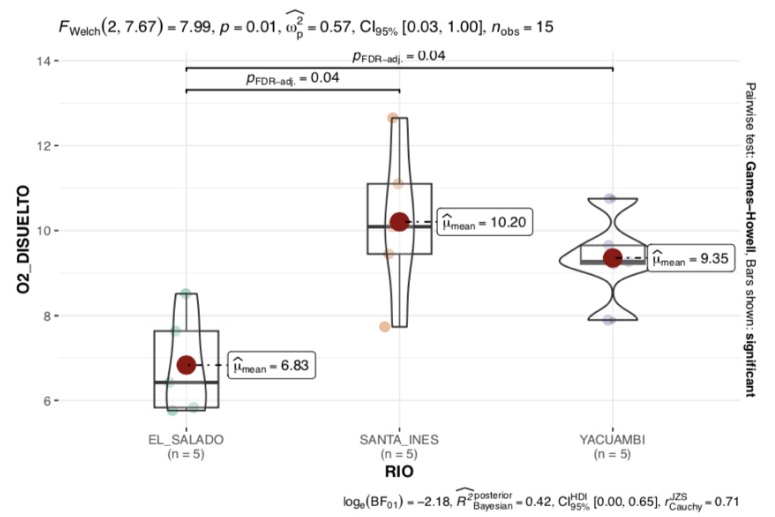
Figura 11. ANOVA paramétrico del oxígeno disuelto en la quebrada Santa Inés, río Yacuambi y río el Salado.
Los valores de conductividad eléctrica (Fig. 12) presentaron diferencias estadísticamente significativas en las zonas estudiadas (p < 0.05). La quebrada Santa Inés registró el mayor nivel de conductividad, seguida del río Yacuambi y río El Salado.
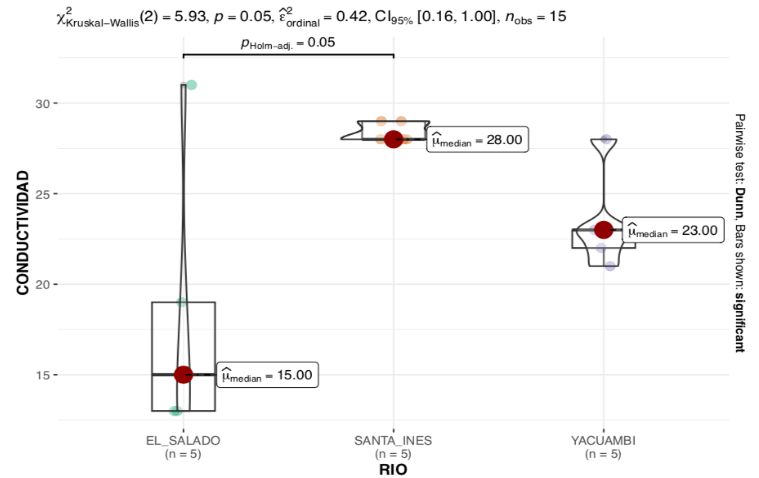
Figura 12. ANOVA no paramétrico de la conductibilidad en la quebrada Santa Inés, río Yacuambi y río el Salado, cantón Yacuambi
El Índice Diatómico General (IDG) (Fig. 13) mostró diferencias en los cuerpos de agua estudiados (p < 0.05). La quebrada Santa Inés reflejó un mayor nivel de IDG seguido por el río Yacuambi y El Salado.
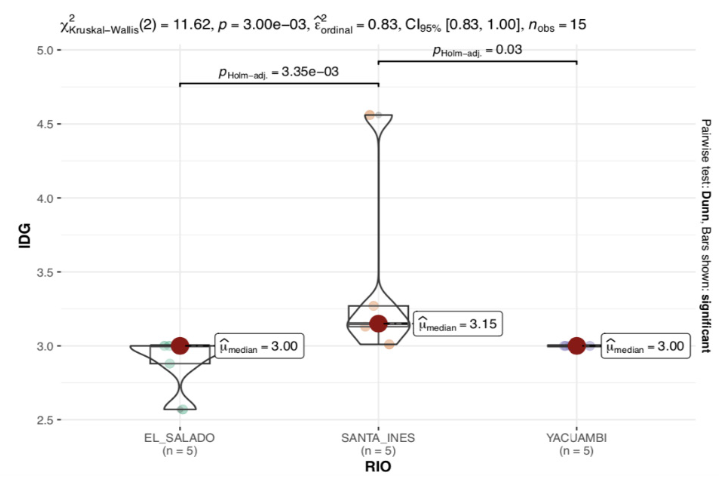
Figura 13. ANOVA no paramétrico del IDG en la quebrada Santa Inés, río Yacuambi y río el Salado.
En el Análisis de Componentes Principales (ACP) de la quebrada Santa Inés (Fig. 14), el primer componente principal (CP1) explica el 42.8 % del total de la varianza obtenida, influenciada principalmente por las variables de “riqueza” y “diversidad”. El segundo componente principal (CP2) representa el 27.7 % de la varianza, asociada a la presencia de organismos como “Planothidium lanceolatum” y “Gomphonema sp1”. En general, el 70.4 % del total de la varianza observada es explicado por los dos componentes principales.
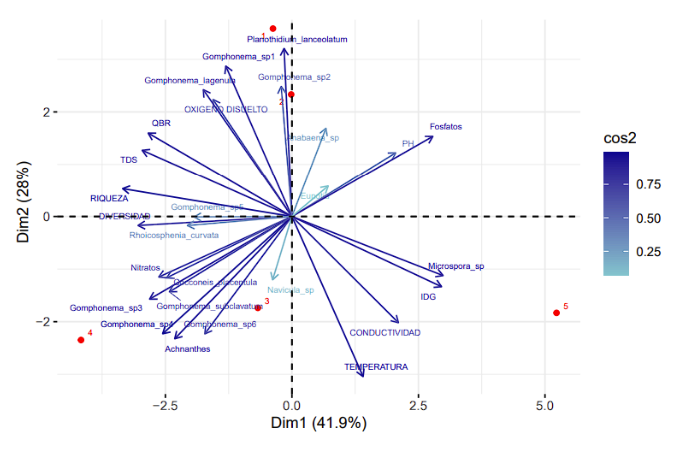
Figura 14. Análisis de componentes principales entre variable bióticas y géneros de diatomeas en la quebrada Santa Inés, cantón Yacuambi
En la Figura 15, se puede observar la variabilidad explicada para cada componente principal de la quebrada Santa Inés.
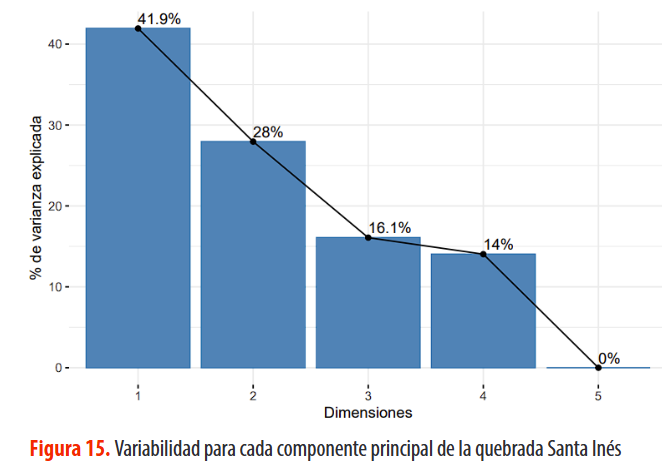
Figura 15. Variabilidad para cada componente principal de la quebrada Santa Inés
Con respecto al río Yacuambi (Fig. 16), el primer componente principal (CP1) explica el 63.1 % de la varianza total, la cual se debe por la abundancia del género “Gomphonema”. El segundo componente principal (CP2) representa el 23.2 % de la varianza, en donde, se destacan los géneros: “Encyonema” y “Ulnaria sp2” como los más representativos. En general, el 86.3 % del total de la varianza observada es explicado por los dos componentes principales.
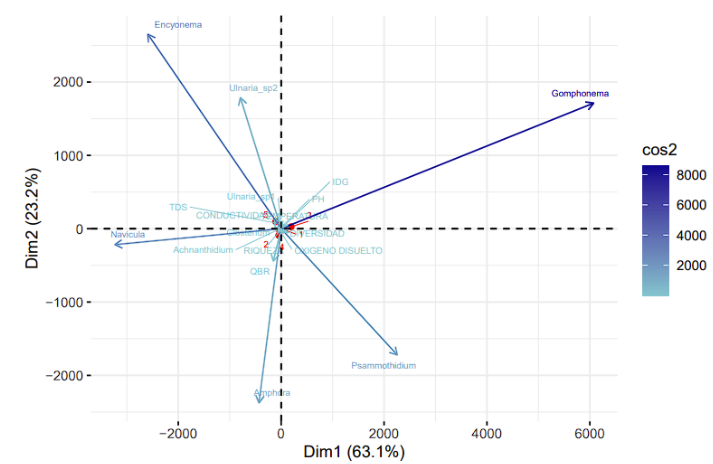
Figura 16. Análisis de componentes principales entre variables bióticas y géneros de organismos fotosintéticos en el río Yacuambi, cantón Yacuambi
En la Figura 17, se puede observar la variabilidad explicada para cada componente principal del Río Yacuambi.
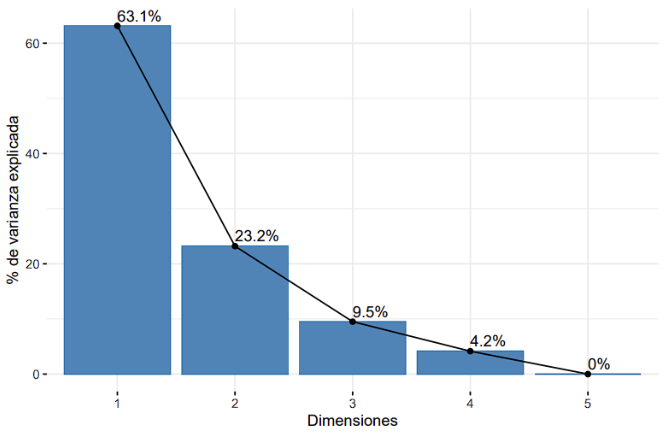
Figura 17. Variabilidad para cada componente principal del Río Yacuambi
El Análisis de Componentes Principales del río El Salado (Fig. 18) el primer componente principal (CP1) explica el 37.4 % del total de la varianza obtenida, influenciado por las variables: “navicula” y “riqueza”. El segundo componente principal (CP2) explica el 32 % del total de la varianza total, asociado principalmente a las variables “temperatura”, “oxígeno disuelto” y “Sólidos Totales Disueltos (TDS)”. En general, el 69.4 % del total de la varianza observada es explicado por los dos componentes principales.
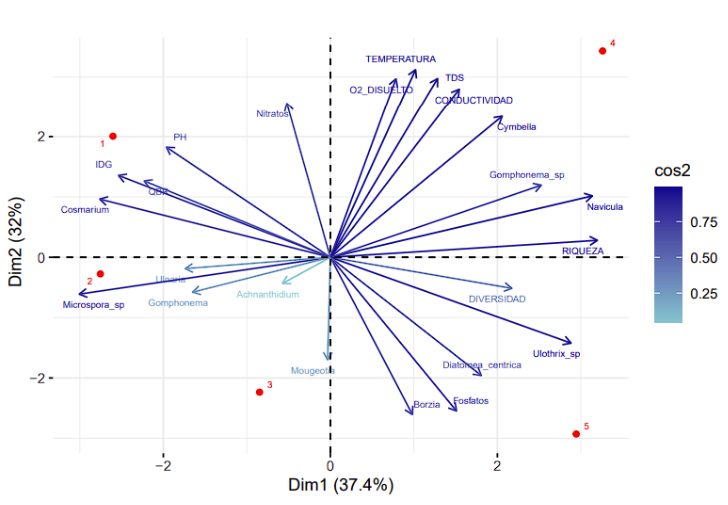
Figura 18. Análisis de componentes principales entre variables bióticas y géneros de organismos fotosintéticos en el río el Salado, cantón Yacuambi
En la Figura 19, se puede observar la variabilidad explicada para cada componente principal del río El Salado.
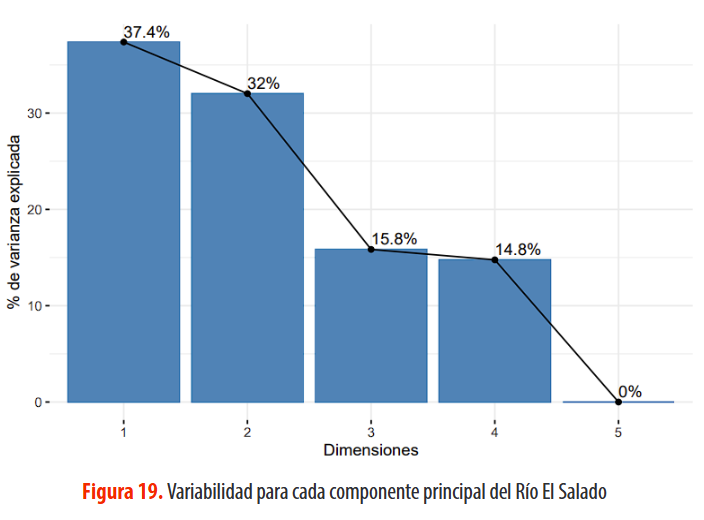
Figura 19. Variabilidad para cada componente principal del Río El Salado
DISCUSIÓN
La evaluación de la calidad del bosque de ribera permitió evidenciar el impacto de la minería artesanal no regulada en la vegetación ribereña, donde los ríos Yacuambi y El Salado mostraron zonas de mala calidad riparia, a diferencia de la quebrada Santa Inés, que presentó una calidad intermedia. Según Cabo et al. [19], la vegetación ribereña juega un papel importante en la calidad del agua, ya que actúa como una barrera fisicoquímica que retiene contaminantes y nutrientes. Además, un estado saludable de la vegetación ribereña proporciona sombra que regula la temperatura y mantiene una buena oxigenación [20]. Estas condiciones podrían explicar el desarrollo de ciertos grupos de comunidades fotosintéticas indicadoras de una buena calidad de agua. Por lo tanto, el índice QBR es una herramienta rápida que permite determinar el estado de la calidad de ribera [2], misma que puede estar vinculada a la calidad del agua.
El uso de comunidades de diatomeas para evaluar la calidad del agua influenciada por actividades mineras resulta eficaz debido a la tolerancia de estos organismos a los cambios de las condiciones de pH, conductividad, requerimientos de oxígeno y presencia de nutrientes [15]. Los fosfatos en la quebrada Santa Inés y el río El Salado superaron los límites permisibles (>0,01 mg/L) según los Criterios Ecológicos de Calidad de Agua propuestos en México[21]. Investigadores como Maza [22], indican que el aumento de fosfato es el resultado del desarrollo de actividades agrícolas y ganaderas, las cuales aportan nutrientes en la columna de agua. Por otro lado, Cabo et al. [19], mencionan que el aumento de nutrientes como el fosfato, puede ser el resultado de la destrucción de la vegetación ribereña, en este caso por la actividad minera, debido a que esta vegetación actúa como una barrera fisicoquímica que retiene contaminantes y regula la entrada de nutrientes a los cuerpos de agua.
En Ecuador, la minería artesanal ha generado un aumento de la contaminación en sectores cercanos a ríos o afluentes [23]. Para investigadores como Sánchez y Ortiz [24], el desarrollo de la minería trae consigo problemas ambientales, mismos que desencadenan conflictos socioambientales. En la actualidad, los ríos Yacuambi y El Salado enfrentan situaciones de contaminación por actividades mineras sin precedentes, intervenciones que han ocasionado conflictos socioambientales entre miembros de las comunidades, y además, han alterado las condiciones ecológicas y de funcionalidad ecosistémica de los cuerpos de agua y zonas riparias.
Las actividades mineras no reguladas constituyen un problema para el medio ambiente, pues la inadecuada disposición de los relaves, aguas residuales y desmontes causan filtraciones de drenaje ácido y contaminantes (metales pesados) en cuerpos acuáticos, que afectan a la diversidad biológica [4]. Según Bonnineau et al. [25], la incorporación excesiva de nutrientes y metales pesados a los cuerpos acuáticos afecta la composición del fitoplancton, donde las diatomeas presentan géneros teratológicos, es decir, organismos con deformaciones en los frústulos, por lo que es necesario considerar estas deformaciones al evaluar la calidad del agua en los ríos Yacuambi y El Salado. La diversidad de organismos fotosintéticos responde a ciertas condiciones ambientales que determinan su distribución y abundancia en la columna de agua, entre las cuales se encuentran el tipo de sustrato, el drenaje del sistema, la luz y la concentración de nutrientes [26]. Además, Alave-Choque [27] menciona que una alta diversidad de organismos fotosintéticos puede determinar una buena calidad de agua. Los resultados de esta investigación demuestran que existe una mayor diversidad de diatomeas en la quebrada Santa Inés y, por lo tanto, una mejor calidad de agua en comparación con los ríos Yacuambi y El Salado.
En un estudio de calidad de agua con organismos fitoplanctónicos en el río Chicama, Perú [5], se evidenció que un sistema acuático bajo la presión de la contaminación se caracteriza por presentar un bajo número de especies con un gran número de individuos, contrastando con una comunidad sin perturbaciones antrópicas, la cual presenta una alta diversidad de especies con un bajo número de individuos. Con base en lo anterior, la diversidad y la riqueza de fitoplancton influenciada por actividades mineras en los ríos Yacuambi y El Salado fue menor en comparación a la quebrada Santa Inés, la cual sirvió de referencia para el desarrollo de esta investigación, debido a que esta microcuenca es el punto de captación de agua para la población de Yacuambi, la cual se encuentra intervenida por la presencia de actividades agropecuarias.
El Índice Diatómico General (IDG) resulta un método eficiente que permite determinar las perturbaciones ambientales en un ecosistema acuático mediante la identificación a nivel de género de diatomeas [28]. En esta investigación, el IDG determinó una contaminación media con una eutrofización acentuada en la mayoría de los puntos de monitoreo. Sin embargo, el río El Salado presentó dos puntos de monitoreo con una contaminación fuerte, reflejando la desaparición de especies tolerantes a la contaminación, por lo que este río sería el más afectado por las actividades mineras, siendo necesaria la constante evaluación de su calidad de agua, estudiando parámetros fisicoquímicos que incluyan metales pesados como mercurio, plomo, arsénico, entre otros, y la identificación a nivel de especies para mejorar las evaluaciones biológicas.
El Análisis de Componentes Principales (ACP) en la quebrada Santa Inés evidenció que existe una relación positiva entre la diversidad y la riqueza de comunidades fotosintéticas, propiciando el desarrollo de organismos como Planothidium lanceolatum. En un estudio del valor indicador de las comunidades de algas bentónicas en el río Magdalena, en México [29], se describe a la especie Planothidium lanceolatum como un bioindicador de condiciones oligotróficas, es decir, sus organismos se desarrollan en mayor cantidad en ambientes con bajas concentraciones de nutrientes, por lo tanto, es un indicador de una buena calidad ambiental. En el río Yacuambi, el ACP revela la importancia del género Gomphonema, cuyo desarrollo se ve favorecido por el aumento de la concentración de nutrientes [30], por ende, tienden a formar grandes colonias. Por otro lado, en el río El Salado el ACP muestra que el género Navicula es tolerante a la contaminación orgánica [29]. Además, Passy [31], clasifica a Navicula como un organismo adaptado a ambientes turbulentos y altas concentraciones de nutrientes, como nitratos y fosfatos, lo que favorece su proliferación.
De acuerdo con los resultados generados en esta investigación, es necesario establecer programas de monitoreo de calidad de agua que incluyan mediciones periódicas a lo largo del tiempo, de manera consistente y en intervalos regulares, para recopilar datos confiables y detectar posibles cambios en la calidad del agua. Para ello, se debe tomar en cuenta la ubicación específica de las operaciones mineras y las fuentes potenciales de contaminación en el área, lo cual permitirá enfocar esfuerzos de monitoreo en las zonas más críticas y evaluar los posibles impactos causados por la actividad minera en las aguas cercanas.
CONCLUSIONES
La evaluación de la calidad de agua fundamentada en bioindicadores (organismos fotosintéticos) y otros parámetros fisicoquímicos posibilitó determinar una línea base en torno a las condiciones de salud biológica de cuerpos de agua amenazados por presiones antrópicas, como herramienta para el monitoreo y control permanente de su estado ecológico, en la que puedan participar entidades competentes y miembros de las comunidades. Los resultados de esta investigación posibilitan determinar las condiciones de calidad de agua en ríos con diferente grado de intervención antrópica.
De acuerdo con el nivel de conservación, la quebrada Santa Inés presenta mejores condiciones de calidad de agua que el resto de cuerpos hídricos estudiados. Sin embargo, la mayoría de los puntos reflejan indicios de una eutrofización acentuada, atribuida principalmente a las altas concentraciones de nutrientes (fosfatos y nitratos), resultado de las actividades ganaderas en las zonas ribereñas. Por otro lado, los ríos Yacuambi y El Salado muestran impactos significativos derivados de las actividades mineras, lo cual se refleja en la evaluación de la calidad del agua mediante bioindicadores como mecanismo complementario a la evaluación fisicoquímica.
Por lo tanto, el uso de comunidades de diatomeas como bioindicadores de la calidad del agua es un factor clave para la toma de decisiones informadas basadas en datos ecológicos concretos. Esta investigación permitió que la ciudadanía y las autoridades conozcan y evalúen las condiciones de calidad de agua de los ríos más importantes en los que se realizan actividades mineras, de manera que es imperante plantear que los planes y programas de desarrollo del cantón Yacuambi contemplen la necesidad de estudiar e implementar programas de monitoreo del estado de salud de los recursos hídricos de forma permanente, así como proyectos de restauración y recuperación de las áreas destruidas.
AGRADECIMIENTOS
Nuestro agradecimiento a COMUNIDEC Fundación de Desarrollo y a la Dirección de Investigación de la Universidad Nacional de Loja por el financiamiento de esta investigación. Al Gobierno Autónomo Descentralizado Municipal del cantón Yacuambi por su colaboración y acompañamiento en el reconocimiento de las zonas para el monitoreo y al Laboratorio de Ecología Acuática de la Universidad Técnica Particular de Loja por brindarnos el espacio y las condiciones necesarias para llevar a cabo la fase de laboratorio de este proyecto.
CONTRIBUCIONES DE LOS AUTORES
Conceptualización: Alonso Cartuche
Metodología: Alonso Cartuche, Roberth Yaguana y Josselyn Balcazar
Recopilación de datos: Roberth Yaguana y Josselyn Balcazar
Análisis formal: Alonso Cartuche, Nikolay Aguirre, Max Encalada y Vinicio Alvarado
Análisis e interpretación de datos: Roberto Bustillos y Alonso Cartuche
Redacción, revisión y edición: Alonso Cartuche, Roberth Yaguana, Nikolay Aguirre y Vinicio Alvarado
DECLARACIÓN SOBRE EL USO DE TECNOLOGÍAS DE IA GENERATIVA Y ASISTIDA EN LA REDACCIÓN
La elaboración de este trabajo no requirió el uso de Inteligencia Artificial (IA).
DECLARACIÓN DE DISPONIBILIDAD DE DATOS
Los datos de esta investigación están disponibles previa solicitud al autor correspondiente, en casos excepcionales.
CONFLICTO DE INTERÉS
Los autores manifiestan que no existe conflicto de intereses en este trabajo de investigación. Todos los autores han aprobado y autorizan su publicación.
REFERENCIAS
[1] Larreal-Murell, J.A., Rojas-Badía, M.M., y Romeu-Álvarez, B., Rojas-Hernández, N. M., & Heydrich-Pérez, M. (2013). Bacterias indicadoras de contaminación fecal en la evaluación de la calidad de las aguas: revisión de la literatura. Revista CENIC. Ciencias Biológicas, 44(3), 24-34. https://www.redalyc.org/pdf/1812/181229302004.pdf
[2] Stulzer, E. F., Villalobos-Sand, N., Castro, L. P., & Schulz, C. (2017). Evaluación breve de la presencia de diatomeas y su relación con algunos parámetros físico-químicos en el río Pirro, Heredia, Costa Rica. Uniciencia, 31(2), 99-109. :// dialnet.unirioja.es/servlet/articulo?codigo=6067684
[3] Calizaya-Anco, J., Avendaño-Cáceres, M., & Delgado-Vargas, I. (2013). Evaluación de la calidad del agua fluvial con diatomeas (Bacillariophyceae), una experiencia en Tacna, Perú. Revista peruana de medicina experimental y salud pública, 30, 58-63. tps://www.scielosp.org/pdf/rpmesp/2013.v30n1/58-63/es
[4] Franco, P., Franco, P., Sulca, L., y Oyague, E. (2018). Diatomeas teratológicas como organismos bioindicadores de la calidad del agua del río tingo, Hualgayoc, Cajamarca. Ciencia y Desarrollo, 17(1), 26–33.
[5] Santillán-Aredo, S. R. y Guerrero-Padilla, A. M. (2018). Macroinvertebrados y fitoplancton como bioindicadores de contaminación en la cuenca del río Chicama, Perú. Revista Tecnología en Marcha, 31(4), 97–110. https://doi. org/10.18845/tm.v31i4.3968
[6] López-Rodríguez, M. C., Leira, M., Valle, R., y Moyá-Niell, G. (2016). El fitoplancton como indicador de calidad de masas de agua muy modificadas en la DMA. El lago artificial de As Pontes (A Coruña. España). NACC: Nova acta científica compostelana. Bioloxía, 23, 8. https://portalinvestigacion.udc.gal/documentos/5d1df6ee29995204f767cd2e
[7] Loza, S., Benavides, R., Brenes, C., y Ballestero, D. (2018). Estructura del fitoplancton en las épocas seca y lluviosa en el golfo de Papagayo, Costa Rica. Revista de Ciencias Marinas y Costeras, 10 (2). https://doi.org/10.15359/revmar.10-2.1
[8] Potapova, M. G. y Charles, D. F. (2002). Benthic diatoms in USA rivers: distributions along spatial and environmental gradients. Journal of biogeography, 29(2), 167–187. https://doi.org/10.1046/j.1365-2699.2002.00668.x
[9] Berlino, M., Mangano, M. C., Di Bona, G., Lucchese, M., Terzo, S. M. C., De Vittor, C., D’Alessandro, M., Esposito, V., Gambi, M. C., Del Negro, P., & Sarà, G. (2024). Functional diversity and metabolic response in benthic communities along an ocean acidification gradient. Marine Environmental Research, 198, 106520 https://doi.org/10.1016/j. marenvres.2024.106520
[10] Rumeau, A. y Coste, M. (1988). Initiation à la systématique des diatomées d’eau douce. Pour l’utilisation pratique d’un indice diatomique générique. Bulletin Français de la Pêche et de la Pisciculture, (309), 1–69. https://doi.org/10.1051/ kmae:1988009
[11] GADM de Yacuambi. (2019). Plan de desarrollo y ordenamiento territorial del cantón Yacuambi 2019-2023. https:// gadyacuambi.gob.ec/images/2021/LOTAIP2021/PDYOT_2019_2023_TOMOI_final_2021.pdf
[12] Guaillas, M. (2015). Plan de Desarrollo y Ordenamiento Territorial del cantón Yacuambi. https://es.scribd.com/ document/442317687/Diagnostico-por-componentes-canton-Yacuambi
[13] López, E., Vásquez-Ramos, J., Villa-NavarroI, F., y Reinoso-Florez, G. (2015). Evaluación de la calidad del bosque de ribera, utilizando un método simple y rápido en dos ríos de bosque seco tropical (Tolima, Colombia). Tumbaga, 1(10), 1. https://dialnet.unirioja.es/servlet/articulo?codigo=5644630
[14] Munné, A., Prat, N., Solà, C., Bonada, N., y Rieradevall, M. (2003). A simple field method for assessing the ecological quality of riparian habitat in rivers and streams: QBR index. Aquatic conservation: marine and freshwater ecosystems, 13(2), 147–163.https://doi.org/10.1002/aqc.529
[15] Lobo, EA, Heinrich, CG, Schuch, M., Wetzel, CE, Ector, L. (2016). Diatomeas como bioindicadores en ríos. En: Necchi JR, O. (eds.) Algas fluviales. Springer, Cham. https://doi.org/10.1007/978-3-319-31984-1_11
[16] Guzman, B. y Leiva, D. (2017). Diatomeas como bioindicadores para la evaluación de la calidad del agua en la cuenca del río Utcubamba, Amazonas - Perú. Revista Científica UNTRM Ciencias Naturales e Ingeniería, 2(1), 16. https:// www.researchgate.net/publication/321204426_Diatomeas_como_bioindicadores_para_la_evaluacion_de_la_ calidad_del_agua_en_la_cuenca_del_rio_Utcubamba_Amazonas_-_Peru
[17] McAlice, B. J. (1971). Phytoplankton sampling with the Sedgewick- Rafter Cell. Limnology and Oceanography, 16(1), 19-28. https://www.academia.edu/3259035/Phytoplankton_sampling_with_the_Sedgwick_Rafter_cell
[18] Vargas, E. C. (2014). Análisis taxonómico de las principales especies de diatomeas (Bacillariophyceae) en seis sitios en la cuenca del río Sarapiquí, Heredia, Costa Rica [Tesis doctoral, Universidad de Costa Rica]. https://www. academia.edu/11706400/An%C3%A1lisis_taxon%C3%B3mico_de_las_principales_especies_de_diatomeas_ Bacillariophyceae_en_seis_sitios_en_la_cuenca_del_r%C3%ADo_Sarapiqu%C3%AD_Heredia_Costa_Rica http://www.biologia.ucr.ac.cr/TesisLic/EdwinCespedesVargas.pdf
[19] Cabo, L., Faggi, A., Miguel, S., y Basílico, G. (2019). Rehabilitación de las riberas de un sitio de la cuenca baja del río Matanza-Riachuelo. Biología Acuática, 33. https://doi.org/10.24215/16684869e005
[20] Elosegi, A. y Sabater, S. (2009). Conceptos y técnicas en ecología fluvial. Fundación BBVa. https://www.fbbva.es/wpcontent/uploads/2017/05/dat/DE_2009_conceptos_ecologia_fluvial.pdf
[21] Centro de Calidad Ambiental. (1989). Acuerdo por el que se establecen los criterios ecológicos de calidad del agua CECCA-001 / 89. http://legismex.mty.itesm.mx/acu/acca001.pdf
[22] Maza, J. (2017). Cuantificación de la variabilidad espacial y temporal de iones de fosfato en dos cuencas andinas altas del sur del Ecuador [Tesis de pregrado, Universidad Politécnica Salesiana]. https://dspace.ups.edu.ec/ bitstream/123456789/14968/1/UPS-CT007384.pdf
[23] Oviedo-Anchundia, R., Moina-Quimí, E., Naranjo-Morán, J., & Barcos-Arias, M. (2017). Contaminación por metales pesados en el sur del Ecuador asociada a la actividad minera. Bionatura, 2, 437-441. https://doi.org/10.21931/ RB/2017.02.04.5
[24] Sanchez, E. y Ortiz, L. (2016). Escenarios ambientales y sociales de la minería a cielo abierto. Inventio, la génesis de la cultura universitaria en Morelos.https://inventio.uaem.mx/index.php/inventio/article/view/323
[25] Morin, S., Cordonier, A., Lavoie, I., Arini, A., Blanco, S., Duong, T. T., Tornés, E., Bonet, B., Corcoll, N., Faggiano, L., Laviale, M., Pérès, F., Becares, E., Coste, M., Feurtet-Mazel, A., Fortin, C., Guasch, H. & Sabater, S. (2012). Consistencia en la respuesta de las diatomeas a entornos contaminados con metales. En H. Guasch, A. Ginebreda y A. Geiszinger (Eds.), Contaminantes emergentes y prioritarios en ríos (The Handbook of Environmental Chemistry, vol. 19). Springer. https:// doi.org/10.1007/978-3-642-25722-3_5
[26] Cajamarca-Tovar, N., Gaona-Castro, L. N., Jimenez-Vargas, N., Acosta-Salinas, M. I., & Camargo-Cortes, L. (2021). Diversidad de Perifiton como indicador de calidad de agua en Caño Barandas, Reserva Natural El Diamante de las Aguas, Guaviare, Colombia. Revista de la Asociación Colombiana de Ciencias Biológicas, 143–153. https://doi. org/10.47499/revistaaccb.v1i33.243
[27] Alave-Choque, H. (2018). Evaluación del perifiton como indicador de calidad de agua en el embalse Cerro Blanco de la Empresa Prestadora de Servicios de Tacna. https://alicia.concytec.gob.pe/vufind/Record/ UNJB_647cc7dc2ce4ed6a87084204024dcf0e
[28] Baylón, M., Arias, J., Cárdenas, R., Arias, C., Cárdenas, A., & Castillo, R. (2018). Evaluación de la diversidad de algas fitoplanctónicas como indicadores de la calidad del agua en lagunas altoandinas del departamento de Pasco (Perú). Ecología Aplicada, 17(1), 119. ttp://www.scielo.org.pe/scielo.php?script=sci_arttext&pid=S1726-22162018000100013
[29] Carmona Jiménez, J., Ramírez Rodríguez, R., Bojorge-García, M. G., González Hidalgo, B., & Cantoral-Uriza, E. A. (2016). Estudio del valor indicador de las comunidades de algas bentónicas: Una propuesta de evaluación y aplicación en el río Magdalena, Ciudad de México. Revista internacional de contaminación ambiental, 32(2). https://doi.org/10.20937/RICA.2016.32.02.01
[30] Palmer, C. M. (1969). A composite rating of algae tolerating organic pollution. Journal of phycology, 5(1), 78–82. https://doi.org/10.1111/j.1529-8817.1969.tb02581.x
[31] Passy, S. (2007). Diatom ecological guilds display distinct and predictable behavior along nutrient and disturbance gradients in running waters. Aquatic Botany, 86(2), 171–178. https://doi.org/10.1016/j.aquabot.2006.09.018
Notas de autor
cartuchea@gmail.com
Información adicional
redalyc-journal-id: 7261