ARTIGO DE REVISÃO
Bioimpressão no Transplante de Órgãos: Dos modelos Experimentais às Perspectivas Clínicas
Bioprinting in Organ Transplantation: From Experimental Models to Clinical Prospects
Bioimpressão no Transplante de Órgãos: Dos modelos Experimentais às Perspectivas Clínicas
Brazilian Journal of Transplantation, vol. 28, e1825, 2025
Associação Brasileira de Transplante de Órgãos
Received: 03 February 2025
Accepted: 14 March 2025
RESUMO
Introdução: A bioimpressão despontou como uma tecnologia inovadora no transplante de órgãos e na medicina regenerativa, visando solucionar desafios urgentes, como a escassez de órgãos de doadores e a necessidade de reparo eficaz de tecidos. Ao aproveitar as técnicas avançadas de impressão 3D, a bioimpressão permite a fabricação de tecidos e órgãos funcionais com propriedades arquitetônicas e biológicas precisas.
Métodos: Esta revisão fornece uma análise detalhada dos últimos avanços em bioimpressão, concentrando-se em técnicas de ponta, no desenvolvimento de biotintas e em suas aplicações na engenharia de tecidos. Ela examina os avanços significativos na criação de protótipos de órgãos vascularizados e transplantáveis e explora a função da bioimpressão na medicina personalizada.
Resultados: As descobertas destacam o impacto transformador da bioimpressão no campo biomédico, particularmente em testes de medicamentos, modelagem terapêutica e estratégias de tratamento específicas para o paciente. Além disso, os principais desafios — incluindo limitações tecnológicas, preocupações éticas e considerações regulatórias — são discutidos para fornecer uma compreensão abrangente do progresso do campo e dos possíveis obstáculos.
Conclusão: A bioimpressão é imensamente promissora para revolucionar a saúde global, oferecendo soluções para a escassez de órgãos e o avanço da medicina regenerativa. No entanto a pesquisa e a inovação contínuas são necessárias para superar os desafios existentes e facilitar sua tradução clínica para a prática médica convencional.
Descritores: Engenharia de Tecidos+ Tecnologias de Impressão 3D+ Viabilidade do Enxerto+ Inovação Biomédica+ Construções Implantáveis.
ABSTRACT
Background: Bioprinting has emerged as an innovative technology in organ transplantation and regenerative medicine, aiming to address pressing challenges such as the shortage of donor organs and the need for effective tissue repair. By leveraging advanced 3D printing techniques, bioprinting enables the fabrication of functional tissues and organs with precise architectural and biological properties.
Methods: This review provides an in-depth analysis of the latest advancements in bioprinting, focusing on cutting-edge techniques, the development of bioinks, and their applications in tissue engineering. It examines significant breakthroughs in the creation of vascularized and transplantable organ prototypes and explores the role of bioprinting in personalized medicine.
Results: The findings highlight the transformative impact of bioprinting in the biomedical field, particularly in drug testing, therapeutic modeling, and patient-specific treatment strategies. Additionally, key challenges—including technological limitations, ethical concerns, and regulatory considerations—are discussed to provide a comprehensive understanding of the field’s progress and potential obstacles.
Conclusion: Bioprinting holds immense promise for revolutionizing global healthcare by offering solutions for organ shortages and advancing regenerative medicine. However, continued research and innovation are necessary to overcome existing challenges and facilitate its clinical translation into mainstream medical practice.
Descriptors: Tissue Engineering, 3D Printing Technologies, Graft Viability, Biomedical Innovation, Implantable Constructs.
INTRODUÇÃO
A bioimpressão é um subconjunto inovador da impressão 3D que envolve a deposição camada por camada de células vivas e biomateriais para criar estruturas que imitam a complexidade de tecidos e órgãos naturais. Essa tecnologia utiliza biotintas — compostas de células, fatores de crescimento e materiais biocompatíveis — para fabricar construtos com precisas propriedades arquitetônicas e funcionais. O processo é meticulosamente controlado para garantir a viabilidade e a colocação correta das células, facilitando o desenvolvimento de construtos de tecidos que podem se integrar perfeitamente ao corpo humano.1
A bioimpressão emprega várias técnicas para obter uma fabricação precisa de tecidos. A bioimpressão baseada em extrusão utiliza um fluxo contínuo de biotinta extrudada por meio de um bocal, o que a torna ideal para imprimir grandes estruturas de tecido com alta densidade celular. A bioimpressão baseada em jato de tinta, por outro lado, emprega forças térmicas ou acústicas para ejetar gotículas de biotinta, permitindo a padronização de alta resolução de células e biomateriais. A bioimpressão assistida por laser usa feixes de laser focalizados para depositar biotintas com precisão excepcional, o que a torna particularmente útil para criar arquiteturas teciduais complexas2. Cada método tem vantagens distintas e é selecionado com base nos requisitos específicos do tecido que está sendo fabricado.
As origens da bioimpressão estão profundamente enraizadas na evolução das tecnologias de impressão 3D. Em 1984, Charles Hull introduziu a estereolitografia, uma técnica que lançou as bases para a impressão 3D, permitindo a criação de objetos por meio de camadas sequenciais de materiais. Inicialmente, esse método encontrou aplicações em engenharia e manufatura. No final da década de 1990, os avanços na ciência dos materiais levaram ao desenvolvimento de materiais biocompatíveis adequados para aplicações médicas, abrindo caminho para o surgimento da bioimpressão2. Um marco significativo foi alcançado em 1999, quando o Dr. Anthony Atala e sua equipe no Wake Forest Institute for Regenerative Medicine imprimiram com sucesso um suporte (scaffold) para uma bexiga humana, que foi então cultivada com as células do próprio paciente para criar um órgão funcional3. Esse avanço demonstrou o potencial da bioimpressão na medicina regenerativa. Os desenvolvimentos subsequentes incluíram a impressão de rins funcionais em miniatura em 2002 e o patenteamento de técnicas de bioimpressão a jato de tinta pelo Dr. Thomas Boland em 2003, que utilizou impressoras modificadas para depositar células em matrizes 3D organizadas4. Essas conquistas fundamentais impulsionaram a bioimpressão de uma estrutura conceitual para um campo em expansão com implicações clínicas significativas.
A importância da bioimpressão para lidar com a escassez de órgãos não pode ser superestimada. O transplante tradicional de órgãos enfrenta desafios significativos, incluindo o suprimento limitado de órgãos de doadores e o risco de rejeição imunológica. A bioimpressão oferece uma solução promissora ao permitir a fabricação de órgãos específicos para o paciente usando suas próprias células, reduzindo assim a probabilidade de rejeição e eliminando a dependência da disponibilidade de um doador5. Essa abordagem não apenas tem o potencial de salvar inúmeras vidas, mas também de revolucionar o campo da medicina regenerativa ao fornecer opções terapêuticas personalizadas, adaptadas às necessidades individuais dos pacientes. À medida que a pesquisa avança, a bioimpressão tem potencial para se tornar uma tecnologia fundamental no desenvolvimento de tecidos e órgãos funcionais, atendendo à demanda crítica por transplantes e avançando na medicina personalizada.
METODOLOGIA
Uma abordagem de revisão de escopo foi empregada para conduzir essa revisão da literatura, garantindo uma análise ampla e abrangente do campo. A seguir, é apresentada uma análise detalhada da metodologia, incluindo a estratégia de pesquisa, os critérios de inclusão/exclusão, o processo de triagem e a avaliação da qualidade.
Estratégia de pesquisa
Foi realizada uma pesquisa abrangente em quatro grandes bases de dados acadêmicas — PubMed, Google Scholar, Scopus e Web of Science — para identificar artigos e estudos relevantes sobre bioimpressão. A pesquisa se concentrou nas seguintes palavras-chave e combinações booleanas para maximizar a cobertura: “Bioprinting”, “3D Bioprinting”, “Organ Transplantation”, “Regenerative Medicine”, “Personalized Medicine”, “Bioinks”, “Vascularization in Bioprinting”.
Sinônimos e termos relacionados foram incluídos na estratégia de pesquisa para garantir uma ampla recuperação da literatura. A pesquisa foi restrita a artigos revisados por pares publicados em inglês entre 2018 e 2025. A estratégia de busca foi projetada para capturar a amplitude e a profundidade do campo, incluindo os avanços tecnológicos, biológicos e clínicos da bioimpressão.
Critérios de inclusão e exclusão
Os seguintes critérios de inclusão e exclusão foram aplicados para selecionar estudos relevantes para esta revisão:
Critérios de inclusão
- 1. Publicações em periódicos revisados por pares;
- 2. Estudos com foco específico em tecnologias e aplicações de bioimpressão;
- 3. Artigos que abordam os avanços na bioimpressão 3D de órgãos, medicina personalizada e terapias regenerativas;
- 4. Artigos que relatam avanços experimentais, computacionais ou clínicos em bioimpressão.
Critérios de exclusão
- 1. Estudos publicados em outros idiomas que não o inglês;
- 2. Artigos não revisados por pares, anais de conferências e resumos;
- 3. Artigos sem validação experimental, como artigos de opinião e modelos teóricos sem implementação prática;
- 4. Estudos que não se concentraram na bioimpressão de órgãos ou que não tinham relevância para aplicações clínicas.
Processo de triagem e seleção
A pesquisa inicial produziu um total de 141 artigos. O processo de seleção consistiu em três fases:
Fase 1: Remoção de duplicatas usando um software de gerenciamento de referências: todos os artigos coletados foram examinados em busca de entradas duplicadas. Após essa etapa, 83 artigos únicos permaneceram.
Fase 2: triagem de títulos e resumos: os títulos e resumos dos artigos restantes foram revisados de forma independente. Os estudos que claramente não atendiam aos critérios de inclusão com base no resumo foram excluídos. Essa etapa resultou na retenção de 62 artigos.
Fase 3: triagem de textos completos: os textos completos dos 62 artigos restantes foram avaliados quanto à relevância e à qualidade. Os artigos foram excluídos se não apresentassem dados robustos, metodologia detalhada ou alinhamento com os objetivos desta revisão. Após essa análise rigorosa, 48 artigos foram selecionados para inclusão na revisão final.
Extração de dados
Um formulário padronizado de extração de dados foi desenvolvido para capturar as principais informações de cada estudo, incluindo: autor(es) e ano de publicação; projeto e metodologia do estudo; principais descobertas e conclusões; relevância da bioimpressão no transplante de órgãos e na medicina regenerativa.
A extração de dados foi realizada de forma independente para garantir a precisão e a consistência.
Avaliação da qualidade
A qualidade dos estudos incluídos foi avaliada por meio das ferramentas de risco de viés ROBIS (Risk of Bias in Systematic Reviews) e Cochrane risk-of-bias, garantindo o rigor metodológico. Os estudos experimentais foram avaliados quanto à reprodutibilidade, análises estatísticas e controles, enquanto os estudos computacionais e baseados em simulação foram avaliados quanto às métricas de validação. Os estudos clínicos foram revisados quanto à conformidade ética, tamanho da amostra e relevância translacional.
Limitações da metodologia
Embora essa revisão de escopo garanta uma ampla cobertura do campo, algumas limitações são reconhecidas. Primeiro, a restrição da pesquisa a publicações em inglês pode ter excluído estudos relevantes em outros idiomas. Segundo, a preferência por literatura revisada por pares pode ter ignorado descobertas emergentes na área, mas não publicadas. Por fim, a natureza dinâmica dos avanços da bioimpressão necessita de atualizações contínuas desta revisão à medida que novos estudos se tornam disponíveis.
Fluxograma PRISMA
Para aumentar a transparência, um fluxograma PRISMA (Fig. 1) foi incluído para ilustrar o processo gradual de seleção de estudos. O diagrama detalha o número de registros identificados, selecionados, excluídos e incluídos em cada estágio, juntamente com os motivos das exclusões.
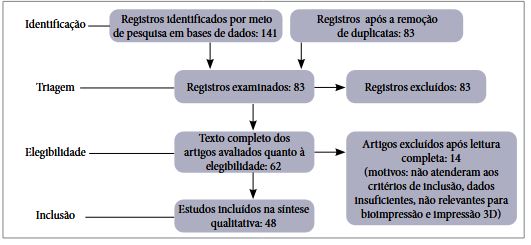
Figura 1
Fluxograma PRISMA.
Fonte: Elaborada pelo autor.
RESULTADOS
Avanços significativos na tecnologia de bioimpressão foram alcançados, especialmente no desenvolvimento de estruturas de órgãos vascularizados, biotintas aprimoradas e maior precisão na inserção de células. Inovações como a bioimpressão multimaterial e o design assistido por IA contribuíram para aumentar a fidelidade e a funcionalidade da impressão, permitindo arquiteturas teciduais mais complexas e melhores taxas de sobrevivência das células impressas. Esses avanços tecnológicos marcam uma etapa crucial em direção à tradução clínica da bioimpressão, aprimorando a integridade estrutural e funcional dos construtos bioimpressos.
Em termos de aplicações clínicas, a bioimpressão tem demonstrado um potencial considerável em testes de medicamentos, cicatrização de feridas e regeneração de tecidos. Os tecidos bioimpressos estão sendo atualmente usados como modelos para pesquisa farmacêutica, fornecendo plataformas mais precisas para avaliar a eficácia e a toxicidade de medicamentos e, ao mesmo tempo, reduzir a dependência de testes em animais. Além disso, os enxertos de pele com bioimpressão demonstraram sucesso na cicatrização de feridas, acelerando a regeneração do tecido e melhorando a integração com os tecidos circundantes. Embora órgãos bioimpressos totalmente funcionais ainda não estejam disponíveis para transplante, houve progresso na impressão de tecidos hepáticos e cardíacos, com modelos pré-clínicos demonstrando propriedades funcionais promissoras. Esses avanços indicam que a bioimpressão pode eventualmente levar a transplantes de órgãos personalizados, adaptados às necessidades individuais dos pacientes.
Apesar desses desenvolvimentos promissores, os desafios éticos e regulatórios continuam sendo barreiras significativas para a adoção generalizada da bioimpressão. As preocupações éticas incluem questões de consentimento do paciente, fornecimento de biotintas e o uso de materiais geneticamente modificados, que levantam questões relacionadas aos direitos dos doadores e à segurança a longo prazo. As agências reguladoras, como a Food and Drug Administration (FDA; Administração de Alimentos e Medicamentos, em português) e a Agência Europeia de Medicamentos (AEM), continuam a refinar as políticas que regem os produtos médicos bioimpressos, exigindo uma validação extensa para garantir sua segurança e eficácia antes da aprovação para uso humano. Além disso, questões de acessibilidade devem ser abordadas para evitar que a bioimpressão exacerbe as disparidades na área da saúde, garantindo que seus benefícios alcancem diversas populações de pacientes em vez de permanecerem restritos a instituições com recursos financeiros.
Tecnologias e técnicas de bioimpressão
A bioimpressão abrange uma série de técnicas sofisticadas projetadas para fabricar estruturas biológicas complexas e funcionais. Entre os principais métodos estão a bioimpressão baseada em extrusão, a bioimpressão a jato de tinta e a estereolitografia. A bioimpressão baseada em extrusão envolve a deposição contínua de biotinta por meio de um bocal, permitindo a criação de construtos intrincados e permeados de células com alta densidade celular6. Esse método é particularmente vantajoso para a produção de estruturas de tecido maiores devido à sua capacidade de imprimir com uma variedade de viscosidades e materiais. A bioimpressão por jato de tinta, por outro lado, utiliza forças térmicas ou acústicas para ejetar gotículas de biotinta em um substrato, permitindo a padronização em alta resolução de células e biomateriais. Essa técnica é conhecida por sua velocidade e precisão, o que a torna adequada para aplicações que exigem arranjos celulares detalhados. A estereolitografia emprega luz para curar seletivamente biotintas fotossensíveis, facilitando a construção de estruturas com resolução e complexidade excepcionais7. Essa abordagem é particularmente útil para a fabricação de suportes com características arquitetônicas precisas.
O ponto central para o sucesso dessas técnicas de bioimpressão é a seleção de biotintas apropriadas, que são formulações compostas de células vivas e biomateriais que imitam o ambiente da matriz extracelular. As biotintas devem possuir propriedades que suportem a viabilidade, a proliferação e a diferenciação das células, além de fornecer a integridade mecânica necessária para a estrutura impressa8. Os componentes comuns de biotintas incluem polímeros naturais, como alginato, gelatina e ácido hialurônico, que oferecem biocompatibilidade e promovem funções celulares. Polímeros sintéticos como polietilenoglicol também são utilizados para aprimorar as propriedades mecânicas e adaptar as taxas de degradação9. A escolha da biotinta é fundamental, pois influencia a capacidade de impressão, a estabilidade estrutural e o desempenho biológico do construto bioimpresso.
A integração de suportes e matrizes celulares na bioimpressão é essencial para replicar a arquitetura complexa dos tecidos nativos. Suportes fornecem uma estrutura tridimensional que sustenta a fixação de células e orienta o desenvolvimento do tecido. Em algumas técnicas de bioimpressão, os materiais sintéticos são impressos para formar moldes ou camadas rígidas que contêm a biotinta, evitando que ela se espalhe e mantendo a forma desejada do construto10. Esses suportes podem ser projetados para se degradarem com o tempo, permitindo que o tecido em desenvolvimento substitua o material do suporte à medida que ele adquire maturidade. A combinação de suportes com biotintas carregadas de células permite a fabricação de construtos teciduais que imitam fielmente as propriedades estruturais e funcionais dos tecidos naturais, avançando no campo da medicina regenerativa.11
Inovações e avanços recentes
Os recentes avanços na bioimpressão impulsionaram significativamente o campo para a fabricação de tecidos e órgãos funcionais, abordando desafios críticos na medicina regenerativa. As inovações nas técnicas de bioimpressão permitiram a criação de arquiteturas teciduais complexas que imitam fielmente suas contrapartes naturais12. Por exemplo, pesquisadores desenvolveram métodos para bioimprimir tecidos adiposos espessos com redes vasculares integradas, aumentando a viabilidade e a funcionalidade dos construtos. Esses desenvolvimentos são fundamentais para superar as limitações anteriores relacionadas à espessura do tecido e à difusão de nutrientes.13
Houve um progresso notável na bioimpressão de protótipos de órgãos, como o rim, o fígado e o coração. Em 2024, um estudo demonstrou a bioimpressão de tecidos hepáticos com arquiteturas vasculares complexas, que exibiram funções hepáticas essenciais e capacidade de resposta a tratamentos com medicamentos14. Da mesma forma, avanços na engenharia de tecidos cardíacos levaram à bioimpressão bem-sucedida de tecidos cardíacos que demonstram contrações sincronizadas e propriedades eletrofisiológicas semelhantes às do tecido cardíaco nativo15. Esses protótipos representam marcos significativos para o desenvolvimento de órgãos bioimpressos totalmente funcionais para transplante.
Um aspecto fundamental da bioimpressão de tecidos funcionais é a incorporação de redes vasculares para garantir o fornecimento adequado de nutrientes e oxigênio. Estudos recentes têm se concentrado no acoplamento sinérgico entre bioimpressão 3D e estratégias de vascularização para aumentar a viabilidade do tecido. Por exemplo, pesquisadores exploraram o uso de gradientes de fatores de crescimento e sistemas de cocultura para promover a formação de redes vasculares hierárquicas em tecidos bioimpressos16. Adicionalmente, abordagens de modelagem computacional foram empregadas para projetar uma vasculatura sintética em escala de órgão, facilitando a biomanufatura de construtos teciduais maiores e mais complexos. Esses esforços são cruciais para abordar os desafios associados à vascularização em tecidos bioimpressos, aproximando assim o campo da realização de órgãos bioimpressos transplantáveis.17
Aplicações em medicina regenerativa
A bioimpressão surgiu como uma abordagem transformadora na medicina regenerativa, oferecendo soluções inovadoras para engenharia de tecidos e cicatrização de feridas. Ao depositar células e biomateriais com precisão, a bioimpressão permite a criação de construtos teciduais complexos que imitam fielmente os tecidos nativos. Essa tecnologia facilita o desenvolvimento de enxertos customizados conforme as necessidades específicas do paciente, aumentando assim a eficácia dos tratamentos para várias lesões e condições degenerativas.18
No âmbito da regeneração de ossos e cartilagens, a bioimpressão tem demonstrado um potencial significativo. Ao utilizar biotintas compostas de células e biomateriais de suporte, pesquisadores fabricaram com sucesso construtos teciduais que promovem a regeneração de tecidos ósseos e cartilaginosos19. Essas estruturas bioimpressas proporcionam um ambiente propício para a proliferação e a diferenciação celular, levando à restauração da função em tecidos esqueléticos danificados. Essa abordagem é promissora para lidar com os desafios associados a defeitos ósseos e lesões de cartilagem, oferecendo um caminho para melhorar os resultados dos pacientes.20
A bioimpressão da pele representa um avanço significativo no tratamento de lesões por queimadura. Os métodos tradicionais de enxerto de pele geralmente enfrentam limitações, como a morbidade do local doador e a disponibilidade limitada de tecido saudável. A bioimpressão oferece uma alternativa promissora ao permitir a fabricação de construtos de pele que podem ser customizados de acordo com a geometria da ferida do paciente21. Essa abordagem não apenas acelera o processo de cura, mas também melhora os resultados estéticos e funcionais das vítimas de queimaduras. Estudos recentes destacaram o potencial dos substitutos de pele bioimpressos na promoção da cicatrização de feridas e na redução da formação de cicatrizes, melhorando assim a qualidade de vida de pacientes com queimaduras graves.22,23
Bioimpressão para transplante de órgãos
A bioimpressão é uma promessa significativa para o transplante de órgãos, mas vários desafios impedem a criação de órgãos totalmente funcionais e transplantáveis. Um dos principais obstáculos é replicar as intrincadas redes vasculares essenciais para o fornecimento de nutrientes e a remoção de resíduos em tecidos espessos. A obtenção da densidade celular e da organização espacial necessárias para imitar a funcionalidade do tecido nativo continua sendo complexa23. Adicionalmente, garantir a integridade mecânica e a viabilidade de longo prazo dos órgãos bioimpressos apresenta dificuldades substanciais. É fundamental a seleção de biotintas adequadas que favoreçam a proliferação e a diferenciação celular e, ao mesmo tempo, mantenham a capacidade de impressão e a estabilidade estrutural. Além disso, a integração de construtos bioimpressos com os sistemas biológicos do hospedeiro, incluindo a compatibilidade imunológica e o estabelecimento de interfaces funcionais com os tecidos existentes, apresenta outros desafios.24
Apesar desses obstáculos, notáveis metas de pesquisa foram alcançadas no campo da bioimpressão para transplante de órgãos. Por exemplo, pesquisadores conseguiram bioimprimir construtos teciduais do fígado que exibem as principais funções hepáticas, como a produção de albumina e a atividade da enzima citocromo P450, indicando o potencial para testes de medicamentos e aplicações de modelagem de doenças25. Na engenharia de tecidos cardíacos, os avanços levaram à bioimpressão desses tecidos demonstrando contrações sincronizadas e propriedades eletrofisiológicas semelhantes às do miocárdio nativo. Esses desenvolvimentos representam etapas significativas em direção à criação de órgãos bioimpressos adequados para transplante.26
Uma vantagem interessante da bioimpressão é seu potencial para atenuar a rejeição de órgãos. Ao utilizar as células do próprio paciente para criar biotintas, os órgãos bioimpressos podem ser customizados de acordo com o perfil genético e imunológico exclusivo do indivíduo, reduzindo assim o risco de rejeição imunológica27. Essa abordagem personalizada não apenas aumenta a biocompatibilidade, mas também elimina a necessidade de terapias imunossupressoras, que estão associadas a efeitos colaterais adversos e maior suscetibilidade a infecções.
O transplante tradicional de órgãos depende de órgãos de doadores, que geralmente são limitados, levando a longas listas de espera e altas taxas de mortalidade entre os pacientes que aguardam transplantes. A bioimpressão, por outro lado, tem o potencial de gerar órgãos sob demanda, resolvendo o problema da escassez. No entanto, embora os tecidos bioimpressos tenham demonstrado propriedades funcionais promissoras em estudos pré-clínicos, alcançar a funcionalidade total do órgão comparável à dos órgãos de doadores continua sendo um desafio.28
Embora a bioimpressão elimine os custos associados à logística relacionada à aquisição e ao transplante de órgãos, ela introduz despesas relacionadas a equipamentos especializados, ao desenvolvimento de biotintas e aos altos custos para garantir a conformidade regulatória. Os avanços na automação e nas técnicas de produção escalonáveis serão cruciais para reduzir esses custos ao longo do tempo.
O caminho para a tradução clínica de órgãos bioimpressos envolve uma validação rigorosa por meio de estudos pré-clínicos e clínicos. As agências reguladoras, como a FDA e a EAM, exigem dados abrangentes de segurança e eficácia antes de aprovar órgãos bioimpressos para transplante humano. Atualmente, os tecidos bioimpressos têm sido usados principalmente em testes de medicamentos e modelagem de doenças, com apenas alguns casos alcançando aplicações clínicas em estágio inicial. A superação dos obstáculos regulatórios será essencial para que a bioimpressão se torne uma alternativa comum ao transplante tradicional de órgãos.
Papel na medicina personalizada
A bioimpressão surgiu como uma tecnologia essencial na medicina personalizada, permitindo a customização de tecidos e órgãos para atender às necessidades específicas do paciente. Ao utilizar as células do próprio paciente, a bioimpressão facilita a criação de construtos teciduais sob medida que se alinham às características anatômicas e fisiológicas individuais, aumentando assim a eficácia das intervenções terapêuticas29. Essa abordagem não apenas melhora os resultados do tratamento, mas também minimiza o risco de rejeição imunológica, pois os tecidos bioimpressos são inerentemente compatíveis com o sistema imunológico do paciente.
No campo dos testes de medicamentos e da modelagem de doenças, a bioimpressão oferece avanços significativos. As metodologias tradicionais de teste de medicamentos geralmente se baseiam em modelos animais, que podem não reproduzir com precisão as respostas fisiológicas humanas, o que leva a possíveis discrepâncias nos perfis de eficácia e toxicidade dos medicamentos30. Os modelos de tecidos humanos bioimpressos fornecem uma plataforma mais precisa para avaliar as respostas aos medicamentos, reduzindo assim a dependência de testes em animais e aumentando a validade preditiva dos estudos pré-clínicos31. Além disso, esses modelos bioimpressos podem ser adaptados para representar estados de doença específicos, permitindo investigações mais precisas sobre os mecanismos da doença e o desenvolvimento de terapias direcionadas.
A implementação da bioimpressão específica do paciente também levanta considerações éticas importantes. Questões como o suprimento de células, o consentimento para seu uso e as implicações de longo prazo da criação de tecidos bioimpressos merecem uma deliberação cuidadosa32. Adicionalmente, é necessário abordar o potencial da bioimpressão de exacerbar as disparidades na área da saúde, especialmente se o acesso a esses tratamentos avançados for limitado a determinadas populações. As estruturas regulatórias precisam evoluir para garantir a aplicação ética das tecnologias de bioimpressão, equilibrando a inovação com a segurança do paciente e o acesso equitativo.33
Desafios e limitações
A bioimpressão, embora promissora, enfrenta vários desafios tecnológicos e biológicos que impedem seu avanço para a aplicação clínica. Um problema significativo é a escalabilidade; a fabricação de tecidos e órgãos em escala humana requer durações de impressão prolongadas, durante as quais a manutenção da viabilidade celular se torna um desafio34. A exposição prolongada a estressores ambientais durante longos períodos de impressão pode comprometer a saúde das células, levando à redução da funcionalidade do tecido bioimpresso.35
Adicionalmente, a complexidade da engenharia de tecidos com estruturas intrincadas apresenta obstáculos substanciais. A obtenção da densidade celular e da organização espacial necessárias para imitar a funcionalidade do tecido nativo continua complexa. Garantir a integridade mecânica e a viabilidade em longo prazo dos órgãos bioimpressos apresenta dificuldades substanciais36. É fundamental a seleção de biotintas adequadas que apoiem a proliferação e a diferenciação celular e, ao mesmo tempo, mantenham a capacidade de impressão e a estabilidade estrutural. Além disso, a integração de construtos bioimpressos com os sistemas biológicos do hospedeiro, incluindo a compatibilidade imunológica e o estabelecimento de interfaces funcionais com os tecidos existentes, apresenta outros desafios.37
Embora a tradução clínica permaneça em seus estágios iniciais, os tecidos bioimpressos já estão sendo utilizados em pesquisas farmacêuticas para testes de medicamentos, reduzindo a dependência de modelos animais. Adicionalmente, o desenvolvimento de enxertos de pele bioimpressos para vítimas de queimaduras tem demonstrado aplicações clínicas promissoras. Esses sucessos iniciais oferecem um vislumbre do potencial mais amplo da bioimpressão, uma vez que a escalabilidade e os desafios regulatórios sejam resolvidos.
Os desafios regulatórios e de ensaios clínicos complicam ainda mais o avanço das tecnologias de bioimpressão. A natureza multifacetada dos produtos bioimpressos, que combinam aspectos de impressão 3D, terapia celular e implantes personalizados, apresenta um desafio único para as estruturas regulatórias existentes38. As regulamentações atuais podem não abordar adequadamente as complexidades inerentes aos tecidos bioimpressos, necessitando do desenvolvimento de novas diretrizes para garantir a segurança e a eficácia.
O custo e a acessibilidade também representam barreiras significativas para a adoção generalizada das tecnologias de bioimpressão. Os altos custos associados a equipamentos de bioimpressão, materiais e pessoal especializado limitam a acessibilidade, principalmente em ambientes com recursos limitados39. Essa barreira econômica poderia exacerbar as disparidades existentes na área da saúde, restringindo os benefícios dos avanços da bioimpressão a instituições e populações com recursos financeiros. Abordar esses problemas de custo e acessibilidade é crucial para a implementação equitativa da bioimpressão na prática clínica.32
Implicações éticas, legais e sociais
O surgimento da tecnologia de bioimpressão, especialmente na fabricação de tecidos e órgãos humanos, apresenta uma gama complexa de implicações éticas, legais e sociais que merecem uma análise minuciosa.
Do ponto de vista ético, a criação de tecidos e órgãos humanos por meio da bioimpressão levanta questões sobre os limites morais da intervenção científica em processos biológicos naturais. Embora essa tecnologia tenha a promessa de aliviar a escassez de órgãos, ela também suscita preocupações quanto à mercantilização da vida humana e ao potencial de criação de entidades que desafiam nossas definições de personalidade40. Além disso, o uso de células humanas na bioimpressão exige uma análise cuidadosa do consentimento do doador e do fornecimento ético de materiais biológicos.41
Do ponto de vista jurídico, a bioimpressão se cruza com questões complexas de propriedade intelectual. Determinar a patenteabilidade de materiais bioimpressos é um desafio, pois os sistemas tradicionais de patentes geralmente excluem produtos derivados de fenômenos naturais. Essa ambiguidade complica a proteção das inovações em bioimpressão e pode prejudicar o avanço do campo42. Adicionalmente, a classificação dos órgãos bioimpressos sob as estruturas legais existentes permanece sem solução. Por exemplo, se os órgãos bioimpressos forem considerados equivalentes aos órgãos humanos naturais, eles poderão se enquadrar em regulamentações como a Lei Nacional de Transplante de Órgãos (National Organ Transplant Act), que proíbe a venda de órgãos humanos nos Estados Unidos, afetando assim a comercialização de produtos bioimpressos.32
Socialmente, a bioimpressão tem o potencial de impactar significativamente a equidade global na área da saúde. Os altos custos associados às tecnologias de bioimpressão podem limitar o acesso a tratamentos avançados, principalmente em locais com poucos recursos, exacerbando assim as disparidades existentes na área da saúde33. Além disso, a capacidade de produzir tecidos e órgãos humanos pode levar a debates sociais sobre a definição de vida e o status moral das entidades bioimpressas. Essas discussões necessitam de um envolvimento público inclusivo para navegar pelas implicações sociais da bioimpressão de forma responsável.43
ORIENTAÇÕES FUTURAS
O campo da bioimpressão está prestes a passar por avanços significativos, impulsionados por tendências emergentes, como a integração da inteligência artificial (IA) e da robótica. A convergência da IA com a bioimpressão permite a análise de dados biológicos complexos, facilitando o design de construtos teciduais mais precisos e funcionais44. Os algoritmos de IA podem otimizar os parâmetros de impressão em tempo real, aumentando a fidelidade e a eficiência do processo de bioimpressão. Adicionalmente, a incorporação de sistemas robóticos, especialmente a bioimpressão 3D com braço robótico, oferece maior automação e precisão, permitindo a fabricação de estruturas teciduais complexas com alta precisão espacial.45
A colaboração interdisciplinar desempenha um papel central no avanço das tecnologias de bioimpressão. A fusão de conhecimentos especializados de áreas como biologia, engenharia, ciência dos materiais e ciência da computação promove a inovação e aborda desafios multifacetados inerentes à bioimpressão46. Essa abordagem colaborativa, muitas vezes chamada de bioconvergência, aproveita diversas metodologias para solucionar problemas complexos na medicina regenerativa e em outras áreas.
Olhando para o futuro, espera-se que a próxima década testemunhe desenvolvimentos transformadores em bioimpressão e medicina regenerativa. Prevê-se que os avanços em IA e robótica refinem ainda mais as técnicas de bioimpressão, permitindo a produção de tecidos e órgãos mais complexos e funcionais47. Além disso, a integração contínua de abordagens interdisciplinares provavelmente produzirá soluções inovadoras para as limitações atuais, como a vascularização e a maturação do tecido. Esses desenvolvimentos prometem aproximar a bioimpressão das aplicações clínicas, potencialmente revolucionando a medicina personalizada e abordando a escassez global de órgãos transplantáveis.48
CONCLUSÃO
A bioimpressão surgiu como uma tecnologia pioneira com imenso potencial para revolucionar a medicina, abordando desafios críticos no transplante de órgãos, terapias regenerativas e medicina personalizada. Esta revisão da literatura explorou os princípios fundamentais, os avanços tecnológicos e as aplicações da bioimpressão, ao mesmo tempo em que esclareceu as implicações éticas, legais e sociais. A integração de tecnologias de ponta, como inteligência artificial e robótica, juntamente com a colaboração interdisciplinar, está abrindo caminho para avanços transformadores no campo. Embora desafios como escalabilidade, vascularização, obstáculos regulatórios e acesso equitativo permaneçam significativos, a pesquisa e a inovação em andamento continuam a expandir os limites do que é possível. Ao vislumbrar um futuro em que os tecidos e órgãos bioimpressos se tornem amplamente disponíveis, esse campo tem a promessa de preencher as lacunas no setor de saúde global, oferecendo esperança de melhores resultados para os pacientes e uma nova era na medicina regenerativa.
AGRADECIMENTOS
Não aplicável.
REFERÊNCIAS
Persaud A, Maus A, Strait L, Zhu D. 3D Bioprinting with Live Cells. Eng Regen 2022;3(3):292-309. https://doi.org/10.1016/j.engreg.2022.07.002
Gu Z, Fu J, Lin H, He Y. Development of 3D bioprinting: From printing methods to biomedical applications. Asian J Pharm Sci 2019;15(5):529-57. https://doi.org/10.1016/j.ajps.2019.11.003
Atala A, Bauer SB, Soker S, Yoo JJ, Retik AB. Tissue-engineered autologous bladders for patients needing cystoplasty. Lancet 2006;367(9518):1241-6. https://doi.org/10.1016/S0140-6736(06)68438-9
Mierke CT. Bioprinting of cells, organoids and organs-on-a-chip together with hydrogels improves structural and mechanical cues. Cells 2024;13(19):1638. https://doi.org/10.3390/cells13191638
Jongh D, Massey EK, Cronin AJ, Schermer MHN, Bunnik EM, VANGUARD Consortium. Early-phase clinical trials of bio-artificial organ technology: A systematic review of ethical issues. Transpl Int 2022;35:10751. https://doi.org/10.3389/ti.2022.10751
Fang Y, Guo Y, Liu T, Xu R, Mao S, Mo X, et al. Advances in 3D bioprinting. Chin J Mech Eng 2022;1(1):100011. https://doi.org/10.1016/j.cjmeam.2022.100011
Budharaju H, Sundaramurthi D, Sethuraman S. Embedded 3D bioprinting – An emerging strategy to fabricate biomimetic & large vascularized tissue constructs. Bioact Mater 2023;32:356-84. https://doi.org/10.1016/j.bioactmat.2023.10.012
Chen X, Anvari-Yazdi AF, Duan X, Zimmerling A, Gharraei R, Sharma N, et al. Biomaterials / bioinks and extrusion bioprinting. Bioactive Materials 2023;28:511-36. https://doi.org/10.1016/j.bioactmat.2023.06.006
Brahme P, Rarokar N, Kumbhalkar R, Saoji S, Khedekar P. Natural and synthetic polymeric hydrogel: a bioink for 3D bioprinting of tissue models. J Drug Deliv Sci Technol 2024(Part A);106204. https://doi.org/10.1016/j.jddst.2024.106204
Do AV, Khorsand B, Geary SM, Salem AK. 3D Printing of Scaffolds for Tissue Regeneration Applications. Adv Healthc Mater 2015;4(12):1742-62. https://doi.org/10.1002/adhm.201500168
Selim M, Mousa HM, Abdel-Jaber G, Barhoum A, Abdal-Hay A. Innovative designs of 3D scaffolds for bone tissue regeneration: Understanding principles and addressing challenges. Eur Polym J 2024;215:113251. https://doi.org/10.1016/j.eurpolymj.2024.113251
Mirshafiei M, Rashedi H, Yazdian F, Rahdar A, Baino F. Advancements in tissue and organ 3D bioprinting: Current techniques, applications, and future perspectives. Mater Des 2024;240:112853. https://doi.org/10.1016/j.matdes.2024.112853
Datta P, Ayan B, Ozbolat IT. Bioprinting for vascular and vascularized tissue biofabrication. Acta Biomater 2017;51:1-20. https://doi.org/10.1016/j.actbio.2017.01.035
Wang X, Zhang D, Singh YP, Yeo M, Deng G, Lai J, et al. progress in organ bioprinting for regenerative medicine. Engineering 2024;42:121-42. https://doi.org/10.1016/j.eng.2024.04.023
Cui H, Miao S, Esworthy T, Zhou X, Lee SJ, Liu C, et al. 3D bioprinting for cardiovascular regeneration and pharmacology. Adv Drug Deliv Rev 2018;132:252-69. https://doi.org/10.1016/j.addr.2018.07.014
Yeo M, Sarkar A, Singh YP, Derman ID, Datta P, Ozbolat IT. Synergistic coupling between 3D bioprinting and vascularization strategies. Biofabrication 2023;16(1):012003. https://doi.org/10.1088/1758-5090/ad0b3f
Sexton ZA, Hudson AR, Herrmann JE, Shiwarski DJ, Pham J, Szafron JM, et al. Rapid model-guided design of organ-scale synthetic vasculature for biomanufacturing. ArXiv 2023;arXiv:2308.07586v1. https://doi.org/10.48550/arXiv.2308.07586
Tripathi S, Mandal SS, Bauri S, Maiti P. 3D bioprinting and its innovative approach for biomedical applications. MedComm 2022;4(1):e194. https://doi.org/10.1002/mco2.194
Chiticaru EA, Ioniță M. Commercially available bioinks and state-of-the-art lab-made formulations for bone tissue engineering: a comprehensive review. Mater Today Bio 2024;29:101341. https://doi.org/10.1016/j.mtbio.2024.101341
Zhou J, Li Q, Tian Z, Yao Q, Zhang M. Recent advances in 3D bioprinted cartilage-mimicking constructs for applications in tissue engineering. Mater Today Bio 2023;23:100870. https://doi.org/10.1016/j.mtbio.2023.100870
Varkey M, Visscher DO, van Zuijlen PPM, Atala A, Yoo JJ. Skin bioprinting: the future of burn wound reconstruction? Burns Trauma 2019;7:4. https://doi.org/10.1186/s41038-019-0142-7
Kolimi P, Narala S, Nyavanandi D, Youssef AAA, Dudhipala N. Innovative treatment strategies to accelerate wound healing: trajectory and recent advancements. Cells 2022;11(15):2439. https://doi.org/10.3390/cells11152439
Huang G, Zhao Y, Chen D, Wei L, Hu Z, Li J, et al. Applications, advancements, and challenges of 3D bioprinting in organ transplantation. Biomater Sci 2024;12(6):1425-44. https://doi.org/10.1039/d3bm01934a
Mathur V, Agarwal P, Kasturi M, Srinivasan V, Seetharam RN, Vasanthan KS. Innovative bioinks for 3D bioprinting: Exploring technological potential and regulatory challenges. J Tissue Eng 2025;16:1-31. https://doi.org/10.1177/20417314241308022
Mota C, Camarero-Espinosa S, Baker MB, Wieringa P, Moroni L. Bioprinting: from tissue and organ development to in vitro models. Chem Rev 2020;120(19):10547-607. https://doi.org/10.1021/acs.chemrev.9b00789
Wang Z, Wang L, Li T, Liu S, Guo B, Huang W, Wu Y. 3D bioprinting in cardiac tissue engineering. Theranostics 2021;11(16):7948-69. https://doi.org/10.7150/thno.61621
Yaneva A, Shopova D, Bakova D, Mihaylova A, Kasnakova P, Hristozova M, et al. The progress in bioprinting and its potential impact on health-related quality of life. Bioengineering 2023;10(8):910. https://doi.org/10.3390/bioengineering10080910
Shopova D, Yaneva A, Bakova D, Mihaylova A, Kasnakova P, Hristozova M, et al. (Bio)printing in personalized medicine-opportunities and potential benefits. Bioengineering 2023;10(3):287. https://doi.org/10.3390/bioengineering10030287
Lam EHY, Yu F, Zhu S, Wang Z. 3D bioprinting for next-generation personalized medicine. Int J Mol Sci 2023;24(7):6357. https://doi.org/10.3390/ijms24076357
Parihar A, Parihar DS, Gaur K, Arya N, Choubey VK, Khan R. 3D bioprinting for drug development and screening: recent trends towards personalized medicine. Hybrid Adv 2024;100320. https://doi.org/10.1016/j.hybadv.2024.100320
Yang K, Wang L, Vijayavenkataraman S, Yuan Y, Tan E, Kang L. Recent applications of three-dimensional bioprinting in drug discovery and development. Adv Drug Deliv Rev 2024;115456. https://doi.org/10.1016/j.addr.2024.115456
Ricci G, Gibelli F, Sirignano A. Three-dimensional bioprinting of human organs and tissues: bioethical and medico-legal implications examined through a scoping review. Bioengineering 2023;10(9):1052. https://doi.org/10.3390/bioengineering10091052
Kantaros A, Ganetsos T, Petrescu FIT, Alysandratou E. Bioprinting and intellectual property: challenges, opportunities, and the road ahead. Bioengineering 2025;12(1):76. https://doi.org/10.3390/bioengineering12010076
Vijayavenkataraman S. 3D bioprinting: challenges in commercialization and clinical translation. J 3D Print Med 2023;7(2):3DP8. https://doi.org/10.2217/3dp-2022-0026
Xu HQ, Liu JC, Zhang ZY, Xu CX. A review on cell damage, viability, and functionality during 3D bioprinting. Mil Med Res 2022;9(1):70. https://doi.org/10.1186/s40779-022-00429-5
Derman ID, Moses JC, Rivera T, Ozbolat IT. Understanding the cellular dynamics, engineering perspectives and translation prospects in bioprinting epithelial tissues. Bioact Mater 2024;43:195-224. https://doi.org/10.1016/j.bioactmat.2024.09.025
Hasan MM, Ahmad A, Akter MZ, Choi YJ, Yi HG. Bioinks for bioprinting using plant-derived biomaterials. Biofabrication 2024;16(4):042004. https://doi.org/10.1088/1758-5090/ad6932
Mladenovska T, Choong PF, Wallace GG, O’Connell CD. The regulatory challenge of 3D bioprinting. Regen Med 2023;18(8):659-74. https://doi.org/10.2217/rme-2022-0194
Tong A, Pham QL, Abatemarco P, Mathew A, Gupta D, Iyer S, et al. Review of low-cost 3D bioprinters: state of the market and observed future trends. SLAS Technol 2021;26(4):333-66. https://doi.org/10.1177/24726303211020297
Kirillova A, Bushev S, Abubakirov A, Sukikh G. Bioethical and legal issues in 3D bioprinting. Int J Bioprint 2020;6(3):272. https://doi.org/10.18063/ijb.v6i3.272
Gilbert F, O’Connell CD, Mladenovska T, Dodds S. Print me an organ? Ethical and regulatory issues emerging from 3D bioprinting in medicine. Sci Eng Ethics 2017;24(1):73–91. https://doi.org/10.1007/s11948-017-9874-6
Devarapalli P, Ajay D. The impact of 3D bioprinting innovation on IP ecosystem and patent law: an Indian and US perspective. In: Singh K, Chongtham N, Trikha R, Bhardwaj M, Kaur S, editors. Science, technology and innovation ecosystem: an Indian and global perspective. 2024. p. 197-210. https://doi.org/10.1007/978-981-97-2815-2_9
Vijayavenkataraman S, Lu W, Fuh J. 3D bioprinting – an ethical, legal and social aspects (ELSA) framework. Bioprinting 2016;1-2:11–21. https://doi.org/10.1016/j.bprint.2016.08.001
Zhang Z, Zhou X, Fang Y, Xiong Z, Zhang T. AI-driven 3D bioprinting for regenerative medicine: from bench to bedside. Bioact Mater 2024;45:201-30. https://doi.org/10.1016/j.bioactmat.2024.11.021
Barjuei ES, Shin J, Kim K, Lee J. Precision improvement of robotic bioprinting via vision-based tool path compensation. Sci Rep 2024;14:17764. https://doi.org/10.1038/s41598-024-68597-z
Aljohani W, Ullah MW, Zhang X, Yang G. Bioprinting and its applications in tissue engineering and regenerative medicine. Int J Biol Macromol 2017;107:261-75. https://doi.org/10.1016/j.ijbiomac.2017.08.171
Jain P, Kathuria H, Dubey N. Advances in 3D bioprinting of tissues/organs for regenerative medicine and in-vitro models. Biomaterials 2022;287:121639. https://doi.org/10.1016/j.biomaterials.2022.121639
Jovic TH, Combellack EJ, Jessop ZM, Whitaker IS. 3D bioprinting and the future of surgery. Front Surg 2020;7:609836. https://doi.org/10.3389/fsurg.2020.609836
DECLARAÇÃO DO USO DE INTELIGÊNCIA ARTIFICIAL GENERATIVA
FINANCIAMENTO
DISPONIBILIDADE DE DADOS DE PESQUISA
Author notes
* Autor correspondente: kiroloss.eskandar@gmail.com
Conflict of interest declaration
