Resumen: El cáncer de seno es un grupo de enfermedades con gran impacto a nivel mundial dado que es una de las patologías con mayor prevalencia en mujeres y el cáncer con mayor tasa de mortalidad en varios países (GLOBOCAN 2012). El uso de la farmacogenética y farmacogenómica, en pacientes con cáncer de seno tiene como fin, generar una salud personalizada que permita tratar a cada paciente como individuo y no como enfermedad, pues cada paciente tiene necesidades particulares a la hora de suministrarle un tratamiento. El propósito de esta revisión es identificar las variantes genéticas reportadas en la literatura científica, donde se evalúan diferentes poblaciones y su posible uso como herramienta para medicina de precisión. En población colombiana es poca la caracterización poblacional que existe y por tanto estudios poblacionales son necesarios para definir los perfiles genéticos que deberán implementarse en nuestra población.
Palabras clave:cáncer de senocáncer de seno, farmacocinética farmacocinética, tamoxifeno tamoxifeno, hormonoterapia hormonoterapia.
Abstract: Breast cancer is one of the most prevalent diseases in women with increasing mortality in several countries (GLOBOCAN 2012). The use of pharmacogenetics and pharmacogenomics in patients with breast cancer allows generating personalized health for treating each patient as an individual, as each patient has unique needs when supplying a treatment. The purpose of this review is to identify genetic variants reported in the scientific literature, where different populations are evaluated and for possible use as a tool for medical precision. Colombian population is unique and therefore population studies are needed to define the genetic profiles to be implemented.
Keywords: breast cancer, pharmacokinetic, tamoxifen, hormone therapy.
Artículos
Tratamiento de cáncer de seno y farmacogenética
Treatment of breast cancer and pharmacogenetics
Universidad Nacional de Colombia
Recepción: 18 Septiembre 2015
Aprobación: 12 Abril 2016
El cáncer de seno esta conformado por un grupo de neoplasias malignas que tiene su origen en la proliferación acelerada a causa de pérdida del control del ciclo celular por alteración en al menos uno de los siguientes genes: BRCA1, BRCA2, P53 y PTEN, y en otros casos por razones desconocidas (Dunning et al., 1999). Puede estar localizado a nivel de los ductos o los lobulillos siendo el ductal el más frecuente. El término «Carcinoma in situ» se refiere al tipo de cáncer que se encuentra confinado en la luz de los ductos o de los lobulillos glandulares, sin invadir los tejidos vecinos. Por su parte, el carcinoma invasivo prolifera hasta romper la llamada membrana basal y extenderse infiltrando los tejidos que rodean a los ductos y lobulillos mamarios, penetrando así el tejido circundante (McCafferty et al., 2009).
Se presenta tanto en hombres y mujeres, aunque el cáncer de mama femenino es más frecuente. Las cifras reportadas para mortalidad por cáncer de seno en el periodo del 2000- 2006 en Colombia fueron de 12.287 personas, con una tasa cruda de 8,3 anual y una tasa ajustada por edad de 9,2 anual (Piñeros et al., 2010), adicionalmente, de acuerdo a lo reportado por GLOBOCAN (2012) la tasa de incidencia de cáncer de seno en mujeres para Colombia fue del 23,4% (8.686 casos) y la tasa de mortalidad fue del 13,8% (2.649 defunciones) (Ferlay et al., 2012).
Con el fin de clasificar los diferentes estadios de esta enfermedad se manejan diferentes esquemas, dentro de los que cabe mencionar, el sistema TNM que se basa en la clasificación por tamaño del tumor (T), si el tumor se ha diseminado a los ganglios linfáticos (N), en las axilas o aún no se ha diseminado, y si el tumor ha pasado a procesos metastásicos (M) y por otro lado la clasificación anatomopatológica, dentro de la que se evalúa; el estado de los receptores hormonales, grado histológico y tamaño. (Singletary et al., 2002).
Actualmente la clasificación molecular es la más usada y está basada en análisis de microarreglos, donde se estratifica el cáncer mamario en cuatro subtipos: 1) luminal; 2) similar a basal; 3) similar a normal y 4) HER2/ERBB2, (Perou et al., 2000; Sotiriou et al., 2003; Rodríguez et al., 2016).
Para los procesos de clasificación se emplean los receptores de superficie, que median procesos de transcripción celular. En la glándula mamaria se expresan tres receptores importantes: receptor de estrógeno (RE), receptor de progesterona (RP) y receptor de factor de crecimiento epidérmico humano 2 (HER2/neu). Estos receptores se encargan de llevar a cabo procesos de replicación que en condiciones fisiológicas normales mantienen el equilibrio celular, pero en procesos tumorales permiten la replicación de células tumorales que los sobre expresan y generan el rápido crecimiento del tumor. Aquellas células que no tengan ninguno de estos receptores se denominan basales o triple negativas (Dent et al., 2007).
Los cánceres de seno se clasifican sobre la base de las necesidades de crecimiento como dependiente de estrógeno y tumor independiente de estrógenos (Stoll BA., 1969; Furth J., 1975; Lacroix y Leclercq, 2004). Los RE hacen referencia a un grupo de receptores celulares que son activados por la hormona denominada 17β-estradiol o estrógeno. Los RE son proteínas intracelulares que al unirse a su ligando favorecen su translocación al núcleo e inducción de la expresión de genes específicos. (De vita et al., 1984). Al bloquear la actividad de estas hormonas con terapia hormonal, se detiene el crecimiento de las células del cáncer.
Estado de HER2. Se refiere a un oncogén que ayuda al crecimiento, división y reparación celular. Cuando las células tienen demasiadas copias de este gen, las células (incluyendo las cancerosas) se multiplican más rápidamente (Cabrera M. 2005; Piccart et al., 2005; Sánchez et al., 2008). Se sobre expresa en aproximadamente 25-30 % de las pacientes con cáncer de seno. Esto está asociado a un aumento en la actividad biológica del tumor. Las pacientes con cáncer de mama que presentan amplificación de HER2/ neu presentan generalmente una forma más agresiva de cáncer, además de una mayor resistencia a tratamientos convencionales. Sin embargo, son pacientes que responden mejor al tratamiento combinado de quimioterapia con trastuzumab, un anticuerpo monoclonal humanizado que se dirige contra el dominio extracelular del receptor Her2/neu, aumentando la tasa de supervivencia de las pacientes (McCafferty et al., 2009).
Actualmente mediante la identificación de receptores hormonales se determina si las células cancerosas pueden reaccionar a un tratamiento en particular.
En la figura 1, se muestra la Guía de manejo de pacientes con cáncer de seno del INC del 2013 donde se indican las opciones de tratamiento para pacientes con cáncer de seno, estratificándolo en no invasivo, localmente diseminado y metastásico.
La terapia local tiene como objetivo tratar el tumor en un sitio específico, sin afectar el resto del cuerpo. La cirugía y la radioterapia son ejemplos de terapias locales (Rosenberg, S. A., 2000).
La terapia sistémica se administra por vía oral o directamente en el torrente sanguíneo para llegar a las células cancerosas que se hayan podido propagar más allá del seno. La quimioterapia, terapia hormonal y inmunoterapia son terapias sistémicas.
Dentro de las alternativas de tratamiento se encuentran medidas quirúrgicas que contemplan lumpectomía, cuadrantectomía, mastectomía y mastectomía bilateral, por otro lado la radioterapia, la quimioterapia y la hormonoterapia, son alternativas que suelen usarse de manera combinada.
Para el propósito de esta revisión nos centraremos en los polimorfismos identificados en respuesta a hormonoterapia y quimioterapéuticos.
Descripción de los principales hormono terapéuticos: Los medicamentos de hormonoterapia que se usan para tratar el cáncer de seno con receptores de hormonas positivos actúan de dos formas (figura 2):
-
• Reducción de la concentración de estrógeno en el cuerpo.
• Bloqueo de la acción del estrógeno en las células del cáncer de seno.
Los medicamentos indicados para la hormonoterapia también pueden utilizarse para ayudar a reducir o desacelerar el crecimiento del cáncer de seno in situ, en estado avanzado o metastásico con receptores hormonales positivos.
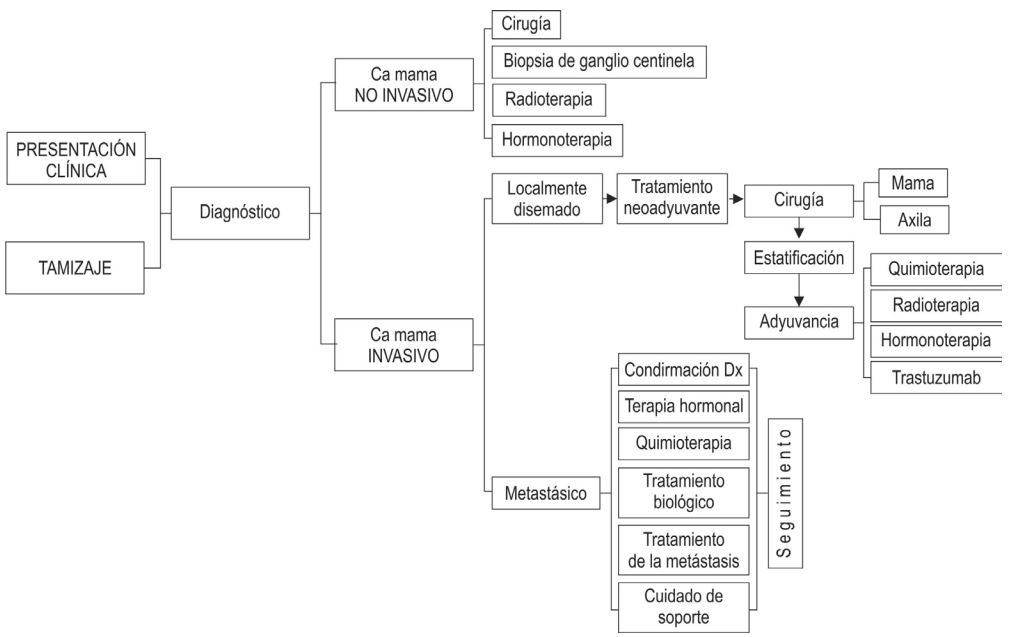
Figura 1
Algoritmo de manejo general en pacientes con Cáncer de seno. INC, 2013.
Protocolo de manejo pacientes cáncer de seno, Instituto Nacional de Cancerología (INC), 2013.
Existen varios tipos de medicamentos de hormonoterapia, entre los que se incluyen: inhibidores de aromatasa (IA), moduladores selectivos de los receptores de estrógeno y antagonistas del receptor de estrógeno, (figura 2), a continuación se describen cada uno de ellos.
Detienen la producción de estrógeno en mujeres postmenopáusicas, mediante el bloqueo de la enzima aromatasa (ver figura 2), que convierte el andrógeno en pequeñas concentraciones de estrógeno en el cuerpo. Los inhibidores de aromatasa no pueden impedir que los ovarios produzcan estrógeno, por lo que solamente son adecuados para mujeres postmenopáusicas.
Los agentes anti aromatasas se clasifican en 2 grupos:
Inhibidores e inactivadores de aromatasas. Los inhibidores se unen de forma transitoria a la aromatasa y los inactivadores se unen de forma permanente a la enzima. En la actualidad están aprobados 2 inhibidores:
-
• Arimidex (nombre genérico: anastrozol)
• Femara (nombre genérico: letrozol) Y un inactivador de aromatasas:
• Aromasin (nombre genérico: exemestano)
Son agentes que se unen al receptor de estrógeno donde simulan la actividad de los estrógenos en ciertos tejidos, mientras inhiben su acción en otros. Los MSRE tienen una variada actividad: compuestos con actividad totalmente agonista, como la hormona endógena estrógeno; compuestos con actividad agonista en algunos tejidos y antagonista en otros, como el tamoxifeno.
Es un modulador selectivo de los receptores de estrógenos. Su mecanismo de acción se basa en su efecto antiestrogénico, bloquea la acción de esta hormona que estimula el desarrollo de las células tumorales (figura 2). Su acción no se limita a la mama, pues diferentes órganos tienen receptores para estrógenos. En el útero (figura 2) tiene un efecto agonista estrogénico y en el hueso mejora la asimilación de calcio, por lo que es beneficioso en la osteoporosis.
El tamoxifeno es considerado como un profármaco ya que necesita ser transformado a sus respectivos metabolitos, los cuales son los responsables de su actividad farmacológica. Este fármaco tiene metabolismo primario y secundario el cual se lleva a cabo en el hígado, principalmente por las enzimas del citocromo P450, (figura 3). (Higgins et al., 2009 y Goetz et al., 2005).Y dependiendo la integridad de los diversos citocromos los pacientes pueden ser caracterizados como metabolizador ultrarrápido (UM), metabolizador normal (EM), metabolizador intermedio (IM) y metabolizador lento (PM) (Rodriguez e Ingelman., 2006).
El N-desmetiltamoxifeno es el metabolito más abundante sin embargo no es el responsable de la actividad de tamoxifeno; el metabolito 4-hidroxitamoxifeno representa menos del 10 % de la oxidación primaria de tamoxifeno catalizada por las enzimas CYP3A4 y CYP3A5, (figura 3) sin embargo se considera que su papel en el efecto farmacológico es muy importante ya que tiene un efecto antiestrogénico 100 veces superior al del tamoxifeno. Estudios han demostrado que hay otro metabolito, el 4-hidroxi-N-desmetil tamoxifeno (endoxifeno) el cual es formado a partir de la oxidación de N-desmetiltamoxifeno catalizado por la enzima CYP2D6; endoxifeno es más importante que 4-hidroxitamoxifeno ya que contribuye de manera más significativa en el efecto total anticanceroso de tamoxifeno, por lo tanto es el responsable de la actividad de este fármaco. (Goetz et al., 2005).

Figura 2
Síntesis de estrógenos, acción de hormonoterapéuticos y efecto del tamoxifeno sobre los receptores de estrógenos. Tamoxifeno (TAM) se une competitivamente a los receptores de estrógeno de tumores de seno produciendo un complejo nuclear que disminuye la síntesis de ADN e inhibe los efectos del estrógeno. Su acción no se limita a la mama, pues diferentes órganos tienen receptores para estrógenos (Figura 2B) (útero y hueso). En el útero tiene paradójicamente un efecto agonista estrogénico generando en algunos casos cáncer de útero y en el hueso mejora la asimilación de calcio, por lo que es beneficioso en la osteoporosis (Carpenter R. y Miller WR. 2005)
Los antagonistas del receptor de estrógeno (ARE) bloquean los efectos del estrógeno en el tejido mamario. Los ARE funcionan de una forma similar a los (MSRE). Los ARE se unen a los receptores del estrógeno en las células mamarias. Si un ARE se une al receptor del estrógeno, no hay espacio suficiente para que el estrógeno se acople a la célula (figura 2). Si el estrógeno no está unido a la célula de la mama, la célula no recibe las señales del estrógeno que le indican que debe crecer y multiplicarse. Además, los ARE tienen otros beneficios:
-
• Reducen la cantidad de receptores de estrógeno.
• Cambian la forma de los receptores de estrógeno en las células mamarias
Hay un ARE disponible para tratar el cáncer de mama de receptores de hormonas positivos:
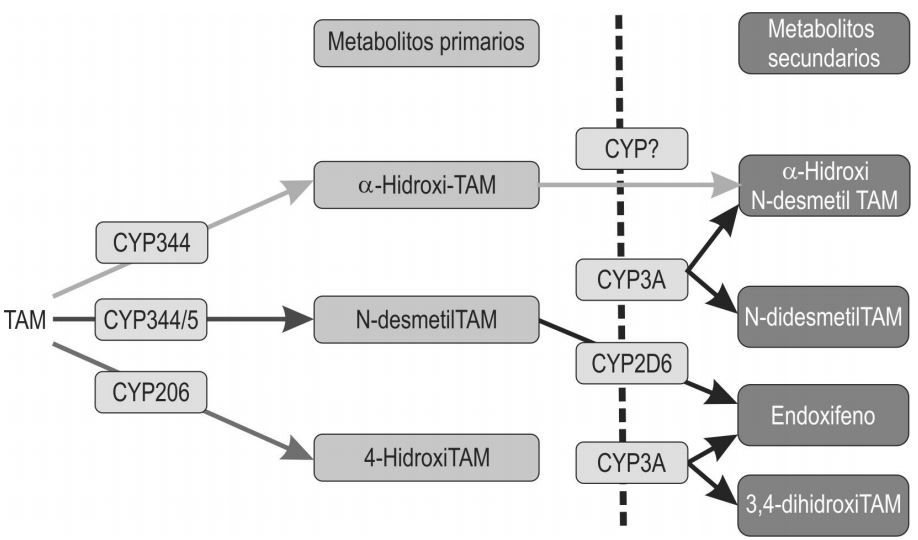
Figura 3
Metabolismo del tamoxifeno. Metabolitos primarios y secundarios. Tomado de Desta et al., (2005).
Fulvestrant es un medicamento que actúa por efecto antagonista sobre los receptores de estrógeno y se encuentra indicado para tratar a mujeres en edad postmenopáusica que presenten cáncer de mama en fase avanzada, únicamente en caso de que el tumor tenga receptores hormonales positivos y la enfermedad no responda a otros medicamentos bloqueantes de estrógenos, como el tamoxifeno. El mecanismo de acción del fármaco se basa en inactivar la acción de los estrógenos. El medicamento se presenta en forma de solución para administrar por vía intramuscular, la dosis habitual es 500 mg una vez al mes. Los efectos secundarios más frecuentes que se han observado consisten en dolor de cabeza, sensación de sofoco, vómitos o diarrea, erupción cutánea, dolor de espalda, reacciones alérgicas, aumento de los niveles de bilirrubina en sangre, fallo hepático, sensación de cansancio y riesgo aumentado de tromboembolismo.
Por otra parte, trastuzumab (comercializado con la marca Herceptin®) es un anticuerpo monoclonal humanizado. El trastuzumab se une selectivamente al receptor HER2. El HER2 se sobre expresa en la superficie de algunas células cancerosas y estimula la proliferación de éstas células. Cuando el trastuzumab se une al HER2 inhibe la proliferación celular. Trastuzumab se emplea en el tratamiento de pacientes con cáncer de seno que tienen expresión positiva del oncogen HER2. El trastuzumab es un producto biotecnológico producido en células de ovario de hámster chino (CHO) en cultivo.
Luego de revisar las diferentes alternativas de tratamiento y evaluando el esquema de manejo propuesto por el INC en el 2013, el hormonoterapéutico de primera elección es tamoxifeno, como previamente se sugirió en un estudio de costo-efectividad, donde se estableció tamoxifeno como la mejor alternativa para Colombia (Chicaíza, 2008) por otra parte los regímenes de quimioterapia están basados en antraciclinas asociados o no con taxanos. De manera que en el contexto de respuesta a tratamiento es importante tener en cuenta todos los factores que pueden incidir en la respuesta a tratamiento en una paciente con cáncer de seno, para esto es preciso evaluar factores tales como condiciones subyacentes, características propias del fármaco y farmacogenéticos de cada paciente (figura 4).
Diversas condiciones pueden incidir en la respuesta a hormonoterapia, es el caso del estudio realizado por Simonsson et al., (2013) donde se encontró que un moderado y alto consumo de café se asocia con una disminución significativa del riesgo de los primeros eventos en los pacientes tratados con tamoxifeno y el estado de los receptores hormonales. Si se confirma, quizás se justifique nuevas recomendaciones en relación con el consumo de café durante el tratamiento con tamoxifeno. Igualmente diversas publicaciones indican que la epigenética también incide en la respuesta a hormonoterapéuticos como el tamoxifeno. (Eccles et al., 2013, Pathiraja, et al., 2010, Van´t Veer et al., 2002).
En la tabla 1 se citan los principales polimorfismos asociados a respuesta en los diferentes tratamientos de hormonoterapia en pacientes con cáncer de seno.
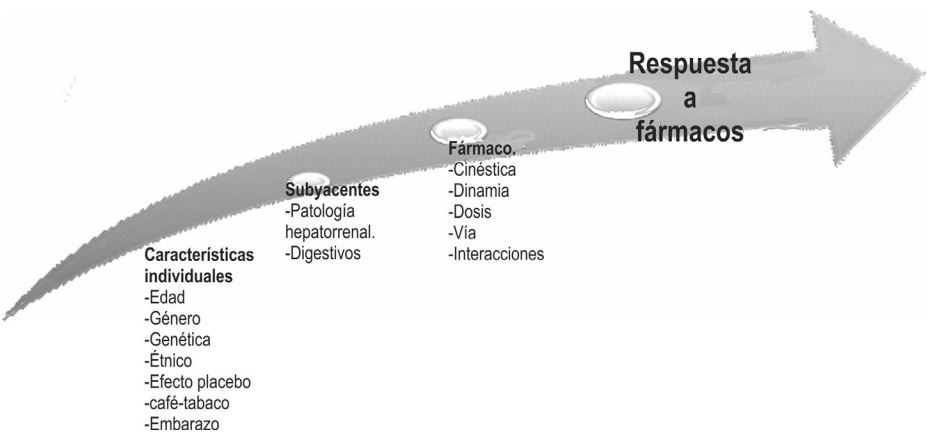
Figura 4
Factores que inciden en la respuesta a fármacos. En la figura se indican los factores individuales, propios del fármaco y condiciones subyacentes que inciden en la respuesta a un fármaco. Basada en Gurrola et al., 2010.
Variantes genéticas asociadas a respuesta en hormonoterapeuticos. (Saladores et al., 2013).
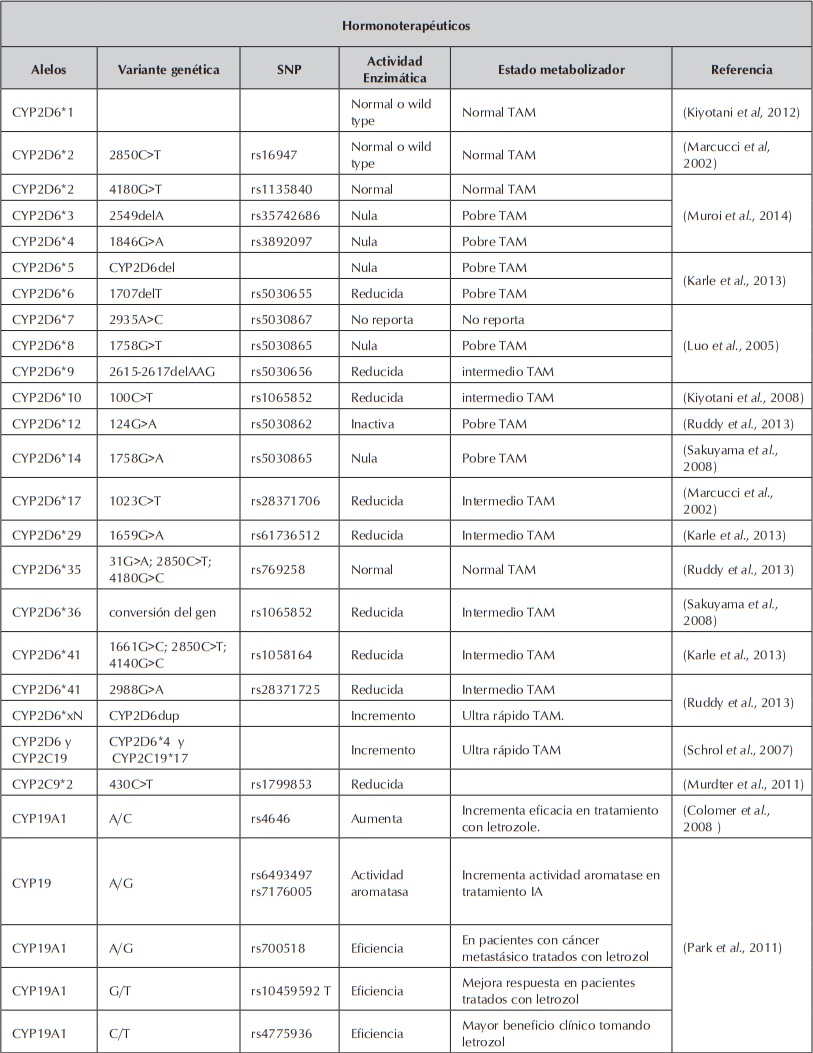
Variantes genéticas asociadas a respuesta en hormonoterapeuticos. (Saladores et al., 2013). Cont.
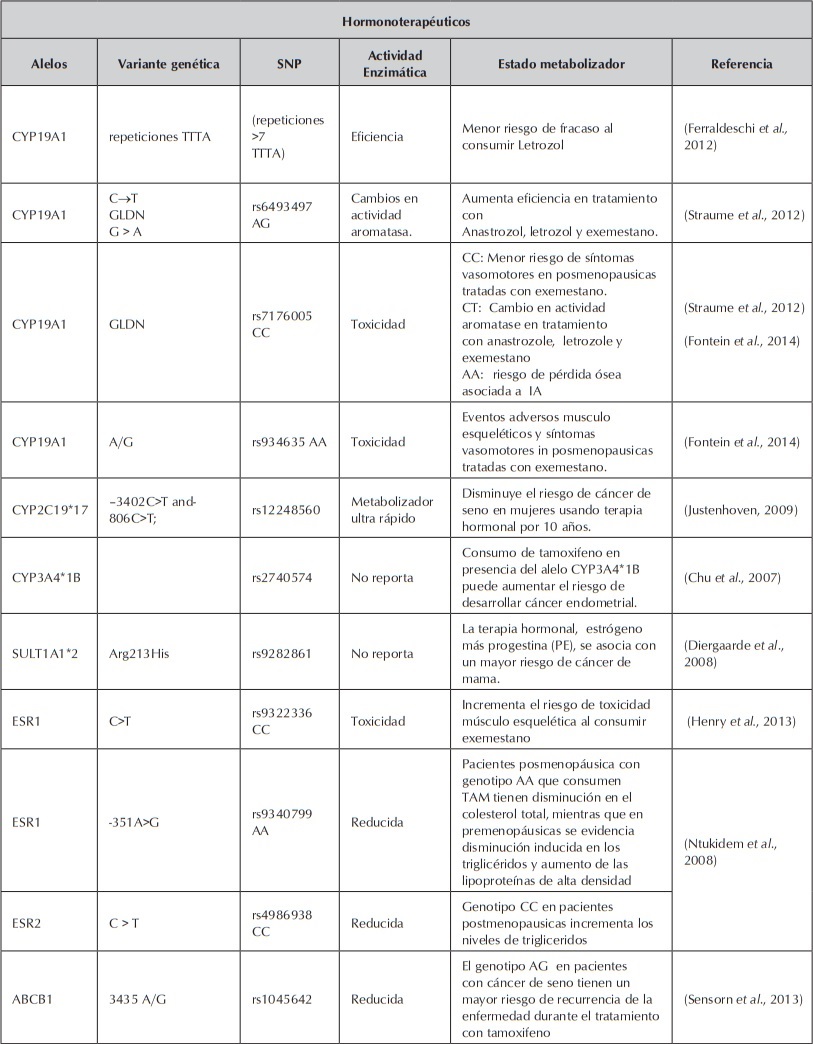
Variantes genéticas asociadas a respuesta en hormonoterapeuticos. (Saladores et al., 2013). Cont.
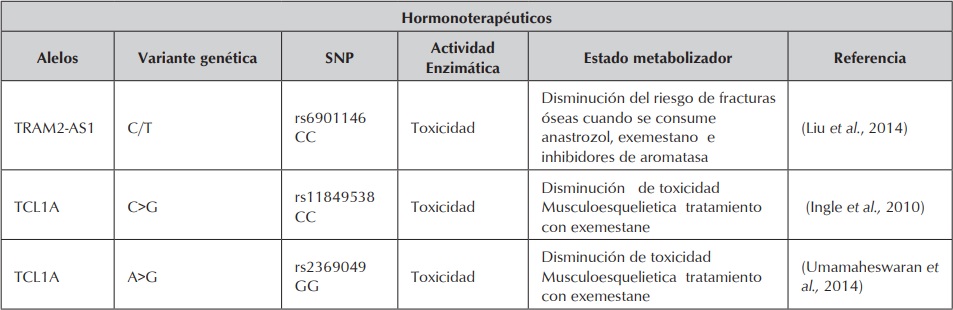
Como se mencionó previamente las frecuencias alélicas de CYP2D6 varían entre poblaciones, muchas de las cuales están recopiladas en la base de datos “CYP2D6 allele nomenclature”pero algunas aún no han sido incluidas, por esta razón en la tabla 2 se indican las que se han reportado después del 9-Dec-2014 que no están incluidas en “CYP2D6 allele nomenclature”. (PharmGKB CYP2D6 Allelic Variation Summary)
Por otra parte el tratamiento con quimioterapia en cáncer de seno incluye la combinación de diferentes medicamentos. Los protocolos basados en antraciclinas se han convertido en el estándar de quimioterapia adyuvante y neoadyuvante para la mayoría de pacientes, esto basados en las evidencias clínicas de eficacia en comparación con otros protocolos utilizados previamente (Hassan et al., 2010). Recientemente, taxanos, como docetaxel y paclitaxel, fueron incluidos en los protocolos basados en antraciclinas, mostrando reducción en el riesgo a recurrencia (De Laurentiis et al., 2008; Martin et al., 2010; Jacquin et al., 2012).
Dentro de la clasificación de los quimioterapéuticos describiremos las características de los más usados: están los agentes alquilantes que tienen su efecto directamente sobre el ADN evitando la reproducción de las células cancerosas, no son específicos de la fase; en otras palabras, actúan en todas las fases del ciclo celular. Por ejemplo la ciclofosfamida (Cytoxan®), carboplatino y oxaliplatino.
Antimetabolitos, interfieren con el crecimiento del ADN y del ARN al sustituir la síntesis de purinas y pirimidinas. Estos agentes dañan las células durante la fase S. Por ejemplo 5-fluorouracilo (5-FU), metrotexato.
Antraciclinas son antibióticos contra el cáncer que interfieren con las topoisomerasas fundamentales en la replicación de ADN. Estos medicamentos ejercen su acción en todas las fases del ciclo celular. Por ejemplo Doxorrubicina (Adriamycin®) y Epirubicina (Ellence®).
Inhibidores de la mitosis, son alcaloides de origen vegetal y otros compuestos derivados de productos naturales. Pueden detener la mitosis mediante su acción en los microtubulos. Son ejemplo Taxenos: paclitaxel (Taxol®) y docetaxel (Taxotere®).
Los protocolos de quimioterapia para cáncer de seno que se emplean actualmente son:
-
• CMF: ciclofosfamida , metotrexato, y 5-FU.
• CAF (o FAC): ciclofosfamida, doxorrubicina y 5-FU.
• AC: doxorrubicina y ciclofosfamida.
• EC: epirrubicina y ciclofosfamida.
• TAC: docetaxel , doxorrubicina y ciclofosfamida.
• AC → T: doxorrubicina y ciclofosfamida seguida de paclitaxel o docetaxel.
Trastuzumab (Herceptin) se puede administrar con el paclitaxel o el docetaxel para tumores HER2/neu positivos.
-
• A → CMF: doxorrubicina, seguida de CMF.
• CEF (FEC): ciclofosfamida, epirrubicina y 5-FU (a esto le puede seguir docetaxel).
• TC: docetaxel y ciclofosfamida.
• TCH: docetaxel, carboplatino, y trastuzumab, para tumores HER2/neu positivos.
Algunos otros medicamentos de quimioterapia que se usan para tratar a pacientes con cáncer de seno incluyen cisplatino, vinorelbina (Navelbine®), capecitabina (Xeloda®), doxorrubicina liposomal (Doxil®), gemcitabina (Gemzar®), mitoxantrona, exabepilona (Ixempra®), paclitaxel basado en albúmina (Abraxane®) y eribulina (Halaven®). Los medicamentos de terapia dirigida trastuzumab y lapatinib (Tykerb®) se pueden usar con estos medicamentos de quimioterapia para tumores que son HER2/neu positivos (Marsha S. y Liu G., 2009).
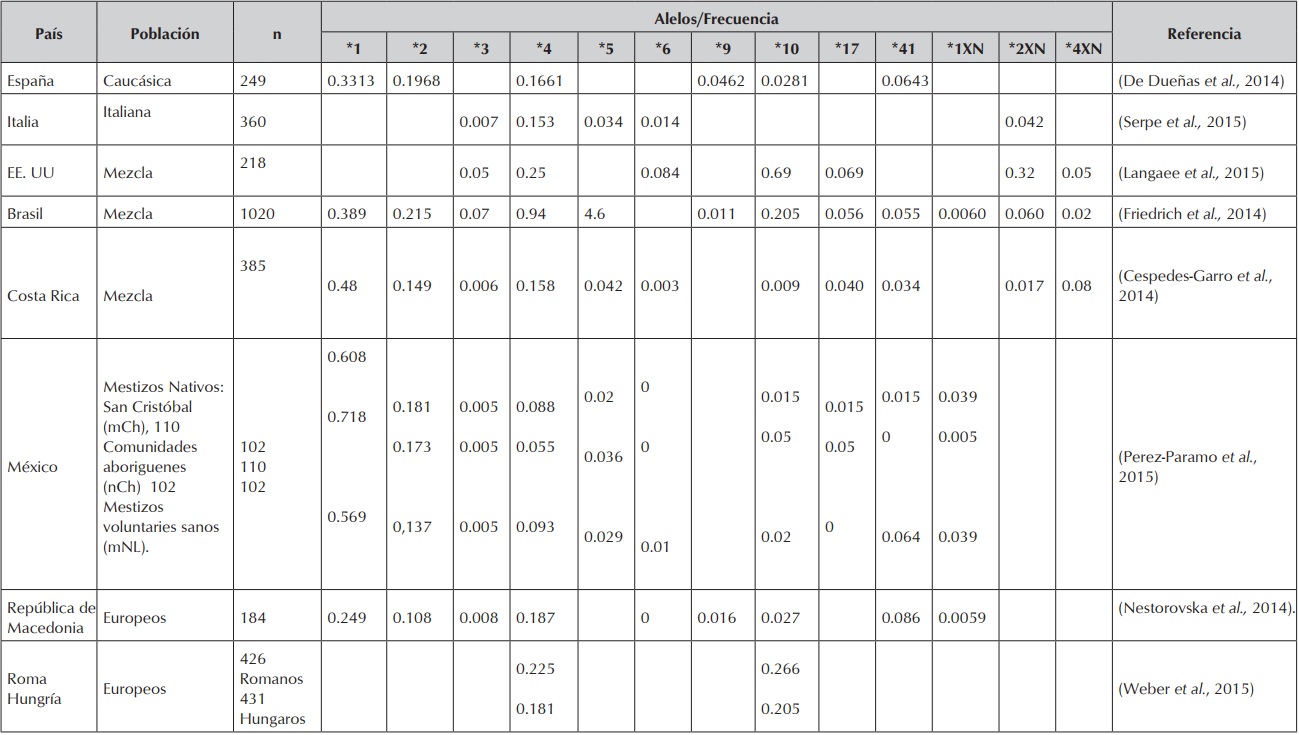
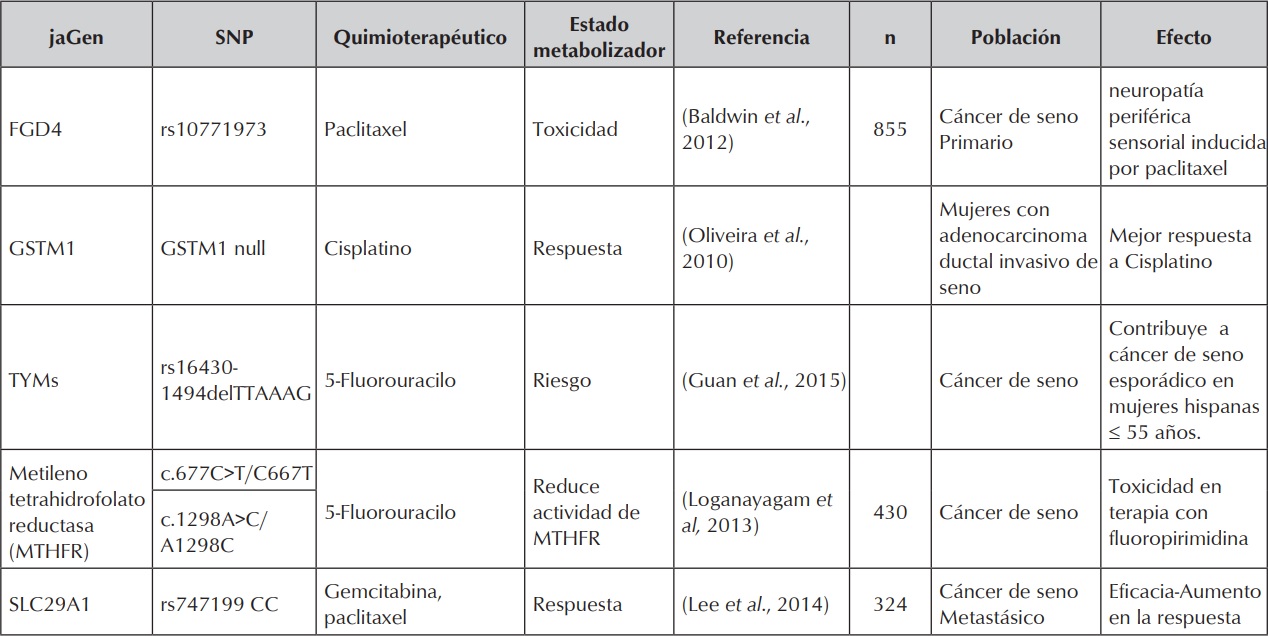
Las variantes genéticas asociadas a respuesta a quimioterapéuticos son diversas y varian entre poblaciones (tabla 3).
Frecuencias alélicas para los haplotipos de CPY2D6 en diferentes poblaciones.
Por otra parte, en la actualidad se encuentran test autorizados para ser practicados en mujeres con cáncer de seno; OncotypeDX®, MammaPrint®, AmpliChip CYP450®, Hercep Test™ y Endopredict®, (Rodríguez et al., 2016) que ayudan a tomar decisiones con respecto a tratamiento, pero que para población nacional presentan un costo alto y no existe una validación en población colombiana que permita garantizar, costo efectividad total.
Variantes genéticas asociadas a respuesta a quimioterapéuticos.
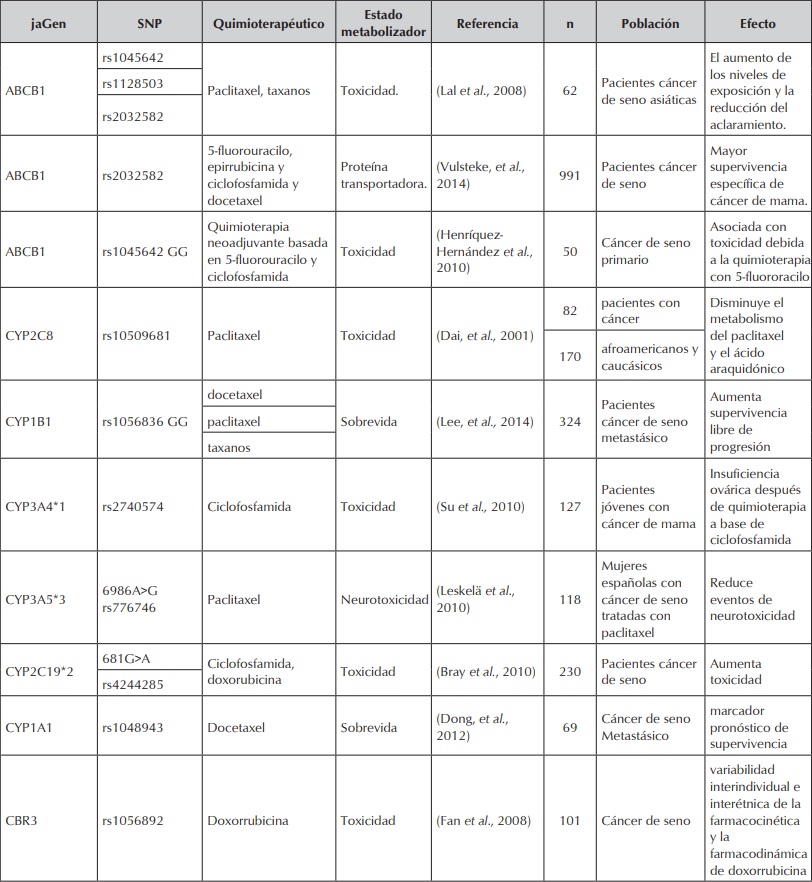
Variantes genéticas asociadas a respuesta a quimioterapéuticos. Cont.
La variabilidad humana hace necesario caracterizar cada población, para obtener la descripción de los polimorfismos genéticos asociadas con diferentes desenlaces, en farmacogenética conocer la frecuencia de variantes propias de población colombiana en diversas enzimas asociadas a respuesta a medicamentos usados en el tratamiento de cáncer de seno permitirá identificar patrones para prescribir un tratamiento que realmente pueda ser asimilado, evitando de este modo la presentación de efectos adversos ocasionados por toxicidad fuera del blanco y en aquellos que se identifique un genotipo pobre metabolizador se podrán implementar ajustes de dosis u otros esquemas de tratamiento. Teniendo en cuenta que el tamoxifeno es el hormono terapéutico de primera elección, se hace necesario evaluar los polimorfismos presentes en CYP2D6, para realizar la categorización de las pacientes en metabolizadoras lentas, intermedias o ultra rápidas. Una vez identificado su fenotipo se podrá prescribir el tratamiento adecuado.
Una vez identificadas las variantes genéticas frecuentes en población colombiana, esta información permitirán generar “kits en casa” que incluyan las variantes clínicas más relevantes y frecuentes, a un costo más accesible que permita realizar un tamizaje previo a suministrar un determinado tratamiento, generando la posibilidad de efectuar direccionamiento terapéutico. Se requiere caracterizar nuestra población pues solo cuando conozcamos las particularidades de nuestra población podremos generar soluciones a medida que nos acercaran a una medicina de precisión.

Figura 1
Algoritmo de manejo general en pacientes con Cáncer de seno. INC, 2013.
Protocolo de manejo pacientes cáncer de seno, Instituto Nacional de Cancerología (INC), 2013.

Figura 2
Síntesis de estrógenos, acción de hormonoterapéuticos y efecto del tamoxifeno sobre los receptores de estrógenos. Tamoxifeno (TAM) se une competitivamente a los receptores de estrógeno de tumores de seno produciendo un complejo nuclear que disminuye la síntesis de ADN e inhibe los efectos del estrógeno. Su acción no se limita a la mama, pues diferentes órganos tienen receptores para estrógenos (Figura 2B) (útero y hueso). En el útero tiene paradójicamente un efecto agonista estrogénico generando en algunos casos cáncer de útero y en el hueso mejora la asimilación de calcio, por lo que es beneficioso en la osteoporosis (Carpenter R. y Miller WR. 2005)

Figura 3
Metabolismo del tamoxifeno. Metabolitos primarios y secundarios. Tomado de Desta et al., (2005).

Figura 4
Factores que inciden en la respuesta a fármacos. En la figura se indican los factores individuales, propios del fármaco y condiciones subyacentes que inciden en la respuesta a un fármaco. Basada en Gurrola et al., 2010.
Variantes genéticas asociadas a respuesta en hormonoterapeuticos. (Saladores et al., 2013).

Variantes genéticas asociadas a respuesta en hormonoterapeuticos. (Saladores et al., 2013). Cont.

Variantes genéticas asociadas a respuesta en hormonoterapeuticos. (Saladores et al., 2013). Cont.

Frecuencias alélicas para los haplotipos de CPY2D6 en diferentes poblaciones.

Variantes genéticas asociadas a respuesta a quimioterapéuticos.

Variantes genéticas asociadas a respuesta a quimioterapéuticos. Cont.

