APLICAÇÃO DE REVESTIMENTO COM EXTRATOS DE JUREMA PRETA NO CONTROLE DE ANTRACNOSE EM FRUTOS DE MANGA
COATING APPLICATION WITH EXTRACTS OF JUREMA PRETA FOR THE CONTROL OF ANTHRACNOSE ON MANGO FRUITS
APLICAÇÃO DE REVESTIMENTO COM EXTRATOS DE JUREMA PRETA NO CONTROLE DE ANTRACNOSE EM FRUTOS DE MANGA
Revista Iberoamericana de Tecnología Postcosecha, vol. 17, núm. 2, pp. 205-216, 2016
Asociación Iberoamericana de Tecnología Postcosecha, S.C.
Resumo: Parte da produção agrícola é perdida durante o armazenamento pelo desenvolvimento de doenças e alterações físico-químicas. Com o objetivo de evitar essas perdas, avaliou-se o revestimento de frutos de manga com extratos de jurema preta e associado à cera de carnaúba e amido de milho. No experimento I, avaliou-se o desenvolvimento da Antracnose e a conservação dos frutos. Para isso, os frutos foram revestidos com extratos de jurema preta, extratos + cera de carnaúba e extratos + amido de milho. Os tratamentos foram aplicados nos frutos, nas concentrações de 0 a 5 mg.mL-1 e posteriormente realizou-se a inoculação dos frutos com Colletotrichum gloeosporioides. Avaliou-se: pH, acidez, SST, SST/AT do suco; severidade da doença e perda de massa nos frutos. No experimento II, Avaliou-se a severidade da doença, período de incubação e área abaixo da curva de progresso da doença (AACPD), aplicando-se os extratos e os extratos + cera de carnaúba nas concentrações de 0, 5, 10 e 15 mg.mL-1 e um fungicida. No experimento I, os extratos + cera de carnaúba reduziram a perda de massa, a Antracnose e retardaram o amadurecimento. Quando associados ao amido de milho, os resultados não foram satisfatórios. Os extratos brutos reduziram a doença, porém não retardaram os processos de amadurecimento. No experimento II, o tratamento cera de carnaúba + extrato a 10 mg.mL-1 expressou a menor AACPD, reduziu a doença em 95%, apresentou maior período de incubação e menor incidência.
Palavras-chave: Antifúngico, Cera de carnaúba, Mimosa tenuiflora, Pós-colheita.
Abstract: Part of agricultural production is lost during storage by the development of diseases and physical-chemical changes. With the objective to avoid these losses, it was evaluated the coating of mango fruits with extracts of jurema preta and associated with carnauba wax and corn starch. In experiment I, it was evaluated the development of Anthracnose and conservation of fruits. For this reason, the fruits were coated with extracts of jurema preta, extracts + carnauba wax and extracts + corn starch. The treatments were applied in the fruits, at concentrations of 0 to 5 mg.mL-1 and subsequently took place the inoculation of fruits with Colletotrichum gloeosporioides. It was evaluated: pH, acidity, SST, SST/AT juice; disease severity and loss of mass in fruits. In experiment II, it was evaluated the disease severity, incubation period and area under the disease progress curve (AUDPC), applying the extracts and the extracts + carnauba wax in the concentrations of 0, 5, 10 and 15 mg.mL-1 and a fungicide. In experiment I, the extracts + carnauba wax reduced the loss of mass, Anthracnose and delayed ripening. When associated to maize starch, the results were not satisfactory. The crude extracts reduced the disease, but does not have delayed ripening processes. In experiment II, treatment carnauba wax + extract at 10 mg.mL-1 expressed the smaller AUDPC, reduced the disease in 95%, presented higher incubation period and lower incidence.
Keywords: Antifungal, Carnauba wax, Mimosa tenuiflora, Post-harvest.
INTRODUÇÃO
A produção brasileira de alimentos vem atingindo novos patamares todos os anos, como resultado das tecnologias aplicadas no campo para o aumento da produtividade e a anexação de novas fronteiras agrícolas. Contudo, parte dessa produção não chega à mesa da população, ela é perdida durante o armazenamento, principalmente quando é infectada por patógenos próprios da fase de pós-colheita ou quando encontram condições favoráveis ao seu desenvolvimento.
As perdas na pós-colheita ocasionada por Antracnose tem grande importância para uma série de culturas, pois seu agente etiológico, o Colletotrichum gloeosporioides causa muitos prejuízos por tornar os frutos impróprios ao consumo, além de potencializar o desenvolvimento de saprófitos. Vários estudos foram realizados com o propósito de reduzir as infecções desse patógeno em frutos de manga (Lemos et al. 2013), goiaba (Fischer et al. 2012); pimenta (Souza et al. 2012) e banana (Celoto et al. 2011). Esses autores têm procurado controlar a Antracnose de forma eficiente utilizando produtos alternativos, como a utilização de óleos essenciais e extratos vegetais (Lemos et al. 2013; Souza et al. 2012; Celoto et al. 2011) e revestimentos comestíveis (Dung et al. 2008).
Estudos realizados por Fischer et al. (2009) mostraram que a Antracnose incidiu em 100% sobre 15 variedades de manga, um dia após o armazenamento. Esses frutos também apresentaram podridões pedunculares causadas por Lasiodiplodia theobromae, Fusicoccum spp. e Dothiorella spp., potencializando as perdas em pós-colheita tanto pelo aspecto visual quanto pela podridão.
Produtos convencionais também foram avaliados e alguns já se apresentaram ineficientes no controle da Antracnose (Fischer et al. 2012). Os dados apresentados por esses autores são preocupantes, pois mostram o desenvolvimento de raças resistentes aos produtos químicos, o que aumenta os custos de produção e compromete a saúde dos consumidores.
Para evitar a seleção de patógenos resistentes é necessário o desenvolvimento de produtos que não potencialize essa seleção e que não sejam maléficos à saúde dos consumidores. Além de assegurar a disponibilidade de produtos livres de microrganismos é desejável também que os produtos tenham seu tempo de prateleira prolongado.
Esse trabalho teve como principal objetivo avaliar a atividade dos extratos de jurema preta isoladamente e associado com cera de carnaúba e amido de milho no controle da Antracnose em frutos de manga cv. Tommy Atkins e retardar os processos de senescência.
MATERIAL E MÉTODOS
Preparo do extrato. Foram coletadas cascas do caule de jurema preta, Mimosa tenuiflora (Wild) Poiret, em área de Caatinga, Petrolina- PE, no mês de agosto de 2014, seguindo as coordenadas geográficas, 9º19’ S, 40º31’W. Os ensaios foram desenvolvidos nos laboratórios de Bioquímica Vegetal, Microbiologia e Instituto de Pesquisas em Substancias Bioativas – IPESB da Universidade Federal do Vale do São Francisco (UNIVASF), no Campus de Juazeiro Bahia. O processamento do material vegetal e as concentrações do extrato foram realizadas segundo Borges et al. (2013).
Obtenção dos isolados. O isolado de Colletotrichum gloeosporioides foi obtido de frutos com sintomas característicos da doença, coletado em uma propriedade particular no Município de Juazeiro da Bahia, que foi isolado e purificado em Batata Dextrose Agar (BDA) e incubado por sete dias sob Demanda Bioquímica de Oxigênio (BOD) a 25 °C e fotoperíodo de 12 horas.
Ao atingir sete dias de incubação, foram adicionados 10 mL de água destilada e esterilizada (ADE) em cada placa de Petri, em seguida o crescimento fúngico foi raspado com auxílio de uma escova para liberação dos conídios e filtrado em gaze, sendo a concentração da suspensão dos conídios determinada em câmara de Neubauer e expresso em conídios.mL-1.
Experimento I. Avaliação dos revestimentos à base de extratos de jurema preta, extratos + amido de milho e extratos + cera de carnaúba sobre frutos de manga no controle da Antracnose
Os frutos de manga cv. Tommy Atkins foram obtidos de uma propriedade local, no Município de Juazeiro-BA e tratados no laboratório de Bioquímica Vegetal da UNIVASF. Os frutos foram lavados em água corrente com sabão, secos e desinfestados com álcool 70% e solução de hipoclorito de sódio 0,7% e logo depois, lavados em água corrente e colocados para secar. Após a secagem os frutos foram marcados quatro círculos na superfície dos frutos, dois em cada extremidade, e efetuados raspagens com uma lixa (150) provocando ferimentos para simular danos mecânicos próprios do processo de transporte e então aplicados os tratamentos. Foram avaliados 36 tratamentos, 18 sem alterar o pH e 18 alterando-se o pH dos extratos para 10 utilizando-se hidróxido de sódio 0,1 mol.L-1. T0: controle positivo; T1: aplicação de extrato bruto de M. tenuiflora (EB) a 1,0 mg. mL-1 ; T2: aplicação de EB a 2,0 mg. mL-1; T3 aplicação de EB a 3,0 mg. mL-1; T4 aplicação de EB a 4,0 mg. mL-1; T5 aplicação de EB a 5,0 mg. mL-1; T6: aplicação de amido de milho a 4%; T7: aplicação de EB a 1,0 mg. mL-1 + amido de milho a 4%; T8: aplicação de EB a 2,0 mg. mL-1 + amido de milho a 4%; T9: aplicação de EB a 3,0 mg. mL-1 + amido de milho a 4%; T10: aplicação de EB a 4,0 mg.mL-1 + amido de milho a 4%; T11: aplicação de EB a 5,0 mg. mL-1 + amido de milho a 4%; T12: aplicação de cera de carnaúba (1:1); T13: aplicação de EB a 1,0 mg. mL-1 + cera de carnaúba; T14: aplicação de EB a 2,0 mg. mL-1 + cera de carnaúba; T15: aplicação de EB a 3,0 mg. mL-1 + cera de carnaúba; T16: aplicação de EB a 4,0 mg. mL-1 + cera de carnaúba; T17: aplicação de EB a 5,0 mg. mL-1 + cera de carnaúba. Os tratamentos T18 a T36 são os mesmos tratamentos já citados com o pH dos extratos alterados para 10.
Vinte e quatro horas após a aplicação dos tratamentos realizou-se a inoculação de C. gloeosporioides sobre os ferimentos. Foi depositada uma gota de 40 μL da suspensão de C. gloeosporioides com concentração de 107 conídios.mL-1. Os frutos foram incubados em BOD por 24 horas (UR% 75 ± 2% e 20 °C ± 2). Passado o período de incubação os frutos foram mantidos em ambiente controlado (UR% = 60% +/- 5 e T=27°C) durante 17 dias sendo que as avaliações tiveram início no décimo dia após inoculação.
Analises físico-química
Sólidos Solúveis Totais do suco (SST). Foi determinado por refratômetro, utilizando-se um refratômetro digital e os conteúdos expressos em percentagem.
Acidez Total Titulável do suco(AT). Foi determinada através da titulação de 5 mL de suco na proporção de 1:10 de água destilada, para melhorar a visualização do ponto de viragem, com NaOH a 0,1 M, devidamente padronizado com bifitalato de potássio utilizando-se fenolftaleína 1% como indicador do ponto de viragem (pH 8). Os valores obtidos foram expressos em grama de acido cítrico.100 mL-1 de suco, conforme AOAC (1995).
Equivalente grama de acido cítrico em 100 mL de suco = V.f.M.ME.100/P, onde: V= volume gasto de NaOH (L), f= fator de correção do NaOH, M = moralidade do NaOH, ME = Massa em equivalente grama do acido cítrico, P = volume da polpa.
pH do suco. A medida foi realizada diretamente sobre o suco concentrado, utilizando-se um pHmetro de bancada.
Perda de massa fresca dos frutos. Essa mediada física determina a perda de massa entre duas pesagens subsequentes. Realizou- se seis pesagens em intervalos de 24 horas, iniciando-se 10 dias após a inoculação. Para determinação da massa utilizou-se uma balança digital com uma casa decimal. Os valores obtidos foram expressos percentagem de massa perdidos diariamente.
PM (%) = Mi-Mf .100/Mi; onde: PM = perda de massa Mi = massa inicial; Mf = massa final
Avalição da doença dos frutos. Foram feitas medidas do diâmetro, em centímetros, das lesões, ocasionadas pelo patógeno inoculado, em seguida considerando-se a área da lesão circular, calculou-se a área do circulo através da formula: A= π x r2. Para sintomas de podridão que incidiu sobre toda a superfície dos frutos e não eram sintomas característicos reproduzidos pelo patógeno inoculado, considerou-se a área do fruto, calculado através do softwere QUANT.
O delineamento experimental, para as variáveis: pH do suco, acidez do suco, perda de massa, sólidos solúveis e severidade foi inteiramente ao acaso (DIC) com cinco repetições e as medias dos tratamentos comparadas pelo teste de Scott-Knott a 5% de probabilidade utilizando-se o programa ASSISTAT e medias transformadas para X=√x
Experimento II. Obtenção, inoculação dos frutos e aplicação dos revestimentos
Os frutos de manga tiveram a mesma origem dos utilizados no experimento I e foram desinfestados utilizando-se o mesmo procedimento.
Foram marcados dois círculos na superfície dos frutos, um em cada extremidade, e efetuados cinco furos equidistantes em cada área delimitada com auxilio de uma agulha até a profundidade de dois milímetros, em seguida foram aplicados os seguintes tratamentos: T1: testemunha positiva, controle; T2: testemunha negativa, fungicida SPORTAK®, principio ativo: N- propyl - N- [2- (2,4,6- trichlorophenoxy) ethyl]imidazole- 1- carboxamide (PROCLORAZ) a 1,1µL.mL-1; T3: aplicação de extrato bruto de jurema preta (EB) a 5,0 mg.mL-1 ; T4: aplicação de EB a 10,0 mg.mL-1; T5: aplicação de EB a 15,0 mg.mL-1; T6: aplicação de cera de carnaúba (1:1); T7: aplicação de EB 5,0 mg.mL-1 + cera de carnaúba; T8: aplicação de EB 10 mg. mL-1 + cera de carnaúba; T9: aplicação de EB 15 mg.mL-1 + cera de carnaúba.
Vinte e quatro horas após a aplicação dos tratamentos realizou-se a inoculação de 40µL da suspensão de conídios de C. gloeosporioides na concentração de 107 conídios por mililitro. Realizada a inoculação os frutos foram mantidos em BOD (T= 27ºC e UR=80%) durante sete dias. A avaliação da severidade da doença foi iniciada 48 horas após a inoculação, sendo realizadas seis avaliações da severidade com intervalo de 24 horas, e posterior cálculo da área abaixo da curva de progresso da doença (AACPD), através da fórmula AACPD = Σ(yi + yi+1)/2 * (ti+1 – ti), onde: i = número de avaliações; y = severidade da antracnose (mm); t = tempo (dias) (Shaner & Finney, 1977).
O delineamento dos experimentos foi inteiramente ao acaso (DIC) com nove repetições. Os dados experimentais foram analisados pelo programa ASSISTAT e as médias comparadas pelo teste de Tukey a 5% de probabilidade e as médias transformadas para X=√x.
O período de incubação (PI) compreendido entre a inoculação e o surgimento da doença foi avaliado em horas, intervalo de 24 horas, sendo o delineamento experimental inteiramente casualisado e as medias das nove repetições comparadas pelo teste de Scott- knott a 5% de probabilidade, suas medias transformadas para X=√x.
Incidência da doença é o surgimento da doença em determinado período de tempo, calculado em percentagem em relação aos frutos sadios. Para avaliação estatística da média das nove repetições foi utilizado regressão na analise de variância, utilizando-se o programa computacional ASSISTAT.
RESULTADOS E DISCUSSÃO
No experimento I, as aplicações dos revestimentos apresentaram eficiência no controle da Antracnose em frutos de manga cv Tommy Atkins e retardaram os processos de amadurecimento dos frutos, tanto para os extratos que tiveram seu pH ajustado para 10, quanto sem alteração (pH 7), com destaque para o revestimento a base de extratos + cera de carnaúba nas concentrações de 4 e 5 mg.mL-1, que reduziram significativamente as perdas de massa e a severidade da doença (Tabela 1). Foi possível observar que a simples alteração do pH dos revestimentos para básico foi suficiente para reduzir, no geral, o desenvolvimento da doença e a perda de massa dos frutos, por isso, dar-se-á ênfase a discussão dos tratamentos sem alteração do pH.
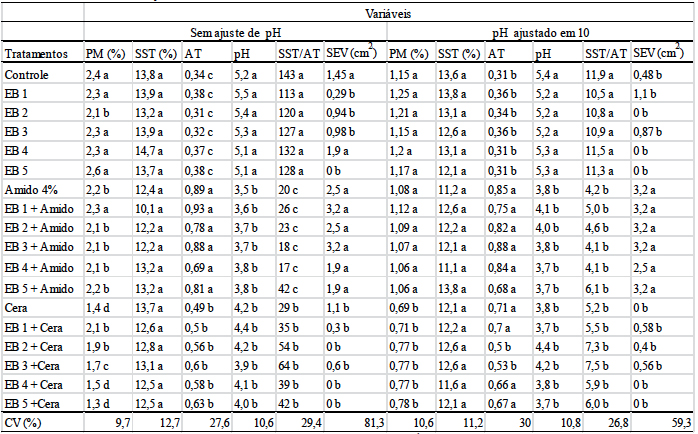
EB1, EB2, EB3, EB4, EB5 (Extrato bruto nas concentrações: 1; 2; 3; 4; 5 mg.mL-1 respetivamente); A+EB: Extrato bruto nas respectivas concentrações + amido de milho; C+EB: Extrato bruto nas respectivas concentrações + cera de carnaúba. Médias seguidas da mesma letra não diferem entre si pelo teste de Scott-Knott a 5% de probabilidade.
A influencia do pH sobre o crescimento micelial e esporulação de Aspergillus parasiticus foi observado por Abubakar et al. (2013), constatando que com o aumento do pH do meio houve redução da massa de micélio e da esporulação. Com pH 4 a massa seca obtida pesou 355,67 mg enquanto com pH 10 esse valor reduziu para 302,73 mg e para esporulação a redução nesse intervalo de pH, foi mais drástica, caindo de 4,5 para 2,8x107 esporos.mL-1.
Quanto a redução dos processos de amadurecimento e conservação física e química dos frutos os tratamentos à base de jurema preta + cera de carnaúba ( EB + Cera) apresentaram as menores medias de perda de massa, acidez, pH do suco e não diferiu estatisticamente dos demais tratamentos em relação aos sólidos solúveis totais (SST).
Os efeitos positivos da cera de carnaúba relatados por Dang e et al. (2008) foram: o retardo do amadurecimento e da perda de massa dos frutos de manga revestidos, redução da taxa de respiração, do pico climatérico, exibição de melhor coloração, altas concentrações de monoterpenos, sesquiterpenos, aldeídos e norisoprenoides e aumento do total de aromas voláteis. Revestimentos com quitosana também conservaram a cor, firmeza, aumentaram o tempo de prateleira e reduziram a carga microbiana em frutos de mamão (González-Aguilar et al. 2009).
A conservação dos valores de acidez, em relação ao controle, podem inferir que os processos de maturação dos frutos revestidos com cera de carnaúba e amido de milho foram reduzidos, enquanto os revestidos somente com os extratos reduziram a acidez, indicando que os frutos amadureceram ao longo do experimento (Tabela. 1). Esses dados estão de acordo com Santos et al. (2011) que observaram a influencia do amido de milho na redução da transpiração e perda de massa em frutos de manga Tommy Atkins.
A relaçao entre a doçura (SST) e sua acidez total (AT) é de grande importância, pois o sabor dos frutos é dado pela razão entre essas variáveis. Quando o fruto está verde há uma predominância da acidez, à medida que os mesmos vão amadurecendo há redução da acidez e intensificação dos açúcares. A dinâmica entre a intensificação dos sólidos solúveis e redução da acidez em frutos de manga cv Tommy Atkins foi acompanhado por Pinto et al. (2008), constatando que os sólidos solúveis passaram de 7,89 °Brix na colheita para 15,08 °Brix, 46 dias após a colheita, enquanto para a acidez ocorreu o inverso, passando de 0,84 para 0,23 mg de ácido cítrico por 100 mL.
Na avaliação do controle da Antracnose e outras doenças de pós-colheita os revestimentos com extratos de M. tenuiflora e extratos + cera de carnaúba foram eficientes, seja do patógeno inoculado, de patógenos latentes ou do ambiente, que surgiram durante o período de armazenamento e avaliação dos tratamentos. Os EB e C+EB, com exceção do EB4, não apresentaram diferença significativa entre si (Tab. 1). Esses dados revelam que os extratos apresentam atividade antifúngica com destaque para o tratamento EB5, C+EB2, C+EB4 e C+EB5 indicando também que há uma correlação positiva entre a cera de carnaúba e o extrato de M. tenuiflora.
A eficiência dos extratos vegetais na redução da Antracnose da banana foi observado por Celoto et al. (2011) ao avaliarem os extratos aquosos e metanólicos de Momordica charantia não observaram diferença significativa, quando os tratamentos foram aplicados 1 e 24 horas antes da inoculação, com o fungicida tiofanato metílico e o efeito sinérgico do revestimento de óleos essenciais, de canela e capim limão associados à goma arábica, reduziram em mais de 70% da incidência da Antracnose em frutos de banana e mamão, além de retardarem o amadurecimento (Maqbool et al. 2011).
Os revestimentos extratos + amido (A+EB) apresentaram as maiores médias de severidade, que se intensificaram pela presença de bactérias e leveduras, causadoras da podridão nos frutos, não havendo variação quanto a alteração da concentração dos extratos e do pH.
A infestação da doença nestes tratamentos pode explicar as maiores médias da acidez nos mesmos, ocasionados pelo processo de fermentação anaeróbia, ao invés de estar relacionada com a redução dos processos metabólicos que levam a um maior tempo de prateleira. Esses tratamentos apresentaram odor desagradável, próprio de processos de putrefação e aspecto não desejável para o consumo.
Nos estudos realizados por Santos et al. (2011) observou-se que frutos de manga cv Tommy Atkins revestidos com amido de milho nas concentrações de 4 e 6% também apresentam os sintomas em estagio de decomposição. A limitação de oxigênio na presença de carboidrato leva ao processo fermentativo, através da síntese de acetaldeído e etanol, resultando no desenvolvimento de odores e sabores desagradáveis.
Nos estudos realizados por Gonzalez-Aguilar et al. (2008) foi possível observar que os revestimentos utilizados sobre frutos de manga foram eficientes para manter a qualidade do produto e impedir a formação do etanol, já os não tratados produziram acetaldeído.
A atividade antifúngica de sachês contendo óleos essenciais de capim limão e orégano, inibiram o crescimento de Alternaria alternata, Colletotrichum gloeosporioides, Lasidiplodia theobromae e Xanthomonas campestresin vitro, mas não influenciaram nos processos de maturação dos frutos (Medeiros et al. 2011). Também observaram que houve redução dos sólidos solúveis e intensificação da acidez, sendo que no nono dia de armazenamento aproximadamente 40% dos frutos de todos os tratamentos apresentavam podridão.
Foram observadas podridões pedunculares causadas por Fusicoccum parvum e Lasiodiplodia theobromae provavelmente originados no campo e a presença de Aspergillus ninger e Penicillium spp. que provavelmente tenha origem no ambiente de armazenamento e podridão por bactérias e leveduras. Estudos realizados por Moura et al. (2012) revelaram que o C. gloeosporioides estava presente em todos os tratamentos sendo responsável por 75% de incidência da doença enquanto L. theobromae, Fusicoccum aesculi causadores das podridões pedunculares causaram 11 e 5,5% de incidência respectivamente, já o A. niger e Alternaria sp foram responsáveis por 2,7 e 1,3% respectivamente.
A presença de microrganismos no ambiente de armazenamento foram identificadas antes e após o armazenamento de diferentes cultivares de maçãs. Dentre os microrganismos dominantes no ambiente destacaram-se os fungos Penicillium spp., Alternaria sp., Botrytis sp., Aspergillus spp. e Macrocarpum Cladosporium; as bactérias Pseudomonas fluorescens e Bacillus cereus; e as leveduras Candida curvata e Candida famata, Pichia carsonii, Pichia etchellsii. Os microrganismos mais frequentemente encontrados na superfície da maçã pertencem aos géneros Penicillium spp., Alternaria sp., Aspergillus sp., Cladosporium sp., Candida sp. e Bacillus sp. (Juhnevica, Skudra, Skudra. 2011).
O desenvolvimento natural desses patógenos foram observados por Fischer et al. (2009) ao avaliarem o desenvolvimento da Antracnose e podridões pedunculares sobre 15 variedades de mangas, constatando a incidência de 100% da Antracnose um dia após o armazenamento em todas as variedades e em menor percentagem as podridões pedunculares. O desenvolvimento de doenças em manga está relacionado com a capacidade das variedades produzirem o resorcinol. Quanto maior a concentração de 5-n-heptadecenylresorcinol e 5-n-pentadecylresorcinol na casca dos frutos menor eram as lesões causadas pelo C. gloesosporioides (Hassan et al. 2007).
A atividade antifúngica de sachês contendo óleos essenciais de capim limão e orégano inibiram o crescimento de Alternaria alternata, Colletotrichum gloeosporioides, Lasidiplodia theobromae e Xanthomonas campestres in vitro, mas não influenciaram nos processos de maturação dos frutos (MEDEIROS et al., 2011). Esses autores também observaram que houve redução dos sólidos solúveis e intensificação da acidez, sendo que no nono dia de armazenamento aproximadamente 40% dos frutos de todos os tratamentos apresentavam podridão.
Comportamento similar ao observado por Medeiros et al. (2011), foram observados nos tratamentos revestidos com amido de milho que intensificaram a acidez atribuindo-se esse aumento aos processos de fermentação anaeróbia que causaram escurecimento dos frutos e apresentaram odores desagradáveis tornando-se impróprios para o consumo (Figura 1A), ao passo que o tratamento controle e os revestidos com extratos apresentaram comportamento similar aos descritos por Pinto et al. (2008) para os processos de amadurecimento e ainda apresentando-se próprio para o consumo (Figura 1B). Os tratamentos com cera de carnaúba, também apresentaram-se próprios para o consumo no final do experimento (Figura 1C), porém com ao processos de maturação reduzidos o que não impediu a redução da acidez.

Figura 1
Frutos de manga após 17 dias de experimento
(A) Fruto revestido com amido de milho, com estagio avançado de decomposição. (B) Fruto revestido com extratos brutos, apresentando aspecto de murcha pela perda de água, mas apropriado para o consumo. (C) Fruto revestido com cera de carnaúba, apresentando ótima aparência e apropriada para o consumo
Foram observadas podridões pedunculares causadas por Fusicoccum parvum (Figura 2A) e Lasiodiplodia theobromae (Figura 2B) provavelmente originados no campo e a presença de Aspergillus ninger e Penicillium spp. (Figura 2C) que provavelmente tenha origem no ambiente de armazenamento, e podridão por bactérias e leveduras. Nesse experimento foram considerados os sintomas causados por esses patógenos que fazem parte dos microrganismos de pós-colheita e que potencializam os danos causados pelo C. gloeosporioides (Figura 2D) artificialmente inoculado.
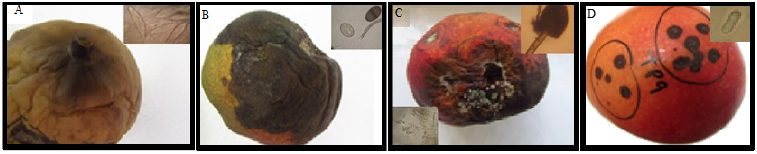
Figura 2
Sintomas de doenças de pós-colheita em frutos de manga
(A) Podridão peduncular causado por Fusicoccum parvum e seu agente etiológico. (B) Podridão peduncular causado por Lasiodiplodia theobromae e seu agente etiológico. (C) Sinais de Aspergillus ninger e Penicillium spp e suas estruturas. (D) Sintomas de antracnose e seu agente etiológico
No Experimento II os tratamentos apresentaram diferença significativa entre si, confirmando a eficiência dos extratos + cera de carnaúba (C+EB) através da redução da área abaixo da curva de progresso da doença (AACPD), incidência da doença e aumento do período de incubação (P.I) (Tabela. 2).
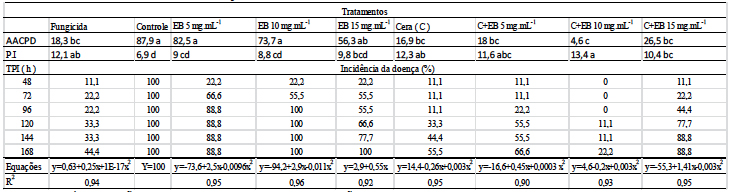
TPI (Tempo pós-inoculação). Medias seguidas pelas mesmas letras não diferem entre si pelo teste de Tukey a 5% de probabilidade, para as variáveis AACPD (CV = 69%) e P.I (CV = 18,9%). Para a incidência da doença as regressões foram significativos a 5% de probabilidade pelo Teste F.
O tratamento C+EB10 apresentou às menores medias de AACPD, porém não diferiu significativamente do fungicida PROCLORAZ (imidazolilcarboxamida) nem dos tratamentos com cera de carnaúba. Esse tratamento reduziu a AACPD em aproximadamente 95%, enquanto o tratamento com o fungicida reduziu 80% em relação ao controle, o que assegura o potencial do produto alternativo no controle da doença causada pelo Colletotrichum gloeosporioides no pós-colheita (Tab. 2).
O C. gloeosporioides tem uma ampla faixa de germinação e infecção, sendo sua faixa ótima estimada pelo modelo Beta molecular entre 20 e 25 °C. As temperaturas mínimas e máximas ajustadas por esse modelo foi de 9,5 e 44,1 °C, associados a períodos de molhamento. Nos processos de infecção e colonização a incidência aumentou ao elevar a temperatura até 30 °C ocasionando 100% de incidência 10 dias após a inoculação. Quando essa temperatura cai pela metade, a incidência da doença é reduzida para 50% no prazo de 14 dias após a inoculação (Soares et al. 2008).
Porém, baixas temperaturas não resolvem todos os problemas, já que patógenos como Botrytis cinerea se desenvolvem, ainda que lentamente a 0 ºC e algumas espécies vegetais são susceptíveis a danos pelo frio entre 8 e 10 °C (Senhor, 2009). Outra combinação que revelou efeito positivo no controle da Antracnose em frutos banana foi à mistura de óleo de soja e os fungicidas picoxistrobina + ciproconazol e óleo de soja mais trifloxistrobina + tebuconazol.
Esses fungicidas associados ao óleo foram capazes de reduzir significativamente a AACPD da doença em até 78,8%, quando comparado com os fungicidas aplicados sem o óleo que reduziram no máximo 30,4%, sendo que o fungicida picoxistrobina + ciproconazol apresentou médias estatisticamente iguais à testemunha (Fernandes & Bonaldo, 2011). Óleos essenciais de Copaíba, Andiroba, Babaçu, coco, Neem, Eucalipto, Semente de Uva, Amendoa, Hortelã, Pau Rosa, foram eficientes na redução da Antracnose em pimenta (Souza et al. 2012). Fungicida do grupo dos imidazole, também utilizado nesse experimento, mostrou eficiência no controle da Antracnose em frutos de manga cv UBA, o qual apresentou as menores médias em relação aos produtos alternativos (Lemos et al. 2013).
A incidência da antracnose nos frutos de manga foi em torno de 74% aos sete dias após a inoculação. O tratamento controle apresentou 100% de incidência na primeira avaliação, 48 horas após a inoculação (Tabela 2), enquanto o tratamento C+EB10 atrasou o surgimento da doença em 48 horas, a partir da primeira avaliação e reduziu a incidência da Antracnose em aproximadamente 78% sete dias após a inoculação. Os demais tratamentos apresentaram incidência da antracnose entre 10%, nos frutos tratados com fungicida e revestidos com cera de carnaúba, e 20% nos revestidos com os extratos, na primeira avaliação.
O aumento significativo da incidência e severidade da Antracnose em frutos de goiaba, com o avanço do estádio de maturação, reduz o período comercialização (Fischer et al. 2012). O período de incubação foi significativamente menor nos frutos do tratamento controle, não diferindo dos revestimentos com os extratos em suas respectivas concentrações, ao passo que o período de incubação do C+EB10 apresentaram significativamente as maiores médias do período de incubação. Podendo este dado ser associado à baixa incidência e severidade da doença (Tabela. 2).
Extratos brutos de M. tenuiflora têm apresentado atividade antimicrobiana, inibindo o crescimento micelial, esporulação e germinação de Alternaria cucumerina (Borges et al. 2013), anti-inflamatória, antioxidante, inibidora de acetilcolinesterase (Cruz, 2013) e mostrou eficiência no tratamento de úlceras (Rivera-Arce et al. 2007). Apesar do seu efeito tóxico frente a diversos microrganismos, os extratos não induziram a hemólise em eritrócitos, mutações nem dano cromossomal, segundo estudos realizados por Silva et al. (2013).
A atividade dos extratos de jurema preta pode ser explicada pela atividade de uma gama de compostos bioativos existentes em todas as partes da planta, dos quais muitos já foram identificados como flavonona, flavonoides, flavonóis, taninos, terpenos e outros que fazem parte dos compostos fenólicos (Cruz, 2013), capazes de inibir a germinação de fitopatógenos, segundo Salas et al. (2011) e formar complexo com as proteínas das paredes dos fungos e rompê-las, conforme descrição realizada por Arif et al. (2011).
CONCLUSÕES
Os extratos de Mimosa tenuiflora asociados com cera de carnaúba tem potencial na conservação das características físicas e químicas dos frutos prolongando o tempo de prateleira e reduzindo a antracnose. O uso do amido de milho como revestimento não controlou a antracnose e ainda potencializou os processos de decomposição dos frutos, sendo improprio para essa finalidade.
Referências
AOAC - Official of analysis of the Association of Official Analytical Chemists. 1995. Official Methods of Analysis. 17ª ed. Washington, 1115p.
Abubakar, A., Suberu, H.A., Bello, I.M., Abdulkadir, R., Daudu, O.A. & Lateef, A.A. 2013. Effect of pH on mycelial growth and sporulation of Aspergillus parasiticus. Journal of Plant Sciences.1:64-67.
Arif, T., Mandal, T.K. & Dabur, R. 2011. Natural products: Anti – fungal agents derived from plants, Research Signpost. 81:283 – 311.
Borges, I.V., Peixoto, A.R., Cavalcanti, L.S., Lima, M.A.G. & Silva, M.S. 2013. Extratos de jurema preta no controle de mancha-de-alternaria em melancia. Revista Caatinga. 26:36 - 45.
Celoto, M.I.B., Papa, M.F.S., Sacramento, L.V.S. & Celoto, F.J. 2011. Atividade antifúngica de extratos de Momordica charantia L. sobre Colletotrichum musae. Rev. Bras. Pl. Med. 13:337-341.
Cruz, M.P. 2013. Isolamento e identificação de compostos bioativos de mimosa hostilis Benth. 205f . (Tese de doutorado)- Universidade Federal da Bahia, Salvador, 2013.
Dantas, A.F.M., Riet-Correa, F., Medeiros, R.M.T., Galiza, G.J.N. De, Pimentel, L. Da A., Anjos, B.L. Dos, & Mota, R.A. 2010. Malformações congênitas em ruminantes no semiárido Nordeste Brasileiro. Pesq. Vet. Bras. 30:807-815.
Dang, K.T.H., Singh, Z. & Swinny, E.E. 2008. Edible coatings influence fruit ripening, quality,and aroma blosynthesis in mongo fruit. J. Agric food chem. 56:1361-1370.
Fernandes, S.O. & Bonaldo, S.M. 2011. Controle de antracnose (Colletotrichum musae) e conservação em pós-colheita de banana ‘nanica’ no norte de Mato Grosso. enciclopédia biosfera, Centro Científico Conhecer. 7:237-247.
Fischer, I.H., Arruda, M.C. De, Almeida, A.M. De, Galli, J.A., Bertani, R.M. De A. & Jerônimo, E.M. 2009. Doenças pós-colheita em variedades de manga cultivadas em pindorama. Rev. Bras. Frutic. 31:352-359.
Fischer, I.H., Silva, B.L. Da, Soares, A.R., Arruda, M.C. De, Parisi, M.C.M. & Amorim, L. 2012. Efeito de fungicidas e produtos alternativos no controle da antracnose e da pinta preta da goiaba. Semina, Ciências Agrárias. 33:2753-2766.
Juhnevica, K., Skudra, G. & Skudra, L. 2011. Evaluation of microbiological contamination of apple fruit stored in a modified atmosphere. Environmental and Experimental Biology. 9:53–59.
González-Aguilar, G.A., Celis, J., Sotelo-Mundo, R.R., Rosa, L.A. De La, Rodrigo-Garcia, J. & Alvarez-Parrilla, E. (2008). Physiological and biochemical changes of different fresh-cut mango cultivars stored at 5 C. International Journal of Food Science and Technology. 43:91–101.
González-Aguilar, G.A., Valenzuela-Soto, E., Lizardi-Mendoza, J., Goycoolea, F., Martínez-Téllez, M.A., Villegas-Ochoa, M.A., Monroy-García, I.N. & Ayala-Zavala, J.F. 2009. Effect of chitosan coating in preventing deterioration and preserving the quality of fresh-cut papaya ‘Maradol’. J Sci Food Agric. 89:15–23.
Lemos, L.M.C., Coutinho, P.H., Salomão, L.C.C., Siqueira, D.L. De, & Cecon, P.R. 2013. Controle da antracnose na pós-colheita de manga ‘UBÁ’ com o uso de produtos alternativos. Rev. Bras. Frutic.35:962-970.
Maqbool, M., Ali, A., Alderson, P.G., Mohamed, M.T.M., Siddiqui, Y. & Zahid, N. 2011. Postharvest application of gum Arabic an essential oils for controlling anthracnose and quality of banana and papaya during cold storage. Postharvest Biology and Technology. 62:71-76.
Medeiros, E.A.A., Soares, N. De F.F., Polito, T. De O. S., Sousa, M.M. De, & Silva, D.F.P. 2011. Sachês antimicrobianos em pós- colheita de manga. Rev. Bras. Frutic. volume especial:363-370.
Moura, M.D.C.S., Peixoto, A.R., Souza, E.M., Martins, R. Dos S. & Cavalcanti, L.S. 2012. Potencial de produtos bióticos e abióticos como indutores de resistência no controle de podridões pós-colheita em manga, no Submédio São Francisco. Revista Caatinga. 25:44-49.
Pinto, P.A. Da C., Choudhury, M.M., Lins, J.A. De, Homma, S., Pinto, A.A.C., Silva, C.P Da, & Oliveira, R.S. 2008. Qualidade pós- colheita de frutos de mangueira (Mangifera indica L) var. 'Tommy Atkins' sob sistema orgânico no submédio São Francisco (Brasil). IBADER: Instituto de Biodiversidade Agraria e Desenvolvemento Rural Recursos Rurais. 1:5-12.
Rivera-Arce, E., Chávez-Soto, M.A., Herrera-Arellano, A., Arzate, S., Agüero, J., Feria-Romero, I.A., Cruz-Guzmán, A. & Lozoya, X. 2007. Therapeutic effectiveness of a Mimosa tenuiflora córtex extract in venous leg ulceration treatment. Journal of ethnopharmacology. 109:521-528.
Salas, P.M., Céliz, G., Geronazzo, H., Daz, M. & Resnik, S.L. 2011. Antifungal activity and enzymatically – modified flavonoids isolated from citrus species. Food Chemistry. 124:1411-1415.
Santos, A.E.O. Dos, Assis, J.S. De, Berbet, P.A., Santos, O.O. Dos, Batista, P.F. & Gravina, G. de A. 2011. Influência de biofilmes de fécula de mandioca e amido de milho na qualidade pós-colheita de mangas ‘Tommy Atkins’. Rev. Bras. Ciênc. Agrár. 6:508-513.
Shaner, G. & Finey, R.F. 1977. The effects of nitrogen fertilization on the expression of slow-mildewing resistance in Knox wheat. Phytopathology, [Minnesota]: The American Phytopathological Society. 67:1051-1056.
Silva, V.A., Gonçalves, G.F., Pereira, M.S.V., Gomes, I.F., Freitas, A.F.R., Diniz, M.F.F.M. & Pessôa, H.L.F. 2013. Assessment of mutagenic, antimutagenic and genotoxicity effects of Mimosa Tenuiflora. Rev. Bras. Farmacogn. Braz. J. Pharmacogn. 23:329
Souza, M.L. De, Morgado, C.M.A., Marques, K.M., Mattiuz, C.F.M. & Mattiuz, B. 2011. Pós-colheita de mangas ‘tommy atkins’ recobertas com quitosana. Rev. Bras. Frutic. Especial:37-343.
Sousa, R.M.S., Serra, I.M.R.S. & Melo, T.A. 2012. Efeito de óleos essenciais como alternativa no controle de Colletotrichum gloeosporioides, em pimenta. Summa Phytopathol. 38:42-47.
Hassan, M.K., Dann, E.K., Irving, D.E. & Coates, L.M. 2007. Concentrations of constitutive alk(en)ylresorcinols in peel of commercial mango varieties and resistance to postharvest anthracnose. Physiological and Molecular Plant Pathology. 71:158-165.
Senhor, R.F., Souza, P.A. De., Neto, R.C.A. & Maracujá, P.B. 2009. Manejo de doenças pós-colheita. Revista Verde. 4: 00 – 13.
Soares, A.R., Lourenço, S.A. & Amorim, L. 2008. Infecção de goiabas por Colletotrichum gloeosporioides e Colletotrichum acutatum sob diferentes temperaturas e períodos de molhamento. Tropical plant patology. 33:265-272.
Souza, R.S.O. De., Albuquerque, U.P. De., Monteiro, J.M. & Amorim, E.L.C. de. 2008. Jurema-Preta (Mimosa tenuiflora [Willd.] Poir.): a Review of its Traditional Use, Phytochemistry and Pharmacology. Brazilian Archives of Biology and Technology. 51:937-947.
Autor notes
Autor para correspondência: E-mail: acacio.figueiredo@univasf.edu.br