Reportes frutas
Potencial antifungico de nanoparticulas de quitosano y extracto de Arándano sobre Colletotrichum fragariae en fresa
Antifungal potential of chitosan nanoparticles and cranberry extract against Colletotrichum fragariae in strawberry
Potencial antifungico de nanoparticulas de quitosano y extracto de Arándano sobre Colletotrichum fragariae en fresa
Revista Iberoamericana de Tecnología Postcosecha, vol. 19, núm. 1, 2018
Asociación Iberoamericana de Tecnología Postcosecha, S.C.
Recepción: 05 Febrero 2018
Aprobación: 16 Abril 2018
Publicación: 30 Junio 2018
Resumen:
El quitosano tiene importancia en agricultura debido a sus propiedades antimicrobianas, a su abundancia en la naturaleza y su no toxicidad. El objetivo de este trabajo fue evaluar la capacidad antifungica de nanoparticulas de quitosano y nanoparticulas de quitosano con extracto de arandano in vitro contra Colletotrichum fragariae e in situ en fresas almacenadas a temperatura de 5 °C y a temperatura ambiente. El ensayo in vitro se realizo por el método de dilución en agar, se determino el crecimieno micelial y se uso un diseño estadistico completamente al azar. El efecto de las nanopartículas sobre frutos de fresa almacenadas se evaluo sobre variables fisiologicas (respiración, perdida de peso, fenoles) y de calidad (color, firmeza, acidez y SST) bajo un diseño completamente al azar con arreglo factorial. Para la infección (incidencia y severidad ) se aplico un diseño estadistico completamente al azar. In vitro ambas nanoparticulas llegaron aproximadamente hasta el 100% de inibicion del crecimiento miceliar. En ambas temperaturas las nanoparticulas no influyeron sobre la mayoria de las variables, pero subieron la respiración en el caso de la temperatura de 5°C, adelantó la maduración y el desarollo de la infección. A temperatura ambiente las nanoparticulas bajaron la infección. La temperatura de almacenamiento por lo tanto puede influir sobre el efecto de las nanoparticulas. Palabras claves adicionales: fungico, nanopartículas, Colletotrichum fragariae, extractos botanicos Antifungal potential of chitosan nanoparticles and cranberry extract against Colletotrichum fragariae in Strawberry.
Palabras clave: fungico, nanopartículas, Colletotrichum fragariae, extractos botánicos.
Abstract: Chitosan is important in agriculture because its antimicrobial properties, its abundance in nature, and its non-toxicity. Antifungal capacity of chitosan nanoparticles and chitosan nanoparticles with cranberry extract against Colletotrichum fragariae were evaluated in vitro and in situ on strawberries stored at 5°C and at room temperature. The in vitro assay was performed by the agar dilution method, mycelial growth was determined and a completely randomized statistical design was used. The physiological (breathing, weight loss, phenols), quality (color, firmness, acidity and SST) were evaluated under a completely randomized design with factorial arrangement and for infection (incidence and severity) was applied a statistical design completely random. In vitro both nanoparticles reached approximately 100% of grow mycelial inhibition. In strawberries at both temperatures the nanoparticles not influenced on most parameters, but increased respiration at temperature of 5 °C, advanced maturation and development of the infection . While in treated strawberries at room temperature the infection was lower than control. The storage temperature can therefore influence on the effect of the nanoparticles.
Keywords: Postharvest, fungal development, nanoparticles, Colletotrichum fragariae, botanic extracts.
INTRODUCCIÓN
La fresa (Fragaria x ananassa Duchesne) es un fruto perecedero que se caracteriza por sus altas tasas de respiración y elevada actividad metabólica, condiciones que limitan su vida de anaquel y propician el desarrollo de hongos fitopatógenos. La Antracnosis, causada por Colletotrichum acutatum, Colletotrichum fragariae y Colletotrichum gloeosporioides, es una de las mayores enfermedades fúngicas de la fresa que causa graves pérdidas en pre y postcosecha (Howard et al., 1992 y Xie et al., 2010). La estrategia convencional para el control de antracnosis en la etapa precosecha y postcosecha de diversos productos hortofrutícolas se basa sobre el uso de fungicidas de síntesis (Siddiqui y Ali, 2014) los cuales causan resistencia en los hongos (Romanazzi y Feliziani, 2016). Otras estrategias de control incluyen el uso de compuestos naturales amigables con el medio ambiente y de baja toxicidad.
En este sentido, el uso de sustancias naturales como el quitosano (polímero de la glucosamina y N-acetilo glucosamina), extractos vegetales y aceites esenciales, representan una alternativa importante para el control de hongos fitopatogenos (Bautista-Baños et al., 2003; Romanazzi, 2010; Romanazzi et al., 2013). El quitosano es una de las alternativas más viables para la formulación de cubiertas o nanopartículas, debido a su biocompatibilidad, actividad biológica y biodegradabilidad. Se ha reportado que las aplicaciones de quitosano en etapa precosecha de la fresa, disminuyen las perdidas en postcosecha (Feliziani et al., 2015). Su efecto se debe a que el quitosano es una macromolécula policatiónica derivada de los grupos amino por lo que puede reaccionar con proteínas, lípidos y material genético; el grado de reacción depende de su estructura cristalina, grado de acetilación y peso molecular (Lizardi-Mendosa et al., 2016). Además, la biodegradabilidad y la no toxicidad del quitosano (Carlson, 2008; Salzar-Leyva et al., 2014) permite su uso en el control de enfermedades postcosecha de varias frutas y hortalizas. El quitosano puede aplicarse de manera aislada o en combinación con aceites esenciales y extractos vegetales, cuya composición incluye sustancias activas, como terpenoides, esteres, aldehídos y compuestos fenolicos, que tienen propiedades antibacteriales y antifungicas (Sotelo-Boyás et al., 2015). Ermis et al., (2015) demostraron la actividad antifungica de extractos de arandano sobre hongos xerófilos y no xerófilos. Morán Mejía (2016) reporto la inhibición del crecimiento micelial (83 %) de Alternaria alternata con nanopartículas de quitosano combinadas con extracto etanólico de arándano.
El quitosano es una alternativa para la formulación de nanoparticulas de manera aislada o en combinación con extractos o aceites vegetales. Las nanopartículas, debido a su tamaño tienen una elevada superficie de contacto, que les permite ser altamente reactivas y les confiere elevada capacidad antifúngica y antibacteriana (Sotelo-Boyás et al., 2015). Se ha demostrado in vitro que las nanoparticulas de quitosano disminuyeron el crecimiento micelial de Rhizopus sp. Colletotrichum capsici, Colletotrichum gloeosporioides y Aspergillus niger (Chookhongkha et al., 2013). No hay reportes sobre el efecto de nanopartículas de quitosano con o sin extractos de arándano sobre Colletotrichum fragariae. El objetivo de este trabajo fué evaluar in vitro e in situ la eficiencia de nanoparticulas de quitosano (NPQ) y nanoparticulas de quitosano con extracto etanolico de arandano (NPQEEA), para el control del hongo Colletotrichum fragariae en fresa.
MATERIALES Y METODOS
Aislamiento y activación hongo
Colletotrichum fragariae se aisló de fresas enfermas con antracnosis, la cual se caracterizó, en frutos maduros por la presencia de lesiones hundidas, de forma circular o irregular, inicialmente acuosas y posteriormente secas, de color marrón oscuro a negro. El aislamiento del patógeno asociado a los frutos con antracnosis, se caracterizó por la formación de colonias de color pálido-salmón-anaranjado a gris-oliváceo o gris-oscuro. De acuerdo con Smith y Black (1990), y Gunnel y Gubler (1992) el color de las colonias de C. fragariae y C. gloeosporioides en PDA es parecido (blanco a gris, gris olivo hasta gris oscuro). In vitro el hongo produjo conidios en conidióforos dispersos, esporodoquios y setas fértiles. Los de conidióforos fueron variables en forma y tamaño; los de esporodoquios fueron uniformes en tamaño (17.2×4.4µm). El hongo aislado se mantuvo en Papa Dextrosa Agar (PDA) durante nueve días a 28 °C. Para mantener la patogenicidad del hongo se realizarón periódicas inoculaciones y reaislamientos a partir de fresas infectadas.
Extracto de arándano
Se obtuvo por el método de maceración descrito por Garduño Pizaña et al., 2010, que consistió en triturar 100 g de frutos de arándano y posteriormente colocarlos en 500 mL de etanol (Mena, Mexico) durante 24 horas a temperatura ambiente. La solución obtenida se filtró con papel Whatman No. 10 y se concentró en rotavapor a una temperatura de 65ºC (BUCHI R-220) el concentrado, se colocó en frascos color ámbar y se almaceno a 40ºC.
Elaboración de nanoparticulas y caracterización
Las NPQ se obtuvieron con el método de nanoprecipitación (Luque-Alcaraz et al., 2012) 0.05 % w/v de quitosano (comercial, peso molecular de 89305 g∙mol-1; viscosidad 440 mL/g y acetilación de 10.7±0.2 %), se disolvió en una solución acuosa de ácido acético (Fermont, México) al 1 % v/v y el pH se ajustó a 5.6 con NaOH 1N. Para obtener la fase solvente; 18.75 mL de la solución de quitosano se añadió con bomba peristáltica (Masterflex modelo 77120-62) a 300 mL de fase no solvente y se mantuvo la mezcla en agitación. Como fase no solvente se utilizó etanol puro para las NPQ y 5 g extracto etanólico de arándano∙en 100mL-1 etanol para las NPQEEA. Las soluciones de NPQ y NPQEEA se concentraron en rotavapor a 40°C y 30 rpm y se guardaron en refrigeración. La solución de nanopartículas se coloco en microceldas de carbono y se dejaron secar a temperatura ambiente durante 24 hrs. El tamaño y morfología de las nanoparticulas fue observada por Microscopía Electrónica de Transmisión (TEM) en un microscopio JEM-2100 Mca Jeol con un voltaje de aceleración de 200 kV el cual proporciona una buena iluminación en altas amplificaciones para la obtención de imágenes de alta resolución de .27 nm.
Actividad antifúngica in vitro de las nanoparticulas de quitosano
Se utilizó el método propuesto por Garduño Pizaña et al., 2010, que consistió en mezclar medio de cultivo de PDA con las NPQ y NPQEEA a las concentraciones de 25, 50 y 75 µL/mL. La mezcla obtenida se vació en cajas Petri (60 x 15 mm), se colocó en el centro de cada caja un disco de agar de 3 mm que contenia el patógeno y se incubo a una temperatura de 28±2 °C. Se consideraron seis repeticiones por cada concentración de las NPQ y NPQEEA. El testigo consistió de cajas Petri conteniendo únicamente PDA. El crecimiento micelial (diámetro de la colonia) se midió con un vernier todos los días y se registró para cada tratamiento hasta que la placa testigo fue completamente colonizada con el micelio. Posteriormente, para evaluar la actividad fungicida o fungistática de los tratamientos evaluados, se resembraron discos de agar conteniendo el hongo proveniente de cada tratamiento en medio PDA.
Pruebas in situ en fresa
Se utilizó fresa procedente de dos sitios de producción. El primer lote de fresas de invernadero cv. se adquirio del municipio de Tepoztlan en el estado de Morelos, México. El segundo lote de fresas de campo cv. “Camino Real”, se compró en Villa Guerrero en el estado de México. Las fresas se seleccionaron considerando el color en su superficie (3/4 de color rojo). Las fresas fueron transportadas al laboratorio de Tecnología Postcosecha del CEPROBI-IPN y se seleccionaron de acuerdo a su tamaño y la ausencia de daños visibles.
Las fresas seleccionadas se lavaron por tres minutos en una solución de hipoclorito de sodio a 200 ppm y posteriormente se sumergieron por tres minutos en agua destilada. Se formaron 4 lotes para llevar a cabo la aplicación de los siguientes tratamientos por aspersión: 1) solución de NPQ [75µL/mL], 2) solución de NPQEA [75µL/mL], 3) quitosano 1,5% (Q) y 4) sin aplicación de tratamiento (grupo control). Posterior a la aplicación de tratamientos se asperjo una solución de esporas de Colletotrichum fragariae (1x105 esporas∙mL-1) y se dejo secar el fruto. Las fresas fueron envasadas en contenedores de ptereftalato de polietileno (PET, grosor 330 µm) y se almacenaron a dos diferentes temperaturas (5 y 20 °C). Después de 15 días de almacenamiento en refrigeración las fresas se mantuvieron a temperatura ambiente. Cada unidad experimental contenía 90 g de producto, con tres repeticiones por tratamiento. Las evaluaciones se realizaron los días 0, 3, 6, 9 y 12 de muestreo.
Variables fisiológicas/bioquímicas
Pérdida de peso. Se evaluó por diferencia entre el peso de las fresas en el día cero y de cada uno de los días de evaluación. Los resultados se expresaron en porcentaje. Se utilizó una balanza (modelo CS 200, Ohaus Corporation, USA) con capacidad de 200g x 0.1g
Intensidad Respiratoria. Se cuantificó con la metodología propuesta por Ishikawa et al., (1997). 90 g de fresa se envasaron en vasos de vidrio sellados herméticamente con una tapa equipada con un septum de caucho de silicona. Después de 1 h a 25 ± 2°C, se recuperó el gas contenido en el espacio de cabeza de los viales. 1 mL del gas recuperado se inyectó en un cromatógrafo de gases 7890B GC (Agilent Technologies, U.S.A). El helio se utilizó como gas acarreador a una velocidad de flujo de 10 mL min-1. Se utilizaron dos detectores (FID/TCD) y dos columnas HP-PLOT/Q y CP-MOLSIEVE 5A (Agilent Technologies, U.S.A). Las temperaturas del inyector y detectores FID y TCD fueron de 220, 300 y 250°C, respectivamente. La intensidad respiratoria se expresó en mL CO2 Kg-1 h-1.
Fenoles totales. Se uso la metodología de Singleton y Rossi (1965). 1 g de fresa se maceró con 5 mL de metanol (Fermont, México) al 80%. La mezcla se centrifugó a 8000 rpm por 10 minutos y se recuperó el sobrenadante. La mezcla de reacción contenía 3980 µL de H2O destilada, 750 µL de Na2CO3 (Fermont, México) al 20%, 250 µL de reactivo Folin-Cicalteau (Hycel, México) y 20 µL de sobrenadante. Las mezclas se incubaron durante dos horas en oscuridad y posteriormente se midió la absorbancia a 760 nm en un espectrofotómetro G10S (Thermo scientific China). Los fenoles se expresaron como mg de acido galico/g de peso fresco y se utilizó una curva de calibración de ácido gálico para su cuantificación.
Color. Se determinó con un colorimetro Baking Meter BC-10 (Konica Minolta Sensing, Japón), evaluando el color en dos puntos equidistantes del fruto. Se obtuvieron valores de L, a y b, a partir de los cuales se calculó el ángulo de tono (Hue) y el indice de saturación (chroma) para evaluar la variación de color (McGuire, 1992).
Firmeza. Se midió con un penetrómetro digital 53205 Fruit Pressure Tester (Technical System Italy) equipado con una punta cilíndrica de 8 mm. La firmeza se expresó en Newtons (N).
Sólidos solubles totales (SST). Se determinaron con un refractómetro de mano (0-32%) N-1E (ATAGO 01018 Japón) y se expresaron como °Brix, calibrado con una gota de agua destilada. Se obtuvo el jugo de las muestras de fresa y se colocó una gota en el refractómetro para determinar ºBrix.
Acidez titulable (AT). Se realizó de acuerdo con la metodología de la AOAC (1984). 20 g de muestra se pesaron y se licuaron en 100 mL de agua destilada. Se tomó una alicuota de 5 mL de la mezcla y se tituló con NaOH al 0.1 N, utilizando como indicador 2 gotas de fenolftaleina en solución alcohólica al 1%. El porcentaje de acidez se calculó en relacion al ácido cítrico (meq=0.064).
Porcentaje de infección y severidad. El porcentaje de infección se determinó mediante la siguiente fórmula:
% de infección = Número de frutos infectados x 100/Número de frutos tratados.
Para severidad se usó una escala subjetiva de 5 niveles . Donde 0, representa a los frutos sanos; 1) del 1-25% de superficie infectada; 2) del 26-50% de superficie infectada, 3) del 46-75% de superficie infectada, 4) del 76-100% de superficie infectada con micelio.
Análisis estadistico de los datos
Los datos de las pruebas in vitro, de incidencia y severidad se analizaron como un diseño completamente al azar y se realizo un análisis de varianza con una comparación de medias de Tukey. Los datos del ensayo in situ se analizaron como un diseño completamente al azar con arreglo factorial y la comparación de medias se realizó utilizando la prueba de Tukey (P≤0.05) utilizando el software Info Stat 2012.
RESULTADOS Y DISCUSIÓN
Prueba in vitro de las nanoparticulas
La observación al TEM mostró un tamaño medio de 3 nm para las NPQ y de 26 nm para las NPQEEA (fig. 1A y 1B). El tamaño nanométrico de las partículas les confiere una mayor área de superficie de contacto que les permite adherirse firmemente sobre la superficie de los hongos destruyendo la integridad de la membrana (Hernández-Téllez et al., 2016). Ademas Ma y Lim (2003) observaron que el pequeño tamaño de las nanoparticulas les permite difundirse en el interior de las células, a diferencia del quitosano puro. Esto puede implicar anomaliás a nivel de ADN y ARN que provocan la muerte celular de los microorganismos. Las NPQ y las NPQEEA presentaron la mejor inibición sobre Colletorichum fragariae a la concentracion de 75 µL/mL, esta concentración se uso en los experimentos in situ.
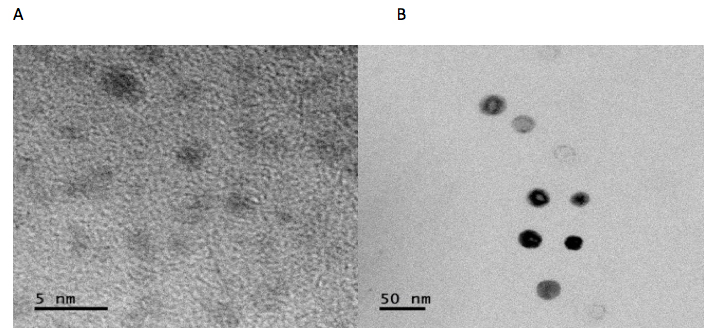
Figura 1
Imagen TEM de: (A) nanopartículas de quitosano (NPQ) 3 nm y (B) nanopartículas de quitosano más extracto etanólico de arándano (NPQEEA) 26 nm.
Fuente: elaboración propia.
Las NPQ y NPQEA (Figura 2A y 2B) tuvieron un efecto inhibitorio significativo (P ≤ 0,05) sobre el crecimiento micelial de Colletotrichum fragariae, los tratamientos con NPQ inhibieron el hongo con respecto al testigo en un 22% (25 µL/mL), 64% (50 µL/mL) y 99% (75 µL/mL) y presentaron la menor tasa de crecimiento. Mientras las NPQEA inibieron en un 43% a una concentración de 50 µL/mL y a la concentración de 75 µL/mL llegaron hasta el 100% de inibición y presentó un efecto fungicida. Otros estudios confirman la bondad del quitosano aplicado a la nanotecnologia para controlar el genero Colletotrichum: Chookhongkha et al., (2013) observaron in vitro que las nanoparticulas de quitosano en PDA 0.6 % w/v retrasaron el desarollo de este hongo; Zahid et al., (2013) reportan un estudio in vitro con la nanoemulsion de quitosano de bajo peso molecular a la concentracion 1%, bajó la germinación de conidios, el desarrollo de micelio y la esporulación, en comparación con el testigo, mostrando ser una buena técnica biofungicida contra Colletotrichum gleosporioides; en un estudio sobre antracnosis en mango Chowdappa et al., (2014) reportaron que las nanopartículas de quitosano y plata a la concentración 0.5 y 1% redujeron del 47,5 a 71,3% respectivamente el desarrollo del hongo.
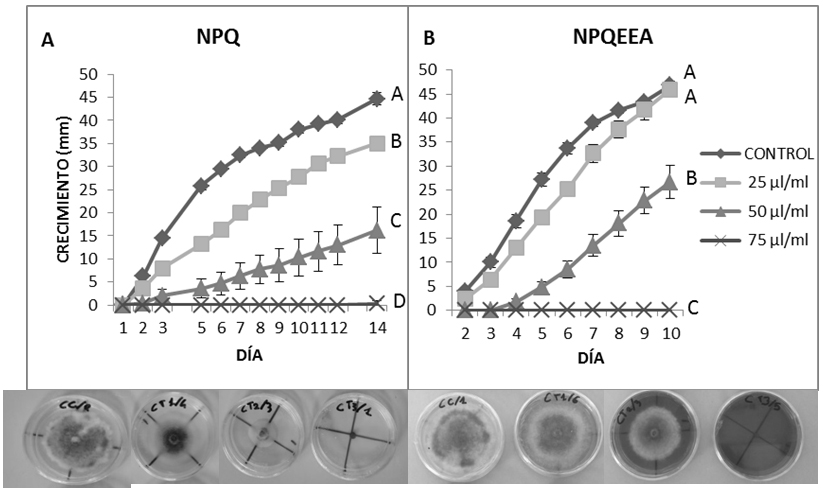
Figura 2
Cinética de crecimiento de Colletotrichum fragariae en NPQ (A) y en NPQEEA (B); letras distintas indican diferencias significativas (P ≤ 0,05) de los valores integrativos de la curva de crecimiento entre los tratamientos. En C están las cajas tratadas con NPQ y en D las tratadas con NQEEA respectivamente: control y concentraciones de 25, 50 y 75 µl/ml.
Fuente: elaboración propia.
Pruebas in situ
Pérdida de peso. No se observaron diferencias significativas entre los tratamientos (p ≤ 0,05) (figura 3A). Resultados similares publicaron Perdones et al., (2012) quienes no detectaron un efecto significativo sobre la reducción en la pérdida de peso de fresas almacenadas en refrigeración, utilizando cubiertas de quitosano o en combinación con aceite esencial de limón; no se detectaron diferencias en la resistencia al vapor de agua entre las cubiertas y el control. Las cubiertas no mejoran la resistencia al vapor de agua debido a la alta permeabilidad del quitosano, a la alta humedad relativa (90%) y cuando las películas son plastificadas la propiedad de barrera se reduce (Vargas et al., 2011). En desacuerdo con este trabajo Han et al., 2004 reportaron una disminución de aproximadamente 20% de la perdida de peso de fresas tratadas con una cubierta de quitosano al 2% comparadas con el control bajo refrigeración. Existen evidencias de la aplicación de cubiertas de quitosano para reducir la pérdida de agua de los frutos (Han et al., 2004; Vargas et al., 2006; Hernández-Muñoz et al., 2006; Hernández-Muñoz et al., 2008; Perdones et al., 2012).
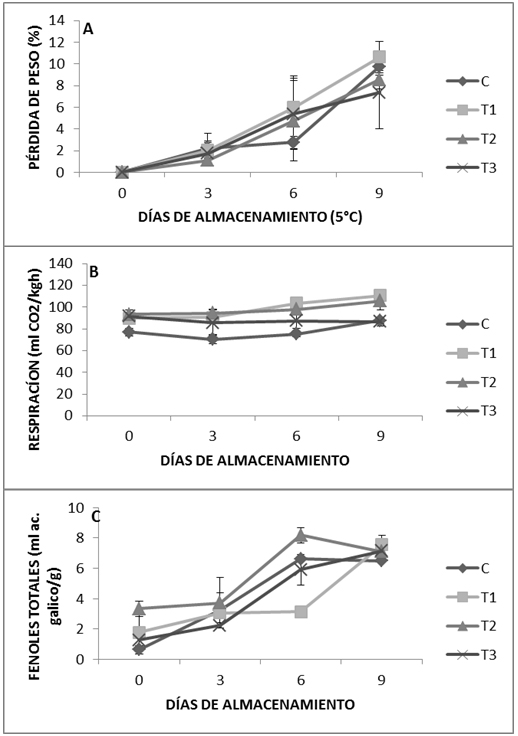
Figura 3
Representación gráfica de perdida de peso (A), respiración (B) y fenoles totales (C) en fresas tratadas con NPQ (T1), con NPQEEA (T2) y con Q 1,5% (T3) almacenadas durante nueve días a 5ºC.
Las barras verticales indican las desviación estándar.
Fuente: elaboración propia.Intensidad respiratoria. Se encontraron diferencias significativas (P≤0.05) entre los diferentes tratamientos y el grupo control (Fig 3B) de las fresas almacenadas a 5ºC. Al día 0 las fresas tratadas con NPQ, NPQEEA y Q tuvieron aproximadamente el mismo nivel de respiración 91 mL CO2 Kg-1 h-1, las fresas del grupo control presentaron un valor 15% menor. Al día 9 las fresas tratadas con NPQ y NPQEEA mostraron los niveles más altos de respiración 110,50±3,79 mL CO2 Kg-1 h-1 y 105,65±8,62 mL CO2 Kg-1 h-1 respectivamente, las fresas control y tratadas con Q mostraron los niveles mas bajo 87,56 mL CO2 Kg-1 h-1 y 86,44 mL CO2 Kg-1 h-1 respectivamente.
Los resultados obtenidos coinciden con los reportados por Vargas et al., (2006) quienes indicaron que hubo una disminución de la tasa de respiración en las fresas tratadas con quitosano al 1% y quitosano al 1% en combinación con ácido oleico a concentraciones de 1, 2 y 4 % (v/v). Hernández-Muñoz et al., (2008) reportaron que después de la aplicación de cubiertas de quitosano el nivel de respiración fue más alto que el control pero en los días siguientes los tratamientos presentaron menores tasas de respiración que el control. El quitosano tiene la habilidad de formar una cubierta semipermeable que puede reducir la producción de O2, CO2 y etileno así como la transpiración retrasando la maduración de los productos (Bautista-Baños et al., 2005). El tamaño nanometrico de las nanoparticulas que confiere al quitosano elevada reactividad (Shukla et al., 2013), junto a la falta de la formación de una cubierta capaz de reducir la permeabilidad de gases y agua, puede haber determinado el aumento de respiración en las fresas tratadas con NPQ y NPQEEA.
Fenoles totales. El contenido fenolico mostró diferencias (P ≤ 0,05) entre los tratamientos y entre los días (Fig 3C). Las fresas tratadas con NPQ despues del dia 6 mostraron un rapido aumento de fenoles, mientras las tratadas con Q aumentarón costantemente. El tratamiento NPQEEA fue el que mostró los valores más altos de fenoles en el día cero fué 4 veces mayor y en el día seis fué un 24% mayor comparado con el control. Esto puede ser debido al elevado contenido fenólico del extracto de arándano, (Moran Mejía et al., 2017). Además el quitosano puede activar la sintesis de nuevos compuestos fenolicos (Bautista-Baños et al., 2005). Estos resultados no coinciden con los reportados por Wang y Gao (2013) quienes observaron que, cubiertas de quitosano a las concentraciones de 0,5, 1,0 y 1,5%, pueden retrasar el aumento de los fenoles en fresa almacenada a 5°C.
Parámetros de calidad
Color. La luminosidad y el valor de hue (figura 4A-C) de las muestras no mostró diferencias estadísticas significativas (P ≤ 0,05) durante los días de almacenamiento y entre los tratamientos con nanoparticulas y el control. Vargas et al. (2006) indicaron que no hubo diferencias en los parámetros de color de las fresas tratadas con quitosano al 1% almacenadas a 4±1 °C respecto al control; es decir, la cubierta no modificó los valores de L, hue y croma
Firmeza. La firmeza fue estadísticamente igual entre todos los tratamientos y los días de almacenamiento, lo cual pudo deberse a que el índice de madurez de las fresas fue uniforme (Fig 4D)
Acidez titulable y sólidos solubles totales. No se obtuvieron diferencias estadísticas significativas entre los tratamientos para estos dos parámetros (figura 4E-F) durante el almacenamiento. Estos resultados coinciden con los reportados por Vargas et al. (2006) quienes indicaron que en las fresas almacenadas a 4±1°C, no se encontraron diferencias en el contenido de SST y acidez durante el almacenamiento y entre los tratamientos.
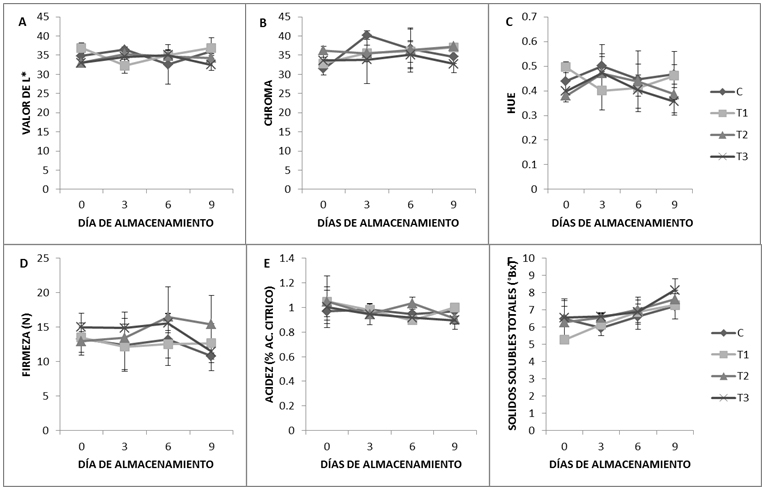
Figura 4
Representación gráfica de L (A), chroma (B), hue (C), firmeza (D), SST (E) y acidez (F) en fresas tratadas con NPQ (T1).
Fuente: elaboración propia.
Parámetros de infección
Además de Colletotrichum fragariae se desarrollaron otros hongos como Alternaria, Botrytis y Fusarium los cuales se consideraron para evaluar los parámetros de infección (incidencia, severidad). Como muestra la figura 5 la incidencia (A), y severidad (B) aumentaron significativamente (P ≤ 0,05) en todos los tratamientos, cuando las fresas se colocaron a temperatura ambiente. La infección al día 16 fue 74% mas alta en las fresas tratadas con NPQEEA, con respecto al control y también mostraron los máximos niveles de severidad. Las fresas tratadas con quitosano al final se comportaron como las fresas control, este resultado está en desacuerdo con los reportes de varios autores quienes tuvieron una significante reducción de la enfermedades de las fresas utilizando cubiertas de quitosano (Han et al., 2004; Vargas et al., 2006; Hernández-Muñoz et al., 2008). Como ya se demostró in vitro, las NPQ y NPQEEA tienen actividad antifúngica, sin embargo, in situ no se observó el mismo comportamiento.
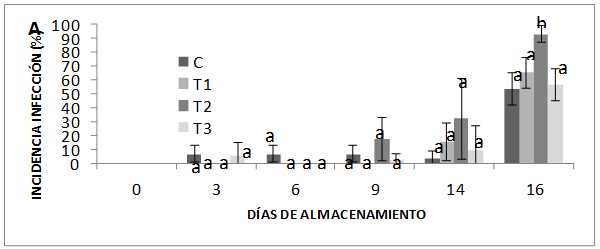
Figura 5
Representación gráfica de la infección (A) y severidad (B) de fresas tratadas con NPQ (T1), NPQEEA (T2) y Q 1,5% (T3), almacenadas durante diez y seis días a 5ºC.
Las barras verticales indican las desviación estándar. Letras diferentes muestran diferencias significativas (Tukey a una P ≤ 0,05) entre los tratamientos.
Fuente: elaboración propia.Prueba preventiva a temperatura ambiente
Parámetros fisiológicos y bioquímicos
Los tratamientos no influyeron sobre la pérdida de peso. Estos resultados previamente han sido reportados por otros autores por ejemplo Hernández-Muñoz et al. (2006) en un experimento con fresas tratadas con quitosano al 1,5% y almacenadas a 20°C, encontraron que hasta el segundo día de almacenamiento las fresas con y sin tratamiento presentaban el mismo valor de pérdida de peso.
Por otra parte, los tratamientos influyeron sobre la respiración de las fresas (P≤0,05). En el día 0 todas las fresas tratadas mostraron valores de CO2 superiores a las fresas control; la máxima respiración fue en las fresas tratadas con Q. Al segundo día todas las fresas, con excepción de las tratadas con NPQEEA, aumentaron sus niveles de respiración a temperatura ambiente se observó un rápido aumento de la respiración que fue significativo. Con respecto al contenido de fenoles totales no hubo diferencias significativas entre los tratamientos (Cuadro 1).
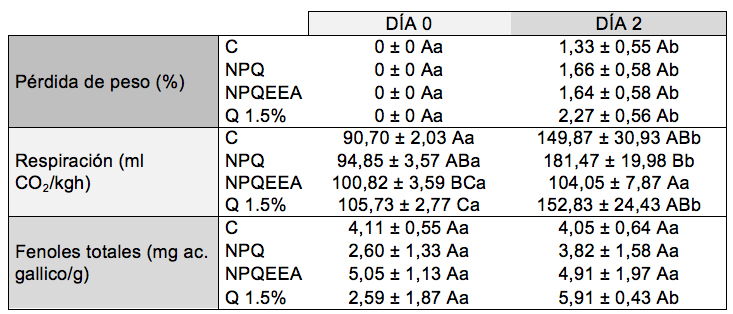
Las letras mayúsculas indican diferencias significativas (Tukey a una P ≤ 0,05) entre los tratamientos; las letras minúscula entre los días.
Fuente: elaboración propia.Parámetros de calidad
El Cuadro 2 muestra los resultados obtenidos para estos parámetros. Los tratamientos fueron estadísticamente iguales y no tuvieron efecto sobre L, chroma y hue. La firmeza no varió entre los cuatro tratamientos que fueron estadísticamente igual. Los tratamientos evaluados (Q, NPQ y NPQEEA), no influyeron en el contenido de acidez y SST, no habiendo diferencias estadísticas (P ≤ 0,05) entre las fresas tratadas y las fresas no tratadas.
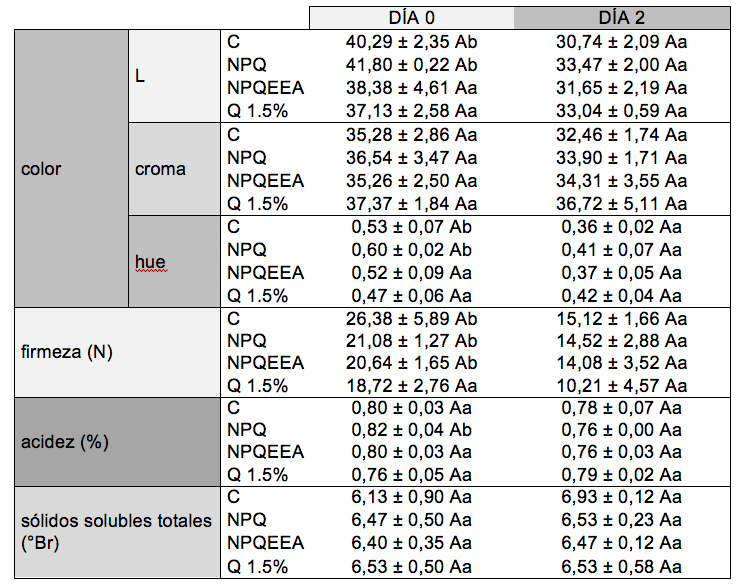
Las letras mayusculas indican diferencias significativas (Tukey a una P ≤ 0,05) entre los tratamientos; las letras minúscula entre los días.
Fuente: elaboración propia.Parámetros de infección
También en este caso todos los hongos desarrollados (Colletotrichum, Alternaria, Fusarium, Rhizhopus) se consideraron para evaluar los parámetros de infección (incidencia y severidad). A temperatura ambiente se observó un rápido desarrollo de la infección. Las fresas control llegaron a una intensidad de infección del 90% casi el doble de las fresas tratadas con NPQ, NPQEEA y Q, los diferentes tratamientos no influyeron sobre la severidad de infección que fue igual en todas las fresas (Figura 6).
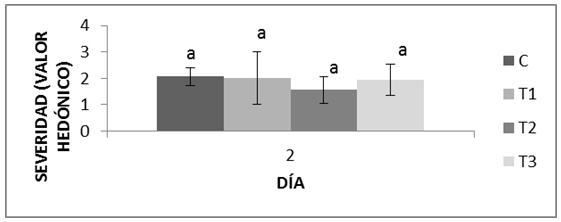
Figura 6
Representación gráfica de la incidencia de la infección y severidad en fresas tratadas con NPQ (T1), NPQEEA (T2) y Q 1,5% (T3) almacenadas a temperatura ambiente.
Las barras verticales indican las desviación estándar. Letras diferentes muestran diferencias significativas (Tukey a una P ≤ 0,05) entre los tratamientos.
Fuente: elaboración propia.CONCLUSIONES
Las NPQ y NPQEEA tuvieron un tamaño de 3 y 26 nm respectivamente. Éstas fueron altamente eficientes en la inhibición del crecimiento in vitro de Colletotrichum fragariae, a la concentración de 75 µl/ml. En ambas temperaturas la respiración mostro diferencias significativas entre los tratamientos los cuales mostraron valores de CO2 superiores a las fresas control. Los parámetros de calidad no mostraron diferencias significativas entre los tratamientos a las dos temperaturas ensayadas. Por otra parte, en la prueba in situ a temperatura de 5°C y a temperatura ambiente las NPQ y NPQEEA no tuvieron efecto inhibitorio sobre los hongos Fitopatógenos.
Agradecimientos
Los autores agradecen al Dr. Hugo Martinez del Centro de Nanociencias y Micro y Nanotecnologías del IPN por su apoyo en el análisis de Microscopía Electrónica de Transmisión.
REFERENCIAS
Barrera-Necha, L.L., Correa-Pacheco, Z., Bautista-Baños, S., Hernández López M., Martínez-Jiménez, J.E., and Moran-Mejía, A. 2018. Synthesis and characterization of chitosan nanoparticles loaded botanical extracts with antifungal activity on Colletotrichum gloeosporioides and Alternaria species. Advances in Microbiology (aceptado)
Bautista-Baños, S., Hernández-Lauzardo, A., Velázquez del Valle, M., Bosquez-Molina, E. and Sánchez-Domínguez, D. 2005. Quitosano: una alternativa natural para reducir microorganismos postcosecha y mantener la vida de anaquel de productos hortofrutícola. Revista Iberoamericana de Tecnología Postcosecha. 7, pp:1-6.
Bautista-Baños, S., Hernández-López, M., Bosquez-Molina, E., and Wilson C. 2003. Effects of chitosan and plant extracts on growth of Colletotrichum gloeosporioides, anthracnose levels and quality of papaya fruit. Crop Protection 22, pp1087-1092.
Carlson, R., Taffs, R., Davison, W., and Stewart, P. 2008. Anti-biofilm properties of chitosan-coated surfaces. Journal of Biomaterials Science Polymer Edition. 19, pp:1035-1046.
Chookhongkha, N., Sopondilok, T., and Photchanachai, S. 2013. Effect of chitosan and chitosan nanoparticles on fugal growth and chilli seed quality. Acta Horticulturae 973:231-237.
Chowdappa, P., Shivakumar, C., Chethana, S., and Madhura, S. 2014. Antifungal activity of chitosan-silver nanoparticles composite against Colletotrichum gloeosporioides associated with mango anthracnose. African Journal of Microbiology research. 81, pp:1803-1812.
Ermis, E., Hertel, C., Schneider, C., Carle, R., Stintzing, F., and Schmidt, H. 2015. Characterization of in vitro antifungal activities of small and American cranberry (Vaccinium oxycoccos L. and V. macrocarpon Aiton) and lingonberry (Vaccinium vitis-idaea L.) concentrates in sugar reduced fruit spreads. International Journal of Food Microbiology, 204, pp:111-117.
Feliziani, E., Landi, L., and Romanazzi, G. 2015. Preharvest treatments with chitosan and other alternatives to conventional fungicides to control postharvest decay of strawberry. Carbohydrate Polymers. 132, pp:111-117.
Garduño-Pizaña, C., Barrera-Necha, L., and Rios-Gómez, M. (2010). Evaluation of the Fungicidal Activity of Leaves Powders and Extracts of Fifteen Mexican Plants Against Fusarium oxysporum f.sp. gladioli (Massey) Snyder and Hansen. Plant Pathology Journal. 9 (3), pp:79-87.
Gunnell, P. S., and Gubler, W. D. 1992. Taxonomy and morphology of Colletotrichum species pathogenic to strawberry. Mycologia 84: 157-165.
Han, C., Zhao, Y., Leonard, S., and Traber, M. 2004. Edible coatings to improve storability and enhance nutritional value of fresh and frozen strawberries (Fragaria x ananassa) and raspberries (Rubus ideaus). Postharvest Biology and Technology. 33, pp:67-78.
Hernández-Muñoz, P., Almenar, E., Del Valle, V., Velez, D., and Gavara, R. 2008. Effect of chitosan coating combined with postharvest calcium treatment on strawberry (Fragaria × ananassa) quality during refrigerated storage. Food Chemistry. 110, pp:428–435.
Hernández-Muñoz, P., Almenar, E., Ocibo, M., and Gavara, R. 2006. Effect of calcium dips and chitosan coatings on postharvest life of strawberries (Fragaria x ananassa). Postharvest Biology and Technology. 39, pp:247-253.
Hernández-Téllez, C., Plascencia-Jotomea, M., and Cortez-Rocha, M. 2016. Chitosan-Based Bionanocomposites: Development and Perspectives In Food and Agricultural Applications. Pp: 315-338. In: Bautista-Baños S., Romanazzi G. y Jiménez-Aparicio A. (eds.). Chitosan in the Preservation of Agricultural Commodities. Academic Press. 366p.
Howard, C., Maas, J., Chandler, C., and Albregts, E. 1992. Anthracnose of strawberry caused by the Colletotrichum complex in Florida. Plant Disease. 76 pp: 976-981.
Ishikawa, Y., Hirata, T., and Hasegawa, Y. 1997. Development of simple Gas permeability measurement for polymeric films-on high Gas permeability films for MA packaging of fresh produce. Journal of Packaging Science and Technology. 6, pp:213–220.
Lizardi-Mendosa, J., Argüelles-Monal, W., and Goycoolea-Valencia, F. 2016. Chemical Characteristics and Functional Properties of Chitosan. P: 3-31. In: Bautista-Baños S., Romanazzi G. y Jiménez-Aparicio A. (eds.). CHITOSAN in the Preservation of Agricultural Commodities. Academic Press. 366p.
Luque-Alcaraz, A., Lizardi, J., Goycoolea, F., Valdez, M., Acosta, A., Iloki-Assanga, S., Higuera-Ciapara, I., and Arguelles-Monal, W. 2012. Characterization and antiproliferative activity of nobiletinloaded chitosan nanoparticles. Journal of Nanomateriales. Pp:1-7.
Ma, Z. and Lim, L. 2003. Uptake of chitosan and associated insulin in Caco-2 cell monolayers: a comparison between chitosan molecules and chitosan nanoparticles. Pharmaceutical. Research. 20 (11), pp: 1812-1819.
McGuire, R.G. 1992. Reporting of objective color measurements. Hort Science. 27, pp:1254-1255.
Perdones, A., Sánchez-González, L., Chiralt, A., and Vargas, M. 2012. Effect of chitosan–lemon essential oil coatings on storage-keeping quality of strawberry. Postharvest Biology and Technology. 70, pp:32–41.
Romanazzi, G. 2010. Chitosan treatment for the control of postharvest decay of table grapes, strawberries and sweet cherries. In: Sivakumar, D. (Ed.), Fresh Produce – Special Issues: New Trends in Postharvest Management of Fresh Produce, vol. 4. Global Science Books, Ltd., UK, pp. 111–115.
Romanazzi, G., Feliziani, E., Santini, M., and Landi, L. 2013. Effectiveness of postharvest treatment with chitosan and other resistance inducers in the control of storage decay of strawberry. Postharvest Biology and Technology. 75, pp 24-27.
Salzar-Leyva, J., Lizardi-Mendosa, J., Ramírez-Suarez, J., García-Sanchez, G., Ezquerra-Brauer, J., Valenzuela-Soto, E., Carvillo-Ruiz, M., Lugo-Sanchez, M., and Pacheco-Aguirar, R. 2014. Utilization of chitin and chitosan based materials for protease immobilization: stabilization effects and applications. Revista Mexicana de Ingeniería Química. 13 (1), pp:129-150.
Shukla, S., Mishra, A., Arotiba, O., and Mamba, B. 2013. Chitosan based nanomaterials: a state-of-the-art review. International Journal of Biological Macromolecules. 59, pp: 46-58.
Singleton, V., and Rossi, J. 1965. Colorunetry of total phenolics with phosphomolybdic-phosphotungstic acid reagents. Amer. J. Enol. Viticult. 16, pp:144-58.
Smith, B. J., and Black, L. L. 1990. Morphological, cultural, and pathogenic variation among Colletotrichum species isolated from strawberry. Plant Dis. 74: 69-76.
Sotelo-Boyás, M., Valverde-Aguilas, G., Plascencia-Jatomea, M., Correa-Pacheco, Z., Jiménez-Aparicio, A., Solorza-Feria, J., Barrera-Necha, L., and Bautista-Baños, S. 2015. Characterization of Chitosan Nanoparticles added with Essencial Oils. In vitro effect on Pectobacterium Carotovorum. Revista Mexicana de Ingeniería Química. 14 (3), pp:589-599.
Vargas, M., Albors, A., Chiralt, A., and González-Martínez, C. 2006. Quality of cold-stored strawberries as affected by chitosan-oleic acid edible coatings. Postharvest Biology and Technology. 41, pp:164-171.
Vargas, M., Albors, A., Chiralt, A., and González-Martínez, C. 2011. Water interactions and microstructure of chitosan-methylcellulose composite films as affected by ionic concentration. LWT – Food Science and Technology. 44,pp:2290–2295.
Xie, L., Zhang, J., Wan, Y., and Hu, D. 2010. Identification of Colletotrichum spp. Isolated from strawberry in Zhejiang Province and Shanghai City, China. Journal of Zhejiang University SCIENCE B, 11, pp:61-70.
Zahid, N., Alderson, P., Ali, A., Maqbool, M., and Manickam, S. (2013). In vitro control of Colletotrichum gloeosporioides by using chitosan loaded nanoemulsions. Acta Hortic. 1012, 769-774
Wang, S., and Gao, H. 2013. Effect of chitosan-based edible coating on antioxidants, antioxidant enzyme system, and postharvest fruit quality of strawberries (Fragaria x aranassa Duch.). Food Science and Technology. 52:71-79.
Notas de autor
* Autor de correspondencia: L. L. Barrera-Necha. E-mail: lbarera@ipn.mx