Reportes procesamiento
Variación nutrimental y funcional de pulpa de Guayaba en respuesta a diferentes temperaturas de almacenamiento
Nutrimental and functional variation of guava pulp in response to different storage temperatures
Variación nutrimental y funcional de pulpa de Guayaba en respuesta a diferentes temperaturas de almacenamiento
Revista Iberoamericana de Tecnología Postcosecha, vol. 19, núm. 1, 2018
Asociación Iberoamericana de Tecnología Postcosecha, S.C.
Recepción: 02 Marzo 2018
Aprobación: 25 Mayo 2018
Publicación: 30 Junio 2018
Resumen: La guayaba en un fruto de alto consumo principalmente en las regiones tropicales y subtropicales, esto debido a su agradable sabor y sus propiedades nutritivas y medicinales, es una fruta climatérica debido a la capacidad que tiene de madurar después de su cosecha. En el presente trabajo se determinó la variación del contenido de diferentes compuestos nutricionales y funcionales presentes en la pulpa de guayaba de tres cultivares “calvillo (Cca)”, “peruano (Cpe)” y “rosa (Cro)”, cuando las pulpas fueron sometidas a diferentes temperaturas (congelación: -20±1°C y refrigeración: 4±1°C) y tiempos de almacenamiento (1 a 16 días). Los resultados muestran que las pulpas frescas de Cca y Cro contienen mayor cantidad de compuestos fenólicos que Cpe, 278.65±5.40, 210.69±10.27 y 81.25±3.4 mg de ácido gálico/100g de pulpa respectivamente, en condiciones de refrigeración los tres cultivares tuvieron un aumento de estos compuestos con máximos del 10.71% en Cca, 20.38% en Cro y del 87.91% en Cpe; mientras que en condiciones de congelación el aumento máximo fue de 103.15% en Cca, 124.92% en Cro y 470.43% en Cpe, es decir el cultivar peruana fue la más favorecida con ambos tratamientos. En cuanto a actividad antioxidante determinada mediante los métodos ABTS y DPPH el aumento más significativo se dio en las condiciones de congelamiento para los tres cultivares. La vitamina C presentó valores en pulpa fresca de 336.63±14.17 en Cca, 383.67±4.41 en Cro y para Cpe de 214.62 ± 10.18 mg de ácido ascórbico/100g de pulpa, estos valores tuvieron un aumento en condiciones de refrigeración hasta 26.63% en Cca, 8.81% en Cro y del 4.79% en Cpe, mientras que en condiciones de congelación el aumento máximo en Cca fue de 38.86%, 14.94% en Cro y en 21.23% en Cpe. La acidez titulable y sólidos solubles aumentaron en ambas condiciones de almacenamiento a través del tiempo.
Palabras clave: nutricional, funcional, pulpa de guayaba, temperatura.
Abstract: Guava is a tropical fruit rich in high-profile nutrients. With its unique flavor, taste, and health-promoting qualities, the fruit fits into the category of new functional foods. Is considered a climacteric fruit due to its capacity to ripen after harvest. In the present work, the content of different nutritional and functional compounds present in the guava pulp of three cultivars "calvillo (Cca)", "peruana (Cpe)" and "rosa (Cro)" was determined under two different storage temperatures (freezing: -20 ± 1 °C and cooling: 4 ± 1 ° C) and times (1 to 16 days). The results show that fresh pulps of the Cca and Cro contain more phenolic compounds than the Cpe cultivars, 278.65 ± 5.40, 210.69 ± 10.27 and 81.25 ± 3.4 mg of gallic acid / 100g of pulp respectively, under refrigeration condition Cca had a maximum increase of these compounds of 10.71%, Cro 20.38% and Cpe 87.91%; while in freezing conditions the top increase for Cca was 103.15%, 124.92% in Cro and 470.43% for Cpe, this latter was the most favored with both treatments. In terms of antioxidant activity determined by the ABTS method the most significant increase occurred in the freezing conditions for the three cultivars. The fresh pulp presented values of Vitamin C as follows: 336.63 ± 14.17 in Cca, 383.67 ± 4.41 in Cro and for Cpe 214.62 ± 10.18 mg ascorbic acid/100g pulp. These values had a maximum increase in refrigeration conditions of 26.63% for Cca, 8.81% in Cro and 4.79% in Cpe; while in freezing conditions the increase for Cca was 38.86%, 14.94% in Cro and 21.23% for Cpe. Parameters such as titratable acidity and soluble solids increased in both storage conditions through time.
Keywords: Guava pulp, functional compounds, cooling storage.
INTRODUCCIÓN
La alimentación humana ha cambiado en las últimas dos décadas, el creciente número de personas que consumen frutas y vegetales debido a los efectos benéficos que los fitoquímicos tienen sobre la salud (Leifert y Abeywardena, 2008); ha aumentado la demanda de frutos y vegetales saludables que contengan antioxidantes naturales, tales como la vitamina A, E y C polifenoles, carotenoides y otros compuestos capaces de neutralizar radicales libres (Piljac Zegarac et al., 2010), muestra de ello son los alimentos denominados de cuarta gama, “alimentos que han sido pre-elaborados, sin cocción y envasados en recipientes bajo atmósferas controladas”, y los de tercera gama “alimentos congelados” los cuales permiten disponer rápidamente de un alimento nutritivo y natural (Artés-Hernández et al., 2009).
Un fruto que emerge como atractivo para el desarrollo de estos productos es la guayaba, la cual es originaria de Centroamérica, que según la variedad o el cultivar el fruto puede ser redondo o en forma de pera, cáscara de color verde-amarillo o amarillo-rosado, pulpa de color blanca, rosada o amarilla y su peso oscila entre 50-1000 gramos (García et al., 2010). Constituida principalmente por compuestos como ácido ascórbico, niacina, azucares, taninos, carotenoides, polifenoles y fibra (Jiménez-Escrig et al., 2001; Mahattanatawee et al., 2006; Moreno et al., 2014). Se cultiva principalmente para su consumo en fresco, pero por ser una fruta climatérica, después de ser cosechada sufre pérdida de peso y reducción de su vida útil de 5 a 7 días limitando su comercialización en mercados de igual manera con la madurez pierde gradualmente su valor nutricional (Chitarra y Chitarra, 2005).
El Estado de México ocupa el cuarto lugar a nivel nacional en producción de guayaba antecedido solo por Michoacán Aguascalientes y Zacatecas, los municipios de dicho estado con más producción son Coatepec Harinas con una superficie de 345 has sembradas y una producción de 5,175 toneladas, en segundo lugar, Temascaltepec con una superficie de 154 has y 1617 toneladas cosechadas y por último Zumpahuacán con 128 has y una cosecha de 1024 toneladas (SEDAGRO, 2016). Las pérdidas económicas que registran los productores son debido principalmente a el carácter climatérico del fruto, su mal manejo postcosecha y daños por magulladuras, rajaduras, granizo, raspaduras, rozaduras, costras, manchas o quemaduras de sol que afectan la calidad de la fruta. En México se pierde el 57 % de producción total de guayaba (Sangerman et al., 2013). Por lo que muchos de los estudios que se han realizado con este fruto son relacionados a la pérdida de su calidad en respuesta al tipo y tiempo de almacenamiento (Yam Tzec et al., 2010).
Algunos de los compuestos fenólicos totales (CFT) presentes en los frutos de guayaba son el ácido elágico y glicosilados de miricetina y apigenina (Moreno et al., 2014) los cuales contribuyen a la alta capacidad antioxidante del fruto, además del licopeno, carotenoides, polifenoles y la vitamina C (Almeida et al., 2011). La cantidad de estos compuestos benéficos depende del grado de madurez, variedad o cultivar, clima, composición del suelo y condiciones de almacenamiento (Haminiuk et al., 2012).
Se ha descrito que el tiempo y las altas temperaturas de almacenamiento (40°C y 50°C) afectan la estabilidad de la vitamina C, licopeno, compuestos fenólicos totales presentes en jugo de guayaba rosa, también la capacidad antioxidante se ve reducida con el aumento de la temperatura de almacenamiento. Ordoñez-Santos y Vázquez-Riascos (2010) describen que no existe diferencia significativa en los grados brix del néctar y pulpa de guayaba después de 240 días de almacenamiento a 10 ± 2 °C, sin embargo, el tiempo de almacenamiento afecta el contenido de vitamina C, el pH, la acidez titulable (Kader y Watkins, 2002; García et al., 2011). Se han reportado reducciones del 36% del contenido de vitamina C y perdidas de licopeno de hasta 17.6% en jugo de guayaba almacenado durante 210 días a 4°C y pérdidas del 70% de vitamina C en mermelada de guayaba almacenada durante 90 días a 25°C. (Rodriguez-Amaya, 2001; Jawaheer et al., 2003)
El contenido de CFT varía con el estado de maduración de los frutos de guayaba, siendo más elevados en los estados pintón y maduro que en el verde y el sobremaduro respectivamente, por otra parte la actividad antioxidante determinada mediante el método ABTS, muestra en el estado maduro de la mayoría de las variedades sus valores más elevados (22-48 micromoles trolox/g de fruta), siendo una excepción el cultivar regional rosa que exhibe su mayor valor en el estado pintón (21.19- 48 micromoles de trolox/g de fruta)se observa que a medida que la fruta madura se presenta una capacidad mayor de bloqueo de los radicales libres (Thaipong et al., 2006).
En la presente investigación se analizó la variación de los componentes nutricionales y funcionales como son vitamina C, compuestos fenólicos totales, capacidad antioxidante, sólidos solubles totales, pH y acidez titulable de la pulpa de guayaba de tres diferentes cultivares sometidos a dos temperaturas de almacenamiento post cosecha -20 y 4 °C.
MATERIALES Y MÉTODOS
Material vegetal
Los frutos de guayaba de tres cultivares: Calvillo (Cca), Rosa (Cro) y peruano (Cpe), se recolectaron en octubre de 2016, en la localidad de Tlapizalco situada en el Municipio de Zumpahuacán Estado de México a una altitud de 1780 metros sobre el nivel del mar.
Preparación de las pulpas
Se lavó y desinfectó 3 Kg de los frutos de cada cultivar, se secaron a temperatura ambiente 25 ± 2 °C, posteriormente se cortaron en trozos retirándoles los huesos y se procedió a molerlos en una licuadora industrial, marca acros, hasta obtener una pasta uniforme, la cual se envasó al vacío en bolsas de polipropileno con un contenido neto de 100g. Se almacenaron siete muestras en refrigeración y siete en congelación a temperaturas de 4 ± 1°C y -20 ± 1°C respectivamente. Se utilizó como el control una muestra de 100g de cada cultivar, es decir se realizaron las mediciones inmediatamente después de realizado el proceso de molienda.
Determinación de compuestos fenólicos totales (CFT)
Se preparó una solución madre, 9 repeticiones de cada muestra, para cada cultivar se utilizaron 0.5 g de pulpa y se les adicionó 50 mL de agua destilada, se sometieron a agitación por un periodo de 10 minutos para homogeneizar la mezcla, se centrifugaron a 4000rpm y el sobrenadante fue lo que se utilizó para las determinaciones (solución madre). Se tomaron 50 µL de cada solución madre para realizar la determinación de compuestos fenólicos.
El contenido de compuestos fenólicos totales se determinó mediante el método colorimétrico Follin-Ciocalteu con algunas variaciones, las lecturas se realizaron a una longitud de onda de 760 nm en un espectrofotómetro Perkin-Elmer UV-VIS lamda 25, se utilizó ácido gálico como patrón de referencia. Los resultados fueron expresados como mg de ácido gálico equivalentes por cada 100 g de pulpa.
Actividad antioxidante por los métodos DPPH y ABTS
Determinación de actividad antioxidante mediante el método de DPPH (Kedare y Sing, 2011; Shimakura et al., 2014). Se utilizó una solución metanólica de DPPH (0.00295g de DPPH + 50 mL de metanol al 80%). A un volumen de 250 µL de solución madre se le adicionó 1 mL de DPPH se homogeneizaron y se dejaron reaccionar en la oscuridad por un periodo de 30 minutos. Las medidas se realizan a una longitud de onda de 517 nm. Los resultados son expresados en micromoles equivalentes de Trolox (µM TEAC ).
La actividad inhibidora del radical ABTS.+ se midió de acuerdo al método descrito por Re et al., (1999) con algunas modificaciones en cuanto a las concentraciones de los extractos. Se utilizó una solución acuosa formada por 20mL de agua destilada y 77.6 mg de ABTS al cual se le adicionaron 13.2 mg de Persulfato de Potasio, se incubaron en la oscuridad y durante 24 horas, seguido de este tiempo se realizó una dilución de la solución del radical ABTS.+ en etanol absoluto hasta obtener una absorbancia de 0.7 ± 0.02 a 732nm. A un volumen de 250 μL de solución madre se le agregaron 1250 μL del radical ABTS.+ diluido, se agitaron para homogeneizar y se dejaron en reposo durante 30 minutos. La absorbancia se midió a una longitud de onda de 732nm.
Determinación de vitamina C
Para la determinación de vitamina C las muestras fueron preparadas con 10 g pulpa aforados a 100 mL con agua destilada agitando hasta homogeneizar. La concentración de vitamina C se determinó mediante yodimetría, debido a que la reacción entre el yodo y ácido ascórbico presentan una estequiometria 1:1, utilizando almidón soluble como indicador y una solución 0.25M de yodo como agente valorante, los resultados se expresan en mg de ácido ascórbico por cada 100g de pulpa.
Acidez titulable
Para la determinación de la acidez titulable se utilizaron igualmente 10 g de pulpa aforados a 100 mL con agua destilada, de esta solución se tomaron 20mL para realizar las titulaciones, en este caso se tituló con NaOH 0.1 N y como indicador se utilizó fenolftaleína, los resultados se expresan en mg de ácido cítrico por cada 100g de pulpa.
Determinación de sólidos solubles totales y pH
Dichos compuestos fueron determinados con la ayuda de un refractómetro digital de mano (Pocket ATAGO) y un potenciómetro manual en el caso de los sólidos solubles se colocó 1 g de pulpa en el lector del refractómetro y se procedió a tomar la lectura, para el pH el electrodo del potenciómetro se introdujo directamente en las pulpas y se registró la lectura que se mantuvo estable una vez transcurridos 20 segundos.
Análisis estadístico
Se empleó un diseño completo al azar. Los resultados fueron procesados mediante una ANOVA de una vía, seguida de una prueba de contrastes múltiples de Dunnett, en ambas el nivel de significancia mínimo aceptado fue de p<0.05.
RESULTADOS Y DISCUSIÓN
El contenido de compuestos fenólicos totales (CFT) en las pulpas analizadas utilizando el método de Folin-Ciocalteu se expresan en términos de equivalentes de ácido gálico (AGE) (los valores obtenidos para la curva de calibración fue r2=0.9949 y la ecuación resultante fue: y= -0.0069+1517x). El contenido de CFT aumento en ambas condiciones de almacenamiento con respecto a la muestra control. En refrigeración presento un aumento del 10.71% para el Cca, un 20.38 % para Cro y un 87.91 % para Cpe en los días 1, 2 y 1 respectivamente (figura 1). Mientras que en las pulpas congeladas el aumento se dio desde el día 1 hasta el día 16 en los tres cultivares, siendo Cpe el que mayor aumento presento con un 470.43 %, seguida de Cro con un aumento del 124.92% y por último el Cca con 103.15% de aumento los tres cultivares presentaron su máximo en el día 16 de congelación (figura 1).
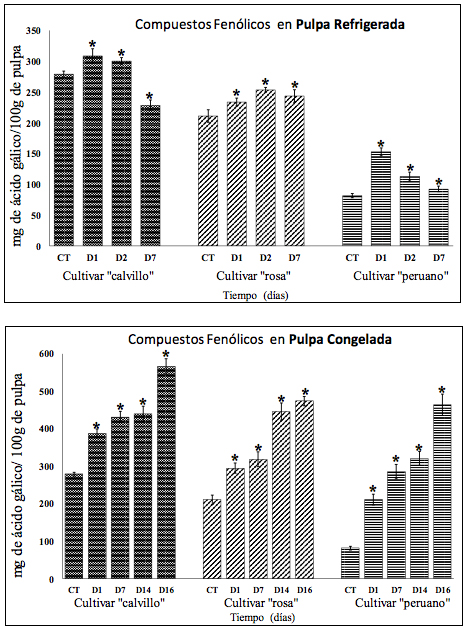
Figura 1
Contenido de compuestos fenólicos en pulpa refrigerada y pulpa congelada de los tres cultivares en los días 1, 2 y 7 (D1, D2 y D7) comparados contra el control (CT).
Los (*) denotan diferencia significativa contra el control p<0.05 (análisis realizado mediante una prueba de ANOVA de una vía seguida de una prueba post-hoc de Dunnett).
Fuente: elaboración propia.Existe una disminución en la concentración de CFT en condiciones de almacenamiento a temperatura ambiente en frutos de guayaba (Siqueira et al., 2011); sin embargo, el aumento de CFT en respuesta a las bajas temperaturas ha sido reportado en otras frutas, como es el caso de fresas, y frambuesas almacenadas a -20°C por 12 meses, que incrementaron su contenido en 19 y 10% al finalizar el almacenamiento (Šamec y Piljac-Žegarac, 2015). Otros estudios reportan un comportamiento similar en cerezas almacenadas a 4°C, las cuales muestran un incremento de 72,5% en el contenido de CFT, mientras que en moras refrigeradas a 1°C durante 15 días los aumentos van del 9,5% al 54,1%, y en moras azules después de 90 días congeladas a -27.5 °C 11.71 % (Piljac-Žegarac y Šamec, 2011; Bouzari et al., 2015). El aumento en el contenido de CFT en frutos almacenados a bajas temperaturas puede explicarse en parte debido a que, durante la congelación, los compuestos fenólicos se pueden extraer de forma más fácil, esto es debido, a la degradación de estructuras celulares durante la exposición a bajas temperaturas de almacenamiento o la molienda en el caso de las pulpas (Bakowska-Barczak y Kolodziejczyk, 2008), una razón más para el aumento del contenido de CFT, sería la reducción de la actividad oxidativa de las enzimas dando como resultado una menor degradación de estos componentes (Bouzari et al., 2015).
La actividad antioxidante determinada mediante el método de DPPH esta expresada en µM TEAC /g de pulpa. En pulpas refrigeradas el máximo registro para Cca fue el día 1, mientras que para Cro fue los días 2 y 7 y para Cpe los días 1 y 2, en el Cca se aprecia una disminución significativa de la actividad antioxidante el día 7 (figura 2). En las pulpas congeladas el máximo aumento en los Cca y Cro se registró en los días 1 y 16 mientras que en el Cpe tuvo su mayor aumento el día 1. Cabe destacar que los tres cultivares muestran un comportamiento similar, un aumento en el día 1, seguido de una disminución en el día 7 y seguido de esto un aumento paulatino hasta el día 16 (figura 2).
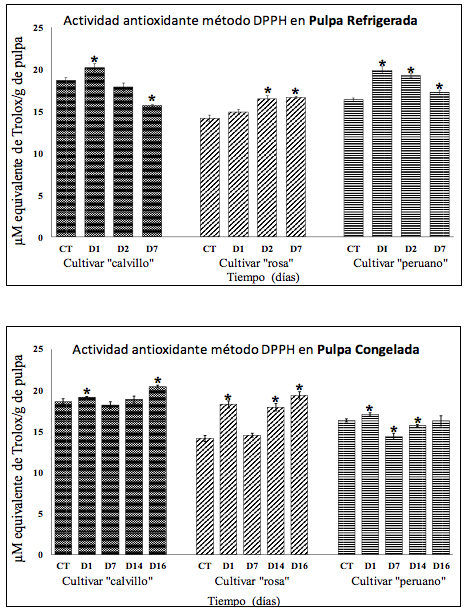
Figura 2
Actividad antioxidante determinada mediante el método de DPPH en pulpa refrigerada y pulpa congelada de los tres cultivares en los días 1, 2 y 7 (D1, D2 y D7) comparados contra el control (CT).
Los (*) denotan diferencia significativa contra el control p<0.05 (análisis realizado mediante una prueba de ANOVA de una vía seguida de una prueba post-hoc de Dunnett).
Fuente: elaboración propia.La actividad antioxidante determinada mediante el método de ABTS esta expresada en µM TEAC /g de pulpa. En pulpas refrigeradas el máximo registro para Cca fue el día 1, mientras que para Cro fue los días 2 y 7 y para Cpe los días 1 y 2. En el Cca se aprecia una disminución significativa de la actividad antioxidante el día 7 (figura 3). En las pulpas congeladas el máximo aumento en el Cca se registró en los días 1, 14 y 16; mientras que en Cro se presentó en los días 7, 14 y 16; el Cpe tuvo su mayor aumento el día 1 (figura 3).
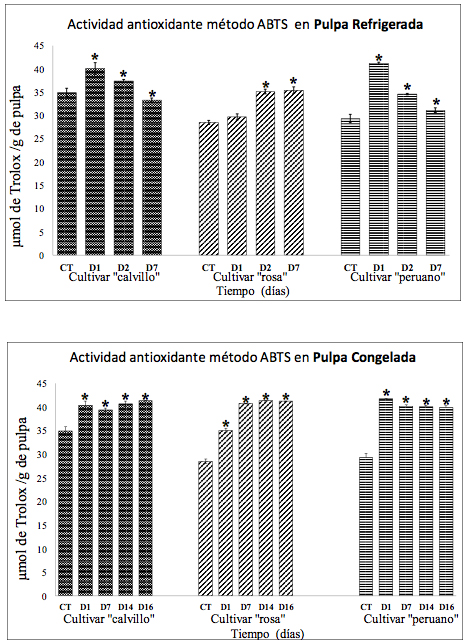
Figura 3
Actividad antioxidante determinada mediante el método de ABTS en pulpa refrigerada y pulpa congelada de los tres cultivares en los días 1, 2, 7, 14 y 16 (D1, D2, D7, D14 Y D16) comparados contra el control (CT).
Los (*) denotan diferencia significativa contra el control p<0.05 (análisis realizado mediante una prueba de ANOVA de una vía seguida de una prueba post-hoc de Dunnett).
Fuente: elaboración propia.Esta tendencia se observó de igual manera en un estudio realizado en arándanos refrigerados a 5 °C por un intervalo de 3 a 7 semanas, los cuales mostraron un aumento en la actividad antioxidante al final de las 3 semanas (Connor et al., 2002). Por su parte, Reque et al. (2014), describen un aumento significativo de la actividad antioxidante en frutos congelados a -18 °C durante 6 meses. En su estudio se evidenció que las frutas congeladas mostraron aumento significativo de capacidad antioxidante durante los primeros meses de almacenamiento, lo que coincide con el incremento descrito en el presente estudio para pulpas congeladas y analizadas mediante los métodos DPPH Y ABTS. La actividad antioxidante puede incrementarse debido a una fuerte tendencia de los polifenoles a las reacciones de polimerización; sin embargo, cuando el grado de esta excede un valor crítico, el incremento de la complejidad molecular y la reducción de la disponibilidad de grupos hidroxilos junto con el impedimento estérico, reducen la disponibilidad de los mismos en la reacción con los radicales DPPH y ABTS, lo que provocaría una disminución, tal como se observa en la presente investigación en el día 2 en pulpas refrigeradas (Šamec, 2015). Además, esta reducción de la capacidad antioxidante también puede asociarse a una la degradación de antocianinas (Kalt et al., 2003; Cordenunsi et al., 2005; He et al., 2010; Moreno et al., 2013). A ello se suma el proceso de pardeamiento de la fruta después de la molienda realizada en el tratamiento de la muestra, donde el ácido clorogénico junto con la polifenol oxidasa PPO, favorecerían la degradación de antocianinas al verse aumentada la actividad enzimática por el pH ácido (Kader et al., 1998), rango al que pertenece el pH de las pulpas analizadas en este estudio de 2.66 a 3.83. Sumado a ello, con el envejecimiento de la fruta se produce la formación de otros ácidos orgánicos con actividad antioxidante (Kalt et al., 2003), los cuales serían responsables del cambio en la curva y posterior incremento en la actividad antioxidante hacia el final del presente estudio en pulpas analizadas mediante el método DPPH.
Generalmente se describe que la actividad antioxidante esta correlacionada positivamente con el contenido de compuestos fenólicos totales y antocianinas. A pesar de ello algunos trabajos han reportado una correlación baja (Heinonen et al., 1998); y otros han reportado que en algunas pulpas congeladas de frutas no existe relación alguna entre el contenido de vitamina C con la capacidad antioxidante (Hassimoto et al., 2005), esto último es similar a lo encontrado en este trabajo.
Los resultados del análisis de vitamina C, acidez titulable, solidos solubles y pH se muestran en el cuadro 1. Se observa en pulpas refrigeradas que la vitamina C aumenta en Cca y Cpe para el día 7 de almacenamiento con un 26.63 y 4.79% respectivamente, en Cro el máximo aumento se presentó al día 1 de almacenamiento con un 8.81%, y para el día 7 los valores están muy por debajo del control. El contenido de vitamina C, en pulpas congeladas muestra un aumento máximo para el día 1 en los tres cultivares: Cca 38.86%, Cpe21.23% y Cro14.94 %; seguida de una disminución gradual hasta el día 14 en el que los valores medios están por debajo de los valores del control, los valores de vitamina C se encuentran entre los rangos reportados (Tanwar et al., 2014).
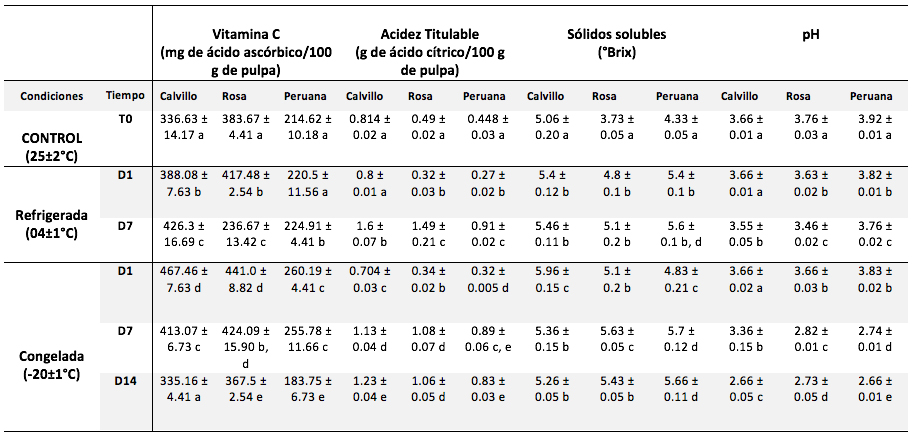
Fuente: elaboración propia.
El pH en pulpas refrigeradas tuvo su máxima disminución en el día 7 en los tres cultivares con un 3.0 % para el Cca, 7.97 % para el Cro y 4.08 % en Cpe. Mientras que en pulpas congeladas la mayor disminución se presentó en el día 14 en todos los cultivares con un 27.32 % para Cca, 27.39 % para el Cro y 32.14 % en Cpe, este parámetro esta correlacionado con la acidez titulable, la cual en pulpas refrigeradas mostró su aumento máximo en el día 7 en los tres cultivares, con valores de 96.56% para Cca, 204.81% en Cro y 103.12% en Cpe. Para las pulpas congeladas el Cca exhibió su máximo aumento en el día 14 mientras que los Cro y Cpe mostraron el máximo en el día 7, con valores de 51.10, 120.4 y 98.66% respectivamente.
En el parámetro de los sólidos solubles en pulpas refrigeradas se observó el aumento máximo en el día 7 en los tres cultivares con valores de 7.9% para Cca36.72 % en Cro y 29.33% para Cpe. Mientras que en pulpas congeladas el Cca mostro el máximo en el día 1, Cro y Cpe el día 7 con valores de 17.78, 50.93 y 31.66% respectivamente, este comportamiento coincide con lo reportado en un estudio realizado por Bouzari et al., (2015) quienes explica que durante el almacenamiento en frío los frutos pierden peso lo que produce un incremento en su concentración de azúcares.
CONCLUSIONES
La concentración de compuestos fenólicos en las pupas refrigeradas de los tres cultivares aumentó el día 1 con respecto al control, siguiendo una disminución gradual durante su almacenamiento hasta el día 7 mientras que en las pulpas congeladas de los tres cultivares existe un aumento de la concentración de compuestos fenólicos desde el día uno hasta el dieciséis. La actividad antioxidante exhibida por las pulpas de los tres cultivares esta correlacionada con la cantidad de compuestos fenólicos presentes en cada tratamiento y no así con la concentración de vitamina C. La congelación disminuye más los valores de pH que la refrigeración; mientras que la acidez titulable tiene comportamientos similares en las pulpas congeladas y refrigeradas. La pulpa del fruto de la guayaba es una buena opción para consumir como un alimento de la tercera gama, que conserva sus propiedades nutrimentales y funcionales a bajas temperaturas, asegurando su calidad durante la etapa de almacenamiento. Además, ofrece una nueva manera de comercializar el fruto a los productores de la región.
Agradecimientos
Al Tecnológico de Estudios Superiores de Villa Guerrero, por las facilidades otorgadas para desarrollar el presente proyecto.
Referencias
Almeida, M., P. de Sousa, Â. Arriaga, G. do Prado, C. Magalhães, G. Maia, and T, de Lemos. 2011. Bioactive compounds and antioxidant activity of fresh exotic fruits from northeastern Brazil. F.Res. Inter. 44: 2155–2159.
Artés-Hernández, F., E. Aguayo, P. Gómez, y F, Artés. 2009. Innovaciones Tecnológicas para preservar la calidad de los productos vegetales mínimamente procesados o de la “cuarta gama”. Rev. Hort. Int. 69:52-55.
Bakowska-Barczak, A., and P, Kolodziejczyk. 2008. Evaluation of Saskatoon berry (Amelanchier alnifolia Nutt.) cultivars for their polyphenol content, antioxidant properties, and storage stability. J Agric Food Chem. 56:9933–9940.
Bouzari, A., D. Holstege, and D, Barrett. 2015. Mineral, fiber, and total phenolic retention in eight fruits and vegetables: a comparison of refrigerated and frozen storage. J Agric Food Chem. 63:951–956.
Chitarra, M., and A, Chitarra. 2005. Postharvest of fruits and vegetables: physiology and handling. UFLA. Lavras, pp. 783.
Connor, A., J. Luby, J. Hancock, S. Berkheimer, and E, Hanson. 2002 Changes in fruit antioxidant activity among blueberry cultivars during cold-temperature storage. J Agric Food Chem. 50:893–898.
Cordenunsi, B., M. Genovese, J. do Nascimento, N. Hassimotto, R. dos Santos, and F, Lajolo. 2005. Effects of temperature on the chemical composition and antioxidant activity of three strawberry cultivars. Food Chem. 91:113–121.
García, C., K. Cury, and S, Dussan. 2011. Comportamiento Poscosecha y Evaluación de Calidad de Fruta Fresca de Guayaba en Diferentes Condiciones de Almacenamiento. Rev. Fac. Nac. Agron. 64:
García, C., K. Cury, y S. Dussán 2010. Evaluación poscosecha y estimación de vida útil de guayaba fresca utilizando el modelo de Weibull. Acta Agron. 59 347-355.
Haminiuk, W. G. Maciel, M. Plata-Oviedo, and R, Peralta. 2012. Phenolic compounds in fruits – an overview. Int. Jour. Food Sci.47:2023-2044.
Hassimoto, N., M. Genovese, and F, Lajolo. 2005. Antioxidant activity of dietary fruits, vegetables and commercial frozen fruit pulps. J. Agric. Food Chem. 53:2928-2935.
He, F., L. Mu, G. Yan, N. Liang, Q. Pan, J. Wang, M. Reeves, and C, Duan. 2010. Biosynthesis of anthocyanins and their regulation in colored grapes. Mol Basel Switz. 15:9057-9091.
Heinonen, A., A. Meyer and E, Frankel. 1998. Antioxidant activity of berry phenolics on human low-density lipoprotein and liposome oxidation. J. Agric. Food Chem. 46:4107- 4112.
Jawaheer, B., D. Goburdhun, and A, Ruggoo. 2003. Effect of processing and storage of guava into jam and juice on the ascorbic acid content. Plant Foods for Human Nutrition. 58:1-12.
Jiménez-Escrig, A., M. Rincón, R. Pulido, and F, Saura-Calixto.†. 2001. Guava fruit (Psidium guajava l.) As a new source of antioxidant dietary fiber. J. Agric. Food Chem. 49: 5489–5493
Kader, A. and C. Watkins. 2002. Postharvest Technology of Horticultural Crops. University of California Agriculture and Natural Resources Communication Services. pp. 535.
Kader, F., J. Haluk, J. Nicolas, and M, Metche. 1998. Degradation of Cyanidin 3-Glucoside by Blueberry Polyphenol Oxidase: Kinetic Studies and Mechanisms. J Agric Food Chem. 46: 3060–306.
Kalt, W., C. Lawand, D. Ryan, J. McDonald, H. Donner, and C, Forney. 2003. Oxygen radical absorbing capacity, anthocyanin and phenolic content of highbush blueberries (Vaccinium corymbosum) during ripening and storage. J Am Soc Hortic Sci. 128:917-923.
Kedare, S., and R. Sing. 2011. Genesis and development of DPPH method of antioxidant assay. J. Food Sci. Technol. 48: 412–422.
Leifert, W., and M, Abeywardena. 2008. Cardioprotective actions of grape polyphenols. Nutr. Res. 28:729–737.
Mahattanatawee, K., J. Manthey, G. Luzio, S. Talcott, K. Goodner, and E, Baldwin. 2006. Total antioxidant activity and fiber content of select florida-grown tropical fruits. Journal of Agriculture and Food Chemistry 54: 7355-7363.
Moreno, C., M. Andrade, A. Cancellón, y G, Díaz. 2013. Estudio de la capacidad antioxidante durante el almacenamiento refrigerado de naranjilla (Solanum quitoense) tratada con radiación UV-C. Rev. Iber. Tec. Post. 14:125-132.
Moreno, M., I. Zampini, M. Costamagna, J. Sayago, R. Ordoñez, and M, Isla. 2014. Phytochemical composition and antioxidant capacity of Psidium guajava fresh fruits and flour. Food and Nutrition Sciences. 5:725-732.
Ordóñez-Santos, L., and A, Vázquez-Riascos. 2010. Effect of processing and storage time on the vitamin C and lycopene contents of nectar of pink guava (Psidium guajava L.). Arch Latinoam Nutr. 60:280-284.
Piljac-Žegarac, J., and D, Šamec. 2011. Antioxidant stability of small fruits in postharvest storage at room and refrigerator temperatures. Food Res Int. 44:345–350.
Piljac-Zêgarac, J., L. Valek, T. Stipcêvic, and S, Martínez. 2010. Electrochemical determination of antioxidant capacity of fruit tea infusions. Food Chem. 12: 820-825.
Re, R., N. Pellegrini, A. Proteggente, A. Pannala, M. Yang, and C, Rice-Evans. 1999. Antioxidant activity applying an improved ABTS radical cation decolorization assay. Free Rad. Biol. Med. 26:1231–1237.
Reque, P., R. Steffens, A. Jablonski, S. Flôres, A. Rios, and E, de Jong. 2014. Cold storage of blueberry (Vaccinium spp.) fruits and juice: Anthocyanin stability and antioxidant activity. J Food Compos Anal. 33:111–116.
Rodriguez-Amaya, D. 2001. A guide to carotenoid analysis in foods. ILSI Press. USA. Pp64.
Šamec, D., and J, Piljac-Žegarac. 2015. Fluctuations in the levels of antioxidant compounds and antioxidant capacity of ten small fruits during one year of frozen storage. Int J Food Prop. 18:21–32.
Sangerman, J., S. Larqué, B. Navarro, R. Schwentesius, H. Damián, y S, Cuevas. 2013. Producción de guayaba (Psidium guajava (L.) Burn.) en el Estado de México, México. Rev. Mex. Cien. Agr. 4:1081-1093.
SEDAGRO 2016. Producción agropecuaria por municipio 2016. Disponible en: http://sedagro.edomex.gob.mx/produccion_floricola. [Consulta: 25 abril 2017].
Shimakura, T., Y. Sumikura, T. Yamazaki, A. Tada, T. Kashiwagi, H. Ishikawa, T. Matsui, N. Sugimoto, H. Akiyama, and H, Ukeda. 2014. Applicability of the DPPH assay for evaluating the antioxidant capacity of food additives-inter-laboratory evaluation study-. Analyt. Sci 30:717-721.
Siqueira, A., J. da Costa, M. Afonso, and E, Clemente. 2011. Pigments of guava paluma cultivar stored under environmental conditions. Afri. J. Food Sc. 5:320-323.
Tanwar, B., B. Andallu, and S, Chandel. 2014. Influence of processing on physicochemical and nutritional composition of Psidium Guajava L. (Guava) products. Int. Agric. Food Sci. Technol. 5:47-54.
Thaipong, K., U. Boonprakoba, K. Crosbyb, L. Cisneros-Zevallos and D, Byrne. 2006. Comparison of ABTS, DPPH, FRAP, and ORAC assays for estimating antioxidant activity from guava fruit extracts. J. Food Compos. Anal. 19:669–675.
Yam-Tzec, J., C. Villaseñor-Perea, E. Romantchik-Kriuchkova, M. Soto-Escobar, y M, Peña-Peralta. 2010. Una revisión sobre la importancia del fruto de Guayaba (Psidium guajava L.) y sus principales características en la postcosecha. Rev. Cien. Téc. Agrop. 19:74-82.
Notas de autor
* Autor de Correspondencia: Andrés A. Domínguez Guadarrama. E-mail: dgandalf@hotmail.com