Reportes Procesamiento
Recepción: 13 Agosto 2018
Aprobación: 25 Septiembre 2018
Publicación: 10 Diciembre 2018
Resumen: El agua disponible a nivel celular así como la temperatura, afectan significativamente el crecimiento y desarrollo de las hortalizas y también influyen posteriormente en la etapa postcosecha, afectando su calidad y vida útil. En este sentido, el principal problema de la rúcula (Eruca sativa) es su rápido deterioro luego de su recolección, ocasionado principalmente por la pérdida de agua, provocando su marchitamiento. En este trabajo se evaluó, mediante un sistema modelo experimental, la influencia del estrés osmótico, en las propiedades superficiales de protoplastos aislados de nervaduras de hojas de rúcula. Se observó, en la superficie de los protoplastos aislados la formación de regiones hidrofóbicas cuando el volumen celular se incrementa, según se detectó mediante el empleo de la sonda Merocianina 540 (MC540). El análisis del equilibrio de las especies del colorante indica que la distribución de monómeros y dímeros de MC540 varía en cada estadío osmótico. Se sugiere que lo observado es una consecuencia de los cambios producidos en el empaquetamiento superficial a nivel de la membrana, debido a la afinidad de este colorante con los ambientes lipídicos, que podrían ser importantes para la interacción de enzimas y otros solutos producidos por las plantas durante el estrés hídrico. Este análisis puede ser de importancia para predecir los cambios en el estado del cultivo bajo ciertas condiciones, causadas por estreses bióticos y abióticos, y también para obtener información sobre los cambios que ocurren en la morfología a nivel celular, producidos en los diversos estadios de conservación de la rúcula. Por medio de la metodología aplicada sería posible comprender mejor los procesos involucrados, relacionándolos con los cambios macroscópicos, ampliando así las herramientas tecnológicas para el control de los procesos que afectan la calidad poscosecha de hortalizas.
Palabras clave: Rúcula, protoplastos, sistema modelo, estrés.
Abstract: The available water at cellular level and the temperature significantly affect the growth and development of the vegetables and also subsequently influence the postharvest stage, affecting its quality and shelf life. In this sense, the main problem of the arugula (Eruca sativa) is its rapid deterioration after harvesting, caused mainly by the loss of water, causing its wilting. In this work, the influence of osmotic stress on the surface properties of protoplasts isolated from ribs of arugula leaves was evaluated by means of an experimental model system. The formation of hydrophobic regions on the surface was observed in the isolated protoplasts, when the cell volume increases as detected by the use of the Merocyanine 540 probe (MC540). The balance analysis of the dye species indicates that the monomer and dimer distribution of MC540 varies at each osmotic stage. It is suggested that what is observed is a consequence of changes in surface packing at the membrane level, due to the affinity of this dye with lipid environments, which could be important for the interaction of enzymes and other solutes produced by plants during water stress. This analysis can be important to predict the changes in the state of the crop under certain conditions, caused by biotic and abiotic stresses, and also to obtain information about the changes that occur in the morphology at the cellular level, produced in the different stages of conservation of the arugula. Through the applied methodology it would be possible to better understand the processes involved, relating them to macroscopic changes, thus expanding the technological tools for the control of processes that affect the post-harvest quality of vegetables.
Keywords: Rocket, protoplasts, model system, stress.
Introducción
El almacenamiento de hortalizas de hojas ocasiona la pérdida de agua, aún bajo refrigeración. Esto puede atribuirse a cambios en la permeabilidad de la membrana celular debido a una combinación de factores tales como la disfunción de los canales de agua (acuaporinas), la modificación del transporte iónico por enzimas específicas y la presencia de ROS que afecta los lípidos (Reyes, 2007). También hay segundos y terceros mensajeros, como EROS y Ca+2 involucrados en la inducción de la expresión de genes de interés, en respuesta al estrés (Munemasa, 2015). El estrés hídrico, osmótico y térmico implican modificaciones en los flujos de los iones Ca+2, H+, Cl- y K+ además de la pérdida de agua, en respuesta a señales hormonales traducidas por receptores específicos que se encuentran en la membrana plasmática y el citoplasma.
Las actividades de las bombas y canales que conducen esos iones modifican la polarización de la membrana plasmática vegetal y las membranas de vacuolas (Zhu, 2016). Esto puede implicar el intercambio de agua a través de la membrana afectando el potencial de membrana. En este sentido, la acción del estrés hídrico se puede visualizar en dos aspectos: a- el agua puede entrar y salir a través de la membrana cuando las células se someten a soluciones hipertónicas o hipotónicas; b- los osmolitos pueden alterar el ambiente acuoso de los lípidos en la membrana misma, causando defectos de empaque y fallas topológicas. Específicamente, este último proceso puede cambiar las propiedades de superficie de las membranas que afectan los sitios específicos para compuestos biológicos tales como aminoácidos y péptidos (Disalvo et al., 2013). Estos efectos pueden ser relevantes en membranas de células de hojas sometidas a estrés hídrico durante los procesos de conservación y almacenamiento de alimentos.
No se encontraron antecedentes sobre estudios relacionados con las propiedades de superficie de protoplastos en relación con los cambios de membrana producidos en el proceso de estrés osmótico de vegetales. Por esta razón, el propósito de este trabajo fue caracterizar los cambios en las propiedades superficiales originadas en la membrana plasmática de rúcula por estrés osmótico empleando el colorante MC540 como sonda que es altamente sensible a la polaridad ambiental y a los cambios de viscosidad (Cunderlíková y Sikurová, 2001).
Se dispone de amplia información en bibliografía sobre la interacción de MC540 con sistemas de membranas modelo como liposomas y vesículas como también de los cambios estructurales en el empaquetamiento de la membrana lipídica. Se conoce que diferentes especies de MC540 como dímeros y monómeros pueden particionar entre el agua y la fase lipídica (Bernik y Disalvo, 1996). Así mismo, el espectro de absorción de la merocianina 540 en presencia de vesículas artificiales cambia de un espectro acuoso a un espectro más similar al del colorante en solventes hidrofóbicos, cuando la temperatura aumenta a través de la temperatura de transición de fase (Lelkes y Miller, 1980).
Además, a medida que las bicapas atraviesan su transición de fase, se produce una serie de cambios en sus propiedades. La viscosidad de la bicapa disminuye, la membrana se expande lateralmente, se contrae transversalmente y el movimiento de la cadena lateral del ácido graso aumenta, mientras que la disposición y el empaquetamiento semicristalino cerrado de los grupos de cabeza desaparecen. Las bicapas de fase fluida se unen fuertemente al monómero de merocianina 540, mientras que las membranas de fase de gel no lo hacen (Willamson y Mattocks,1983).
Este colorante se utilizó ampliamente para monitorear el potencial transmembrana en muestras biológicas e informar cambios en la polarización de células muy pequeñas. Las medidas de las emisiones de fluorescencia de células individuales marcadas con MC540 fueron útiles para detectar cambios en el potencial de membrana en células de plantas para la clasificación de células y para la identificación de resistencia en el germoplasma de manzana. Además, para estudiar las funciones de los metabolitos tóxicos de patógenos y para determinar la acción del metabolito en la membrana (Mezzetti et al., 1992). Sin embargo, los estudios sobre la interacción de la sonda con las células vegetales son escasos.
Por lo tanto, es interesante estudiar los cambios en las propiedades biofísicas de los microambientes superficiales de protoplastos extraídos de hortalizas con esta sonda, para analizar el comportamiento de las diferentes especies de colorantes implicadas en el equilibrio durante el estrés osmótico.
Este análisis puede ser de importancia para predecir los cambios en el estado del cultivo bajo ciertas condiciones, causadas por estreses bióticos y abióticos, y también para obtener información sobre los cambios que ocurren en la morfología a nivel celular, producidos en los diversos estadios de conservación de la rúcula. Por medio de las metodologías aplicadas sería posible comprender mejor los procesos involucrados, relacionándolos con los cambios macroscópicos, ampliando así las herramientas tecnológicas para el control de los procesos que afectan la calidad poscosecha de hortalizas.
Materiales y métodos
Cultivo de Rúcula
Las plantas de rúcula (Eruca Sativa Mill) se cultivaron utilizando un sistema hidropónico comercial con solución nutritiva específica para Hortalizas (Hidroponía Cáceres Hnos., Concordia, Entre Ríos, Argentina). Las semillas se germinaron en espuma fenólica durante dos semanas, y luego se transfirieron al sistema de cultivo para su crecimiento y posteriormente se cosecharon para la extracción de protoplastos.
Preparación de protoplastos
Los protoplastos de rúcula se aislaron mecánicamente de hojas realizando un raspado de la nervadura en solución hipertónica de sacarosa 0,6 M con el fin de evitar daños en la membrana y la pared celular. Después de la plasmólisis, los protoplastos se filtraron a través de una malla de acero inoxidable de 100 μm para retener trazas de tejido vegetal y luego se dispersaron en una solución hipotónica de sacarosa para liberar los protoplastos. La suspensión se centrifugó a 4500 rpm durante 5 minutos y el precipitado se resuspendió en una solución de interés.
Soluciones de estrés osmótico
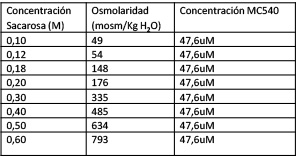
La osmolaridad y las concentraciones se enumeran en la Tabla 1. Las suspensiones de protoplastos sin colorante se usaron como referencia para compensar los efectos de la turbidez. Los espectros se obtuvieron en una muestra de 2 ml de suspensión de protoplastos con una densidad óptica constante (DO) a 600 nm. Luego se añadieron 100 μL de solución acuosa MC540 de 100 μM a todas las suspensiones y se incubaron durante 30 minutos.
Concentraciones de sacarosa con su correspondientes medidas de osmolaridad y concentración de MC540 en las celdas
Estrés osmótico
El estrés osmótico fue inducido por diferentes concentraciones de sacarosa preparadas con concentraciones y osmolaridad, listadas en la Tabla 1. La osmolaridad se determinó con un osmómetro de marca Loser Typ M 10/25 μL.
Métodos espectroscópicos
Se utilizó Merocianina con una constante de extinción molar ε = 0.6 x 105 M-1cm-1 de Sigma Chemical (USA), como sonda para la caracterización espectroscópica de la superficie de protoplastos sometidas a diferentes estreses osmóticos. La solución original de MC 540 se preparó en agua destilada y se almacenó a 5 ºC. Todas las preparaciones de colorante se envolvieron en papel de aluminio y se mantuvieron en la oscuridad. Se tomaron alícuotas de 100 μL de solución acuosa de MC540 y se añadieron a 2 ml de solución de protoplastos de OD a 600 nm conocida, en cubetas de vidrio de 1 cm de paso óptico. Los espectros como los de la Figura 4 se tomaron después de incubar durante 30 minutos. Para estudiar los efectos del estrés osmótico, los protoplastos se suspendieron en diferentes concentraciones de sacarosa y los espectros MC540 se obtuvieron en un espectrofotómetro de doble haz Jasco V-630.
Empleando la función picos y línea de base, del software Origin versión 8.0 SR3, se realizó el ajuste de múltiples picos espectrales que se obtuvieron mediante deconvolución utilizando la función gaussiana (basado en el módulo de ajuste de curvas no lineales de Origin). Los múltiples picos se ajustaron como la acumulación de la función gaussiana. El área del pico se determinó como la integral entre los límites de las bandas de absorbancia. Con respecto al espectro normalizado de MC540 al aumentar la concentración de osmolitos, no se observaron cambios espectrales de colorante con el aumento de la concentración de sacarosa, por lo tanto, no hubo interacción de la sonda con el osmolito.
Observaciones microscópicas
Los protoplastos se incubaron 10 minutos, antes de medir los diámetros por microscopía en un microscopio OLYMPUS CKX41.
Resultados
Propiedades espectroscópicas de MC540 en protoplastos
Los protoplastos se colectaron a la osmolaridad de 446 mosm/kg H2O con sacarosa. Después de centrifugar, el sobrenadante se eliminó y los protoplastos se suspendieron en soluciones de diferentes osmolaridades.
Los cambios de tamaño celular se midieron después de una hora de incubación con cada concentración de sacarosa como se muestran en la Figura 1. En el rango entre 200 a 650 mosm/Kg H2O, se observó una disminución atenuada del volumen con la osmolaridad según lo informado previamente por Ohshima (Ohshima et al., 2011). El punto de inflexión encontrado a 175 mosm/kg H2O sugiere un cambio en el régimen de los flujos de agua, es decir, al menos dos compartimentos de agua diferentes. Uno correspondería al agua libre en el volumen celular y el otro al agua comprometida con las estructuras celulares, como las membranas. Se puede obtener un volumen excluido correspondiente a 5 μm de diámetro por extrapolación a cero de la inversa de la presión osmótica (Figura 1). Este volumen excluido correspondería a estructuras celulares (membranas y macromoléculas) con sus correspondientes capas de hidratación (agua no osmótica). Los cambios en las propiedades de la membrana superficial alrededor de este punto se analizan a continuación mediante la inspección de los espectros de MC540.
La relación de absorbancia de 570 nm y 500 nm aumentó hasta alcanzar un valor constante por encima de OD 0.035, lo que denota que la superficie del protoplasto está saturada con el colorante en esta OD (Figura 1B). Por lo tanto, la variación en la relación de absorbancia como una función de las condiciones que pueden afectar la membrana del protoplasto se estudió en este rango de OD.
Caracterización de cambios superficiales de células bajo estrés osmótico
El efecto de las presiones osmóticas inducidas por sacarosa en la superficie de los protoplastos fue monitoreado por los cambios espectrales de MC540 (Figura 2). El aumento de las concentraciones del osmolito promovió la aparición de un hombro a 570 nm y una disminución en el pico a 504 nm en el rango de 49.5 a 154.7 mosm/Kg H2O.
El efecto se observa mejor en la Figura 1B, donde se compara la absorbancia a 570 nm con el cambio de diámetro, para diferentes osmolaridades. La absorbancia a 570 nm aumentó a aproximadamente 6 um y disminuyó significativamente cuando las células se hincharon.
Por lo tanto, los cambios en la absorbancia a 570 nm indican que las variaciones de volumen celular causados por la ósmosis afectaron la superficie de la membrana en diferentes etapas. Esto podría estar relacionado con diferentes cambios topológicos producidos por la compresión, la curvatura y la deshidratación parcial. Para estudiar estas posibilidades, las componentes espectrales de MC se analizan a continuación.
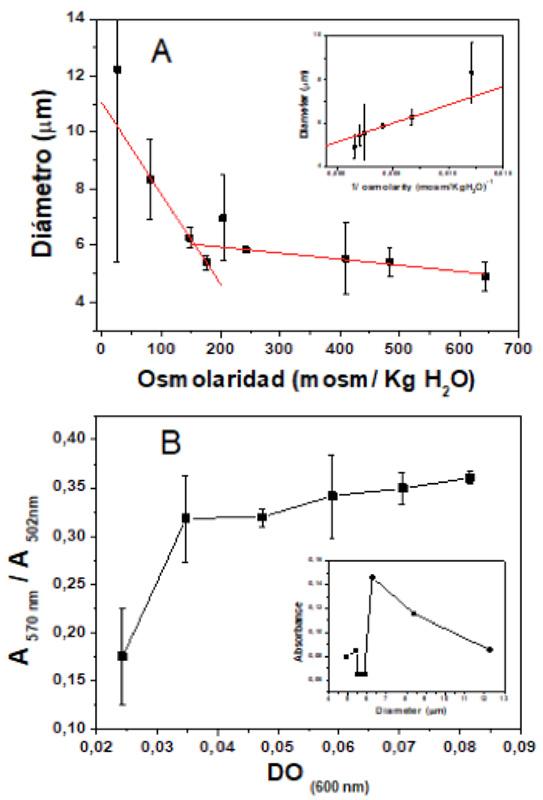
Figura 1
Efecto de la osmolaridad sobre el diámetro de protoplastos
(A) Diámetro de protoplastos en función de la osmolaridad, el punto de inflexión a 153 mosm/Kg H2O es equivalente a 0,18 M de Sacarosa. El inserto en la figura representa el diámetro de protoplastos versus 1/osmolaridad, que proporciona el volumen excluido correspondiente a un diámetro de 5,13 um. (B) Relación de absorbancia a 570 nm y 502 nm, en función de los incrementos de densidad óptica. En el inserto se observa la absorbancia del monómero de MC540 en membrana en función del diámetro de los protoplastos.
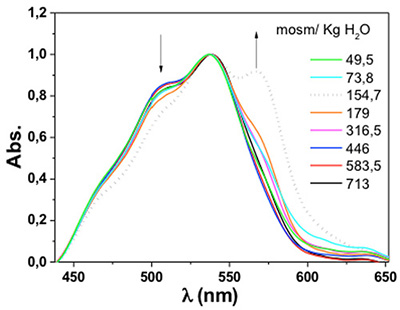
Figura 2
Espectros de absorción de MC540 en protoplastos de rúcula normalizados por el máximo, en concentraciones crecientes de sacarosa de 0.1 M a 0.6 M
Descomposición espectral y cambios de polaridad
La banda de absorbancia a 570 nm es característica del monómero de MC en fases lipídicas en el estado líquido cristalino (Lelkes y Miller, 1980). El área máxima para esta banda de absorbancia se encuentra en 149.5 mosm/kg H2O a la cual el diámetro celular es de 6.26 μm. Por lo tanto, sugiere que bajo estas condiciones los monómeros del colorante pueden adsorberse a sitios hidrófobos de los protoplastos en la interfaz. Cutro y Disalvo, (2015) describieron este comportamiento en sistemas modelos de lípidos y tribuyeron a la formación de defectos de empaquetamiento en la interfase de membrana debido a la inducción de la curvatura.
De manera similar, en el protoplasto, los monómeros insertados en las membranas pueden estar perturbados por el estado osmótico. Esto quiere decir que el equilibrio de las especies de colorante se modula por el estado de empaquetamiento e hidratación de la membrana. Los resultados previos apoyan esta conclusión según lo discutido por Bernik y Disalvo (1996). En la Figura 3 se muestra la deconvolución de los cambios espectrales de MC540. Originados por presiones osmóticas por sobre el punto de inflexión de 149,5 mosm/kg H2O.
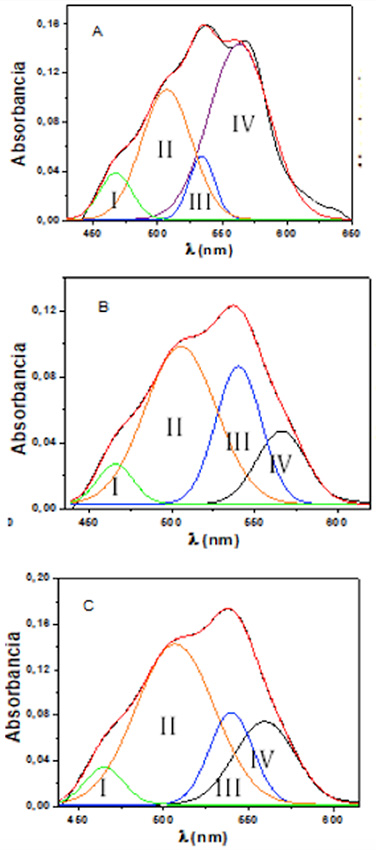
Figura 3
Deconvolución espectral de MC540 en presencia de protoplastos a diferentes presiones osmóticas (A) 149,5 mosm / Kg H2O (B) 205 mosm / Kg H2O (C) 612 mosm / Kg H2O respectivamente
(Banda I poliagregados, II dímeros en agua, III monómeros en agua y dímeros en la membrana, IV monómeros en membranas).
En diferentes estados osmóticos, los protoplastos presentaron una distribución diferente de las especies del colorante. La absorbancia a 450, 500, 530 y 570 nm corresponden a las siguientes especies de colorantes respectivamente: (I) poliagregados en agua; (II) dímero en agua; (III) dímero en la membrana y monómero en agua; (IV) monómero en la membrana (Kaschny y Goñi, 1992).
La evolución de las especies del colorante MC540 con la concentración se muestra en la Figura 4. En este rango de concentración, el diámetro celular varía ligeramente y se observa una disminución gradual del monómero en la membrana (banda IV) en paralelo a un aumento en el área de la banda correspondiente al dímero en fase acuosa (banda II). La formación de esta banda depende del equilibrio monómero/dímero y serviría como control para detectar cualquier cantidad significativa de colorante en el agua.
Se observó una conversión de monómeros a dímeros en medios acuosos (banda IV y banda II) al aumentar la concentración de sacarosa. Se sabe que el dímero de MC540 incrementa con el empaquetamiento de fosfolípidos (Kaschny y Goñi, 1992). La formación de dímeros en solución (banda II) es estimulada por el empaquetamiento de lípidos y por el aumento en la densidad de carga por unidad de área. Esto facilita la agregación y la formación de poliagregados de colorante. Finalmente, la especie (I) se ve favorecida en microambientes polares donde la densidad de carga superficial aumenta como resultado del empaque de fosfolípidos. Se observaron efectos similares en estudios de difusión lateral de fosfolípidos, que es un fenómeno importante en la dinámica de las membranas (Lelkes y Miller, 1980).
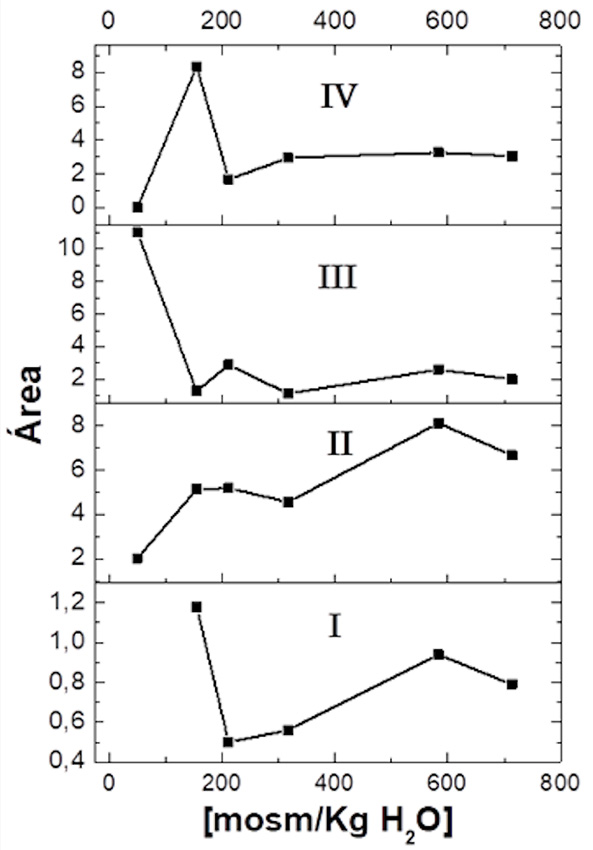
Figura 4
Efecto de la concentración de sacarosa en las áreas de las componentes espectrales de MC 540 en protoplastos de rúcula
(I) Poliagregados; (II) dímeros en agua; (III) monómeros en agua/dímeros en membrana y (IV) monómeros en la membrana.
La banda IV correspondiente al monómero en la membrana es especialmente sensible a los cambios en la polaridad. Incrementos en la polaridad del solvente producen desplazamientos hipsocrómicos de la banda del monómero.
Este comportamiento solvatocrómico del colorante fue demostrado en un amplio rango de constantes dieléctricas de solventes (Lelkes y Miller, 1980; Mateasik, 2002; Reichardt, 2003). Por lo tanto, es interesante estudiar las propiedades de la superficie alrededor del rango de 150 mosm / Kg H2O y en la zona de transición, para caracterizar los efectos causados por el estrés en la superficie de la célula. Se observó un aumento en la polaridad por encima de 200 mosm/Kg H2O de sacarosa, con la disminución del diámetro de los protoplastos (Figura 5).
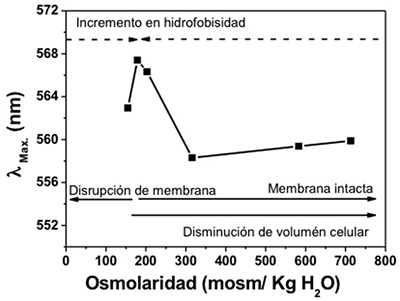
Figura 5
Evolución en la longitud de onda máxima de absorción del componente monomérico de MC540 en fase lipídica de protoplastos de rucula, en función de la concentración de sacarosa
El incremento en la curvatura de los protoplastos más pequeños y la mayor densidad superficial de fosfolípidos provocado por la osmolaridad, acrecentaron la polaridad superficial en la región por encima de 200 mosm/kg H2O de sacarosa, facilitando el acceso de las moléculas de agua debido a la pérdida de hidrofobicidad superficial. En este entorno, la afinidad del colorante por la superficie celular disminuye, acompañada por un desplazamiento hipsocrómico de la banda del monómero en la fase lipídica, similar al comportamiento observado en vesículas modelo (Willamson y Mattocks, 1983). Por otro lado, el área máxima correspondiente a la banda de absorbancia del monómero en membrana Figura 4 (IV) corresponde al desplazamiento máximo de la longitud de onda. Esto justifica la unión del monómero en la interfaz a medida que la superficie se vuelve más hidrófoba e indica el potencial de la sonda para evaluar la polaridad de los microambientes utilizando el desplazamiento en la longitud de onda de las especies monoméricas del colorante. En la Figura 6, se muestra que la ruptura celular se produce en osmolaridades por debajo de 175 mosm/kg H2O y se compara el efecto osmótico sobre el diámetro celular y la absorción del monómero en membrana.
El cambio espectral de la banda a 570 nm puede emplearse como indicativo de la unión preferencial del monómero a bicapas en fase expandida, donde la mayoría de las moléculas adquieren el espectro de absorción característico de las moléculas en un entorno hidrófobo. Los cambios en el empaquetamiento molecular de la bicapa son los responsables de la diferencia de afinidad del monómero de MC 540 con la superficie del protoplasto.
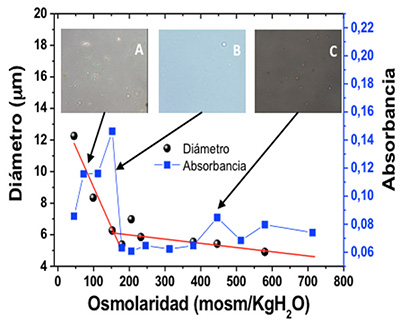
Figura 6
Efecto osmótico sobre el diámetro y la absorbancia de protoplastos de rúcula
Fotografía en 40X de protoplastos en solución de sacarosa (A) 49.5, (B) 155 y (C) 446 mosm / kg H2O
DISCUSION
Se encontró que los efectos del estrés osmótico modificaron las propiedades de superficie de los protoplastos de rúcula. El aumento de la sacarosa externa produjo, como es conocido, una disminución del diámetro del protoplasto. Sin embargo, en estas condiciones se detectaron dos estadíos en la salida de agua desde el interior celular, lo cual indicaría la presencia de dos poblaciones diferentes de agua asociados a la membrana. La señal máxima de MC540 se detectó en el punto de inflexión del diámetro frente a la concentración, indicando cambios en la superficie celular en respuesta al estrés osmótico.
La expansión lipídica, similar a la observada en la transición de fase, puede ser causada por cambios en la osmolaridad del medio al que están sujetos los protoplastos, siendo el principal determinante de la interacción entre la bicapa y MC540 el estado de empaque inducido por ósmosis. Los experimentos realizados proporcionan información sobre la relación entre el empaquetamiento de los lípidos y la polaridad de la superficie celular, que se incrementa con la disminución del volumen celular. El empaquetamiento puede producir cambios topológicos y deshidratación parcial en la célula. Esto podría estar relacionado con la formación de dominios en la membrana plasmática, que Merocyanine 540 detecta en una gran variedad de células. Este estudio enfatiza la importancia de las posibles funciones de los dominios lipídicos en la fisiología de las células vegetales. Y cómo, en condiciones de estrés, podrían proporcionar las condiciones fisicoquímicas favorables para desencadenar múltiples procesos de señalización.
De esta forma se podría utilizar la información obtenida con el objetivo de enviar y dirigir compuestos que retarden el envejecimiento a la superficie celular.
Conclusiones
Los resultados obtenidos empleando protoplastos como un sistema modelo y utilizando técnicas espectroscópicas simples, proporcionan información de interés para proyectos de investigación aplicada en poscosecha y para estudios de fisiología de vegetal. De esta forma se podría relacionar la evolución de diferentes estadios postcosecha, observados macroscópicamente en la rúcula, con cambios internos a nivel celular.
Por medio de las metodologías aplicadas sería posible comprender mejor los procesos involucrados a nivel de membrana celular, relacionándolos con los cambios macroscópicos, ampliando así las herramientas tecnológicas para el control de los procesos que afectan la calidad poscosecha de hortalizas.
Referencias
Bernik DL, Disalvo E (1996) Determination of the dimerization constant of merocyanine 540 at the membrane interface of lipid vesicles in the gel state. Chemistry and Physics of Lipids 82: 111-123.
Cunderlíková B, Sikurová L (2001) Solvent effects on photophysical properties of merocyanine 540. Chemical Physics 263: 415-422.
Cutro AC, Disalvo E (2015) Phenylalanine Blocks Defects Induced in Gel Lipid Membranes by Osmotic Stress. The journal of physical chemistry B 119: 10060-10065.
Disalvo EA, Hollmann A, Semorile L, Martini MF (2013) Evaluation of the Defay-Prigogine model for the membrane interphase in relation to biological response in membrane-protein interactions. Biochimica et biophysica acta 1834-1839.
Kaschny P, Goñi F (1992) The components of merocyanine-540 absorption spectra in aqueous and bilayer environments. Eur J Biochem 207: 1085-1091.
Lelkes PI, Miller IJ (1980) Perturbations of membrane structure by optical probes: I. Location and structural sensitivity of merocyanine 540 bound to phospholipid membranes. Membrane Biol 52: 1-15.
Mateasik A, Sikurová L, Chorvat D (2002) Interaction of merocyanine 540 with charged membranes. Bioelectrochem 55: 173- 175.
Mezzetti B, Zimmerman RH, Mischke C, Rosati P, Hammerschlag F (1992) Merocyanine 540 as an optical probe to monitor the effects of culture filtrates of Phytophthora cactorum on apple cell membranes. Plant Science 83: 163-167.
Munemasa S, Hauser F, Park J, Waadt R, Brandt B, et al. (2015) Mechanisms of abscisic acid-mediated control of stomatal aperture. Curr Opin Plant Biol 28: 154-162.
Ohshima Y, Iwasaki I, Suga S, Murakami M, Inoue K, et al. (2001) Low Aquaporin Content and Low Osmotic Water Permeability of the Plasma and Vacuolar Membranes of a CAM Plant Graptopetalum paraguayense: Comparison with Radish Plant Cell Physiol 42: 1119-1129.
Reyes LF, Villarreal JE, Zevallos LC (2007) The increase in antioxidant capacity after wounding depends on the type of fruit or vegetable tissue. Food Chem 101: B1254-1262.
Willamson P, Mattocks KR (1983) Merocyanine 540, a fluorescent probe sensitive to lipid packing. Schlegel, Biochimica et biophysica acta 732: 387-393.
Zhu JK (2016) Abiotic Stress Signaling and Responses in Plants. Cell 167: 313-324.
Notas de autor
ICyTA-FAyA-UNSE. Av. Belgrano (S) 1912, Santiago del Estero. Argentina.
Autora de correspondencia: S. del C. Rodríguez. E-mail: silviadepece@hotmail.com
