Reportes Frutas
Efecto de la aplicación exógena de etileno en el metabolismo de pulpa y cáscara de plátano
Effect of exogenous ethylene application on banana pulp and peel metabolism
Efecto de la aplicación exógena de etileno en el metabolismo de pulpa y cáscara de plátano
Revista Iberoamericana de Tecnología Postcosecha, vol. 20, núm. 2, 2019
Asociación Iberoamericana de Tecnología Postcosecha, S.C.
Recepción: 02 Octubre 2019
Aprobación: 22 Noviembre 2019
Publicación: 15 Diciembre 2019
Resumen: Etileno exógeno (1 µmol/mol) fue aplicado en frutos de plátano durante 24 h. Se evaluó el efecto de este compuesto tanto en cáscara como en pulpa de plátanos con madurez comercial. Los resultados se compararon con frutos testigo que no recibieron una incubación con etileno. Las variables analizadas fueron la tasa respiratoria, producción de etileno, α y β caroteno y carbohidratos tanto en cáscara como en pulpa de plátano. Después de 24 h, los frutos tratados mantuvieron la tasa respiratoria (12.89 mL CO2/kg.h) y se incrementó 3 veces el etileno endógeno (2.51 µL/kg.h). Esto no afectó el contenido de α y β-caroteno de la cáscara y la pulpa del fruto. Aunque en cáscara hubo una reducción del 31 % en glucosa, del 37 % en fructosa y del 44.7 % en sacarosa, en la pulpa no hubo un cambio significativo. Estos resultados pueden ayudar a comprender mejor los efectos del estrés producido por etileno en frutos climatéricos como el plátano, el cuál normalmente es mantenido junto a otras fuentes que generan este gas.
Palabras clave: condición de estrés, carotenoides, tasa respiratoria.
Abstract: Exogenous ethylene (1 µmol/mol) was applied to banana fruits for 24 h. The effect of this compound in both peel and banana pulp with commercial maturity was evaluated. The results were compared with control fruits that did not receive an incubation with ethylene. The variables analyzed were respiratory rate, production of ethylene, α and β carotene and carbohydrates both in peel and in banana pulp. After 24 h, the treated fruits maintained the respiratory rate (12.89 mL CO2/kg.h) and endogenous ethylene was increased 3 times (2.51 µL/kg.h). This does not affect the α and β-carotene content of the skin and pulp of the fruit. Although in shell there was a 31% reduction in glucose, 37% in fructose and 44.7% in sucrose, in the pulp there was no significant change. These results can help to better understand the effects of stress produced by ethylene in climatic fruits such as bananas, which are normally maintained together with other sources that generate this gas.
Keywords: stress conditions, carotenoids, respiratory rate.
Introducción
Los plátanos son cultivados en más de 120 países alrededor del mundo, representando una importante fuente de carbohidratos. En México, la producción de plátano alcanzó alrededor de 2.3 millones de toneladas durante el último año, indicando un aumento del 21 % a partir de la última década (SIAP, 2018). Al ser una fruta climatérica, se cosecha durante su madurez fisiológica y se transporta a su destino en donde generalmente se induce su maduración con la aplicación de etileno bajo condiciones controladas (García et al., 2007). El etileno es una hormona natural que se comercializa en distintas presentaciones pudiendo ser aplicada en solución acuosa -por inmersión o aspersión- o gaseosa en etapa postcosecha para acelerar la maduración de los frutos (Coro-Haro, 2017). El impacto que genera dicha hormona ha sido foco de numerosos estudios ya que la exposición de etileno, aún a bajas concentraciones, da inicio a una cascada de señalizaciones metabólicas responsables de cambios en el color, valor nutricional, compuestos volátiles, tasa respiratoria, modificación del almidón en azúcares, entre otros (Nordey et al., 2016; Golden et al., 2014; Xiao et al., 2013). Se ha demostrado que el uso de etefón y etileno exógeno aplicado en frutos tiene como resultado una adecuada maduración conservando un color uniforme, firmeza deseable y calidad aceptable (Dhall y Singh, 2013). Por otro lado, Scriven et al. (1989) evaluaron las características organolépticas de plátanos con maduración inducida por etileno y concluyeron que tanto en la pulpa como en la cáscara se aceleró su maduración, sin embargo, en la pulpa era más evidente. Dado que la mayoría de los plátanos son madurados bajo este procedimiento, es de gran importancia conocer las modificaciones que se presentan a nivel fisicoquímico al ser expuestos a dichas atmosferas. Por ello, el objetivo de la presente investigación fue evaluar los cambios en la tasa respiratoria, el contenido de carbohidratos y carotenoides en cáscara y pulpa de plátano por efecto de la aplicación de etileno exógeno.
Materiales y métodos
Material vegetal
Se utilizaron frutos de plátano “Cavendish” clase 1 del productor Coliman®, cosechados en la zona costera del estado de Colima. Los frutos se obtuvieron de un mercado local, localizado en Hermosillo, Sonora, México. En la muestra, se tomaron dos racimos de plátanos al azar pero que no presentaran lesiones, en estado de madurez comercial y de tamaño homogéneo. Se tomaron plátanos del mismo racimo para reducir la variabilidad.
Aplicación de etileno
Se pesó y determinó el volumen de los frutos, posteriormente fueron etiquetados dos de ellos como plátano 1 y otros como 2. Los plátanos marcados como 2 se colocaron en recipientes de 4085 mL. En seguida, se le inyectaron 10 mL de un patrón estándar de etileno de 1 ppm (1 µmol/mol, PRAXAIR, MEX) y se incubaron durante 24 h a una temperatura de 25 ºC (TA). Los plátanos marcados como 1 no se les aplicó etileno y se usaron como testigo.
Producción de CO2 y etileno
Los gases de CO2 y C2H4 fueron determinados con el método descrito por Watada y Massie (1981), con algunas modificaciones. Los gases producidos se evaluaron antes y después del tratamiento con etileno. Se extrajo 1 mL de gas del espacio de cabeza y se inyectó a un cromatógrafo de gases Star 3400CX (VARIAN, AUS) equipado con un detector de conductividad térmica (TCD) acoplado a uno de ionización de flama (FID). Se utilizó una columna metálica de 2 m de largo y 1/8” de diámetro interno, empacada con Hayesep N 80/100 (SUPELCO, USA). Los valores se reportaron como mL CO2 y µL C2H4/kg.h.
Alfa y beta carotenos
Se obtuvieron dos muestras de cáscara y pulpa de cada plátano. Para el caso de la cáscara, previamente se le retiró cuidadosamente la pulpa. Posteriormente, todas las muestras se liofilizaron. El polvo se utilizó para los análisis posteriores tanto de cáscara como de pulpa. La cuantificación de alfa y beta carotenos en las muestras de plátano se llevaron a cabo por el protocolo de Riso y Porrini (1997), con algunas modificaciones. Se pesaron 0.5 g del polvo liofilizado a los cuales se les agregó 5 mL de metanol y enseguida se homogenizó en un agitador VORTEXER II (VWR, USA). La solución se incubó a TA durante 1 h en agitación. Se centrifugó la solución a 3500 rpm a 4 ºC por 10 min. El sobrenadante metanol se transfirió a un matraz de 25 mL. Al precipitado se le realizaron dos extracciones con 5 mL de Tetrahidrofurano (THF, SIGMA-ALDRICH, USA) en cada ocasión y se centrifugó en las mismas condiciones que el metanol. El sobrenadante resultante se agregó al matraz de 25 mL que contenía el metanol. Este se aforó a 25 mL con THF. 5 mL de la solución fueron secados con un sistema a base de N2 en un baño de agua a 40 ºC. Los carotenos se resuspendieron con 500 µL de etanol, posteriormente se filtró con Acrodisc de 13 mm y 0.2 µm de Nylon para inyectarse en el cromatógrafo. Se utilizó un Agilent Technologies 1260 equipado con un detector de arreglo de diodos y un sistema de inyección automatizado. La fase móvil consistió en acetonitrilo-metanol-THF en una proporción 58-35-7 % respectivamente. La columna usada fue una Microsorb 100-3 C18 100x4.6 mm acoplada a una precolumna zorbax SB-C18 4.6x12.5 mm 5-Micron. El flujo fue de 1 mL/min y la solución estándar consistió en una mezcla de alfa y beta caroteno grado reactivo a una concentración de 2 y 4 µg/mL, respectivamente. Los resultados se expresaron en µg de α o β caroteno por cada 100 g de peso seco.
Carbohidratos
Se utilizó la metodología propuesta por Arenas et al. (1995), con modificaciones. Duplicados de pulpa y cáscara del tejido previamente liofilizado, fueron pulverizados en un mortero. Se pesó aproximadamente 1g para la pulpa y 0.2 g para cáscara, se les adicionó un volumen de etanol–agua [80:20], y se dejó macerar durante toda la noche a temperatura ambiente (20-25 °C). Finalmente, se tomó con una jeringa un volumen pequeño del sobrenadante el cual fue filtrado a través de una membrana Nylon de 0.2 µm. La muestra se inyectó a un cromatógrafo de líquidos UltiMate 3000 (Thermoscientific, USA), acoplado a un detector de índice de refracción (ERC RefractoMax 520). Se utilizó una columna Microsorb 100-3 NH2 100 х 4.6 mm. La separación de los azúcares se realizó a 35 ºC a flujo isocrático de 1.0 mL/min con acetronitrilo-agua [80:20]. La caracterización y cuantificación de los carbohidratos presentes en las muestras se realizó mediante la comparación de los tiempos de retención y las áreas bajo la curva de los picos de estándares de fructuosa, glucosa y sacarosa (SIGMA-ALDRICH, St. Louis, Mo, USA). Los resultados se expresaron como g de carbohidratos por cada 100 g de peso seco.
Diseño experimental
El diseño fue completamente al azar, en un ANOVA de una sola vía con una confiabilidad del 95 %. Las diferencias se analizaron por el método de Tukey-Kramer empleando el paquete estadístico NCSS versión 2011.
Resultados y discusión
Producción de CO2 y etileno
El comportamiento de la tasa respiratoria (CO2) de ambas muestras antes de ser sometidas al tratamiento presentaron valores semejantes de 13.89 y 14.02 mL/kg.h (Figura 1A). Pasadas las 24 h, se observó una disminución de la tasa respiratoria de 8.64 mL/kg.h para el testigo, mientras que el plátano tratado presentó un valor de 12.89 mL/kg.h. La respuesta del fruto tratado aparenta una actividad metabólica más estable, quizás promovida por el exceso de etileno. Por su parte, Belew et al. (2016), al aplicar tabletas liberadoras de etileno en plátanos observaron una disminución de la respiración tanto en frutos tratados y el testigo. Mientras que Liu et al. (2004), reportaron un aumento 12.9 a 62.9 mL CO2/kg.h. Es claro que el comportamiento varía, entre otras cosas, por el estado de madurez o variedad usada, y que, en el patrón respiratorio de los frutos climatéricos al haber alcanzado su máxima producción, tiende a disminuir al acercarse la senescencia. En el caso de la muestra tratada con etileno se observó que 1 ppm fue suficiente para que el fruto manifestará un incremento de 0.66 a 2.51 µL/kg.h después de 24 h (Figura 1B). Estudios previos indican que la aplicación exógena de etileno promueve un aumento en la síntesis de etileno endógeno (Liu et al., 1999). Los valores de etileno en los frutos testigo se mantuvieron muy similar (0.89 a 0.80 µL/kg.h). Esto concuerdan con lo que reportan Liu et al. (2004), observando que la producción de etileno aumentó de 0.1 a 0.9 mL/kg.h en frutos expuestos a etileno durante 24 h.
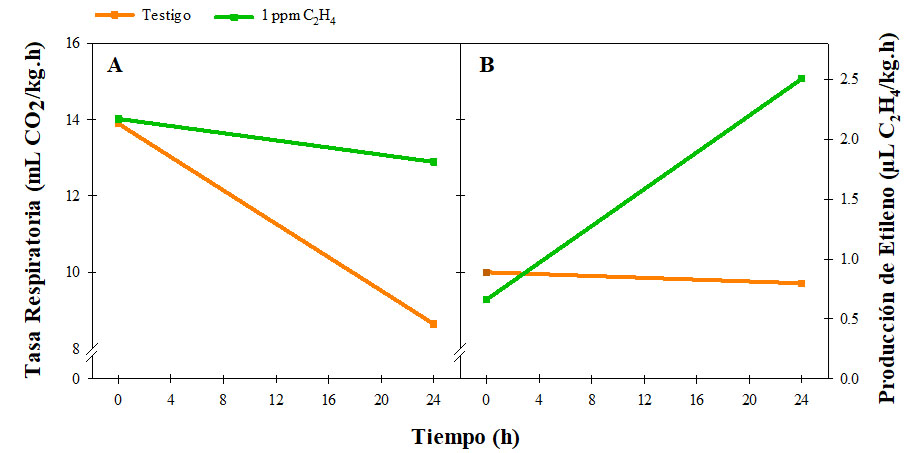
Figura 1
Tasa respiratoria (A) y producción de etileno (B) de frutos de plátano testigo y tratados con 1 ppm de etileno a las 0 y 24 h a 25 °C.
Alfa y beta carotenos
La incubación con exceso de etileno por 24 h en los plátanos no afectó (p≤0.05) la respuesta, tanto en cáscara como en pulpa, del contenido de carotenos (Tabla 1). Es probable que, a pesar de que el etileno exógeno propició un aumento en la respiración, los cambios metabólicos en los carotenos ya habían sucedido dada la madurez del fruto. Sin embargo, resultó interesante notar las diferencias del contenido de carotenos entre cáscara y pulpa. Hubo una diferencia cercana a 22 veces más α-caroteno en la cáscara que en la pulpa, mientras que de β-caroteno la diferencia fue cercana a 51 veces. Ambas moléculas son importantes antioxidantes y en la mayoría de los frutos se encuentran presentes precisamente en la cáscara (Huang, Tanudjaja y Lum, 1999).
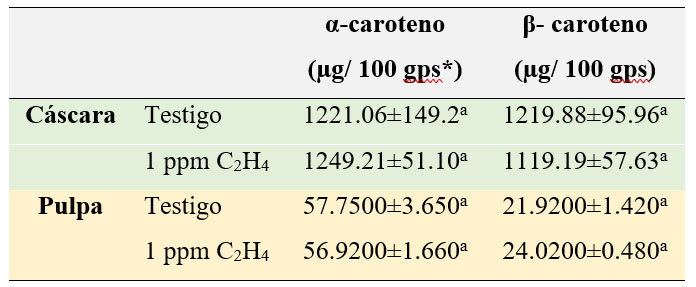
* gramos de peso seco. Media ± desviación estándar de tres muestras. Letras distintas entre testigo y tratamiento presentan diferencias estadísticas.
Aquino et al. (2018), cuantificaron α y β-carotenos en distintas variedades de plátano y mencionan que la cantidad puede variar ya sea por su estado de madurez o la variedad. En la variedad “Prata” reportaron valores entre 58 y 61 µg en pulpa, pero bajas cantidades en cáscara.
Carbohidratos
Los valores de glucosa y fructosa, tanto en cáscara como en pulpa, rondaron entre los 10 y 15 g/100 gps (Tabla 2). No obstante, se encontraron diferencias significativas de estos azúcares en los frutos testigo con valores mayores tanto para cáscara y pulpa.
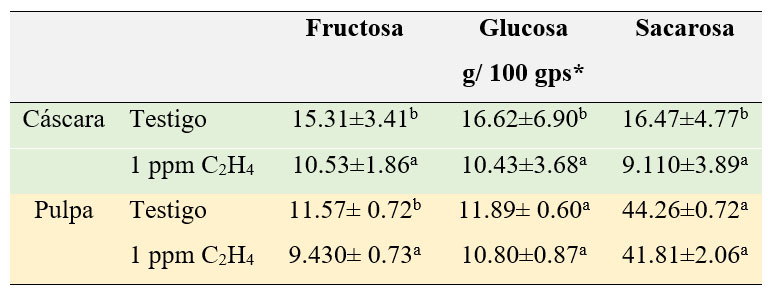
* gramos de peso seco. Media ± desviación estándar de tres muestras. Letras distintas entre testigo y tratamiento presentan diferencias estadísticas.
La presencia de mayor cantidad de azúcares se puede deber al desdoblamiento como parte del proceso de senescencia de los frutos (Yap et al., 2017) y que, en este caso, se manifestó más en los testigos. No se observaron diferencias (p≥0.05) entre la glucosa de la pulpa de testigo y los frutos tratados. Con respecto a sacarosa en cáscara, también se presentaron diferencias entre los plátanos testigo (16.47 g/ 100 gps) y los tratados (9.11 g/ 100 gps), pero no hubo diferencias en la pulpa. Aun así, el contenido de sacarosa resultó 3.4 veces más alto en pulpa que en cáscara con valores entre 41 y 44 g/100 gps. Lizana (1976) reportó valores de sacarosa cercanos a 30 g/100 gps en plátano tratado con 10 ppm durante 24 h y evaluado a los 6 días a 20 °C, coincidiendo con el pico máximo de producción de CO2. En general, los resultados anteriores nos llevan a suponer que la aplicación de etileno durante 24 h en plátano comercialmente maduro, no afecta la concentración de los azúcares en pulpa. García et al. (2007) aplicaron diferentes dosis de etileno (etefón) en plátano, sin embargo, no encontraron diferencias significativas en las variables evaluadas como la pérdida de peso, resistencia al corte, solidos solubles totales y acidez titulable. Los resultados indican que una fuente externa de etileno puede aumentar la producción endógena del plátano, aparentemente sin afectar algunos componentes de la pulpa. No obstante, se potencia la posibilidad de que este mismo fruto influya en la fisiología de otros, socavando su vida de anaquel.
Conclusión
El estrés por etileno exógeno en plátano comercialmente maduro, mantiene la tasa respiratoria y eleva el etileno endógeno sin afectar los antioxidantes y azúcares evaluados en la pulpa.
Referencias
Aquino, C. F., Salomão, L. C. C., Pinheiro-Sant’ana, H. M., Ribeiro, S. M. R., De Siqueira, D. L. y Cecon, P. R. 2018. Carotenoids in the pulp and peel of bananas from 15 cultivars in two ripening stages. Revista Ceres, 65(3): 217–226.
Arenas, M. L., Marín, M., Castro, C. R. y Sandoval, L. 1995. Determinación por HPLC de los azúcares en los frutos de guayaba (Psidium guajava L.) de una plantación comercial del Municipio Mara. Rev. Fac. Agron. (LUZ). 12: 467-483.
Belew, D., Park, D., Tilahun, S. y Jeong, Ch. 2016. The Effects of treatment with ethylene-producing tablets on the quality and storability of banana (Musa sp.). Wonye kwahak kisulchi, Korean J. Hortic. Sci. Technol., 34(5): 746–754.
Coro-Haro, M. E. 2017. Evaluación del etileno como agente madurador en babaco (Vasconcellea x heilbornii var. pentagona). Tumbaco-Ecuador. Tesis, UCE, Quito. 70 p. Obtenido en: http://www.dspace.uce.edu.ec/bitstream/25000/10016/1/T-UCE-0004-19.pdf
Dhall, R. K., y Singh, P. 2013. Effect of ethephon and ethylene gas on ripening and quality of tomato (Solanum lycopersicum L.) during cold storage. J Nutr Food Sci, 3(6): 244. doi: 10.4172/2155-9600.1000244.
García, T., Chaparro, L., Durán, L., Ávila, E. y Barrios, B. 2007. Efecto del etefón (ethrel) y el tiempo de almacenamiento sobre la maduración del plátano (Musa ABB cv. Harton) bajo refrigeración. Bioagro, 19(2): 91–98.
Golden, K. D., Williams, O. J. y Dunkley, H. M. 2014. Ethylene in Postharvest Technology: A Review. Asian Journal of Biological Sciences, 7: 135–143.
Huang, A. S., Tanudjaja, L. y Lum, D. 1999. Content of Alpha-, Beta- Carotene, and Dietary Fiber in 18 Sweetpotato Varieties Grown in Hawaii. Journal of Food Composition and Analysis, 12(2): 147–151.
Liu, S., Yang, Y., Murayama, H., Taira, S. y Fukushima, T. 2004. Effects of CO2 on respiratory metabolism in ripening banana fruit. Postharvest Biology and Technology, 33(1): 27–34.
Liu, X., Shiomi, S., Nakatsuka, A., Kubo, Y., Nakamura, R., y Inaba, A. 1999. Characterization of ethylene biosynthesis associated with ripening in banana fruit. Plant physiology, 121(4): 1257–1265.
Lizana, L. A. 1976. Quantitative evolution of sugars in banana fruit ripening at normal to elevated temperatures. Acta Horticulturae, (57): 163–178. doi:10.17660/actahortic.1976.57.20
Nordey, T., Léchaudel, M., Génard, M. y Joas, J. 2016. Factors affecting ethylene and carbon dioxide concentrations during ripening: Incidence on final dry matter, total soluble solids content and acidity of mango fruit. Journal of plant physiology, 196-197: 70–78.
Riso P. y Porrini M. 1997. Determination of carotenoids in vegetable foods and plasma. Int J Vitam Nutr Res, 67(1):47–54.
Scriven, F. M., Gek, C. O. y Wills, R. B. H. 1989. Sensory differences between bananas ripened without and with ethylene. HortScience, 24: 983–984.
SIAP. 2018. Servicio de Información Agroalimentaria y Pesquera. Disponible en: https://nube.siap.gob.mx/cierreagricola/
Watada A. y Massie D. 1981. A compact automatic system for measuring CO2 and C2H4 evolution by harvest horticultural crops. HortScience 16:39– 41.
Xiao, Y. Y., Chen, J. Y., Kuang, J. F., Shan, W., Xie, H., Jiang, Y. M. y Lu, W. J. 2013. Banana ethylene response factors are involved in fruit ripening through their interactions with ethylene biosynthesis genes. Journal of experimental botany, 64(8): 2499–2510.
Yap, M., Fernando, W. M., Brennan, C. S., Jayasena, V. y Coorey, R. 2017. The effects of banana ripeness on quality indices for puree production. LWT-Food Science and Technology, 80: 10–18.
Notas de autor
Correo electrónico de autor para correspondencia: otortoledo@ciad.mx.