Reportes Frutas
Evaluación fisicoquímica y antioxidante de naranjilla (Solanum quitoense Lam.) durante la maduración
Physicochemical and antioxidant evaluation of naranjilla (Solanum quitoense Lam.) during maturation
Evaluación fisicoquímica y antioxidante de naranjilla (Solanum quitoense Lam.) durante la maduración
Revista Iberoamericana de Tecnología Postcosecha, vol. 22, núm. 2, 2021
Asociación Iberoamericana de Tecnología Postcosecha, S.C.
Recepción: 12 Julio 2021
Aprobación: 18 Noviembre 2021
Publicación: 31 Diciembre 2021
Resumen: En semillas, tejidos placentarios y piel de la fruta de naranjilla (Solanumquitoense) cosechada en cinco grados de madurez (GM) se analizaron: tasa respiratoria (TR), vitamina C, color superficial (L*, a*, b*, Cr y °H), distribución de clorofila, carotenoides, azúcares totales, compuestos fenólicos y capacidad antioxidante. La TR y vitamina C se incrementan mientras avanza la maduración alcanzando los mayores valores en los GM 5, y 4 y 5, respectivamente. Por otro lado, el color verde de los GM 1, 2 y 3 está relacionado con altos contenidos de clorofila. El color amarillo de los GM 4 y 5 se relaciona con un incremento de carotenoides (pigmento amarillo/naranja) y disminución de clorofila. El análisis de azúcares reductores y compuestos fenólicos en semillas, tejidos placentarios y piel del fruto permitió comprobar que la piel es la zona del fruto en el que se presentan mayoritariamente estos compuestos, seguida de los tejidos placentarios y semillas, y que también aumentan durante la maduración. La capacidad antioxidante aumenta durante la maduración siendo diferente en las tres zonas del fruto. Los tejidos placentarios presentaron mayor capacidad antioxidante, seguidos de la piel y semillas. Siendo la piel y semillas subproductos agroindustriales, es importante conocer su composición con el fin de buscar una aplicación que permita su aprovechamiento, por ejemplo, en el desarrollo de nuevos productos alimenticios.
Palabras clave: carotenoides, color, estados de madurez, fenoles totales, vitamina C.
Abstract: The following parameters were analyzed in naranjilla (Solanum quitoense) harvested at five maturity index (MI): respiratory rate (TR), vitamin C, surface color (L*, a*, b*, Cr and °H), chlorophyll distribution, carotenoids, total sugars, phenolic compounds and antioxidant capacity in seeds, placental tissues and fruit skin. TR and vitamin C increase as maturation progresses reaching the highest values in MD 5, and 4 and 5, respectively. On the other hand, the green color of MD 1, 2 and 3 is related to high chlorophyll content. The yellow color of MD 4 and 5 is related to an increase in carotenoids (yellow / orange pigment) and a decrease in chlorophyll. The analysis of reducing sugars and phenolic compounds in seeds, placental tissues and skin of the fruit, allowed to verify that the skin is the part of the fruit in which these compounds are mainly located, followed by placental tissues and seeds, and that they also increase during the maturation process. The antioxidant capacity increases during ripening, being different in the three areas of the fruit. Placental tissues have a greater antioxidant capacity, followed by skin and seeds. Because the skin and seeds are agro-industrial by-products, it is important to know their composition to find an application that allows their use, for example, in the development of new food products.
Keywords: carotenoids, color, maturity degrees, total phenols, vitamin C.
INTRODUCCIÓN
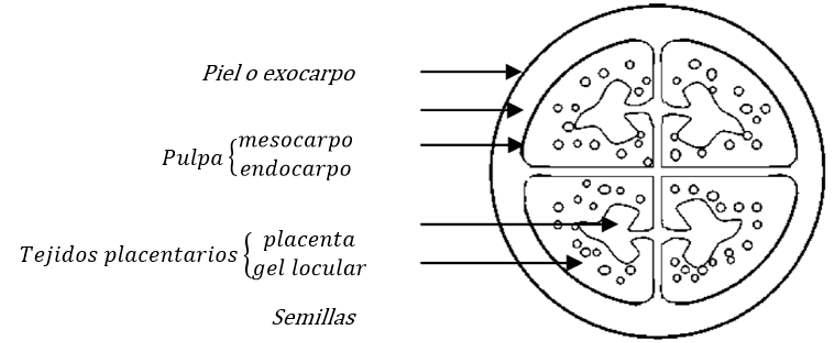
La naranjilla (Solanum quitoense Lam), también conocida como lulo, es una fruta (Solanaceae) cultivada en las regiones subtropicales de bosques húmedos situados a lo largo de la cordillera de los Andes en países como Ecuador, Colombia y Perú, además de países de América Central como Guatemala y Costa Rica (IICA, 2007). Su consumo en los últimos años ha aumentado debido a su atractivo de carácter exótico y sabor agridulce, además de tener un amplio potencial nutricional con la presencia de vitamina A, C, B1 y B2, proteínas y minerales; y en el sector industrial debido a su empleo en la fabricación pulpas, mermeladas, helados, jugo y néctares, entre otros y para fines medicinales (Forero et al., 2014a). La planta de la naranjilla es herbácea y de tallos robustos, pudiendo llegar a medir hasta 3 m de altura. El fruto, de color amarillo o naranja intenso en su grado de madurez más elevado, tiene forma redonda u ovoide y su estructura interna consta de cuatro compartimientos divididos por una membrana conocida como tejidos placentarios o pulpa. Cada compartimiento contiene pulpa verdosa y muy jugosa de característica cítrica y aromática, en la que se encuentran numerosas semillas planas y duras. El fruto, además, consta de una pubescencia o pelaje marrón que lo cubre hasta alcanzar completamente la madurez (ICA, 2011; Rojas, 2004; Valverde et al., 2010). En la figura 1 se muestra una sección transversal de la naranjilla en la que se aprecia su parecido con el tomate y se identifican las tres zonas comentadas: 1) la piel o exocarpo, 2) la pulpa compuesta de mesocarpo o endocarpo y 3) los tejidos placentarios que incluyen la placenta, gel locular y semillas (figura 1).
En Ecuador, la producción de naranjilla se concentra en diferentes provincias de la región amazónica y de la sierra (en los flancos de la cordillera andina). Durante muchos años se convirtió en la base económica de algunos pueblos, ya que la mayoría de sus agricultores utilizaba a la naranjilla como cultivo de iniciación por tratarse de un cultivo que da frutos durante todo el año (Rojas, 2004; Valverde et al., 2010). Posteriormente, el crecimiento en la demanda dio paso al aumento en la cantidad de sembríos. Sin embargo, este cultivo solo refleja mayor rendimiento en el primer ciclo de siembra.
Actualmente se comercializan diferentes variedades de naranjilla, entre las que destacan: Baeza agria, de aplicación industrial en la producción de refrescos o jugos y helados; Baeza dulce, que presenta una corteza más gruesa y por ello es más fácil de transportar y almacenar; e INIAP-Quitoense o Híbrida que se caracteriza por ser un cultivo de mayor rendimiento y mayor resistencia a las condiciones climáticas y a las plagas (Andrade-Cuvi et al., 2016). Según García y García (2001), la naranjilla es un fruto de carácter climatérico que presenta diferentes etapas durante su formación y crecimiento hasta alcanzar la madurez fisiológica. Sin embargo, debido a su alta intensidad respiratoria este fruto puede ser separado de la planta sin la necesidad del desarrollo completo. Estas condiciones metabólicas unidas a la concentración de etileno permiten que la naranjilla siga respirando y consumiendo metabolitos producidos durante la fotosíntesis, tales como azúcares y ácidos orgánicos (Ochoa et al., 2016). Producto de esta transformación se generan compuestos aromáticos, azúcares simples y compuestos antioxidantes que dotan a la naranjilla de unas características propias, además de liberar ATP, energía en forma de calor, CO2 y agua, lo que influye directamente en la pérdida de peso y deterioro del fruto convirtiéndolo en un producto perecible (Ochoa et al., 2016; Ramírez et al., 2018).
Entre los cambios que experimenta la naranjilla durante la maduración, el color es uno de los más importantes, empleándose como criterio de evaluación tanto para su cosecha como para su posterior consumo (Andrade-Cuvi et al., 2019). Estos cambios de color se deben fundamentalmente a la degradación de la clorofila por sistemas enzimáticos que llevan a la generación de carotenoides (Conesa et al., 2019). Estas sustancias juegan un papel importante en la calidad de frutas y vegetales y tanto la calidad nutricional y funcional de estos pigmentos se relaciona directamente con el grado de madurez, observándose una variación en su concentración durante el proceso de maduración (Mejía et al., 2012).
Además de con el grado de madurez, la distribución de los compuestos bioactivos en el fruto varía en función de las diferentes estructuras o partes del fruto consideradas. Según Gancel at al. (2008), la industria alimentaria no reconoce el valor nutricional rico en β-carotenos y fenoles presentes en los desechos como piel y semillas de frutos como la naranjilla, tomando en cuenta solo el aporte dado por la pulpa. Sin embargo, debido a la importancia de estos compuestos bioactivos para la salud, las investigaciones se han centrado en determinar el contenido de estos compuestos en diferentes frutos de comportamiento climatérico y en evaluar cómo su contenido se puede ver afectado en relación con la variedad, el grado de madurez o las condiciones de cultivo, entre otras variables. Estos estudios se llevan a cabo por la necesidad de la industria alimentaria de satisfacer las demandas actuales de la población, como el consumo de productos naturales y saludables (Valenzuela & Pérez, 2016) o encontrar nuevas fuentes de extracción de compuestos funcionales que puedan ser incorporados en formulaciones de alimentos y preservar las características sensoriales y de calidad de sus productos, otorgando valor agregado de forma que se reemplace o reduzcan potenciales riesgos que involucran la utilización de antioxidantes artificiales (Lado Lindner, 2015).
Numerosos estudios han sido publicados acerca del contenido de compuestos fenólicos, carotenos y vitaminas antioxidantes en diversas frutas y hortalizas. Según Gancel et al. (2008), estas moléculas son metabolitos esenciales para el desarrollo temprano de las plantas y actúan como reductores atrapando radicales libres previniendo para prevenir el daño celular. Es sabido que una dieta rica en frutos verdes, rojos y naranjas puede reducir directamente el riesgo de padecer algunas formas de cáncer o sufrir enfermedades cardiovasculares (Jáuregui et al., 2007). Los compuestos carotenoides son reconocidos por su carácter antioxidante liposoluble y estructura provitamina A, es decir, este compuesto ingresa al organismo como β-caroteno y en la mucosa intestinal es transformado en vitamina A (Bertram & Bortkiewicz, 1995).
Es importante conocer cómo varía el contenido de compuestos antioxidantes en la naranjilla durante la maduración, tanto en las semillas como en los tejidos placentarios y en piel. El objetivo general de esta investigación fue determinar los cambios fisiológicos y antioxidantes que experimentan las diferentes partes del fruto de naranjilla (S. quitoense) durante la maduración.
MATERIALES Y MÉTODOS
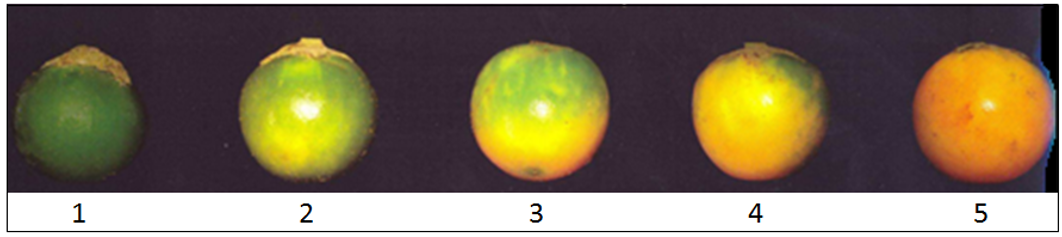
Material vegetal: La naranjilla (Solanum quitoense) fue cosechada en la provincia de Pichincha, cantón de San Miguel de los Bancos (00°01'23"N, 78°53'31"O) y seleccionada por ausencia de defectos de acuerdo con los grados de madurez (GM) entre 1 y 5 como se observa en la figura 2 (NTE INEN 2303, 2009). El trabajo experimental se llevó a cabo en el Centro de Investigación de Alimentos (CIAL), Facultad de Ciencias de la Ingeniería e Industrias, Universidad UTE (Quito, Ecuador).
Una vez seleccionados los frutos, se limpiaron y se dividieron en dos grupos: frutos enteros utilizados para determinar la tasa de respiraciónµ, el ácido ascórbico y el color; frutos procesados de los que se obtuvieron las tres partes (1) piel (exocarpo), (2) pulpa y tejidos placentarios (incluidos la placenta y el gel locular) y (3) semillas, cada una de las cuales fue congelada con nitrógeno líquido para su posterior análisis bioquímico. Para la determinación de la materia seca (expresado como base seca -b.s.-), se tomaron muestras frescas de cada zona del fruto, se pesaron y se sometieron a secado por convección a 65 °C por 24 h, de acuerdo con el método de Almanza Merchán (2016).
Tasa de respiración (TR): Se utilizó el método de atmósfera confinada. Para cada grado de madurez, tres o cuatro naranjillas fueron colocadas en envases herméticos de 2,6 L. Se empleó un medidor de gases Meter Vitrio GC-2028 con el que se obtuvieron registros de la concentración CO2 (%) en el espacio de cabeza al inicio y después de 60 min a temperatura ambiente (Forero et al., 2014b). Los resultados se expresaron como mgCO2/kg*h.
Determinación de vitamina C: La vitamina C se puede determinar por métodos espectrofotométricos, enzimáticos y cromatográficos; la AOAC (Association of Official Analytical Chemists) emplea la titulación como método oficial (Pertuzatti et al., 2015). En esta investigaicón se empleó el método de la AOAC (1990). Para ello se preparó una disolución de 2,6-dicloroindofenol al 0,04% que se estandarizó con una solución patrón de ácido ascórbico al 0,02% para determinar la cantidad de volumen en función de la cantidad de ácido ascórbico presente en la disolución. Por otro lado, se extrajeron 10 mL de extracto líquido de naranjilla para cada uno de los GM analizados. El extracto se filtró con un lienzo y al filtrado se le agregaron 50 mL de ácido oxálico al 1 % previamente a su titulación con el reactivo 2,6-dicloroindofenol estandarizado, hasta viraje a color rosa pálido. Los resultados se expresaron en mg de vitamina C (ácido ascórbico) por 100 ml de filtrado.
Color superficial externo e interno: Se midió en forma aleatoria en seis naranjillas de cada uno de los cinco GM. Cada medida se tomó cuatro veces, tanto en la piel como en el interior (tejidos placentarios) de cada uno de los frutos. Para ello se utilizó un colorímetro Konica Minolta Chroma Meter CR400. Se tomaron medidas según la escala CIE L*a*b*, de luminosidad (L*) además de los descriptores cromáticos rojo/verde (a*) y amarillo/azul (b*). A partir de los cuales se calcularon el tono, matiz o longitud de onda dominante (°H) y el Croma como un indicador de la saturación o intensidad (INIA, 2007).
Determinación de clorofila y carotenoides: Se pesaron de 0,5 a 3,0 g de tejido congelado (de acuerdo con el GM y la parte del fruto -semilla, pulpa/tejidos placentarios y piel-) y se añadieron 15 mL de acetona al 80 %. Posteriormente la mezcla se mantuvo en agitación constante durante 24 horas en oscuridad. Transcurrido este tiempo, la fase líquida se filtró y se utilizó para las medidas espectrofotométricas. De acuerdo con el método de Wellburn (1994), se determinaron los contenidos de α-clorofila, β-clorofila, clorofila total y carotenoides, mediante las ecuaciones: clorofila α = {[(11,75·A662)-(2,35·A645))·ml acetona]/mg muestra}; clorofila β = {[(11,75·A645)-(2,35·A662))·ml acetona]/mg muestra}; clorofila total = (clorofila α + clorofila β); y carotenoides = {[(1000·A470)-(2,35·Cl α) – (81,4·Cl β)]/227}. Los resultados se expresaron como µg/g tejido en base seca (b.s.).
Azúcares reductores: Su contenido se determinó por espectrofotometría en condiciones similares a las descritas por Mejía et al. (2007). Se tomó 50 µL de muestra (extracto etanólico), se adicionó 75 µL de agua destilada y 500 µL de antrona al 0,05 % (preparada disolviendo 0,125 g de antrona en 100 mL de H2SO4), con lo que el volumen final de reacción fue de 625 µL. La mezcla de reacción se sometió a ebullición a un baño térmico durante 10 min e inmediatamente fue introducida en un baño de hielo para detener la reacción. Posteriormente se midió la absorbancia a 660 nm. Se realizó una curva de calibración con una disolución stock de glucosa (200 µg/mL) que abarcó un rango de 0 a 240 µg/mL con un R2 = 0,98). El análisis se realizó por triplicado. Los resultados se expresaron en µg de glucosa/g tejido en base seca (b.s.).
Determinación de fenoles totales (FT) y capacidad antioxidante:
- Preparación de extractos: Los extractos se prepararon con muestras congeladas en nitrógeno líquido. Durante todo el proceso de extracción la temperatura se mantuvo en torno a 4°C. Se colocó cada muestra (aproximadamente 2,5 gramos) en un tubo cónico agregando inmediatamente 10 mL de solvente (etanol) al 96 % y se homogenizó usando un agitador magnético. El homogenizado se centrifugó a 6000 rpm durante 15 min (Andrade-Cuvi et al., 2016). El sobrenadante fue recogido para posteriores análisis.
- Fenoles totales (FT): Se llevó a cabo mediante el método colorimétrico con el reactivo de Folin-Ciocalteau (Singleton, Rossi & Rossi, 1965) con ligeras modificaciones. A volúmenes entre 20 y 50 µL de muestra se agregaron 1200 µL de agua bidestilada y 100 µL de reactivo de Folin-Ciocalteau 1 N; después de 3 minutos se agregó 100 µL de una solución de Na2CO3 20 % (P/V) en NaOH 0,1N, completando con agua destilada un volumen final de reacción de 1550 µL. Después de un tiempo de reposo de 60 minutos en oscuridad, se realizaron medidas de absorbancia es un espectrofotómetro Thermo Spectronic, Genesys 20 a 760 nm. Se realizó una curva de calibración con una disolución stock de ácido gálico (250 µg/mL) que abarcó un rango de 0 a 1400 µg/mL con un R2 = 0,96. Las medidas se realizaron por triplicado y los resultados se expresan en µg de ácido gálico por gramo de tejido en base seca.
- Actividad antioxidante medida por el radical ABTS: Se determinó por espectrofotometría basándose en la decoloración del radical ABTS∙+ [2,2 'azinobis-(ácido3-etilbenzotiazolina-6-sulfónico], de acuerdo con la metodología de propuesta por Re et al. (1999). A 20 μL de extracto etanólico se añadió 1000 μL de la dilución del radical ABTS∙+, se homogenizó en un agitador vortex y se dejó reposar durante 6 min en oscuridad. Las lecturas se realizaron a 734 nm. Se preparó una curva de calibración usando trolox (6-hidroxi-2,5,7,8 tetrametilcromo-2 ácido carboxílico) 0,5 mM como antioxidante sintético de referencia, que abarcó un rango de 0 a 0,5 μmol trolox/μL con un R2= -0,99. El ensayo se realizó por triplicado los resultados se expresaron como μmol de trolox por gramo de tejido en base seca.
- Actividad antioxidante medida por el radical DPPH: Se determinó siguiendo la metodología propuesta por Moreno et al., (2014), a volúmenes entre 20 y 40 µL de extracto etanólico se añadió 1000 µL de la solución de DPPH disuelto en etanol (0,06 mM). La mezcla se homogenizó en un agitador vortex y se dejó reposar durante 30 min en oscuridad. Las lecturas se realizaron a 734 nm. Se preparó una curva de calibración usando trolox (6-hidroxi-2,5,7,8 tetrametilcromo-2 ácido carboxílico) 0,5 mM como antioxidante sintético de referencia, que abarcó un rango de 0 a 0,8 μmol trolox/μL con un R2= -0,99. El ensayo se realizó por triplicado los resultados se expresaron como μmol de trolox por gramo de tejido en base seca.
Diseño experimental y análisis estadístico:
Se aplicó un diseño completamente al azar. Las variables independientes fueron los grados de madurez y las zonas del fruto (piel, tejido placentario y semillas) y las variables dependientes fueron los análisis de color, tasa de respiración, vitamina C, además del contenido de clorofila, β-carotenos, azúcares totales, FT y la capacidad antioxidante. Los resultados se analizaron utilizando el paquete informático InfoStat versión 2010 (Grupo InfoStat, FCA, Universidad Nacional de Córdoba, Argentina) con un análisis de varianza (ADEVA) simple (tasa de respiración, vitamina C, color, clorofila, β-carotenos) y factorial AxB (azúcares totales, FT y capacidad antioxidante). Las medias fueron comparadas mediante la prueba LSD con un nivel de significancia de 0,05.
RESULTADOS Y DISCUSIÓN
Tasa de respiración. La tasa de respiración (TR) de la naranjilla en los diferentes grados de madurez se muestra en la figura 3. Se observa un incremento gradual en la TR a medida que avanza la maduración. El GM 1 presenta el mínimo valor de TR (2,77 mgCO2/kg∙h) que se incrementa en los GM 2, 3 y 4, entre los que no se encuentran diferencias significativas. La mayor TR se presenta en el GM 5 con un valor de 17,76 mgCO2/kg∙h, lo que indica que en este estado de desarrollo de la fruta se están llevando a cabo procesos de respiración (consumo de O2 y producción de CO2) con mayor intensidad que los demás GM, lo que además está relacionado con la síntesis adicional de etileno que a su vez contribuye en la aceleración del proceso de respiración conocido como pico climatérico (Almanza Merchán, 2016).
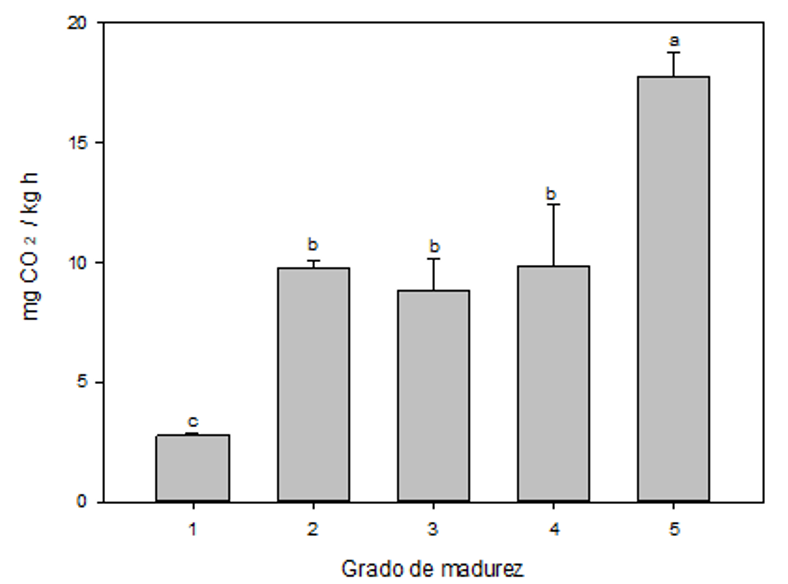
Figura 3
Tasa de respiración de naranjilla para los cinco grados de madurez considerados
* Letras diferentes indican diferencias significativas entre grados de madurez (p < 0,05)
La naranjilla se cosecha con una madurez comprendida entre el GM 4 y 5 (con un desarrollo de color amarillo del 75 al 100 %). La alta TR en la última etapa de madurez (GM 5) se debe posiblemente al activo crecimiento que presentan el exocarpo y el mesocarpo del fruto, que van de la mano con los cambios de coloración superficiales producidos por la degradación de clorofila y síntesis de carotenos. La hipótesis sobre la coloración en el exocarpo (piel) está basada en el transporte de carbohidratos, nitrógeno y hormonas del fruto, regulado por condiciones climáticas o de almacenamiento. La concentración de ácidos orgánicos durante el desarrollo desciende como consecuencia de la dilución, causada por la acumulación de agua y la respiración (Azcón-Bieto et al., 2013).
Determinación de vitamina C. El ácido ascórbico o vitamina C, es una vitamina de carácter hidrosoluble y termolábil. Está ampliamente distribuida en productos de origen vegetal principalmente vegetales de hoja verde y frutos cítricos. Se evalúa su contenido con la finalidad de buscar nuevas fuentes de esta vitamina cuyo consumo se asocia con el fortalecimiento del sistema inmune.
El contenido de vitamina C (mg/100 ml de filtrado) del fruto entero de naranjilla en función del GM se muestra en la figura 4. Se observa que a medida que progresa la maduración del fruto, se incrementa también su contenido en vitamina C. Entre el GM 1 (2,3 mg vitamina C/100 ml de filtrado) y el GM 4 (31,2 mg vitamina C/100 g ml de filtrado) se produce un incremento del 90 % de vitamina C que se mantiene más o menos constante hasta el grado de madurez 5 (no se encontró diferencias significativas entre los grados de madurez 4 y 5). Resultados similares han sido reportados por Acosta et al. (2009) y González et al. (2013) en naranjilla de diferentes grados de madurez.
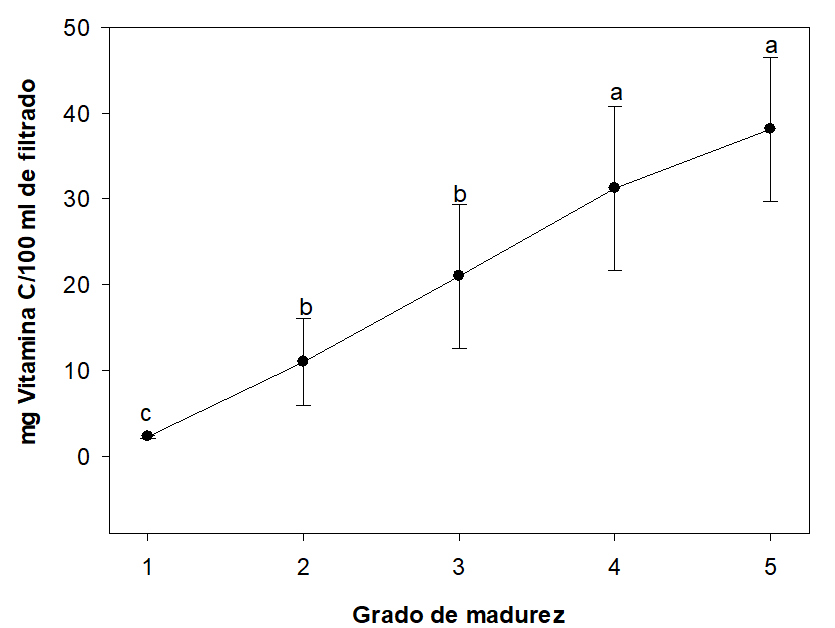
Figura 4
Variación del contenido de vitamina C en la naranjilla en función del grado de madurez
* Letras diferentes indican diferencias significativas entre grados de madurez (p < 0,05).
La concentración de vitamina C (ácido ascórbico) está directamente relacionada con la variedad y localización de los cultivos (Casierra et al., 2004). La determinación del contenido de vitamina C en frutos con diferentes GM se realiza con dos objetivos: conocer la fisiología de maduración del fruto y lograr extraer la mayor cantidad de antioxidantes posible a partir de productos de desecho o subproductos resultante de su procesado industrial.
Medición de color. El color es un índice de cosecha en frutos como el plátano, el mango, la papaya y el tomate, y está relacionado con la aceptabilidad del consumidor en el momento de compra. Durante la maduración se producen cambios de color tanto en el interior como en el exterior del fruto. En las figura 5 y se muestran los valores de L*, a* y b* de la naranjilla en función del GM, y en la figura 6 se pueden observar los cambios en los valores de tono (°H) y cromoa (Cr) durante la maduración. En la figura 4 se puede observar que en el tejido placentario y semillas (interior) los valores de L, a* y b* disminuyen a medida que aumenta la madurez, siendo en el GM 1 cuando estos parámetros presentaron valores significativamente mayores. Por el contrario, en la superficie de la naranjilla (piel) los valores de L, a* y b* aumentaron con el grado de madurez de la fruta, siendo en los GM 4 y 5 cuando estos parámetros mostraron valores significativamente más elevados.
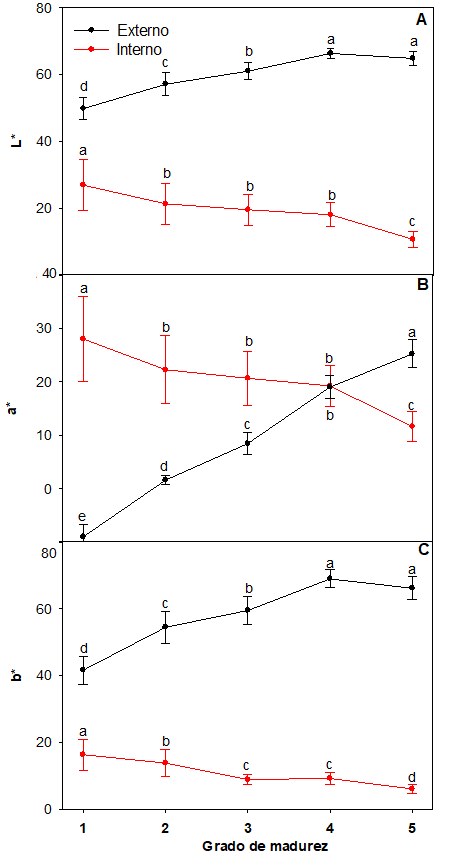
Figura 5
Variación de los parámetros de color superficial externo e interno de naranjilla A) L*, B) a* y C) b* en función del grado de madurez
* Letras diferentes indican diferencia significativa entre los grados de madurez (p < 0,05).
En cuanto a los valores de tono (°H) y cromo (Cr) medidos en el interior del fruto (figura 6a) se observa un descenso con el grado de madurez. Concretamente, la intensidad de color de la pulpa y las semillas (°H) disminuye en un 7,89 % y la cromaticidad (Cr) en un 40,59 %. Esto quiere decir que la estructura interna de la naranjilla se va oscureciendo debido al proceso de maduración, adquiriendo la pulpa un color verde oscuro (Rojas, 2004). A diferencia de la piel (color externo, figura 6b) de la fruta donde se observa un incremento de Cr del 70,96 % y disminución de °H del 67,70 %.
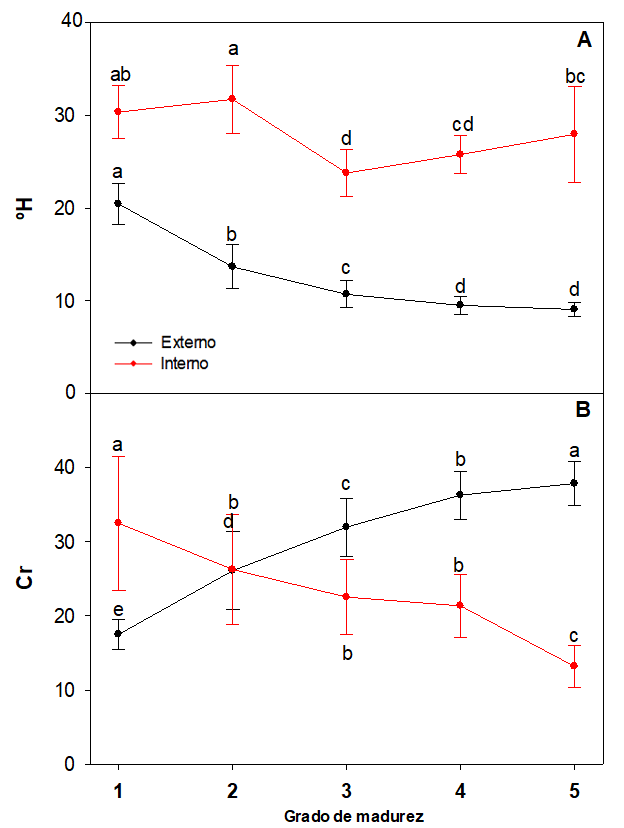
Figura 6
Variación de los parámetros de color superficial externo e interno de naranjilla A) °H y B) Cr en función del grado de madurez
* Letras diferentes indican diferencias significativas en los grados de madurez (p < 0,05)
Los cambios de colores en el pericarpio de la naranjilla son causados por la degradación de ciertos pigmentos como la clorofila, la síntesis de β-carotenos y la acumulación de compuestos fenólicos. Según Azcón-Bieto y Talón (2008), uno de los factores principales por los que tiene lugar la variación del color en un fruto climatérico es su separación de la planta, lo que implica la interrupción del transporte de hormonas como la gibelerina y citoquininas que son sintetizadas en la raíz y el nitrógeno que es absorbido por la misma. Con esta separación se promueve la transformación de cloroplastos a cromoplastos. Además, durante el proceso de maduración los genes estimulados por el etileno sintetizan proteínas o enzimas entre las que se encuentra la enzima poligalacturonasa implicada en este proceso de pigmentación-despigmentación-pigmentación (Manrique, 2003).
Determinación de clorofila y carotenoides. La concentración de clorofila y carotenoides en la fruta está relacionada con la desaparición del color verde y el desarrollo del color amarillo/naranja (indicador de madurez) que se muestra en la figura 7. El contenido de clorofila y carotenoides de la piel, los tejidos placentarios (placenta) y las semillas de naranjilla durante la maduración, se muestra en la figura 8.

Figura 7
Apariencia interna y externa de naranjilla en los cinco grados de madurez considerados
Según se puede observar en la figura 8a, el contenido de clorofila y carotenoides alcanzó los valores más bajos en las semillas, seguidas de los tejidos placentarios y la piel. Entre los GM 1 y 5 se observaron incrementos del 71% y 78 % para clorofila y carotenoides en las semillas, respectivamente, lo que corresponde con una intensificación en el color blanquecino-amarillento durante la maduración.
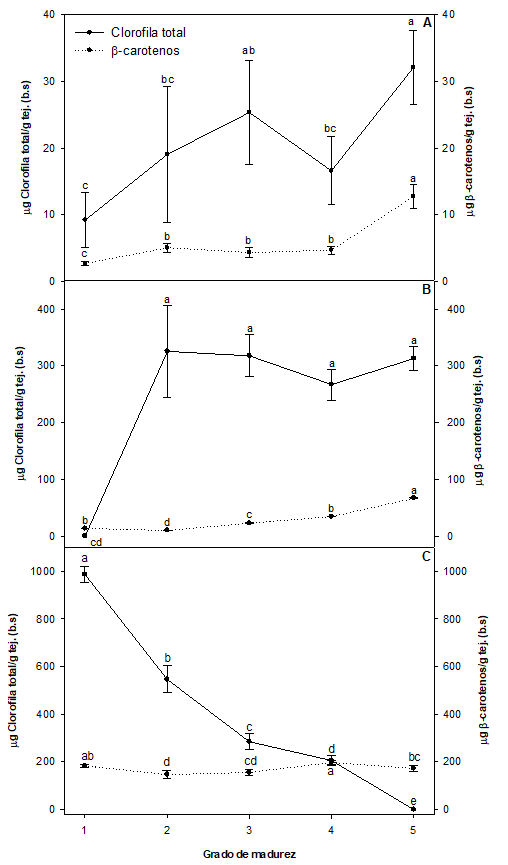
Figura 8
Variación de Clorofila Total y β-carotenos en semillas (A), tejidos placentarios (B) y piel (C) de naranjilla en función del grado de madurez.
* Letras distintas indican diferencia significativa entre grados de madurez (p < 0,05).
Un consumidor habitual de naranjilla puede diferenciar su estado por el color de su pulpa. Generalmente la naranjilla de pulpa verde es utilizada para la elaboración de jugos, helados y postres, en tanto que la naranjilla con pulpa de color amarillo/marrón es utilizada para elaboración de pulpas y procesados. La variedad de naranjilla utilizada en esta investigación se caracteriza por su pulpa de color verde (figura 8b). Al comparar el contenido en clorofila de la pulpa de frutos con GM 1 y 5, se encontró un incremento del 178 % mientras que los carotenoides se incrementaron en un 80 %.
Por el contrario, en la piel (figura 8c) el contenido de clorofila disminuyó gradualmente durante la maduración (80 %) y el contenido en carotenoides se incrementó (8 %) hasta el GM 4 y, a partir del cual disminuyó ligeramente alcanzando valores del mismo orden que los obtenidos en la piel de frutos con un grado de madurez. Los cambios de color observados y la relación con el contenido de clorofila/β-carotenos se producen normalmente durante el proceso de maduración fisiológica. Según explican Merzlyak y Solovchenko (2002), Manrique (2003), y Lado Lindner (2015), la biosíntesis de los carotenos comienza mediante el proceso de desverdizado o degradación del pigmento clorofílico, además de la producción y aplicación exógena estimulante de una fitohormona llamada etileno, considerada en poscosecha como una de las principales causas de la maduración.
El grupo de carotenos como xantófilas y ésteres de ácido graso de caroteno están asociados a los plastoglólublos presentes en las células de la clorofila, que captan energía a longitudes de onda específicas y poseen la capacidad de transferirlas a la clorofila. Sin embargo cuando se acumulan, esta energía luminínica y la ruta fotoquímica se interrumpe, el transporte electrónico disminuye la eficiencia (proceso conocido como fotoinactivación) y de forma masiva se producen carotenoides alcanzando un mayor grado de concentración, formando un extenso sistema de dobles enlaces conjugados de la cadena poliénica formando así un cromóforo (estructura responsable de la absorción de luz visible) de color característico amarillo-naranja. Ante la necesidad de la estabilización enérgetica los carotenoides son capaces de disipar los excesos de energía y proteger los fotosistemas sirviendo como sustancias fotoprotectoras de especies reactivas al oxígeno y otros radicales libres.
Azúcares reductores. Durante la fase de crecimiento, los frutos experimentan cambios metabólicos que son responsables de la síntesis de diversos metabolitos, tales como compuestos fenólicos, almidón, azúcares solubles (sacarosa, glucosa, fructosa), ácidos orgánicos y hormonas (Handa et al., 2012).
En la figura 9 se muestra el contenido en azúcares reductores (µg de glucosa/g tejido en base seca) en la semilla, la placenta y la piel de naranjilla para cada uno de los 5 grados de madurez analizados. En las semillas, la mayor cantidad de azúcares reductores se presentó en los primeros grados de madurez, justo después de la antesis o expansión de la flor/fruto hasta su completo desarrollo y funcionalidad (Almanza Merchán, 2016). Presentó un valor de 213,93 µg de glucosa/g tejido en base seca que disminuyó durante la maduración alcanzando un valor de 6,31 µg de glucosa/g tejido en base seca en el GM 5.
En el tejido placentario la concentración de azúcares reductores fue baja respecto con a la de las semillas y la piel y aumentó con el grado de madurez, encontrándose un valor de 24,57 µg de glucosa/g tejido en base seca en la muestra correspondiente al GM 5. En la piel el contenido de azúcares reductores también se incrementó durante la maduración, pero de forma más gradual obteniéndose valores de 56,52 y 141,83 µg de glucosa/g tejido en base seca en el piel de los frutos con GM 1 y 5, respectivamente. Durante la maduración, un fruto llega a ser atractivo por su aroma y sabor que resultan de la acumulación de azúcares, pigmentos y compuestos aromáticos (volátiles) (Giovannoni, 2001).
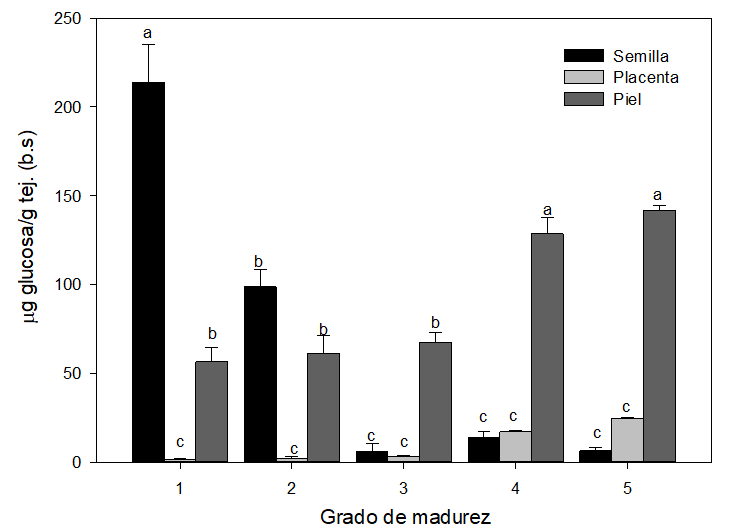
Figura 9
Contenido de azúcares reductores en semilla tejidos placentarios y piel de naranjilla en función del grado de madurez
* Letras distintas indican diferencia significativa entre grados de madurez (p < 0,05).
Según explican Trujillo y Suárez (2010), la maduración de la naranjilla se caracteriza por un aumento de la respiración (de comportamiento sigmoidal) hasta antes de la senescencia que estaría directamente relacionado con el comportamiento fisiológico. El fruto realiza una acumulación de almidón durante su crecimiento y posteriormente, tras un largo proceso de maduración que exige gran cantidad de energía, realiza la hidrólisis a monosacáridos como glucosa y fructosa.
Determinación de fenoles totales. El mayor contenido en compuestos fenólicos se encuentra en la piel de la naranjilla (Loizzo at al., 2019), donde se ha identificado la presencia de ácido clorogénico, ácido cumárico, ácido gálico y rutina, compuestos reconocidos por su actividad antioxidante, antimicrobiana y antitumoral (Heleno et al., 2015; Rice-Evans et al., 1997). Durante la maduración de la naranjilla se observó un incremento en el contenido de FT tanto en la semilla y en los tejidos placentarios como en la piel (figura 10), aumentando en esta última en mucha mayor proporción. Al comparar el contenido de FT de muestras con GM 1 y 5 se observaron incrementos del 40, 32 y 73 % en las semillas, tejidos placentarios y piel, respectivamente. La biosíntesis de compuestos polifenólicos tiene lugar por diferentes vías en las vacuolas de las células vegetales por condensación de productos fotosintéticos originarios de la glucólisis dando lugar a una inmensa variedad de los mismos desde la fenilalanina hasta los compuestos flavonoides (Romojaro, 2016).
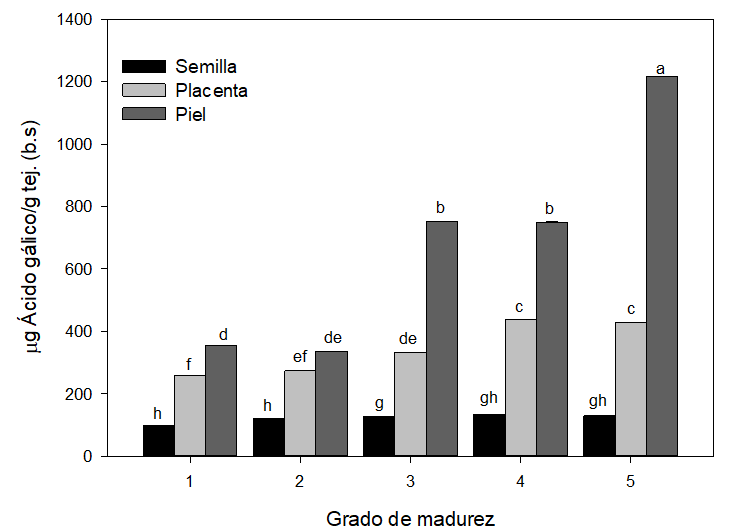
Figura 10
Contenido en fenoles totales en semilla tejidos placentarios y piel de naranjilla en función del grado de madurez
* Letras distintas indican diferencia significativa entre grados de madurez (p < 0,05).
Como se puede observar en la figura 9, el contenido en FT de la piel resultó 1,2 (para GM 1) y 3,1 veces (para GM 5) superior al de los tejidos placentarios. La comparación de los valores entre la piel y las semillas se observa que existen entre 1,3 y 9 veces más FT en la piel. Tanto la composición como la concentración de FT varían durante el desarrollo y la maduración tras la cosecha (poscosecha) y dependerá siempre de la variedad y especie (Jiang & Joyce, 2003; Siriamornpun & Kaewseejan, 2017). La maduración de las frutas generalmente ya acompañada de cambios en el perfil antioxidante fenólico. Se puede producir la degradación de estos compuestos debido a su capacidad para donar electrones con fines de estabilización, protección y defensa a estímulos que afectan a las estructuras celulares dando lugar a la formaicón de semiquinonas y quinonas (Persic et al., 2017). Sin embargo, en este trabajo se observa un aumento progresivo de la cantidad de FT de la naranjilla (comparación entre grados de madurez). Según Dominguez (2011), puede deberse al aumento en el contenido en ácido ascórbico en sus últimos grados de madurez, actuando de manera sinérgica para regenerar estos compuestos mediante el mecanismo de acción antioxidante. De esta manera es posible mantener sus funciones por mayor tiempo, evitando el daño absoluto de biomoléculas y favoreciendo una mayor acumulación en las últimas etapas del proceso de maduración (Gutiérrez et al., 2008; Robards et al., 1999).
Determinación de capacidad antioxidante. La capacidad antioxidante (CA) se determinó mediante dos radicales estables (ABTS y DPPH). En la figura 11 se puede observar que los valores de la CA se encuentran en los tejidos placentarios, seguido de la piel y las semillas. Estos resultados son similares a los encontrados en naranjilla cultivada en Colombia (Loizzo et al., 2019). En general, la CA en las distintas partes del fruto aumentó con el grado de madurez. El análisis con el radical DPPH (figura 11a) mostró incrementos del 13, 49 y 10% en las semillas, tejidos placentarios y piel de la naranjilla, respectivamente. El análisis con el radical ABTS mostró incrementos del 74 y 204% en los tejidos placentarios y la piel de naranjilla, respectivamente. Únicamente CA de las semillas medida con el radical ABTS (figura 11b) mostró una reducción del 31 % con el avance de la maduración.
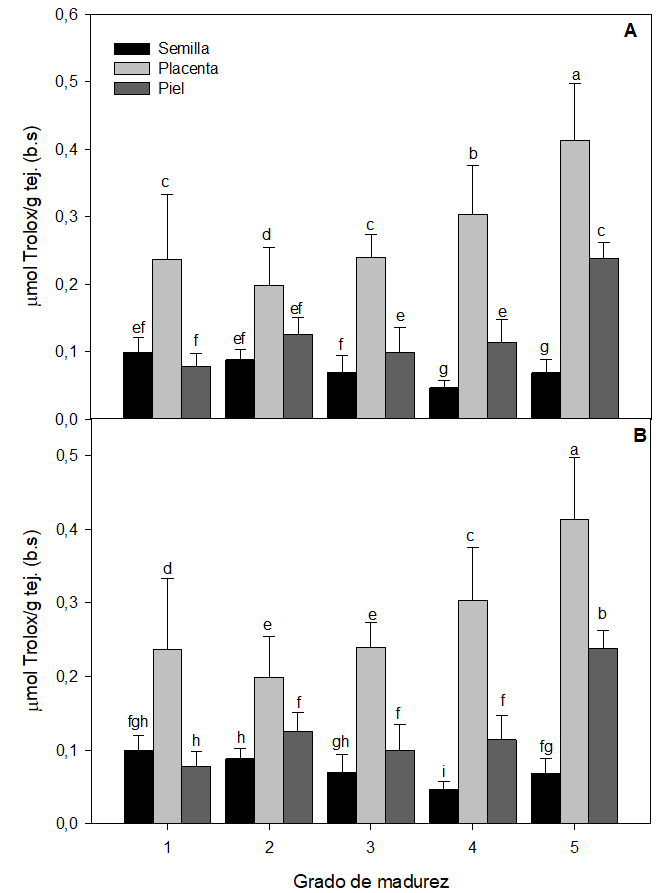
Figura 11
Capacidad antioxidante medida por el radical ABTS A y DPPH B en semilla tejidos placentarios y piel de naranjilla en función del grado de madurez
* Letras diferentes indican diferencias significativas entre grados de madurez (p < 0,05).
La determinación de la actividad antioxidante de la naranjilla durante la maduración permite confirmar que es un fruto con buenas características antioxidantes y que no solo los subproductos generados durante el procesado industrial (piel y semillas) podrían emplearse en el desarrollo de nuevos productos, sino también los frutos con GM 1, 2 ó 3 siendo una alternativa en caso de que el fruto no llegue a su maduración completa en la planta.
CONCLUSIONES
Durante la maduración se producen cambios fisiológicos en la fruta que se ven reflejados en la variación de su tasa respiratoria, color y contenido de compuestos como clorofila, carotenoides, fenoles y azúcares totales. La naranjilla es un fruto climatérico es decir que alcanza su madurez organoléptica en la planta o días posteriores a la cosecha y debe ser cosechada en GM entre 4 y 5. Estos cambios se ven complementados con un incremento en contenido de vitamina C en el fruto. Por otro lado, el cambio del color verde correspondiente a los GM 1, 2 y 3 está relacionado con el alto contenido de clorofila y el desarrollo del color amarillo que se presenta en los GM 4 y 5 se relaciona con el aumento en el contenido de carotenoides (pigmento amarillo/naranja) y disminución de la clorofila.
El análisis de azúcares reductores y compuestos fenólicos en las semillas, tejidos placentarios y piel de la naranjilla permitió comprobar que la piel es la zona del fruto en la que estos compuestos se encuentran en mayor concentración. Además, el contenido de estos compuestos se incrementa durante la maduración. Siendo la piel y las semillas subproductos de la industria, es importante determinar su contenido con el fin de buscar una aplicación que permita su aprovechamiento. En cuanto a la capacidad antioxidante es diferente en la semilla, tejidos placentarios o pulpa y piel de la naranjilla. Los tejidos placentarios presentan mayor capacidad antioxidante, seguida de la piel y las semillas. Durante la maduración la capacidad antioxidante se incrementa en la pulpa y la piel en tanto que en las semillas se mantiene constante. La capacidad antioxidante es una propiedad que debe ser aprovechada tanto para el desarrollo de nuevos productos a partir de subproductos de la industria (piel y semillas) como para el aprovechamiento en caso de que la fruta no llegue al grado de madurez óptimo para el consumo en la planta.
Agradecimientos
Los autores agradecen a Universidad UTE (Quito, Ecuador) y a la Dirección de Investigación y Transferencia Tecnológica ITT. Proyecto de investigación: “Efecto de la aplicación de tratamientos poscosecha sobre la actividad respiratoria y producción de etileno de frutos ecuatorianos” (Código VI.UIO.ING.24).
Referencias
Acosta, O., Pérez, A., & Vaillant, F. (2009). Chemical characterization, antioxidant properties, and volatile constituents of naranjilla (Solanum quitoense Lam.) cultivated in Costa Rica. Archivos latinoamericanos de nutrición, 54(1), 88-94. Recuperado de https://www.researchgate.net/profile/Fabrice_Vaillant/publication/ 26251338_Chemical_characterization_antioxidant_properties _and_volatile_constituents_of_naranjilla_Solanum_quitoense_ Lam_cultivated_in_Costa_Rica/links/00463515f3a0e7a88f000000.pdf
Almanza Merchán, P. (2016). Propiedades Fisicoquímicas durante el Crecimiento y Desarrollo en dos Variedades. Revista Colombiana de Ciencias Hortícolas, 10(2), 222-231. http://dx.doi.org/10.17584/rcch.2016v10i2.5065
Andrade-Cuvi, M. J., Moreno, C., Bravo, J., Guijarro, M., Monar, V., Cevallos, C., & Concellón, A. (2016). Efecto del estado de madurez sobre la calidad de tres variedades de naranjilla (Solanum quitoense Lam). Revista Iberoamericana de Tecnología Postcosecha, 17(2), 217-230. Recuperado de https://www.redalyc.org/pdf/813/81349041008.pdf
Andrade-Cuvi, M. J., Valarezo, L. E., Guijarro-Fuertes, M., Lárraga-Zurita, P., Alcívar León, C. D., Vasco, C., & Vargas-Jentzch, P. (2019). Evaluación del uso de radiación gamma como tratamiento poscosecha en naranjilla (Solanum quitoense). Revista Iberoamericana de Tecnología Postcosecha, 20(1), 1-15. ISSN: 1665-0204. Disponible en: https://www.redalyc.org/articulo.oa?id=813/81359562005
AOAC, A. O. (1990). AOAC 967.21: Ascorbic acid in vitamin preparations and juices. Recuperado de http://www.eoma.aoac.org/methods/info.asp?ID=14258
Azcón-Bieto, J., & Talón, M. (2008). Fundamentos de Fisiología Vegetal (2. ed.). Barcelona: McGraw-Hill.
Bertram, J. S., & Bortkiewicz, H. (1995). Dietary carotenoids inhibit neoplastic transformation and modulate gene expression in mouse and human cells. The American Journal of Clinical Nutrition, 62(6), 1327S-1336S. https://doi.org/10.1093/ajcn/62.6.1327S
Casierra, F., García, E., & Lüdders, P. (2004). Determinación del punto óptimo de cosecha en el lulo (Solanum quitoense Lam. var. quitoense y septentrionale). Agronomía Colombiana, 22(1), 32-39. Recuperado de https://revistas.unal.edu.co/index.php/agrocol/article/view/17765/18591
Conesa, A., Manera, F. C., Brotons, J. M., Fernandez-Zapata, J. C., Simón, I., Simón-Grao, S., Alfosea-Simón, M., Martínez-Nicolás, J. J., Valverde, J. M. & García-Sanchez, F. (2019). Changes in the content of chlorophylls and carotenoids in the rind of Fino 49 lemons during maturation and their relationship with parameters from the CIELAB color space. Scientia Horticulturae, 243, 252-260.
Contreras, J., Calderón, L., Guerra, E., & García, B. (2011). Antioxidant capacity, phenolic content and vitamin C in pulp, peel and seed from 24 exotic fruits from Colombia. Food Research International, 44(7), 2047-2053. doi: 10.1016/j.foodres.2010.11.003
Cuellar, F., Ariza, E., Anzola, C., & Restrepo, P. (2013). Capacidad antioxidante del arazá (Eugenia stipitata Mc Vaugh) durante la maduración. Revista Colombiana de Química, 42(2), 25-27. Recuperado de http://www.scielo.org.co/pdf/rcq/v42n2/v42n2a03.pdf
Dominguez, C. R. (2011). Contenido de compuestos bioactivos y su contribución a la capacidad antioxidante durante la maduración de piña cv. “Esmeralda” (Tesis de Maestría, Centro de Investigación en Alimentación y Desarrollo, A.C., Sonora, México). Recuperado de https://ciad.repositorioinstitucional.mx/jspui/bitstream/1006/179/1/Rosas%20Dominguez_2011_MC.pdf
ETS Laboratories. (2015). Measuring wine color. Recuperado de https://www.etslabs.com/library/37
Forero, D., Orrego, C., Peterson, D., & Osorio, C. (2014a). Chemical and sensory comparison of fresh and dried lulo (Solanum quitoense Lam.) fruit aroma. Food Chemistry, 169, 85-91. https://doi.org/10.1016/j.foodchem.2014.07.111
Forero, N., Gutiérrez, S., Sandoval, R., Camacho, J., & Meneses, M. (2014b). Evaluación poscosecha de las características del lulo (Solanum quitoense) cubierto con hoja de plátano. Temas Agrarios, 19(1), 73-85. Recuperado de https://revistas.unicordoba.edu.co/index.php/temasagrarios/article/view/726/842
Gancel, L., Alter, P., Dhuique-Mayer, C., Ruales, J., & Vaillant, F. (2008). Identifying carotenoids and phenolic compounds in naranjilla (Solanum quitoense Lam. var. Puyo hybrid), and Andean fruit. Journal of Agricultural and Food Chemistry, 56(24), 11890-11899. https://doi.org/10.1021/jf801515p
García, H., & García, M. (2001). Manejo cosecha y postcosecha de mora, lulo y tomate de árbol. Recuperado de https://repository.agrosavia.co/handle/20.500.12324/12834
Giovannoni, J. (2001). Molecular biology of fruit maturation and ripening. Plant Physiology and Plant Molecular Biology, 52, 725-749. doi: 10.1146/annurev.arplant.52.1.725
González, D., Ordóñez, L., Vanegas, P., & Vásquez, H. (2013). Cambios en las propiedades fisicoquímicas de frutos de lulo (Solanum quitoense Lam.) cosechados en tres grados de madurez. Acta Agronómica, 63(1), 11-17. Recuperado de http://www.scielo.org.co/pdf/acag/v63n1/v63n1a02.pdf?fbclid= IwAR2MQB6r9nGJUNnl7tP5Ml_tRr3CgUSjVCO6np5IOsjAe9gQN0-x5sxwy8o
Gutiérrez, D., Ortiz, C., & Mendoza, A. (2008). Medición de fenoles y actividad antioxidante en malezas usadas para alimentación animal. Recuperado de https://www.cenam.mx/simposio2008/sm_2008/memorias/M2/SM2008-M220-1108.pdf
Handa, A., Tiznado-Hernandez, M., & Mattoo, A. (2012). Fruit development and ripening: a molecular perspective. Plant Biotechnology and Agriculture: Prospects for 21st Century, 405-424. https://doi.org/10.1016/B978-0-12-381466-1.00026-2
Heleno, S., Martins, A., Queiroz, M., & Ferreira, I. (2015). Bioactivity of phenolic acids: Metabolites versus parent compounds. Food Chemistry, 173, 501-513. doi:10.1016/j.foodchem.2014.10.057
ICA. (2011). Manejo fitosanitario del cultivo de Lulo (Solanum quitoense Lam.). Recuperado de https://www.ica.gov.co/getattachment/de9f2f66-898a-45b8-848d-0c49a23ca70c/ Manejo-Fitosanitario-del-cultivo-del-lulo-(Solanum.aspx
IICA. (2007). Cultivos de diversión para pequeños productores de frijol y maíz en América Central. Naranjilla y cocona. Recuperado de http://repiica.iica.int/docs/B3198e/B3198e.pdf
INIA. (2007). Efecto de recubrimientos sobre la poscosecha y la evolución del color del zumo de la fruta de naranjo. Agronomía Tropical, 57(2), 131. Recuperado de http://ve.scielo.org/scielo.php?script=sci_arttext&pid=S0002-192X2007000200007
Jáuregui, A. M., Ramos-Escudero, F., Alvarado-Ortíz, C., & Castañeda, B. (2007). Evaluación de la capacidad antioxidante y contenido de compuestos fenólicos en recursos vegetales promisorios. Revista de la Sociedad Química del Perú, 73(3), 142-149. Recuperado de http://www.scielo.org.pe/scielo.php?script=sci_arttext&pid=S1810-634X2007000300003
Jiang, Y., & Joyce, D. (2003). ABA effects on ethylene production, PAL activity, anthocyanin and phenolic contents of strawberry fruit. Plant Growth Regulation, 39, 171-174. https://doi.org/10.1023/A:1022539901044
Lado Lindner, J. (2015). Biosíntesis y acumulación de carotenoides en frutos cítricos y su implicación en la calidad postcosecha (Tesis de doctorado, Universidad de Valencia, Valencia, España). Recuperado de http://roderic.uv.es/handle/10550/44086
Lara, M. (2012). Uso combinado de la radiación UV-C y almacenamiento refrigerado sobre el tiempo de vida útil de la naranjilla (Solanum quitoense Lam.) (Tesis de pregrado, Universidad UTE, Quito, Ecuador). Recuperado de http://repositorio.ute.edu.ec/bitstream/123456789/4954/1/48012_1.pdf
Loizzo, M., Lucci, P., Núñez, O., Tundis, R., Balzano, M., Frega, N., Conte, L., Moret, S., Filatova, D., Moyano, E. & Pacetti, D. (2019). Native Colombian fruits and their by-products: phenolic profile, antioxidant activity and hypoglycaemic potential. Foods, 8(3), 89. doi: 10.3390/foods8030089
López Camelo, A., & Gómez, P. (2004). Comparison of color indexes for tomato ripening. Horticultura Brasileira, 22(3), 534-537. https://doi.org/10.1590/S0102-05362004000300006
Manrique, E. (2003). Los pigmentos fotosintéticos, algo más que la captación de luz para la fotosíntesis. Ecosistemas, 12(1),. Recuperado de https://www.revistaecosistemas.net/index.php/ecosistemas/article/view/250
Mejía, C., Gaviria, D., Duque, A., Rengifo, L., Aguilar, E., & Alegría, A. (2012). Physicochemical characterization of the lulo (Solanum quitoense Lam.) Castilla variety in six ripening stages. Revista de la Facultad de Química Famacéutica, 19(2), 157-165. Recuperado de http://www.scielo.org.co/pdf/vitae/v19n2/v19n2a2.pdf
Mejía, L., Martínez, H., Betancourt, J., & Castrillerón, C. (2007). Aprovechamiento del residuo agroindustrial del mango común (Mangifera indica L.) en la obtención de azúcares fermentables. Ingeniería y Ciencia, 3(6), 41-62. Recuperado de http://publicaciones.eafit.edu.co/index.php/ingciencia/article/view/440
Mendoza, F. A., Arteaga, M., & Pérez, O. (2016). Comportamiento de la vitamina C en un producto a base de lactosuero y pulpa de mango variedad Magdalena River (Mangífera indica L.) durante el secado por aspersión. Revista Chilena de Nutrición, 43(2), 159-166. doi: 10.4067/S0717-75182016000200008
Merzlyak, M., & Solovchenko, A. (2002). Photostability of pigments in ripening apple fruit: a possible photoprotective role of carotenoids during plant senescence. Plant Science, 163(4), 881-888. https://doi.org/10.1016/S0168-9452(02)00241-8
Moreno, E., Ortiz, B., & Restrepo, L. (2014). Contenido Total de Fenoles y Actividad Antioxidante de Pulpa de seis Frutas Tropicales. Revista Colombiana de Química, 43(3), 41-48. Recuperado de http://www.scielo.org.co/pdf/rcq/v43n3/v43n3a06.pdf
NTE INEN 2303, N. (2009). Obtenido de https://archive.org/details/ec.nte.2303.2009
Ochoa, L., Balaguera, H., Ardila, G., Pinzón, E., & Álvarez, J. (2016). Crecimiento y desarrollo del fruto de lulo (Solanum quitoense Lam.) en el municipio de San Antonio del Tequendama (Colombia). Corpoica Ciencia y Tecnología Agropecuaria,17(3), 347-359. doi: http://dx.doi.org/10.21930/rcta.vol17_num3_art:512
Persic, M., Mikulic-Petkovsek, M., Slatnar, A., & Veberic, R. (2017). Chemical composition of apple fruit, juice and pomace and the correlation between phenolic content, enzymatic activity and browning. LWT - Food Science and Technology, 82(1), 23-31. https://doi.org/10.1016/j.lwt.2017.04.017
Pertuzatti, P., Sganzerla, M., Jacques, A., Barcia, M., & Zambiazi, R. (2015). Carotenoids, tocopherols and ascorbic acid content in yellow passion fruit (Passiflora edulis) grown under different cultivation systems. LTW-Food Science and Technology, 64(1), 259-263. doi:10.1016/j.lwt.2015.05.031
Ramírez, F., Kallarackal, J., & Davenport, T. (2018). Lulo (Solanum quitoense Lam.) reproductive physiology: A review. Scientia Horticulturae, 238, 163-176. doi.org/10.1016/j.scienta.2018.04.046
Re, R.; Pellegrini, N.; Proteggente, A.; Pannala, A.; Yang, M. y Rice-Evans, C. (1999) Antioxidant activity applying an improved ABTS radical cation decolorization assay, Free Radicals in Biology and Medicine: 26 (9/10), 1231– 1237. doi.org/10.1016/S0891-5849(98)00315-3
Rice-Evans, C., Miller, N., & Paganga, G. (1997). Antioxidant properties of phenolic compounds. Trends in Plant Science, 2(4), 152-159. doi.org/10.1016/S1360-1385 (97)01018-2
Robards, K., Prenzler, P., Tucker, G., Swatsitang, P., & Glover, W. (1999). Phenolic compounds and their role in oxidative processes in fruits. Food Chemistry, 66(4), 401-436. doi: 10.1016/s0308-8146(99)00093-x
Rojas, J. (2004). Lulo de Castilla (Solanum quitoense L.). En SENA, Caracterización de los productos hortifrutícolas colombianos y establecimiento de las normas técnicas de calidad (pp. 36-43). Recuperado de http://biblioteca.cenicafe.org/bitstream/10778/828/6/Lulo%20de%20Castilla.pdf
Romojaro, M. D. (2016). Tratamientos poscosecha para el control de los daños por frío en frutos climatéricos y no climatéricos (Tesis Doctoral, Universidad de Murcia, Murcia, España). Recuperado de https://www.tdx.cat/bitstream/handle/10803/396310/TMCRC.pdf;jsessionid= 90304E80C951721E968977182895B698?sequence=2
Singleton, V., Rossi, J. A., & Rossi, J. (1965). Colorimetry of Total Phenolics with Phosphomolybdic-Phosphotungstic Acid Reagents. American Journal of Enology and Viticulture, 16(3), 144-158. Recuperado de http://www.ajevonline.org/content/16/3/144
Siriamornpun, S., & Kaewseejan, N. (2017). Quality, bioactive compounds and antioxidant capacity of selected climacteric fruits with relation to their maturity. Scientia Horticulturae, 221, 33-42. https://doi.org/10.1016/j.scienta.2017.04.020
Trevelyan, W. E., Forrest, R. S., & Harrison, J. S. (1952). Determination of yeast carbohydrates with the anthrone reagent. Nature, 170, 626-627. https://doi.org/10.1038/170626a0
Trujillo, N., & Suárez, A. (2010). Evaluación del proceso de maduración del lulo (Solanum quitoense Lam) variedad castilla. Revista @limentech Ciencia y Tecnología Alimentaria, 8(1), 58-66. https://doi.org/10.24054/16927125.v1.n1.2010.471
Valenzuela, C., & Pérez, P. (2016). Actualización en el uso de antioxidantes naturales derivados de frutas y verduras para prolongar la vida útil de la carne y productos cárneos. Revista Chilena de Nutrición, 43(2), 188-195. doi: 10.4067/S0717-75182016000200012
Valverde, F., Espinosa, J., & Bastidas, F. (2010). Manejo de la nutrición del cultivo de naranjilla (Solanum quitoense Lam.) en las zonas de producción de la región Amazónica y Noroccidente de Pichincha. Recuperado de repositorio.iniap.gob.ec/handle/41000/2514
Wellburn, A. R. (1994). The spectral determination of chlorophylls a and b, as well as total carotenoids, using various solvents with spectrophotometers of different resolution. Journal of Plant Physiology, 144(3), 725-749. doi:10.1016/s0176-1617(11)81192-2
Yemm, E. W., & Willis, A. J. (1954). The estimation of carbohydrates in plant extracts by anthrone. Biochemical Journal, 57(3), 508-514. doi: 10.1042/bj0570508
Notas de autor