Producción y Gestión
Estudio cinético de la producción de bioetanol a partir de residuos agroindustriales de la cáscara de banano maduro
Kinetic study of bioethanol production from agroindustrial residues of ripe banana peel
Estudio cinético de la producción de bioetanol a partir de residuos agroindustriales de la cáscara de banano maduro
Industrial Data, vol. 22, núm. 1, 2019
Universidad Nacional Mayor de San Marcos

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-CompartirIgual 4.0 Internacional.
Recepción: 15 Enero 2018
Aprobación: 08 Febrero 2019
Resumen: Esta investigación aborda la aplicación de un compuestode polietilenglicol (PEG) de masa molecular 1500,cuyo objetivo es degradar los compuestos inhibidorespresentes durante la hidrólisis enzimática de la cáscarade banano maduro de la variedad Cavendish. Asimismo,se realizaron tres experimentos al 60% de cáscara debanano molida, en los que se adicionó PEG a diferentes concentraciones: 0,01; 0,02; 0,03 g/g biomasa. La hidrólisis enzimática se realizó con conidios del hongo Trichoderma viride y su posterior fermentación alcohólica fue con levadura activa seca comercial de Saccharomyces cerevisiae, que previamente fue activada. El mejor resultado corresponde al experimento PEG3 (0,03 g/g biomasa), con el que se obtuvo un mayor incremento de azúcares reductores. Además, se encontraron diferencias significativas (p<0,5) para la glucosa obtenida entre los tres tratamientos hidrolíticos. Los resultados demuestran que, a partir de los residuos lignocelulósicos de la cáscara de banano maduro, se puede obtener bioetanol, cuyo rendimiento obtenido de 7% v/v se aproxima a otros reportados en el mismo campo de estudio. Finalmente, el análisis de los costos variables del pretratamiento, aplicado a la cáscara de banano en la producción de etanol obtenido, permite estimar que el método planteado en este artículo es menos costoso comparado con los demás procedimientos, demuestra un mayor rendimiento de bioetanol y se obtiene en menor tiempo.
Palabras clave: Cáscara de banano, polietilenglicol, hidrólisis enzimática, fermentación alcohólica, bioetanol.
Abstract: This research addresses the application of compoundpolyethylene glycol (PEG) of molecular weight 1500,whose objective is to degrade the inhibiting compoundspresent during the enzymatic hydrolysis of Cavendishvariety ripe banana peels. Likewise, three experimentswere conducted on 60% ground banana peel, to whichPEG was added at different concentrations: 0.01; 0.02; and 0.03 g/g biomass. The enzymatic hydrolysis was performed with conidia of the Trichoderma viride fungus and its subsequent alcoholic fermentation with commercial active dry yeast Saccharomyces cerevisiae, which was previously activated. The best result corresponds to the PEG3 experiment (0.03 g/g biomass), with which a greater increase of reducing sugars was obtained. In addition, significant differences were found (p<0.5) in the glucose obtained among the three hydrolytic treatments. The results show that bioethanol can be obtained from the lignocellulosic residues of ripe banana peel, whose 7% v/v yield obtained is close to others reported in the same field of study. Finally, the analysis of the variable costs of the pretreatment, applied to the banana peel for the production of the ethanol obtained, makes it possible to estimate that the method proposed in this article is less expensive compared to other procedures, demonstrating a higher bioethanol yield obtained in less time.
Keywords: Banana peel, polyethylene glycol, enzymatic hydrolysis, alcoholic fermentation, bioethanol.
INTRODUCCIÓN
Las crecientes demandas de combustible derivado del petróleo, debido al rápido desarrollo de la industria automotriz, junto con los problemas de contaminación ambiental, han inspirado los esfuerzos en la exploración de combustibles alternativos (Thangavelu, Saleh y Nasir, 2016). Desde esta perspectiva, se ha fomentado la producción y el consumo de energías renovables, sostenibles y respetuosas con el medioambiente, a través de la biomasa lignocelulósica, la cual puede obtenerse a partir de materiales de desecho de las actividades agrícolas (Conesa, Segui y Fito, 2013). Las fuentes de biocombustibles están distribuidas geográficamente de manera más uniforme que los combustibles fósiles, lo que las convierte en una opción ideal para cumplir con los requerimientos de manera sostenible. Varios promotores de esta alternativa energética subyacen a los crecientes intereses de los biocombustibles, a causa de la creciente incertidumbre de los suministros de petróleo por el aumento de la demanda, la disminución de las reservas conocidas, la preocupación por el calentamiento global y las emisiones de gases de efecto invernadero asociadas con el uso de combustibles fósiles (Saini, Saini y Tewari, 2015).
Los sustratos vegetales están compuestos por celulosa, hemicelulosa y lignina, los cuales eran considerados la materia prima del futuro para la producción de biocombustibles, por su bajo costo y disponibilidad (Abril y Navarro, 2012). La producción y el uso de dichos combustibles ayudan a minimizar las emisiones de gases de efecto invernadero, ya que son obtenidos de fuentes de energía alternativa; asimismo, la producción de bioetanol a partir de materia lignocelulósica implica diferentes etapas: pretratamiento, hidrólisis, fermentación (Silva y Oliveira, 2014).
Por esos motivos, en este estudio se utilizará la cáscara de plátano, la cual es una fuente abundante de material celulósico, que es el constituyente externo del banano, representa alrededor del 40% en peso y tiene el potencial de producir alcohol; sin embargo, es necesario un procesamiento químico y bioquímico para convertir estos polímeros en azúcares monoméricos (Quintero, Martínez, Velasco et al., 2015). Una vez en forma monomérica, los azúcares pueden convertirse mediante microorganismos fermentativos en bioetanol; además, durante la etapa de pretratamiento e hidrólisis, se producen compuestos no deseables que afectan negativamente la tasa de fermentación de la levadura. También, la toxicidad de estos compuestos, llamados inhibidores, sobre los microorganismos es uno de los principales factores limitantes en el rendimiento de bioetanol durante la fermentación (Jaramillo, Gómez y Fontalvo, 2012). Por ello, debe realizarse un pretratamiento antes de la hidrólisis para remover la lignina, hidrolizar la hemicelulosa a azúcares fermentables, y reducir la cristalinidad de la celulosa para liberar la glucosa (Morales, 2012). Esto determina el rendimiento que se obtendría después de la fermentación alcohólica.
En ese sentido, Saval (2012) manifiesta que la hidrólisis enzimática se aplica una vez que los residuos han sido tratados. Así, las cadenas poliméricas son más expuestas para que la generación de compuestos tóxicos no aumente y se evite la adición de compuestos químicos. El proceso se lleva a cabo mediante la adición de enzimas celulíticas al biorreactor (Zhao, Cao, Wang et al., 2013). El uso de la Trichoderma en la industria biotecnológica se debe a su capacidad de producir diversos metabolitos y por su adaptación a diversas condiciones ambientales y sustratos. Por otro lado, la levadura Saccharomyces cerevisiae es usada frecuentemente en la fermentación alcohólica (Sotelo, Avilez y Ginés-Carbajal, 2015), por ser un microorganismo anaeróbico facultativo que tiene la capacidad de fermentar la glucosa y no presentar muchas exigencias en cuanto a nutrientes. Por tal motivo, el objetivo de la presente investigación fue hidrolizar la celulosa y hemicelulosa presente en la cáscara de banano maduro a azúcares reductores y su posterior fermentación alcohólica para obtener bioetanol de segunda generación.
METODOLOGÍA
Materiales
Las cáscaras utilizadas fueron de bananos maduros de la variedad Cavendish. Estas habían sido desechadas de las líneas de producción de la empresa Diana Food S. A., que tiene su planta de procesamiento ubicada en Pasaje, provincia de El Oro, en Ecuador. Asimismo, se empleó polietilenglicol de peso molecular 1500 (PEG 1500) de Sigma-Aldrich (Alemania). El hongo fue obtenido de la marca comercial Trichoeb, proporcionado por Ecua Biológica (Ecuador); y la levadura activa seca fue proporcionada por Levapan (Ecuador).
Pretratamientos
Se molió la cáscara, con la finalidad de aumentar su área de contacto con el hongo, luego se procedió a realizar un tratamiento térmico en una autoclave All American 25X a 121 °C durante 15 minutos.
Diseño del experimento
Se prepararon tres soluciones al 60% de cáscara molida de banano, concentración reportada por Romero, Ayala, y Lapo (2015), ya que, con este porcentaje de cáscara se obtiene mayor concentración de glucosa hidrolizada. Se añadieron 3 concentraciones diferentes de PEG 1500, mostradas en la Tabla 1: PEG1 (0,01); PEG2 (0,02) y PEG3 (0,03 g/g biomasa), para evaluar su efecto como inhibidor en la hidrólisis, ya que la lignina y otros compuestos que se encuentran presentes en los residuos lignocelulósicos limitan la hidrólisis de la celulosa y la hemicelulosa (Ko, Um, Park et al., 2015).
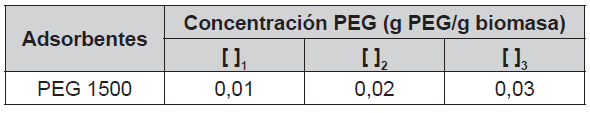
Elaboración propia [ ]1: Concentración 1; [ ]2: Concentración 2; [ ]3: Concentración 3
Hidrólisis enzimática
La hidrólisis enzimática de la biomasa se realizó en biorreactores de 2 L a una concentración de 60% de cáscara, a los cuales se les añadió tres concentraciones diferentes de PEG 1500 (0,01-0,03 g PEG/g biomasa). Estas habían sido disueltas en agua purificada y agitadas durante 5 minutos para que el PEG absorba a los inhibidores de la hidrólisis enzimática. Posteriormente, se adicionó 0,4 g/L de conidios del hongo Trichoderma viride. Se agitó durante 1 hora a 200 rpm y se tomó una muestra cada hora. Durante el proceso se midió pH, °Bx (grados Brix) y oxígeno disuelto, para lo cual se utilizó un medidor portátil de acuerdo a lo manifestado por Tejeda, López, Rojas et al. (2015).
Cuantificación de azúcares reductores
Para la cuantificación de glucosa se tomó una muestra de hidrolizado en un tubo de ensayo y se centrifugó a 10 000 rpm durante 10 min, y con el sobrenadante se hizo una dilución de 1:10. Luego se tomaron 0,5 mL de la dilución y 0,5 mL del reactivo DNS, los cuales se colocaron en un tubo de ensayo en baño de agua a 100 °C por 5 min. En este lapso el ácido 3,5 dinitrosalicílico fue reducido por los azúcares reductores que entran en contacto con el mismo, ocasionando un cambio de color con variaciones de amarillo hasta café (Ávila, Rivas, Hernández et al., 2012). Se enfrió hasta lograr temperatura de ambiente y se adicionó 5 mL de agua destilada. Se agitó y se realizó la lectura a 540 nm en el espectrofotómetro Hach DR 3900 (Canseco, Aráoz, Gusils et al., 2015).
Con el experimento PEG3 (PEG 0,03 g/g cáscara), que fue el tratamiento con el que se obtuvo mayor concentración de glucosa, se realizó la fermentación para la obtención de bioetanol.
Fermentación
Después de la hidrólisis enzimática de la cáscara, se inactivó el hongo pasteurizando el hidrolizado a 90 °C por 10 min (Centeno, 2016). Se trabajó con un volumen de 1000 mL, se controló el pH y se adicionó 800 ufc/mL de levadura seca comercial (Saccharomyces cerevisiae) que previamente fue activada; asimismo, se colocó el jarabe glucosado en un biorreactor anaerobio, donde se tomaron muestras para medir la concentración de alcohol mediante cromatografía de gases. El pH, °Bx y oxígeno disuelto se midieron con un equipo multiparamétrico.
Estimación comparativa de costos variables
Se realizó una estimación comparativa de costos variables del proceso de sacarificación mediante hidrólisis enzimática y de fermentación alcohólica, para lo cual se asumió una base de cálculo de 600 g de cáscara/L de solución.
A continuación, en la Tabla 2 se detallan los costos de los insumos necesarios en el proceso.
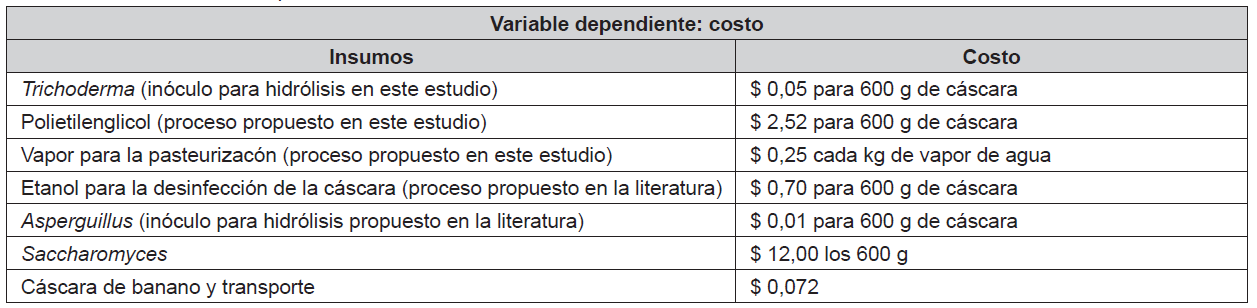
Elaboración propia
RESULTADOS
La Figura 1 presenta la producción de azúcares reductores (mg/L) para los 3 tratamientos y una muestra control durante 24 horas de hidrólisis enzimática.
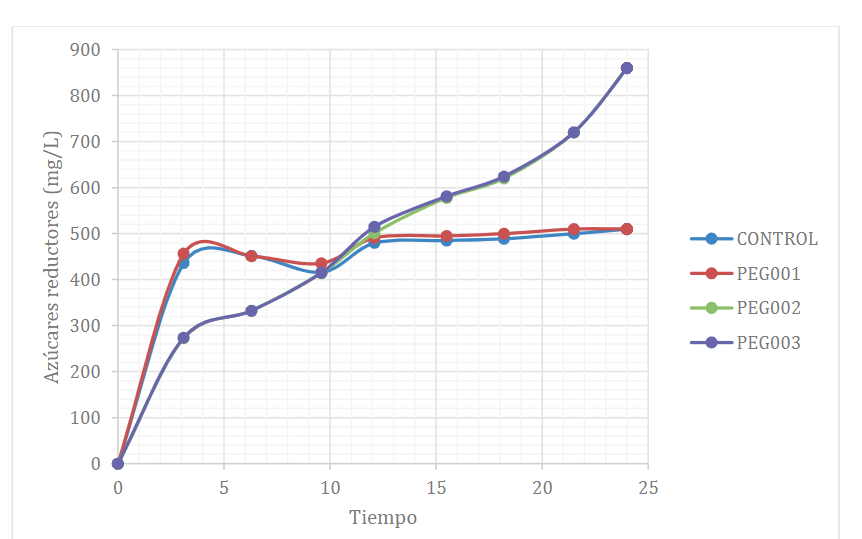
Figura 1
Cinética de la hidrólisis enzimática para los tratamientos durante 24 horas
En el experimento con PEG 0,03 g/g biomasa se alcanzó un incremento de 895,95 (± 1,9) mg/L de azúcares reductores, existiendo diferencias significativas con respecto a los otros tratamientos, tal como se puede evidenciar en la Tabla 3, donde todos los p-value alcanzaron valores menores a 0,05.
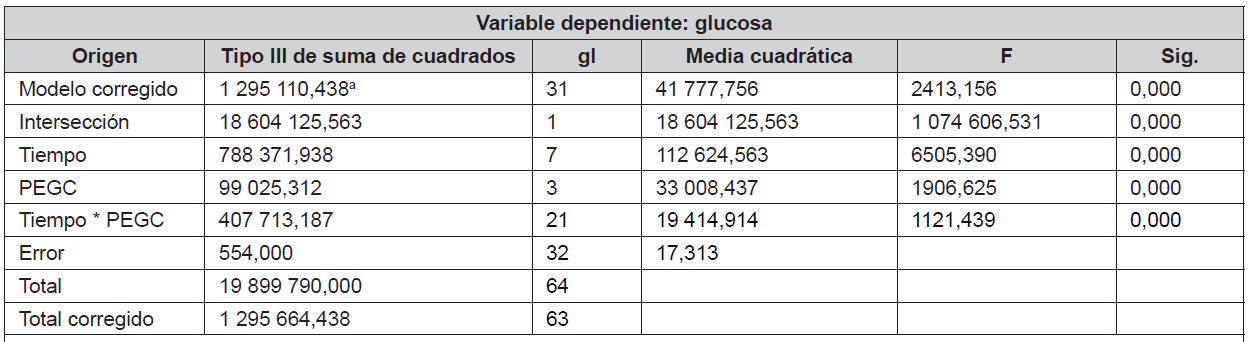
Elaboración propia a. R al cuadrado = 1000 (R al cuadrado ajustada = 0,999)
Por otro lado, la Figura 2 muestra el efecto del polietilenglicol (PEG) agregado a la cáscara de banano maduro molida a diferentes concentraciones (Tabla 1), en la producción de glucosa. Se puede observar que existen diferencias significativas entre los pretratamientos estudiados.
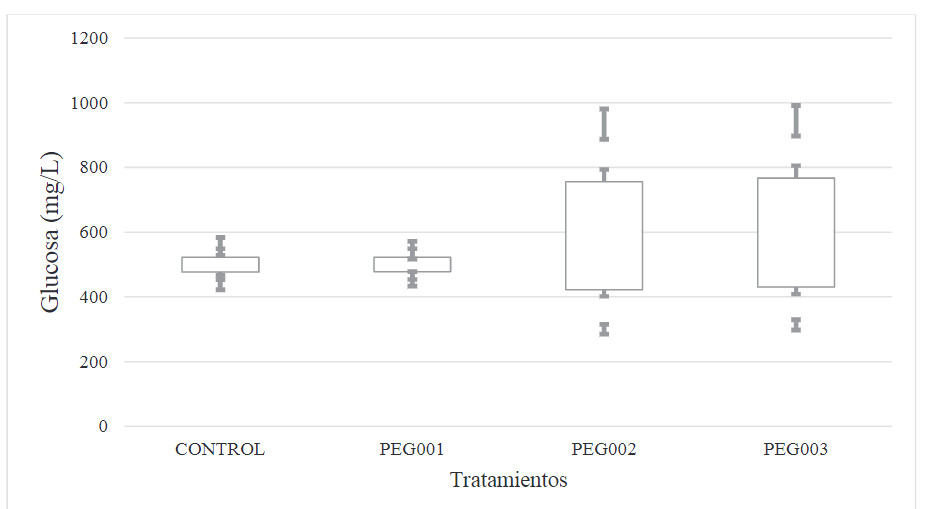
Figura 2
Medias de la evolución de glucosa en función de los pretratamientos aplicados a la cáscara de banano maduro (95% de confianza)
Elaboración propia
Por su parte, la variación del pH respecto al tiempo de hidrólisis enzimática de cáscara de banano maduro en las condiciones de estudio se puede observar en la Figura 3.
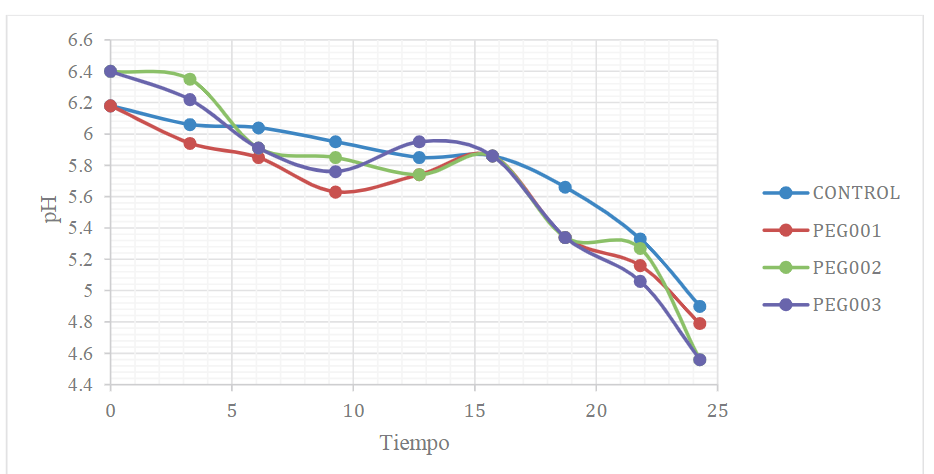
Figura 3
Variación del pH respecto al tiempo para la hidrólisis a una escala de 2 L.
Elaboración propia
Asimismo, la disminución del oxígeno disuelto durante el proceso de hidrolizado, se muestra en la Figura 4.
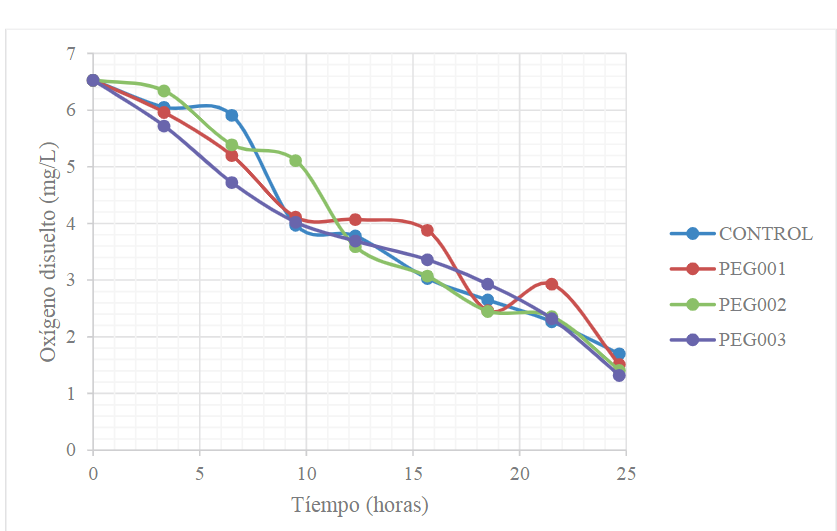
Figura 4
Disminución del oxígeno disuelto para la hidrólisis enzimática a escala de 2 L.
Elaboración propia
Adicionalmente, el comportamiento de la producción de bioetanol durante la fermentación por un periodo de 4 días se observa en la Figura 5.
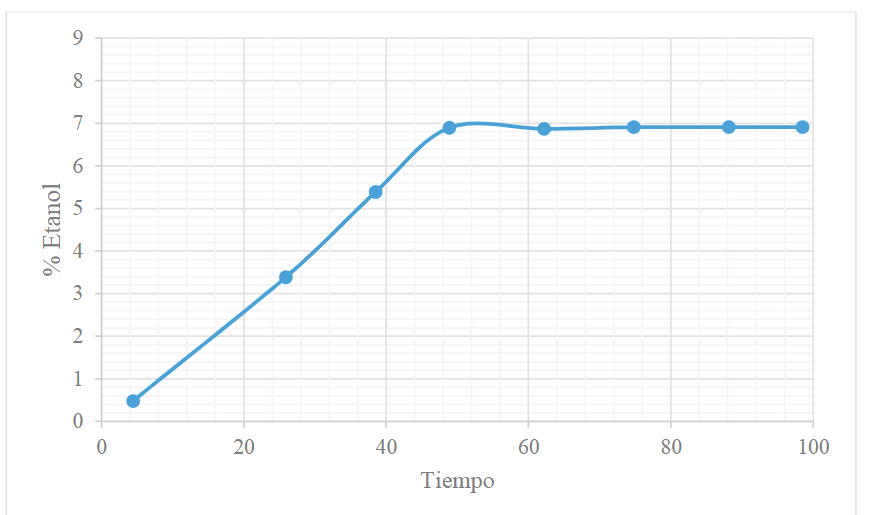
Figura 5
Cinética de la producción de bioetanol durante la fermentación alcohólica
Elaboración propia
DISCUSIÓN
A partir de la Figura 1 se pudo observar que la adición de PEG con concentración de 0,02 y 0,03 g/g biomasa (PEG2 y PEG3) aumenta los rendimientos de azúcares reductores hasta valores de 895,95 (± 1,9) mg/L, lo que permitió obtener un rendimiento de alcohol del 7% v/v (Figura 5). Este rendimiento de etanol obtenido en este estudio es mayor al reportado por Benjamin, Singh, Dipuraj et al. (2014), los cuales encontraron 2,38% y 6% de etanol a los 2 y 7 días respectivamente. Estos autores utilizaron 5% de cáscara en polvo, Aspergillus niger al 3% p/v y pH 6, desinfectada la cáscara de banano con etanol al 70%. Posteriormente, la secaron al sol durante 7 días y la fermentaron con 4% v/v de inóculo de Saccharomyces cerevisiae. Un estudio comparativo de costos variables se puede observar en la Tabla 3. Mayores rendimientos de etanol (59,3% p/v) han sido reportados por Boluda, García, González et al. (2010) a partir de cáscara de mandarina, pero utilizando explosión con vapor como pretratamiento de la biomasa utilizada en la fermentación alcohólica. Precisamente, este pretratamiento tiene la desventaja de causar la generación de inhibidores que afectan el proceso de fermentación, para lo cual debe combinarse con H2SO4 o CO2 para mejorar la eficiencia del proceso; además, existe el riesgo de producción de compuestos fenólicos solubles (Sánchez, Gutiérrez, Muñoz et al., 2010).
Por otra parte, con respecto al descenso del pH en función del tiempo de hidrólisis de la cáscara de banano maduro presente en los tratamientos PEG1, PEG2 y PEG3 (Figura 3), se puede manifestar que este se produce desde 6,2 a 4,9 unidades de pH en el tratamiento de control; de 6,2 a 4,8 en el tratamiento PEG1; de 6,5 a 4,6 en el tratamiento PEG2; y de 6,5 a 4,6 en el tratamiento PEG3; estabilizándose después de 18 horas de hidrólisis en todos los tratamientos, lo cual indica que el hongo modifica el pH del medio de cultivo para su crecimiento y producción de glucosa.
Por su parte, el comportamiento del oxígeno disuelto, respecto al tiempo (Figura 4), se puede observar que decrece conforme avanza la hidrólisis enzimática, debido a que una fracción de este microorganismo lo consume como parte de la vía metabólica aeróbica.
Además, el análisis en los costos variables del pretratamiento aplicado a la cáscara de banano en la producción de etanol obtenido en este estudio, para glucosa producida a partir del mejor tratamiento aplicado (PEG3) en comparación con otros estudios, se presenta en la Tabla 4 lo siguiente.
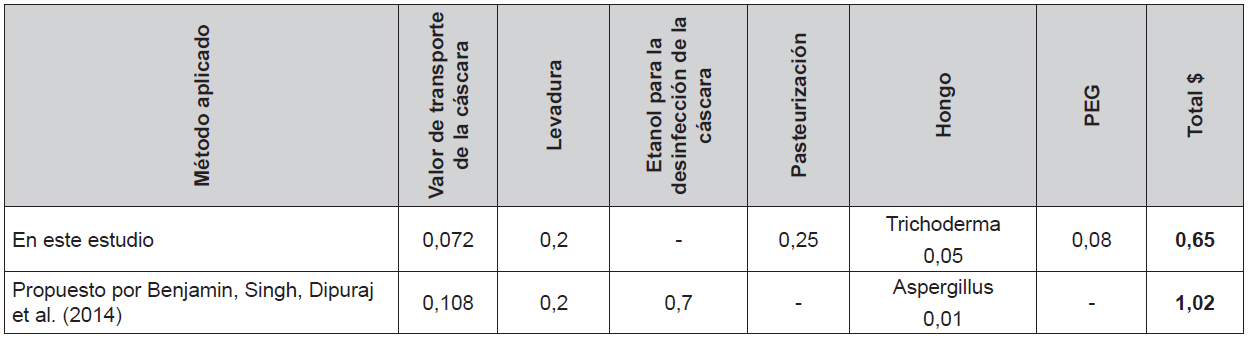
Elaboración propia
Estos costos están calculados en dólares para cada etapa del proceso empleado, tanto en la hidrólisis enzimática como en la fermentación alcohólica, utilizando una base de cálculo de 600 g de cáscara de banano maduro (60% p/v).
Es importante mencionar que el método mencionado por Benjamin, Singh, Dipurak et al. (2014) incluye una etapa de secado de la cáscara de banano por un tiempo de 7 días, lo cual es una desventaja importante para el proceso propuesto por esos autores.
CONCLUSIONES
Se observó que el polietilenglicol (PEG) influye en la conversión de la celulosa de la cáscara de banano maduro en glucosa mediante hidrólisis enzimática. Siendo el tratamiento PEG3, el que produjo mayor cantidad de jarabe glucosado. Se encontraron diferencias significativas para la glucosa obtenida entre los tres tratamientos hidrolíticos. Los resultados demuestran que a partir de residuos lignocelulósicos de la cáscara de banano maduro, se puede obtener bioetanol, cuyo rendimiento obtenido de 7% v/v se aproxima a otros reportados en ese campo de investigación. Por otro lado, el análisis de los costos variables del pretratamiento aplicado a la cáscara de banano en la producción de etanol obtenido permite estimar que el método planteado en este estudio es menos costoso comparado con los demás, a partir del mismo residuo, con mayor rendimiento de bioetanol e incluso en menor tiempo.
Referencias
Abril, A. y Navarro, E. (2012). Etanol a partir de biomasa lignocelulósica. Recuperado de https://www.researchgate.net/profile/ Enrique_Navarro/publication/241216642_ Etanol_a_partir_de_biomasa_lignocelulosica/ links/0c96051c8409028b93000000/Etanol-apartir-de-biomasa-lignocelulosica.pdf
Ávila, R., Rivas, B., Hernández, R. y Chirinos, M. (2012). Contenido de azúcares totales, reductores y no reductores en Agave cocui Trelease. Multiciencias, 12(2), 129-135.
Benjamin, J., Singh, P., Dipuraj, P., Singh, A., Rath, S., Kumar, Y., Masih, H. y Peter, J (2014). Bio-Ethanol production from banana peel by simultaneous saccharification and fermentation process using cocultures Aspergillus niger and Saccharomyces Recuperado de https://www.researchgate.net/profile/ Yashab_Kumar/publication/307175371_BioEthanol_Production_from_Banana_peel_ by_Simultaneous_Saccharification_and_ Fermentation_Process_using_cocultures_ Aspergillus_niger_and_Saccharomyces_ cerevisiae/links/57dcf44b08ae5292a37c902b/ Bio-Ethanol-Production-from-Banana-peelby-Simultaneous-Saccharification-andFermentation-Process-using-coculturesAspergillus-niger-and-Saccharomyces-cerevisiae.pdf
Boluda, M., García, L., González, F., y López, A. (2010). Mandarin peel wastes pretreatment with steam explosion for bioethanol production. Bioresource Technology, 101(10), 3506–3513.
Canseco, M., Aráoz, J., Gusils, C. y Zossi, S. (2015). Validación de metodología para determinación de azúcares reductores totales en vinos fermentados. Revista Industrial y Agrícola de Tucumán, 92(2), 33-38.
Centeno, K. (2016). Efecto de la hidrólisis enzimática y la pasteurización sobre la calidad de una bebida fermentada a base de maíz morado (Zea mays) variedad Kulli. (Tesis de licenciatura). Universidad Nacional de San Agustín de Arequipa, Arequipa. Recuperado de http://repositorio.unsa.edu.pe/bitstream/handle/UNSA/3294/IAceork02.pdf?sequence=1&isAllowed=y
Conesa, C., Segui, L. y Fito, P. (2013). Sacarificación de residuos industriales de piña con mezclas de enzimas comerciales. Recuperado de https://riunet. upv.es/bitstream/handle/10251/28121/ TESIS%20DE%20MASTER%20CLAUDIA.pdf?sequence=1&isAllowed=y
Jaramillo, O., Gómez, M. y Fontalvo, J. (2012). Remoción de los inhibidores de la fermentación etanólica usando membranas de polidimetilsiloxano (PDMS) por pervaporación. Revista ION, 25(1), 51-59.
Ko, J., Um, Y., Park, Y., Seo, J. y Kim, K. (2015). Compounds inhibiting the bioconversion of hydrothermally pretreated lignocellulose. Applied Microbiology and Biotechnology, 99(10), 4201–4212.
Morales, M. (2012). Estrategia para la reconversión de una industria integrada de azúcar y derivados para la producción de etanol y coproductos a partir del bagazo (Tesis doctoral). Universidad Central “Marta Abreu” de Las Villas, Santa Clara. Recuperado de http://dspace.uclv.edu.cu/ bitstream/handle/123456789/6707/Marlen%20 Morales%20Zamora%2C%202012.pdf?sequence=1&isAllowed=y
Quintero, L., Martínez, Y., Velasco, J., Arévalo, A., Muñoz, Y. y Urbina, N. (2015). Evaluación de residuos de papa, yuca y naranja para la producción de etanol en cultivo discontinuo utilizando Saccharomyces cerevisiae. Revista ION, 28(1), 43-53.
Romero, H., Ayala, H. y Lapo, B. (2015). Efecto de tres pre-tratamientos de cáscara de banano para la obtención de jarabe glucosado mediante hidrólisis enzimática. Avances en Química, 10(1), 79-82.
Saini, J., Saini, R., y Tewari, L. (2015). Lignocellulosic agriculture wastes as biomass feedstocks for second-generation bioethanol production: concepts and recent developments. 3 Biotech, 5(4), 337-353.
Sánchez, A., Gutiérrez, A., Muñoz, J. y Rivera, C. (2010). Producción de bioetanol a partir de subproductos agroindustriales lignocelulósicos. Revista Tumbaga, 1(5), 61-91.
Saval, S. (2012). Aprovechamiento de residuos agroindustriales: pasado, presente y futuro. BioTecnología, 16(2), 14-46.
Silva, P. y Oliveira, S. de (2014). Exergy analysis of pretreatment processes of bioethanol production based on sugarcane bagasse. Energy, 76, 130-138.
Sotelo, R., Avilez, R. y Ginés-Carbajal, F. (2015). Obtención de bioetanol mediante la fermentación de jarabes obtenidos de cáscara de naranja. Foro de Estudios sobre Guerrero, 1(2), 589-591.
Tejeda, A., López, Z., Rojas, D., Reyna, M., Barrera, A. y Zurita, F. (2015). Eficiencia de tres sistemas de humedales híbridos para la remoción de carbamazepina. Tecnología y ciencias del agua, 6(6), 19-31.
Thangavelu, S., Saleh, A. y Nasir, F. (2016). Review on bioethanol as alternative fuel for spark ignition engines. Renewable and Sustainable Energy Reviews, 56, 820-835.
Zhao, L., Cao, G., Wang, A., Guo, W., Ren, H. y Ren, N. (2013). Simultaneous saccharification and fermentation of fungal pretreated cornstalk for hydrogen production using Thermoanaerobacterium thermosaccharolyticum W16. Bioresource Technology, 145, 103-107.