ARTÍCULO DE REVISIÓN
Una guía para el estudio de nanopartículas magnéticas de óxidos de hierro con aplicaciones biomédicas. Parte II
A Guide to Study Iron Oxide Magnetic Nanoparticles with Biomedical Applications. Part II
Una guía para el estudio de nanopartículas magnéticas de óxidos de hierro con aplicaciones biomédicas. Parte II
Ingeniería y Ciencia, vol. 13, núm. 26, 2017
Escuela de Ciencias y Humanidades y Escuela de Ingeniería de la Universidad EAFIT
Recepción: 01 Febrero 2017
Aprobación: 15 Abril 2017
Resumen: En esta segunda parte del artículo, se abordará el tema de la caracterización de nanopartículas magnéticas, haciendo énfasis en la interpretación de estas propiedades para definir la aplicación biomédica de los nanosistemas en estudio. Para el caso de nanopartículas de óxidos de hierro, se analizará como estas propiedades influyen en la disipación de calor de las nanopartículas cuando son sometidas a campos de radiofrecuencia, respuesta útil en el tratamiento del cáncer por hipertermia magética. En la hipertermia magnética, las partículas absorben energía de un campo de radio frecuencia y la disipan en forma de calor, los rangos de frecuencia típicamente usados para pruebas in-vivo y en humanos están entre 50 y 1000 kHz y amplitudes entre 5 y 50 kA/m. Las propiedades de interés como magnetización, interacciones entre partículas y su ordenamiento, se estudian a partir de simulaciones computacionales y datos experimentales utilizando modelos de análisis adecuados para cada caso, ya planteados en la primera parte de este artículo. Finalmente se hace una correlación de estas propiedades con la disipación de calor, determinada por métodos calorimétricos, la cual se considera como parámetro de mérito para cuantificar la transducción de energía electromagnética a térmica.
Palabras clave: Cáncer, disipación de calor, hipertermia magnética, nanopartículas magnéticas, óxidos de hierro.
Abstract: In this second part, the magnetic nanoparticles characterization is studied, doing special emphasys in the properties interpretation in order to define the nanosystems applications. In the case of the iron oxide magnetic nanoparticles, the influence of its properties in the heat dissipation under radiofrequency fields is analyzed, this answer is usefull in the cancer treatment by magnetic hyperthermia. In the magnetic hyperthermia treatment, particles absorb energy from a radio frequency magnetic field and dissipate it as heat. For in-vivo test and human assays, frequency ranges between 50 and 1000 kHz and field amplitudes ranges between 5 and 150 kHz are usually used. The main properties, such as magnetization, interactions between particles and particles structuring are studied using experimental data, computational simulations and suitable models for each case studied in the part I of this article. Finally, a correlation between these properties with heat dissipation, measured by calorimetric methods, which is the merit parameter to quantify the electromagnetic energy transduction into heat, is pointed out.
Key words: Cancer, heat dissipation, magnetic hyperthermia, magnetic nanoparticles, iron oxides.
1 Introducción
La aplicación de nanopartículas en problemas biomédicos depende totalmente de sus propiedades físicas y químicas. Así, si se desea adherir un fármaco a la superficie de una nanopartícula, esta debe estar modificada superficialmente para permitir un enlace químico entre la superficie de la partícula y el fármaco 1, donde un agente antinflamatorio como la indometacina ha sido unido a polietilienglicol por medio de la unión química de carboiimidas y después reducidas a nivel nanoscópico por medio del método de nanoprecipitación.
Por otro lado, en hipertermia magnética, se busca que las nanopartículas sean biocompatibles y que su tamaño, o el de sus agregados, no obstruya los vasos mas pequeños del organismo 2. Ultimamente, en vista de aprovechar al máximo las diversas propiedades de los nanosistemas, se han planteado terapias conjuntas, como es el caso de la hipertermia magnética y la fotodinámica usando nanopartículas de óxidos de hierro recubiertas con oro 3, o usadas en conjunto tanto como terapia y como agentes de diagnóstico 4,5.
Debido a que los estudios con seres humanos, requiere de mayor experimentación, a la que actualmente se ha realizado en el tema, existe gran avance en el tratamiento de tumores en modelos murinos 6. De todas formas, es necesario conocer las propiedades de los nanosistemas utilizados antes de ser aplicados en los organismos vivientes, para esto, se debe determinar con exactitud estas propiedades y correlacionarlas de la forma correcta para tratar de predecir su comportamiento en los ambientes biológicos.
Es por esto, que en esta segunda parte del artículo, se presentan dos métodos de sintesis químicas de nanopartículas magnéticas (NPM) de óxidos de hierro, un método en base orgánica, descomposición térmica, y otro método en base acuosa, co-precipitación. Si bien, no son los únicos métodos de síntesis, son los más usados y baratos para la obtención de nanopartículas biocompatibles, aclarando que la síntesis por descomposición térmica no lleva a la obtención inmediata de material biocompatible, las NPM deben ser sometidas a un proceso químico para cambiar su afinidad superficial. Seguidamente, se analizan los principales técnicas de caracterización y cómo analizar los datos que estas arrojan, para finalizar con el estudio de la disipación de calor de la NPM bajo campos de radiofrecuencia, y como esta respuesta se relaciona con las propiedades determinadas por las técnicas de caracterización usadas.
2 Procedimientos de síntesis química de nanopartículas
Existen en la literatura, dos principales procedimientos de síntesis química de NPM de óxidos de hierro, los cuales son ampliamente utilizados para obtener partículas de buena calidad cristalina, uniformidad de forma, uniformidad de tamaño y biocompatibles, lo cual es una condición primordial para las aplicaciones biomédicas.
2.1 Descomposición térmica a altas temperaturas
Este método es útil para la síntesis de NPM de tamaño esférico y de baja polidispersidad de tamaño. En este procedimiento 7,8,9 se utilizan precursores orgánicos conocidos como acetilcetonatos metálicos, tales como cetilacetonato de Fe (III) (Fe(acac)3), acetilacetonato de Fe (II) (Fe(acac)2) y acetilacetonato de Co (Co(acac)2); oleatos como oleato de hierro Fe(ole)3, o también pentacarbonilo de hierro, Fe(CO)5. Los compuestos se deben mezclar en las correctas proporciones para obtener maghemita (γ-Fe2O3), magnetita (FeO.Fe2O3) o ferrita de cobalto (CoO.Fe2O3).
La elección del disolvente de la reacción, el precursor de hierro, la relación Fe:surfactante, la concentración inicial de los reactivos, la temperatura de estabilización de la reacción son factores primordiales para controlar la naturaleza de las partículas, su distribución, la forma de las nanopartículas y el tamaño 10.
Con respecto a la forma de las nanoparticulas esta depende principalmente de la concentración de las especies precursoras. Si la concentración de los precursores es baja, el crecimiento es controlado termodinámicamente y la forma de las partículas tiende a ser la esférica con el objetivo de minimizar su energía superficial de acuerdo a lo reportado en la referencia 11. Por otro lado, si la concentración de los precursores es alta, el crecimiento de las partículas es controlado cinéticamente y las especies precursoras se unen preferentemente a las caras cristalinas con mayor energía superficial dando lugar a partículas con formas diferentes a la esférica tales como por ejemplo cubos 12 o tetraedros 13.
Los surfactantes tienen la capacidad de formar una esfera dinámica de coordinación en la superficie de las partículas durante el crecimiento ya que se adsorben y desorben continuamente 14 produciendo nanopartículas con una mezcla de formas de triángulos, esferas y diamantes. Si se llegará aumentar la proporción del surfactante por ejemplo de dodecilaminada se producen nanoparticulas de forma hexagonal 12,15. El tamaño por otro lado se ve influenciado por el efecto del precursor, del disolvente y surfactante obteniéndose nanoparticulas de 4nm a 20nm respectivamente 7,9.
La influencia en la variación de cada uno de los parámetros de la síntesis conduce a proponer un mecanismo de reacción en el que se generan especies precursoras posibles como el complejo Fe(surfactante)x, el cual se descompone entre los 210-250 oC formando los núcleos. Desde el momento que tiene lugar la nucleación hasta el final de la reacción (calentamiento hasta el punto de ebullición del disolvente y posterior reflujo) tendría lugar el crecimiento. El hecho de que se alcancen elevadas temperaturas hace que se obtengan partículas muy cristalinas ya que los átomos poseen la suficiente energía para ordenarse dentro de la nanopartícula 11.
Para aplicaciones biomédicas, existen determinados factores que condicionan el uso de nanopartículas magnéticas sintetizadas por este método, como son el tamaño de partícula, el tipo de recubrimiento superficial (polimérico y surfactantes, inorgánicos, de carbón y sílica) y las propiedades magnéticas 16, 17, 18.
2.2 Co-precipitación química
A diferencia del método anterior, en este caso lo precursores metálicos son inorgánicos tales como cloruros, nitratos o sulfatos 19,20,21. De igual forma, se deben elegir las cantidades molares adecuadas para obtener el compuesto deseado, y además la capa surfactante 22, que en este caso puede ser una molécula polar que permita la estabilización acuosa de las partículas por repulsión electrostática.
Este método consiste en la adición de una disolución de sal de Fe2+ y otra de Fe3+, ya sea en forma de cloruros, sulfatos, nitratos y percloratos disueltos en agua 23. Los hidróxidos de los metales formados se precipitan con la adición de una solución básica como hidróxido de sodio e hidróxido de amonio. Posteriormente los hidróxidos del metal son lavados para eliminar las sales de cloruros o nitratos solubles del medio. Una desventaja importante de este método es la dificultad para controlar el tamaño de partícula y la distribución de tamaños.
Por ejemplo, una precipitación rápida da como resultado partículas de gran tamaño, sin embargo el tamaño de las nanoparticulas pueden controlarse con el uso de aniones orgánicos quelantes como los carboxilatos (ácido oleico) o polímeros superficiales que actúen como agentes acomplejantes (dextrano y alcohol polivinílico) durante la formación de la magnetita 24. Así mismo, se han estudiado diferentes variantes como ajustes de parámetros como el pH de la reacción, velocidad de agitación, velocidad de adición de las sales de hierro, temperatura y fuerza iónica que permiten obtener una distribución de tamaño más controlada entre 5 y 15 nm 25. La principal ventaja de este procedimiento es que las muestras obtenidas son directamente hidrofílicas y, por lo tanto, estables en medios acuosos, además de simplicidad y bajo costo.
3 Propiedades físicas de nanopartículas de óxidos de hierro
3.1 Determinación de la estructura cristalina por difracción de rayos X
Compuestos como la magnetita y la maghemita, tienen una estructura cristalina conocida como espinela (grupo Fd3m) correspondiente a compuestos de la forma A2+B2 3+ O4 2-. Este tipo de compuestos, se cristalizan en un sistema cúbico centrado en las caras (fcc), en el cual, los aniones óxidos se sitúan en los vértices de la red cúbica, el catión A ocupa los sitios tetraédricos y el catión B ocupa los sitios octaédricos de la red. Esta disposición de los sitios también puede encontrarse invertida es decir, los sitios octaédricos son ocupados por los átomos tipo A, mientras que los átomos tipo B ocupan los sitios tetraédricos, configuración que se conoce como espinela invertida, y que bajo condiciones de temperatura y presión ambiental, corresponde a la estructura cristalina de la magnetita y de la maghemita 26.
Una representación gráfica de esta estructura para la magnetita, se presenta en la Figura 1(a), en la misma se puede observar el parámetro de red y los ángulos de la red cúbica. De igual forma, en la Figura 1(b) se presentan las principales líneas de difracción de rayos X que se obtienen para la espinela cúbica, las líneas más intensas están indexadas con los planos cristalinos correspondientes 27.
Además de identificar la fase cristalina de las nanopartículas, a partir de estas medidas, es posible determinar el tamaño de partícula usando la fórmula de Scherrer. Este procedimiento, usualmente brinda tamaños de partículas diferentes que los obtenidos con los métodos de observación directa, como microscopía electrónica de transmisión o microscopía de fuerza atómica, puesto que, en la escala nanométrica la relación superficie/volumen aumenta, lo cual quiere decir que la mayoría de la masa de la NPM se encuentra en la superficie, lo cual provoca la existencia de una fase no cristalina en la NPM, esta fase se incrementa a medida que el tamaño de la partícula disminuye, igualmente la polidispersidad de forma y tamaño también es causante de una determinación sub o sobre valorada del tamaño de partícula 28, la falta de coordinación cristalina cerca de la superficie de la NPM también puede ser provocada por efectos de la capa surfactante usada para estabilizar en suspensión la NPM 29, lo cual se refleja en de las tensiones y deformaciones dentro de la red cristalina de la NPM. Esto es notorio cuando se realizan medidas de difracción de rayos X a muestras de NPM con diferentes tamaños medios 28.
![(a) Estructura cristalina de la magnetita (figura calculada con Materials Project [30]). (b) Líneas de difracción que se esperan obtener para nanopartículas magnéticas de óxidos de hierro y su respectiva indexación](../1794-9165-ince-13-26-00207-gf1.jpg)
Figura 1:
(a) Estructura cristalina de la magnetita (figura calculada con Materials Project [30]). (b) Líneas de difracción que se esperan obtener para nanopartículas magnéticas de óxidos de hierro y su respectiva indexación
Para el caso de la magnetita, existe la posibilidad de un cambio estructural desde la espinela invertida hacia la espinela normal, cuando es sometida a alta presión (mas de 12 GPa a temperatura ambiente) o temperaturas por debajo de la temperatura ambiente (120 K a presión ambiente). Esta transición se conoce como transición de Verwey y está acompañada con cambios en las propiedades físicas de la magnetita 31,32. Esta transición se presenta en partículas de mas de 18 nm de diámetro y es posible observarla como un salto en la magnetización en función de la temperatura. Un estudio detallado de como la transición de Verwey afecta las propiedades físicas de la magnetita se puede encontrar en la referencia 32.
Si bien, a partir de la difracción de rayos X, no es posible diferenciar la magnetita de la maghemita, es posible identificar si otro tipo de óxidos de α-Fe o β-Fe se han formado 33.
3.2 Dispersion de rayos X a bajos ángulos
Después de la caracterización estructural y magnética de las NPM, es necesario determinar si las partículas se organizan en la suspensión. Es decir, si las interacciones entre las partículas son capaces de formar agregados. La forma y tamaño de estos agregados, dependerá de la competencia entre las interacciones repulsivas y atractivas entre las NPM. Así, interacciones de carácter isótropo conllevarán a la formación de estructuras tridimensionales, mientras que las interacciones de carácter anisótropo conllevarán a la formación de estructuras lineales o bidimensionales.
La técnica de dispersión de rayos X a bajos ángulos (SAXS), permite conocer el estado de agregación de las partículas en suspensión, y además, aplicando el modelo adecuado, es posible conocer el tamaño y forma tanto de los agregados como de las partículas individuales.
Debido a la autosimilaridad en la forma de los agregados, las curvas de SAXS se pueden modelar considerando el patrón de dispersión generado por una estructura cuyo tamaño cumple la regla de fractal de masa, esto es, la masa del agregado es proporcional a 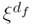 , donde ξ es el radio del agregado y d
f
la dimensión fractal 34.
, donde ξ es el radio del agregado y d
f
la dimensión fractal 34.
De esta forma, se considera que la intensidad de los rayos X dispersados por una suspensión coloidal de NPM de radio r es proporcional al factor de estructura (S(qξ, r)) de un arreglo tipo fractal de masa 35,36,37:
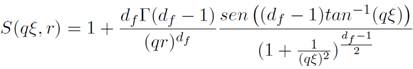 (1)
(1)El patrón SAXS de una suspensión coloidal, cuyas NPM se organizan según la ley de fractal de masa, puede modelarse usando la ecuación (2) 38.
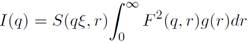 (2)
(2)Donde, F (q, r) es el factor de forma de las NPM, g(r) es la distribución de tamaño de partícula y R es el radio al cual está centrada la función g(r).
En la Figura 2 se presentan simulaciones de curvas y patrones de SAXS obtenidas usando la ecuación (2) para suspensiones de NPM esféricas. Las curvas se presentan como intensidad de la radiación dispersada en función del vector de onda (q), para diferentes configuraciones de partículas con 5 nm de radio.
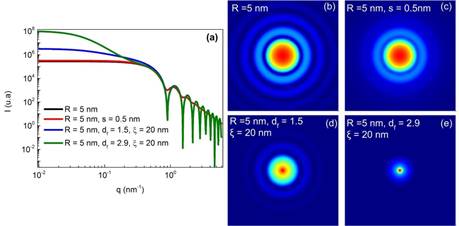
Figura 2:
(a) Curvas de intensidad dispersada en función del vector de onda simuladas para diferentes configuraciones. (b-e) Patrones de dispersión simulados para diferentes configuraciones de tamaño de partículas y agregación.
Se observa un comportamiento característico correspondiente a máximos y mínimos de intensidad, relacionados con el proceso de interferencia entre los rayos X dispersados. El primer mínimo corresponde a q = 4,5/R y está relacionado con el tamaño medio (R) de las partículas.
Los mínimos en las curvas se corresponden con las franjas más oscuras en el patrón de dispersión (Figura 2(b-e)). Estos mínimos, se desvanecen si se aumenta la polidispersidad de tamaño debido a la superposición entre patrones individuales de cada tamaño tal como se observa en la curva roja, para la cual se consideró una distribución gaussiana de tamaños de partícula centrada en 5 nm y con una dispersión de 0.5 nm y en el patrón de la Figura 2(b).
El efecto de la agregación es claramente visible a bajos valores del vector de onda (curvas azul y verde en la Figura 2(a)). Como se dijo anteriormente, valores pequeños de q corresponden a tamaños grandes de partícula, en este caso tamaño del agregado. Para un sistema que no está agregado, (curva negra), para bajos valores de q, la intensidad dispersada se mantiene constante, a medida que las NPM forman agregados hay una cierta dependencia lineal de la intensidad dispersada en esta zona, siendo la pendiente de esta recta la dimensión fractal del agregado. Para la simulación se consideraron dos tipos de arreglos de diferente dimensión fractal y un tamaño de agregado de 20 nm. Finalmente, para los valores mucho más pequeños de q, se recupera la constante, pero esta vez relacionada con el tamaño del agregado, este efecto es claramente visible en la curva verde.
3.3 Determinación del tamaño de partícula y estructura por microscopía electrónica de transmisión
La técnica de microscopía electrónica de transmisión (TEM) se utiliza para determinar la forma, tamaño, dispersión de tamaño, y cristalinidad de las NPM. La calidad de las imágenes obtenidas depende de la resolución del microscopio utilizado, generalmente para para el estudio de NPM es necesario un equipamiento con alta resolución (HRTEM).
Para la determinación del tamaño de partículas, el análisis se realiza mediante una medición individual de cada partícula, esta información se organiza en un histograma, el cual típicamente es ajustado con una función de distribución gaussiana, pero para evitar valores negativos en el ajuste se utiliza una función LogNormal, la cual es una función gaussiana centrada en ln(r o ), siendo r o el centro de la gaussiana.
Los HRTEM, permiten observar NPM individuales e identificar los planos cristalinos de la partícula para determinar su cristalinidad y composición química, cuando es posible. Usualmente la resolución de este microscopio es de 0.17 nm. Una imagen tomada con este tipo de microscopio se puede observar en la Figura 3 para NPM sintetizadas por el método de co-precipitación química (a) y por el método de descomposición térmica (b).
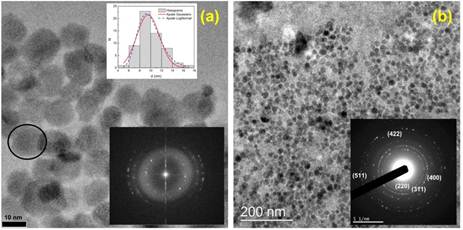
Figura 3:
Imagen TEM de NPM sintetizadas por (a) co-precipitación química (Inset: superior: Histograma de diámetros con ajuste gaussiano y lognormal. Inferior: transformada de Fourier de la imagen), (b) descomposición térmica (Inset: difracción de electrones de la imagen).
Tal como se dijo en la sección de síntesis, las NPM sintetizadas por co-precipitación presentan una mayor dispersión de forma y tamaño, mientras que las NPM sintetizadas por descomposición térmica tienen mayor uniformidad de tamaño y forma.
La calidad cristalina y la composición química de las NPM es posible obtenerse a partir de las imágenes de la Figura 3. El primer método consiste en aplicar la transformada de Fourier a la imagen, tal como se presenta en el inset de la 3(a), esta figura es la representación en el espacio recíproco de la red cristalina. En este caso, se observan máximos de intensidad en forma de anillos que corresponden al espaciamiento de los planos cristalinos, el radio de cada anillo corresponde a una distancia entre planos, para el primernanillo observado, su radio es 0.45 nm que corresponde con la distancia del plano (111) de la magnetita.
Un segundo método, es utilizar difracción de electrones, tal como se presenta en el inset de la 3(b). Esta medida se realiza de forma directa y no necesita de un mayor procesamiento de la imagen. Al igual que en el anterior método, se observan máximos de intensidad correspondientes con los sitios de interferencia constructiva, cada anillo corresponde a un plano cristalino, los cuales han sido indexados correctamente con los planos cristalinos de la magnetita/maghemita según las tarjetas JCPDS 75-0033 for F e 3 O 4 y 39-1346 para γ − F e 2 O 3.
Un tercer método, es medir directamente la distancia entre planos cristalinos, que en la imagen TEM de la Figura 3(a) se observan claramente. Se ha tomado la partícula encerrada en el círculo para medir la distancia entre los planos, el resultado se presenta en la Figura 4.
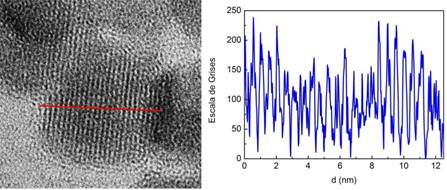
Figura 4:
Imagen TEM de NPM sintetizadas por co-precipitación química donde se observan los planos cristalinos, las distancias entre planos (d) se presentan en la parte derecha de la figura.
El espaciamiento entre planos obtenido en la Figura 4: es d = 0.46±0.01 nm y es comparable con lo reportado en literatura para el plano (111) 39, 40.
La técnica TEM resulta útil para determinar la cristalinidad y composición de las NPM, lo cual la hace una técnica versatil y que algunas veces podría reemplazar la tecnica de difracción de rayos X.
3.4 Propiedades magnéticas determinadas por magnetometría
Con las técnicas de magnetometría, es posible medir el momento magnético de las NPM, así como su respuesta colectiva a los campos magnéticos.
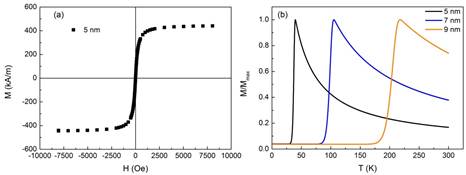
Figura 5
Simulación para un sistema de NPM de 5 nm de diametro y µ = 25190 µ B de una (a) curva de magnetización en función del campo magnético a 300 K y (b) curva de magnetización en función de la temperatura a bajos campos bajo el protocolo ZFC. También se presenta el corrimiento de la temperatura de bloqueo con el tamaño de partícula.
Si esta respuesta colectiva, sigue el comportamiento establecido por la función de Langevin tal como se explicó en la parte I de este artículo 41, el sistema presenta un comportamiento superparamagnético, caracterizado por una curva de magnetización (M vs H) sin histéresis. En el superpara- magnetismo, en ausencia de campo aplicado, las energía térmica es mayor que la energía de anisotropía magnética, por lo cual, la distribución de direcciones de momentos magnéticos es aleatoria y no hay una dirección preferencial de orientación. Esto se puede modificar disminuyendo la temperatura, de forma que la energía de anisotropía magnética sea mayor que la energía térmica, cuando esto sucede, se genera una orientación preferencial y el sistema presenta una pequeña magnetización a campo nulo, generando curvas de M vs H con histéresis.
En la Figura 5(a) se presenta una simulación de la curva de magnetización de una suspensión superparamagnética de partículas de magnetita de 5 nm de radio, cuya magnetización es de 446 kA/m. De esta forma, a cada partícula le corresponde un momento magnético de 25190 µ B y una constante de anisotropía magnética K = 25 kJ/m3. Estos datos han sido tomados de la referencia 42 y son considerados para resolver la función de Langevin y así obtener la curva de magnetización.
Los datos usados en la simulación anterior son los valores típicos para magnetita bulk. Para el caso de las NPM la anisotropía superficial juega un papel dominante y por lo tanto la magnetización de saturación tiende a disminuir del valor bulk de 446kA/m o 86 Am2/kg. Esto se puede visualizar en la Figura 6 donde se han medido curvas de magnetización para tres muestras con diferentes tipos de tamaño.
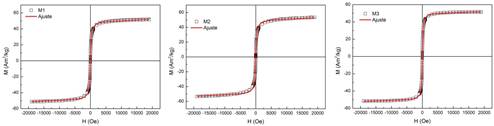
Figura 6:
Curvas de magnetización a temperatura ambiente de NPM de magnetita sintetizadas por co-precipitación química
En este, caso la ecuación de Langevin se utilizó para ajustar las curvas de magnetización experimental, para así obtener M s y el momento magnético medio de las NPM µ. Estos valores se presentan en la Tabla 1, donde los valores de M s son casi la mitad del valor en bulk y tanto el momento magnético como la magnetización de saturación aumentan con el tamaño de partícula, reflejando una menor influencia de la anisitropía superficial.
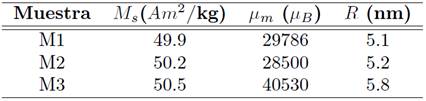
Por otro lado, se observa en la Figura 5(b), la simulación de la magnetización en función de la temperatura. Después de enfriar la muestra en ausencia de campo magnético, se aplica un pequeño campo y se registra la magnetización al aumentar la temperatura, este procedimiento se conoce como medidas de zero field cool (ZFC). Los mismos parámetros anteriormente considerados se utilizaron para realizar la simulación de la Figura 5(b) usando el modelo propuesto por Tournus, Tamion y Bonet (43), 44 (ecuación (3)), en el cual se considera que la magnetización se divide en dos componentes: el primero correspondiente a la magnetización de las partículas superparamagneticas, cuyo comportamiento está dado por la función de Langevin, y el segundo corresponde a la magnetización de las partículas que no se comportan como superparamagnéticas, y por lo tanto la energía de anisotropía es mayor a la energía magnética y a la energía térmica.
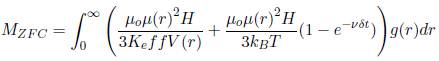 (3)
(3)3.5 Medidas calorimétricas de disipación de calor en campos de radiofrecuencia
La calidad de las NPM para su aplicación en hipertermia magnética, se mide por medio de su capacidad de absorber energía de un campo magnético RF y disiparla en forma de calor; el parámetro que cuantifica esta capacidad es el SAR. Como se expresó en primera parte de este artículo, el SAR depende tanto de parámetros del campo, como la amplitud y la frecuencia, como de los parámetros del medio como la viscosidad y de los propiedades de las partículas como su tamaño y propiedades magnéticas.
En la Figura 7 se presentan resultados experimentales del SAR en función del cuadrado de la amplitud del campo aplicado para la muestra M3, algunas de sus propiedades se presentaron en la Tabla 1, y del SAR como función de la frecuencia del campo RF para la misma muestra, consistente en NPM de magnetita de 25 nm de diámetro y M s = 73 Am 2/kg. Para las simulaciones se usó una constante de anisotropía efectiva (K eff ) de 4.7 kJ/m 3 para la muestra M3 y de 2.9 kJ/m 3 para la muestra M4.
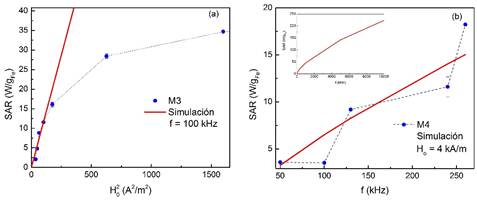
Figura 7:
(a) SAR en función del cuadrado de la amplitud de campo (H o 2) a frecuencia constante de 100 kHz para la muestra M3 de la Tabla 1. (b) SAR en función de la frecuencia del campo RF a amplitud de campo constante de 4 kA/m para la muestra M3 de la Tabla 1. Inset: Extrapolación del SAR a frecuencias mayores a las medidas experimentalmente. Las líneas contínuas representan la simulación del SAR usando la ecuación (20) de la parte I
Se observa en la Figura 7(a), que la simulación usando la ecuación 20 de la parte 1, solo reproduce los valores de SAR para campos menores a 10 kA/m, observandose un comportamiento lineal del SAR como función de H o 2. Este comportamiento es el esperado y predicho por la teoría de respuesta lineal y expuesto en la ecuación 20 de la parte 1. Para campos mayores a 10 kA/m la linealidad se pierde, puesto que la teoría de respuesta lineal ya no es válida y la capacidad de absorber energía del campo RF, relacionada con el área del ciclo de magnetización, tiende a obtener un valor máximo. El máximo valor de SAR se logra cuando el campo aplicado es lo suficientemente intenso para magnetizar a saturación la muestra.
En el caso de la Figura 7(b), se observa que si bien, el valor numérico del SAR no es reproducido por la simulación, si es posible reproducir el comportamiento creciente de los datos. En el inset de esta misma figura se observa una extrapolación del SAR hasta una frecuencia de 10000 kHz, con el fin de demostrar el comportamiento siempre creciente del SAR con la frecuencia del campo aplicado.
El valor de K eff usado es menor que el valor reportado para magnetita (23 -41 kJ/m 3) o para maghemita en bulk (4.6 kJ/m 3) 42. Está disminución en el valor de K eff a partir del valor del bulk tiene dos origenes, el primero es la disminución del tamaño de partícula, a medida que se disminuye la dimensión, la anisotropía superficial domina sobre la anisotropía volumétrica, resultado en una disminución de la anisotropía total. La segunda corresponde a una disminución debida a las interacciones dipolares, tal como fue expuesto en la primera parte de este artículo.
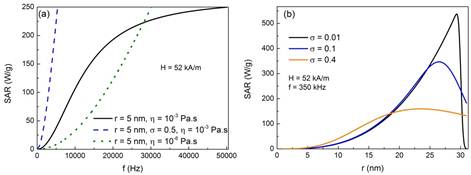
Figura 8:
(a) Dependencia del SAR con la frecuencia del campo RF y las propiedades de las partículas y el medio. (b). Dependencia del SAR con el tamaño de partícula y su polidispersidad usando la ecuación 20
En la Figura 8(a), se observa el comportamiento del SAR en función de la frecuencia del campo RF para diferentes parámetros, del medio y las partículas. El SAR aumenta a medida que aumenta la frecuencia, presentando dos tipos de comportamientos, una zona de rápido aumento (frecuencias bajas) y una zona de un aumento lento (frecuencias altas). Este tipo de comportamiento está relacionado con la funcionalidad de la componente fuera de fase de la susceptibilidad (χ(f )) la cual presenta un máximo que coincide con el punto de inflexión de la curva negra en la Figura 8(a). Después del máximo de χ(f ), el comportamiento del SAR lo determina la componente lineal de la ecuación para determinar el SAR.
Por otro lado, un aumento en el SAR para todo el rango de frecuencias, se logra aumentando la polidispersidad de tamaño de las NPM, tal como se observa en la Figura 8(a). Si bien, esto es posible, la adecuada elección de una frecuencia para obtener el mayor SAR, depende de que tan cerca se encuentren las partículas de su condición de resonancia, dada por ωτ =1, siendo τ dependiente del tamaño de partícula. De esta forma, al tener una distribución de tamaños, también se tiene una distribución de tiempos de relajación. El mayor SAR se obtendrá si se hace coincidir lo máximos de la distribución de tamaños y la susceptibilidad fuera de fase.
Este efecto puede visualizarse en la Figura 8(b), en la cual se han simulado curvas de SAR como función del tamaño de partícula para diferentes anchos (σ) de una distribución LogNormal de tamaños. Se observa el máximo SAR cuando se cumple la condición de resonancia, pero en esa condición, el SAR disminuye cuando aumenta la polidispersidad, lo contrario se observa cuando se sale de la condición de resonancia, donde, para los mayores tamaños se activa el mecanismo de relajación de Néel, y para menores tamaños se activa el mecanismo de relajación de Brown.
Si se disminuye la viscosidad del medio, es decir, se permite que las partículas roten sin oposición del medio en el cual se encuentran dispersas, se libera el mecanismo de relajación de Brown, y por lo tanto se modifica el tiempo de relajación de las NPM, resultando esto, en una modificación del SAR. Si bien, como se presenta en la curva verde punteada de la Figura 8(a) para bajas frecuencias, esto conlleva a una disminución del SAR, es posible, aumentando la frecuencia, llevar al sistema a una condición donde esto se revierte.
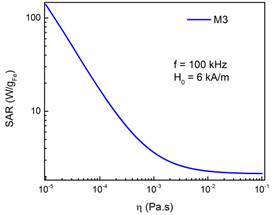
Figura 9:
Dependencia del SAR con la viscosidad del medio para la muestra M3 usando la ecuación 20 de la parte I
Una simulación para la muestra M3 del SAR como función de la viscosidad del medio se presenta en la Figura 9, en esta figura se observa como el SAR disminuye a medida que la viscosidad de la muestra aumenta, esto es consitente con observaciones experimentales del SAR en diferentes medios viscosos, donde se ha observado que cuando el mecanismo de Brown se activa (baja viscosidad), el SAR aumenta en comparación del SAR determinado usando solo el mecanismo de Néel 45.
Para finalizar, se presenta en la Figura 10 el comportamiento del SAR en función de los parámetros físicos de la partícula, tales como tamaño, magnetización de saturación e interacción dipolar, modulada por la concentración de la muestra M3 para una frecuencia de 100 kHz y H o = 6kA/m.
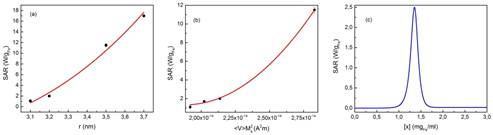
Figura 10:
Dependencia del SAR con la (a) el tamaño de partícula, (b) el factor <V>M s 2 y (c) la concentración para la muestra M3, para una frecuencia de 100 kHz y H o = 6kA/m. Las lineas contínuas en (a) y (b) representan el mejor ajuste logrado para los datos experimentales.
De esta forma se observa como el SAR aumenta cuando aumenta el tamaño de partícula y el factor <V>M s 2 que corresponde al prefactor en la ecuación 20 de la parte I. Los puntos de la Figura 10(a) fueron ajustados con un polinomio de tercer orden, comprobando el modelo expuesto anteriormente, mientras que los datos de la Figura 10(b) fueron ajustados con un polinomio de segundo orden. Si bien es el comportamiento esperado para los datos de SAR vs r, se espera que el comportamiento del SAR vs <V>M s 2 sea lineal. Desviaciones a este comportamiento se podrían atribuir a la depedencia con el tamaño de partícula con la constante de anisotropía y con el hecho de que se está forzando el modelo al sacar de la integral el volumen de la partícula, el cual está convolucionado con el factor de frecuencia.
En la Figura 10(c), se presenta la dependencia del SAR con la interacción dipolar magnética, modulada por la concentración de partículas, para la muestra M3. El comportamiento observado en la Figura 10(c) es predicho tanto por las ecuaciones presentadas en la parte I, la energía ∆E de la barrera de energía, es linealmente proporcional a un término dependiente de la distancia entre partículas. De esta forma, al dismuniur la concentración, se aumenta la distancia entre partículas, se aumenta la energía de la barrera y por lo tanto se modifica el tiempo de relajación de las NPM, a condición de amplitud (6 kA/m) y frecuencia constante (100 kHz), el máximo SAR ocurre cuando la distancia entre partículas es tal, que se cumple la condición de resonancia antes descrita.
4 Conclusiones
El uso de nanopartículas magnéticas de óxidos de hierro en el tratamiento del cáncer por hipertermia magnética, es posible si se conocen las propiedades físicas y químicas de las NPM, en especial, las que determinan la transducción de energía electromagnética a energía térmica. El desarrollo de modelos matemáticos ha permitido determinar estas propiedades a partir del análisis de los datos obtenidos experimentalmente.
Igualmente, se hace necesario una correcta interpretación de los datos, permitiendo obtener una predicción aceptable de la disipación de calor bajo campos de radiofrecuencia. En este sentido, es útil determinar la variación de esta propiedad al variar los parámetros del campo RF y del medio en el cual se encuentran dispersas la NPM, ya que en una aplicación práctica, las NPM dentro del tumor se encuentran agregadas y en un entorno fisícamente interactuante y químicamente agresivo.
Los datos obtenidos a partir de la caracterización, permiten que se desarrollen nuevos métodos de síntesis, o se modifiquen los ya existentes para que su respuesta disispativa se de dentro de la teoría de respuesta lineal, para así poder aplicar de forma predictiva los modelos estudiados en este artículo.
Agradecimientos
Los autores agradecen la colaboración de la Institución Universitarua CES- MAG (Pasto-Colombia), el Centro de Investigación de Materiales de la Universidad de Nariño (Pasto-Colombia), el Instituto de Física de La Plata (La Plata-Argentina) y a Colciencias-Colombia.
Referencias
1. J. Lin, Z. Pan, L. Song, Y. Zhang, Y. Li, Z. Hou, and C. Lin, “Design and in vitro evaluation of self-assembled indometacin prodrug nanoparticles for sustained/controlled release and reduced normal cell toxicity,” Applied Surface Science, vol. 425, pp. 674 - 681, 2017. (Online). Available:http://www.sciencedirect.com/science/article/pii/S016943321732024X 208
2. Z. Nemati, S. Salili, J. Alonso, A. Ataie, R. Das, M. Phan, and H. Srikanth, “Superparamagnetic iron oxide nanodiscs for hyperthermia therapy: Does size matter?” Journal of Alloys and Compounds, vol. 714, pp. 709 - 714, 2017. (Online). Available: http://www.sciencedirect.com/science/article/pii/S0925838817314068 209
3. A. Sood, V. Arora, J. Shah, R. Kotnala, and T. K. Jain, “Multifunctional gold coated iron oxide core-shell nanoparticles stabilized using thiolated sodium alginate for biomedical applications,” Materials Science and Engineering: C, vol. 80, pp. 274 - 281, 2017. (Online). Available: http://www.sciencedirect.com/science/article/pii/S0928493116324067 209
4. J.-Q. Tang, X.-Y. Hou, C.-S. Yang, Y.-X. Li, Y. Xin, W.-W. Guo, Z.-P. Wei, Y.-Q. Liu, and G. Jiang, “Recent developments in nanomedicine for melanoma treatment,” International Journal of Cancer, vol. 141, no. 4, pp. 646-653, 2017. (Online). Available: http://dx.doi.org/10.1002/ijc.30708 209
5. C. Strehl, L. Maurizi, T. Gaber, P. Hoff, T. Broschard, A. R. Poole, H. Hofmann, and F. Buttgereit, “Modification of the surface of superparamagnetic iron oxide nanoparticles to enable their safe application in humans,” International Journal of Nanomedicine, vol. 11, pp. 5883-5896, 2016. (Online). Available: http://dx.doi.org/10.2147/IJN.S110579 209
6. A. K. Silva, A. Nicolas-Boluda, L. Fouassier, and F. Gazeau, “Overcoming the tumor microenvironment: the role of nanohyperthermia,” Nanomedicine, vol. 12, no. 11, pp. 1213-1215, 2017. (Online). Available: https://doi.org/10.2217/nnm-2017-0096209
7. S. Sun, H. Zeng, D. B. Robinson, S. Raoux, P. M. Rice, S. X. Wang, and G. Li, “Monodisperse mfe2o4 (m = fe, co, mn) nanoparticles,” Journal of the American Chemical Society, vol. 126, no. 1, pp. 273-279, 2004, pMID: 14709092. (Online). Available: http://dx.doi.org/10.1021/ja0380852 210, 211
8. A. G. Roca, M. P. Morales, K. O’Grady, and C. J. Serna, “Structural and magnetic properties of uniform magnetite nanoparticles prepared by high temperature decomposition of organic precursors,” Nanotechnology, vol. 17, no. 11, p. 2783, 2006. (Online). Available: http://stacks.iop.org/0957-4484/17/i=11/a=010 210
9. T. Yang, C. Shen, Z. Li, H. Zhang, C. Xiao, S. Chen, Z. Xu, D. Shi, J. Li, and H. Gao, “Highly ordered self-assembly with large area of fe3o4 nanoparticles and the magnetic properties,” The Journal of Physical Chemistry B, vol. 109, no. 49, pp. 23 233-23 236, 2005, pMID: 16375287. (Online). Available: http://dx.doi.org/10.1021/jp054291f 210, 211
10. T. Hyeon, S. S. Lee, J. Park, Y. Chung, and H. B. Na, “Synthesis of highly crystalline and monodisperse maghemite nanocrystallites without a size-selection process,” Journal of the American Chemical Society , vol. 123, no. 51, pp. 12 798-12 801, 2001, pMID: 11749537. (Online). Available: http://dx.doi.org/10.1021/ja016812s 210
11. P. Tartaj, M. del Puerto Morales, S. Veintemillas-Verdaguer, T. González- Carreño, andC. J. Serna , “The preparation of magnetic nanoparticles for applications in biomedicine,” Journal of Physics D: Applied Physics, vol. 36, no. 13, p. R182, 2003. (Online). Available: http://stacks.iop.org/0022-3727/36/i=13/a=202 210, 211
12. N. R. Jana, Y. Chen, and X. Peng, “Size- and shape-controlled magnetic (cr, mn, fe, co, ni) oxide nanocrystals via a simple and general approach,” Chemistry of Materials, vol. 16, no. 20, pp. 3931-3935, 2004. (Online). Available: http://dx.doi.org/10.1021/cm049221k 210
13. P. D. Cozzoli, E. Snoeck, M. A. Garcia, C. Giannini, A. Guagliardi, Cervellino, F. Gozzo, A. Hernando, K. Achterhold, N. Ciobanu, F. G. Parak, R. Cingolani, and L. Manna, “Colloidal synthesis and characterization of tetrapod-shaped magnetic nanocrystals,” Nano Letters, vol. 6, no. 9, pp. 1966-1972, 2006. (Online). Available: http://dx.doi.org/10.1021/nl061112c 210
14. C. B. Murray, S. Sun, W. Gaschler, H. Doyle, T. A. Betley, and C. R. Kagan, “Colloidal synthesis of nanocrystals and nanocrystal superlattices,” IBM Journal of Research and Development, vol. 45, no. 1, pp. 47-56, Jan 2001. 210
15. J. Cheon, N.-J. Kang, S.-M. Lee, J.-H. Lee, J.-H. Yoon, and S. J. Oh, “Shape evolution of single-crystalline iron oxide nanocrystals,” Journal of the American Chemical Society , vol. 126, no. 7, pp. 1950-1951, 2004, pMID: 14971924. (Online). Available: http://dx.doi.org/10.1021/ja038722o 210
16. D. K. Yi, S. T. Selvan, S. S. Lee , G. C. Papaefthymiou, D. Kundaliya, and J. Y. Ying, “Silica-coated nanocomposites of magnetic nanoparticles and quantum dots,” Journal of the American Chemical Society, vol. 127, no. 14, pp. 4990-4991, 2005, pMID: 15810812. (Online). Available: http://dx.doi.org/10.1021/ja0428863 211
17. T. Pellegrino, L. Manna , S. Kudera, T. Liedl, D. Koktysh, A. L. Rogach, S. Keller, J. Rädler, G. Natile, and W. J. Parak, “Hydrophobic nanocrystals coated with an amphiphilic polymer shell: A general route to water soluble nanocrystals,” Nano Letters , vol. 4, no. 4, pp. 703-707, 2004. (Online). Available: http://dx.doi.org/10.1021/nl035172j 211
18. B. BITTOVA, J. P. VEJPRAVOVA, M. P. DEL MORALES, A. G. ROCA, D. NIZNANSKY, and A. MANTLIKOVA, “Influence of aggregate coating on relaxations in the systems of iron oxide nanoparticles,” Nano, vol. 07, no. 01, p. 1250004, 2012. (Online). Available: http://www.worldscientific.com/doi/abs/10.1142/S179329201250004X 211
19. I. Nedkov, T. Merodiiska, L. Slavov, R. Vandenberghe, Y. Kusano, and J. Takada, “Surface oxidation, size and shape of nano-sized magnetite obtained by co-precipitation,” Journal of Magnetism and Magnetic Materials, vol. 300, no. 2, pp. 358 - 367, 2006. (Online). Available: http://www.sciencedirect.com/science/article/pii/S0304885305005433 211
20. K. Tao, H. Dou, and K. Sun, “Interfacial coprecipitation to prepare magnetite nanoparticles: Concentration and temperature dependence,” Colloids and Surfaces A: Physicochemical and Engineering Aspects, vol. 320, no. 1-3, pp. 115 - 122, 2008. (Online). Available: http://www.sciencedirect.com/science/article/pii/S0927775708000721 211
21. T. J. Daou, G. Pourroy, S. Bégin-Colin, J. M. Grenèche, C. Ulhaq-Bouillet, P. Legaré, P. Bernhardt, C. Leuvrey, and G. Rogez, “Hydrothermal synthesis of monodisperse magnetite nanoparticles,” Chemistry of Materials , vol. 18, no. 18, pp. 4399-4404, 2006. (Online). Available: http://dx.doi.org/10.1021/cm060805r 211
22. D. Kim, S. Lee, K. Im, K. Kim, K. Kim , I. Shim, M. Lee, and Y.-K. Lee, “Surface-modified magnetite nanoparticles for hyperthermia: Preparation, characterization, and cytotoxicity studies,” Current Applied Physics, vol. 6, Supplement 1, pp. e242 - e246, 2006, Nano Korea 2005 Symposium (Online). Available: http://www.sciencedirect.com/science/article/pii/S1567173906000496 211
23. R. Massart, “Preparation of aqueous magnetic liquids in alkaline and acidic media,” IEEE Transactions on Magnetics, vol. 17, no. 2, pp. 1247-1248, Mar 1981. 211
24. S. Laurent, D. Forge, M. Port, A. Roch, C. Robic, L. Vander Elst , and R. N. Muller, “Magnetic iron oxide nanoparticles: Synthesis, stabilization, vectorization, physicochemical characterizations, and biological applications,” Chemical Reviews, vol. 108, no. 6, pp. 2064-2110, 2008, pMID: 18543879. (Online). Available: http://dx.doi.org/10.1021/cr068445e 212
25. D. C. Lee, D. K. Smith, A. T. Heitsch, and B. A. Korgel, “Colloidal magnetic nanocrystals: synthesis, properties and applications,” Annu. Rep. Prog. Chem., Sect. C: Phys. Chem., vol. 103, pp. 351-402, 2007. (Online). Available: http://dx.doi.org/10.1039/B605630J 212
26. M. E. Fleet, “The structure of magnetite: Symmetry of cubic spinels,” Journal of Solid State Chemistry, vol. 62, no. 1, pp. 75 - 82, 1986. (Online). Available: http://www.sciencedirect.com/science/article/pii/0022459686902185 212
27. A. Jain, S. P. Ong, G. Hautier, W. Chen, W. D. Richards, S. Dacek, S. Cholia, D. Gunter, D. Skinner, G. Ceder, and K. A. Persson, “The Materials Project: A materials genome approach to accelerating materials innovation,” APL Materials, vol. 1, no. 1, p. 011002, 2013. (Online). Available: http://link.aip.org/link/AMPADS/v1/i1/p011002/s1&Agg=doi 212
28. G. F. Goya, T. S. Berquó, F. C. Fonseca, andM. P. Morales , “Static and dynamic magnetic properties of spherical magnetite nanoparticles,” Journal of Applied Physics, vol. 94, no. 5, pp. 3520-3528, 2003. (Online). Available: http://dx.doi.org/10.1063/1.1599959 213
29. M. Khalkhali, K. Rostamizadeh, S. Sadighian, F. Khoeini, M. Naghibi, and M. Hamidi, “The impact of polymer coatings on magnetite nanoparticles performance as mri contrast agents: a comparative study,” DARU Journal of Pharmaceutical Sciences, vol. 23, no. 1, p. 45, 2015. (Online). Available: http://dx.doi.org/10.1186/s40199-015-0124-7 213
30. K. Persson, “Materials data on fe3o4 (sg:227) by materials project,” Jan 2015. (Online). Available: http://www.osti.gov/dataexplorer/servlets/purl/1194194 213
31. G. K. Rozenberg, Y. Amiel, W. M. Xu, M. P. Pasternak, R. Jeanloz, M. Hanfland, and R. D. Taylor, “Structural characterization of temperature- and pressure-induced inverse↔normal spinel transformation in magnetite,” Phys. Rev. B, vol. 75, p. 020102, Jan 2007. (Online). Available: http://link.aps.org/doi/10.1103/PhysRevB.75.020102214
32. F. Walz, “The verwey transition - a topical review,” Journal of Physics: Condensed Matter, vol. 14, no. 12, p. R285, 2002. (Online). Available: http://stacks.iop.org/0953-8984/14/i=12/a=203 214
33. S. Sun andH. Zeng , “Size-controlled synthesis of magnetite nanoparticles,” Journal of the American Chemical Society , vol. 124, no. 28, pp. 8204-8205, 2002, pMID: 12105897. (Online). Available: http://dx.doi.org/10.1021/ja026501x 214
34. D. W. SCHAEFER, “Polymers, fractals, and ceramic materials,” Science, vol. 243, no. 4894, pp. 1023-1027, 1989. (Online). Available: http://science.sciencemag.org/content/243/4894/1023 214
35. E. S. Gonçalves, D. R. Cornejo, C. L. P. Oliveira, A. M. Figueiredo Neto , J. Depeyrot, F. A. Tourinho, and R. Aquino, “Magnetic and structural study of electric double-layered ferrofluid with mnfe2o4@γ fe2o3 nanoparticles of different mean diameters: Determination of the magnetic correlation distance,” Phys. Rev. E, vol. 91, p. 042317, Apr 2015. (Online). Available: http://link.aps.org/doi/10.1103/PhysRevE.91.042317 214
41. T. Freltoft, J. K. Kjems, and S. K. Sinha, “Power-law correlations and finite- size effects in silica particle aggregates studied by small-angle neutron scattering,” Phys. Rev. B , vol. 33, pp. 269-275, Jan 1986. (Online). Available: https://link.aps.org/doi/10.1103/PhysRevB.33.269 214
37. S.-H. Chen and J. Teixeira, “Structure and fractal dimension of protein- detergent complexes,” Phys. Rev. Lett., vol. 57, pp. 2583-2586, Nov 1986. (Online). Available: https://link.aps.org/doi/10.1103/PhysRevLett.57.2583 214
38. A. Guinier and G. Fournet, Small-angle scattering of X-rays, ser. Structure of matter series . Wiley, 1955. 215
39. Z. Zhou, Z. Zhao, H. Zhang, Z. Wang, X. Chen, R. Wang, Z. Chen, and J. Gao, “Interplay between longitudinal and transverse contrasts in fe3o4 nanoplates with (111) exposed surfaces,” ACS Nano , vol. 8, no. 8, pp. 7976-7985, 2014, pMID: 25093532. (Online). Available: http://dx.doi.org/10.1021/nn5038652 218
40. H. Yang, T. Ogawa, D. Hasegawa, and M. Takahashi, “Synthesis and magnetic properties of monodisperse magnetite nanocubes,” Journal of Applied Physics , vol. 103, no. 7, p. 07D526, 2008. (Online). Available: http://dx.doi.org/10.1063/1.2833820 218
41. D. F. Coral and J. Mera, “Una guía para el estudio de nanopartículas magnéticas de óxidos de hierro con aplicaciones biomédicas. parte 1,” Ingeniería y Ciencia - ing.cienc., vol. 13, no. 25, pp. 229-249, 2017. 219
47. R. Rosensweig, “Heating magnetic fluid with alternating magnetic field,” Journal of Magnetism and Magnetic Materials , vol. 252, pp. 370 - 374, 2002, proceedings of the 9th International Conference on Magnetic Fluids. (Online). Available: http://www.sciencedirect.com/science/article/pii/S0304885302007060 220, 222
43. F. Tournus and E. Bonet, “Magnetic susceptibility curves of a nanoparticle assembly, i: Theoretical model and analytical expressions for a single magnetic anisotropy energy,” Journal of Magnetism and Magnetic Materials, vol. 323, no. 9, pp. 1109 - 1117, 2011. (Online). Available: http://www.sciencedirect.com/science/article/pii/S0304885310008401 221
44. F. Tournus and A. Tamion, “Magnetic susceptibility curves of a nanoparticle assembly ii. simulation and analysis of zfc/fc curves in the case of a magnetic anisotropy energy distribution,” Journal of Magnetism and Magnetic Materials , vol. 323, no. 9, pp. 1118 - 1127, 2011. (Online). Available: http://www.sciencedirect.com/science/article/pii/S0304885310008413 221
45. D. Serantes, K. Simeonidis, M. Angelakeris, O. Chubykalo-Fesenko, M. Marciello, M. d. P. Morales, D. Baldomir, and C. Martinez-Boubeta, “Multiplying magnetic hyperthermia response by nanoparticle assembling,” The Journal of Physical Chemistry C, vol. 118, no. 11, pp. 5927-5934, 2014. (Online). Available: http://dx.doi.org/10.1021/jp410717m 225