Virus de la influenza
Virus de la influenza
Biomédica, vol. 36, núm. 2, 2016
Instituto Nacional de Salud
Recepción: 23 Noviembre 2015
Aprobación: 01 Marzo 2016
El virus de la influenza es un importante agente patógeno humano que causa infecciones respiratorias y una considerable morbimortalidad anual a nivel mundial (1,2). El virus puede circular esporádicamente durante brotes locales como parte de una epidemia estacional o puede generar una pandemia mundial. Durante las epidemias estacionales, la mortalidad se reporta principalmente entre personas muy jóvenes y adultos mayores; la Organización Mundial de la Salud estima que cada año se presentan entre tres y cinco millones de casos de enfermedad grave y de 250.000 a 500.000 muertes en el mundo (3,4). Las pandemias de influenza se presentan cuando se produce un reordenamiento genético del virus (antigen shift) que da lugar a una variante antigénicamente novedosa para la cual no hay anticuerpos en la población. Hasta la fecha se han reportado pandemias en 1918, 1957, 1968 y 2009, las cuales causaron la muerte de 60 millones de personas, aproximadamente (5,6,7,8).
El virus de la influenza pertenece a la familia Orthomixoviridae y comprende tres tipos (A, B y C), cuyas diferencias radican en la base de un antígeno soluble (antígeno S) que se asocia con la ribonucleoproteína interna del virión; el tipo viral puede diferenciarse a partir de las propiedades biológicas de las proteínas proyectadas en la superficie de la envoltura, las glucoproteínas hemaglutinina (H) y neurominidasa (N) (9), diferenciación que da lugar a 15 subtipos de H y nueve subtipos de N. Sin embargo, solo tres subtipos de la hemaglutinina (H1, H2 y H3) y dos subtipos de la neurominidasa (N1 y N2) se han establecido en la población humana (10).
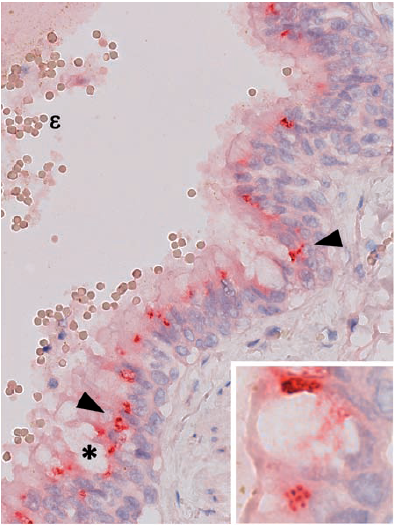
Figura 1.
Antígenos del virus de influenza A H1N1/v09 en células infectadas de tejido pulmonar de un paciente fallecido por la influenza, cuyo caso fue reportado en la pandemia de 2009 en Colombia.
Se observa inmunorreacción en las células del epitelio pseudoestratificado (puntas de flecha) y en las células caliciformes (*) del bronquiolo pulmonar. El epitelio bronquiolar está cubierto a lo largo de toda su superficie con moco rico en polisacáridos, y sus células presentan el antígeno viral con una distribución homogénea y persistente en la superficie apical del citoplasma. En la región basal del epitelio se observan células que descansan sobre la lámina propia sin ningún cambio morfológico evidente. En el inserto sobresale la presencia del antígeno viral en las células caliciformes del epitelio bronquiolar. Se observan eritrocitos en la luz del bronquiolo (ε). Inmunohistoquímica mediante el sistema de fosfatasa alcalina; anticuerpo usado: anti-influenza A para antígeno viral (Chemicon International), 1.000X; inserto, 3.200X.
El diagnóstico clínico de la infección por el virus de la influenza es presuntivo, por lo cual se requiere la confirmación por el laboratorio. Los métodos tradicionales de diagnóstico incluyen el aislamiento viral o la serología (11,12), la detección del genoma viral mediante la hibridación in situ o PCR de transcripción inversa en tiempo real (realtime reverse transcriptase PCR, rRT-PCR) para evaluar la expresión génica en los tejidos y células (13,14,15), y la detección de antígenos mediante anticuerpos monoclonales y policlonales en los tejidos fijados con formol e incluidos en parafina utilizando métodos inmunohistoquímicos (16,17,18).
Uno de los principales tipos de células que el virus infecta son las células ciliadas del epitelio bronquiolar, como se ilustra en la figura 1. En este tipo celular, la localización de los antígenos virales en el epitelio bronquiolar está asociada a la presencia de los receptores ácido siálico y galactosa α-2,6. Estos receptores son reconocidos por la hemaglutinina de la partícula viral que media la formación del endosoma en la célula huésped (19,20), y se encuentran distribuidos principalmente en el epitelio bronquiolar y en menor medida en las áreas alveolares (21).
Conflicto de intereses
Los autores declaramos que no existen conflictos de intereses.
Agradecimientos
Este trabajo fue financiado por la Dirección de Investigación en Salud Pública del Instituto Nacional de Salud.
Referencias
1. Schnitzler SU, Schnitzler P. An update on swine-origin influenza virus A/H1N1: A review. Virus Genes. 2009;39:279-92. http://dx.doi.org/10.1007/s11262-009-0404-8
2. Taubenberger J, Morens D. The pathology of influenza virus infections. Annu Rev Pathol. 2008;3:499-522. http://dx.doi.org/10.1146/annurev.pathmechdis.3.121806.154316
3. World Health Organization. Influenza (seasonal). Fact sheet N° 211, March, 2014. Fecha de consulta: 14 de octubre de 2015. Disponible en: http://www.who.int/mediacentre/factsheets/fs211/en.
4. Barker W, Mullooly J. Pneumonia and influenza deaths during epidemics: Implications for prevention. Arch Intern Med. 1982;142:85-9. http://dx.doi.org/10.1001/archinte.1982.00340140087016
5. Michaelis M, Doerr HW, Cinatl J Jr. An influenza A H1N1 virus revival - pandemic H1N1/09 virus. Infection. 2009;37: 381-9. http://dx.doi.org/10.1007/s15010-009-9181-5
6. Sullivan SJ, Jacobson RM, Dowdle WR, Poland GA. 2009 H1N1 influenza. Mayo Clin Proc. 2010;85:64-76. http://dx.doi.org/10.4065/mcp.2009.0588
7. Craighead J. Influenza viruses. En: Craighead J, editor. Pathology and pathogenesis of human viral disease. First edition. St. Louis: Academic Press; 2000. p. 35-46.
8. Instituto Nacional de Salud. Semana epidemiológica número 18 de 2010. Boletín Epidemiológico Semanal del 2 al 8 de mayo de 2010. Bogotá, D.C.: INS; 2010.
9. Hinrichs S, Harrison C, Haggerty S. Viral diseases. En: Damjanov I, Linder J, editors. Anderson’s pathology. Tenth edition. St. Louis: Mosby Yearbook Inc.; 1996. p. 922-3.
10. Nicholson K, Wood J, Zambon M. Influenza. Lancet. 2003; 362:1733-45. http://dx.doi.org/10.1016/S0140-6736(03)14854-4
11. Teichtahl H, Buckmaster N, Pertnikovs E. The incidence of respiratory tract infection in adults requiring hospitalization for asthma. Chest. 1997;112:591-6. http://dx.doi.org/10.1378/chest.112.3.591
12. Mäkelä MJ, Nikkari S, Meurman O, Laine M, Arvilommi H. Virus-specific, antibody-secreting cells during upper respiratory infections. J Med Virol. 1995;47:416-20.
13. Guarner J, Shieh W, Dawson J, Subbarao K, Shaw M, Ferebee T, et al. Immunohistochemical and in situ hybridization studies of influenza A virus infection in human lungs. Am J Clin Pathol. 2000;114:227-33. http://dx.doi.org/10.1309/HV74-N24T-2K2C-3E8Q
14. Cheon S, Chae C, Lee Y. Detection of nucleic acids of porcine reproductive and respiratory syndrome virus in the lungs of naturally infected piglets as determined by in-situ hybridization. J Comp Pathol. 1997;117:157-63.
15. World Health Organization. CDC protocol of real time RTPCR for influenza H1N1. Geneva: WHO Fecha de consulta: 19 de noviembre de 2015. Disponible en: http://www.who.int/csr/resources/publications/swineflu/realtimeptpcr/en/.
16. Haines D, Waters E, Clark E. Immunohistochemical detection of swine influenza virus in formalin-fixed and paraffin-embedded tissues. Can J Vet Res. 1993;57:33-6.
17. Vincent L, Janke B, Paul P, Halbur P. A monoclonal antibody–based immunohistochemical method for the detection of swine influenza virus in formalin-fixed, paraffinembedded tissues. Vet Diagn Invest.1997;9:191-5. http://dx.doi.org/10.1177/104063879700900214
18. Guarner J, Paddock C, Shieh W, Packard M, Patel M, Montague J, et al. Histopathologic and immunohistochemical features of fatal influenza virus infection in children during the 2003-2004 season. Clin Infect Dis. 2006;43:132-40. http://dx.doi.org/10.1086/505122
19. Rogers G, Paulson J. Receptor determinants of human and animal influenza virus isolates: Differences in receptor specificity of the H3 hemagglutinin based on species of origin. Virology. 1983;127:361-73.
20. Gagneux P, Cheriyan M, Hurtado-Ziola N, van der Linden E, Anderson D, McClure H, et al. Human-specific regulation of alpha 2-6-linked sialic acids. J Biol Chem. 2003;278: 48245-50. http://dx.doi.org/10.1074/jbc.M309813200
21. Nelli R, Kuchipudi S, White G, Pérez B, Dunham S, Chang K. Comparative distribution of human and avian type sialic acid influenza receptors in the pig. BMC Vet Res. 2010;6:4. http://dx.doi.org/10.1186/1746-6148-6-4