PRESENTACIÓN DE CASO
Recepción: 19 Abril 2016
Aprobación: 28 Marzo 2017
DOI: 10.7705/biomedica.v38i0.3273
Resumen:
El factor de necrosis tumoral alfa (FNTα) es una citocina fundamental en la reacción inmunitaria frente al cáncer y a infecciones tales como la tuberculosis. Esta molécula también desempeña un papel fundamental en la patogenia de enfermedades complejas y de difícil tratamiento, como la artritis reumatoidea, la espondilitis anquilosante, la enfermedad de Crohn, la psoriasis y la colitis ulcerativa, condiciones que suelen requerir el uso de medicamentos que antagonizan la función del factor de necrosis tumoral alfa, el cual se ha relacionado con un incremento del riesgo de desarrollar tuberculosis, micosis y otras infecciones graves.
Se reporta el caso de un hombre de 68 años de edad con diagnóstico de enfermedad de Crohn, a quien se le administró tratamiento con antagonistas del FNTα, debido a lo cual desarrolló tuberculosis diseminada. El diagnóstico se hizo con base en los hallazgos histológicos y mediante pruebas de biología molecular.
Se discuten la presentación clínica y el manejo del caso, y se hace un análisis comparativo de los casos de tuberculosis asociados al tratamiento con antagonistas del FNTα reportados en Colombia durante los últimos diez años, con especial énfasisen la detección y el tratamiento de la tuberculosis latente.
Palabras clave: Mycobacterium tuberculosis, tuberculosis, tuberculosis latente, enfermedad de Crohn, diagnóstico, factor de riesgo, factor de necrosis tumoral alfa, Colombia.
Abstract:
Tumor necrosis factor-α (TNF-α) is an important fundamental cytokine during the immune response against cancer and infections such as tuberculosis. This molecule also plays a key pathogenic role in complex and difficult-to-treat diseases such as rheumatoid arthritis, ankylosing spondylitis, Crohn’s disease, psoriasis and ulcerative colitis. The treatment of these diseases frequently needs TNF-αantagonists, which has been related to an increased risk of developing tuberculosis, mycoses, and other severe infections.
We report the case of a 68-year-old man with Crohn’s disease, who developed disseminated tuberculosis due to anti-TNF-α immunosuppressive therapy. The diagnosis was based on the histopathological findings and molecular biology assays.
We discuss the clinical presentation and workup of this case, and we present a comparative analysis of tuberculosis cases associated with anti-TNF-α reported in Colombia during the last 10 years emphasizing on the diagnosis and treatment of latent tuberculosis.
Key words: Mycobacterium tuberculosis, tuberculosis, latent tuberculosis, Cronh’s disease, diagnosis, risk factor, tumor necrosis factor-alpha, Colombia.
Durante los últimos 15 años, los medicamentos con efectos antagonistas del factor de necrosis tumoral alfa (FNTα) han demostrado ser una excelente alternativa en el tratamiento de enfermedades inflamatorias mediadas por el sistema inmunitario cuando estas no responden a los medicamentos inmunomoduladores convencionales. Sin embargo, se ha observado que su uso se asocia con un riesgo mayor de desarrollar infecciones por agentes patógenos intracelulares tales como Mycobacterium tuberculosis1. También, su uso se ha asociado con el fenómeno llamado “reacción paradójica” durante el tratamiento antituberculoso, es decir, un empeoramiento de las lesiones tuberculosas existentes o la aparición de nuevas lesiones 2.
Un tercio de la población mundial está infectada con M. tuberculosis y 10 % de los infectados desarrolla la enfermedad en algún momento de su vida, la mitad de ellos durante los 18 primeros meses después de la infección inicial y, el otro 5 %, en algún momento posterior de su vida 3. La Organización Mundial de la Salud estimó que en el 2014 se presentaron en el mundo 9,6 millones de casos nuevos de tuberculosis, y 1,5 millones de personas murieron a causa de la enfermedad 4. En Colombia, la tuberculosis continúa siendo un grave problema de salud pública; en el 2015 se reportaron 12.918 casos, de los cuales el 81 % correspondió a la forma pulmonar y, el 19 % restante, a formas extrapulmonares 5.
La enfermedad de Crohn es una enfermedad inflamatoria del intestino cuyo tratamiento depende de su gravedad: se administran altas dosis de mesalazina en los casos leves, corticosteroides en casos moderados y agentes anti-FNTα u otros inmunosupresores en los casos graves 6. En Colombia, no existe información sobre el comportamiento epidemiológico de esta enfermedad, en tanto que en Puerto Rico se ha reportado una prevalencia de 41,2 por 100.000 habitantes 7, y en algunas regiones de Europa la prevalencia puede alcanzar los 322 casos por 100.000 8.
Se presenta el caso de un paciente que desarrolló tuberculosis pulmonar e intestinal como resultado de la administración de infliximab en el tratamiento de la enfermedad de Crohn y en quien, además, se presentó el fenómeno de reacción paradójica al desarrollar lesiones ganglionares durante su tratamiento contra la tuberculosis, manifestación que se presenta en 10 a 15 % de los casos de tuberculosis activa y cuyo manejo consiste en la continuación del tratamiento y la administración de esteroides en casos graves 2. Se presenta, asimismo, un análisis comparativo de los casos de tuberculosis asociados al uso de agentes anti-FNTα reportados en Colombia durante los últimos diezaños 9-14.
Descripción del caso
Se trata de un hombre de 68 años de edad, procedente de Cúcuta, con antecedentes de obesidad de grado II (índice de masa corporal: 36,3 kg/m2) y consumo crónico semanal de alcohol hasta la embriaguez durante cerca de 40 años. Su cuadro clínico se había iniciado tres años antes con la aparición de una lesión inflamatoria en el áreaperianal derecha, la cual evolucionó a una úlcera dolorosa de bordes mal definidos, con secreción purulenta y fétida, quedías despuésse convirtió en un absceso perianal que requirió drenaje quirúrgico y tratamiento antibiótico. Durante los meses posteriores, aparecieron tres abscesos satélites que se acompañaron de diarrea con moco y sangre, urgencia para defecar y flatulencia, astenia, adinamia e hiporexia.
En la evaluación por coloproctología se evidenciaron múltiples fístulas perianales; se tomaron biopsias de colon y recto, cuyo estudio evidenció un patrón histológico compatible con la enfermedad de Crohn. Con base en estos resultados y el cuadro clínico descrito, se diagnosticó enfermedad de Crohn perianal con fístulas (figura 1), y se inició tratamiento con 3.000 mg de mesalazina al día. Un mes después, se practicó fistulotomía y se continuó el manejo de las lesiones perianales con curaciones. Las lesiones residuales persistieron con presencia de material purulento y sangrado intermitente.
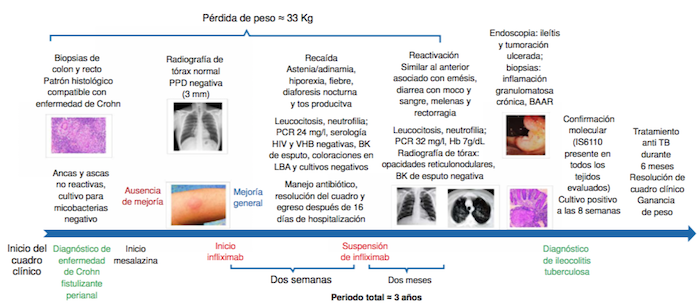
Figura 1
Representación de los eventos relevantes del caso clínico descrito. VHB: virus de la hepatitis B; BK: baciloscopia; LBA: lavado broncoalveolar; BAAR: bacilos ácido-alcohol resistentes
Dado que una radiografía de tórax previa se había interpretada como normal y que la prueba cutánea de derivado proteico purificado o tuberculina (Tuberculin PurifiedProteinDerivative, PPD) fue negativa (3 mm), se prescribió unagente anti-FNTα(imfliximab, 5 mg por kg de peso, con ciclos en las semanas 0, 2 y 6, y repetición a las 8 semanas), con lo cual se logró una mejoría general de los síntomas.
Dos semanas después, el paciente presentó una recaída clínica (figura 1) caracterizada por astenia, adinamia, hiporexia, fiebre intermitente, diaforesisnocturna y tos productiva, por lo cual acudió a urgencias donde se lo encontró en condiciones generales regulares, deshidratado, disneico, taquicárdico e hipotenso. Este cuadro clínico se interpretó como sepsis de posible origen respiratorio. En la tomografía computadorizada (TC) de tórax se observaron opacidades retículo-nodulares gruesas en ambos campos pulmonares. Tras 16 días de hospitalización bajo tratamiento antibiótico con amikacina y piperacilina-tazobactam, el paciente egresó con resolución del cuadro clínico y se le suspendió el infliximab.
Dos meses después, el paciente consultó por un cuadro clínico de 15 días de evolución muy similar al del ingreso inmediatamente anterior (figura 1), acompañado en esa ocasión de emesis, diarrea con moco y sangre, pérdida de peso (≈33 kg desde el inicio del cuadro), melenas y rectorragia.
En el momento de la hospitalización, estaba en malas condiciones generales, deshidratado, disneico, taquicárdico e hipotenso. Se inició manejo antibiótico con vancomicina y piperacilina-tazobactam, y se le trasfundieron dos unidades de glóbulos rojos.
En la radiografía de tórax se apreciaron opacidades retículo-nodulares en ambos campos pulmonares (figura 2), hallazgos confirmados por TC (figura 3). La baciloscopia seriada de esputo fue negativa para bacilos ácido-alcohol resistentes (BAAR), y en la colonoscopia y la ileoscopia practicadas se encontró ileítis, una tumoración ulcerada junto a la válvula íleocecal y una lesión ulcerada en el recto distal (figura 4 A y B). Se tomaron, entonces, biopsias de recto, colon e íleon cuyo estudio histopatológico informóun proceso inflamatorio granulomatoso crónico constituido por granulomas poco estructurados en todas las muestras evaluadas. Con la coloración de Ziehl-Neelsen (ZN) se demos-traron BAAR en todas las muestras (figura 5 A y B). Debido a estos hallazgos, se inició inmediatamente el tratamiento antituberculoso, además de la administración de mesalazina (4.000 mg al día).
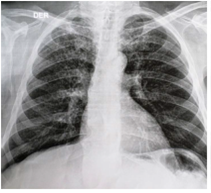
Figura 2
Radiografía simple de tórax con evidencia de opacidades retículo-nodulares en ambos campos pulmonares
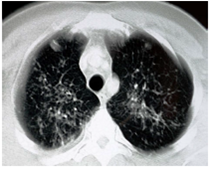
Figura 3
Tomografía computadorizada de tórax de alta resolución, ventana para pulmón. En ambos campos pulmonares se observa disminución de la transparencia y engrosamiento de los tabiques interlobulillares debido a lesiones micronodulares distribuidas difusamente
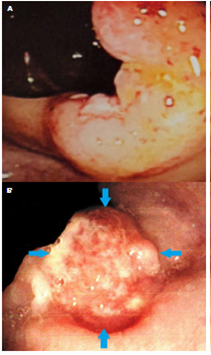
Figuras 4
Fotografías endoscópicas de colon y recto. A. Sobre la válvula ileocecal se observa una tumoración ulcerada de aspecto polipoide e irregular. B. En el conducto rectal se observa una lesión ulcerada de un centímetro de diámetro (flechas), su centro es granular y presenta exudado fibrinopurulento
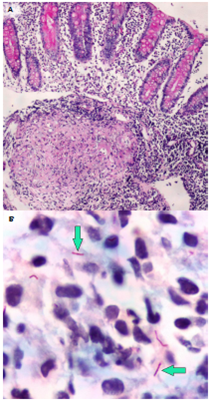
Figura 5
A. Mucosa del colon comprometida por reacción granulomatosa en la lámina propia; se observa un granuloma poco formado y sin necrosis. Hematoxina y eosina, 4X. B. En el mismo tejido se aprecian BAAR (flechas). Ziehl-Neelsen, 100X
El análisis del tejido incluido en bloques de parafina, mediante reacción en cadena de la polimerasa (PCR) en busca de la secuencia de inserción IS6110 (presente en el complejo M. tuberculosis), fue positivo en todos los especímenes, con lo cual se confirmó el diagnóstico de ileítis y colitis tuberculosa. El diagnóstico de tuberculosis pulmonar se comprobó mediante el cultivo de esputo en medio de Ogawa-Kudoh, el cual fue positivo a la octava semana de incubación. El paciente evolucionó satisfactoriamente con el tratamiento antituberculoso, y los síntomas gastrointestinales y respiratorios desparecieron.
El análisis del tejido incluido en bloques de parafina, mediante reacción en cadena de la polimerasa (PCR) en busca de la secuencia de inserción IS6110 (presente en el complejo M. tuberculosis), fue positivo en todos los especímenes, con lo cual se confirmó el diagnóstico de ileítis y colitis tuberculosa. El diagnóstico de tuberculosis pulmonar se comprobó mediante el cultivo de esputo en medio de Ogawa-Kudoh, el cual fue positivo a la octava semana de incubación. El paciente evolucionó satisfactoriamente con el tratamiento antituberculoso, y lossíntomas gastrointestinales y respiratorios desparecieron.
En el inicio del segundo mes de tratamiento, apareció una tumoración submandibular similar a una adenomegalia (figura 6). Se practicóbiopsia por escisión y de piel, cuya evaluación histopatológica reportócompromiso dérmico por infiltrado linfohistiocitario con tendencia a la formación de granulomas, en tanto que la tinción de ZN mostró formas bacilares fragmentadas. La tumoración no requirió manejo adicional y se interpretó como una reacción paradójica.
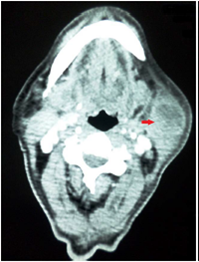
Figura 6
Tomografía de cuello con contraste. Sobre el músculo esternocleidomastoideo y bajo la glándula parótida, se observa una lesión nodular de centro hipodenso que capta anularmente el contraste (flecha). Los hallazgos descritos son indicativos de adenomegalia cervical izquierda.
El paciente culminó su tratamiento antituberculoso de seis meses, dos de tratamiento intensivo con cuatro medicamentos (rifampicina, isoniacida, pirazinamida y etambutol) y cuatro de mantenimiento (rifampicina e isoniacida). La administración de mesalazina continuó y, en el último control médico, se encontró remisión completa de los síntomas respiratorios y gastrointestinales, y ganancia de 10 kg de peso.
El presente caso se publica con la autorizacióndel paciente.
Casos de tuberculosis asociados al uso de medicamentos anti-FNTα en Colombia
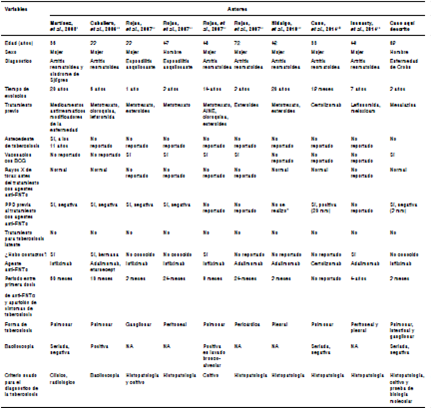
Con el propósito de conocer y discutir los casos de tuberculosis asociada con el uso de medicamentos anti-FNTα reportados previamente en Colombia, se adelantó una búsqueda bibliográfica de reportes de caso, empleando los siguientes términosde búsqueda: tuberculosis, TNF, anti-TNF y Colombia en Google Académico; tuberculosis, TNF y anti-TNF en los campos de título y resumen en la base de datos Scielo-Colombia, y tuberculosis, TNF y anti-TNF en los campos de título y resumen, y Colombia en todos los campos en el buscador PubMed.Se obtuvieron seis reportes que describían nueve casos 9-14 (cuadro 1).
Características de los casos analizados y del caso descrito en el presente artículo
Discusión
Hasta la fecha se ha aprobado el uso clínico de cuatro anticuerpos monoclonales ‘humanizados’ (infliximab, adalimumab, golimumab y certolizumab) y de un receptor soluble (etarnecept) con efectos anti-FNTα para el tratamiento de enfermedades inflamatorias mediadas por el sistema inmunitario 1,15.
El FNTα es una molécula con diversas funciones biológicas: tiene un papel fundamental en la reacción inmunitaria a infecciones y al cáncer, y en la fisiopatología de muchas enfermedades mediadas por el sistema inmunitario 15. Se sabe que es fundamental en la reacción inmunitaria frente a bacterias intracelulares, y en el mantenimiento de la fisiología e integridad del granuloma, razón por la cual se cree que su antagonismo se asocia con un mayor riesgo de desarrollar tuberculosis 16.
Tal riesgo se hizo evidente en el curso de diversos estudios clínicos sobre el desarrollo de medicamentos. En 1999, durante el estudio de Maini, et al., sobre la utilidad del infliximab para el tratamiento de la artritis reumatoidea resistente, un paciente desarrolló tuberculosis y falleció 17. En el clásico estudio de Keane, et al., en el 2001, se diagnosticaron 70 casos de tuberculosis en pacientes bajo tratamiento con infliximab alrededor del mundo 18. En algunos metaanálisis recientes, se encontró que el uso conjunto de otros medicamentos inmunosupresores, como el metotrexato y la azatioprina, y de agentes anti-FNTα aumentaba de manera sinérgica el riesgo de desarrollar tuberculosis, hasta 13 veces más en quienes recibían el tratamiento combinado que en quienes solo recibían los medicamentos anti-FNTα 19.
Con base en la información de los sistemas de vigilancia, en los Estados Unidos se evidenció que la tasa de incidencia de tuberculosis en pacientes con artritis reumatoidea aumentó de 6,2 por 100.000 habitantes a 144 por 100.000 entre quienes recibían infliximab, y a 35 por 100.000 habitantes en quienes recibían etanercept 20.
La incidencia de tuberculosis en pacientes bajo tratamiento anti-FNTα varía según los estudios y áreas geográficas: en España, por ejemplo, en un estudio de vigilancia activa se recopilaron los datos de 71 centros de información de un total de 1.540, y se estimó una incidencia de tuberculosis en pacientes que recibían infliximab de 1.893 por 100.000 habitantes, frente a la reportada previamente de 21 por 100.000 en la población general, y de 95 por 100.000 en individuos con artritis reumatoidea sin tratamiento anti-FNTα 21.
Por otro lado, en un estudio de la Food and Drug Administration (FDA) en el que se recolectó información sobre sistemas de registro de efectos secundarios a medicamentos, fue posible calcular tasas mundiales de tuberculosis de 20,7 por 100.000 habitantes bajo tratamiento con etenercept y de 47,6 casos por 100.000 de quienes recibían infliximab 22.
En un estudio prospectivo adelantado en Francia por Tubach, et al., se encontró una incidencia anual ajustada de tuberculosis de 9,3 (rango: 0,0 a 9,4) por 100.000 individuos bajo tratamiento con etanercept, de 187,5 (rango: 0,1 a 374,8) por 100.000 tratados con infliximab, y de 215,0 (rango: 0,0 a 521,7) por 100.000 en aquellos en tratamiento con adalimumab, frente a una incidencia de 8,7 por 100.000 en la población general 23.
En un estudio nacional que incluyó 10.712 individuos en tratamiento anti-FNTα en Inglaterra, Dixon, et al., encontraron que la tasa más alta de incidencia de tuberculosis se registró en quienes recibían tratamiento con adalimumab, con 144 eventos por 100.000 personas por año, seguido de los tratados con infliximab, con 136 eventos por 100.000 personas por año, y por último, en quienes recibían etanercept, con 39 eventos por 100.000 personas por año. Asimismo, encontraron que el periodo promedio entre el inicio de la administración de agentes anti-FNTα y el diagnóstico de tuberculosis, era de 13,4 meses con etanercept, de 18,5 meses con adalumumab y de 5,5 con infliximab 24.
Es evidente que el riesgo fue mayor para aquellos pacientes que recibían anticuerpos monoclonales que para quienes recibían receptores solubles. En esta serie, el medicamento más frecuentemente usado fue el anticuerpo monoclonal infliximab, con cinco casos y un periodo promedio entre el inicio del tratamiento y el diagnóstico de tuberculosis de 19,8 meses (rango: 3 a 60); tres pacientes recibieron adalimumab, con un periodo promedio de 25 meses (rango: 3 a 48) entre su inicio y el diagnóstico de tuberculosis; un paciente recibió tratamiento combinado con adalimunab y etarnecept, y después de 10 meses del inicio, se le diagnóstico la enfermedad; en el caso de quien recibió certolizumab, el reporte no indica el periodo de diagnóstico de la tuberculosis.
El caso aquí descrito es particularmente interesante, pues el paciente fue tratado con el anticuerpo monoclonal infliximab, y el periodo comprendido entre el inicio del tratamiento y el cuadro clínico atribuido a la tuberculosis fue de los más breves reportados en esta serie (figura 1), ya que solo recibió dos ciclos del medicamento (dos semanas) (cuadro 1 y figura 1).
En cuanto a la forma de presentación de la enfermedad, las series publicadas muestran un gran porcentaje de tuberculosis extrapulmonar y diseminada, en comparación con el de tuberculosis pulmonar (80 %) en la población general. Tal es el caso del estudio de Keane, et al., en el que se registró que 31 % de los pacientes habían presentado tuberculosis pulmonar, 33 %, extrapulmonar, y 24 %, diseminada. En esa misma serie, en 20 % de los casos se reportó el uso reciente de esteroides y, en 40 %, de metotrexato más esteroides. Con respecto a la técnica de diagnóstico, la que más contribuyó fue el cultivo (57 %), seguida de la histopatología o la tinción de ZN (23 %), en tanto que con las pruebas de biología molecular se diagnosticó el 3 % de los casos, y se detectó exposición reciente a la tuberculosis en dos casos 18.
En la presente serie, en cuatro casos se presentó enfermedad pulmonar, en cuatro, extrapulmonar, y en dos hubo compromiso de dos o más órganos (tuberculosis diseminada), entre ellos, el del caso aquí descrito, en quien se documentó compromiso pulmonar, intestinal y ganglionar. Entre las técnicas usadas para el diagnóstico, aunque el número de eventos descritos no permite hacer un análisis profundo, el comportamiento difiere del previamente descrito en otros estudios (cuadro 1). En seis casos, incluido el que aquí se presenta, se aplicó la prueba de PPD antes del inicio del tratamiento con anti-FNTα, y solo en uno se registró una medida interpretada como positiva (20 mm); este paciente no recibió tratamiento para la tuberculosis latente, se le trató con certolizumab y, posteriormente, desarrolló tuberculosis pulmonar.
La mayoría de los casos de tuberculosis asociados al uso de medicamentos anti-FNTα, se debe a la reactivación de una tuberculosis latente 25. Como se mencionó anteriormente, usualmente los casos ocurren al inicio del tratamiento, como lo describieron Wallis, et al., al encontrar una tasa de desarrollo de tuberculosis superior a 80 por 100.000 durante los primeros 90 días de tratamiento con infliximab, la cual disminuyó a 15 por 100.000 entre los 91 y 180 días y fue inferior a 5 por 100.000 personas después de los 271 días 20. En la serie aquí analizada, dos de los cinco pacientes que recibieron infliximab, incluido aquel cuyo caso se presenta, desarrollaron la enfermedad alrededor de los 90 días después de la primera dosis.
La detección y el tratamiento de la infección latente son, sin duda, la mejor estrategia para evitar el desarrollo de tuberculosis en pacientes con factores de riesgo 26, como los infectados por HIV 27, los diabéticos 28 y, evidentemente, quienes reciben tratamiento anti-FNTα 1. Sin embargo, actualmente no existe una prueba de referencia para el diagnóstico de la infección tuberculosa latente 26.
Hay dos metodologías para detectar la tuberculosis latente y la ‘evidencia’ clínica muestra que ambas son aceptables, pero no perfectas. Con ninguna de las dos técnicas se puede diferenciar objetivamente entre la tuberculosis activa y la latente, distinguir entre reactivación o reinfección, ni tampoco brindar información con respecto a las distintas fases de la infección por M. tuberculosis26.
Por un lado, está la prueba de PPD, ampliamente conocida y utilizada, que comúnmente se usa en Colombia y, por otro, los ensayos de medición de producción de interferón gamma (Interferon γ Relase Assays, IGRA), los que ya se encuentran disponibles en varias instituciones de alta complejidad en el país.
Es poca la sensibilidad de las dos pruebas cuando se usan en individuos con alteraciones inmunológicas como los aquí analizados, y tienen un bajo valor predictivo positivo (2,7 %; IC95% 2,3-3,2) de la progresión a la enfermedad activa 29. No obstante, para detectar la infección latente, se toman como base los resultados positivos en alguna de las dos pruebas mencionadas en individuos sin síntomas de enfermedad activa 25.
Durante años, el pilar del tratamiento de la tuberculosis latente ha sido la administración de isoniacida diariamente durante un periodo de seis a 12 meses. En algunos estudios también se ha demostrado la eficacia de esquemas terapéuticos semanales directamente observados de isoniacida más rifapentina durante tres meses 25. En varios estudios, se sugiere que la detección y el tratamiento de la tuberculosis latente antes del inicio la administración de agentes anti-FNTα, previene efectivamente la reactivación de la enfermedad, con una eficacia reportada de entre 60 y 90 % 1,11,30.
Sin embargo, en algunos estudios se ha descrito el desarrollo de tuberculosis durante el tratamiento, incluso en pacientes que lo habían recibido para la forma latente, por lo cual variables como el cumplimiento y la duración han demostrado ser fundamentales 31. Por otro lado, también los episodios de infección posteriores a la tamización, así como la reactivación de una infección no detectada mediante las pruebas disponibles, son posibles explicaciones de este fenómeno.
Recientemente, en un trabajo adelantado en Colombia en el cual se analizó el seguimiento con PPD en una cohorte histórica de pacientes con enfermedad reumática, se encontró que el 23,5 % (12 de 51 casos) presentaba conversión de PPD (de negativa a positiva) durante el tratamiento con medicamentos anti-FNTα 32. Tales hallazgos suponen la necesidad de estudiar estrategias de tamización, periódicas y, ojalá, duales (PPD e IGRA).
Órganos académicos como el American College of Rheumatology, la Sociedad Española de Neumología y Cirugía Torácica, la Sociedad Española de Patología Digestiva y la Sociedad Española de Reumatología, entre otras, recomiendan repetir la tamización con PPD o IGRA cuando la exploración inicial ha sido negativa, cuando solo hay cambios en la sintomatología clínica, o tras una posible exposición a M. tuberculosis 33,34.
Por otra parte, en otro estudio reciente en Colombia, se encuestaron especialistas en el manejo de enfermedades intestinales inflamatorias, entre ellas la enfermedad de Crohn, y se indagó sobre su conducta en los pacientes que requieren tratamiento biológico, y se encontró que solo el 40 % de los médicos encuestados ofrecían tratamiento profiláctico para la tuberculosis latente antes de iniciar la administración de medicamentos anti-FNTα 35. Esto sugiere que puede haber una subestimación del riesgo por parte del clínico o, incluso, desconocimiento, conclusión a la que también llegaron los autores del estudio colombiano antes mencionado 32.
Es evidente, entonces, la necesidad de descartar la tuberculosis latente en aquellos individuos en los que se va a iniciar el tratamiento con agentes anti-FNTα. No hay ‘evidencia’ clínica suficiente para sugerir que los IGRA son superiores a la PPD en la detección de la tuberculosis latente en pacientes con enfermedades inflamatorias mediadas por el sistema inmunitario, quienes se beneficiarían del tratamiento profiláctico 28. No obstante, debido a las especiales características de los IGRA, hay una tendencia internacional a usarlos en lugar de la PPD.
En un estudio prospectivo de Chang, et al., de 107 pacientes con un seguimiento promedio de 18 meses, se recomienda que, en países donde la prevalencia de tuberculosis sea intermedia y la aplicación de la vacuna BCG sea obligatoria en el momento del nacimiento, como en Colombia, se debe usar IGRA en lugar de PPD para detectar la forma latente en individuos con enfermedades inflamatorias mediadas por el sistema inmunitario antes de iniciar el tratamiento con agentes anti-FNTα.
Por otro lado, en algunos estudios se sugiere que, en países con prevalencia moderada y alta, o en pacientes con factores de riesgo para tuberculosis, se debe usar una estrategia que incluya ambas pruebas, lo cual podría mejorar la sensibilidad 37.
Por último, independientemente de si se usan uno o ambos métodos, es fundamental recordar que tanto los IGRA como la PPD son ayudas diagnósticas y que una aproximación razonable debe incluir el análisis integral de la historia clínica del paciente, especialmente lo que hace referencia a sus antecedentes y factores de riesgo, utilizando herramientas de predicción del riesgo multivariado, tal como la desarrollada por Menzies, et al. 38. Esta última puede favorecer la detección de la tuberculosis latente y, por consiguiente, su tratamiento, en pacientes en quienes deba iniciarse la administración de agentes anti-FNTα (está disponible en: http://www.tstin3d.com/en/calc.html).
Referencias
1. Xie X, Li F, Chen JW, Wang J. Risk of tuberculosis infection in anti-TNF-a biological therapy: From bench to bedside. J Microbiol Immunol Infect. 2014;47:268-74. https://doi.org/10.1016/j.jmii.2013.03.005
2. Unlu M, Cimen P, Ayranci A, Akarca T, Karaman O, Dereli MS. Disseminated tuberculosis infection and paradoxical reaction during antimycobacterial treatment related to TNF-alpha blocker agent Infliximab. Respir Med Case Rep. 2014;13:43-7. https://doi.org/10.1016/j.rmcr.2014.09.005
3. Andrews JR, Noubary F, Walensky RP. Risk of progression to active tuberculosis following reinfection with Mycobacterium tuberculosis. Clin Infect Dis. 2012;54:784-91. https://doi.org/10.1093/cid/cir951
4. World Health Organization. Global tuberculosis report 2015. Geneva. Fecha de consulta: 3 de marzo de 2016. Disponible en: http://apps.who.int/iris/bitstream/10665/191102/1/9789241565059_eng.pdf
5. Instituto Nacional de Salud. Boletín epidemiológico semana 53, 2015. Fecha de consulta: 3 de marzo de 2016. Disponible en: http://www.ins.gov.co/boletin-epidemiologico/Boletn%20Epidemiolgico/2015%20Boletin%20epidemiologico%20Semana%2052.pdf
6. Baumgart DC, Sandborn WJ. Crohn's disease. Lancet. 2012;380:1590-605. https://doi.org/10.1016/S0140-6736(12)60026-9
7. Pérez-Perdomo R, Pérez-Cardona CM. An epidemiological review of tuberculosis in the Puerto Rican population. PR Health Sci J. 1999;18:117-22.
8. Molodecky N, Soon I, Rabi D, Ghali W, Ferris M, Chernoff G, et al. Increasing incidence and prevalence of the inflammatory bowel diseases with time, based on systematic review. Gastroenterology. 2012;142:46-54. https://doi.org/10.1053/j.gastro.2011.10.001
9. Martínez JV, Medina Y, Parga R, Restrepo JF, Iglesias-Gamarra A, Rondón F. Reactivación de tuberculosis pulmonar (TBC) con el uso de antagonistas del factor de necrosis tumoral alfa (FNTa) en artritis reumatoide. A propósito de un caso. Rev Colomb Reumatol. 2005;12:54-61.
10. Caballero C, Pinzón L. Artritis reumatoide tratada con inhibidores del factor de necrosis tumoral a (Anti-TNF-a) y tuberculosis pulmonar. Salud Uninorte. 2006;22:29-39.
11. Rojas-Villarraga A, Agudelo C, Pineda R, Porras A, Matute G, Anaya JM. Tuberculosis in patients treated with tumor necrosis factor-alpha antagonists living in an endemic area. Is the risk worthwhile? Biomédica. 2007;27:159-71. https://doi.org/10.7705/biomedica.v27i2.212
12. Hidalgo P, Echeverri J, Gutiérrez J. Tuberculosis pleural asociada con adalimumab en un paciente con artritis reumatoide. Infectio. 2010;14:47-54. https://doi.org/10.1016/S0123-9392(10)70092-8
13. Cano D, Rodríguez J, Torres C. Terapias biológicas y tuberculosis. Un riesgo manejable. Perspectiva Neumológica. 2014;16. http://www.neumologica.org/sites/default/files/pdf/perspectiva_neumologica/PN-VOL-16-1-05-2014%20Terapiabiologica.pdf
14. Insuasty J, Bolívar A, Calvo L, Roberto S. Tuberculosis peritoneal simulando cáncer de ovario. Acta Med Colomb. 2014;39:383-7.
15. Salgado E, Gómez-Reino JJ. The risk of tuberculosis in patients treated with TNF antagonists. Expert Rev Clin Immunol. 2011;7:329-40. https://doi.org/10.1586/eci.11.6
16. O'Garra A, Redford P, McNab F, Bloom C, Wilkinson RJ, Berry M. The immune response in tuberculosis. Annu Rev Immunol. 2013;31:475-527. https://doi.org/10.1146/annurev-immunol-032712-095939
17. Maini R, St Clair EW, Breedveld F, Furst D, Kalden J, Weisman M, et al. Infliximab (chimeric anti-tumour necrosis factor alpha monoclonal antibody) versus placebo in rheumatoid arthritis patients receiving concomitant methotrexate: A randomised phase III trial. ATTRACT Study Group. Lancet. 1999;354:1932-9. https://doi.org/10.1016/S0140-6736(99)05246-0
18. Keane J, Gershon S, Wise RP, Mirabile-Levens E, Kasznica J, Schwieterman WD, et al. Tuberculosis associated with infliximab, a tumor necrosis factor alpha-neutralizing agent. N Engl J Med. 2001;345:1098-104. https://doi.org/10.1056/NEJMoa011110
19. Lorenzetti R, Zullo A, Ridola L, Diamanti AP, Laganà B, Gatta L, et al. Higher risk of tuberculosis reactivation when anti-TNF is combined with immunosuppressive agents: A systematic review of randomized controlled trials. Ann Med. 2014;46:547-54. https://doi.org/10.3109/07853890.2014.941919
20. Wallis RS, Broder MS, Wong JY, Hanson ME, Beenhouwer DO. Granulomatous infectious diseases associated with tumor necrosis factor antagonists. Clin Infect Dis. 2004;38:1261-5. https://doi.org/10.1086/383317
21. Gómez-Reino JJ, Carmona L, Valverde VR, Mola EM, Montero MD, BIOBADASER Group. Treatment of rheumatoid arthritis with tumor necrosis factor inhibitors may predispose to significant increase in tuberculosis risk: A multicenter active-surveillance report. Arthritis Rheum. 2003;48:2122-7. https://doi.org/10.1002/art.11137
22. Gardam MA, Keystone EC, Menzies R, Manners S, Skamene E, Long R, et al. Anti-tumor necrosis factor agents and tuberculosis risk: Mechanism of action and clinical management. Lancet Infect Dis. 2003;3:148-55. https://doi.org/10.1016/S1473-3099(03)00545-0
23. Tubach F, Salmon D, Ravaud P, Allanore Y, Goupille P, Bréban M, et al. Risk of tuberculosis is higher with anti-tumor necrosis factor monoclonal antibody therapy than with soluble tumor necrosis factor receptor therapy: The three-year prospective French Research Axed on Tolerance of Biotherapies registry. Arthritis Rheum. 2009;60:1884-94. https://doi.org/10.1002/art.24632
24. Dixon WG, Hyrich KL, Watson KD, Lunt M, Galloway J, Ustianowski A, et al. Drug-specific risk of tuberculosis in patients with rheumatoid arthritis treated with anti-TNF therapy: Results from the British Society for Rheumatology Biologics Register (BSRBR). Ann Rheum Dis. 2010;69:522-8. https://doi.org/10.1136/ard.2009.118935
25. Getahun H, Matteelli A, Chaisson RE, Raviglione M. Latent Mycobacterium tuberculosis infection. N Engl J Med 2015;372:2127-35. https://doi.org/10.1056/NEJMra1405427
26. Pai M, Denkinger CM, Kik SV, Rangaka MX, Zwerling A, Oxlade O, et al. Gamma interferon release assays for detection of Mycobacterium tuberculosis infection. Clin Microbiol Rev. 2014;27:3-20. https://doi.org/10.1128/CMR.00034-13
27. Jurado LF, Murcia MI, Hidalgo P, Leguizamón JE, González LR. Diagnóstico genotípico y fenotípico de tuberculosis ósea y miliar en un paciente VIH positivo en Bogotá, Colombia. Biomédica. 2015;35:8-15. https://doi.org/10.7705/biomedica.v35i1.2275
28. Jurado LF, Palacios DM, Álvarez J, Baldión M, Campos G. Diagnóstico patológico y molecular de un caso de tuberculosis laríngea primaria en un médico. Biomédica. 2014;34:15-20. https://doi.org/10.7705/biomedica.v34i1.1624
29. Landry J, Menzies D. Preventive chemotherapy. Where has it got us? Where to go next? Int J Tuberc Lung Dis. 2008;12:1352-64.
30. Akolo C, Adetifa I, Shepperd S, Volmink J. Treatment of latent tuberculosis infection in HIV infected persons. Cochrane Database Syst Rev. 2010;20:CD000171. https://doi.org/10.1002/14651858.CD000171.pub3
31. Sichletidis L, Settas L, Spyratos D, Chloros D, Patakas D. Tuberculosis in patients receiving anti-TNF agents despite chemoprophylaxis. Int J Tuberc Lung Dis. 2006;10:1127-32.
32. Muñoz OM, Hurtado-Uriarte M, Fernández-Ávila D, Hidalgo P, Gutiérrez-Dávila JM. Conversión de tuberculosis latente en un grupo de pacientes tratados con terapia biológica en una unidad de reumatología. Revista Colombiana de Neumología. 2014;26:116-22.
33. Furst DE, Keystone EC, So AK, Braun J, Breedveld FC, Burmester GR. Updated consensus statement on biological agents for the treatment of rheumatic diseases 2012. Ann Rheum Dis. 2013;72:ii2-34. https://doi.org/10.1136/annrheumdis-2013-203348
34. Mir-Viladrich I, Daudén-Tello E, Solano-López G, López-Longo FJ, Taxonera-Samso C, Sánchez-Martínez P, et al. Documento de consenso sobre la prevención y el tratamiento de la tuberculosis en pacientes candidatos a tratamiento biológico. Arch Bronconeumol. 2016;52:36-45. https://doi.org/10.1016/j.arbres.2015.04.016
35. Juliao F, Agudelo Y, Yepes Delgado C. Variación en el cuidado de pacientes con enfermedad inflamatoria intestinal (EII): resultado de una encuesta. Rev Col Gastroenterol 2014;29:11-8.
36. Chang B, Park HY, Jeon K, Ahn JK, Cha HS, Koh EM, et al. Interferon-gamma release assay in the diagnosis of latent tuberculosis infection in arthritis patients treated with tumor necrosis factor antagonists in Korea. Clin Rheumatol. 2011;30:1535-41. https://doi.org/10.1007/s10067-011-1771-9
37. Winthrop KL, Weinblatt ME, Daley CL. You can't always get what you want, but if you try sometimes (with two tests-TST and IGRA-for tuberculosis) you get what you need. Ann Rheum Dis. 2012;71:1757-60. https://doi.org/10.1136/annrheumdis-2012-201979
38. Menzies D, Gardiner G, Farhat M, Greenaway C, Pai M. Thinking in three dimensions: A web-based algorithm to aid the interpretation of tuberculin skin test results. Int J Tuberc Lung Dis. 2008;12:498-505.
Notas
Notas de autor
*Correspondencia: Leonardo F. Jurado, Departamento de Microbiología, Facultad de Medicina, Universidad Nacional de Colombia, Carrera 30 N°45-03, edificio 471, piso 3, Bogotá, D.C., Colombia Teléfono: (312) 873 7570 lfjuradoz@unal.edu.co
