REVISIÓN DE TEMA
Aceites esenciales y sus componentes como una alternativaen el control de mosquitos vectores de enfermedades
Essential oils and their components as an alternative in the control of mosquito vectors of disease
Aceites esenciales y sus componentes como una alternativaen el control de mosquitos vectores de enfermedades
Biomédica, vol. 37, núm. 2, 2017
Instituto Nacional de Salud
Recepción: 30 Agosto 2016
Aprobación: 27 Abril 2017
Resumen: Más de la mitad de la población humana está expuesta a contraer infecciones transmitidas pormosquitos. El cambio climático y la aparición de cepas resistentes a los insecticidas tradicionalmenteutilizados han motivado la búsqueda de nuevos agentes capaces de controlar las poblaciones demosquitos. Los aceites esenciales han resultado ser eficaces agentes repelentes y larvicidas. El objetivo de este trabajo fue revisar las investigaciones llevadas a cabo en los últimos años sobrela actividad larvicida de los aceites esenciales y sus componentes contra mosquitos de los génerosAedes, Anopheles y Culex, así como los últimos reportes sobre su posible mecanismo de acción.
Palabras clave: aceites volátiles, insectos vectores, vectores de enfermedades, larvicidas, terpenos.
Abstract: More than half of the human population is exposed to mosquito-borne infections. Climate change and theemergence of strains resistant to traditionally used insecticides have motivated the search of new agentsfor mosquito population control. Essential oils have been effective repellents and larvicidal agents.The aim of this work was to review research studies conducted in recent years on the larvicidal activityof essential oils and their components against Aedes, Anopheles and Culex mosquitoes, as well as thelatest reports about their possible mechanism of action.
Key words: Oils, volatile, insect vectors, disease vectors, larvicides, terpenes.
Más de la mitad de la población humana estáexpuesta a contraer infecciones transmitidas pormosquitos. La falta de tratamientos y vacunas eficacespara muchas de estas enfermedades haceque su control dependa principalmente de la utilizacióndeagentesinsecticidas(1).Losindividuosquehabitan en las áreas tropicales están más expuestos a contraer enfermedades transmitidaspor vectores y este riesgo ha aumentado en otraszonas debido a la globalización (2).
Culex, Aedes y Anopheles son vectores de diversasenfermedades, como la filariasis, el dengue,la malaria, y otras. Culex quinquefasciatus estápresente en vastas regiones tropicales del mundo,es la principal plaga doméstica en muchas áreasurbanas y está implicada en la transmisión demuchos agentes patógenos, entre ellos, el causantede la filariasis linfática. Esta enfermedad estáampliamente distribuida en las zonas tropicales, conalrededor de 120 millones de personas infectadasen todo el mundo (3).
Aedes aegypti es el principal vector del dengueclásico y el dengue hemorrágico. La incidenciadel dengue ha aumentado 30 veces en las últimasdécadas y cerca de dos quintas partes de la poblaciónmundialestáahoraenriesgo(4).
Seestimaqueunos2,5millonesdepersonasvivenenmásde100paísesendémicosyque50millonesdeinfeccionesseproducenanualmente(5).
LosmosquitosdelgéneroAedestambiénpuedentransmitirotrosvirus,comoeldelNiloOccidental,delcualyasehanreportadovarioscasosdeinfecciónenelcontinenteamericano(6),asícomolafiebredechikungunya,producidaporunalfavirusenexpansióngeográfica(7,8)ylaenfermedadcausadaporelvirusZika,elcualesunflavivirusquesetransmitetantoenáreasurbanascomo selváticas.
La malaria, o paludismo, es una enfermedad causada por parásitos del género Plasmodiumque se transmiten a las personas por la picaduradel mosquito Anopheles. Según las últimas estimaciones,198 millones de casos de malaria seprodujeron a nivel mundial en el 2013 y la enfermedaddiolugara584.000muertes(9).
Béguin,etal.,hanpronosticadoquemásde200millonesdeindividuosestarán en riesgo para el 2050 debidoal acelerado cambio climático y la lentitud en eldesarrollo socioeconómico de los países del tercermundo (10), los cuales se ubican principalmenteen las zonas endémicas, por lo que es claro quelas actividades del hombre y las alteraciones enla biodiversidad de los ecosistemas afectan demanera significativa el número y el movimientode las especies de reservorios y vectores, y, enconsecuencia, la incidencia de las enfermedadestransmitidas por vectores en humanos (11).
Es evidente que el cambio climático representa ungrave problema al aumentar los rangos geográficosde riesgo de las enfermedades transmitidas porvectores. La Organización Mundial de la Salud(OMS) ha estimado que, si las temperaturas globalesseincrementande2a3°Cparael2030,comoseespera, la población en riesgo de infectarsecon malaria, por ejemplo, aumentará de 3 a 5 %(12). Por otro lado, el uso intensivo de insecticidassintéticos en el control de los mosquitos ha generadomuchos problemas y ha tenido un impacto negativoen el medio ambiente, así como resistencia(13), con efectos indeseables sobre organismos noespecíficos y sobre la vida silvestre (14,15).
La resistencia de los mosquitos a los insecticidasse ha reportado en todo el mundo, como puedecomprobarse por los hallazgos en Tanzania (16), Grecia (17), México (18), Tailandia (19) y Colombia(20), por mencionar solo algunos países. Debidoa la alta incidencia de cepas resistentes a losinsecticidas tradicionalmente utilizados, hoy sebuscan nuevos métodos para el control de los mosquitos. Losproductosnaturalesdeorigenvegetalconactividadinsecticidapotencial,seconsideranalternativasválidasfrentealospesticidassintéticosconvencionalesenelcontroldeunaampliavariedaddeinsectos, plagas y vectores.
A lo largo de la historia, las plantas y los insectoshan coexistido y evolucionado en paralelo. Lasplantas han aprovechado a los insectos comoagentes polinizadores, pero también han tenidoque desarrollar mecanismos de defensa contrainsectos depredadores (21). En este contexto, los aceites esenciales y sus componentes se destacancomo compuestos potencialmente útiles contra losinsectos (22,23).
Aceites esenciales y su composición química
Los aceites esenciales son sustancias de origenvegetal cuyas mezclas de metabolitos secundariosvolátiles,insolublesenagua,lesconfierencaracterísticasparticulares según sus diferentesproporciones (24). Estos aceites se originan en lostejidos secretores de las plantas y, por lo general,son líquidos a temperatura ambiente, más ligerosque el agua, de olor fuerte y penetrante querecuerda su planta de origen, e incoloros o de coloramarillo traslúcido (25).
Su función es variada en las plantas: son agentesde polinización y sirven de reserva y de protección,ya que defienden a la planta de otras plantas,de algunos insectos y de microorganismos. Losaceites esenciales se clasifican con base endiferentes criterios: su consistencia, su origeny la composición química de sus componentesmayoritarios (26).
En cuanto a su composición química, se encuentranprincipalmente terpenos y fenilpropanos, a partir delos cuales se pueden constituir aldehídos, alcoholes,ésteres y cetonas, entre otros. Estos compuestosson los responsables de la fragancia y las propiedadesbiológicasdelosaceitesesenciales. Esimportanteresaltarque85%deestosaceitessueletenerunoodoscompuestosmayoritarios,mientrasqueelrestodesucomposiciónconsisteendecenasdecompuestos minoritarios (24,25).
Losaceitesesencialessehanestudiadoantetodocomoagentes antimicrobianos. El de orégano,por ejemplo, se ha analizado ampliamente por su actividad contra bacterias Gram positivas y Gramnegativas (27), así como contra hongos filamentosos,levaduras y protozoarios (28,29).
Como ya se mencionó, los aceites esencialespueden ser una fuente alternativa de agentes decontrol de mosquitos y otros insectos, ya que sonricos en compuestos con actividad biológica, sonbiodegradables y se transforman en productos notóxicos, son amigables con el medio ambiente yestán potencialmente adecuados para su uso enlos programas de control integral (21,30,31). Dehecho, muchos investigadores han informado sobrela eficacia de los aceites esenciales como agentescontra larvas y ejemplares adultos y, asimismo,como repelentes (14,23,30-32).
En este contexto, el propósito de este trabajo fuerevisar y evaluar las investigaciones llevadas acabo en los últimos años sobre la actividad larvicidade los aceites esenciales y sus componentes, asícomo los últimos reportes sobre sus posibles mecanismosdeacciónylosestudioshechosmediantemodeladomolecular. Acontinuaciónsepresentalaactividadbiológicacontralaslarvasdemosquitosde81 aceites esenciales y 68 de sus moléculas.
Actividad larvicida de los aceites esenciales
Desde hace décadas se vienen utilizando diversaspartes de las plantas y sus extractos como agentesrepelentes e insecticidas contra distintas especiesde insectos (30). El limoneno y el carvacrol, porejemplo, son dos terpenos utilizados frecuentementecomo insecticidas, en tanto que el aceite esencialde eucalipto se ha empleado ampliamente comorepelente natural de insectos (31).
La actividad larvicida de los aceites esenciales ysus componentes generalmente se evalúan conel método propuesto por la OMS en el 2005 paraestandarizar los procedimientos de evaluaciónde la actividad larvicida en el laboratorio y encampo (33). Varios autores han desarrollado suspropios criterios sobre lo que se considera unagente larvicida, pero la mayoría coincide en queun producto vegetal puede considerarse como unlarvicida eficaz solo si tiene una concentración letal50 (CL50) por debajo de los 100 µg/ml (ppm) (32).
En el cuadro 1 se presenta la actividad de 81aceites esenciales a las 24 horas de exposiciónen larvas de tercer y cuarto estadios. Los criteriosde búsqueda fueron las palabras clave "actividadlarvicida" y "aceites esenciales", y se incluyerontodos los reportes de actividad sobre Culex, Aedesy Anopheles publicados entre 2010 y 2015. La búsqueda se llevó a cabo en las bases de datos deScience Direct, Scientific Electronic Library Onliney Google Scholar.
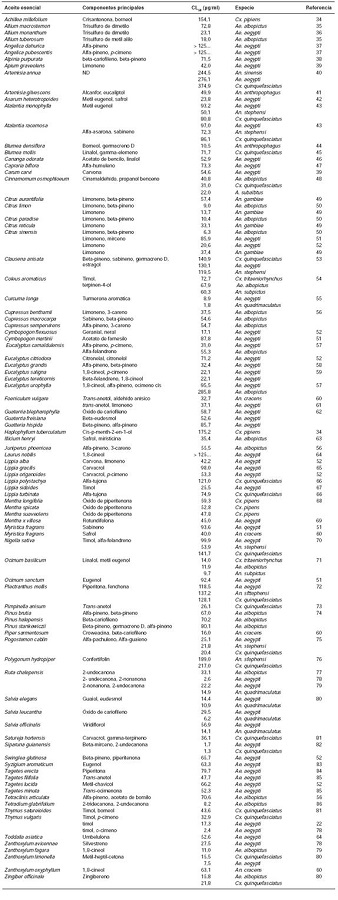
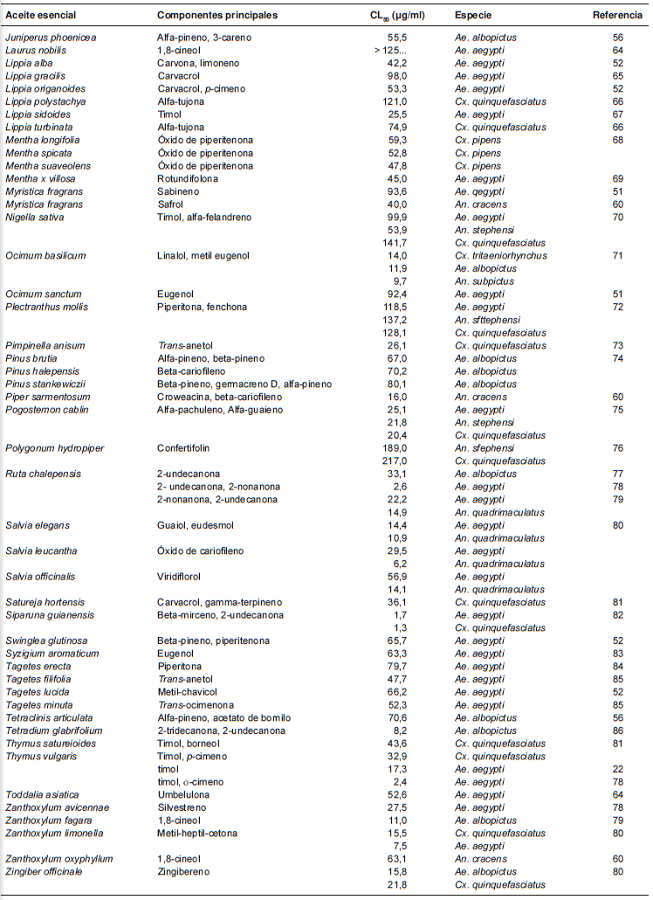
Los aceites esenciales de plantas pertenecientesa las familias botánicas Lamiaceae, Myrtaceae yPoaceae se han reportado ampliamente comoagentes repelentes y larvicidas (87). Gillij, et al.,demostraron que los aceites esenciales extraídosde catorce plantas tenían efecto repelente y larvicidacontra Ae.aegypti (88).
Distintos extractos de Cymbopogon se han utilizadotradicionalmente para repeler a los mosquitos (89).Este género produce los repelentes naturales másutilizados en el mundo (87). La actividad larvicida deC. flexuosus y C. martinii se ha evaluado en larvasde Ae.aegypti, con una CL50 de 17,1 y 87,88 µg/ml, respectivamente (51,52). Los aceites esenciales del género Cymbopogon se caracterizan por teneraltas concentraciones de geraniol y sus derivados.
Los de Ocimum spp. también se han utilizadotradicionalmente como repelentes (90). En O.basilicum se ha demostrado una actividad larvicidarelevante. Govindarajan, et al., reportaron que esteaceite esencial tiene una CL50 menor de 15 µg/mlcontra larvas de Ae. albopictus, An. subpictus yCx. tritaeniorhynchus,en tanto que el de Ocimumsanctum registra una CL50mayor de 90 µg/ml (51).
Las propiedades repelentes y larvicidas del géneroEucalyptus spp. contra mosquitos y otros artrópodosdañinos están bien documentadas (91). El aceiteesencial de Eucalyptus globulus,por ejemplo,poseeactividad larvicidacontra Ae. aegypti (43), y los deE. gunii, E. saligna y E. tereticornis han presentadouna CL50 cercana a 20 µg/ml (59). Por otro lado,el aceite esencial de E. citriodora no registra unabuena actividad repelente contra Ae. aegypti,perosí contra An. dirus y Cx. quinquefasciatus (92), y losde E. urophylla y E. citriodora no poseen actividadlarvicida relevante (52,57), lo cual pone de manifiestoque la actividad larvicida no se presenta siempre yque, incluso, puede depender del sexo.
Los aceites esenciales extraidos del géneroCinnamomum poseen una importante actividadlarvicida; de hecho, se ha reportado que el de C.zeylanicum es el de mayor actividad repelente, puesen una concentración de 0,11 µg/cm2 logra repeler el 100 % de los mosquitos de An. stephensi y Cx.quinquefasciatus durante ocho horas, aproximadamente(93).Porlogeneral,elcinamaldehídoeselcomponentemayoritariodelosaceitesesencialesdeestegénero.Aestefenilpropanoselehanatribuidovariostipos importantes de actividad biológica (48).
También se ha comprobado una relevante actividadlarvicida en los cítricos. Los aceites esenciales deCitrus limon y C. sinensis son los de mayor actividad larvicida en Ae. albopictus, con una CL50 de 9,08 y 6,33 µg/ml, respectivamente (50). Elaceite esencial de C. sinensis se ha estudiadoampliamente, y en las publicaciones revisadas seregistra una tendencia a la resistencia de Ae. aegyptia dicho aceite (51). La mayoría de los autores hanpropuesto que la actividad presente en los aceitesesenciales del género Citrus se debe al limoneno,el terpeno más abundante en ellos (48,52).
Existen varios informes de que los compuestos2-undecanona y 2-nonanona son los mayoritariosen el aceite esencial de Ruta chalepensis y losresponsables de su actividad repelente y larvicida.Auna concentración de 0,080 µg/cm,este aceite tiene un porcentaje de repelencia de 90 %y un tiempo de protección de 90 minutos (77), yvarios autores han demostrando su eficacia comorepelente y larvicida contra Ae. aegypti y An.quadrimaculatus (78).
Los aceites esenciales con mayor actividad larvicidareportada en la presente revisión fueronlos de Curcuma longa y Siparuna guianensis.Ali, et al., reportaron que el aceite esencial deC. longa tiene una CL50de 1,8 µg/ml contra An.quadrimaculatus y que la turmerona aromáticaes su compuesto mayoritario (55). Por su parte,Aguiar, et al., reportaron una CL50de 1,76 y 1,36µg/ml contra Ae. aegypti y Cx. quinquefasciatus,respectivamente, con el aceite esencial de S.guianensis, el cual está principalmente constituidopor beta-mirceno y 2-undecanona (82). Por otrolado, los aceites esenciales con menor actividad larvicidafueronlosdeAchilleamillefolium,Angelicadahurica,Angelicapubescentis,Artemisiaannua,Clausenaanisata, Coriandrum sativum, Croton heliotropiifolius, Haplophyllum tuberculatum, Laurusnobilis, Plectranthus mollis y Polygonum hydropiper,todos ellos con actividades mayores de 100 µg/ml(34,40,53,72).
Como ya se mencionó, los aceites esenciales sonmezclas complejas, y su actividad repelente y larvicidase ha correlacionado, por lo general, consus componentes mayoritarios. Sin embargo, esbien conocido que todos sus componentes puedeninteractuar y modular la actividad biológica (94).
Actividad larvicida de las moléculas puras yefecto de sinergia y antagonismo
Los reportes sobre la actividad repelente y larvicidadeloscomponentespurossonmásescasos en comparación con los relacionados con losaceites esenciales. En la presente revisión, serecopilaron informes sobre la actividad larvicida de68 componentes de diversos aceites esenciales(cuadro 2) y en la figura 1 se pueden observar lasestructuras químicas de las moléculas con mayoractividad larvicida.
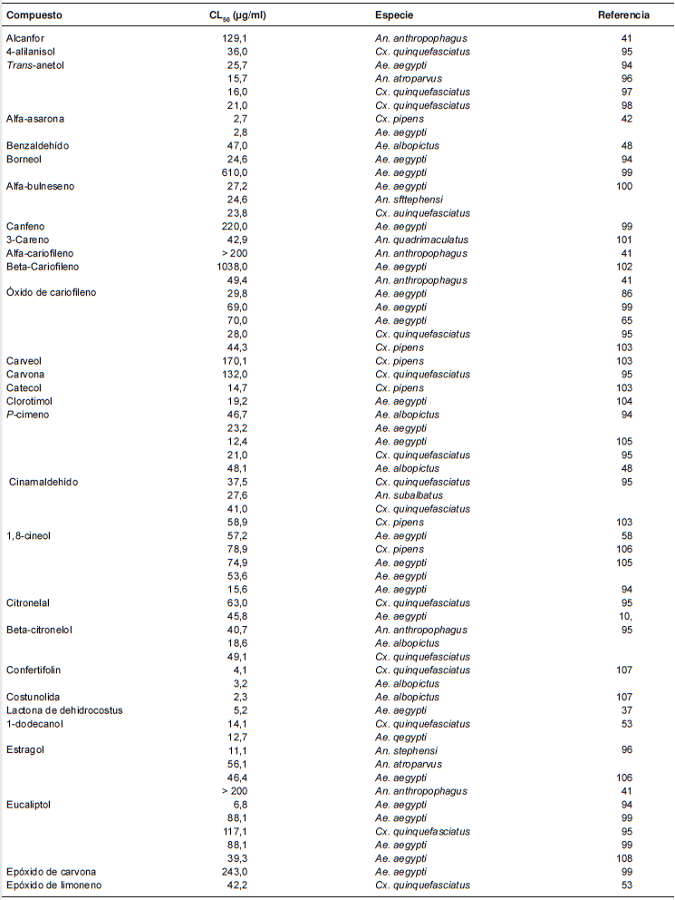
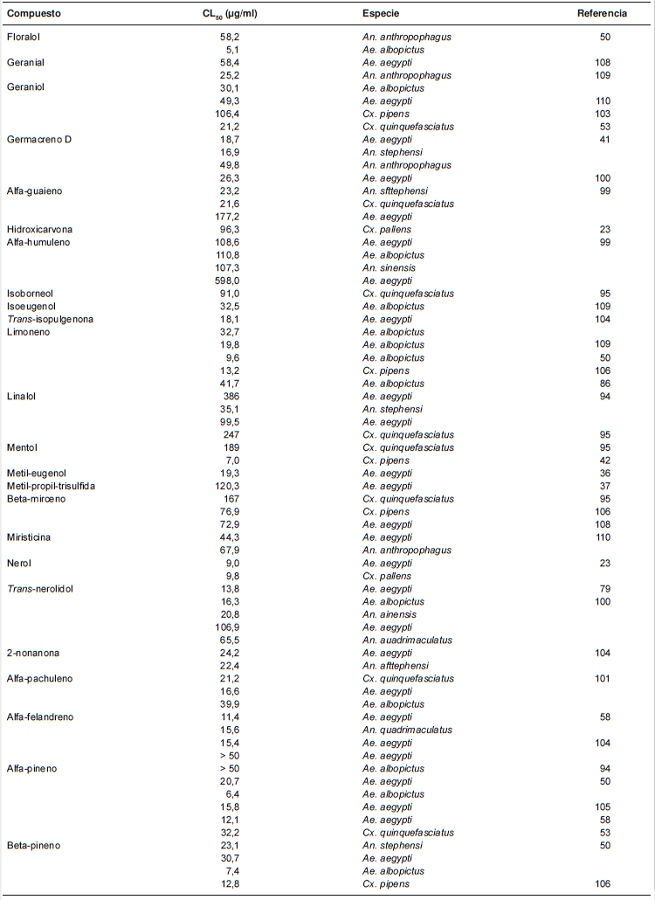
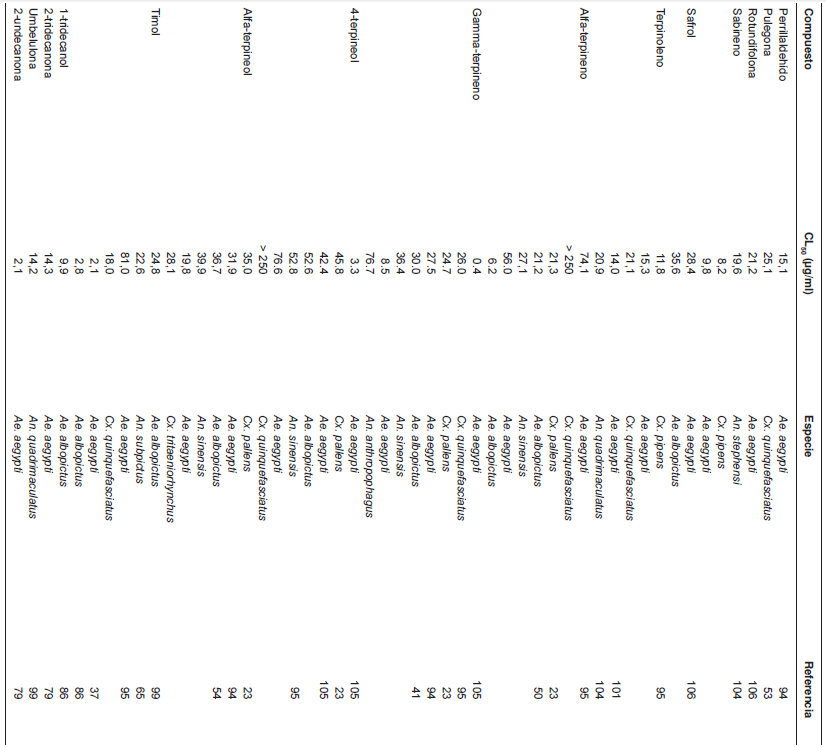
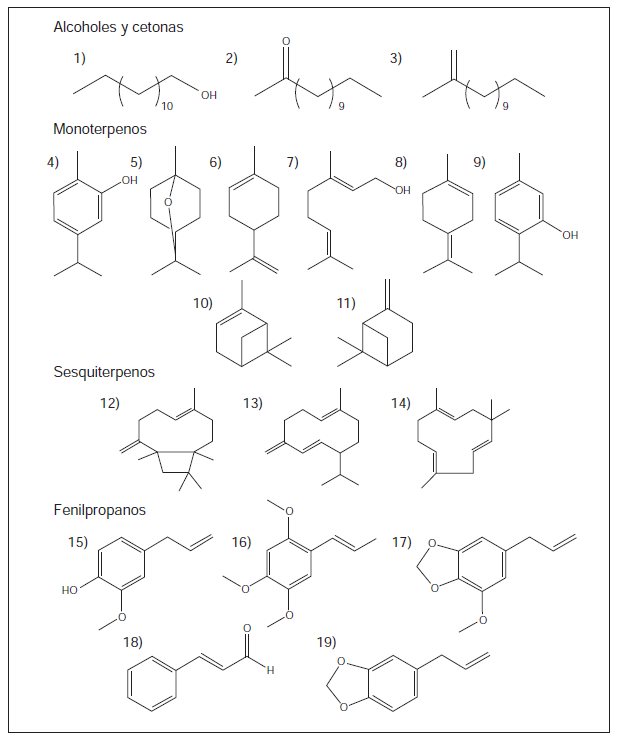
Figura 1
Estructuras químicas de los compuestos con mayor actividad larvicida. 1) 1-tridecanol; 2) 2-undecanona; 3) 2-tridecanona; 4) carvacrol; 5) eucaliptol; 6) limoneno; 7) geraniol; 8) terpinoleno; 9) timol; 10) alfa-pineno; 11) beta-pineno; 12) beta-cariofileno; 13)germacreno D; 14) beta-humuleno; 15) eugenol; 16) asarona; 17) miristicina; 18) cinamaldehído; 19) safrol
Algunos de los compuestos con mayor actividadlarvicida son la 2-undecanona y el 1-tridecanol,con una CL50de 2,1 y 9,95 µg/ml, respectivamente(79,37). Liu, et al., reportaron una CL50de 2,86 µg/mlpara la 2-tridecanona (86). Varios fenilpropanoides,como el trans-anetol, el cinamaldehído o el eugenol,han presentado una importante actividad larvicida,en tanto que la alfa-asaronafue el fenilpropanoidecon mayor actividad larvicida, con una CL50de 2,7y de 2,8 µg/ml contra Cx. pipens y Ae. aegypti,respectivamente (42). El alfa-cariofileno y el betacariofileno,este último con actividad repelenterelevante, no han presentado actividad larvicida(41,102), mientras que el óxido de cariofileno sí. Los sesquiterpenos con mayor actividad fueron lalactona de dehidrocostus y la costunolida, con unaCL50 de 2,34 y 3,26 µg/ml contra Ae. albopictus(107), y el confertifolin con una LC50 de 3,09 y 4,18µg/ml contra An. sfttephensi y Cx. quinquefasciatus,respectivamente (76).
Ali, et al., evaluaron la actividad repelente y larvicidade la 2-nonanona y la 2-undecanona paradeterminar qué componente era el responsable dela actividad del aceite esencial de R. chalepensis(79). Sus resultados demostraron que se requierenconcentraciones menores de 2-undecanona pararepeler mosquitos y eliminar larvas de Ae. aegypti yAn. quadrimaculatus. Estos datos sobre el efecto delaceite esencial en su conjunto y de los componentesmayoritarios por separado, son interesantes. El aceite esencial de R. chalepensis ha registrado una CL50 de 22,2 µg/ml contra larvas de Ae. aegypti,mientras que la de su compuesto mayoritario esde CL50de 14,37 µg/m, lo cual permitiría concluirque la 2-undecanona es la responsable de laactividad larvicida del aceite esencial; sin embargo,es importante resaltar que el aceite esencial en suconjunto posee menor actividad, por lo que se podríaconcluir que se produce un efecto antagónico entretodos sus componentes.
Los efectos sinérgicos y antagónicos de los componentes de los aceites esenciales se han demostrado(111) y se han discutido con anterioridad (112,113).Se demostró, por ejemplo, que las combinacionesde linalol y 1,8-cineol tenían efectos sinérgicos en la mortalidad de diversos insectos (114), en tantoque la mezcla de timol y trans-anetol tenía efectossinérgicos sobre la actividad larvicida contraSpodoptera litura (115). Estos resultados indicanque la actividad larvicida de los aceites esencialesno se asocia únicamente con los compuestosmayoritarios, sino que otras moléculas presentesen menor proporción también contribuyen a suactividad (111-115).
El estudio de los efectos sinérgicos se orienta aencontrar mezclas de compuestos que produzcanmejores efectos con menor concentración. En unamplio estudio, se demostró el efecto sinérgico demás de 20 sustancias en diferentes combinacionescontra larvas de Cx.quinquefasciatus; entre lascombinaciones más efectivas se encontraron lasde limoneno con trans-anetol y de carvona con carvacrol(116).
Porotrolado,enestemismoestudio, se señala que la actividad larvicida del borneol yel alcanfor se potencializa cuando se los mezcla,en tanto que de manera aislada no exhiben unaactividad significativa. Liu, et al., también han estudiadolos efectos sinérgicos y encontraron quela actividad repelente de la mezcla de aceites deArtemisia princeps y Cinnamomum alcanfora erasignificativamente mayor que la de cada uno deestos por separado (116).
Es necesario ampliar las investigaciones sobre los mecanismos implicados en las interacciones entre los componentes que mejoran o dificultan la actividad repelente y la larvicida, y resaltar la importancia de estudiar dichas actividades en los componentes puros, pues sus mecanismos de acción ofrecen resultados más claros e, incluso,permiten generar modelos predictivos basados enla relación entre su estructura y su actividad.
Relación entre estructura y actividad y entrepropiedad y actividad
Existe una amplia documentación sobre estosdos tipos de relación de los fitoquímicos y de suactividad larvicida (117,118). Dichos estudios hancontribuido a la búsqueda y el diseño de nuevoscompuestos con mayor actividad larvicida, y han aportado información sobre su modo de acción en los insectos. Se ha reportado que los anillosaromáticos y los grupos hidroxilos resultan enun aumento de la actividad, particularmente enpresencia de grupos fenólicos (119). Además, los grupos hidroxilos parecen disminuir la actividad, yaque al sustituir un grupo carbonilo con un grupohidroxilo, el resultado final es la disminución de laactividad larvicida (120).
García, et al., por ejemplo, demostraron que delos monoterpenos pulegol (alcohol monoterpeno)y pulegona (cetona monoterpeno), el primeroera menos tóxico contra los adultos de Triboliumcastaneum (121), debido a que los grupos hidroxiloaumentan la polaridad de las moléculas, lo cualdificulta su penetración en las cutículas de laslarvas (122).
Algunos autores han estudiado la importanciade los grupos cetónicos en la estructura de losterpenoides. Los reportes demuestran que la presenciadeungrupocarboniloexocíclicoyeldobleenlaceconjugadoparecencontribuiralaactividadlarvicida(69).Engeneral,lasustitucióndeldobleenlaceporungrupoepóxidodisminuyelaactividad(69,123).En otros estudios se ha demostrado laimportancia de los dobles enlaces en las estructurasterpénicas. Porejemplo,elbeta-pinenotienemayoractividadlarvicidaqueelalfa-pinenocontraAe.aegypti,locualsehaasociadoconelhechodequeeldobleenlacedelbeta-pinenoseencuentra fueradelanillo,mientrasqueelalfa-pinenotieneeldobleenlace sobre este (58).
Se ha informado que los aldehídos aislados no sonimportantes para el efecto larvicida; sin embargo,cuando el aldehído está conjugado con un sistemaaromático, esto contribuye positivamente a su actividad(124). Este efecto se observa en la granpotencia larvicida del cinamaldehído, un fenilpropanoidetotalmenteconjugado(103).Dehecho,elnúmerodedoblesenlacesconjugadoscontribuyeaaumentar la actividad. Se ha reportado que elp-cimeno, el timol, el carvacrol y el eugenol exhibenmayor actividad que la carvona, los pinenos y losterpinenos (99), lo cual evidencia que la influenciade la densidad electrónica y el carácter plano deestas estructuras tienen un papel importante en suactividad biológica (125).
Se ha evaluado la importancia del grupo éster enla actividad larvicida y se ha encontrado que, alsustituir el grupo hidroxilo por un grupo acetato, laactividad larvicida aumenta significativamente (69).
Además de los estudios sobre la relación de la actividad larvicida y la estructura, se han llevado acabo otros sobre la relación entre las propiedadesfisicoquímicas y moleculares y dicha actividad. Seha observado que el carácter hidrófilo (hydrofilicity) y la capacidad de polarización (refractivity) molarse encuentran en relación negativa con la toxicidad de las cumarinas contra Cx. pipens y Ae. aegypti (118). Esta relación negativa también seha informado en los terpenos y terpenoides conactividad larvicida (23). El carácter lipófilo de losaceites y sus componentes también tiene un rolclave. Se ha observado que la lipofilia está muyrelacionada con la inhibición y la desactivaciónenzimática (21). La importancia de la lipofilia delos terpenos y terpenoides se ha confirmado alestudiar la relación entre propiedad y actividad, enlos cuales el perfil hidrofóbico se ha relacionadoestrechamente con la actividad larvicida (119).Lucía, et al., desarrollaron un modelo con base enla actividad de seis monoterpenos y observaronque, cuando los valores de la presión de vapor y elcoeficiente de partición del octanol y el agua (LogP)disminuían, también lo hacía la concentración letalde la actividad larvicida contra Ae. aegypti (105).
Este acentuado efecto de la lipofilia se explica porel hecho de que el principal canal de entrada delos componentes en el organismo es táctil (cutículaexterna), y el efecto larvicida se evalúa principalmentemediante la inmersión de larvas en unambiente acuoso donde se aplica el aceite esencial,de manera que puede plantearse que la particiónse produce entre el ambiente hidrófilo (agua) yun entorno lipófilo (epicutícula larval), por lo cualla hidrofobia de la molécula desempeña un papelimportante en la intoxicación de la larva (126).
Otros descriptores relacionados con la actividadlarvicida son el momento dipolar, el punto deebullición y la presión de vapor (127). El momentodipolar es un indicador de la lipofilia y la hidrofobia(128) y se lo ha asociado con la actividad repelente(129). Por otra parte, se ha demostrado que losrepelentes más eficaces poseen un punto de ebulliciónyunapresióndevaporquelespermitetenermayortiempodecontactoconlosmosquitos(127).Enunestudiollevadoacaboconsesquiterpenosseencontró que la actividad repelente de estoscompuestos se relacionaba principalmente con lapresión de vapor y con parámetros electrónicos,así como con la capacidad de polarización de lamolécula (POL) y el orbital molecular desocupadode menor energía (Lowest Unoccupied MolecularOrbital, LUMO) (130), de tal manera que, en susmodelos, la actividad repelente aumentó a medidaque disminuyó la capacidad de polarización, mientrasque los parámetros LUMO mantuvieron unarelación directa con la actividad. En la figura 2 seilustra el mapeo de los orbitales frontera del orbital molecular ocupado de mayor energía (Highest Occupied Molecular Orbital, HOMO) y del LUMOde sesquiterpenos con actividad larvicida.
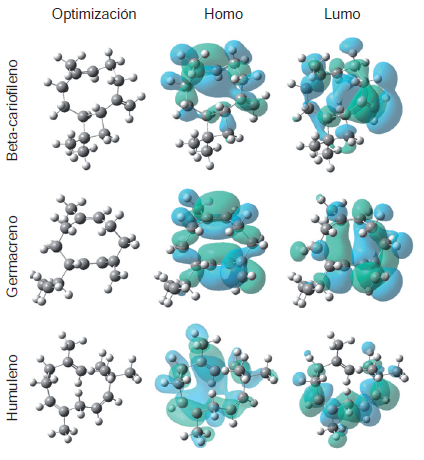
Figura 2
Mapeo de orbitales HOMO y LUMO de sesquiterpenos con actividad larvicida a partir de una optimización, y cálculo de la energía de nivel mediante el método de Hartree-Fock utilizando un conjunto de base 6-311(d,p): 1) beta-cariofileno; 2) germacreno D; 3) humuleno
Las energías del orbital molecular ocupado de mayorenergía y del orbital desocupado de menor energía(EHOMO y ELUMO) forman parte de los descriptoresmecánico-cuánticos más populares. De hecho, enmuchos casos estos orbitales determinan la reacciónquímica de un compuesto y el posible mecanismode ella (125). El orbital HOMO se emplea como unindicador de las zonas de alta densidad electrónica,pues estas exhiben una región propicia para elataque de compuestos electrófilos, mientras que unreactivo o compuesto nucleófilo es atraído hacia laszonas de más baja densidad electrónica indicadaspor el orbital LUMO (125).
Mecanismo de acción
Muchos grupos de investigación se han centradoen la eficiencia larvicida de los aceites esenciales,sin embargo, hay poca información concluyentesobre su mecanismo de acción contra las larvasy los insectos adultos. La primera complicación sedebe a que es difícil determinar los mecanismosde acción de un producto que no es una sustanciapura, sino una mezcla de varios componentes, yaque todas las interacciones entre los compuestospueden influir en la actividad (131).
En algunos reportes se ha señalado que los aceitesesenciales o sus componentes monoterpenoidesproducen intoxicación neurotóxica, similar a laproducida por los organofosforados y carbamatos,mediante la inhibición de la enzima acetilcolinesterasa(132,133). El efecto neurotóxico seproduce cuando, en la transmisión del impulsonervioso, la acetilcolina es liberada de las vesículasde las terminales nerviosas cuando estas son despolarizadasy,acontinuación,laacetilcolinaingresaala sinapsis y se une al receptor postsináptico.Esta posee una vida media corta debido a lapresencia de la acetilcolinesterasa, una enzimaque hidroliza la unión éster de la molécula, conlo cual se interrumpe la actividad estimuladora.La inhibición de la acetilcolinesterasa prolonga latransmisión eléctrica, ya que la acetilcolina estáestimulada (134).
En un estudio comparativo de la acción fumígenade los aceites esenciales obtenidos de plantasde la familia Labiatae y el limoneno en adultosde Rhyzopertha dominica,sedemostró que losaceites esenciales en conjunto inhibían en 65 %la acetilcolinesterasa, en tanto que el limoneno lo hacía solamente en el 2 % (117). Además, losautores observaron que los aceites esencialesincrementaron significativamente los niveles deadenosín monofosfato cíclico (incluso con muybajas concentraciones), lo cual sugiere una posibleacción sobre la octopamina.
Se ha reportado también que el aceite esencialde Artemisia maderaspatana inhibe la acetilcolinesterasaconunaconcentracióninhibitoriamedia(CI50)de31,33µg/ml(135).Enan,etal.,obtuvieronresultadossimilares en moscas y cucarachas expuestas a eugenol y alfa-terpineol y demostraron que estos compuestos producían efectos deexcitación extrema en los insectos, ocasionandoposteriormente la muerte (136).
También, se ha demostrado que el limoneno, elmirceno, el linalol y el terpineol son agentes neurotóxicoscontra la mosca común (137), resultadosque confirman la hipótesis de que el linalol es unfuerte inhibidor de la acetilcolinesterasa (138). Dehecho, en estudios de simulación computacional seha demostrado que el linalol es capaz de interactuarcon dicha enzima en Ae. aegypti, lo cual demuestraque este se une a un sitio hidrofóbico interactuandocon algunos aminoácidos lipófilos, como la glicina412, 409, 412 y la isoleucina 413 (139).
Por otro lado, se ha reportado que el aceite esencialde Zingiber officinale altera el comportamientodel sistema colinérgico (140). Asimismo, se hademostrado que el alfa-pineno y el beta-pinenoson capaces de inhibir la acetilcolinesterasa, sinembargo, a pesar de que los pinenos inhiben fuertementelaenzima,nopresentanactividadlarvicidarelevante(141,142), efecto que se ha atribuido aque los pinenos no logran penetrar la cutícula delinsecto (143). Otros autores han demostrado queel beta-felandreno es un potente inhibidor de laacetilcolinestersa, al igual que el ocimeno cis y elestragol (144).
En otros estudios de acoplamiento molecular, seha reportado que el eucaliptol y el carvacrol soncapaces de unirse con mayor eficacia que laacetilcolina a la acetilcolinesterasa de Ae.aegypti(145). Asimismo, en estudios de simulación computacionalsehademostradoqueelbeta-cariofilenotienemejor energía libre de enlace que la acetilcolinesterasa,por lo cual también constituye uninhibidor competitivo (146). Sin embargo, algunosautores concuerdan en que, en la mayoría delos casos, no hay relación entre la inhibiciónde la acetilcolinesterasa y los compuestos quedemuestran tener mayor efecto larvicida, por locual han sugerido que el mecanismo de accióndebe ser otro (144,145).
La octopamina también ha sido un blanco delos estudios sobre la actividad de los aceitesesenciales. Está presente en el sistema nerviosode todos los insectos y actúa como neurotransmisor,neurohormona y neuromodulador (147).Otra función que se le atribuye está relacionadacon el comportamiento activo o de "atención", por loque se ha sugerido que forma parte de un sistemageneral que prepara al insecto para su actividad vigorosa. Algunos autores han planteado que loscomponentes de los aceites esenciales actúanbloqueando los receptores de la octopamina (131)y produciendo alteraciones neurológicas gravescon efectos nocivos para los insectos. El eugenoly el timol, por ejemplo, pueden funcionar medianteel bloqueo de estos receptores (147,148). Con elacoplamiento molecular se ha demostrado que elcarvacrol, el eugenol y el eucaliptol son capaces deinteractuar en el sitio de unión del receptor oambde la octopamina de Ae.aegypti (145).
Otro mecanismo propuesto es la interacción delos componentes de los aceites esenciales conlos receptores GABA. Se ha demostrado que eltimol, por ejemplo, interactúa con estos receptores en un sitio de unión aun no identificado (148,149).Algunos sesquiterpenos tricíclicos han resultadoser potentes inhibidores de estos receptores (150).Asimismo, la tujona, un monoterpenoide bicíclico,se ha clasificado como un insecticida neurotóxicoque también actúa sobre estos receptores (151).
Recientemente, se reportó que los terpenos y losterpenoides son capaces de interactuar con laproteína transportadora de esterol (AeSCP-2) deAe.aegypti, por lo que supone un nuevo y potencialblanco terapéutico (152).
La información que se ha reseñado permite concluirque los componentes de los aceites esenciales notendrían un solo mecanismo de acción. Además,todo indica que ejercen diversos efectos en elinsecto, una vez que atraviesan su cutícula.
Con respecto a la dilucidación del mecanismode acción, son pocos los estudios de simulacióncomputacional. Actualmente, la mayoría de losblancos propuestos para el control de Ae. aegypti,se encuentra en forma cristalizada, registrada enbases de datos como la del Proteín Data Bank(PDB) (145,148,152). En el caso de otros génerosy especies, las secuencias aminoacídicas de estasproteínas se encuentran en bases de datos comolas del National Center for Biotechnology Information(NCBI). Esta información es de gran utilidad, ya quemediante herramientas computacionales como elacoplamiento y la dinámica molecular se puede llevara cabo la búsqueda racional de posibles blancosbiológicos y la dilucidación de sus mecanismos deacción, así como el diseño de nuevos compuestoslarvicidas. La figura 3 ilustra las propuestasde blancos terapeúticos de los componentes deaceites esenciales, algunas de ellas contruídas porhomología en nuestro grupo de investigación.
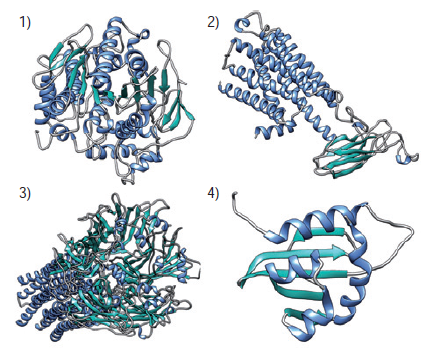
Figura 3
Dianas biológicas implicadas en el mecanismo de acción de los aceites esenciales y sus componentes. 1) Acetilcolinesterasa de Ae. aegypti modelada por homología utilizando la secuencia GenBank ABN09910.1, y usando como templete el modelo el PDB: 2W6C; 2) receptor oamb de octopamina de An.sinensis modelada por homología utilizando la secuencia GenBank KFB42017.1, y usando como templete el modelo el PDB: 2Y03; 3) receptor GABA de Cx. quinquefaciatus modelado por homología utilizando la secuencia GenBank EDS38917.1, y usando como templete el modelo el PDB: 5CFB; 4) proteína transportadora de esterol de Ae. aegypti cristalizada reportada con el PDB: 2KSH
Conclusiones
En la búsqueda de alternativas reales que puedanaplicarse en los programas de control de enfermedadestransmitidas por vectores, los aceitesesenciales constituyen una excelente alternativapor su considerable potencial como repelentes ylarvicidas, su bajo nivel de toxicidad para los mamíferosy su limitado impacto ambiental. Además,algunos, como el metileugenol, la alfa-asarona y lapelitorina, han demostrado ser eficaces contra Cx.p. pallens resistente a clorpirifos, fenitrotión, fentióny alfa-cipermetrina.La actividad repelente y larvicida de los aceitesesenciales es de gran importancia porque demuestraque no es necesario producir un compuesto activo puro, ya que el uso de varios de ellos enconjunto puede ser una solución más barata, eficazy sencilla. Asimismo, el estudio de los efectossinérgicos entre los componentes de los aceitesesenciales y las mezclas de ellos ha abierto elcamino para el reemplazo de los productos sintéticosutilizados tradicionalmente.
El estudio de los componentes puros es crucial paraentender el mecanismo de la acción que ejercen sobre las larvas y los moquitos adultos. Por otra parte, las nuevas herramientas computacionalestodavía no se han explorado suficientemente, porlo que representan un área de estudio prometedorapara la dilucidación de los mecanismos de acción,y el diseño y la búsqueda racional de moléculascon actividad larvicida.
La mayoría de las investigaciones sobre aceitesesenciales como nuevos agentes larvicidas se hallevado a cabo en laboratorio, pero si se los quiereproponer como una solución real y utilizarlos en losprogramas de salud pública, se requiere la investigaciónencampo,demaneraquelascondicionesgeográficasyclimáticasseanlasquedeterminenlafactibilidad y pertinencia de su uso.
Referencias
1. KumarK, SharmaAK, KumarS, PatelS, SarkarM, ChauhanLS. Multiple insecticide resistance/susceptibility status of Culex quinquefasciatus, principal vector of bancroftian filariasis from filaria endemic areas of northern India. Asian Pac J Trop Dis. 2011;4:426-9. https://doi.org/10.1016/S1995-7645(11)60119-3
2. TatemAJ, HuangZ, DasA, QiQ, RothJ, QiuY. Air travel and vector-borne disease movement. Parasitol. 2012;139:181630. https://doi.org/10.1017/S0031182012000352
3. RamaiahKD, OttesenEA. Progress and impact of 13 years of the Global Programme to Eliminate Lymphatic Filariasis on reducing the burden of filarial disease. PLoS Negl Trop Dis. 2014;8:e3319. https://doi.org/10.1371/journal.pntd.0003319
4. CampbellLP, LutherC, Moo-LlanesD, RamseyJM, Danis LozanoR, PetersonAT. Climate change influences on global distributions of dengue and chikungunya virus vectors. Philos Trans R Soc Lond B Biol Sci. 2015;370:20140135. https://doi.org/10.1098/rstb.2014.0135
5. BhatiaR, DashAP, SunyotoT. Changing epidemiology of dengue in South-East Asia. WHO South East Asia J Public Health. 2013;2:23. https://doi.org/10.4103/2224-3151.115830
6. TolleMA. Mosquito-borne diseases. Curr Probl Pediatr Adolesc Health Care. 2009;39:97-140. https://doi.org/10.1016/j.cppeds.2009.01.001
7. FischerD, ThomasSM, SukJE, SudreB, HessA, TjadenNB, et al. Climate change effects on Chikungunya transmission in Europe: Geospatial analysis of vector's climatic suitability and virus' temperature requirements. Int J Health Geogr. 2013;12:51. https://doi.org/10.1186/1476072X-12-51
8. van BortelW, DorleansF, RosineJ, BlateauA, RoussetD, MatheusS, et al. Chikungunya outbreak in the Caribbean region, December 2013 to March 2014, and the significance for Europe. Euro Surveill. 2014;19:20759.
9. World Health Organization. World Malaria Report 2015. Geneva: WHO; 2015. Fecha de consulta: 15 de junio de 2015. Disponible en: Disponible en: http://www.who.int/malaria/publications/world-malaria-report-2015/report/en/ .
10. BéguinA, HalesS, RocklövJ, ÅströmC, LouisVR, SauerbornR. The opposing effects of climate change and socio-economic development on the global distribution of malaria. Glob Environ Chang. 2011;21:1209-14. https://doi.org/10.1016/j.gloenvcha.2011.06.001
11. LaniakGF, OlchinG, GoodallJ, VoinovA, HillM, GlynnP, et al. Integrated environmental modeling: A vision and roadmap for the future. Environ Model Softw. 2013;39:3-23. https://doi.org/10.1016/j.envsoft.2012.09.006
12. ShumanEK. Global climate change and infectious diseases. New Eng J Med. 2010;362:1061-3. https://doi.org/10.1056/NEJMp0912931
13. OcampoCB, Salazar-TerrerosMJ, MinaNJ, McAllisterJ, BrogdonW. Insecticide resistance status of Aedes aegypti in 10 localities in Colombia. Acta Trop. 2011;118:37-44. https://doi.org/10.1016/j.actatropica.2011.01.007
14. MirandaJE, NavickieneHM, Nogueira-CoutoRH, De BortoliSA, KatoMJ, da Silva BolzaniV, et al. Susceptibility of Apis mellifera (Hymenoptera: Apidae) to pellitorine, an amide isolated from Piper tuberculatum (Piperaceae). Apidologie. 2003;34:409-15. https://doi.org/10.1051/apido:2003036
15. LinH, Chuan-huaX, Jin-junW, MingL, Wen-caiL, ZhimoZ. Resistance selection and biochemical mechanism of resistance to two acaricides in Tetranychus cinnabarinus (Boiduval). Pest Biochem Physiol. 2009;93:47-52. https://doi.org/10.1016/j.pestbp.2008.11.001
16. MatowoJ, KitauJ, KabulaB, KavisheR, OxboroughR, KaayaR, et al. Dynamics of insecticide resistance and the frequency of kdr mutation in the primary malaria vector Anopheles arabiensis in rural villages of Lower Moshi, North Eastern Tanzania. J Parasitol Vector Biol. 2014;6:31-41. https://doi.org/10.5897/JPVB2013.0143
17. VontasJ, KioulosE, PavlidiN, MorouE, Della TorreA, RansonH. Insecticide resistance in the major dengue vectors Aedes albopictus and Aedes aegypti. Pest Biochem Physiol. 2012;104:126-31. https://doi.org/10.1016/j.pestbp.2012.05.008
18. Chino-CantorA, Sánchez-ArroyoH, Ortega-ArenasLD, Castro-HernándezE. Insecticide susceptibility of Aedes aegypti L. (Diptera: Culicidae) in Guerrero, México. Southwestern Entomol. 2014;39:601-12. https://doi.org/10.3958/059.039.0319
19. OvergaardHJ, SandveSR, SuwonkerdW. Evidence of anopheline mosquito resistance to agrochemicals in northern Thailand. Southeast Asian J Trop Med Public Health.2005;36(Suppl.4):152-7.
20. CondeM, OrjuelaLI, CastellanosCA, Herrera-VarelaM, LicastroS, QuiñonesML. Insecticide susceptibility evaluation in Aedes aegypti populations of Caldas, Colombia, in 2007 and 2011. Biomédica. 2015;35:43-52. https://doi.org/10.7705/biomedica.v35i1.2367
21. LangenheimJH. Higher plant terpenoids: A phytocentric overview of their ecological roles. J Chem Ecol. 1994;20:1223-80. https://doi.org/10.1007/BF02059809
22. WangZQ, PerumalsamyH, WangM, ShuS, AhnYJ. Larvicidal activity of Magnolia denudata seed hydrodistillate constituents and related compounds and liquid formulations towards two susceptible and two wild mosquito species. Pest Manag Sci. 2015;72:897-906. https://doi.org/10.1002/ps.4064
23. MasseboF, TadesseM, BekeleT, Gebre-MichaelMB. Evaluation on larvicidal effects of essential oils of some local plants against Anopheles arabiensis Patton and Aedes aegypti Linnaeus (Diptera, Culicidae) in Ethiopia. Afr J Biotechnol. 2009;8:4183.
24. CastilloS, Pérez-AlfonsoCO, Martínez-RomeroD, GuillénF, SerranoM, ValeroD. The essential oils timol and carvacrol applied in the packing lines avoid lemon spoilage and maintain quality during storage. Food Control. 2014;35:132-6. https://doi.org/10.1016/j.foodcont.2013.06.052
25. BakkaliF, Averbeck S. Averbeck D, IdaomarM. Biological effects of essential oils-a review. Food Chem Toxicol. 2008;46:446-75. https://doi.org/10.1016/j.fct.2007.09.106
26. BurtS. Essential oils: Their antibacterial properties and potential applications in foods-a review. Int J Food Microbiol. 2004;94:223-53. https://doi.org/10.1016/j.ijfoodmicro.2004.03.022
27. PesaventoG, CalonicoC, BiliaAR, BarnabeiM, CalesiniF, AddonaR, et al. Antibacterial activity of Oregano, Rosmarinus and Thymus essential oils against Staphylococcus aureus and Listeria monocytogenes in beef meatballs. Food Control. 2015;54:188-99. https://doi.org/10.1016/j.foodcont.2015.01.045
28. SaracN, UgurA. Antimicrobial activities of the essential oils of Origanum onites L., Origanum vulgare L. subspecies hirtum (Link) Ietswaart, Satureja thymbra L., and Thymus cilicicus Boiss. & Bal. growing wild in Turkey. J Med Food. 2008;11:568-73. https://doi.org/10.1089/jmf.2007.0520
29. SantoroGF, das Graças CardosoM, GuimarãesLG, SalgadoAP, Menna-BarretoRF, SoaresMJ. Effect of oregano (Origanum vulgare L.) and thyme (Thymus vulgaris L.) essential oils on Trypanosoma cruzi (Protozoa: Kinetoplastida) growth and ultrastructure. Parasitol Res. 2007;100:783-90. https://doi.org/10.1007/s00436-006-0326-5
30. ProphiroJS, da SilvaMA, KanisLA, da SilvaBM, Duque-LunaJE, da SilvaOS. Evaluation of time toxicity, residual effect, and growth-inhibiting property of Carapa guianensis and Copaifera sp. in Aedes aegypti. Parasitol Res. 2012;110:713-9. https://doi.org/10.1007/s00436-0112547-5
31. BatishDR, SinghHP, KohliRK, KaurS. Eucalyptus essential oil as a natural pesticide. Forest Ecol Manag. 2008;256:2166-74. https://doi.org/10.1016/j.foreco.2008.08.008
32. KiranSR, BhavaniK, DeviPS, RaoBR, ReddyKJ. Composition and larvicidal activity of leaves and stem essential oils of Chloroxylon swietenia DC against Aedes aegypti and Anopheles stephensi. Bioresour Technol. 2006;97:2481-4. https://doi.org/10.1016/j.biortech.2005.10.003
33. World Health Organization. Guidelines for laboratory and field testing of mosquito larvicides. Geneva: WHO; 2005. Fecha de consulta: 15 de junio de 2015. Disponible en:Disponible en:http://www.who.int/whopes/guidelines/en/ .
34. BenelliG, BediniS, FlaminiG, CosciF, CioniPL, AmiraS, et al. Mediterranean essential oils as effective weapons against the West Nile vector Culex pipiens and the Echinostoma intermediate host Physella acuta: What happens around? An acute toxicity survey on non-target mayflies. Parasitol Res. 2015;114:1011-21. https://doi.org/10.1007/s00436-014-4267-0
35. LiuXC, LiuQY, ZhouL, LiuZL. Evaluation of larvicidal activity of the essential oil of Allium macrostemon Bunge and its selected major constituent compounds against Aedes albopictus (Diptera: Culicidae). Parasit Vector. 2014;7:184. https://doi.org/10.1186/1756-3305-7-184
36. MoonHI. Larvicidal activity of major essential oils from stems of Allium monanthum Maxim. against Aedes aegypti L. J Enzyme Inhib Med Chem. 2011;26:827-30. https://doi.org/10.3109/14756366.2011.558842
37. TabancaN, GaoZ, DemirciB, TechenN, WedgeDE, AliA, et al. Molecular and phytochemical investigation of Angelica dahurica and Angelica pubescentis essential oils and their biological activity against Aedes aegypti, Stephanitis pyrioides, and Colletotrichum Species. J Agric Food Chem. 2014;62:8848-57. https://doi.org/10.1021/jf5024752
38. SantosGK, DutraKA, BarrosRA, da CâmaraCA, LiraDD, GusmãoNB, et al. Essential oils from Alpinia purpurata (Zingiberaceae): Chemical composition, oviposition deterrence, larvicidal and antibacterial activity. Ind Crop Prod. 2012;40:254-60. https://doi.org/10.1016/j.indcrop.2012.03.020
39. PitasawatB, ChampakaewD, ChoochoteW, JitpakdiA, ChaithongU, KanjanapothiD, et al. Aromatic plant-derived essential oil: An alternative larvicide for mosquito control. Fitoterapia. 2007;78:205-10. https://doi.org/10.1016/j.fitote.2007.01.003
40. CheahSX, TayJW, ChanLK, JaalZ. Larvicidal, oviposition, and ovicidal effects of Artemisia annua (Asterales:Asteraceae) against Aedes aegypti, Anopheles sinensis, and Culex quinquefasciatus (Diptera: Culicidae). Parasitol Res. 2013;112:3275-82. https://doi.org/10.1007/s00436-013-3506-0
41. ZhuL, TianY. Chemical composition and larvicidal activity of essential oil of Artemisia gilvescens against Anopheles anthropophagus. Parasitol Res. 2013;112:1137-42. https://doi.org/10.1007/s00436-012-3243-9
42. PerumalsamyH, ChangKS, ParkC, AhnYJ. Larvicidal activity of Asarum heterotropoides root constituents against insecticide-susceptible and-resistant Culex pipiens pallens and Aedes aegypti and Ochlerotatus togoi. J Agric Food Chem. 2010:58:10001-6. https://doi.org/10.1021/jf102193k
43. ArunKD, KumarS, SwamyJP. Larvicidal activity and leaf essential oil composition of three species of genus Atalantia from south India. Int J Mos Res. 2015;2:25-9.
44. ZhuL, TianY. Chemical composition and larvicidal activity of Blumea densiflora essential oils against Anopheles anthropophagus: A malarial vector mosquito. Parasitol Res. 2011;109:1417-22. https://doi.org/10.1007/s00436-011-2388-2
45. SenthilkumarA, KannathasanK, VenkatesaluV. Chemical constituents and larvicidal property of the essential oil of Blumea mollis (D. Don) Merr. against Culex quinquefasciatus. Parasitol Res. 2008;103:959-62. https://doi.org/10.1007/s00436-008-1085-2
46. TanLTH, LeeLH, YinWF, ChanCK, Abdul KadirH, ChanKG, et al. Traditional uses, phytochemistry, and bioactivities of Cananga odorata (Ylang-Ylang). Evid Based Complement Alternat Med. 2015;2015:896314. https://doi.org/10.1155/2015/896314
47. SouzaLG, AlmeidaMC, MonteFJ, SantiagoGM, Braz-FilhoR, LemosTL, et al. Chemical constituents of Capraria biflora (Scrophulariaceae) and larvicidal activity of essential oil. Química Nova. 2012;35:2258-62. https://doi.org/10.1590/S0100-40422012001100032
48. ChengSS, LiuJY, HuangCG, HsuiYR, ChenWJ, ChangST. Insecticidal activities of leaf essential oils from Cinnamomum osmophloeum against three mosquito species. Bioresource Technol. 2009;100:457-64. https://doi.org/10.1016/j.biortech.2008.02.030
49. AkonoPN, DongmoPM, TongaC, KouotouS, KekeunouS, MagneGT, et al. Larvicidal activity of essential oils from pericarps of ripe Citrus fruits cultivated in Cameroon on pyrethroids sensitive and resistant strains of Anopheles gambiae Giles, 1902. J Entomol Zool Studies. 2015;3:334-9.
50. GiatropoulosA, PapachristosDP, KimbarisA, KoliopoulosG, PolissiouMG, EmmanouelN, et al. Evaluation of bioefficacy of three Citrus essential oils against the dengue vector Aedes albopictus (Diptera: Culicidae) in correlation to their components enantiomeric distribution. Parasitol Res. 2012;111:2253-63. https://doi.org/10.1007/s00436-012-3074-8
51. TennysonS, SamrajDA, JeyasundarD, ChalieuK. Larvicidal efficacy of plant oils against the dengue vector Aedes aegypti (L.) (Diptera: Culicidae). Middle-East Journal of Scientific Research. 2013;13:64-8. https://doi.org/10.5829/idosi.mejsr.2013.13.1.64107
52. VeraSS, ZambranoDF, Méndez-SánchezSC, RodríguezSanabriaF, StashenkoEE, LunaJE. Essential oils with insecticidal activity against larvae of Aedes aegypti (Diptera: Culicidae). Parasitol Res. 2014;113:2647-54. https://doi. org/10.1007/s00436-014-3917-6
53. GovindarajanM. Chemical composition and larvicidal activity of leaf essential oil from Clausena anisata (Willd.) Hook. f. ex Benth (Rutaceae) against three mosquito species. Asian Pac J Trop Med. 2010;3:874-7. https://doi.org/10.1016/S1995-7645(10)60210-6
54. GovindarajanM, SivakumarR, RajeswaryM, VeerakumarK. Mosquito larvicidal activity of timol from essential oil of Coleus aromaticus Benth. against Culex tritaeniorhynchus, Aedes albopictus, and Anopheles subpictus (Diptera: Culicidae). Parasitol Res. 2013;112:3713-21. https://doi.org/10.1007/s00436-013-3557-2
55. AliA, WangYH, KhanIA. Larvicidal and biting deterrent activity of essential oils of Curcuma longa, ar-turmerone, and curcuminoids against Aedes aegypti and Anopheles quadrimaculatus (Culicidae: Diptera). J Med Entomol. 2015;52:979-86. https://doi.org/10.1093/jme/tjv072
56. GiatropoulosA, PitarokiliD, PapaioannouF, PapachristosDP, KoliopoulosG, EmmanouelN, et al. Essential oil composition, adult repellency and larvicidal activity of eight Cupressaceae species from Greece against Aedes albopictus (Diptera: Culicidae). Parasitol Res. 2013;112:1113-1123. https://doi.org/10.1007/s00436-012-3239-5
57. ChengSS, HuangCG, ChenYJ, YuJJ, ChenWJ, ChangST. Chemical compositions and larvicidal activities of leaf essential oils from two eucalyptus species. Bioresour Technol. 2009;100:452-6. https://doi.org/10.1016/j.biortech.2008.02.038
58. LucíaA, González-AudinoP, SeccaciniE, LicastroS, ZerbaE, MasuhH. Larvicidal effect of Eucalyptus grandis essential oil and turpentine and their major components on Aedes aegypti larvae. J Am Mosq Control Assoc. 2007;23:299-303. https://doi.org/10.2987/8756-971X(2007)23[299:LEOEGE]2.0.CO;2
59. LucíaA, LicastroS, ZerbaE, MasuhH. Yield, chemical composition, and bioactivity of essential oils from 12 species of Eucalyptus on Aedes aegypti larvae. Entomol Exp Appl. 2008;129:107-14. https://doi.org/10.1111/j.15707458.2008.00757.x
60. IntirachJ, JunkumA, TuetunB, ChoochoteW, ChaithongU, JitpakdiA, et al. Chemical constituents and combined larvicidal effects of selected essential oils against Anopheles cracens (Diptera: Culicidae). Psyche. 2012;2012:1-11. https://doi.org/10.1155/2012/591616
61. RochaDK, MatoscO, NovoaMT, FigueiredoAC, DelgadoM, MoiteiroC. Larvicidal activity against Aedes aegypti of Foeniculum vulgare essential oils from Portugal and Cape Verde. Nat Prod Commun. 2015;10:677-82.
62. AcioleSD, PiccoliCF, CostaEV, Navarro-SilvaMA, MárquesFA, Sales-MaiaBH, et al. Insecticidal activity of three species of Guatteria (Annonaceae) against Aedes aegypti (Diptera: Culicidae). Revista Colombiana de Entomología. 2011;37:262-8.
63. LiuXC, LiuQY, ZhouL, LiuZL. Larvicidal activity of essential oil derived from Illicium henryi Diels (Illiciaceae) Leaf. Trop J Pharm Res. 2015;14:111-6. https://doi.org/10.4314/tjpr.v14i1.16
64. TabancaN, AvontoC, WangM, ParcherJF, AliA, DemirciB, et al. Comparative investigation of Umbellularia californica and Laurus nobilis leaf essential oils and identification of constituents active against Aedes aegypti. J Agric Food Chem. 2013;61:12283-91. https://doi.org/10.1021/jf4052682
65. SilvaWJ, DóriaGA, MaiaRT, NunesRS, CarvalhoGA, BlankAF, et al. Effects of essential oils on Aedes aegypti larvae: Alternatives to environmentally safe insecticides. Bioresource Technol. 2008;99:3251-5. https://doi.org/10.1016/j.biortech.2007.05.064
66. GleiserRM, ZygadloJA. Insecticidal properties of essential oils from Lippia turbinata and Lippia polystachya (Verbenaceae) against Culex quinquefasciatus (Diptera: Culicidae). Parasitol Res. 2007;101:1349-54. https://doi.org/10.1007/s00436-007-0647-z
67. LimaGP, de SouzaTM, de Paula FreireG, FariasDF, CunhaAP, RicardoNM, et al. Further insecticidal activities of essential oils from Lippia sidoides and Croton species against Aedes aegypti L. Parasitol Res. 2013;112:1953-8. https://doi.org/10.1007/s00436-013-3351-1
68. KoliopoulosG, PitarokiliD, KioulosE, MichaelakisA, TzakouO. Chemical composition and larvicidal evaluation of Mentha, Salvia, and Melissa essential oils against the West Nile virus mosquito Culex pipiens. Parasitol Res. 2010;107:327-35. https://doi.org/10.1007/s00436-010-1865-3
69. LimaTC, da SilvaTK, SilvaFL, Barbosa-FilhoJM, MarquesMO, SantosRL, et al. Larvicidal activity of Mentha x villosa Hudson essential oil, rotundifolone and derivatives. Chemosphere. 2014;104:37-43. https://doi.org/10.1016/j.chemosphere.2013.10.035
70. RajGA, ChandrasekaranM, KrishnamoorthyS, JayaramanM, VenkatesaluV. Phytochemical profile and larvicidal properties of seed essential oil from Nigella sativa L. (Ranunculaceae), against Aedes aegypti, Anopheles stephensi, and Culex quinquefasciatus (Diptera: Culicidae). Parasitol Res. 2015;114:3385-91. https://doi.org/10.1007/s00436-015-4563-3
71. GovindarajanM, SivakumarR, RajeswaryM, YogalakshmiK. Chemical composition and larvicidal activity of essential oil from Ocimum basilicum (L.) against Culex tritaeniorhynchus, Aedes albopictus and Anopheles subpictus (Diptera: Culicidae). Exp Parasitol. 2013;134:7-11. https://doi.org/10.1016/j.exppara.2013.01.018
72. KulkarniRR, PawarPV, JosephMP, AkulwadAK, SenA, JoshiSP. Lavandula gibsoni and Plectranthus mollis essential oils: Chemical analysis and insect control activities against Aedes aegypti, Anopheles sfttephensi and Culex quinquefasciatus. J Pest Sci. 2013;86:713-8. https://doi.org/10.1007/s10340-013-0502-1
73. PavelaR. Insecticidal properties of Pimpinella anisum essential oils against the Culex quinquefasciatus and the non-target organism Daphnia magna. J Asia-Pacific Entomol. 2014;17:287-93. https://doi.org/10.1016/j.aspen.2014.02.001
74. KoutsavitiK, GiatropoulosA, PitarokiliD, PapachristosD, MichaelakisA, TzakouO. Greek Pinus essential oils: Larvicidal activity and repellency against Aedes albopictus (Diptera: Culicidae). Parasitol Res. 2015;114:583-92. https://doi.org/10.1007/s00436-014-4220-2
75. GokulakrishnanJ, KuppusamyE, ShanmugamD, AppavuA, KaliyamoorthiK. Pupicidal and repellent activities of Pogostemon cablin essential oil chemical compounds against medically important human vector mosquitoes. Asian Pac J Trop Dis. 2013;3:26-31. https://doi.org/10.1016/S2222-1808(13)60006-7
76. MaheswaranR, IgnacimuthuS. Bioefficacy of essential oil from Polygonum hydropiper L. against mosquitoes, Anopheles stephensi and Culex quinquefasciatus. Ecotoxicol Environ Saf. 2013;97:26-31. https://doi.org/10.1016/j.ecoenv.2013.06.028
77. ContiB, LeonardiM, PistelliL, ProfetiR, OuerghemmiI, BenelliG. Larvicidal and repellent activity of essential oils from wild and cultivated Ruta chalepensis L.(Rutaceae) against Aedes albopictus Skuse (Diptera: Culicidae), an arbovirus vector. Parasitol Res. 2013;112:991-9. https://doi.org/10.1007/s00436-012-3221-2
78. LópezLAP, YaelC, CirioAT. Essential oils from Zanthoxylum fagara Wild Lime, Ruta chalepensis L. and Thymus vulgaris L.: Composition and activity against Aedes aegypti larvae. Pak J Pharm Sci. 2015;28:1911-5.
79. AliA, DemirciB, KiyanHT, BernierUR, TsikoliaM, WedgeDE, et al. Biting deterrence, repellency, and larvicidal activity of Ruta chalepensis (Sapindales: Rutaceae) essential oil and its major individual constituents against mosquitoes. J Med Entomol. 2013;50:1267-74. https://doi.org/10.1603/ME12177
80. MathewJ, ThoppilJE. Chemical composition and mosquito larvicidal activities of Salvia essential oils. Pharm Biol. 2011; 49:456-63. https://doi.org/10.3109/13880209.2010.523427
81. PavelaR. Larvicidal property of essential oils against Culex quinquefasciatus Say (Diptera: Culicidae). Ind Crops Prod. 2009;30:311-5. https://doi.org/10.1016/j.indcrop.2009.06.005
82. AguiarRW, dos SantosSF, da Silva MorgadoF, AscencioSD, de Mendonça LopesM, VianaKF, et al. Insecticidal and repellent activity of Siparuna guianensis Aubl.(Negramina) against Aedes aegypti and Culex quinquefasciatus. PloS One. 2015;10:e0116765. https://doi.org/10.1371/journal.pone.0116765
83. BarbosaJD, SilvaVB, AlvesPB, GuminaG, SantosRL, SousaDP, et al. Structure-activity relationships of eugenol derivatives against Aedes aegypti (Diptera: Culicidae) larvae. Pest Manag Sci. 2012;68:1478-83. https://doi.org/10.1002/ps.3331
84. MarquesMM, MoraisSM, VieiraÍG, VieiraMG, SilvaAR, De AlmeidaRR, et al. Larvicidal activity of Tagetes erecta against Aedes aegypti. J Am Mosq Control Assoc. 2011;27:156-8. https://doi.org/10.2987/10-6056.1
85. RuizC, CachayM, DomínguezM, VelásquezC, EspinozaG, VentosillaP, et al. Chemical composition, antioxidant and mosquito larvicidal activities of essential oils from Tagetes filifolia, Tagetes minuta and Tagetes elliptica from Perú. Planta Med. 2011;77:PE30. https://doi.org/10.1055/s0031-1282361
86. LiuXC, LiuQ, ChenXB, ZhouL, LiuZL. Larvicidal activity of the essential oil from Tetradium glabrifolium fruits and its constituents against Aedes albopictus. Pest Manag Sci. 2015;71:1582-6. https://doi.org/10.1002/ps.3964
87. TrongtokitY, RongsriyamY, KomalamisraN, ApiwathnasornC. Comparative repellency of 38 essential oils against mosquito bites. Phytother Res. 2005;19:303-9. https://doi.org/10.1002/ptr.1637
88. GillijYG, GleiserRM, ZygadloJA. Mosquito repellent activity of essential oils of aromatic plants growing in Argentina. Bioresour Technol. 2008;99:2507-15. https://doi.org/10.1016/j.biortech.2007.04.066
89. MooreSJ, HillN, RuizC, CameronMM. Field evaluation of traditionally used plant-based insect repellents and fumigants against the malaria vector Anopheles darlingi in Riberalta, Bolivian Amazon. J Med Entomol. 2007;44:62430. https://doi.org/10.1093/jmedent/44.4.624
90. de PaulaJP, Gomes-CarneiroM, PaumgarttenFJ. Chemical composition, toxicity and mosquito repellency of Ocimum selloi oil. J Ethnopharmacol. 2003;88:253-60. https://doi.org/10.1016/S0378-8741(03)00233-2
91. JaensonTG, PålssonK, Borg-KarlsonAK. Evaluation of extracts and oils of mosquito (Diptera: Culicidae) repellent plants from Sweden and Guinea-Bissau. J Med Entomol. 2006;43:113-9. https://doi.org/10.1093/jmedent/43.1.113
92. PhasomkusolsilS, SoonweraM. Comparative mosquito repellency of essential oils against Aedes aegypti (Linn.), Anopheles dirus (Peyton and Harrison) and Culex quinquefasciatus (Say). Asian Pac J Trop Biomed. 2011;1:S113-8. https://doi.org/10.1016/S2221-1691(11)60136-6
93. AmerA, MehlhornH. Repellency effect of forty-one essential oils against Aedes, Anopheles, and Culex mosquitoes. Parasitol Res. 2006;99:478-90. https://doi.org/10.1007/s00436-006-0184-1
94. WaliwitiyaR, KennedyCJ, LowenbergerCA. Larvicidal and oviposition?altering activity of monoterpenoids, transanithole and rosemary oil to the yellow fever mosquito Aedes aegypti (Diptera: Culicidae). Pest Manag Sci. 2009; 65:241-8. https://doi.org/10.1002/ps.1675
95. PavelaR. Acute toxicity and synergistic and antagonistic effects of the aromatic compounds of some essential oils against Culex quinquefasciatus Say larvae. Parasitol Res. 2015;114:3835-53. https://doi.org/10.1007/s00436015-4614-9
96. SousaRMO, RosaJS, SilvaCA, AlmeidaMTM, NovoMT, CunhaAC, et al. Larvicidal, molluscicidal and nematicidal activities of essential oils and compounds from Foeniculum vulgare. J Pest Sci. 2015;88:413-26. https://doi.org/10.1007/s10340-014-0628-9
97. PavelaR. Essential oils for the development of eco-friendly mosquito larvicides: A review. Ind Crops Prod. 2015;76:174-187. https://doi.org/10.1016/j.indcrop.2015. 06.050
98. RanaIS, RanaAS. Efficacy of essential oils of aromatic plants as larvicide for the management of filarial vector Culex quinquefasciatus Say (Diptera: Culicidae) with special reference to Foeniculum vulgare. Asian Pac J Trop Dis. 2012;2:184-9. https://doi.org/10.1016/S22221808(12)60044-9
99. SantosSR, SilvaVB, MeloMA, BarbosaJD, SantosRL, de SousaDP, et al. Toxic effects on and structuretoxicity relationships of phenylpropanoids, terpenes, and related compounds in Aedes aegypti larvae. Vector Borne Zoonotic Dis. 2010;10:1049-54. https://doi.org/10.1089/vbz.2009.0158
100. GokulakrishnanJ, KuppusamyE, ShanmugamD, AppavuA, KaliyamoorthiK. Pupicidal and repellent activities of Pogostemon cablin essential oil chemical compounds against medically important human vector mosquitoes. Asian Pac J Trop Dis. 2013;3:26-31. https://doi.org/10.1016/S2222-1808(13)60006-7
101. AliA, TabancaN, OzekG, OzekT, AytacZ, BernierUR, et al. Essential oils of Echinophora lamondiana (apiales: Umbelliferae): A relationship between chemical profile and biting deterrence and larvicidal activity against mosquitoes (Diptera: Culicidae). J Med Entomol. 2015;52:93-100.https://doi.org/10.1093/jme/tju014
102. DóriaGA, SilvaWJ, CarvalhoGA, AlvesPB, CavalcantiSC. A study of the larvicidal activity of two Croton species from northeastern Brazil against Aedes aegypti. Pharm Biol. 2010;48:615-20. https://doi.org/10. 3109/13880200903222952
103. RadwanMA, El-ZemitySR, MohamedSA, SherbySM. Larvicidal activity of some essential oils, monoterpenoids and their corresponding N-metil carbamate derivatives against Culex pipiens (Diptera: Culicidae). Int J Trop Ins Sci. 2008;28:61-8. https://doi.org/10.1017/S1742758408962366
104. ChengSS, ChuaMT, ChangEH, HuangCG, ChenWJ, ChangST. Variations in insecticidal activity and chemical compositions of leaf essential oils from Cryptomeria japonica at different ages. Bioresource Technol. 2009;100:465-70. https://doi.org/10.1016/j.biortech.2007.11.060
105. LucíaA, ZerbaE, MasuhH. Knockdown and larvicidal activity of six monoterpenes against Aedes aegypti (Diptera: Culicidae) and their structure-activity relationships. Parasitol Res. 2013;112:4267-72. https://doi.org/10.1007/s00436-013-3618-6
106. Perumalsamy H, Kim NJ, Ahn, AJ. Larvicidal activity of compounds isolated from Asarum heterotropoides against Culex pipiens pallens, Aedes aegypti, and Ochlerotatus togoi (Diptera: Culicidae). J Med Entomol. 2009;46:1420-3. https://doi.org/10.1603/033.046.0624
107. LiuZL, HeQ, ChuSS, WangCF, DuSS, DengZW. Essential oil composition and larvicidal activity of Saussurea lappa roots against the mosquito Aedes albopictus (Diptera: Culicidae). Parasitol Res. 2012;110:2125-30. https://doi.org/10.1007/s00436-011-2738-0
108. KaufmanPE, MannRS, ButlerJF. Evaluation of semiochemical toxicity to Aedes aegypti, Ae. albopictus and Anopheles quadrimaculatus (Diptera: Culicidae). Pest Manag Sci. 2010;66:497-504. https://doi.org/10.1002/ps.1899
109. LiuXC, DongHW, ZhouL, DuSS, LiuZL. Essential oil composition and larvicidal activity of Toddalia asiatica roots against the mosquito Aedes albopictus (Diptera: Culicidae). Parasitol Res. 2013;112:1197-203. https://doi.org/10.1007/s00436-012-3251-9
110. AliA, MurphyCC, DemirciB, WedgeDE, SampsonBJ, KhanIA, et al. Insecticidal and biting deterrent activity of rose-scented geranium (Pelargonium spp.) essential oils and individual compounds against Stephanitis pyrioides and Aedes aegypti. Pest Manag Sci. 2013;69:1385-92. https://doi.org/10.1002/ps.3518
111. LahlouM. Methods to study the phytochemistry and bioactivity of essential oils. Phytotherapy Res. 2004;18:435-48. https://doi.org/10.1002/ptr.1465
112. ShaalanEAS, CanyonD, YounesMW, Abdel-WahabH, MansourAH. A review of botanical phytochemicals with mosquitocidal potential. Environ Int. 2005;31:1149-66. https://doi.org/10.1016/j.envint.2005.03.003
113. PavelaR. Acute and synergistic effects of some monoterpenoid essential oil compounds on the house fly (Musca domestica L.). J Essent Oil Bear Pl. 2008;11:451-9. https://doi.org/10.1080/0972060X.2008.10643653
114. KoulO, SinghR, KaurB, KandaD. Comparative study on the behavioral response and acute toxicity of some essential oil compounds and their binary mixtures to larvae of Helicoverpa armigera, Spodoptera litura and Chilo partellus. Ind Crops Prod. 2013;49:428-36. https://doi.org/10.1016/j.indcrop.2013.05.032
115. HummelbrunnerLA, IsmanMB. Acute, sublethal, antifeedant, and synergistic effects of monoterpenoid essential oil compounds on the tobacco cutworm, Spodoptera litura (Lep., Noctuidae). J Agricul Food Chem. 2001;49:715-20. https://doi.org/10.1021/jf000749t
116. LiuCH, MishraAK, TanRX, TangC, YangH, ShenYF. Repellent and insecticidal activities of essential oils from Artemisia princeps and Cinnamomum alcanfora and their effect on seed germination of wheat and broad bean. Bioresour Technol. 2006;97:1969-73. https://doi.org/10.1016/j.biortech.2005.09.002
117. KostyukovskyM, RafaeliA, GileadiC, DemchenkoN, ShaayaE. Activation of octopaminergic receptors by essential oil constituents isolated from aromatic plants: Possible mode of action against insect pests. Pest Manag Sci. 2002;58:1101-6. https://doi.org/10.1002/ps.548
118. WangZ, KimJR, WangM, ShuS, AhnYJ. Larvicidal activity of Cnidium monnieri fruit coumarins and structurally related compounds against insecticide-susceptible and insecticide-resistant Culex pipiens pallens and Aedes aegypti. Pest Manag Sci. 2012;68:1041-7. https://doi.org/10.1002/ps.3265
119. ScottiL, ScottiMT, SilvaVB, SantosSR, CavalcantiSC, MendoncaFJJr. Chemometric studies on potential larvicidal compounds against Aedes aegypti. Med Chem. 2014;10:201-10. https://doi.org/10.2174/15734064113099990005
120. LeeS, PetersonCJ, CoatsJR. Fumigation toxicity of monoterpenoids to several stored product insects. J Stored Prod Res. 2003;39:77-85. https://doi.org/10.1016/S0022-474X(02)00020-6
121. GarcíaM, DonadelOJ, ArdanazCE, TonnCE, SosaME. Toxic and repellent effects of Baccharis salicifolia essential oil on Tribolium castaneum. Pest Manag Sci. 2005;61:612-8. https://doi.org/10.1002/ps.1028
122. LópezÓ, Fernández-BolañosJG, GilMV. New trends in pest control: The search for greener insecticides. Green Chem. 2005;7:431-42. https://doi.org/10.1039/B500733J
123. SantosSR, MeloMA, CardosoAV, SantosRL, de SousaDP, CavalcantiSC. Structure-activity relationships of larvicidal monoterpenes and derivatives against Aedes aegypti Linn. Chemosphere. 2011;84:150-3. https://doi.org/10.1016/j.chemosphere.2011.02.018
124. AbdelgaleilSA, MohamedMI, BadawyME, El-aramiSA. Fumigant and contact toxicities of monoterpenes to Sitophilus oryzae (L.) and Tribolium castaneum (Herbst) and their inhibitory effects on acetylcholinesterase activityJ Chem Ecol. 2009;35:518-25. https://doi.org/10.1007/s10886-009-9635-3
125. Andrade-OchoaS, Nevárez-MoorillónGV, SánchezTorresLE, Villanueva-GarcíaM, Sánchez-RamírezBE, Rodríguez-ValdezLM, et al. Quantitative structureactivity relationship of molecules constituent of different essential oils with antimycobacterial activity against Mycobacterium tuberculosis and Mycobacterium bovis. BMC Comp Alt Med. 2015;15:332. https://doi.org/10.1186/s12906-015-0858-2
126. LomonacoD, SantiagoGM, FerreiraYS, ArriagaÂM, MazzettoSE, MeleG, et al. Study of technical CNSL and its main components as new green larvicides. Green Chem. 2009;11:31-3. https://doi.org/10.1039/B811504D
127. WangZ, SongJ, ChenJ, SongZ, ShangS, JiangZ, et al. QSAR study of mosquito repellents from terpenoid with a six-member-ring. Bioorg Med Chem Lett. 2008;18:2854-9. https://doi.org/10.1016/j.bmcl.2008.03.091
128. BegumNA, RoyN, LaskarRA, RoyK. Mosquito larvicidal studies of some chalcone analogues and their derived products: Structure-activity relationship analysis. Med Chem Res. 2011;20:184-91. https://doi.org/10.1007/s00044-010-9305-6
129. MaD, BhattacharjeeAK, GuptaRK, KarleJM. Predicting mosquito repellent potency of N, N-diethyl-m-toluamide (DEET) analogs from molecular electronic properties. Am J Trop Med Hyg. 1999;60:1-6.
130. PaluchG, GrodnitzkyJ, BartholomayL, CoatsJ. Quantitative structure-activity relationship of botanical sesquiterpenes: Spatial and contact repellency to the yellow fever mosquito, Aedes aegypti. J Agric Food Chem. 2009;57:7618-25. https://doi.org/10.1021/jf900964e
131. RattanRS. Mechanism of action of insecticidal secondary metabolites of plant origin. Crop Protection. 2010;29:91320. https://doi.org/10.1016/j.cropro.2010.05.008
132. IsmanMB. Plant essential oils for pest and disease management. Crop Protection. 2000;19:603-8. https://doi.org/10.1016/j.cropro.2010.05.008
133. ZarradK, HamoudaAB, ChaiebI, LaarifA, JemâaJM. Chemical composition, fumigant and anti-acetylcholinesterase activity of the Tunisian Citrus aurantium L. essential oils. Ind Crops Prod. 2015;76:121-7. https://doi.org/10.1016/j.indcrop.2015.06.039
134. HoughtonPJ, RenY, HowesMJ. Acetylcholinesterase inhibitors from plants and fungi. Natural Prod Rep. 2006;23:181-99. https://doi.org/10.1039/B508966M
135. SNJyotshna, SrivastavaN, SinghB, ChandaD, ShankerK. Chemical composition and acetylcholinesterase inhibitory activity of Artemisia maderaspatana essential oil. Pharm Biol. 2015;53:1677-83. https://doi.org/10.3109/13880209.2014.1001405
136. EnanEE. Insecticidal activity of essential oils: Octopaminergic sites of action. Comp Biochem Physiol C Toxicol Pharmacol. 2001;130:325e337. https://doi.org/10.1016/S1532-0456(01)00255-1
137. CoatsR, KarrLL, DrewesCD. Toxicity and neurotoxic effects of monoterpenoids in insects and earthworms. En: HedinP, editor. Natural occurring pest bioregulators. Washington, D.C.: American Chemical Society; 1991. p.305-16.
138. RyanMF, ByrneO. Plant-insect coevolution and inhibition of acetylcholinesterase. J Chem Ecol.1988;14:1965-75. https://doi.org/10.1007/BF01013489
139. PraveenaA, SanjayanKP. Inhibition of acetylcholinesterase in three insects of economic importance by linalol, a monoterpene phytochemical. En: AmbroseDP, editor. Insect pest management, a current scenario, entomology research unit. Palayamkottai, India: St. Xavier's College; 2011. p. 340-5.
140. FelipeCF, FonsêcaKS, dos Reis BarbosaAL, BezerraJN, NetoMA, de França FontelesMM, et al. Alterations in behavior and memory induced by the essential oil of Zingiber officinale Roscoe (ginger) in mice are cholinergic dependent. J Med Plants Res. 2008;2:163-70.
141. YeomHJ, KangJS, KimGH, ParkIK. Insecticidal and acetylcholine esterase inhibition activity of Apiaceae plant essential oils and their constituents against adults of German cockroach (Blattella germanica). J Agric Food Chem. 2012;60:7194-203. https://doi.org/10.1021/jf505927n
142. KimSW, KangJ, ParkIK. Fumigant toxicity of Apiaceae essential oils and their constituents against Sitophilus oryzae and their acetylcholinesterase inhibitory activity. J Asia-Pacific Entomol. 2013;16:443-8. https://doi.org/10. 1016/j.aspen.2013.07.002
143. SeoSM, JungCS, KangJ, LeeHR, KimSW, HyunJ, et al. Larvicidal and acetylcholine esterase inhibitory activity of apiaceae plant essential oils and their constituents against Aedes albopictus, and formulation development. J Agric Food Chem. 2015;63:9977-86. https://doi.org/10.1021/acs.jafc.5b03586
144. YeomHJ, JungCS, KangJ, KimJ, LeeJH, KimDS, et al.)Insecticidal and acetylcholine esterase inhibition activity of asteraceae plant essential oils and their constituents against adults of the German cockroach (Blattella germanica. J Agric Food Chem. 2015;63:2241-8. https://doi.org/10.1021/jf505927n
145. KhanikorB, ParidaP, YadavRNS, BoraD. Comparative mode of action of some terpene compounds against octopamine receptor and acetyl cholinesterase of mosquito and human system by the help of homology modeling and docking studies. J Appl Pharm Sci. 2013;3:6-12. https://doi.org/10.7324/JAPS.2013.30202
146. UnnithanAR. In vitro sensitivity assay of Lantana camara against Aedes agypti with supplementary facts from GC MS and in silico analysis. J Biomed Pharm Sci. 2015;4:5-9.
147. EnanEE. Molecular and pharmacological analysis of an octopamina receptor from American cockroach and fruit fly in response to plant essential oils. Arch Insect Biochem Physiol. 2005;59:161-71. https://doi.org/10.1002/arch.20076
148. EnanEE. Molecular response of Drosophila melanogaster tyramine receptor cascade to plant essential oils. Insect Biochem Mol Biol. 2005;35:309-21. https://doi.org/10.1016/j.ibmb.2004.12.007
149. PriestleyCM, WilliamsonEM, WaffordKA, SattelleDB. Thymol, a constituent of thyme essential oil, is a positive allosteric modulator of human GABA A receptors and a homo-oligomeric GABA receptor from Drosophila melanogaster. Br J Pharmacol. 2003;140:1363-72. https://doi.org/10.1038/sj.bjp.0705542
150. BloomquistJR, BoinaDR, ChowE, CarlierPR, ReinaM, González-ColomaA. Mode of action of the plantderived silphinenes on insect and mammalian GABA A receptor/chloride channel complex. Pest Biochem Physiol. 2008;91:17-23. https://doi.org/10.1016/j.pestbp.2007.12.002
151. HöldKM, SirisomaNS, IkedaT, NarahashiT, CasidaJE. alfa Thujone (the active component of absinthe): gammaAminobutyric acid type A receptor modulation and metabolic detoxification. Proc Natl Acad Sci. 2000;97:382631.https://doi.org/10.1073/pnas.070042397
152. KumarPS, ChezhianA, RajaPS, SathiyapriyaJ. Computational selections of terpenes present in the plant Calotropis gigantea as mosquito larvicides by blocking the sterol carrying protein, AeSCP-2. Bangladesh J Pharmacol. 2012;7:1-5. https://doi.org/10.3329/bjp.v7i1.8414
Notas de autor
Correspondencia: Sergio Andrade-Ochoa, Escuela Nacional de Ciencias Biológicas, Instituto Politécnico Nacional, Prolongación de Carpio y Plan de Ayala S/N, Colonia Santo Tomás 11340, Ciudad de México, México Teléfono: (52) (614) 182 1518 s.andrade.rat@gmail.com