Comunicación breve
Caracterización molecular de enterobacterias multirresistentes en dos departamentos de la selva peruana
Molecular characterization of multiresistant enterobacteria in two departments of the Peruvian jungle
Caracterización molecular de enterobacterias multirresistentes en dos departamentos de la selva peruana
Biomédica, vol. 41, núm. 2, Supl., pp. 180-187, 2021
Instituto Nacional de Salud
Recepción: 15 Julio 2021
Aprobación: 03 Agosto 2021
Publicación: 03 Agosto 2021
Resumen
Introducción.: La aparición de enterobacterias multirresistentes y productoras de betalactamasas de espectro extendido (BLEE) en pacientes de consulta externa con infecciones urinarias, representa un problema de salud pública en Perú.
Objetivos.: Caracterizar molecularmente enterobacterias multirresistentes aisladas de pacientes con diagnóstico de infección urinaria y procedentes de dos departamentos de la selva peruana.
Materiales y métodos.: Se hizo un estudio descriptivo, observacional y retrospectivo de 61 aislamientos de urocultivo procedentes de la selva peruana durante 2017 y 2018. Los perfiles de resistencia se identificaron utilizando el sistema automatizado MicroScan™ y para la detección de los genes blaTEM , blaCTX-M , blaSHV se empleó una reacción en cadena de la polimerasa (PCR) convencional.
Resultados.: Las enterobacterias positivas para BLEE más frecuentes por departamento fueron Escherichia coli en Madre de Dios (25%, 10/40) y Ucayali (76,2%, 16/21). En ambos departamentos, el gen blaCTX-M fue el más frecuente (25/61; 41), seguido por blaTEM (15/61; 24,6%) y blaSHV (10/61; 16,4%). En el perfil de sensibilidad antimicrobiana, se detectó 72,6% de resistencia contra ampicilina, 82,3 % contra cefalotina y 88,7% contra nitrofurantoína.
Conclusiones.: El porcentaje de cepas de enterobacterias multirresistentes productoras de BLEE en ambos departamentos fue del 57,4% y el gen bla CTX-M fue el más frecuente.
Palabras clave: Enterobacteriaceae+ farmacorresistencia microbiana+ resistencia betalactámica+ genes.
Abstract
Introduction.: The emergence of multiresistant enterobacteria producing extended- spectrum beta-lactamase (ESBL) in outpatients with urinary tract infections represents a public health problem in Perú.
Objectives.: To characterize multiresistant enterobacteria isolated from patients diagnosed with urinary tract infection in two Peruvian jungle departments using molecular techniques.
Materials and methods.: We conducted a descriptive, observational, and retrospective study of 61 urine culture isolates from two departments in the Peruvian jungle during 20172018. Resistance profiles were identified using the MicroScan™ automated system and a conventional polymerase chain reaction (PCR) was used for the detection of blaCTX-M , blaTEM and blaSHV genes..
Results.: The most common positive ESBL enterobacteria for each department were Escherichia coli in Madre de Dios (10/40; 25%) and Ucayali (16/21; 76.2%). Gene blaCTX-M was the most prevalent in both departments (25/61; 41%), followed by blaTEM (15/61; 24.6%), and blaSHV (10/61; 16.4%). As for the antimicrobial susceptibility profile, we detected resistance levels of 72.6% for ampicillin, 82.3% for cephalothin, and 88.7% for nitrofurantoin.
Conclusions.: BLEE-producing multi-resistant enterobacteria strains in both departments were 57.4% and blaCTX-M was the most common gene.
Keywords: Enterobacteriaceae, drug resistance microbial, beta-lactam resistance, genes.
La resistencia a los antibióticos es hoy una de las mayores amenazas para la salud mundial 1. Las infecciones de las vías urinarias se encuentran entre las infecciones bacterianas más comunes en todo el mundo y su tratamiento constituye un reto cada vez mayor, a medida que aumentan las tasas de resistencia a los antibióticos estándar 2,3.
Las betalactamasas son enzimas bacterianas capaces de hidrolizar los antibióticos betalactámicos, inhibiendo su mecanismo de acción y haciéndolos inefectivos 4,5. Las enzimas betalactamasas de espectro extendido (BLEE) están entre las de mayor relevancia clínica e incluyen tres tipos principales: TEM, SHV y CTX-M. Hasta la fecha, se han reportado más de 400 tipos de estas enzimas y la CTX-M es la que más frecuentemente se reporta en todo el mundo 6.
Según los datos de la Organización Panamericana de Salud (OPS) recolectados por la Red Latinoamericana de Vigilancia de la Resistencia a los Antimicrobianos (ReLAVRA), en Latinoamérica, la resistencia a los betalactámicos ha demostrado ser más grave que en otras regiones del mundo 7,8,9. En Perú, por ser un país megadiverso, es necesario hacer estudios por regiones (costa, sierra y selva), porque los factores ambientales y socioeconómicos intervienen en el perfil de sensibilidad de cada agente patógeno 10. En la región de la selva, es necesario controlar la propagación de las bacterias multirresistentes y actualmente no se hace vigilancia epidemiológica molecular que brinde datos confiables para mitigar el problema, debido a la falta de insumos, infraestructura y recursos humanos en los laboratorios.
Los estudios se han centrado hasta ahora en la región de la costa, y es necesario hacer los análisis genotípicos de los agentes patógenos en otros establecimientos de salud de la sierra y la selva, para establecer la prevalencia y el alcance de la resistencia bacteriana, cerrar la brecha de información y proporcionar una base que oriente el tratamiento empírico 11.
En ese contexto, el objetivo del estudio fue caracterizar molecularmente enterobacterias multirresistentes aisladas de pacientes con diagnóstico de infección urinaria procedentes de dos departamentos de la selva peruana.
Materiales y métodos
Pacientes y material biológico
Se hizo un estudio descriptivo, observacional y retrospectivo en aislamientos bacterianos de muestras de orina procedentes de los hospitales públicos regionales de nivel II de Santa Rosa y Pucallpa, en los departamentos de Madre de Dios y Ucayali, respectivamente. Se analizaron 61 aislamientos de enterobacterias exclusivamente de pacientes adultos (mayores de 18 años) con diagnóstico de infección urinaria, atendidos en consulta externa durante 2017 y 2018 y procedentes de la región de selva. Se excluyeron las cepas aisladas que no fueran enterobacterias.
Identificación bacteriana
La identificación y el perfil de sensibilidad se determinaron seleccionando las colonias en agar MacConkey mediante el uso del sistema automatizado MicroScan™ (AutoScan-4) y de paneles para bacterias Gram negativas (Dade MicroScan™), siguiendo las indicaciones del manual estandarizado 12. Se utilizaron 26 antimicrobianos para cada cepa y, con los valores de la concentración inhibitoria mínima (CIM), se interpretó el perfil de resistencia antibiótica según los puntos de corte recomendados por el Clinical and Laboratory Standards Institute 2020 13. La presencia de BLEE se detectó mediante la lectura de los paneles MicroScan Type 66 (SMN:1711680) con el programa “LabPro Command Center”, los cuales constituyen un método confirmatorio de detección para las bacterias de tipo BLEE que puede personalizarse. Este método de detección utiliza la CMI de los antibióticos ceftazidima, aztreonam, cefotaxima, cefpodoxima y ceftriaxona.
Para el control de calidad de las pruebas de sensibilidad, se usaron la cepa Klebsiella pneumoniae ATCC 700603 como control positivo para la producción de BLEE y, la de Escherichia coli ATCC 25922, como control negativo.
Extracción de ADN genómico
En la extracción del ADN genómico de las cepas de enterobacterias, se utilizó el método basado en columnas de silicagel del estuche innuPREP Bacteria DNA™ (Analytikjena, Alemania), con el cual fue necesario que el crecimiento bacteriano se encontrara en la fase logarítmica. El ADN aislado se almacenó a -20 °C hasta la amplificación de cada gen por PCR convencional.
Reacción en cadena de la polimerasa
La amplificación mediante PCR se utilizó para detectar los genes BLEE (blaCTX-M , blaTEM , blaSHV ); los iniciadores empleados fueron los descritos por Kiratisin, et al. 14, y Arce, et al. 15 (cuadro 1).
La mezcla de la reacción se ajustó a una concentración final de 25 μl según las condiciones descritas en el protocolo. La mezcla maestra fue la siguiente: 10 μl de solución tampón para PCR 10x incluido Mg (abm), 1 μl de dNTP (abm), 0,5 μl de Primer-F, 0,5 μl de Primer-R (Macrogen, South Korea), 17,3 μl de agua ultrapura (Invitrogen), 0,2 μl de Taq ADN polimerasa (abm) y 2,5 μl de ADN genómico previamente extraído de cada cepa bacteriana.
La PCR se llevó a cabo en un termociclador T100TM (Thermal Cycler, BioRad, Estados Unidos) bajo las siguientes condiciones: predesnaturalización a 94 °C por 7 minutos, desnaturalización a 94 °C por 50 s, hibridación a 52-55 °C por 1 minuto, extensión a 72 °C por 60 s repetidos en 35 ciclos, y un ciclo de extensión final de 5 minutos a 72 °C y un tiempo infinito a 8 °C.

F: Forward; R: Reverse; CTX-M: cefotaximasas; TEM: temoniera; SHV: sulfhidrilo variable; pb: pares de bases; bla: genes de resistencia a betalactamasas
Electroforesis
El producto de amplificación se analizó por electroforesis en gel de agarosa al 1,5 % (Cleaver Scientific), usando como solución tampón de carga y revelador el Safe-GreenTM (abm). Para verificar el tamaño del ADN amplificado, se empleó el marcador de peso molecular de 100 pb (opti DNA Marker - abm™). La corrida electroforética se llevó a 120 V por 40 minutos en el sistema de electroforesis con documentación runSTATION complete (Cleaver Scientific, United Kindom).
Análisis estadístico
La base de datos se analizó con el programa Stata 15.0. Las medidas de frecuencia se presentan como frecuencias relativas (porcentajes). El gráfico de barras se elaboró con el programa Microsoft Excel. 2019. Por ser un estudio observacional, no requirió de variables dependientes e independientes.
Consideraciones éticas
Los dos establecimientos de salud aprobaron el protocolo de estudio. Se garantizó la confidencialidad de los datos de los pacientes. El estudio fue evaluado y aprobado por el Comité de Ética de la Universidad Peruana Unión (N2019-CEUPeU-0001).
Resultados
De los 61 pacientes que acudieron a consulta externa, el 65,6% (40/61) provenía del departamento de Madre de Dios (Hospital Regional de Santa Rosa) y el 34,4% (21/61) del departamento de Ucayali (Hospital Regional de Pucallpa). El 57,4% (35/61) resultó ser positivo para BLEE, y la edad media fue de 41 años. Las enterobacterias identificadas como positivas para BLEE fueron: E. coli con 42,6% (26/61), K. pneumoniae con 8,2% (5/61), Enterobacter cloacae con 1,6 (1/61), Acinetobacter baumannii con 1,6 % (1/61), Klebsiella oxytoca con 1,6% (1/61), y Enterobacter aerogenes con 1,6 % (1/61) (cuadro 2).
El gen más frecuente en los aislamientos fue el blaCTX-M con 41 % (25/61) seguido por el blaTEM con 24,6 % (15/61) y el blaSHV con el 16,4 % (10/61). En el departamento de Madre de Dios, los genes detectados en E. coli fueron blaCTX-M (n=6; 15 %), blaTEM (n=8; 20 %) y blaSHV (n=4; 10 %) y en K. pneumoniae los genes blaCTX-M (n=2; 5 %), blaTEM (n=2; 5 %) y blaSHV (n=4, 10 %). En el departamento de Ucayali los genes detectados en E. coli fueron blaCTX-M (n=16, 76,2 %), blaTEM (n=2, 9,5 %) y blaSHV (n=4, 10 %), en tanto que en K. pneumoniae no se detectó ninguno de estos (cuadro 3).
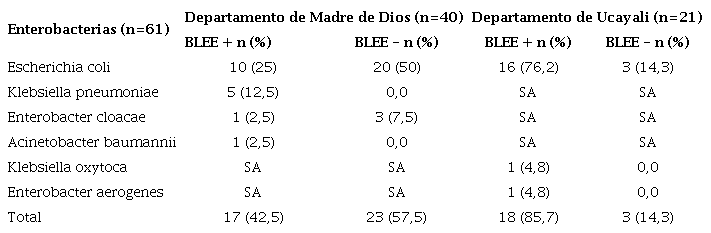
BLEE: betalactamasas de espectro extendido; SA: sin aislamiento bacteriano
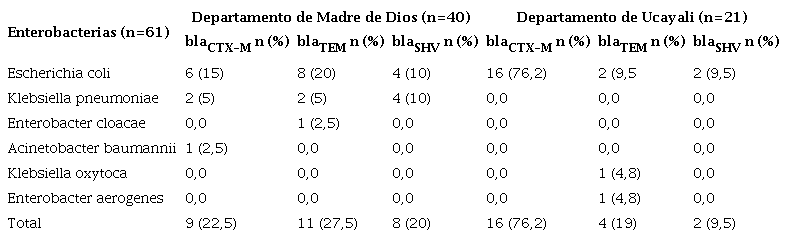
Genes de resistencia a betalactamasas: blaCTX-M,blaTEM y blaSHV
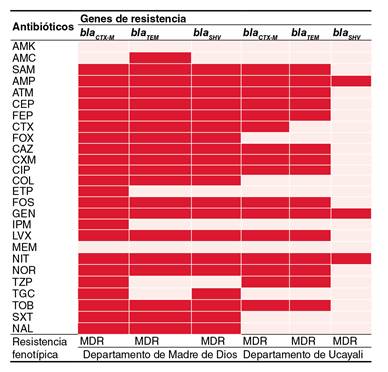
Figura 1
Perfil de resistencia genotípica y genes de resistencia a betalactamasas (BLEE) en enterobacterias de dos hospitales de la selva peruana
AMK: amikacina; AMC: amoxicilina con ácido clavulánico; SAM: ampicilina con sulbactam; AMP: ampicilina; ATM: aztreonam; CF: cefalotina; FEP: cefepima; CTX: cefotaxima; FOX: cefoxitina; CAZ: ceftazidima; CXM: cefuroxima; CIP: ciprofloxacina; COL: colistina; ETP: ertapenem; FOS: fosfomicina; GEN: gentamicina; IPM: imipenem; LVX: levofloxacina; MEM: meropenem; NIT: nitrofurantoína; NOR: norfloxacina; TZP: piperacilina con tazobactam; TGC: tigeciclina; TOB: tobramicina; SXT: trimetoprim sulfametoxazol; NAL: ácido nalidíxico; MDR: multirresistencia (resistente, por lo menos, a uno de dos o tres clases de antibióticos)
Para analizar la resistencia fenotípica con base en los genes blaCTX-M , blaTEM y blaSHV , se evaluaron todos los aislamientos bacterianos positivos para BLEE y se observó, por lo menos, la expresión de uno de los genes en cada aislamiento, además, se evidenció también que otros aislamientos codificaron dos o más genes de resistencia a betalactamasas siendo estos considerados multirresistentes, como se muestra en la figura 1. En el departamento de Madre de Dios y Ucayali, se observó multirresistencia a la mayoría de antibióticos, excepto frente a amikacina (AMK) y meropenem (MEM) como es el caso de Ucayali.
Se detectaron altos porcentajes de resistencia a ampicilina (72,6%), aztreonam (51,6%), cefalotina (82,3%), cefotaxima (54,8%), cefuroxima (51,6%), ciproflaxina (50%), nitrofurantoína (88,7%), norfloxacina (54,8%) y ácido nalidíxico (57,4%). No se detectaron aislamientos resistentes a amikacina, imipenem, meropenem o tigeciclina (figura 2).
Discusión
El propósito del estudio fue determinar la aparición de enterobacterias productoras de BLEE en los pacientes de consulta externa que acudieron a los hospitales de los departamentos de Madre de Dios y Ucayali. En el 57,4% de los aislamientos, las enterobacterias fueron productoras de BLEE, sobre todo E. coli y K. pneumoniae, lo que coincide con lo reportado por Olarte, et al. 9, y Arce, et al. 15. Morejón 16 señala que no solo E. coli y K. pneumoniae pueden ser productoras de BLEE, lo que concuerda con nuestro reporte, en el que se identificaron otras especies, como E. cloacae, A. baumannii, K. oxytoca, y E. aerogenes, las cuales, además, representaron el 11,4% de los aislamientos positivos para BLEE.
Según García, et al. 17, es importante resaltar la amplia distribución de los genes responsables de la resistencia a antibióticos betalactámicos en las distintas enterobacterias, así como la presencia simultánea de varios genes. En cuanto a los aislamientos, la mayoría de los estudios muestra un predominio de BLEE de tipo CTX-M en E. coli. En el presente estudio, el 36,1% de las cepas de E. coli expresó el gen blaCTX-M y el 16,3% el blaTEM , en tanto que el 3,3% de K. pneumoniae expresó los genes blaCTX-M y blaTEM ; además, se registraron los genes blaSHV en el 9,9% de E. coli y el 6,6% de K. pneumoniae, así como la coexistencia de los tres genes: blaCTX-M , blaTEM y blaSHV en el 4,9% de E. coli. En su estudio Galván, et al. 18, reportaron una frecuencia de 55 % del gen blaCTX-M en y la coexistencia de blaCTX-M y blaTEM en 24% de los aislamientos de E. coli en orina. Por otro lado, nuestros resultados difieren de lo reportado por Castro, et al. 19 en su estudio en E. coli productoras de BLEE aisladas de urocultivos de pacientes de la comunidad de Chilpancingo, México, en los que registraron un 95% de blaTEM , el más frecuente, seguido por blaCTX-M en el 50% y blaSHV en el 5,5%.
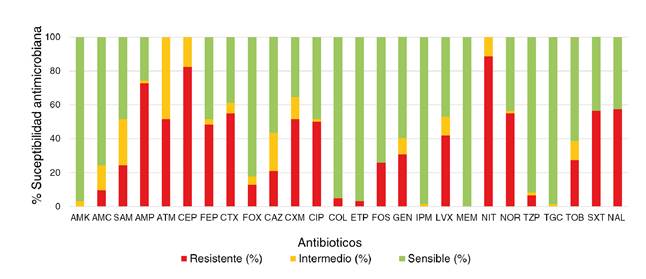
Figura 2
Porcentaje de sensibilidad antimicrobiana
AMK: amikacina; AMC: amoxicilina con ácido clavulánico; SAM: ampicilina con sulbactam; AMP: ampicilina; ATM: aztreonam; CF: cefalotina; FEP: cefepima; CTX: cefotaxima; FOX: cefoxitina; CAZ: ceftazidima; CXM: cefuroxima; CIP: ciprofloxacina; COL: colistina; ETP: ertapenem; FOS: fosfomicina; GEN: gentamicina; IPM: imipenem; LVX: levofloxacina; MEM: meropenem; NIT: nitrofurantoína; NOR: norfloxacina; TZP: piperacilina con tazobactam; TGC: tigeciclina; TOB: tobramicina; SXT: trimetoprim sulfametoxazol; NAL: ácido nalidíxico
En cuanto a la frecuencia de los genes de resistencia a betalactamasas detectados en cada departamento, el gen blaTEM representó el 20% en Madre de Dios y, el blaCTX-M , el 76,2% en Ucayali. Tales registros concuerdan con lo reportado por García, et al. 17, en relación con la detección del gen blaCTX-M en aislamientos productores de BLEE, lo cual explica suficientemente el fenotipo resistente. En el presente estudio, en el 41% de los aislamientos analizados la enzima CTX-M fue la responsable del patrón de multirresistencia, independientemente de la presencia de las enzimas de los tipos TEM y SHV, cuyos genes también fueron detectados; este porcentaje concuerda con estudios realizados en cepas de E. coli comunitarias a nivel mundial, con reportes de 40 a 70% de BLEE de tipo CTX-M 20.
Morejón 16 ha señalado que la cefepima puede ser efectiva frente a muchas cepas de BLEE, particularmente las SHV. Suarez, et al. 21, mencionan que la nitrofurantoína es la mejor opción en las infecciones urinarias de origen comunitario producidas por E. coli. En este sentido nuestro reporte difirió, ya que la prueba de sensibilidad antimicrobiana evidenció que la mayoría de las enterobacterias positivas para BLEE presentaron multirresistencia, siendo el aztreonan, la cefepima y la nitrofurantoína los antibióticos más sensibles, lo cual es una razón suficiente para abogar por el uso racional de los antimicrobianos para atenuar la velocidad del incremento o aparición de nuevas multirresistencias.
En conclusión, los resultados del estudio en los departamentos de la selva peruana señalan que la frecuencia de enterobacterias multirresistentes productoras de BLEE fue de 57,4% y que el gen blaCTX-M fue el más frecuente. Este reporte, basado en la caracterización molecular, puede contribuir a ofrecer el tratamiento antimicrobiano correcto y, además, tiene importancia epidemiológica, ya que aporta información molecular sobre la resistencia bacteriana en la comunidad
Agradecimientos
A la Escuela Profesional de Medicina Humana de la Facultad de Ciencias de la Salud de la Universidad Peruana Unión
Referencias
Organización Mundial de la Salud. Resistencia a los antibióticos 2021. Fecha de consulta: 3 de mayo del 2021. Disponible en: https://bit.ly/3h0V2Ch
Yábar MN, Curi-Pesantes B, Torres CA, Calderón-Anyosa R, Riveros M, Ochoa TJ. Multiresistance and factors associated with the presence of extended-spectrum betalactamases in Escherichia coli strains isolated from urine culture. Rev Perú Med Exp Salud Pública. 2017;34:660-5. https://doi.org/10.17843/rpmesp.2017.344.2922
Sbiti M, Lahmadi K, Louzi L. Profil épidémiologique des entérobactéries uropathogènes productrices de bêta-lactamases à spectre élargi. Pan Afr Med J. 2017;28:29. https://doi.org/10.11604/pamj.201728.29.11402
Rada AM, Hernández GC, Restrepo E, Villegas MV. Distribución y caracterización molecular de betalactamasas en bacterias Gram negativas en Colombia, 2001-2016. Biomédica. 2019;39:199-220. https://doi.org/10.7705/biomedica.v39i3.4351
Díaz MJ, Amar PW, Angulo LM, BS. Prevalencia de Escherichia coli productor de betalactamasas de espectro extendido (BLEE) y otras resistencias en urocultivos en un hospital general de Ica, Perú. Revista Médica Panacea. 2015;5:20-4. https://doi.org/10.35563/rmp.v5i1.68
Marcos-Carbajal P, Salvatierra G, Yareta J, Pino J, Vásquez N, Díaz P, et al. Caracterización microbiológica y molecular de la resistencia antimicrobiana de Escherichia coli uropatógenas de hospitales públicos peruanos. Rev Peru Med Exp Salud Pública. 2021;38:119-23. https://doi.org/10.17843/rpmesp.2021.381.6182
Red Latinoamericana de Vigilancia de la Resistencia a los Antimicrobianos (ReLAVRA). Magnitud y tendencias de la resistencia a los antimicrobianos en Latinoamérica. RELAVRA 2014, 2015, 2016. Fecha de consulta: 3 de mayo del 2021. Disponible en: https://bit.ly/2R4PqfT
Mostajo AG, Díaz CA, Morón PR. Frecuencia de infección del tracto urinario intrahospitalaria por enterobacterias productoras de betalactamasas de espectro extendido y factores asociados en un hospital nacional. Revista de la Sociedad Peruana de Medicina Interna. 2015;28:113-20.
Olarte LT, Cáceres GD, Cortés JA. Nuevas cefalosporinas. Rev Chil Infectol. 2018;35:465-75. https://doi.org/10.4067/s0716-10182018000500465
Instituto Geográfico Nacional, 1989. Atlas del Perú. Lima-Perú. Fecha de consulta: 3 de mayo del 2021. Disponible en: https://bit.ly/3y8M2kA
Astete S, Madrid L, Fukuda F, Buckley A, Meritens D, Menchola JV. Sensibilidad antibiótica de los gérmenes causantes de infecciones urinarias en pacientes ambulatorios en el Hospital Nacional Arzobispo Loayza. Rev Soc Per Med Inter. 2004;17:5-8.
Beckman C. MicroScan. Manual de procedimiento para microorganismos gramnegativos, LabPro multirregional ≥ V4.42. U.S.A. August 2019. Fecha de consulta: 3 de mayo de 2021. Disponible en: https://bit.ly/307u5Tq
Clinical & Laboratory Standards Institute. M100: Performance Standards for Antimicrobial Susceptibility Testing, 30th edition. Clinical & Laboratory Standards Institute. Fecha de consulta: 1 de mayo de 2021. Disponible en: https://clsi.org/standards/products/microbiology/documents/m100/
Kiratisin P, Apisarnthanarak A, Laesripa C, Saifon P. Molecular characterization and epidemiology of extended-spectrum-beta-lactamase-producing Escherichia coli and Klebsiella pneumoniae isolates causing health care-associated infection in Thailand, where the CTX-M family is endemic. Antimicrob Agents Chemother. 2008;52:2818-24. https://doi.org/10.1128/AAC.00171-08
Arce Z, Núñez JL, Clavo RF, Valverde DF. Detección del gen CTX-M en cepas de Escherichia coli productoras de β-lactamasas de espectro extendido procedentes del Hospital Regional de Lambayeque; Chiclayo-Perú: noviembre 2012-julio 2013. Revista Del Cuerpo Médico Hospital Nacional Almanzor Aguinaga Asenjo. 2013;6:12-5.
Morejón-García M. Betalactamasas de espectro extendido. Revista Cubana de Medicina. 2013;52:272-80.
García MH, Valdez CA, Porta TV. Detección de los genes de β-lactamasas blaTEM, blaSHV y blaCTX-M en aislamientos de Escherichia coli comunitarios. Revista Científica de la Facultad de Ciencias Químicas y Farmacia. 2019;28:45-56.
Galván F, Agapito J, Bravo N, Lagos J, Tamariz J. Caracterización fenotípica y molecular de Escherichia coli productoras de β-Lactamasas de espectro extendido en pacientes ambulatorios de Lima, Perú. Revista Médica Herediana. 2016;27:22-9.
Alarcón NC, González JF, Sarabia RL, Sánchez JS, Rosas MR. Caracterización de β-lactamasas de espectro extendido producidas por Escherichia coli de infecciones del tracto urinario adquiridas en la comunidad de Chilpancingo. Guerrero, México. 2014. Fecha de consulta: 1 de mayo de 2021. Disponible en: http://tlamati.uagro.mx/t51/t512.pdf
Rodríguez-Villalobos H, Bogaerts P, Berhin C, Bauraing C, Deplano A, Montesinos I, et al. Trends in production of extended-spectrum β-lactamases among Enterobacteriaceae of clinical interest: Results of a nationwide survey in Belgian hospitals. J Antimicrob Chemother. 2011;66:37-47. https://doi.org/10.1093/jac/dkq388
Suárez-Trueba B, Milián-Samper Y, Espinosa-Rivera F, Hart-Casares M, Llanes-Rodríguez N, Martínez-Batista ML. Susceptibilidad antimicrobiana y mecanismos de resistencia de Escherichia coli aisladas a partir de urocultivos en un hospital de tercer nivel. Revista Cubana de Medicina. 2014;53:3-13
Notas
Notas de autor
*Correspondencia: Pool Marcos Carbajal, Universidad Peruana Unión, Escuela Profesional Medicina Humana, Laboratorio de Investigación en Biología Molecular, Lima, Perú Teléfono: (019) 9332 8351 poolmarcos@upeu.edu.pe y poolmarcoscarbajal@gmail.com
Declaración de intereses