Artículos
Astrocitos: acción e interacción en el Sistema Nervioso*
Astrocytes: Action and Interaction in The Nervous System
Astrócitos: ação e interação no Sistema Nervoso
Astrocitos: acción e interacción en el Sistema Nervioso*
Revista Med, vol. 32, núm. 1, pp. 83-100, 2024
Universidad Militar Nueva Granada. Facultad de Medicina
Recepção: 03 Agosto 2023
Aprovação: 26 Abril 2024
Publicado: 29 Junho 2024
Resumen: Los astrocitos, junto con los oligodendrocitos, y microglia hacen parte del tejido de neuroglia acompañante de las neuronas. Debido a la importancia y avances en esta área se plantea esta revisión bibliográfica, la cual se llevó a cabo a través de la búsqueda de "astrocitos" en revistas relacionadas con neurociencias a nivel celular y molecular como "Glia, Cells, Neuron", de los últimos cinco años (2018-2023), con el fin de recopilar la información sobre estructura y función de estas células gliales. Se reseña la evolución de la glía, los tipos de astrocitos y la estructura y función de los astrocitos. Los astrocitos interactúan con otras células y con los sistemas circulatorio, inmune y neuroendocrino; son fundamentales para el metabolismo, sinaptogénesis, neurogénesis, neuroplas-ticidad y neuroprotección.
Palabras clave: Actividad neuronal, astroglia, glía, microglía.
Abstract: Astrocytes, alongside oligodendrocytes and microglia, constitutes the glia tissues that accompany neurons. Given the significance and advancements in this field, this bibliographic review aims to in compile the information related to the structure and function of astrocytes. The review was conducted by searching for "astrocytes" in neurosciences journals at the cellular and molecular levels, such as "Glia'', "Cells", and ''Neuron", published within the last five years (2018-2023). The review encompasses the evolution of glia, types of astrocytes, and the structure and function of these cells. Additionally, it explores how astrocytes interact with other cells, as well as circulatory, immune, and neuroendocrine systems, highlighting their essential roles in metabolism, synaptogenesis, neuro-plasticity, and neuroprotection.
Keywords: Neuronal Activity, Astroglia, Glia, Microglia.
Resumo: Os astrócitos, juntamente com os oligodendrócitos e a micróglia, fazem parte do tecido de neuroglia que acompanha os neurônios. Devido à importância e aos avanços nesta área, propõe-se esta revisão bibliográfica, a qual foi realizada através da busca por "astrócitos" em revistas relacionadas a neurociências a nível celular e molecular como "Glia, Cells, Neuron", dos últimos cinco anos (2018-2023), com o objetivo de compilar informações sobre a estrutura e função dessas células gliais. É abordada a evolução da glia, os tipos de astrócitos e a estrutura e função dos astrócitos. Os astrócitos interagem com outras células e com os sistemas circulatório, imune e neuroendócrino; são fundamentais para o metabolismo, sinaptogênese, neurogênese, neuroplasticidade e neuroproteção.
Palavras-chave: Atividade neuronal, astroglia, glia, microglia.
Introducción
Los astrocitos (Ast) son las células gliales más numerosas del sistema nervioso central (SNC) (figura 1); en el cerebro del humano adulto comprenden del 20 % al 40 % de la materia gris cerebral 1,2; la sustancia blanca presenta mayor cantidad que la gris 3. Los Ast pueden activar genes o vías de señalización o expresión de proteínas que permiten su acción e interacción con otras células gliales y neuronas para mantener la homeostasis del SNC; alteraciones en cualquiera de estos procesos pueden acarrear disfunción, además pueden experimentar cambios morfológicos/fisiológicos y aumentar con la senectud en el caso de mamíferos, primates, roedores y humanos, o con el progreso de algunas enfermedades neurodegenerativas o desórdenes del sistema nervioso de los humanos 4-6.
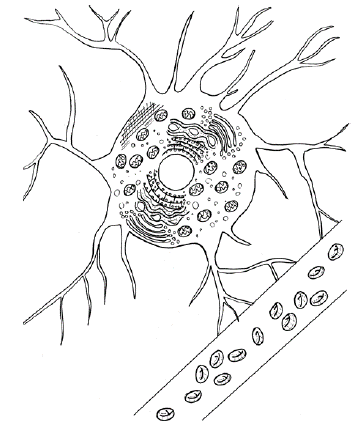
Figura 1
Astrocito conectado a un vaso sanguíneo
Fuente: elaboración propia.
Los Ast hacen parte de la barrera hematoencefálica del cerebro (BHE), regulan y modulan los neurotransmisores y señales moleculares, interactúan con otras células de la glía, del sistema inmunitario y neuroendocrino, y son indispensables para regular el metabolismo de las neuronas. Con el fin de evidenciar la importancia, participación específica en la homeostasis del SNC y los avances en este tema se plantea esta revisión basada en información bibliográfica de los últimos cinco años (2018-2023).
La investigación sobre Ast se basa en modelos de animales mamíferos, principalmente en ratones y macacos, Macaca mulatta, y en el humano asociado con el avance del conocimiento de las enfermedades neurodegenerativas y desordenes del SNC 7-10.
Evolución de la glía
Las células del sistema nervioso al parecer coevolucionaron con diferencias funcionales, las neuronas asociadas a la generación del potencial de acción y sinapsis, y la neuroglia, a la homeostasis y defensa. La evolución de la neuroglia es concomitante con la evolución de los bilateria y del SNC; además se expresa de manera diferencial tanto en protostomados como en deuterostomados. En los primeros predomina la glía parenquimatosa, desde algunos platelmintos como tricladidos y policladidos, anélidos, moluscos, nematodos (Caenorhabditis elegans) y con desarrollo notable en insectos, especialmente estudiadas en Drosophila. Por otro lado, en los deuterostomados prevalece la glía radial, se encuentra en algunos acelomorfos y en equinodermos, cefalocordados y cordados. Dentro de los anamniotas se destaca el pez cebra (Danio rerio) como modelo para estudio de los Ast. Los Ast guardan mayor similitud entre los amniotas, y en los mamíferos hay diferencias notables, v. g. entre los Ast de roedores y humanos tanto en tamaño (los Ast humanos triplican el tamaño de los murinos), expresión diferencial de los genes (a nivel del metabolismo mitocondrial, defensa, espacio extracelular y factores secretados), en respuesta a los agonistas de los diferentes receptores y con mayor diversidad estructural y funcional en los Ast humanos. Por otra parte, los primates y humanos también difieren del resto de mamíferos, por el papel que juegan con relación al comportamiento y cognición; además en los humanos son mucho más complejos, respecto a su expresión génica differencial, estructura, función y perfil transcriptómico especializado, v. g. en la expresión de genes del metabolismo mitocondrial en humanos y chimpancé, al parecer con mayor capacidad metabólica en los humanos 11-15.
Tipos de astrocitos
Por su morfología y organización espacial los Ast se clasifican en protoplásmicos, caracterizados por un soma pequeño, muchos organelos, procesos muy ramificados y localizados en la sustancia gris (figura 1) y fibrosos con cuerpo poligonal, pocos organelos y un proceso largo sin ramificaciones, ubicados en la sustancia blanca; ambos Ast se conectan con los vasos sanguíneos a través de los pies perivasculares 16-18.
Los Ast piales son una población de Ast protoplásmicos localizados en la superficie cortical debajo de la piamadre, caracterizados por sus procesos de largo diferencial, dependiendo del grupo de mamíferos; en primates son largos, gruesos y se extienden hasta las capas corticales más profundas, no están asociados a los vasos sanguíneos, y en roedores forman la glía limitante, cuya función es proporcionar una barrera protectora 19.
Según su respuesta inmunológica ante patógenos/daño del sNc, los Ast experimentan cambios llamados astrocitosis reactiva o astrogliosis o gliosis reactiva o reacción de astrocitos o reactivación de astrocitos. Los Ast reactivos son de dos tipos, los A1 son proinflamatorios o de fenotipo neurotóxico y los A2 antiinflamatorios o de fenotipo neuroprotector. La astrocitosis reactiva puede ser inducida por la microglía. Los Ast expresan de forma diferencial proteínas o receptores, así como responden a factores de manera diferente. Respecto a los Ast A1 hay un subtipo denominado Ast reactivo C3+, con receptores del complemento 3 (C3aR) 1,3,16,20-25.
Estructura y función de los astrocitos
Los filamentos intermedios que hacen parte del citoesqueleto están formados por la proteína ácida fibrilar glial (GFAP), cuya función es mantener la estructura, movimiento y cambio de forma de los Ast. Las uniones entre los Ast acoplados forman redes, con estructura sincitial; la transferencia de moléculas entre las células y la matriz extracelular está mediada por uniones comunicantes y hemi-canales formados por conexinas, en particular la conexina-43 (Cx43), la cual es altamente expresada en los que hacen parte de BHE; esta conexina también es responsable del transporte de metabolitos, como glucosa y lactato a través de las redes astrocí-ticas. Otras moléculas de adhesión entre Ast y neuronas son astrotactinas y protocadherinas, ambas cooperan significativamente en el desarrollo de circuitos neuronales y formación de sinapsis 17,18,20,26-29.
Los Ast presentan heterogeneidad morfológica (HM) dependiente de: (a) su ubicación por estrato y órgano/región v. g. los Ast protoplásmicos corticales muestran cuatro subtipos morfológicos, con distribución proporcional diferencial a través de las distintas capas corticales; de la misma forma, en la circunvolución dentada la HM se relaciona con la estratificación de esta área; los Ast de los estratos corticales además de diferir en la morfología también divergen en la señalización y paisaje transcriptómico; según la región del encéfalo donde se ubiquen presentan una HM y funcional, v. g., los Ast del mesencéfalo vs. los Ast del telencéfalo; (b) a nivel del dimorfismo sexual, v. g. en la expresión diferencial de los genes del ciclo celular de la astroglía durante el desarrollo del cerebro según el sexo en ratones, pez cebra y humanos; por otra parte, en adultos humanos hay cambios en el número, diferenciación y función, de acuerdo con el sexo 6,13,30-32.
De las sinapsis tripartitas coordinadas por los Ast se pasó a la teoría sináptica multipartita que incluye los siguientes elementos: membranas de las neuronas pre- y postsinápticas, procesos tanto de Ast como de microglía y la matriz extracelular. Varios procesos están implicados en esta coordinación, como la modulación de la transmisión y liberación por ejemplo de glutamato, D-serina y ATP, ante altas concentraciones de Ca++ en los Ast; la regulación del flujo extracelular, el trasporte y homeostasis de iones, el flujo de sangre cerebral, la remodelación sináptica y la provisión para mantener la estabilidad de la actividad neuronal.
En la corteza de ratón un Ast puede interactuar con 100.000 sinapsis, y en el humano, hasta con más de 2.000.000 de sinapsis simultáneamente 6,18,20,27,33-36.
Los Ast pueden inducir y regular los procesos de poda de sinapsis, sinaptogénesis, diferenciación neuronal, neurotransmisión y plasticidad; además ejercer un papel neuroprotector al promover el crecimiento dendrítico y la supervivencia y actividades electrofisiológicas de las neuronas. Los Ast secretan sustancias a través de microvesículas o exosomas; estas moléculas secretadas contribuyen a la comunicación celular en el sNc y en la modulación de procesos como plasticidad sináptica, respuesta ante estrés neuronal y neurogénesis. De la misma forma, pueden secretar sustancias ante agentes tóxicos/lesiones como citosinas, quimioci-nas, lipocaina-2, ARN no codificantes, microARN. También regulan las necesidades energéticas tanto para mantener la función neuronal como para movilizar dichas reservas a través del almacenamiento de glucógeno y lípidos, así como del metabolismo oxidativo mitocondrial: activación a conveniencia de la glucolisis total o de oxidación de ácidos grasos y el transporte externo de metabolitos. La optimización de la actividad fagolisosomal de los Ast está relacionada con el correcto funcionamiento a nivel del citoplasma, nucleoplasma, mitocondrias, retículo endoplasmático y aparato de Golgi (figura 1) 1,16,25,37-39.
Reseña de las principales acciones e interacciones de los astrocitos
Relación con la barrera hematoencefálica (BHE)
-
Modulan el flujo cerebral de la BHE al extender sus podocitos que cubren el 99 % de la superficie de los vasos sanguíneos cerebrales. Moléculas secretadas por los podocitos adheridos a la membrana basal de la BHE, tales como Claudin 5, uniones de oclusión, ZO-1 y 2 pueden ajustar la unión estrecha entre las células endoteliales en la BHE en el cerebro, para ejercer una función neuroprotectora. Cambios en la cobertura de Claudin 5 pueden conducir a una hiperpermeabilidad vascular. La permeabilidad de la BHE también está regulada por AQP4, conexina 43 e integrina ß4 6,20,21,40.
-
Mantenimiento de la BHE a través de las proteínas SHH (hedgehog) y ß-catenina que favorecen la unión estrecha e integridad; no obstante, interrumpen BHE local, a través de la liberación del factor de crecimiento endotelial vascular (VEGF), aumentando así la permeabilidad y entrada de células inmunes periféricas 20.
Receptores de membrana, canales iónicos y transportadores
-
La aquaporina-4 (AQP4) ubicada en los podocitos de los Ast regula el transporte de agua adentro/afuera del parénquima cerebral; además presenta inmunoactividad y mantiene la permeabilidad e integridad de la BHE 17,21,41.
-
La enzima glutamina sintetasa de los Ast convierte el glutamato en glutamina. El transportador de glutamato 1 (GLT-I) transporta glutamato al interior celular para limpiar de este aminoácido del espacio extracelular; el transportador EAAT2, localizado principalmente en el Ast, es el responsable de la captación del 90 % del glutamato en el cerebro 3,17,42.
-
Los Ast disponen de canales de potasio (Kir); los canales de K+ tipo Kir4.1 mantienen el potencial de reposo de la membrana de los Ast y su inhibición activa su despolarización. Estos canales eliminan el exceso de K+ extracelular de las sinapsis, a través de su recepción. Los canales Kir4.1 se acoplan a los transportadores de glutamato y de agua (AQP4); así participan en la regulación de estos transportadores, y también modulan la expresión del factor neurotrófico derivado del cerebro (BDNF). La inhibición de Kir4.1 eleva el K+ extracelular, aumenta el glutamato y facilita la expresión de BDNF; todo conducente a elevar la excitabilidad neuronal, la conectividad sináptica y facilitar la plasticidad. Kir4.1 regula la promoción/extinción del miedo en el hipocampo. La disfunción de SODI inhibe la expresión de estos canales trayendo como consecuencia un incremento tanto de K+ como de los niveles del glutamato sináptico, que llevan a la excitotoxicidad e incluso a la muerte de neuronas motoras 18,43,44.
-
En los Ast del hipocampo, la activación de los receptores opioides MOR provocan la activación del canal K2P y la liberación rápida de glutamato. En los Ast del hipocampo K2P/TREKI y MOR están colocalizados. Los receptores MOR de los Ast se relacionan con analgesia y adicción 45.
Relación con neurotransmisores/ neuromoduladores
-
La glutatión S-tranferasa (GSTMI) transporta hacia el espacio extracelular el glutatión, el cual cumple funciones detoxificantes. Los Ast regulan la expresión de GSTMI, que controla la inflamación cerebral, igualmente modulan la actividad y nivel de estrés neuronal durante la inflamación cerebral 46.
-
Los Ast sintetizan y liberan GABA, presentan receptores GABAa y GABAb por consiguiente, controlan el metabolismo y homeostasis de GABA , así mismo conservan el flujo GABA y glutamina entre las neuronas y los Ast (o ciclo GABA-glutamina), necesario para mantener la síntesis de GABA y la señalización inhibitoria 46-48.
-
En el hipocampo se realiza la regulación neuronal del comportamiento según el contexto social (interacción vs. aislamiento social); los Ast a través de TRPAI y GABA después del aislamiento social suprimen el funcionamiento del circuito en el hipocampo, con el consiguiente déficit fisiológico y cognitivo 49.
-
Los Ast de la corteza prefrontal media e hipocampo a través de la regulación de la neurotransmisión glutamatérgica (glutamato/ ATP / adenosina y receptores) mejoran la capacidad cognitiva, la toma de decisiones y la memoria de trabajo 50,51.
-
Regulación del ciclo sueño/vigilia a través del eje adenosina/astrocito/sueño. Los Ast disponen de receptores de adenosina AI (AIR) y de la enzima adenosina quinasa que regulan el sueño. Así mismo, cambios en los Ast, como la disminución tanto del Ca++ como del pH y el aumento del volumen cerebral local, están relacionados con la ampliación de señales sinápticas, probablemente responsables de la formación de la memoria durante el sueño REM; igualmente la disminución del IP3 y de la señalización del calcio, modulan el sueño REM y el ritmo de las oscilaciones theta (5-8 Hz). Por otra parte, la somatostatina secretada por las interneuronas activan los receptores GABAb de los Ast, los cuales mediante la liberación de ATP /adenosina/ AIR mantienen la amplitud de la corriente postsináptica inhibitoria e inhiben las neuronas piramidales de la corteza visual. Los Ast a través de la expresión diferencial de genes (clock, bmal1, per1, per2, cry1) contribuyen a la regulación de los ritmos circadianos independientemente de las neuronas, v. g. los genes per2 permiten la síntesis/recaptación de glutamato, regulando excitabilidad vs. niveles decrecientes de glutamato durante la fase oscura 6,29,52-54.
-
Los receptores endocanabinoides de los Ast actúan en los procesos de modulación del calcio, gliotransmisión de ATP, glutamato, D-serina, GABA, de la activación de la vía adenosina/AiR; metabolismo del ciclo de Krebs/ oxidación de ácidos grasos, glucógeno, disminución de ROS mitocondrial y efectos antiinflamatorios. La activación de los receptores endocanabinoides tipo 1 inducen la secreción de D-serina que impulsan la potenciación a largo plazo (LTP) y la consolidación de la memoria 6,55,56.
-
Los Ast del cerebro actúan en respuesta a los neuromoduladores Ach, NE y serotonina. La NE es regulador de procesos como el aprendizaje y la memoria. NE activa los receptores adrenérgicos ß2 de los Ast, lo cual conduce a la producción de L-lactato durante el procesamiento de la memoria. Ach y Ast actúan en la modelación del proceso visual. El receptor de serotonina astrocítico (5-HT4R) vía de la señalización Ga13-RhoA y Gas inducen cambios morfológicos en los Ast, remodelando la actina; RhoA por su parte interviene en la retracción de los podocitos. Por otra parte, la vía triptófano/serotonina en el Ast puede convertirse en N-acetil serotonina (NAS), capaz de activar BDNF y el receptor TrkB, pero el NAS puede ir a la vía melatonérgica, para producir melatonina, que lleva a optimizar la función de la mitocondria, además tiene efectos antiinflamatorios y antioxidantes 29,57,58.
-
La histamina (ht) cuenta con varios receptores en el Ast HIR, H2R y H3R, todos con funciones diferentes. En el citoplasma de los Ast se encuentra la enzima que degrada la ht HNMT, encargada de regular la concentración de ht en el espacio extracelular del SNC. Esta enzima es un 70 % más activa que la presente en las neuronas, asegurando así su eficiencia en la eliminación e inactivación de la ht. Los receptores HIR de los Ast regulan la excitabilidad neuronal, la supervivencia celular, la modulación de la respuesta inflamatoria, el comportamiento agresivo, los ritmos circadianos y las ondas delta de frecuencias 1,5 a 4 Hz durante la vigilia 59,60.
Metabolismo
-
Los Ast sintetizan la mayor parte de ceruloplasmina del cerebro, proteína encargada de regular la homeostasis del hierro, este último en el hipocampo y en la corteza cerebral contribuye a mantener la memoria y el aprendizaje 10.
-
Los Ast regulan la actividad de MAO-A relacionada con la modulación de los niveles de neurotransmisores y genes de neurotrófinas NTRK2/TrKB 44,61.
-
Los Ast regulan la actividad de MAO-B para la síntesis de GABA en varias regiones del encéfalo (cerebro, estriado, corteza cerebral, hipocampo, mesencéfalo); los Ast liberan GABA vía canal bestrofina-1, con inhibición tónica de las neuronas vecinas; v. g. el GABA astrocítico ejerce un efecto inhibitorio en la excitabilidad de las neuronas del giro dentado del hipocampo y de las células granulosas del cerebelo. Este GABA también está implicado en la inhibición de las neuronas con activación del receptor GA-BRA5 del área hipotalámica lateral, causando una disminución del gasto energético 62-64.
-
La α-sinucleina regula el metabolismo de los ácidos grasos en los Ast; mantiene la homeostasis de los ácidos araquidónico y palmítico y los Ast también se encargan de la destrucción y eliminación de la a-sinucleina proveniente de neuronas por endocitosis y autofagia lososomal a través de lipidación 65.
-
Los Ast a través de varias vías reguladoras contribuyen a la neuroprotección de las neuronas, evitando daños y apoptosis de las neuronas, procesos de oxidación mitocondrial eficientes, limpiando los ROS y mitofagía óptima para eliminar mitocondrias disfuncionales. Además, los Ast expresan receptores de fagocitosis tyro3/Axl/Mertk y Megf10, importantes para eliminar desechos y poda de sinapsis; así como pueden engullir igualmente desechos microgliales, mielina y neuritas distróficas. La proteína quinasa activada por AMP regula la dinámica del ciclo de Krebs de los Ast, a través de la actividad de la piruvato carboxilasa y glutamato deshidrogenasa, favoreciendo la anaplerosis. La expresión de SODI en los Ast cataliza la conversión del superóxido de radicales libres en agua y peróxido de hidrógeno, por consiguiente, con función detoxificante. De igual modo, el ácido fosfatídico cíclico en los Ast ejerce funciones neuroprotectoras en el cerebro. Por último, los Ast activados sintetizan y liberan glutatión antioxidante que protege contra las especies de ROS, y regula la homeostasis redox neuronal (2,21, 65-69).
-
Los Ast actúan en la regulación de la cinasa TORm principalmente durante la deprivación de oxígeno/glucosa, con efectos positivos en el metabolismo como la reducción de ROS, en la sobreexpresión de GLTI y reducción de la excitotoxicidad, y la liberación de VEGF y BDNF que promueven la angiogénesis y mejoran la supervivencia neuronal 70.
-
Los Ast expresan TDP-43 implicada en la regulación de la dinámica y función mitocondrial: polarización de la membrana interna, producción de ATP, control de ROS mitocondrial, así como en la morfología, densidad y largo de las neuritas de las neuronas corticales, contribuyendo así a la plasticidad sináptica. La sobreexpresión de TDP-43 induce en los Ast la activación de la respuesta proinflamatoria mediante la vía NF-KB causando neurotoxicidad; así mismo, la disfunción o pérdida de TDP-43 lleva a cambios en la microglía, a la toxicidad de oligodendrocitos maduros y a déficit motores 71-74.
-
La enzima autotaxina de los Ast cataliza la formación del ácido lisoffosfatídico (LPA) que actúa en la modulación de la transmisión glutamatérgica. El LPA está implicado en procesos del cambio del equilibrio excitación/inhibición (E/I) hacia la hiperexcitabilidad de la corteza cerebral; en la señalización de la modulación astrocítica de la memoria de trabajo y también en la hiperfagia bajo el control de las neuronas AgRP del hipotálamo 51,75-77.
-
Glucogenólisis y lactato de los Ast proporcionan la energía a las neuronas para los procesos del aprendizaje y memoria a largo plazo, en el hipocampo y en el cerebro. La activación glutamatérgica aumenta la glucólisis astrocítica y la liberación del lactato en el espacio extracelular. Las neuronas utilizan lactato para consolidar la memoria, que demanda energía 1,29,78.
-
Síntesis de colesterol en el cerebro. Los Ast son las principales células del cerebro que expresan APOE que transportan colesterol, y regulan la síntesis y liberación de colesterol tanto para las neuronas como para la microglía y conservan su homeostasis. El colesterol transportado por los Ast a través de APOE puede activar la vía de la enzima α-secretasa en la membrana de la neurona y contribuir a establecer la excitabilidad neuronal; sin embargo, el colesterol también puede activar la vía amiloidogénica a través de la activación de ß o γ- secretasa que activa la producción de placas ß-amiloide. Los Ast regulan los ácidos grasos saturados de cadena larga y secretan vesículas con los lípidos: fosfatidilcolina, ceramidas y glucosilceramidas 1,3,79.
-
Los Ast metabolizan ácido linolénico a través de la vía de desaturación y elongación para la producción de DHA y EPA y liberación posterior para su incorporación en fosfolípidos y mediadores lipídicos antinflamatorios, como maresinas, resolvinas y protectinas 8.
-
Los Ast sintetizan serpina3, la cual actúa en la regulación del dolor neuropático y neuroinflamación; se incrementa su síntesis en respuesta a y TNFα, este último factor también puede activar los mastocitos y la microglía para incrementar la respuesta proinflamatoria y dolor crónico 42.
Procesos de aprendizaje, memoria, plasticidad neuronal y comportamiento
-
Los Ast regulan elevan/bajan la concentración de Ca++ permitiendo la modificación de la transmisión sináptica con potenciación/ depresión a largo plazo (LTP/LTD), las sinapsis LTP están relacionadas con el mejoramiento de la memoria en el hipocampo. La expresión del factor de transcripción nuclear IA en Ast maduros del hipocampo, permite los procesos de plasticidad sináptica, activan los circuitos de LTP, el aprendizaje y la memoria 29,81.
-
La comunicación entre neuronas y Ast en la amígdala central/basolateral y la habénula lateral modulan las respuestas de ansiedad/miedo/ depresión. Por otra parte, los Ast expresan el factor de transcripción Sox9 y la proteína S100ß relacionados con la homeostasis del estado de ánimo 35,44.
-
Existe una comunicación bidireccional entre Ast y neuronas y la regulación de las sinapsis del circuito sináptico, entre las neuronas que salen de la corteza entorrinal y llegan a la circunvolución dentada (GC) del hipocampo, a través de las células granulares dentadas (PP-GC). Los Ast ejercen control tanto durante la actividad sináptica basal como en la probabilidad de liberación presináptica en las sinapsis PP-GC, con efectos en la transmisión y plasticidad de las sinapsis PP-GC. Este circuito está implicado en la eficiencia de los procesos de memoria contextual, aprendizaje y modelamiento del comportamiento 82.
-
En el globo pálido externo el aumento de la actividad de los Ast se atenúa ante un comportamiento habitual y mejora frente a un comportamiento dirigido al cumplimiento de objetivos 83.
-
Los Ast sintetizan y liberan factores neurotróficos como BDNF, el factor neurotrófico derivado de la glía, el factor de crecimiento de los fibroblastos 2 y el factor de crecimiento nervioso, todos cooperan en la conservación de la salud neuronal, regulan el crecimiento neuronal y resultan esenciales para la plasticidad neuronal 44.
-
Los Ast captan, reciclan y expresan BDNF en las sinapsis, a través de este factor regulan la supervivencia, diferenciación y crecimiento de las neuronas centrales y periféricas durante el desarrollo y edad adulta, y, de nuevo, ejercen un papel en la consolidación de la memoria del miedo, la extinción del aprendizaje y la plasticidad sináptica. A su vez los Ast reactivos expresan BDNF que coadyuvan en la ruta de migración de los neuroblastos para facilitar la maduración de neuronas nuevas, generadas en la zona subventricular en respuesta a lesiones cerebrales 5,9,84-86.
-
Los Ast expresan moléculas de adhesión tales como efrinas (Eph A3, Eph A4, Eph B1, EphB2, EphB3), neuroliginas (Nlgn1, Nlgn2, Nlgn3), neurexinas (Nrxn1 y Nrxn2), 7-protocadheri-nas y moléculas de expresión de células neuronales NrCAM, todas implicadas en diferentes procesos de formación y función de sinapsis, morfogénesis y maduración de Ast, formación y complejidad dendrítica, regulación de sinapsis E/I. Por ejemplo, la Eph B1 astrocitica regula diferencialmente el desarrollo de circuitos E/I en el hipocampo, durante el desarrollo postnatal inicial; igualmente, en el hipocampo del adulto regula la memoria contextual a largo plazo. Por su parte, la señalización EphA3/ EphA4 entre Ast y neuronas del núcleo supra-quiasmático regula la plasticidad circadiana en respuesta a la luz 36,87,88.
-
Los Ast ejercen un papel neuromodulador a través de la señalización adrenérgica. La excitación (asincronía, hiperactividad) es inducida por la NE en las neuronas de la corteza cerebral; sin embargo, simultáneamente la NE activa los receptores de Adra1a de los Ast que conducen a la sincronía (calma, relajación) cortical bihemisférica. De esta forma los Ast actúan como reguladores de transición entre estados de asincronía/sincronía en la corteza cerebral durante la vigilia, y están implicados mediante esta señalización en los procesos de percepción y cognición 89.
-
Los Ast de la corteza prefrontal (CPF) expresan receptores de dopamina a través de la activación de receptores adrenérgicos a1/Ca2+ y actúan en la regulación de la liberación del ATP astrocítico. La dopamina en la CPF induce ATP extra-celular restringido que lleva a la disminución de las sinapsis y a la supresión de la actividad de un territorio específico de esta corteza, v. g. en el retraso de las tareas de memoria de trabajo 32.
-
Los Ast piales a través de la estimulación simultánea entre los receptores dopaminérgicos (DIR) y colinérgicos muscarínicos (MIR) llevan a mejorar la formación de AMPC, participando en la activación de la actividad cortical 19.
-
Los cambios dependientes de la experiencia sensorial durante el desarrollo y el adulto vs. los circuitos sinápticos están correlacionados con la morfogénesis y sinaptogénesis de los Ast, v. g. los Ast corticales muestran cambios morfológicos y de neurotransmisores, especialmente del glutamato, ante estímulos visuales y táctiles 56.
-
Los Ast mediante la regulación del transporte de neurotransmisores y de la señalización de calcio contribuyen a la función de las neuronas de la corteza motora primaria (MI) durante el aprendizaje motor, y a la ejecución y destrezas del movimiento aprendido. De hecho, en los ratones con un comportamiento motor aprendido, los Ast de MI experimentan cambios en la expresión de los genes de los transportadores de glutamato y GABA, y de genes de proteínas de la matriz extracelular 90.
Procesos de regulación neuroendocrina
-
Los Ast del hipotálamo, núcleo arcuato expresan receptores para la insulina, grelina y leptina, por consiguiente, con funciones en el metabolismo del cuerpo. La señalización de la insulina por parte de los Ast contribuye a la regulación de la temperatura corporal por medio de la estimulación simpática de la activación del tejido adiposo pardo, para la generación de calor. Los receptores de grelina actúan en varias direcciones: en la activación de los Ast, con el incremento de la síntesis de GFAP y cambios en otros receptores, v. g. insulina, GLUT-I, GLAST y en la enzima PYGB. La despolarización de los Ast es causada por el GABA liberado por las neuronas AgRP inducidas por la grelina, circuito que se activa en el ayuno. Por su parte, los receptores de leptina, a través de la vía HI-F1α- VEGF intervienen en la regulación de los procesos de angiogénesis, presión arterial y cambios de la microestructura y permeabilidad de la membrana basal endotelial de la BHE 29,40,91-95.
-
Los Ast expresan receptores hormonales del estrés tales como glucocorticoides y mineralo-corticoides; v. g., la activación de receptores de glucocorticoides están comprometidos con la inhibición de la proliferación de Ast. El estrés crónico asociado con el cortisol afecta la expresión de genes únicos, tales como los GPCR asociados a los receptores de serotonina HTRIB, del factor neurotrófico GDNF y de los receptores del glutamato GRMI y GRM8. Los receptores glucocorticoides del Ast de la corteza frontal media modulan la inducción y activación de serotonina (5HT), la cual impulsa la plasticidad sináptica y gliotransmisión, a través de la modulación de la señalización de calcio, para mantener tanto el estado de ánimo como el cognitivo 5,61,96.
-
Los Ast hacen parte de las células de la eminencia media del sistema endocrino que coadyuvan en la regulación de las funciones entre el hipotálamo y la hipófisis. Tal es el caso de la interacción de neuronas secretoras de GnRH del hipotálamo con los Ast recién nacidos, a través de la vía de señalización de la PGE2, modulan la activación y liberación de la GnRH, una vez se ha iniciado la maduración sexual 97-99.
-
La oxitocina actúa como neuromoduladora de la actividad de la red entre Ast y neuronas; además induce cambios en la citoarquitectura del Ast relacionados con la expresión de GFAP y con la dinámica de microtúbulos/actina. La oxitocina exógena promueve la señalización de calcio de los Ast y activa los segundos mensajeros de vías intracelulares, como AMPC, fosfolipasa C y proteína cinasa C. Los receptores de oxitocina astrocíticos se encuentran en varias áreas del encéfalo, principalmente en el hipotálamo, amígdala y corteza auditiva en roedores, y en humanos en la corteza frontal; al parecer también están implicados en procesos emocionales. La lactancia en murinos esta neuro-modulada tanto por los Ast y la activación de NMDAR y externa de oxitocina en los núcleos paraventricular y supraóptico 56,100.
Interacción con otras células
-
Los Ast pueden mediar la transmigración de células T reactivas en el SNC vía moléculas de adhesión celular quimiocinas y metaloproteinasas. A su vez, las células T modulan el equilibrio de los subtipos de Ast para mantener su homeostasis 16,24.
-
La microglía libera mediadores inflamatorios e induce al cambio de fenotipo de los Ast, esta última acción lo logra a través de la liberación de citosinas de manera diferencial, y los Ast, debido a la estructura de red y movimiento, amplifican la señal de neuroinflamación y la inmunidad periférica. Por otra parte, los Ast y la microglía pueden producir tanto moléculas de óxido nítrico (NO) como de ROS como mecanismo de defensa contra patógenos microbianos. La sinergia entre microglía y Ast contribuye a la eliminación de depósitos de proteínas como α-sinucleína y ß-amiloide; como parte del sistema glinfático, limpian el cerebro de proteínas y metabolitos insolubles que drenan hacia el sistema venoso. Los Ast, a través del factor de transcripción EB, mejora la función lisosomal, e inducen a la captación y degradación de ß-amiloide. Otros mecanismos para la eliminación de ß-amiloide son la liberación de la enzima neprilisina por parte de los Ast, y el aumento de la actividad peroxisomal, para protegerse a sí mismos y a las neuronas de la toxicidad de ß-amiloide 2,3,20,21,52,69,101,102.
-
Los Ast interactúan con los oligodendrocitos para modular la mielinización, estos se conectan entre sí, a través de redes mediadas por conexina. Los Ast a través de la expresión de las semaforinas 3 y 6 actúan para repeler las células precursoras de oligodendrocitos y permitir su diferenciación y mineralización axo-nal. En el tálamo forman redes pangliales con el objetivo de suministrar sustratos de energía para mantener la actividad neuronal; los oligo-dendrocitos ayudan con la trasferencia de estos metabolitos a las neuronas postsinápticas. Así mismo, la señalización conjunta de Ast/ oligodendrocito en el área del córtex del cíngulo anterior y amígdala basolateral promueve la oligodendrogénesis y la mielinización adaptativa, facilitando la recuperación del rendimiento cognitivo (toma de decisiones) y la modulación de la red neuronal del dolor crónico 103-106.
-
Los Ast del mesencéfalo ventral están acoplados a los oligodendrocitos y de estos últimos depende su supervivencia; al parecer su sinergia con las neuronas dopaminérgicas de esta región del encéfalo permiten la regulación de los transportadores de calcio, potasio y glutamato, con tendencia a niveles más bajos, a través de la modulación de los receptores de dopamina D2R de los Ast y de las neuronas dopaminérgicas 31.
-
Los Ast y tanicitos ubicados alrededor de los ventrículos cerebrales están comprometidos con varias funciones, tales como iniciar respuestas inflamatorias inducidas por lipopolisacáridos; a través del receptor vaniloide 1; de la termorregulación en ambientes cálidos menores a 37 °C, y, por medio de la regulación del sodio, aportan en la preservación de la homeostasis de los fluidos corporales 107.
-
La comunicación entre neuronas, Ast, microglía y oligodendrocitos está mediada por los sistemas de señalización purinérgicos: señalización de ATP operados por los receptores P2x y P2Y, señalización de adenosina operados por los receptores AI y A2A. Los receptores de adenosina cooperan para modular la información predominante, codificada a través de la sinapsis. Existe una comunicación bidireccional entre neuronas y Ast a través del ATP mensajero, que coordina la actividad de esta dupla celular, v. g. los receptores P2Y de los Ast son activados por el ATP liberado por las neuronas y los Ast responden activando la señalización de Ca++ y otros procesos como la liberación de neurotransmisores. Los receptores A2A tanto de neuronas como de Ast modulan funciones relacionadas con la motivación y comportamiento dirigido al cumplimiento de objetivos, aspectos cognitivos implicados en el almacenamiento y mejora del proceso incluyendo el aprendizaje y la memoria remota y de trabajo. Los receptores A2A expresados tanto de neuronas como en la glía presentan plasticidad y heterogeneidad funcional, v. g. la respuesta de los receptores con efectos en la función cognitiva es dependiente de la región del cerebro activada, de factores ambientales y de contexto, edad y sexo 76,108-110.
-
Los Ast piales y sus receptores dopaminérgicos pueden regular el modo de activación de las células piramidales, ya sea para la activación regular o en ráfaga 19.
-
La activación del AHR y sus ligandos en el Ast está relacionada con la supresión de la señalización del factor nuclear Kß, disminuyendo el riesgo de contraer enfermedades neurodegenerativas relacionadas con el envejecimiento y a disminuir la inflamación. Igualmente, la activación de AHR de los Ast vía del triptófano derivado de la biota intestinal produce efectos antinflamatorios en SNC 6,111.
Dediferenciación celular
-
A nivel molecular se encontró que los Ast pueden diferenciarse a través de la sinergia de la pérdida dep53 (celular intrínseco) y activación de la señalización EGFR (celular extrínseco) por coalescencia con mTOR, quien aumenta la traducción de los factores de transcripción de las células madre. Esto sugiere que los Ast paren-quimatosos pueden representar una reversión de los programas de desarrollo y su diferenciación a neuroblastos 112.
En síntesis las acciones e interacciones de los Ast las podemos resumir en la tabla 1.

Fuente: síntesis de esta revisión; elaboración propia.
Conclusión
Los Ast participan activamente en el mantenimiento, regulación y homeostasis del SNC. Las investigaciones recientes pretenden descubrir cuáles son las interacciones celulares y moleculares a través de neurotransmisores, neuromoduladores, vías de señalización e integración de circuitos neuronales y su relación con los diferentes procesos de metabolismo, aprendizaje, memoria, comportamiento, acciones neuroendocrinas y neuroplasticidad. Por otra parte, los Ast se expresan y modulan la neurotransmisión de manera diferencial y dependiente del estímulo de la situación/actividad y de la red neuronal en la que participen.
Referencias
W Ng and SY Ng. Remodeling of astrocyte secretome in amyotrophic lateral sclerosis: uncovering novel targets to combat astrocyte-mediated toxicity, Transl Neurodegener. [Internet]. 2022;11(54):1-14. Disponible en: DOI: https://www.doi.org/10.1186/s40035-022-00332-y
St-Pierre MK et al. Astrocytes display ultrastructural alterations and heterogeneity in the hippocampus of aged APP-PS1 mice and human post-mortem brain samples, J Neuroinflammation. [Internet]. 2023;20(1):1-73. Disponible en: DOI: HTTPS://WWW.DOI.ORG/10.1186/S12974-023-02752-7
Garland EF, Hartnell IJ, Boche D. Microglia and As-trocyte Function and Communication: What Do We Know in Humans. Front Neurosci. [Internet]. 2022; 16(824888). Disponible en: DOI: https://www.doi.org/10.3389/fnins.2022.824888
Habib N et al. Disease-associated astrocytes in Alzheimer's disease and aging, Nat Neurosci. [Internet]. 2022;23(6):701-6. Disponible en: DOI: https://www.doi.org/10.1038/s41593-020-0624-8
Zeb S et al. Necroptotic kinases are involved in the reduction of depression-induced astrocytes and fluoxetine's inhibitory effects on necroptotic kinases, Front Pharmacol. [Internet]. 2023;13(1060954). Disponible en: DOI: https://www.doi.org/10.3389/fphar.2022.1060954
Gudkov SV et al. An emerging role of astrocytes in aging/neuroinflammation and gut-brain axis with consequences on sleep and sleep disorders, Aging Res Rev. [Internet] 2023;83(101775). Disponible en: DOI: https://www.doi.org/10.1016/j.arr.2022.101775
Halpern M, Brennand KJ, Gregory J. Examining the relationship between astrocyte dysfunction and neurodegeneration in ALS using hiPSCs. Neurobiol Dis. [Internet]. 2019;132(104562). Disponible en: DOI: https://www.doi.org/10.1016/j.nbd.2019.104562
Leavitt ML, Pieper F, Sachs AJ, Martínez-Trujillo JC. Correlated variability modifies working memory fidelity in primate prefrontal neuronal ensembles. Proc Natl Acad Sci USA. [Internet]. 2017;114(12). Disponible en: DOI: https://www.doi.org/10.1073/pnas.1619949114
Wu N, Sun X, Zhou C, Yan J, Cheng C. Neuroblasts migration under control of reactive astrocyte-derived BDNF: a promising therapy in late neurogenesis after traumatic brain injury. Stem Cell Res Ther. [Internet]. 2023;14(1):1-2. Disponible en: DOI: https://www.doi.org/10.1186/s13287-022-03232-0
Li ZD et al. The divergent effects of astrocyte ceruloplasmin on learning and memory function in young and old mice. Cell Death Dis. [Internet]. 2022;13(11):1-16. Disponible en: https://www.nature.com/articles/s41419-022-05459-4
Verkhratsky A, Nedergaard M. Physiology of Astroglia. Physiol Rev.[Internet]. 2018;98(1):239-389. Disponible en: DOI: https://www.doi.org/10.1152/physrev.00042.2016
Falcone C, Martínez-Cerdeño V. Astrocyte evolution and human specificity. Neural Regen Res. [Internet]. 2023;18(1):1-2. Disponible en: DOI: https://www.doi.org/10.4103/1673-5374.340405
Holt MG. Astrocyte heterogeneity and interactions with local neural circuits. Essays Biochem. [Internet]. 2023;67(1):93-106. Disponible en: DOI: https://www.doi.org/10.1042/EBC20220136
Markey KM, Saunders JC, Smuts J, von Reyn CR, García ADR. Astrocyte development-More questions than answers. Front Cell Dev Biol. [Internet]. 2023;11(1063843). Disponible en: DOI: https://www.doi.org/10.3389/fcell.2023.1063843
Chen J, Poskanze KE, Freeman MR, Monk KR. Live-imaging of astrocyte morphogenesis and function in zebrafish neural circuits. Nat Neurosci. [Internet]. 2020;23(10):1297-1306. Disponible en: DOI: https://www.doi.org/10.1038/s41593-020-0703-x
Szpakowski P, Ksiazek-Winiarek D, Turniak-Kusy M, Pacan I, Glabinski A. Human Primary Astrocytes Differently Respond to Pro- and Anti-Inflammatory Stimuli. Biomedicines. [Internet]. 2022;10(8):1-15. Disponible en: DOI: https://www.doi.org/10.3390/bio-medicines10081769
Forrest SL et al. Distribution Patterns of Astrocyte Populations in the Human Cortex. Neurochem Res. [Internet]. 2023;48(4):1222-1232. Disponible en: DOI: https://www.doi.org/10.1007/s11064-022-03700-2
Schweingruber C, Hedlund E. The Cell Autonomous and Non-Cell Autonomous Aspects of Neuronal Vulnerability and Resilience in Amyotrophic Lateral Sclerosis. Biology. [Internet]. 2022;11(8):1-34. Disponible en: DOI: https://www.doi.org/10.3390/biology11081191
Oda S, Funato H. D1- and D2-type dopamine receptors are immunolocalized in pial and layer I as-trocytes in the rat cerebral cortex. Front Neuroanat. [Internet]. 2023;17(1111008):1-12. Disponible en: DOI: https://www.doi.org/10.3389/fnana.2023.1111008
Liu L, Liu J, Bao J, Bai Q, Wang G. Interaction of Microglia and Astrocytes in the Neurovascular Unit. Front. Immunol. [Internet]. 2020;11(1024):1-11. Disponible en: https://pubmed.ncbi.nlm.nih.gov/32733433/
Gotoh M, Miyamoto Y, Ikeshima-Kataoka H. Astrocytic Neuroimmunological Roles Interacting with Microglial Cells in Neurodegenerative Diseases. IJMS. [Internet]. 2023;24(1599):1-17. Disponible en : DOI: https://www.doi.org/10.3390/ijms24021599
Hartmann K et al. Complement 3+-astrocytes are highly abundant in prion diseases, but their abolishment led to an accelerated disease course and early dysregulation of microglia. Acta neuropathol commun. [Internet]. 2019;7(83):1-15. Disponible en: DOI: https://www.doi.org/10.1186/s40478-019-0735-1
Litvinchuk A et al. Complement C3aR Inactiva-tion Attenuates Tau Pathology and Reverses an Immune Network Deregulated in Tauopathy Models and Alzheimer's Disease. Neuron. [Internet]. 2018;100(6):1337-1353. Disponible en: DOI: https://www.doi.org/10.1016/j.neuron.2018.10.031
Stym-Popper G et al. Regulatory T cells decrease C3-positive reactive astrocytes in Alzheimer-like pathology. J Neuroinflammation. [Internet]. 2023;20(64):1-17. Disponible en: DOI: https://www.doi.org/10.1186/s12974-023-02702-3
Dai N, Jonnes BD, Husain MI. Astrocytes in the neuropathology of bipolar disorder: review of current evidence. Brain Sci. [Internet]. 2022;12(11):1513. Disponible en: DOI: https://doi.org/10.3390/brains-ci12111513
Lanciotti A et al. Megalencephalic Leukoencepha-lopathy with Subcortical Cysts Disease-Linked MLC1 Protein Favors Gap-Junction Intercellular Communication by Regulating Connexin 43 Trafficking in Astrocytes. Cells. [Internet]. 2020;9(6):1425. Disponible en: DOI: https://doi.org/10.3390/cells9061425
Droguerre M et al. A New Tool for in Vivo Study of Astrocyte Connexin 43 in Brain. Sci Rep. [Internet]. 2019;9(1):18292. Disponible en: DOI: https://doi.org/10.1038/s41598-019-54858-9
Dewa KI, Arimura N. Neuronal and astrocytic protein connections and associated adhesión molecules. Neurosci Res. [Internet]. 2023;(187):14-20. Disponible en: DOI: https://doi.org/10.1016/j.neures.2022.09.014
Kofuji P, Araque A. Astrocytes and Behavior. Annu Rev Neurosci. [Internet]. 2021;44(1):49-67, 2021. Disponible en: DOI: https://doi.org/10.1146/annurev-neuro-101920-112225
Rurak GM et al. Sex differences in developmental patterns of neocortical astroglia: A mouse translatome database. Cell Reports. [Internet]. 2022;38(5):110310. Disponible en: DOI: https://doi.org/10.1016/j.celrep.2022.110310
Xin W et al.Ventral midbrain astrocytes display unique physiological features and sensitivity to do-pamine D2 receptor signaling. Neuro psycho pharmacol. [Internet]. 2019;44(2):344-55. Disponible en: DOI: https://doi.org/10.1038/s41386-018-0151-4
Pittolo S et al. Dopamine activates astrocytes in pre-frontal cortex via a1-adrenergic receptors. Cell Reports . [Internet]. 2022;40(13):111426. Disponible en: DOI: https://doi.org/10.1016/j.celrep.2022.111426
Bonifacino T et al. Changes at glutamate tripartite synapses in the prefrontal cortex of a new animal model of resilience/vulnerability to acute stress. Transl Psychiatry. [Internet]. 2023;13(1):62. Disponible en: DOI: https://doi.org/10.1038/s41398-023-02366-w
Nozawa O et al. Necl2/3-mediated mechanism for tripartite synapse formation. Development. [Internet]. 2023;150(4):dev200931. Disponible en: DOI: https://doi.org/10.1242/dev.200931
Yao J et al. A Review of Research on the Association between Neuron-Astrocyte Signaling Processes and Depressive Symptoms. IJMS [Internet]. 2023;24(8,(6985). Disponible en: DOI: https://doi.org/10.3390/ijms24086985
Tan CX, Eroglu C. Cell adhesion molecules regulating astrocyte-neuron interactions. Curr Opin Neurobiol. [Internet]. 2021;(69):170-177. DOI: https://doi.org/10.1016/j.conb.2021.03.015
Blanco-Suárez E, Caldwell ALM, Allen N J. Role of astrocyte-synapse interactions in CNS disorders: Astrocyte-synapse disease. J Physiol. [Internet]. 2017;595(6):1903-1916. Disponible en: doi: https://doi.org/10.1113/JP270988
Nguyen AQ et al. Astrocytic Ephrin-B1 Controls Synapse Formation in the Hippocampus During Learning and Memory. Front Synaptic Neurosci. [Internet]. 2020;12(10). Disponible en: DOI: 10.3389/fnsyn.2020.00010
Viedma-Poyatos Á, González-Jiménez P, Pajares MA, Pérez-Sala D. Alexander Disease GFAP R239C mutant shows increased susceptibility to lipoxidation and elicits mitochondrial dysfunction and oxidative stress. Redox Biol. [Internet]. 2022;55(102415). Disponible en: DOI: https://doi.org/10.1016/j.redox.2022.102415
Gruber T et al. Obesity-associated hyperleptinemia alters the gliovascular interface of the hypothalamus to promote hypertension. Cell Metabolism. [Internet]. 2021;33(6):1155-1170. Disponible en: DOI: https://doi.org/10.1016/j.cmet.2021.04.007
Vincent T et al. Functional Consequences of Neuromyelitis Optica-IgG Astrocyte Interactions on Blood-Brain Barrier Permeability and Granulocyte Recruitment. J Immun. [Internet]. 2008;181(8):5730-5737. Disponible en: DOI: https://doi.org/10.4049/jim-munol.181.8.5730
Toti A et al. Ultramicronized N-palmitoylethanolamine regulates mast cell-astrocyte crosstalk: a new potential mechanism underlying the inhibition of morphine tolerance. Biomolecules. [Internet]. 2023;13(2):233. Disponible en: DOI: https://doi.org/10.3390/biom13020233
Ohno Y, Kunisawa N, Shimizu S. Emerging Roles of Astrocyte Kir4.1 Channels in the Pathogenesis and Treatment of Brain Disease. IJMS. [Internet]. 2021;22(19):10236. Disponible en: DOI: https://doi.org/10.3390/ijms221910236
Li B, Zhang D, Verkhratsky A. Astrocytes in Post-traumatic Stress Disorder. Neurosci Bull. [Internet]. 2022;38(8):953-65. Disponible en: DOI: https://doi.org/10.1007/s12264-022-00845-6
Woo DH et al. Activation of Astrocytic μ-opioid Receptor Elicits Fast Glutamate Release Through TREK-1-Containing K2P CHANNEL IN HIPPOCAM-PAL ASTROCYTES. Front Cell Neurosci. [Internet]. 2018;(12):319. Disponible en: DOI: HTTPS://DOI.ORG/10.3389/FNCEL.2018.00319
Matoba K, Dohi E, Choi EY, Kano S. Glutathione S-transferases Control astrocyte activation and neuronal health during neuroinflammation Front Mol Biosci. [Internet]. 2023;9(1080140). Disponible en: DOI: https://doi.org/10.3389/fmolb.2022.1080140
Andersen JV, Schousboe A, Wellendorph P. Astrocytes regulate inhibitory neurotransmission through GABA uptake, metabolism, and recycling. Essays Biochem. [Internet]. 2023;67(1):77-91. Disponible en: DOI: HTTPS://DOI.ORG/10.1042/EBC20220208
Liu J, Feng X, Wang Y, Xia X, Zheng JC. Astrocytes: GABAceptive and GABAergic Cells in the Brain. Front Cell Neurosci . [Internet]. 2022;16(892497). Disponible en: DOI: https://doi.org/10.3389/fncel.2022.892497
Cheng YT, Woo J, Luna-Figueroa E, Maleki AS, Harmanci AS, Deneen B. Social deprivation induces astrocytic TRPA1- GABA suppression of hippocampal circuits. Neuron. [Internet]. 2023;111(8):1301-1315. Disponible en: DOI: https://doi.org/10.1016/j.neuron.2023.01.015
Von Bohlen V und Halbach. BDNF effects on dendritic spine morphology and hippocampal function. Cell Tissue Res. [Internet]. 2018;373(3):729-741. Disponible en: DOI: https://doi.org/10.1007/s00441-017-2782-x
De Pittà M, Brunel N. Multiple forms of working memory emerge from synapse-astrocyte interactions in a neuron-glia network model. Proc Natl Acad Sci USA. [Internet]. 2022;119(43):1-9. Disponible en: DOI: https://doi.org/10.1073/pnas.2207912119
Padilla-Gil DN. El sueño: fisiología y homeostasis. Rev Colombiana Cienc Anim Recia. [Internet]. 15(1):1-13. DOI: https://doi.org/10.24188/recia.v15.n1.2023.985
Ikoma Y, Takahashi Y, Sasaki D, Matsui K. Properties of REM sleep alterations with epilepsy. Brain. [Internet]. 2023;awac499. Disponible en: DOI: https://doi.org/10.1093/brain/awac499
Henriques VJ, Chiavegato A, Carmignoto G, Gómez-Gonzalo M. Astrocytes Modulate Somatostatin Interneuron Signaling in the Visual Cortex. Cells. [Internet]. 2022;11(9, 1400):1-24. Disponible en: DOI: https://doi.org/10.3390/cells11091400
Eraso-Pichot A, Pouvreau S, Olivera-Pinto A, Gomez-Sotres P, Skupio U, Marsicano G. Endocannabinoid signaling in astrocytes. Glia. [Internet]. 2023;71(1):44-59. Disponible en: DOI: https://doi.org/10.1002/glia.24246
Lawal O, Ulloa Severino FP and Eroglu C. "The role of astrocyte structural plasticity in regulating neural circuit function and behavior", Glia. [Internet]. 2022;70(8):1467-1483. Disponible en: DOI: https://doi.org/10.1002/glia.24191
Domingos C et al. Induced remodeling of astrocytes in vivo by manipulation of astrocytic RhoA activity. Cells. [Internet]. 2023;12(2):331. Disponible en: DOI: https://doi.org/10.3390/cells12020331
Anderson G. Amyotrophic Lateral Sclerosis Pathoe-tiology and Pathophysiology: Roles of Astrocytes, Gut Microbiome, and Muscle Interactions via the Mitochondrial Melatonergic Pathway, with Disruption by Glyphosate-Based Herbicides. IJMS. [Internet]. 2022;24(1):587. Disponible en: DOI: https://doi.org/10.3390/ijms24010587
Kárpáti A et al. Histamine H1 receptor on astrocytes and neurons controls distinct aspects of mouse behavior. Sci Rep. [Internet]. 2019;9(1):16451. Disponible en: DOI: https://doi.org/10.1038/s41598-019-52623-6
Flores Clemente C, Nicolás Vázquez MI, Mera Jiménez E, Hernández Rodríguez M. Inhibition of astro-cytic Histamine N-Methyltransferase as a possible target for the treatment of Alzheimer's disease. Bio- molecules. [Internet]. 2021;26(11,10):1408. Disponible en: DOI: https://doi.org/10.3390/biom11101408
Heard KJ et al. Chronic cortisol differentially impacts stem cell-derived astrocytes from major depressive disorder patients. Transl Psychiatry. [Internet]. 2021;11(1):608. Disponible en: DOI: https://doi.org/10.1038/s41398-021-01733-9
Sa M et al. Hypothalamic GABRA5-positive Neurons Control Obesity via Astrocytic GABA. Neuroscience. [Internet]. 2021. DOI: https://doi.org/10.1101/2021.11.07.467613
Lee JM et al. Generation of Astrocyte-Specific MAOB Conditional Knockout Mouse with Minimal Tonic GABA Inhibition. Exp Neurobiol. [Internet]. 2022;31(3):158-172. Disponible en: DOI: https://doi.org/10.5607/en22016
Sa M, Park G, Lee CJ. Role of Hypothalamic Reactive Astrocytes in Diet-Induced Obesity. Mol Cells. [Internet]. 2022;45(2):65-75. Disponible en: DOI: https://doi.org/10.14348/molcells.2022.2044
Kim S, Pajarillo E, Nyarko-Danquah I, Aschner M, Lee E. Role of Astrocytes in Parkinson's Disease Associated with Genetic Mutations and Neurotoxicants. Cells. [Internet]. 2023;12(4,622):1-19. Disponible en: DOI: https://doi.org/10.3390/cells12040622
De Majo M et al. Granulin loss of function in human mature brain organoids implicates astrocytes in TDP-43 pathology. Stem Cell Rep. [Internet]. 2023;18(3):706-719. Disponible en: https://doi.org/10.1016/j.stemcr.2023.01.012
Brash-Arias D et al. The role of astrocytes with genetic mutations linked to amyotrophic lateral sclerosis. Neurology Perspectives. [Internet]. 2023;3(2):100117. Disponible en: DOI: https://doi.org/10.1016/j.neurop.2023.100117
Voss CM et al. AMP-activated protein kinase (AMPK) regulates astrocyte oxidative metabolism by balancing TCA cycle dynamics. Glia. [Internet]. 2020;68(9):1824-1839. Disponible en: DOI: https://doi.org/10.1002/glia.23808
Hashimoto S et al. Neuronal glutathione loss leads to neurodegeneration involving gasdermin activation. Sci Rep. [Internet]. 2023;13(1):1109. Disponible en: DOI: https://doi.org/10.1038/s41598-023-27653-w
Villa-González M, Martín-López G, Pérez-Álvarez MJ. Dysregulation of mTOR Signaling after Brain Ischemia. IJMS. [Internet]. 2022;23(5):2814. Disponible en: DOI: https://doi.org/10.3390/ijms23052814
Lee S et al. The overexpression of TDP-43 in astrocytes causes neurodegeneration via a PTP1B-media-ted inflammatory response. J Neuroinflammation. [Internet]. 2020;17(1):299. Disponible en: DOI: https://doi.org/10.1186/s12974-020-01963-6
Peng AYT et al. Loss of TDP-43 in astrocytes leads to motor deficits by triggering A1-like reactive phenotype and triglial dysfunction. Proc Natl Acad Sci USA. [Internet]. 2020;117(46):29101-29112. Disponible en: DOI: https://doi.org/10.1073/pnas.2007806117
Kim JH, Rahman MH, Park D, Jo M, Kim HJ, Suk K. Identification of Genetic Modifiers of TDP-43: Inflammatory Activation of Astrocytes for Neuroinflammation. Cells. [Internet]. 2021;10(3):676. Disponible en: DOI: https://doi.org/10.3390/cells10030676
Yang C et al. Low-level overexpression of wild type TDP-43 causes late-onset, progressive neurodegeneration and paralysis in mice. Pandey U, editor. PLoS ONE. [Internet]. 2022;17(2):e0255710. Disponible en: DOI: https://doi.org/10.1371/journal.pone.0255710
Bitar L et al. Inhibition of the enzyme autotaxin reduces cortical excitability and ameliorates the outcome in stroke. Sci Transl Med. [Internet]. 2022;14(641):eabk0135. Disponible en: DOI: https://www.science.org/doi/10.1126/sci-translmed.abk0135
Becker S, Nold A, Tchumatchenko T. Modulation of working memory duration by synaptic and astrocytic mechanisms. PLoS Comput Biol. [Internet]. 2022;18(10):e1010543. Disponible en: DOI: https://doi.org/10.1371/journal.pcbi.1010543
Endle H et al. AgRP neurons control feeding behavior at cortical synapses via peripherally derived lysophospholipids. Nat Metab. [Internet]. 2022;4(6):683-692. Disponible en: DOI: https://doi.org/10.1038/s42255-022-00589-7
Descalzi G, Gao V, Steinman MQ, Suzuki A, Alberini CM. Lactate from astrocytes fuels learning-induced mRNA translation in excitatory and inhibitory neurons", Commun Biol. [Internet]. 2019;2(1):247. Disponible en: DOI: https://doi.org/10.1038/s42003-019-0495-2
Wang H, Kulas JA, Wang C, Holtzman DM, Ferris HA, Hansen SB. Regulation of beta-amyloid production in neurons by astrocyte-derived cholesterol. Proc Natl Acad Sci USA. [Internet]. 2021;118(33):e2102191118. Disponible en: DOI: https://doi.org/10.1073/pnas.2102191118
Phillips GR, Hancock SE, Jenner AM, McLean C, Newell KA, Mitchell TW. Phospholipid Profiles Are Selectively Altered in the Putamen and White Frontal Cortex of Huntington's Disease. Nutrients. [Internet]. 2022;14(10):2086. Disponible en: DOI: https://doi.org/10.3390/nu14102086
Huang AYS et al. Region-Specific Transcriptional Control of Astrocyte Function Oversees Local Circuit Activities. Neuron. [Internet]. 2020;106(6):992-1008. Disponible en: DOI: https://doi.org/10.1016/j.neuron.2020.03.025
Di Castro MA, Volterra A. Astrocyte control of the entorhinal cortex-dentate gyrus circuit: Relevance to cognitive processing and impairment in pathology. Glia. [Internet]. 2022;70(8):1536-1553. Disponible en: DOI: https://doi.org/10.1002/glia.24128
Hong SI et al. Astrocytes in the external globus pallidus coordinate flexibility of action strategy. [Internet]. 2021. Disponible en: Disponible en: https://www.researchsquare.com/article/rs-845991/v1 [Accedido: 4-julio-2023].
Yang JL et al. Transient neurogenesis in ischemic cortex from Sox2 + astrocytes. Neural Regen Res. [Internet]. 2023;18(7):1521. Disponible en: DOI: https://doi.org/10.4103/1673-5374.357910
Albini M, Krawczun-Rygmaczewska A, Cesca F. Astrocytes and brain-derived neurotrophic factor (BDNF). Neurosci Res. [Internet]. 2023. Disponible en: Disponible en: https://linkinghub.elsevier.com/retrieve/pii/S0168010223000354 [Citado el 4 de julio de 2023]
Miranda M, Morici JF, Zanoni MB, Bekinschtein P. Brain-Derived Neurotrophic Factor: A Key Molecule for Memory in the Healthy and the Pathological Brain. Front Cell Neurosci . [Internet]. 2019;13(363). Disponible en: DOI: https://doi.org/10.3389/fn-cel.2019.00363
Koeppen J et al. Functional Consequences of Synapse Remodeling Following Astrocyte-Specific Regulation of Ephrin-B1 in the Adult Hippocampus", J Neurosci. [Internet]. 2018;38(25):5710-5726. Disponible en: DOI: https://doi.org/10.1523/JNEUROSCI.3618-17.2018
Nguyen AQ et al. Astrocytic Ephrin-B1 Controls Excitatory-Inhibitory Balance in Developing Hippo campus. J Neurosci. [Internet]. 2020;40(36):6854-6871. Disponible en: DOI: https://doi.org/10.1523/JNEUROSCI.0413-20.2020
Reitman ME et al. Norepinephrine links astrocytic activity to regulation of cortical state.Nat Neurosci. [Internet]. 2023;26(4):579-593. Disponible en: DOI: https://doi.org/10.1038/s41593-023-01284-w
Delepine C et al. Differential Effects of Astrocyte Manipulations on Learned Motor Behavior and Neuronal Ensembles in the Motor Cortex. J Neurosci. [Internet]. 2023;43(15):2696-2713. Disponible en: DOI: https://doi.org/10.1523/JNEUROSCI.1982-22.2023
Manaserh IH et al. Insulin sensing by astrocytes is critical for normal thermogenesis and body temperature regulation. J Endocrinol. [Internet]. 2020;247(1):39-52. Disponible en: DOI: https://doi.org/10.1530/JOE-20-0052
García-Cáceres C et al. Role of astrocytes, micro-glia, and tanycytes in brain control of systemic metabolism. Nat Neurosci. [Internet]. 2019;22(1):7-14. Disponible en: DOI: https://doi.org/10.1038/s41593-018-0286-y
Estévez Salguero AH. Papel de los astrocitos en la regulación de la homeostasis energética a través de AMPK. Tesis de Doctorado, Universidad de Santiago de Compostela, España. [Internet]. 2022. http://hdl.handle.net/10347/27553
Perea Vega ML. Bases neurobiológicas de los efectos de grelina sobre la plasticidad sináptica hipocampal. Tesis deDoctorado, Universidad Nacional de Córdoba, Argentina. [Internet]. 2022. http://rdu.unc.ar/handle/11086/28272
Varela L et al. Hunger-promoting AgRP neurons trigger an astrocyte-mediated feed-forward au-toactivation loop in mice. J Clin Invest. [Internet]. 2021;131(10):e14423. Disponible en: DOI: HTTPS://DOI.ORG/10.1172/JCI144239
Perea G et al. Dysfunctional serotonergic neuronas-trocyte signaling in depressive-like states. [Internet]. 2023. Disponible en: Disponible en: https://www.researchsquare.com/article/rs-2361503/v1 [citado el 4 de julio de 2023]
Pellegrino G et al. GnRH neurons recruit astrocytes in infancy to facilitate network integration and sexual maturation. Nat Neurosci. [Internet]. 2021;24(12):1660-1672. Disponible en: DOI: https://doi.org/10.1038/s41593-021-00960-z
Prevot V, Sharif A. The polygamous GnRH neuron: Astrocytic and tanycytic communication with a neuroendocrine neuronal population. J Neuroendocrinology. [Internet]. 2022. Disponible en: Disponible en: https://onlinelibrary.wiley.com/doi/10.1111/jne.13104 [Citado el 4 de julio de 2023].
Clayton RW, Lovell-Badge R and Galichet C. The Properties and Functions of Glial Cell Types of the Hypothalamic Median Eminence. Front Endocrinol. [Internet]. 2022;13(953995). Disponible en: DOI: https://doi.org/10.3389/fendo.2022.953995/full
Baudon A et al. Emerging role of astrocytes in oxytocin-mediated control of neural circuits and brain functions. ProgNeurobiol. [Internet]. 2022;7(102328). Disponible en: DOI: https://doi.org/10.1016/j.pneuro-bio.2022.102328
Benedet AL et al. Differences Between Plasma and Cerebrospinal Fluid Glial Fibrillary Acidic Protein Levels Across the Alzheimer Disease Continuum. JAMA Neurol. [Internet]. 78, n.° 12,1471, 2021. DOI: https://doi.org/10.1001/jamaneurol.2021.3671
Zysk M et al. Amyloid-ß accumulation in human astrocytes induces mitochondrial disruption and changed energy metabolism. J Neuroinflammation. [Internet]. 2023;20(1,43). Disponible en: DOI: https://doi.org/10.1186/s12974-023-02722-z
Philippot C et al. Astrocytes and oligodendrocytes in the thalamus jointly maintain synaptic activity by supplying metabolites. Cell Reports . 2021;34(3):108642. Disponible en: DOI: https://doi.org/10.1016/jxel-rep.2020.108642
Su Y et al. Astrocyte endfoot formation controls the termination of oligodendrocyte precursor cell perivascular migration during development. Neuron. [Internet]. 2023;111(2):190-201. Disponible en: DOI: https://doi.org/10.1016/j.neuron.2022.10.032
Hu X, Yu G, Liao X, Xiao L. Interactions Between Astrocytes and Oligodendroglia in Myelin Development and Related Brain Diseases. Neurosci Bull. [Internet]. 2023;39(3):541-552. Disponible en: DOI: https://doi.org/10.1007/s12264-022-00981-z
Hasan M et al. Chemogenetic activation of astrocytes promotes remyelination and restores cognitive deficits in visceral hypersensitive rats. iScience. [Internet]. 2023;26(1):105840. Disponible en: DOI: https://doi.org/10.1016/j.isci.2022.105840
Miyata S. Glial functions in the blood-brain communication at the circumventricular organs. Front Neurosci. [Internet]. 2022;16(991779). Disponible en: DOI: https://doi.org/10.3389/fnins.2022.991779
Lohr C. Role of P2Y receptors in astrocyte physiology and pathophysiology. Neuropharmacology. [Internet]. 2023;223(109311). Disponible en: DOI: https://doi.org/10.1016/j.neuropharm.2022.109311
Launay A et al. The role of adenosine A2A receptors in Alzheimer's disease and tauopathies. Neuropharmacology. [Internet]. 2023;226(109379). Disponible en: DOI: https://doi.org/10.1016/j.neuro-pharm.2022.109379
García CP, Licht-Murava A, Orr AG. Effects of adenosine A2A receptors on cognitive function in health and disease. [Internet]. 2023. Disponible en: Disponible en: https://linkinghub.elsevier.com/retrieve/pii/S0074774223000211 [Citado el 4 de julio de 2023].
Torres-Ramos MA, Morales-López BI. Neuroinflamación mediada por los astrocitos en el envejecimiento y la neurodegeneración a través del factor nuclear Kß y el receptor de hidrocarburos de arilo. Neurobiología. 2022;13(22):1-12.
Simpson Ragdale H et al. Injury primes mutation-bearing astrocytes for dedifferentiation in later life. Curr Biol, [Internet]. 2023;33(6):1082-1098. Disponible en: DOI: https://doi.org/10.1016/j.cub.2023.02.013
Notas
