Artículos
Efectos de la dexmedetomidina en el tratamiento del síndrome de abstinencia por enfermedad adictiva
The effects of dexmedetomidine for the treatment of abstinence syndrome secondary to addictive disease
Efectos de la dexmedetomidina en el tratamiento del síndrome de abstinencia por enfermedad adictiva
Revista de Toxicología, vol. 36, núm. 2, pp. 160-165, 2019
Asociación Española de Toxicología

Esta obra está bajo una Licencia Creative Commons Atribución 4.0 Internacional.
Resumen: El manejo del síndrome de abstinencia está relacionada con cambios cardiovasculares y síntomas disautonómicos que dificultan el tratamiento. La dexmedetomidina es una opción por tener mejor perfil de seguridad. El objetivo de este estudio es describir el grado de agitación y comportamiento cardiorespiratorio de los pacientes con síndrome de abstinencia por enfermedad adictiva manejados con infusión de dexmedetomidina. Estudio de cohorte retrospectivo, se incluyeron pacientes con enfermedad adictiva en proceso de desintoxicación manejados en unidad de cuidados intensivos con infusión de dexmedetomidina. Se realizó un análisis de supervivencia para determinar el tiempo a control del evento con estratificación por el tipo de sustancia y comportamiento cardiovascular. Se incluyeron 83 pacientes, 71 (85,5%) de sexo masculino, con edad mediana de 29 años (RIQ 25–36). Las principales sustancias primarias de adicción fueron heroína (n=25), basuco (n=16) y cannabinoides (n=15). La causa principal de ingreso a unidad de cuidados intensivos fue la disautonomía (n=47). El análisis de supervivencia mostró que se logró el control de la agitación al octavo día en 75% de los pacientes, con un control al quinto día mayor para el grupo opioides-cannabinoides (60%) vs alcohol-benzodiacepinas (20%). El 31,6% presentaron bradicardias asintomáticas durante la infusión de dexmedetomidina. La dexmedetomidina resultó ser un fármaco útil y seguro para controlar la agitación en pacientes con síndrome de abstinencia. Los resultados fueron diferentes en los grupos de cannabinoides y derivados del basuco y los de alcohol y benzodiacepinas. Los efectos cardiovasculares en los pacientes evaluados no requirieron soporte hemodinámico adicional.
Palabras clave: Dexmedetomidina, adicción, síndrome de abstinencia, agonistas de receptores adrenérgicos alfa 2, unidad de cuidado intensivo.
Abstract: The management of abstinence syndrome is associated with cardiovascular derangements and autonomic symptoms making treatment difficult. Dexmedetomidine is an option because of a beneficial safety profile. To describe the degree of agitation and cardiorespiratory behavior of patients with abstinence syndrome secondary to addictive disease managed with an infusion of dexmedetomidine. Retrospective cohort study, patients with additive disease were included during the phase of detoxification treatment managed in the intensive care unit with dexmedetomidine infusion. A survival analysis was carried out to determine the time to symptom control stratified by type of substance and cardiovascular behavior. A total of 83 patients were included, 71 (85,5%) were male sex, median age of 29 years (IQR 25-36). The primary substances were heroin (n=25), basuco (n=16) and cannabinoids (n=15). The most frequent cause of admission to intensive care was dysautonomia (n=47). Survival analysis showed that control of agitation was achieved on the fifth day for the group opioid-cannabinoids (60%) vs. alcohol-benzodiazepines (20%). Bradycardia occurred in 31,6% of patients during dexmedetomidine infusion. Dexmedetomine resulted to be a useful and safe drug to control agitation in patients with abstinence syndrome. The results were different between the groups cannabinoids and basuco derivatives and those for alcohol and benzodiazepines. The cardiovascular effects in the studied patients did not prompt additional hemodynamic support.
Keywords: Dexmedetomidine, addiction, withdrawal syndrome, alpha 2 adrenergic receptor agonists, intensive care unit.
Introducción
La enfermedad adictiva es una patología crónica de difícil control y manejo, cuya historia natural se asocia frecuentemente con recaídas. Las drogas de abuso inducen estados placenteros o alivian la angustia, que al parecer es el efecto deseado por el paciente adicto.
Su uso continuo induce cambios adaptativos, funcionales y morfológicos a nivel celular del sistema nervioso central conduciendo a tolerancia, dependencia física y psicológica (Camí y Farré, 2003).
La rehabilitación del paciente con farmacodependencia se ha reducido a procedimientos de suplencia y a terapia conductual que aparentemente simplifican el problema.
Durante los últimos años, diferentes trabajos han demostrado la seguridad de dexmedetomidina por periodos prolongados, así como nuevas indicaciones derivadas del beneficio de mantener una respiración espontánea y disminuir la frecuencia de delirio, cuando se compara con otros medicamentos como midazolam o propofol (Maldonado et al., 2009; Afonso y Reis, 2013; Wong et al., 2015).
En el manejo integral del paciente con síndrome de abstinencia, dentro de un programa de rehabilitación en un centro de cuarto nivel, se ha empleado un manejo escalonado, con el inicio de la terapia fundamentado en las benzodiacepinas, haloperidol, buspirona, clonidina y ácido valpróico.
El seguimiento durante 5 años, mostró una dificultad en el control de la agitación, con la limitación por las altas dosis requeridas, que inducían cambios de tipo cardiovascular y ventilatorio antes de obtener el efecto deseado.
Como una intervención opcional, se consideró el uso dentro del protocolo la infusión de dexmedetomidina, con un seguimiento en la unidad de cuidados intensivos, en busca de estimar la posibilidad de alteraciones cardiovasculares relacionadas que ameritaran intervención. El objetivo de este artículo es describir los resultados de la terapia a partir de un seguimiento continuo de las variables cardiovasculares, las dosis y los resultados clínicos obtenidos.
Materiales y métodos
Se realizó un estudio con enfoque cuantitativo, analítico, de tipo cohorte retrospectiva, en el cual se revisaron los registros clínicos de todos los pacientes incluidos en la base de datos del servicio de toxicología que fueron atendidos en los pisos de hospitalización en una institución de cuarto nivel, con un programa especial de tratamiento de la adicción en un periodo de cuatro años.
Se incluyeron todos los pacientes con episodios de agitación relacionados con síndrome de abstinencia, por la suspensión de sustancias adictivas entre los grupos de alcohol, benzodiacepinas, cannabinoides, cocaína y sus derivados, hidrocarburos y opioides.
En todos los pacientes se documentó el manejo inicial en el piso de hospitalización con benzodiacepinas intravenosas, alfa 2 agonistas orales, buspirona, carbamazepina y haloperidol a dosis altas, que fallaron en el control adecuado y requirieron manejo en la unidad de cuidados intensivos para la prescripción de dexmedetomidina, en conjunto con otros medicamentos orales.
Se excluyeron del análisis, los pacientes sin criterios de diagnóstico toxicológico o ausencia de seguimiento clínico o cardiovascular.
Una vez seleccionada la muestra, se extrajo la información clínica consignándola en una nueva base de datos de Excel. ® y el análisis estadístico se desarrolló en Stata 14.0 ®
Con el fin de proteger la identidad de los pacientes, se modificó la misma, cambiándola por un número entero de dos dígitos que se convirtió en el código principal para el seguimiento y el enlace de los datos.
Para el análisis de las variables continuas se presentan a través de medidas de tendencia central y dispersión, previo análisis de la distribución de cada una de ellas.
Las variables de tipo categórico, se presentan como porcentaje, en relación con el total de la cohorte.
Para la interpretación del control de la agitación, se desarrolló un análisis de sobrevida, presentándola a partir de la metodología de Kaplan y Meier.
Se definió como fallo si no se lograba control de la agitación y delirio durante el seguimiento de 15 días a partir del día de ingreso a la unidad de cuidados intensivos. La evaluación para el control de la agitación y del delirio fue clínica.
Los pacientes que no presentaron control de la agitación en este periodo o no completaron el tiempo de seguimiento por pérdida de la información, se definieron como censuras.
Se estratificaron los pacientes por cada una de las sustancias principales según el grupo toxicológico así: grupo 1 cocaína - basuco, grupo 2 benzodiacepina – alcohol, grupo 3 opiáceos y sus derivados, grupo 4 cannabinoides y grupo 5 ketamina - hidrocarburos. Para hacer el análisis del tiempo hasta control del delirio se reunieron los datos en dos grupos, un grupo 1, que describe el comportamiento de los pacientes con adicción al alcohol y benzodiacepinas y el grupo 2, en el cual se incluyeron, los adictos a cannabinoides, opioides, cocaína y basuco.
Para establecer la significancia de la diferencia entre los dos grupos se desarrolló una prueba del logaritmo del intervalo, (Log Rank Test) con un valor de p < 0,05 como punto de corte.
Para el análisis cardiovascular, se revisó el registro de evaluación de signos vitales horario por parte del grupo de enfermería en la unidad de cuidados intensivos. Se determinó el valor de cada hora de las variables, frecuencia cardiaca, presión arterial media, dosis de dexmedetomidina, dosis de benzodiacepinas. Así mismo se identificó el uso de agentes vasopresores y la necesidad de barbitúricos usados por dificultad en el control durante la estancia en la UCI. Otras variables analizadas fueron la frecuencia y el tiempo de uso del soporte ventilatorio y la dosis administrada antes del ingreso a la unidad de agonistas alfa 2 y benzodiacepinas.
El protocolo fue evaluado por el comité de ética de investigación de la Fundación Universitaria de Ciencias de la Salud (FUCS), que lo consideró, de acuerdo en la Resolución 8430 de 1993, como un estudio sin riesgo, por lo cual no se solicitó consentimiento informado.
En respeto de la confidencialidad de la historia clínica, la identificación de cada paciente se realizó mediante un número de registro en el protocolo, el cual no forma parte del registro clínico y no permite determinar la identidad de los pacientes.
Resultados
Durante el periodo definido para el análisis se obtuvieron los registros clínicos completos de 83 pacientes, que cumplían los criterios de selección.
La descripción de las variables demográficas se presenta en la tabla 1.
| N | % | |
| Total de Pacientes | 83 | |
| -Edad | ||
| Mediana | 31 | |
| Rango intercuartilico | 25 - 36 | |
| Min – Max | 14 - 70 | |
| Sexo | ||
| Masculino | 71 | 85,5 % |
| Estado civil | ||
| Soltero | 53 | 63,8 % |
| Casado | 17 | 20,4 % |
| Unión libre | 5 | 6 % |
| Separado | 3 | 3,6 % |
| No especificado | 5 | 6,02 % |
| Apoyo familiar | ||
| Si | 66 | 79,5 % |
Se observó el predominio de la enfermedad adictiva en los pacientes de sexo masculino, solteros menores a 40 años. El análisis del soporte familiar se consideró relevante dada la importancia dentro del proceso integral de rehabilitación. En su mayoría, los pacientes contaron con este tipo de acompañamiento durante la terapia, sin encontrar diferencias en el control de la agitación cuando se comparó con el grupo en quienes no se obtuvo.
La tabla 2 incluye los datos relacionados con las sustancias psicoactivas y el tiempo de consumo. La sustancia primaria de adicción fue principalmente heroína seguida por basuco y cannabinoides; con respecto al tiempo de consumo se encontró una mediana de 9 años para el grupo total de pacientes.
| Nº | % | |
| Heroína | 25 | 30,1 % |
| Basuco | 16 | 19,2 % |
| Cannabinoides | 15 | 18% |
| Cocaína | 8 | 9,6 % |
| Opiáceos | 8 | 9,6 % |
| Alcohol | 5 | 6% |
| Benzodiacepina | 4 | 4,8 % |
| Hidrocarburos | 1 | 1,2 % |
| Ketamina | 1 | 1.2 % |
| Tiempo de adicción (años) | ||
| Mediana | 9 | |
| Rango intercuartilico | 5 – 16 |
La sustancia primaria de adicción en los dos sexos fue la heroína, seguida por cocaína y derivados en hombres, sin encontrar diferencia significativa en la incidencia de consumo de otras drogas en el grupo de las mujeres.
Respecto a la edad relacionada con el consumo, se observó que existen diferencias en la droga primaria de adicción dependiendo del grupo etario, con predominio en el consumo de cocaína, basuco y cannabinoides en jóvenes y el alcohol y benzodiacepinas en personas mayores.
El motivo principal que justificó el ingreso a UCI fue la disautonomía no controlada, seguida del riesgo de falla ventilatoria relacionada con las dosis altas de benzodiacepinas. Las dos indicaciones corresponden al 81,9% del total de las causas de ingreso (tabla 3).
| N | % | |
| Disautonomía | 47 | 56,6 % |
| Riesgo de falla ventilatoria | 21 | 25,3 % |
| Sepsis | 8 | 9,6 % |
| Dolor Torácico | 6 | 7,2 % |
| Trauma Craneoencefálico | 1 | 1,2% |
La mitad de los pacientes que ingresaron a la unidad tenían más de 10 días de hospitalización, la estancia en UCI fue inferior a 8 días en el 75% de los pacientes, y el tiempo de hospitalización en estancia general luego del egreso de la unidad tuvo una mediana de 10 días.
| Días de estancia previo ingreso a UCI | |
| Mediana | 10 |
| Rango intercuartílico | 5 – 14 |
| Min – Max | 0 – 34 |
| Días de Estancia en UCI | |
| Mediana | 5 |
| Rango intercuartílico | 3 – 8 |
| Min – Max | 1 – 21 |
| Días de Estancia posterior a egreso de UCI | |
| Mediana | 10 |
| Rango intercuartílico | 5 – 16 |
| Min – Max | 0 – 36 |
| Días de hospitalización total | |
| Mediana | 26,5 |
| Rango intercuartílico | 22 – 37 |
| Min – Max | 9 – 65 |
La comparación de la estancia entre los grupos diagnósticos, solo demostró diferencia en un paciente con dolor torácico desde el ingreso quien requirió procedimientos adicionales relacionados con la probabilidad de enfermedad coronaria. (tabla5).
Comparando la sustancia primaria de adicción con la estancia en UCI encontramos que el grupo alcohol y benzodiacepinas tubo en promedio una mayor estancia en relación a los pacientes que consumen cocaína, opiáceos y cannabinoides. (Tabla 6).
El tiempo de control de la agitación, cuantificado desde el inicio de la infusión, fue de 8 días en el 75 % de los pacientes (Fig. 1), observando una diferencia significativa, a favor de los grupos de canabinoides, derivados del basuco y heroína, control en el día 5 en el 50 % de los pacientes. Menos del 25 % en los grupos de alcohol y benzodiacepinas (Fig. 2).
| Mediana | RIQ | |
| Riesgo de falla ventilatoria | 7 | 9 |
| Trauma Craneoencefálico | 7 | 0 |
| Sepsis | 6,5 | 4 |
| Dolor Torácico | 4,5 | 1 |
| Disautonomía | 4 | 5 |
| Grupo | Promedio Días | Min - Max Días |
| 1 | 4 | 2 – 19 |
| 2 | 7 | 3 – 13 |
| 3 | 5 | 1 -18 |
| 4 | 4 | 1- 21 |
| 5 | 7,5 | 2 – 13 |

Figura 1
Tiempo hasta control del delirio.
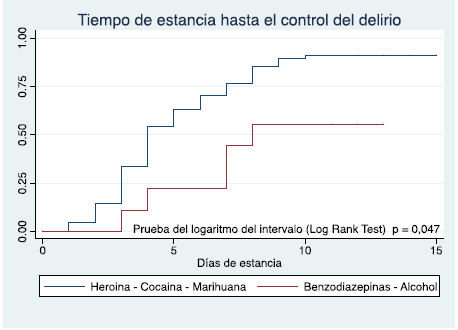
Figura 2
Tiempo hasta control del delirio según grupos de consumo.
Para el análisis del seguimiento cardiovascular, se evaluó el registro de enfermería de cada hora durante un tiempo acumulado de 546 días. La frecuencia cardiaca fue caracterizada como bradicardia cuando el valor fue inferior a 55 latidos por minuto, observando al menos un episodio en el 49 % de los días analizados. El 31,6 % de estos episodios aparecieron durante la infusión de dexmedetomidina, mientras que el 17,2 % apareció sin la administración del medicamento, con una diferencia estadísticamente significativa p = 0,001, (Tabla 7).
| Días de estancia | Reporte de bradicardia FC <55lxm | ||
| No bradicardia | Infusión de dexmedetomidina | Sin dexmedetomidina | |
| 1 | 35 | 18 | 30 |
| 2 | 31 | 42 | 10 |
| 3 | 33 | 36 | 8 |
| 4 | 24 | 29 | 9 |
| 5 | 20 | 20 | 8 |
Adicionalmente, se evaluó el comportamiento de la frecuencia cardiaca, estratificando los grupos de acuerdo a la dosis administrada en 24 horas. Se clasificaron los pacientes en 3 estratos infusión de 100 a 400 mcg/día, con una mediana de 72 lat/min y un rango intercuartílico de 26, dosis mayores de 400 mcg/día 75 latidos/min rango intercuartílico de 27,5 y los que no recibieron el medicamento con un valor de 78 latidos/ min rango intercuartílico de 31. La diferencia no fue estadísticamente significativa p = 0,04. (Fig. 3)
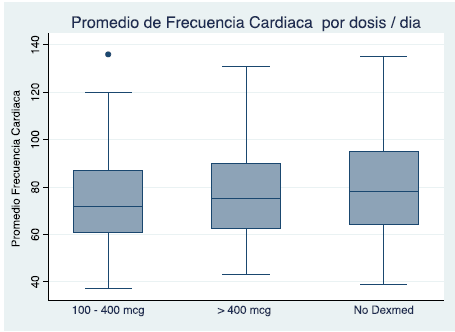
Figura 3
Diagrama de cajas y bigotes de la mediana de la frecuencia cardiaca según la dosis de dexmedetomidina día.
No se encontró relación entre eventos de bradicardia e hipotensión severa. Ningún evento de bradicardia requirió manejo farmacológico o con marcapasos.
Con el fin de evaluar el efecto cardiovascular de los fármacos que recibían en el piso de hospitalización general, se evaluó el comportamiento de la frecuencia cardiaca, durante el primer día de estancia, en el cual no todos los pacientes reciben infusión de dexmedetomidina.
En este grupo se observó en el 89,1 % de los pacientes la administración de clonidina a una dosis promedio de 1200 mcg por día y la infusión de midazolam en el 96,3 % a una dosis promedio de 120 mg/día. No se observaron diferencias estadísticamente significativas. P= 0,04.
En los pacientes con dosis más altas, requirieron con más frecuencia traslado a la UCI.
Ningún paciente requirió electroestimulación con marcapaso y la hipotensión arterial no fue indicación de soporte presor.
En 14 pacientes se inició soporte ventilatorio mecánico, 8 de ellos por imposibilidad de controlar el delirio y con la necesidad de coma barbitúrico. Los 6 restantes, tuvieron causas diferentes.
En el grupo de los pacientes con falla en el control del delirio, 3 tenían adicción a la heroína, 2 al basuco, 2 a cannabinoides y 1 a cocaína.
La mediana del tiempo de estancia fue de 15,5 días, mínimo de 6 días máximo de 21 días con un rango intercuartílico de 6.
Discusión
La adicción a sustancias psicoactivas incluido el alcohol, es un problema de salud pública que trasciende del ámbito clínico al entorno social, económico y político.
El análisis epidemiológico demuestra una frecuencia cada vez mayor en el consumo que a su vez aparece en poblaciones más jóvenes, incluyendo infantes.
De acuerdo con el Informe Mundial sobre las Drogas del 2016 se calcula que 5 de cada 100 personas, entre la segunda y séptima década de la vida, consumieron drogas por lo menos una vez en el 2014 y que más de 29 millones de ellos padecen patologías que han sido asociadas con el consumo como el VIH, la hepatitis B y C y tuberculosis, entre otras.
La mortalidad relacionada con uso de sustancias psicoactivas (SPA) para el 2014 fue de 43,5 muertes por millón de personas y de estas la mitad pudo corresponder a sobredosis y aunque la cifra no incrementó en el 2016 mantiene un valor excesivamente alto y alarmante (World Drug Report, 2015).
En cuanto a la economía, el efecto del consumo de SPA, se ha relacionado con un incremento mundial en el porcentaje destinado para la intervención ya sea en fases tempranas de prevención y promoción o en fases tardías en el tratamiento, dejando de lado las cifras asignadas al control en la producción y distribución (World Drug Report, 2015).
En Colombia según el reporte de drogas del 2015, para el año 2012 el 15,01% de la población había consumido por lo menos una vez en la vida, La mayor frecuencia se vio en hombres menores de 40 años (Plan decenal de salud pública, 2013; Estudio nacional de consumo de sustancias psicoactivas en Colombia, 2013).
La distribución del tipo de sustancia utilizado, de acuerdo al sexo demuestra la predilección de los hombres por el cannabis y las anfetaminas, mientras que en las mujeres, es predominante el uso de antidepresivos y benzodiacepinas, relacionados con enfermedad depresiva.
Por grupo de edad, la predilección por el alcohol y los benzodiacepinas predominó en mayores de 40 años, posiblemente por exposición a otras alternativas en pacientes más jóvenes. La misma explicación se relaciona con los tiempos de adicción, que son más largos en este grupo (Sessler y Verney, 2008; Estudio nacional de consumo de sustancias psicoactivas en Colombia, 2013).
La severidad del cuadro desde la perspectiva clínica queda representada en el tiempo de estancia que se requiere para obtener el control de la agitación. En el estudio no se ha definido la frecuencia del reingreso y no se estimó el tiempo que puede tardar la reinserción dentro de un programa laboral o el retorno a la vida familiar.
El tiempo de estancia de 26 días, supera en más de tres veces el de las patologías de mayor frecuencia. Esto implica un mayor costo de atención en este grupo de pacientes por mayores requerimientos para su control y por supuesto la mayor probabilidad de complicaciones que se presentaron en el 10% de la cohorte.
La atención de 8 días en cuidados intensivos, adquiere también relevancia, no solo por las dificultades intrínsecas a la unidad, sino la falta de recursos para el manejo del paciente agitado de difícil control en comparación con centros de salud mental.
El análisis del costo no fue objeto de este trabajo, pero consideramos que su estimación es relevante dentro del marco gubernamental de control del consumo de drogas.
Dados los criterios con que se seleccionaron los pacientes, la totalidad de la cohorte presentó fallo terapéutico a la intervención de primera línea en el protocolo institucional. Es relevante la mínima relación encontrada entre la dosis administrada de benzodiacepinas y de agonistas alfa orales, con la presencia de eventos adversos.
El efecto cardiocirculatorio de las altas dosis, se estimó por las variables en el primer día de estancia en la UCI. La tercera parte de los pacientes recibieron Dexmedetomidina en infusión, sin presentar diferencias en la frecuencia cardiaca.
El uso de la dexmedetomidina, descrito hace más de veinte años, resulta más útil para facilitar el destete ventilatorio y en algunos casos para el control del dolor o el delirio. En anestesia como adyuvante en algunos procedimientos que requieren la cooperación del paciente o por seguridad ya que no produce depresión respiratoria.
Otros factores considerados como beneficios de este fármaco, se relacionan con la protección miocárdica de la isquemia derivada de una alta carga adrenérgica y la menor frecuencia de delirio en la población de pacientes mayores. Estos efectos, parecen relacionarse con reducción de la estancia en la unidad de cuidados intensivos y en algunas series, en el tiempo de ventilación mecánica.
En los pacientes con agitación relacionada con abstinencia, el cuadro comparte características con el delirio. En la medida en que se han administrado dosis más altas de benzodiacepinas, los cambios en el comportamiento y la percepción de la realidad, se modifica a un punto en que podría clasificarse como un cuadro psicótico. Ante esta situación, los agonistas alfa 2, tienen como principal ventaja, la baja probabilidad de depresión respiratoria, con menos frecuencia de ventilación mecánica y el mantenimiento de los reflejos de protección de la vía aérea, lo que confiere un perfil de seguridad más alto.
El análisis del comportamiento ventilatorio de los pacientes estudiados, confirma la descripción, sin que se presentara durante el seguimiento, ningún episodio de depresión respiratoria que ameritara el control de la vía aérea y el inicio de ventilación mecánica. En los pacientes ventilados que en total fueron el 8 %, la falla en el control de la agitación y la necesidad de una tercera línea de manejo con tiopental sódico, fueron las causas de intubación y soporte con ventilación mecánica.
El uso de altas dosis de dexmedetomidina se ha relacionado con cambios cardiovasculares que tienen el potencial de ocasionar deterioro hemodinámico. En el seguimiento de las variables analizadas, se confirma una menor frecuencia cardiaca en el grupo que recibe la infusión, lo cual es esperado, sin necesidad de soporte con electro estimulación o manejo farmacológico. Llama la atención que no se observó diferencia entre las dosis administradas y el requerimiento de presores que se mantuvo en el grupo de pacientes sépticos. El requerimiento se atribuyó más a la morbilidad infecciosa que de la administración del medicamento.
En cuanto al control del cuadro de agitación, se observa que la mayor parte de los pacientes mejoran al día 8 de tratamiento. Es evidente la diferencia entre los adictos al alcohol y benzodiacepinas comparada con el resto de sustancias. Se obtuvo mejor resultado en los grupos de cannabinoides y derivados del basuco. Es imposible excluir que el tiempo de adicción más que el grupo farmacológico sea la causa de la diferencia en el resultado, considerando este análisis como un futuro objetivo de investigación.
Conclusión
El manejo de la agitación relacionada con el síndrome de abstinencia con la infusión continua de dexmedetomidina parece ser de utilidad, con especial beneficio en pacientes sin protección de la vía aérea, por sus características. En la cohorte se observó un mejor resultado en los grupos con adicción a cannabinoides, cocaína y heroína que en los grupos de alcohol y benzodiacepinas, sin descartar que el tiempo de adicción sea el factor determinante. Los efectos cardiovasculares son evidentes, con una menor frecuencia cardiaca en los días en que se emplea el medicamento, pero no se observó ningún evento grave que ameritara intervención.
En Hospital Infantil de San José la desintoxicación y manejo del delirio secundario a síndrome de abstinencia en los pisos, se basa en benzodiacepinas endovenosas, asociado a alfa 2 agonistas orales, como se recomienda en la literatura. El uso de dexmedetomidina en pacientes con enfermedad adictiva para control de la agitación en desintoxicación tiene poco soporte en la literatura; al respecto, hay reportes de casos de pacientes alcohólicos para el control del síndrome de abstinencia y pacientes en POP que requirieron manejo prolongado con benzodiacepinas y opioides para sedación con fines de acople a ventilación mecánica o control del dolor, no encontramos reportes de uso de dexmedetomidina para manejo de enfermedad adictiva a drogas como la cocaína, cannabinoides, basuco, heroína, hidrocarburos o ketamina (Reoux y Miller, 2000; Rovasalo et al., 2006; Darrouj et al., 2008; Maldonado, 2009; Reade et al., 2009; Riker et al., 2009; Kawaai et al., 2010; Rayner et al., 2012; Ferreira et al., 2015).
De acuerdo con nuestros resultados el control del delirio y la agitación, ocurrió en el 75% de los pacientes al octavo día de manejo.
.Aunque en el momento la FDA autoriza el uso de dexmedetomidina en salas de cirugía y UCI para sedación (Angst et al., 2004) en máximo 24h (Venn et al., 2003; Beg et al., 2016) existen múltiples estudios donde se ha superado este límite, incluso llegando a usarla hasta por 30 días, sin reportar eventos adversos mayores( Riker et al., 2009; VanderWeide et al., 2016).
De acuerdo con lo que reporta la literatura el evento cardiovascular más frecuente es la bradicardia (Bhana et al., 2000; Drummond et al., 2008; Wong et al., 2015) , lo cual también concuerda con lo encontrado en nuestro estudio, no tuvimos ningún reporte de bradicardias severas con descompensación hemodinámica que requiriera manejo farmacológico o con marcapasos.
De los 83 pacientes 8 requirieron escalonar el manejo a coma barbitúrico con soporte ventilatorio por no control de la agitación con dexmedetomidina, lo cual aumenta el tiempo de estancia en UCI, se encontró que las drogas de consumo de estos 8 pacientes fueron el basuco, la heroína, la cocaína y los cannabinoides, sin reportar requerimiento de usos de barbitúricos con alcohol y benzodiacepinas, lo que podría indicar que el alcohol y las benzodiacepinas podrían requerir mayor tiempo para control de la agitación pero con cuadro menos severo en comparación con las otras drogas según lo encontrado con la curva de supervivencia, en la cual se reporta un tiempo menor en días hasta el control de la agitación para opioides y cannabinoides vs alcohol y benzodiacepinas. (Woods et al., 2015)
Creemos que el uso de la dexmedetomidina en los pacientes en proceso de desintoxicación con antecedente de enfermedad adictiva es una opción segura y con mejores resultados en el control de la agitación, que puede disminuir los tiempos de hospitalización y los eventos adversos cardiovasculares y respiratorios secundarios a las altas dosis de medicamentos que se usan de rutina en estos casos
Se requieren más estudios prospectivos que soporten con mayor fortaleza nuestros hallazgos.
Agradecimientos
Agradecemos a la división de investigación de la Fundación Universitaria de Ciencias de la Salud por su asesoría metodológica.
Conflicto de intereses
Los autores declaran que no tienen ningún conflicto de interés respecto a los resultados de este artículo
Financiación
Este estudio no tuvo financiación
Bibliografía
1 Afonso J, Reis F. Dexmedetomidina: papel atual em anestesia e cuidados intensivos. Revista Brasileira de Anestesiologia. 2012;62:125-33.
2 Angst MS, Ramaswamy B, Davies MF, Maze M. Comparative analgesic and mental effects of increasing plasma concentrations of dexmedetomidine and alfentanil in humans. Anesthesiology. 2004;101(3):744-52.
3 Beg M, Fisher S, Siu D, Rajan S, Troxell L, Liu VX. Treatment of Alcohol Withdrawal Syndrome with and without Dexmedetomidine. Perm J. 2016 Spring;20(2):49-53
4 Bhana N, Goa KL, McClellan KJ. Dexmedetomidine. Drugs. 2000;59(2):263-8.
5 Camí J, Farré M. Drug addiction. N Engl J Med. 2003;349(10):975-86.
6 Darrouj J, Puri N, Prince E, Lomonaco A, Spevetz A, Gerber DR. Dexmedetomidine infusion as adjunctive therapy to benzodiazepines for acute alcohol withdrawal. Ann Pharmacother. 2008;42(11):1703-5.
7 Drummond JC, Dao AV, Roth DM, Cheng CR, Atwater BI, Minokadeh A, et al. Effect of dexmedetomidine on cerebral blood flow velocity, cerebral metabolic rate, and carbon dioxide response in normal humans. Anesthesiology. 2008;108(2):225- 32.
8 Ferreira JA, Wieruszewski PM, Cunningham DW, Davidson KE, Weisberg SF. Approach to the Complicated Alcohol Withdrawal Patient. J Intensive Care Med. 2017 Jan;32(1):3-14. Epub 2015 Oct
9 Kawaai H, Satoh J, Watanabe M, Kan K, Ganzberg S, Yamazaki S. A comparison of intravenous sedation with two doses of dexmedetomidine: 0.2 µg/kg/hr Versus 0.4 µg/kg/hr. Anesth Prog. 2010;57(3):96-103.
10 Kreek MJ, LaForge KS, Butelman E. Pharmacotherapy of addictions. Nat Rev Drug Discov. 2002;1(9):710-26.
11 Maldonado JR, Wysong A, van der Starre PJ, Block T, Miller C, Reitz BA. Dexmedetomidine and the reduction of postoperative delirium after cardiac surgery. Psychosomatics. 2009;50(3):206- 17.
12 McLellan AT, Lewis DC, O'Brien CP, Kleber HD. Drug dependence, a chronic medical illness: implications for treatment, insurance, and outcomes evaluation. JAMA. 2000;284(13):1689- 95
13 Ministerio de Justicia y del Derecho, Observatorio de Drogas de Colombia, Ministerio de Salud y Protección Social. Estudio nacional de consumo de sustancias psicoactivas en Colombia - 2013. 2014. p. 175.
14 Ministerio de salud y protección social de Colombia. Plan decenal de salud pública 2012 - 2021. 2013. p. 202.
15 United Nations Office on Drugs and Crime. World Drug Report 2015. New York: United Nations publication; 2015. p. 117.
16 Rayner SG, Weinert CR, Peng H, Jepsen S, Broccard AF, Institution S. Dexmedetomidine as adjunct treatment for severe alcohol withdrawal in the ICU. Ann Intensive Care. 2012;2(1):12.
17 Reade MC, O'Sullivan K, Bates S, Goldsmith D, Ainslie WR, Bellomo R. Dexmedetomidine vs. haloperidol in delirious, agitated, intubated patients: a randomised open-label trial. Crit Care. 2009;13(3):R75.
18 Reoux JP, Miller K. Routine hospital alcohol detoxification practice compared to symptom triggered management with an Objective Withdrawal Scale (CIWA-Ar). Am J Addict. 2000;9(2):135-44.
19 Riker RR, Shehabi Y, Bokesch PM, Ceraso D, Wisemandle W, Koura F, et al. Dexmedetomidine vs midazolam for sedation of critically ill patients: a randomized trial. JAMA. 2009;301(5):489-99.
20 Rovasalo A, Tohmo H, Aantaa R, Kettunen E, Palojoki R. Dexmedetomidine as an adjuvant in the treatment of alcohol withdrawal delirium: a case report. Gen Hosp Psychiatry. 2006;28(4):362-3.
21 Sessler CN, Varney K. Patient-focused sedation and analgesia in the ICU. Chest. 2008;133(2):552-65
22 VanderWeide LA, Foster CJ, MacLaren R, Kiser TH, Fish DN, Mueller SW. Evaluation of Early Dexmedetomidine Addition to the Standard of Care for Severe Alcohol Withdrawal in the ICU: A Retrospective Controlled Cohort Study. J Intensive Care Med. 2016 Mar;31(3):198-204.
23 Venn M, Newman J, Grounds M. A phase II study to evaluate the efficacy of dexmedetomidine for sedation in the medical intensive care unit. Intensive Care Med. 2003;29(2):201-7.
24 Wong A, Smithburger PL, Kane-Gill SL. Review of adjunctive dexmedetomidine in the management of severe acute alcohol withdrawal syndrome. Am J Drug Alcohol Abuse. 2015;41(5):382-91
25 Woods AD, Giometti R, Weeks SM. The use of dexmedetomidine as an adjuvant to benzodiazepine-based therapy to decrease the severity of delirium in alcohol withdrawal in adult intensive care unit patients: a systematic review, JBI Database System Rev Implement Rep. 2015 Jan;13(1):224-52.