Ciencia recreativa
Biopelículas fototróficas, ¿qué longitudes de onda lumínica favorecen su desarrollo y diversidad? Ejemplo de enseñanza de fundamentos de ecología microbiana desde una práctica sencilla de laboratorio escolar
Phototrophic biofilms, which light wavelengths promote their development and diversity? Example of teaching fundamentals of microbial ecology trough a simple school laboratory activity
Biopelículas fototróficas, ¿qué longitudes de onda lumínica favorecen su desarrollo y diversidad? Ejemplo de enseñanza de fundamentos de ecología microbiana desde una práctica sencilla de laboratorio escolar
Revista Eureka sobre Enseñanza y Divulgación de las Ciencias, vol. 14, núm. 3, pp. 647-652, 2017
Universidad de Cádiz

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.
Recepción: 01 Febrero 2017
Aprobación: 03 Julio 2017
Resumen: La existencia de una organización social en los microorganismos, entre ellos las bacterias, es muy poco conocida entre el alumnado de los diferentes niveles de educación. Se tiene el preconcepto de que esta característica se presenta en organismos vivos de mayor complejidad. Las biopelículas constituyen una organización social donde una población bacteriana o una comunidad de diferentes microorganismos procariotas y eucariotas, permanecen adheridas a una matriz extracelular de polímeros sintetizados y excretados por sus propias células. Dentro de la biopelículas podemos encontrar subpoblaciones celulares diferenciadas metabólicamente y con actividades diferentes. La formación de biopelículas bacterianas es la principal causa de las infecciones crónicas en el ser humano y otros mamíferos. Éstas también se forman en el medio ambiente, como por ejemplo en medios acuáticos, donde podemos encontrar las que se constituyen mediante asociaciones de microorganismos fototróficos como las microalgas (cianobacterias, diatomeas y algas verdes). En el presente trabajo se propone una actividad o práctica de laboratorio escolar muy sencilla. En ésta se puede estudiar el efecto de una sola variable sobre el desarrollo y diversidad de una biopelícula de microorganismos fototróficos. La variable mencionada es la longitud de onda de la luz visible que incide en un cultivo de dichos microorganismos. Utilizando filtros de diferentes colores (azul, verde, amarillo y rojo), se observaron resultados diferenciales.
Palabras clave: Biopelículas, Cianobacterias, Ecología microbiana, Didáctica de la microbiología.
Abstract: The existence of a social organization in microorganisms, among them the bacteria, is little known among stutents of diferent educational levels. The most common preconcept is that this characteristic occurs in living organisms with greater complexity. Biofilms constitute a social organization where a bacterial population or a community of different prokaryotic and eukaryotic microorganisms, where the cells remain attached to an extracellular matrix of polymers sintetized and excreted by themselves. Within the biofilms we can find metabolically differentiated celullar subpopulations with different activities. The formation of bacterial biofilms is the main cause of chronic infections in humans and other mammals. These are also found in the environment, for example in aquatic ones, where could find those that are consituted by associations of phototrophic microorganisms such as microalgae (cyanobacteria, diatoms and green algae). In the present work, a very simple school laboratory activity is proposed, where the effect of a single variable on the developmental level and diversity of a biofilm of phototrophic microorganisms can be studied. The variable mentioned is the visible light wave lenght that affects upon a culture of these kinds of microorganisms. Using different color filters (blue, green, yellow and red), differential results were observed.
Keywords: Biofilms, Cyanbacteria, Microbial ecology, Microbiology teaching methods.
Introducción
Diversos factores (físicos, químicos y biológicos) inciden en la distribución y abundancia de los seres vivos en los diferentes ambientes de nuestro planeta. La luz solar es uno de dichos factores ya que es la fuente de energía para los productores primarios de biomasa en las redes tróficas. Dentro de los productores primarios encontramos a las microalgas, un vasto y muy diverso grupo de organismos con representantes de varios de los reinos de los seres vivos (Abuhatab, 2011). Las cianobacterias (Dominio Bacteria, Reino Monera, Phylum Cyanobacteria) junto con las diatomeas (Reino Protista) y las algas verdes o Chlorophyta (Reino Plantae), son de los organismos más abundantes en los ambientes tanto de agua dulce como marina (Stevenson et al. 1996, Cooksey and Wigglesworth-Cooksey 1995). La mayoría de las especies de cianobacterias habitan en el bentos o en las columnas de agua de los lagos, ríos y arroyos de todo el mundo (Bonilla Santibáñez 2009). Éstas poseen cinco tipos principales de morfología características, las cuales son: unicelular, colonial, filamentosa y filamentosa ramificada (Madigan et al. 2010).
En general se tiende a pensar que las bacterias al ser organismos celulares procariotas, la actividad funcional y metabólica de los individuos en una población de estas, es independiente una de otra y su forma de vida es libre. A esta se la llama actualmente forma «planctónica» (Stoodley et al. 2004). Sin embargo, a mediados del siglo xx se encontró que las bacterias acuáticas de agua dulce y marina se presentan en mayor abundancia sobre superficies sólidas que en forma libre o planctónica (Zobell 1943, Cooksey y Wigglesworth-Cooksey 1995). No fue sino hasta hace pocos años, gracias al desarrollo de diversas técnicas moleculares y de cultivo, que se demostró que las bacterias y otros microorganismos, pueden formar asociaciones complejas (entre individuos de la misma especie y de diferentes especies y con diferenciación metabólica y o funcional entre sus miembros), llamadas biopelículas o biofilms en ingles (Stoodley et al. 2004). Las biopeliculas se forman cuando las células quedan adheridas a una superficie mediante una matriz compleja compuesta por productos de secreción de naturaleza polimérica como proteínas, polisacáridos e inclusive ADN. Esta matriz puede facilitar no solo la adhesión de las células, sino además la de sustancias nutritivas, lográndose una mayor concentración disponible para dichas células (Sekar et al. 2002, Baty et al. 2000, Stoodley et al. 2004, Høiby et al. 2010). Las ventajas de esta organización compleja o compor-tamiento «social» no solo se restringen a este fenómeno, también entre las principales, le pueden conferir a la población bacteriana resistencia a antibióticos siendo esta la causa por lo cual se producen infecciones crónicas persistentes, como por ejemplo en la enfermedad respi-ratoria llamada fibrosis quística (Høiby et al. 2010). En dicha infección se desarrollan sobre tejido pulmonar biopelículas de bacterias de la especie Pseudomonas aeruginosa, fenómeno que ha sido ampliamente estudiado como modelo de los mecanismos de formación y desarrollo de las biopelículas en general, demostrándose que dicho fenómeno esta regulado genéticamente por moduladores o señales químicas (por ejemplo, acil-homoserin-lactonas) que las células produ-cen para comunicarse entre si (Costerton y Stewart 2001). Se puede distinguir al menos cinco estadios que pueden tardar pocas horas en completarse (Stoodley 2002, Høiby et al. 2010).
Las biopelículas fototróficas se forman por agrupamientos celulares de los principales microorganismos fotótrofos mencionados en el primer párrafo. Además pueden unirse microorganismos heterótrofos que obtienen su fuente de energía, carbono y nitrógeno a partir de los productos sintetizados por los fotótrofos, principalmente en el interior de las biopelí-culas, dado que no necesitan la exposición directa de la .luz (Roeselers et al. 2008).
Los microorganismos fototróficos poseen diferentes pigmentos para la captación y absorición de las longitudes de onda del espectro lumínico visible, principalmente clorofilas, carotenoides y ficobilinas (Madigan et al. 2010, Bonilla Santibáñez 2009).
El objetivo del presente trabajo fue desarrollar una práctica sencilla de laboratorio escolar, en donde se estudia el efecto de una sola variable, en este caso de la incidencia de luz de diferentes colores o longitudes de onda sobre la formación de biopelículas fototróficas. La pregunta a responder fue: ¿todos los colores favorecen el desarrollo de una biopelícula fototrófica así como tambien su riqueza en diferentes especies o diversidad?
Materiales y metodología
Colecta de agua de laguna
Se tomó una muestra (10 litros) de la columna de agua de la «Laguna del Diario», ubicada en el departamento de Maldonado, sobre la ruta «Interdepartamental» a pocos kiló-metros de las ciudades de Maldonado y Punta del Este (figura 1). Dicha laguna presenta una eutrofización dada la afluencia de excesos de sustancias nutritivas ricas en nitrógeno, fósforo entre otras. La causa de este fenómeno es su proximidad a zonas habitadas como se puede apreciar en la figura 1, provocando que la abundancia de microorganismos en general y especialmente de los fotótrofos sea elevada.
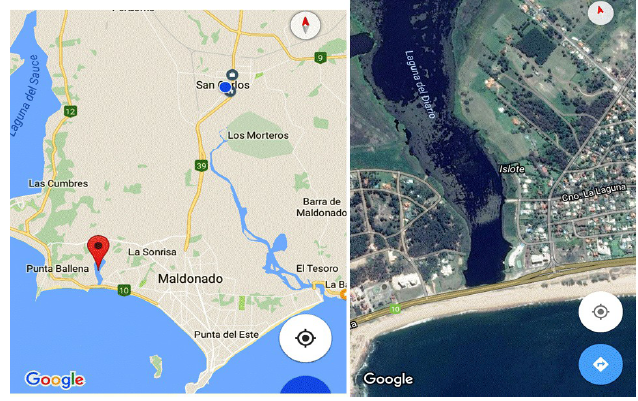
Figura 1.
Mapa de la ubicación de la «Laguna del Diario» y vista satelital de la misma.
Cultivo de biopelículas en laboratorio
Se utilizaron frascos de vidrio (1 litro de capacidad) con caras planas, con el fin de adherir a estas con pegamento de silicona al menos dos portaobjetos de vidrio por cada una en el interior de los frascos. Una vez adheridos dichos portaobjetos, se llenaron los frascos con 900 ml de agua de laguna y como «tratamiento» se envolvió cada frasco con un papel de celofán de un determinado color, el cual actúa como filtro que deja pasar solo una longitud de onda lumínica. Como «controles» se dejaron dos frascos en las mismas condiciones, pero uno de ellos sin envoltura con papel celofán y el otro cubierto con tela negra con la intención de que no pase la luz. Los colores usados fueron: azul (400-450 nanómetros), verde (530-550 nm), amarillo (600-630 nm) y rojo (680-700 nm). Todos los frascos se dejaron en una ventana con luz natural y cada día fueron rotados, con la finalidad de que cada cara reciba la misma cantidad de luz diariamente. En la figura 2 se muestra cómo fueron dispuestos los frascos en la ventana del laboratorio. Cada semana, utilizando pinzas, fueron despegados y retirados un portaobjeto por cada frasco y se observaron al microscopio óptico las biopelículas que sobre ellos se fueron desarrollando, sin utilizar ningún tipo de tinción, ya que se observaron las pigmentaciones naturales de los microorganismos presentes. Se tomaron fotos directamente desde el ocular utilizando la cámara de un smartphone.

Figura 2.
Cultivo de biopelículas fototróficas en frascos envueltos en papel celofán de diferente color.
Resultados
Semana 1
En la figura 3 se observa el desarrollo de biopelículas en la primer semana de incubación. Como se puede apreciar, con el filtro de color amarillo es dónde se observa el mayor desarrollo de cianobacterias coloniales con células de forma de pequeños cocos. El de menor desarrollo con filtro fue el de color azul, y los intermedios fueron el verde, el control 1 (sin filtro), el rojo en orden creciente respectivamente y finalmente sin crecimiento prácticamente el control 2 (envuelto en tela oscura), observándose la presencia de ácaros, como se puede apreciar en la figura 3F. En todos los casos donde hubo desarrollo se observó la misma morfología de colonias ya mencionada.
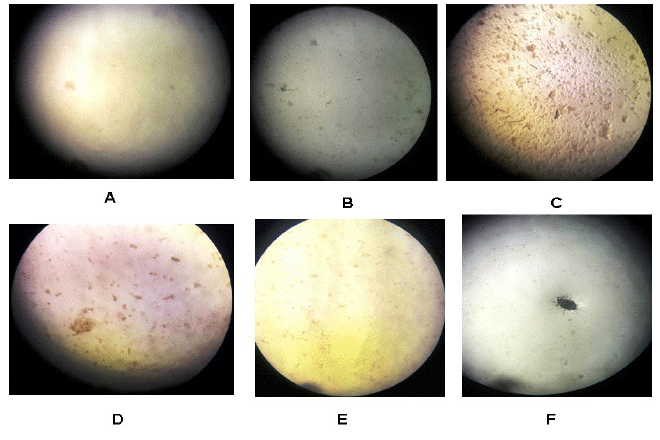
Figura 3.
Desarrollo de biopelículas en la primera semana de incubación. A) con filtro azul, B) con filtro verde, C) con filtro amarillo, D) con filtro rojo, E) sin filtro (control 1), y F) envuelto en tela oscura (control 2). Todas las fotos a un aumento de 400x (objetivo 40x y ocular a 10x).
Semana 2
En la segunda semana de incubación se observa la misma tendencia que en la anterior, presentándose con el color azul el menor desarrollo de los cubiertos con filtro y sin crecimiento significativo con el control oscuro (figura 4). Con respecto a la diversidad, con el control sin filtro se observó la presencia de otra especie diferente, apreciándose ahora además células con forma de filamentosa posiblemente ramificada y también diatomeas (figura 4E).
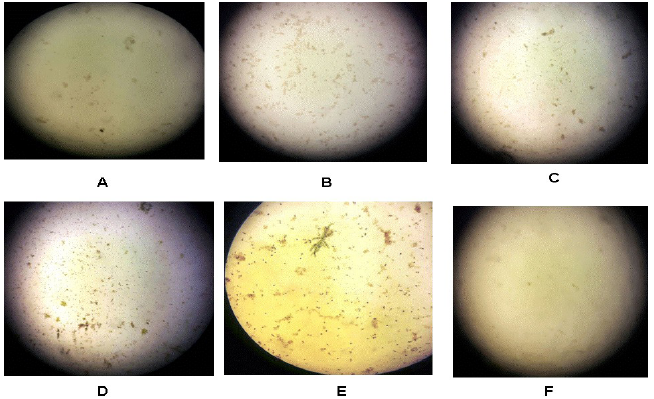
Figura 4.
Desarrollo de biopelículas en la segunda semana de incubación. A) con filtro azul, B) con filtro verde, C) con filtro amarillo, D) con filtro rojo, E) sin filtro (control 1), y F) envuelto en tela oscura (control 2). Todas las fotos a un aumento de 400x (objetivo 40x y ocular a 10x).
Semana 4
A continuación se muestran los resultados de la cuarta semana de incubación, a partir de la cual se observó un cambio notorio en la complejidad o diversidad de las biopelículas de algunos tratamientos. En la figura 5 se muestra el resultado obtenido. Se observa que en los tratamientos con filtro amarillo, rojo y en el control sin filtro (C, D y E respectivamente), se produce la mayor diversidad en las biopelículas, diferenciándose diferentes morfologías, como cianobacterias coloniales, cianobacterias filamentosas y filamentosas ramificadas así como también de diatomeas. La menor diversidad y desarrollo persistió en el tratamiento con filtro azul.
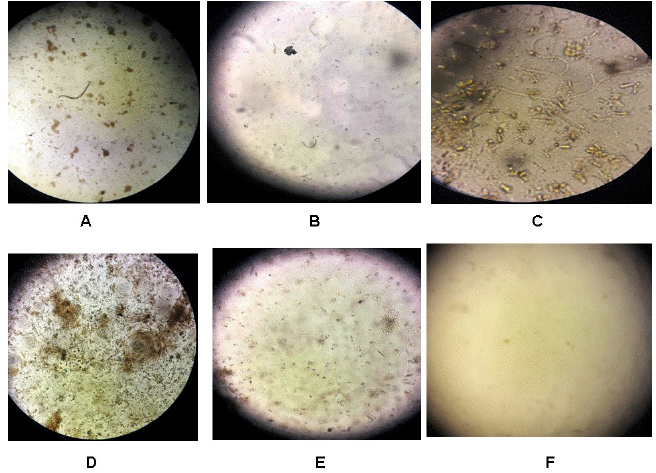
Figura 5 .
Desarrollo de biopelículas en la cuarta semana de incubación. A) con filtro azul, B) con filtro verde, C) con filtro amarillo, D) con filtro rojo, E) sin filtro (control 1), y F) envuelto en tela oscura (control 2). Todas las fotos a un aumento de 400x (objetivo 40x y ocular a 10x).
Discusión
Dado que para el establecimiento de cualquier biopelícula, es necesario que exista una alta tasa de síntesis de polímeros para formar la matriz extracelular que le dará soporte, los resultados obtenidos en cuanto al desarrollo y diversidad observada, especialmente con los filtros de color amarillo y rojo, son explicables mediante el espectro de absorción de los principales pigmentos fotosintéticos que poseen los microorganismos. La clorofila presentes en las cianobacterias es la tipo «a», con picos de absorbancia a 420 nm (azul) y 670 nm (rojo). Además poseen pigmentos accesorios como las ficobilinas en cianobacterias, teniendo picos de absorbancia entre 600 nm (amarillo) y 650 nm (rojo) (Bonilla Santibáñez 2009). Por lo tanto estas últimas longitudes de onda luminica son las más favorables energeticamente. La menor absorbancia de la luz visible por parte de estos últimos pigmentos se da en la longitud de onda del color azul y verde, alrededor de los 450 a 550 nm, por lo cual la luz de estas longitudes no son favorables energeticamente para la síntesis de los polímeros constitutivos de una biopelícula. Por lo tanto, la respuesta a la pregunta inicial fue respondida, no todas las longitudes de onda favorecen por igual al desarrollo y a la diversidad de las biopelículas fototróficas a medida que pasa el tiempo.
Mediante la realización de esta práctica, los alumnos podrán aprender conceptos de ecología como el de las sucesiones biológicas, el de las interacciones entre individuos de la misma población o de diferentes especies (concepto de consorcios, comunidades, etc.) los cuales aparecen en la bibliografía para los diferentes niveles de educación en Biología y que por lo general resultan ser poco atractivos y de difícil comprensión para ellos, debido al grado de abstracción que requieren. Con esta práctica podrán observar el incremento en la diversidad a medida que transcurre el tiempo y según que tratamiento hayan sufrido los cultivos.
Por otro lado, también el presente trabajo practico incentiva a la observación, a la investigación y a la búsqueda de información y conocimiento de otras disciplinas, como la Física, ya que hay que introducirse en el marco teórico de la naturaleza de la luz como onda electromagnética la cual transporta energía y que puede ser absorbida por cierto tipo de moléculas. Se pretende que los alumnos busquen en la bibliografía qué longitudes de onda absorben cada tipo de pigmento presentes en los microorganismos (curvas de absorbancia) y lo correlacionen con los resultados observados.
Finalmente, y como se dijo en un principio, se cambia el preconcepto erróneo de que los microorganismos, en especial las bacterias, no poseen una estructura social en su organización poblacional como otros organismos de mayor complejidad. Entender cómo funciona dicha interacción puede ser clave para comprender cómo distintos factores externos al ecosistema pueden alterar la diversidad y la función de las comunidades de microorganismos.
Agradecimientos
El autor desea agradecer a Laura Acosta, Lorena Colombo, Karen Correa, Andrea Guadalupe y Pía Bermúdez, quienes fueron sus alumnas en el año lectivo 2016 de la asignatura Microbiología, mostrando un muy especial interés por la realización de la práctica descrita, de la cual han desarrollado un material https://youtu.be/ERP0XSRTtDE . También se desea agradecer a la Dra. Viviana Lima Silva por sus valiosas opiniones aportadas al trabajo.
Referencias
Abuhatab Y. A. (2011) Actividad metabólica diaria de Biofilms en el sector medio de un río de alta montaña (Río Tota, Bocaya-Colombia). Tesis de Maestría en Ciencias-Biología. Facultad de Ciencias. Universidad Nacional de Colombia. pp. 1-109.
Baty A. M., Eastburn C. C., Techkarnjanaruk S., Goodman A. E., Geesey G. G. (2000) Spatial and temporal variations in chitinolytic gene expression and bacterial biomass production during chitin degradation. Applied and Environmental Microbiology 66 (8), 3574-3585.
Bonilla Santibañez S. E. (2009) Cianobacterias planctónicas del Uruguay. Manual para la identificación y medidas de gestión (No. 582.232 UNE). UNESCO. Administración de las Obras Sanitarias del Estado (Uruguay). Montevideo. Universidad de la República.
Cooksey K. E., Wigglesworth-Cooksey B. (1995) Adhesion of bacteria and diatoms to surfaces in the sea: a review. Aquatic Microbial Ecology 9, 87-96.
Costerton J. W., Stewart P. S. (2001) Películas bacterianas. Investigación y Ciencia Sept., 55-61.
Høiby N., Bjarnshol, T., Givskov M., Molin S., Ciofu O. (2010) Antibiotic resistance of bacterial biofilms. International Journal of Antimicrobial Agents 35 (4), 322-332.
Madigan M. T., Martinko J. M., Clark D. P. (2010) Brock Biology of Microorganisms. Upper Saddle River, NJ. Pearson Prentice Hall.
Roeselers G., Van Loosdrecht M. C. M., Muyzer G. (2008) Phototrophic biofilms and their potential applications. Journal of Applied Phycology 20 (3), 227-235.
Sekar R. K., Nair V. K., Rao V. N. R., Venugopalan V. P. (2002) Nutrient dynamics and successional changes in a lentic freshwater biofilm. Freshwater Biology 17, 1893-1907.
Stevenson R. J., M. L. Bothwell., R. L. Lowe (eds.) (1996) Algal Ecology – Freshwater Benthic Ecosystems. San Diego, CA. Academic Press.
Stoodley L., Costerton J. W., Stoodley P. (2004) Bacterial biofilms: from the natural environment to infectious diseases. Nature Reviews Microbiology 2 (2), 95-108.
Zobell C. E. (1943) The effect of solid surfaces upon bacterial activity. Journal of Bacteriology 46 (1), 39-56.
Información adicional
Para citar este artículo: Robledo-D'Angelo O. (2017) Biopelículas fototróficas, ¿qué
longitudes de onda lumínica favorecen su desarrollo y diversidad? Ejemplo de
enseñanza de fundamentos de ecología microbiana desde una práctica sencilla de
laboratorio escolar. Revista Eureka sobre
Enseñanza y Divulgación de las Ciencias 14 (3), 647-652. Recuperado
de: http://hdl.handle.net/10498/19513
Enlace alternativo
http://revistas.uca.es/index.php/eureka/article/view/3349 (html)