Formación del profesorado de ciencias
Concepciones epistemológicas sobre enlace químico en la práctica profesional de los profesores de química
Epistemological conceptions of chemical bonding in the professional practice of chemistry teachers
Concepciones epistemológicas sobre enlace químico en la práctica profesional de los profesores de química
Revista Eureka sobre Enseñanza y Divulgación de las Ciencias, vol. 22, núm. 3, pp. 360201-360219, 2025
Universidad de Cádiz
Recepción: 25 Febrero 2025
Revisado: 09 Julio 2025
Aprobación: 08 Septiembre 2025
Resumen: El análisis epistemológico de los conceptos químicos con base en los fundamentos de la filosofía de la química conducen a una transformación en sus formas de enseñanza y evidencian la necesidad de repensar la didáctica de la química. Sin embargo, hay pocas investigaciones acerca de las concepciones epistemológicas que tienen los profesores frente a los conceptos químicos, así como sobre los recursos didácticos y tecnológicos que emplean para explicar estos conceptos. Este artículo tiene como propósito presentar las concepciones sobre enlace químico empleadas por los profesores en ejercicio que cursan estudios de posgrado durante su práctica profesional. Los datos se recolectaron mediante dos cuestionarios abiertos, cuyos resultados mostraron una fuerte dependencia en la interpretación matemática de la diferencia de electronegatividad (Δχ) para explicar este concepto, así como el uso de referencias antropomórficas y modelos simplificados. Las aproximaciones teóricas en torno de la naturaleza del conocimiento químico permitieron a los profesores reflexionar críticamente sus concepciones sobre enlace químico, acercándolos a una perspectiva modelo–teórica relevante para esta investigación.
Palabras clave: Conocimiento químico, Electronegatividad, Enlace químico, Formación posgradual de profesores, Reduccionismo.
Abstract: The epistemological analysis of the chemical concepts grounded in the foundations of the philosophy of chemistry leads to a transformation in teaching practices and highlights the need to rethink chemistry education. However, there is limited research on the epistemological conceptions held by chemistry teachers regarding chemical concepts, as well as on the teaching and technological resources they use to explain these concepts. This paper aims to present the conceptions of chemical bonding held by in-service teachers pursuing postgraduate studies during their professional practice. Data were collected through two open-ended surveys. The findings revealed a predominant reliance on the mathematical interpretation of electronegativity differences (Δχ) to explain this concept, alongside the use of anthropomorphic references and simplified models. Theoretical approaches concerning the nature of chemical knowledge enabled teachers to critically reflect on their conceptions of chemical bonding, bringing them closer to a theoretical model–based view relevant to this research.
Keywords: Chemical knowledge, Electronegativity, Chemical bonding, Postgraduate teacher education, Reductionism.
Introducción
El enlace químico es un concepto clave que ha sido interpretado mediante modelos simbóli-cos construidos a partir de principios físicos (Taber y Coll, 2002). Su relevancia en el ámbito educativo se destacó desde finales del siglo XX, cuando se lo consideró una de las grandes ideas que debía enseñarse a los estudiantes en los cursos introductorios de química (Atkins, 1999; Gillespie, 1997). Bajo una perspectiva filosófica, también ha sido descrito como una de las dos grandes ideas de la química y un tema central en este campo (Scerri, 2023). Desde entonces, se ha debatido ampliamente sobre su existencia (Ochiai, 2025; Seifert, 2023), su significado (Levy et al., 2013), su relación con la estructura química (Ochiai, 2020), y sobre los modelos propuestos para representarlo (Levy et al., 2010), aunque la ambigüedad ha sido una constante en el estudio de estas aproximaciones teóricas (Pizzochero, 2025).
Es importante señalar que los debates filosóficos en torno al enlace químico se han originado a partir de las formas en que se ha enseñado este concepto en el ámbito escolar. Desde hace más de un siglo, los enlaces iónico y covalente se han abordado por separado, aunque forman parte de un modelo continuo (Scerri, 2023). Sin embargo, las recientes discusiones superan estas diferencias e incluyen argumentos más complejos y difíciles de conciliar. Por ejemplo, Coulson (1955, p. 2084), afirmó que el enlace químico no era un objeto real, nunca se había observado y era producto de la imaginación. Pese a ello, Lewis y Pauling desarrollaron sus modelos de pares electrónicos, hibridación y resonancia con base en una concepción estruc-tural del enlace químico, que lo define como una entidad material dentro de una molécula, responsable de la relación submolecular entre centros atómicos de manera espacialmente localizada (Hendry, 2008).
No obstante, estas construcciones teóricas no han incidido significativamente en los modelos que usan los profesores de química para explicar enlace químico, ya que aún se observan referencias antropomórficas (Lee y Cheng, 2014), confusión entre fuerzas intermoleculares e intramoleculares (Levy et al., 2010), nociones macroscópicas en el nivel atómico (Taber, 2001), y la clasificación dicotómica del enlace como iónico o covalente (Levy et al, 2013). Estos errores surgen a partir de una aproximación simplista que usa representaciones concretas sin contexto en la enseñanza del enlace químico (Matus et al., 2011), así como del énfasis excesivo en la regla del octeto como principio explicativo (Levy et al, 2008; García-Franco y Garritz, 2006).
En Colombia, los cursos de química para la formación de profesores incluyen el concepto enlace químico con el fin de representar la estructura química de un material, elaborar explicaciones sobre sus propiedades y diseñar estrategias para su enseñanza y aprendizaje. Sin embargo, ¿qué tan relacionados se encuentran sus significados con la naturaleza del conocimiento químico? Pese a que hay una investigación sobre la estructura conceptual del enlace químico desde una mirada ontológica en la formación posgradual de profesores (Rubiano, 2017), este trabajo presenta algunos aportes desde una perspectiva epistemológica con base en los siguientes objetivos: 1) identificar las ideas previas sobre enlace químico en un grupo de profesores en ejercicio que cursa primer semestre del programa de Maestría en Docencia de la Química de la Universidad Pedagógica Nacional y 2) analizar la estructura conceptual de los profesores frente al enlace químico a partir de las aproximaciones teóricas que tienen en torno de la naturaleza del conocimiento químico.
El reduccionismo: un problema filosófico del conocimiento químico
En el siglo XIX, el positivismo intentó diferenciar la ciencia de la no ciencia con base en dos criterios: el empírico – experimental, donde el conocimiento era científico solo en la medida que podía medirse y observarse, y el lógico – matemático donde las teorías científicas debían ordenarse axiomáticamente y reconstruirse deductivamente; esta corriente filosófica definió que podían unificarse las ciencias y derivar los principios de una ciencia a otra, visión conocida como reduccionismo (Chamizo, 2010).
A principios del siglo XX, la química se intentó reducir a la física con el éxito de la mecánica cuántica, a tal punto que Paul Dirac diría que las leyes fundamentales de la física necesarias para la teoría matemática de una gran parte de la física y de la totalidad de la química estarían completamente conocidas a partir de la mecánica cuántica (Lombardi y Labarca, 2005).
Sin embargo, desde finales del siglo XX se ha señalado que no es posible derivar conceptos químicos a partir de explicaciones físicas (Erduran y Mugaloglu, 2014; Erduran y Scerri, 2002; Scerri y McIntyre, 1997) como lo plantea el reduccionismo epistemológico, en el cual una teoría científica puede reducirse a otra cuando puede deducirse de esta última (Lombardi y Labarca, 2005). Según esta visión, las propiedades de un sistema químico resultarían de las propiedades de sus microunidades físicas subyacentes (Labarca, 2011). No obstante, el único éxito en la derivación de resultados químicos ha dependido de asumir datos químicos previos (Vemulapalli y Byerly, 1999).
Aunque la mecánica cuántica proponga un conjunto de modelos matemáticos exitosos para el campo de la espectroscopía, no puede explicar completamente las propiedades de los átomos ni la periodicidad química; por lo tanto, los hechos empíricos pueden acomodarse en la teoría, pero no derivarse de ésta (Erduran y Scerri, 2002).
El reduccionismo epistemológico en el enlace químico se presenta cuando “desaparece” en los cálculos cuánticos de energía de enlace, puesto que sus microconstituyentes útiles en las predicciones químicas no se ajustan con precisión a la teoría cuántica (Vemulapalli y Byerly, 1999). Sin embargo, el reduccionismo ontológico ha generado mayor debate, al punto que Scerri y McIntyre (1997) afirmaron que “el concepto de enlace químico parece estar perdido en un proceso de reducción” (p. 219), dado que es posible calcular propiedades moleculares sin necesidad de definir las expresiones matemáticas asociadas con el enlace.
Desde esta perspectiva, Lombardi y Martínez (2012) han propuesto la química cuántica como el puente que relaciona la mecánica cuántica con la química estructural para evitar la reducción ontológica del enlace químico. Dentro de la química cuántica se encuentran los modelos de enlace de valencia (EV) y de orbital molecular (OM), los cuales requieren asumir supuestos procedentes de la experimentación química para explicar el enlace químico. En esta medida, no hay una teoría (mecánico–cuántica o estructural) o modelo (EV u OM) que explique completamente el enlace, ni tampoco se pueden atribuir estos últimos a simples aplicaciones de la mecánica cuántica. A pesar de que las dos teorías sean ontológicamente incompatibles entre sí, los modelos de EV y OM adoptan elementos teóricos de cada una para su construcción; de este modo, la química cuántica carece de un referente ontológico propio y se convierte en una herramienta que permite establecer relaciones teóricas entre la química estructural y la mecánica cuántica (Lombardi y Martínez, 2012, p. 666).
El enlace químico en el marco del conocimiento químico
Hendry (2008) distingue una concepción estructural y otra energética del enlace químico, con base en las diferencias entre los modelos de EV y OM. En la concepción estructural, el enlace químico se entiende como una entidad material dentro de la molécula, responsable de la relación submolecular espacialmente localizada entre los núcleos atómicos. Esta idea se alinea con el modelo de Lewis y con algunas interpretaciones del modelo de EV desde la mecánica cuántica, donde el estado enlazado se describe como un híbrido de resonancia y se representa mediante una combinación lineal de funciones de onda formadas a partir de orbitales atómicos. Los electrones son cuánticamente indistinguibles en estas funciones y cumplen con el principio de exclusión de Pauli (Lombardi y Martínez, 2012).
Pauling (1928) profundizó en el modelo mecánico–cuántico del enlace para la molécula H2 desde esta concepción estructural. En este sentido, propuso que el cambio de energía de los electrones derivaba de una función de perturbación f, asociada con la repulsión electrostática (Gavroglu y Simões, 2012), y de una energía de resonancia que resultaba del intercambio electrónico entre los orbitales ψ y Φ. Esta energía se relaciona con la energía del enlace químico entre electrones compartidos (p. 185), siempre que permanezcan localizados entre los núcleos para la formación de una molécula. Esta condición respalda la representación del enlace propuesta en el modelo de Lewis (Figura 1).
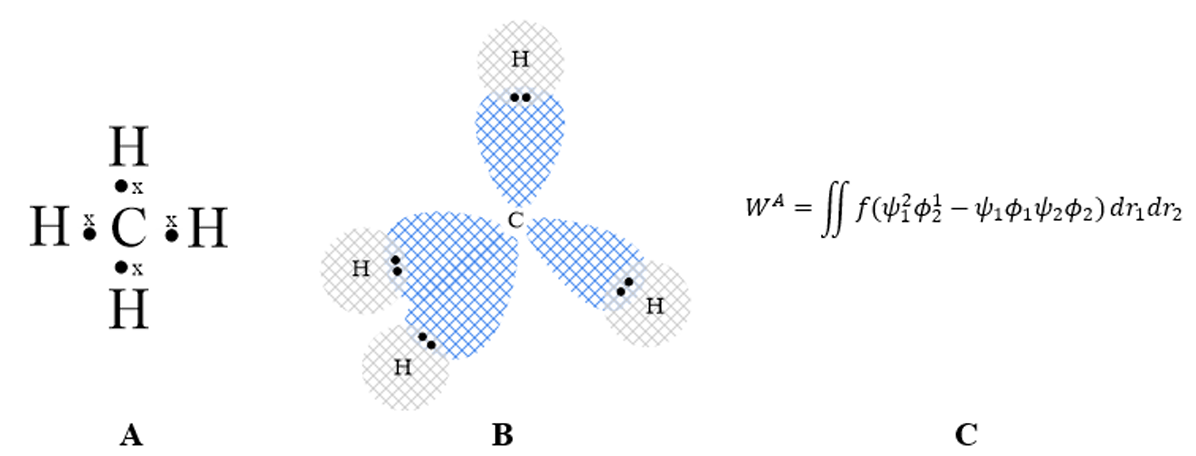
Figura 1
Representaciones sobre la concepción estructural del enlace. Modelo de Lewis (A) y VSEPR (B) para CH4. C. Modelo matemático que relaciona f con la resonancia entre los electrones
Sin embargo, la concepción estructural del enlace enfrenta tres desafíos: 1) el holismo mecánico–cuántico, en el que la función de onda molecular es simétrica con respecto a la permutación de un electrón y no debe depender ni de su identidad ni de su asociación a un núcleo; 2) la deslocalización electrónica, que impide reconocer qué parte de la molécula es responsable de las características asociadas al enlace, y 3) la existencia de moléculas cuyas estructuras no pueden representarse mediante las fórmulas clásicas de valencia, como los compuestos iónicos o covalentes cuyos ángulos y longitudes de enlace requieren uniones entre varios centros atómicos (Hendry, 2008). No obstante, estos límites no anulan el poder explicativo de esta concepción estructural, como se ha argumentado para el enlace covalente (Weisberg, 2008), ya que su uso resulta esencial para comprender la síntesis, la retrosíntesis y la solución de problemas en química orgánica (Ochiai, 2025).
Por su parte, la concepción energética del enlace surge del escepticismo de Coulson frente a los compuestos donde no se cumplen las fórmulas de valencia, y plantea un único argumento para todos los casos donde hay enlace químico: los cambios de energía. Más que una teoría sobre los tipos de enlace, esta concepción se asocia con una teoría del enlazamiento químico (Hendry, 2008).
Esta perspectiva se vincula con una dimensión energética en el nivel molecular basada en la ley de Hess, la cual permite calcular tanto la fuerza y la energía promedio de enlace como las entalpías de atomización y formación de un compuesto (Figura 2) (Jensen, 1998), así como las energías reticulares en sólidos iónicos. Estos valores, medibles empíricamente, no consideran ni la direccionalidad ni la localización del enlace dentro de la molécula (Hendry, 2008).
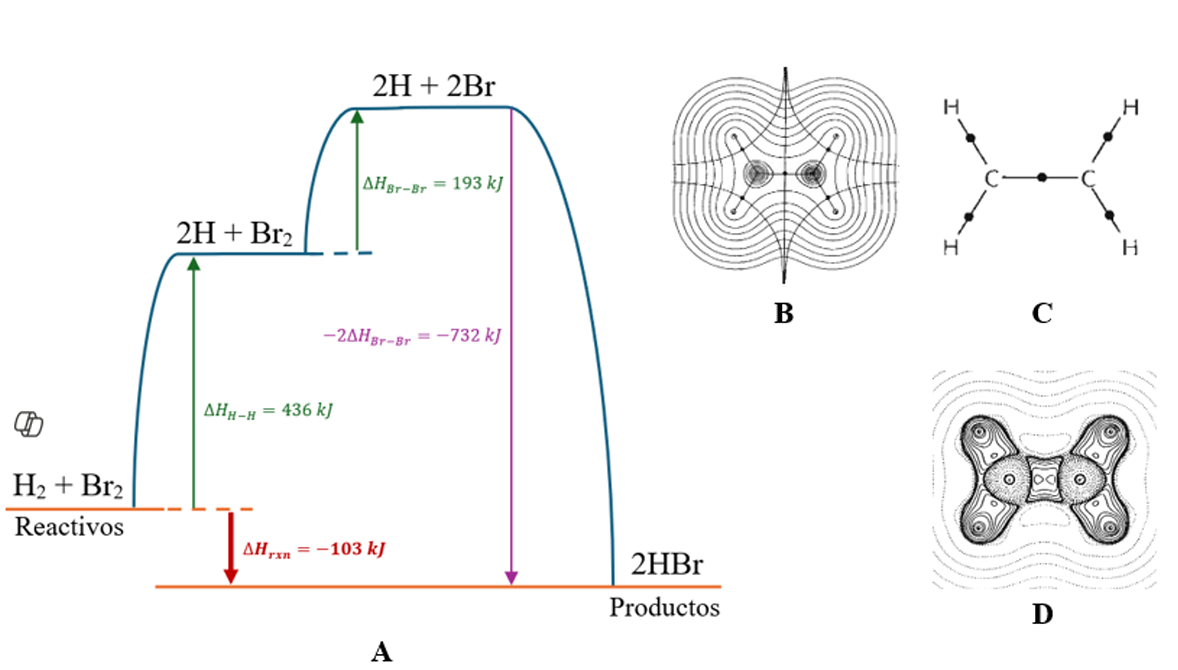
Figura 2
Representaciones sobre la concepción energética del enlace. A. Energías de enlace para la formación de HBr. B. Mapas de contorno de ρ con trayectorias y puntos críticos de enlace para C2H4C. Grafo molecular de C2H4 en su geometría de equilibrio. D. Mapas de contorno laplaciano para C2H4. Imágenes B a D tomadas Gillespie y Popelier (2001)
Desde la perspectiva mecánico–cuántica, la concepción energética no considera la existencia del enlace químico (Coulson, 1955) y se fundamenta en los postulados del modelo de OM, que asume la molécula como una entidad unitaria que no se compone de átomos separados. Este modelo resulta muy útil para explicar la deslocalización electrónica y las funciones de onda moleculares que pueden describirse mediante un electrón, un aspecto que no es posible representar en el modelo de EV (Lombardi y Martínez, 2012).
Bader (2009) criticó la visión estructural al afirmar que el enlace químico está limitado y dominado por el modelo de Lewis, el cual no explica la formación de cristales iónicos, el enlace metálico ni los enlaces de hidrógeno. Incluso, sostuvo que el enlace covalente no se diferencia de las interacciones de van der Waals, ya que ambos parten de un mecanismo cuántico común (Bader et al., 2006). Además, la evidencia reciente que muestra a dos átomos de carbono formando un enlace sigma (σ) mediante el compartimiento de un solo electrón (Shimajiri et al., 2024), junto con la existencia mecánico–cuántica del ion, ponen en duda si el enlace covalente responde estrictamente a la formación de un par electrónico (Scerri, 2023).
A pesar de los esfuerzos del modelo mecánico-cuántico de Heitler y London por mantener el modelo de Lewis, la especie condujo a nuevas explicaciones basadas en los cambios en la función de onda del átomo de hidrógeno, tales como el compartimiento, la contracción inducida y la polarización del orbital (Ruedenberg y Schmidt, 2007). Estos argumentos se integran con la disminución de la energía potencial que resulta del movimiento electrónico entre los núcleos y las regiones adyacentes donde no se presenta el enlace (Needham, 2014). La consideración de estas zonas adicionales es fundamental en los intentos de encontrar un elemento material que defina esta entidad (Scerri, 2023), constituyendo una crítica directa a la concepción estructural planteada.
Finalmente, las aplicaciones de la concepción energética no se limitan al modelo OM, sino que también abarcan el análisis de enlaces con un electrón (Shimajiri et al., 2024), el uso de funciones de localización electrónica (ELF), el estudio de la transferencia electrónica (Piechota y Meyer, 2019) y el enfoque de la teoría cuántica de átomos en moléculas (QTAIM). En este último, se han desarrollado conceptos como las trayectorias de enlace (Bader, 2009) y la densidad electrónica (ρ) (Figura 2) (Gillespie, 2006).
Aunque Weisberg (2008) sostuvo que el modelo OM descarta la concepción estructural en favor de la energética, esta postura ha sido fuertemente criticada (Scerri, 2023). No obstante, la concepción energética no considera el papel del enlace en las fórmulas estructurales donde la valencia es relevante, lo que le resta poder explicativo frente a la concepción clásica de la estructura molecular (Hendry, 2008).
Metodología
Muestra
En esta investigación participaron 22 profesores de química, estudiantes de primer semestre de la Maestría en Docencia de la Química de la Universidad Pedagógica Nacional. El estudio se realizó en el curso Conceptos Químicos e Implicaciones Didácticas I, cuyo programa se centró en la discusión epistemológica y ontológica de la química y los conceptos químicos. Las sesiones abordaron temas como imagen pública de la química, estructura conceptual de la química, leyes, teorías y modelos, naturaleza del conocimiento químico, conceptos químicos e implicaciones didácticas. En la quinta sesión se analizó el concepto de enlace químico, en línea con los objetivos de este trabajo.
Instrumentos
Se diseñaron dos instrumentos. El primero, sobre ideas previas, incluyó 10 preguntas abiertas (P1 a P10) con el fin de indagar las concepciones de los profesores sobre enlace químico, enlace iónico y enlace covalente, así como sobre los términos que utilizaban para explicarlos en el aula. El segundo, centrado en la naturaleza del enlace químico, presentó 2 casos con 3 preguntas abiertas (P1 a P3), con el fin de identificar el impacto de las discusiones sobre la naturaleza del conocimiento químico en la construcción de significados en torno al enlace; la situación II se tomó del capítulo dedicado al enlace químico en el texto de Brown et al. (2014).
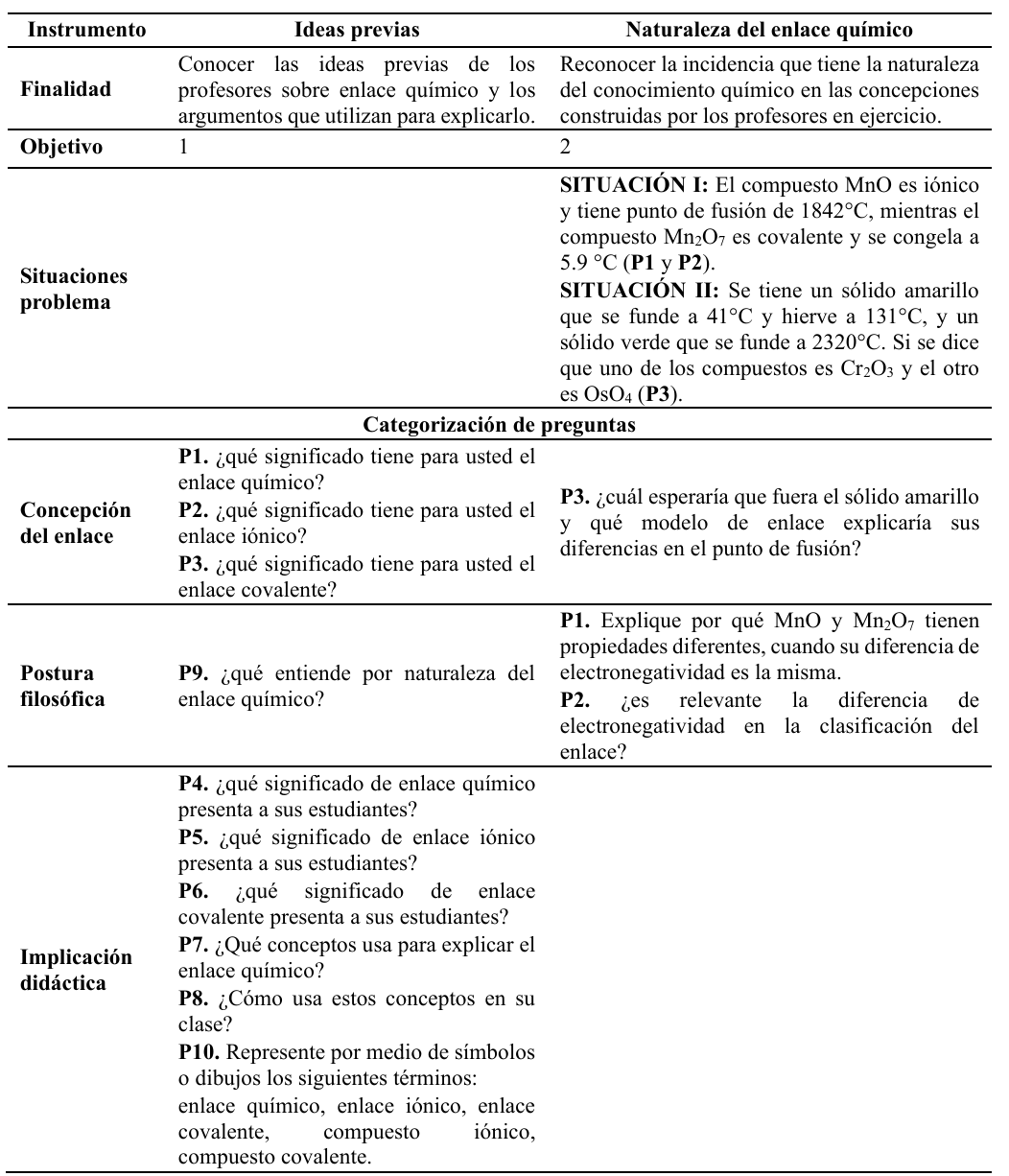
La categorización de las preguntas (Tabla 1) se estructuró en tres ejes: 1) la concepción del enlace, que distingue entre una visión estructural o energética e incluye sus impedimentos pedagógicos y conjeturas (Taber, 1997; Taber, 2001); 2) la postura filosófica, centrada en los fundamentos epistemológicos y ontológicos del conocimiento químico, y 3) la implicación didáctica, que analiza si los términos empleados por los profesores aún responden a la regla del octeto, a las dificultades para transferir entre los niveles molar y molecular (Taber, 2001; Jensen, 1998) o a una clasificación dicotómica del enlace (Lee y Cheng, 2014). El segundo instrumento no abarcó el último eje, ya que se aplicó en la última sesión del curso.
Implementación
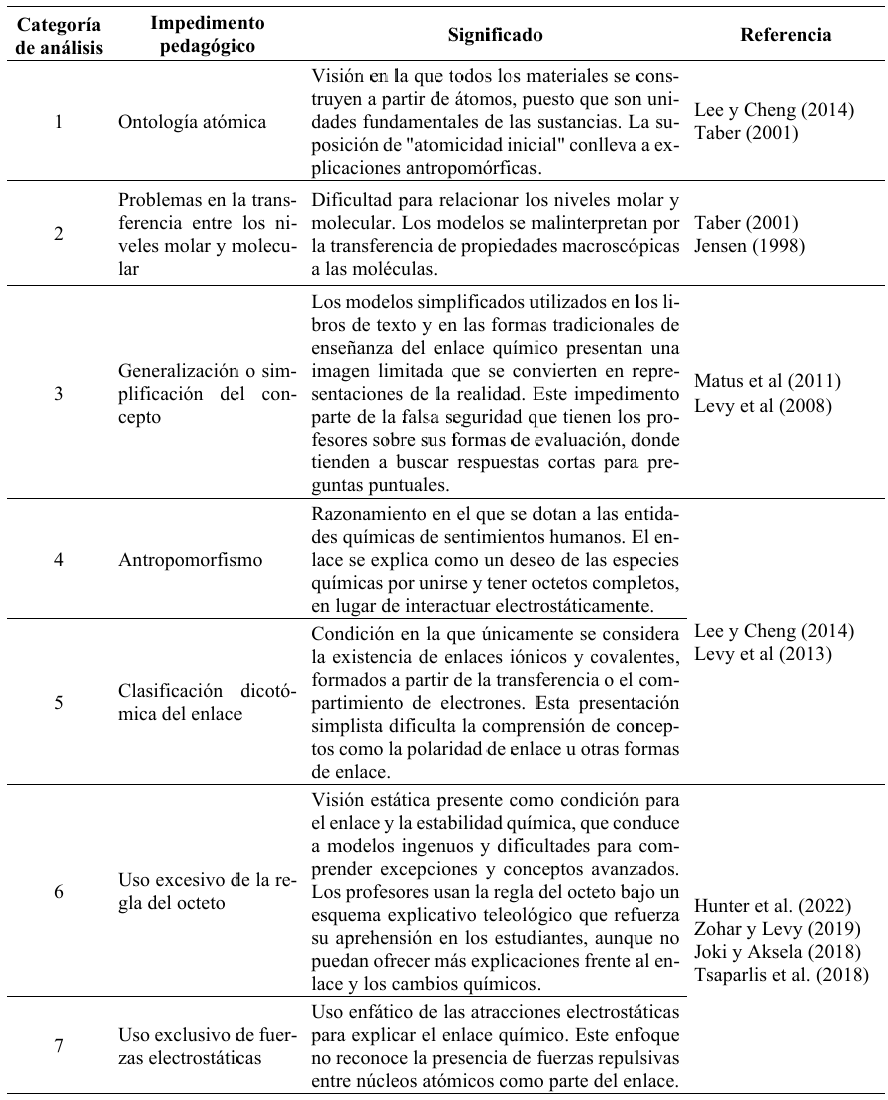
Los instrumentos se aplicaron en las sesiones 1 y 6, cuyos resultados se analizaron siguiendo las metodologías propuestas por otros autores (Hunter et al., 2022; Fatokun, 2016). Las categorías de análisis del primer instrumento se construyeron a partir de los impedimentos pedagógicos asociados con la enseñanza y el aprendizaje del enlace químico (Tabla 2) (Lee y Cheng, 2014; Levy et al., 2013), y las conjeturas que tienen los estudiantes para explicar el enlace iónico (Tabla 3).
El cuestionario sobre la naturaleza del enlace químico se elaboró a partir de la dependencia teórica observada en los profesores, quienes en el instrumento de ideas previas recurrieron a la diferencia de electronegatividad para explicar el enlace. La categoría de análisis se apoyó en su relación con el enlace químico, el estado de oxidación y el punto de fusión, los cuales conforman un modelo continuo relacionado matemática y experimentalmente (Viswanathan y Gulam Razul, 2022; Šima, 2016). En los dos casos se presentaron óxidos de metales de transición, cuyo modelo de enlace no puede predecirse únicamente a partir de la diferencia de electronegatividad (Sproul, 2001).

Resultados y discusión
Instrumento de ideas previas
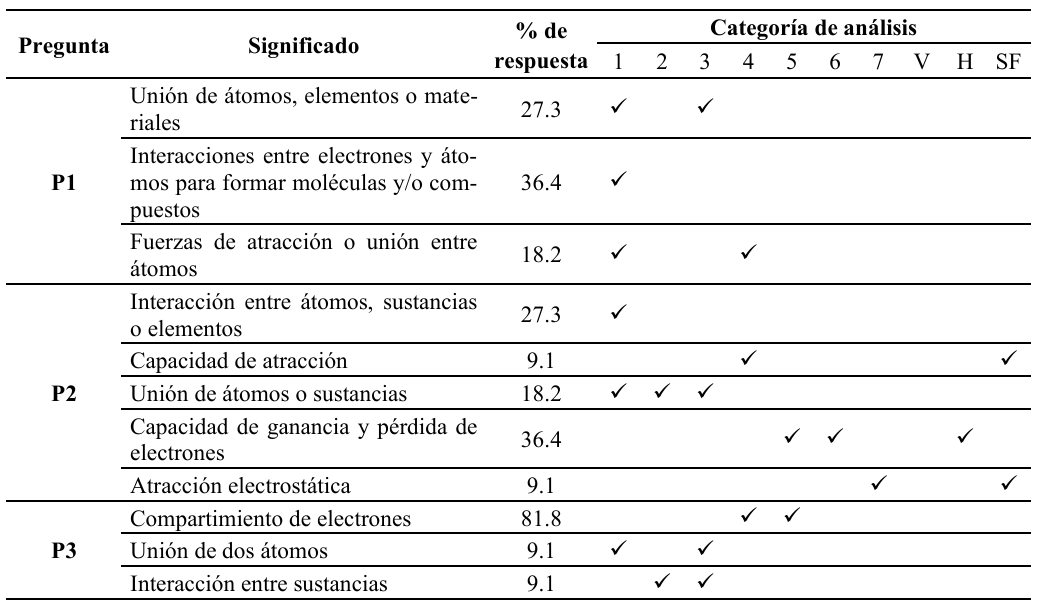
En las preguntas P1 a P3 (Tabla 4), se encontró que los profesores vincularon sus nociones de enlace químico (81.9%) y enlace iónico (45.5%) a una ontología atómica que, aunque está asociada con una concepción estructural del enlace, cae en el reduccionismo ontológico y en una visión realista de esta entidad (Rubiano, 2017; Scerri y McIntyre, 1997). Además, hay una simplificación excesiva de los significados de enlace químico (27.3%), enlace iónico (18.2%) y enlace covalente (18.2%), que surge a partir de un acercamiento tradicional en su enseñanza y no favorecen una interpretación adicional.
Como lo indica la Tabla 2, la ontología atómica conduce a explicaciones antropomórficas, puesto que el supuesto de atomicidad inicial favorece argumentos en los cuales los átomos quieren alcanzar su octeto y se unen con este fin para llegar a su estabilidad química. Estas visiones se reflejaron en el 18.2% de las respuestas a P1, en el 9.1% a P2 y en el 81.8% a P3; en el último caso, el “compartimiento” de electrones es un modelo antropomórfico en el nivel eléctrico y la dimensión estructural del discurso químico (Jensen, 1998), puesto que no hay evidencia de tal comportamiento entre los centros atómicos de una molécula.
Por otra parte, las concepciones de enlace iónico y covalente estuvieron delimitadas por la clasificación dicotómica del enlace, puesto que su comparación en términos de ganancia y pérdida de electrones para el primer término (36.4%), en contraste con el compartimiento de electrones para el segundo, reflejó una clara diferencia que dificulta la comprensión de otras formas de enlace (Lee y Cheng, 2014).
Los profesores presentaron mayores impedimentos pedagógicos al definir el enlace iónico, lo que evidencia los desafíos asociados a su enseñanza y aprendizaje (Taber et al., 2012). Se identificaron las conjeturas H y SF en el 54.5% de las respuestas, debido a una interpretación “molecular” del enlace iónico generada por el énfasis excesivo en el proceso de formación de iones (García-Franco y Garritz, 2006); asimismo, la regla del octeto sigue siendo un argumento en las explicaciones sobre este modelo de enlace, toda vez que el 36.4% de los profesores acuden a la transferencia electrónica como soporte teórico para construir sus significados.
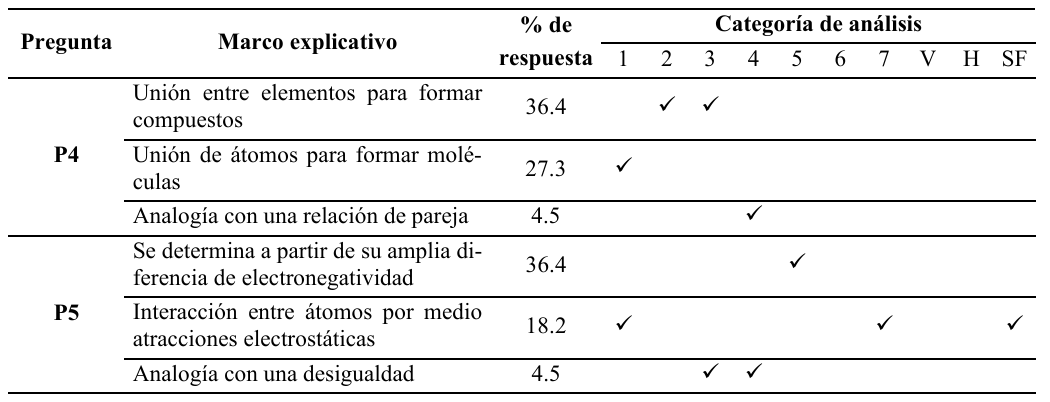
Los marcos explicativos que los profesores consolidaron para los modelos de enlace químico en las preguntas P4 a P6 (Tabla 5), profundizaron los impedimentos pedagógicos 1, 3, 4 y 5, donde el uso de razonamientos antropomórficos fue la dificultad más relevante. No obstante, el 9.1% de las respuestas a la pregunta P5 condicionaron el enlace iónico a la naturaleza de sus constituyentes y lo justificaron con base en la transferencia electrónica, validando tanto un modelo de pares iónicos en vez de una estructura reticular (Hunter et al., 2022), como la dependencia de las propiedades de los compuestos a la suma de las propiedades de sus elementos, problema filosófico conocido como emergencia (Newman, 2013).
La referencia de los profesores hacia el cálculo de la diferencia de electronegatividad para clasificar el enlace iónico (36.4%) y covalente (54.5%), falla al no asegurar qué modelo de enlace explicaría las propiedades físicas y químicas de un material (Levy et al., 2010). Su uso frecuente por su utilidad pragmática puede conllevar a errores en el aprendizaje de la polaridad, y a un posible reduccionismo ontológico por su trasfondo referencial complejo, sustentado en la física de partículas aisladas (Ruthenberg y Martínez-González, 2017).
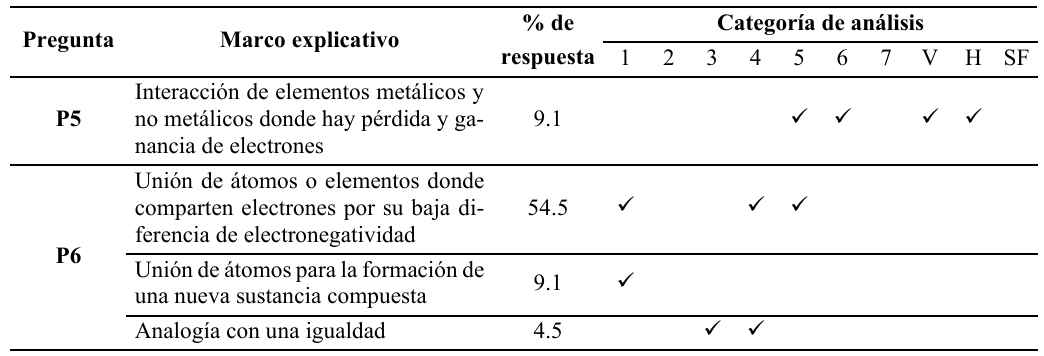
Con el fin de conocer los conceptos que los profesores usan en sus explicaciones frente al enlace químico, las preguntas P7 y P8 corroboraron la importancia de la electronegatividad, la valencia, las estructuras de Lewis y la polaridad en sus construcciones teóricas; en el ítem “otros”, se destaca que un profesor presentó la teoría de OM como un término explicativo y se aproximó a una concepción energética. Los términos restantes siguen ligados a una noción estructural del enlace y a un enfoque electrostático (Figura 3), donde el 45.5% consideró que su uso era esencial para calcular la diferencia de electronegatividad, mientras el 27.3% indicó que los utilizaría para representar las estructuras de Lewis.
Cabe destacar que los profesores usaron los términos átomo y ion de manera indiferente, lo que refleja impedimentos pedagógicos y errores conceptuales provenientes de la ontología atómica y de la dificultad para comprender la naturaleza reticular de los compuestos iónicos. Las respuestas a P7 y P8 evidencian los impedimentos pedagógicos 1, 6 y 7, así como las conjeturas V y SF.
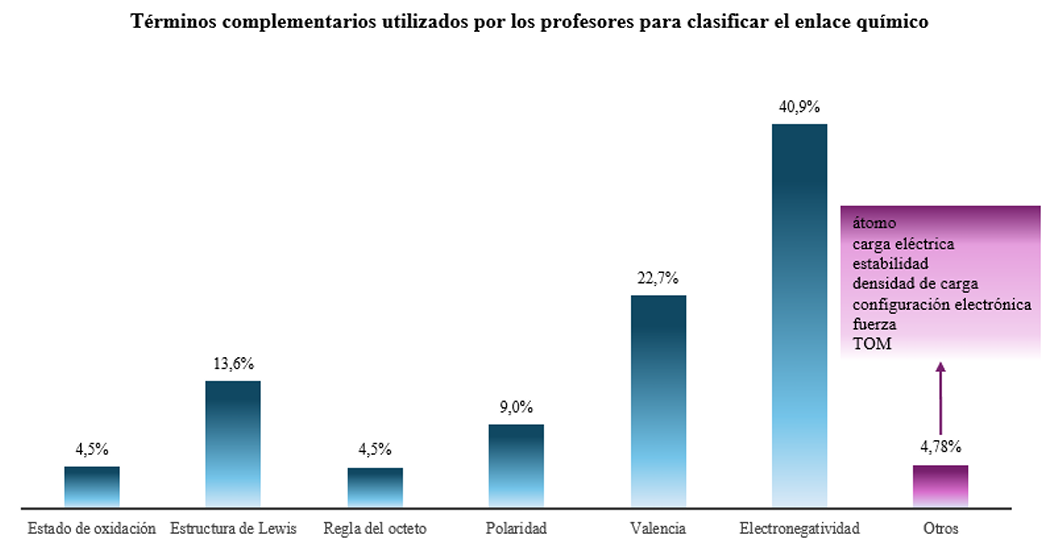
Figura 3
Uso de términos complementarios para explicar el enlace químico
Con relación al significado de la naturaleza del enlace químico, el 54.8% de los profesores no tuvo respuesta, mientras el 27.2% indicó que era una forma de entender el concepto a partir de aproximaciones históricas y epistemológicas. El 18.1% afirmó que esta naturaleza podía explicarse con modelos de esferas y barras o videos tutoriales, lo que evidenció una escasa formación filosófica y epistemológica. En la pregunta P10, los profesores realizaron modelos ingenuos del átomo y el enlace (Zohar y Levy, 2019) limitados por la ontología atómica, la dependencia hacia la regla del octeto y la clasificación dicotómica del enlace, lo cual se relacionó con sus respuestas previas; sin embargo, estos impedimentos fueron más notorios en el enlace covalente, en contraste con lo observado en las preguntas P2 y P5 (Tabla 6).
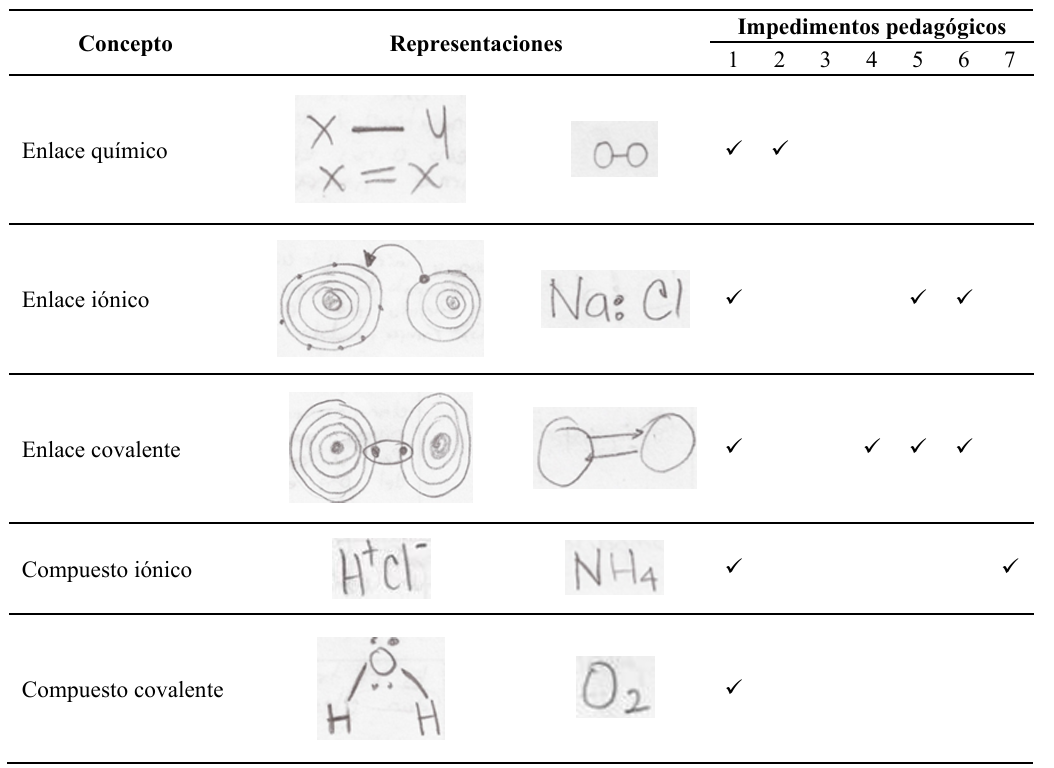
Instrumento sobre naturaleza del enlace químico
A partir de la insistencia de los profesores por explicar el enlace a partir de la interpretación matemática de la diferencia de electronegatividad, este instrumento analizó su eficiencia como herramienta predictiva (Sproul, 2001). En la primera situación, el 36.4% sostuvo que las propiedades físicas de un compuesto dependen de la suma de las propiedades de sus elementos y del número de átomos presentes, recayendo en el problema filosófico de la emergencia (Newman, 2013). Por su parte, el 45.4% afirmó que la electronegatividad no puede explicar las diferencias en los puntos de fusión, lo que evidencia una limitación en su función interpretativa (Sproul, 2001). Además, un profesor manifestó que esta diferencia depende de los números de oxidación para los compuestos iónicos y de la valencia cuántica para cada compuesto, confundiendo las concepciones estructural y energética del enlace.
Las respuestas a P2 no relacionaron, en su mayoría, los conceptos de estado de oxidación, enlace químico, punto de fusión y electronegatividad (Tabla 7), lo que muestra el impacto que tiene la enseñanza tradicional del enlace y el sobreuso de modelos matemáticos que se han dado como definitivos. En algunas respuestas aún se evidencian visiones moleculares del enlace iónico (Taber, 1997), fallas en la relación estructura – reactividad, y conjeturas de SF que confirman la resistencia que tienen los profesores hacia el cambio en su estructura conceptual.
No obstante, el 71.4% de las respuestas sostuvo que la diferencia de electronegatividad no es un criterio relevante para clasificar el enlace, lo que representa un avance significativo en la comprensión de su naturaleza. También se identificaron respuestas que abordaban este concepto desde una perspectiva energética, aunque sin profundizar en los modelos espectros-cópicos de Mulliken y Rochow (Accorinti y Labarca, 2020). Finalmente, algunas posturas asumieron la electronegatividad como una construcción teórica y no como una propiedad (Ruthenberg y Martínez-González, 2017). Estos hallazgos abren nuevas posibilidades para interpretar la electronegatividad y su relación con el enlace químico.
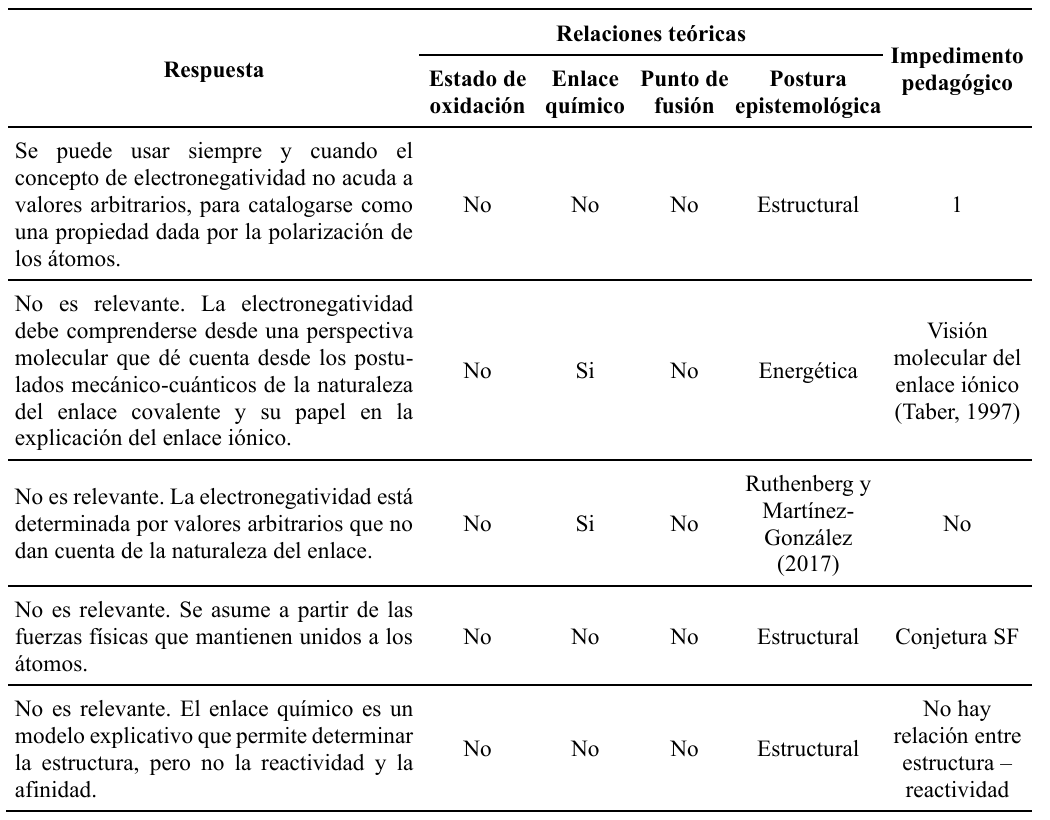
En la situación II, los profesores no identificaron el compuesto ni su modelo de enlace con base en los estados de oxidación del cromo y el osmio. Las respuestas siguieron la misma tendencia de la situación I, y no relacionaron los términos electronegatividad, enlace químico y estado de oxidación como un modelo continuo (Viswanathan y Gulam Razul, 2022; Šima, 2016). El 18.1% no consideró que la pregunta se relacionara con el conocimiento químico y el 31.7% no la respondió, lo que permite afirmar que este caso requiere una explicación más profunda sobre el modelo al que se hace referencia.
¿Otra conjetura para el enlace químico?
Las conjeturas propuestas por Taber (1997) para el enlace iónico provienen de un marco de referencia molecular que se sustenta en un énfasis exagerado en la configuración electrónica, la regla del octeto y la transferencia de electrones en su enseñanza y aprendizaje (García-Franco y Garritz, 2006). Esta línea didáctica no ha cambiado casi tres décadas después, como se muestra en los resultados de este trabajo. No obstante, la discusión epistemológica de la relación entre enlace químico y electronegatividad ha estado desatendida en la investigación en didáctica, cuyos resultados se han limitado a destacar únicamente su importancia en la explicación de conceptos como polaridad de enlace (Tsaparlis et al., 2018; Fatokun, 2016), fuerzas de enlace (Zohar y Levy, 2019) y la relación covalencia – ionicidad como un modelo continuo (Dhindsa y Treagust, 2014; Levy et al., 2008).
El impacto de esta indiferencia en la enseñanza del enlace químico no es menor, ya que muchos profesores siguen acudiendo confiadamente a la diferencia de electronegatividad para clasificar el enlace y proponer estructuras de Lewis. Sin embargo, el problema no radica en el uso de este recurso, sino en la poca comprensión sobre sus alcances y límites, los cuales dependen en gran medida de la interpretación que se tenga de la electronegatividad al construir su marco explicativo. La Tabla 8 propone algunas hipótesis que podrían explicar esta dependencia, fundamentadas en el realismo ingenuo que persiste en los docentes frente a este concepto y sus desafíos epistemológicos.

Si futuros trabajos sobre el enlace químico validan estas hipótesis, podría consolidarse una nueva conjetura en la cual el tipo de enlace se determine únicamente con base en la diferencia de electronegatividad (Δχ) entre los elementos involucrados. Este enfoque asumiría como valores de referencia Δχ > 1.7 para enlaces iónicos, 0.5 ≤ Δχ ≤ 1.7 para enlaces covalentes polares y Δχ < 0.5 para enlaces covalentes no polares. Sin embargo, esta división desestima al menos la mitad de la información contenida en los valores absolutos de electronegatividad, los cuales ofrecen un mayor poder predictivo para reconocer el enlace entre elementos que la simple diferencia matemática de estos (Sproul, 2001).
No obstante, no es necesario renunciar al cálculo de Δχ en la enseñanza del enlace químico, siempre y cuando se lleve al aula como una construcción heurística de un concepto teórico relacional entre los elementos (Ruthenberg y Mets, 2020; Leach, 2013). De esta forma, los estudiantes podrán comprender sus alcances en la predicción del enlace para compuestos sencillos como NaCl o H2O. Es importante resaltar que esta aproximación debe sustentarse en los aspectos epistemológicos mencionados, para evitar que se convierta en un simple atajo de razonamiento que dificulte el pensamiento crítico en los estudiantes (Talanquer, 2010).
Conclusiones
Aunque el presente trabajo mostró las dificultades que tuvieron los profesores para vincular argumentos epistemológicos en la construcción de significados sobre enlace químico desde una perspectiva modelo – teórica, impedimentos pedagógicos y conjeturas en sus nociones y representaciones gráficas, se destaca el valioso avance que presentaron al desvincular la interpretación matemática de la diferencia de electronegatividad como recurso teórico para clasificarlo. Este punto de partida abre nuevos horizontes hacia un análisis reflexivo en torno a la enseñanza y el aprendizaje de estos conceptos en el aula.
No obstante, el uso de esta herramienta matemática no debe estigmatizarse si se enseña como una construcción heurística basada en la naturaleza relacional de los elementos químicos (Leach, 2013). De lo contrario, se estaría cayendo en la conjetura propuesta en este trabajo, que se activa cuando se asignan valores fijos de electronegatividad a los elementos, como si fuera una propiedad natural empíricamente medible.
En relación con los significados del enlace químico, los profesores pueden optar por una concepción estructural afín con el modelo de Lewis y EV, o elegir una concepción energética que se asocia con nuevas formas de enlace y que explica los fenómenos más recientes en la dimensión energética del nivel molecular en las especies químicas (Jensen, 1998). Aunque Bader (2009) haya criticado el modelo tradicional de enlace desde una perspectiva energética, no implica que haya una prevalencia teórica de esta visión sobre la concepción estructural (Scerri, 2023).
Es claro que la concepción estructural y la visión realista del enlace generan mayor confianza en los profesores por su familiaridad con los conceptos aprendidos durante su formación, así como por su éxito en el análisis retrosintético y la química orgánica (Ochiai, 2025). Sin embargo, no se debe caer en el realismo ingenuo y creer que los modelos físicos y simbólicos provistos en los libros de texto son representaciones fieles de lo que sucede a nivel molecular y energético (Matus et al, 2011).
Respecto a los significados del enlace iónico y covalente, las aplicaciones propuestas por García-Franco y Garritz (2006) se consideran vigentes y fáciles de implementar en el aula. No obstante, resulta pertinente evaluar la secuencia alternativa de enseñanza del enlace químico propuesta por Dhindsa y Treagust (2014), procurando no depender en exceso de la diferencia de electronegatividad y el solapamiento de orbitales como principios explicativos.
Agradecimientos
A los revisores de este trabajo por sus valiosos aportes.
Referencias bibliográficas
Accorinti, H. L., y Labarca, M. G. (2020). Commentary on the models of electronegativity. Journal of Chemical Education, 97(10), 3474-3477.
Atkins, P. (1999). Chemistry: the great ideas. Pure and Applied Chemistry, 71(6), 927-929.
Bader, R. (2009). Bond Paths Are Not Chemical Bonds. The Journal of Physical Chemistry, 113(38), 10391-10396.
Bader, R., Hernández-Trujillo, J. y Cortés-Guzman, F. (2006). Chemical Bonding: From Lewis to Atoms in Molecules. Journal of Computational Chemistry, 28(1), 4 -14.
Brown, T., LeMay Jr, H., Murphy, C., Bursten, B. y Woodward, P. (2014). Química. La Ciencia Central (Decimosegunda ed.). Pearson Education.
Cairns, M. (2023). Electronegativity as a new case for emergence and a new problem for reductionism. Foundations of Chemistry, 27(1), 1-16.
Chamizo, J. (2010). El conocimiento químico. En J. A. Chamizo (Ed.), Historia y Filosofía de la Química. Aportes para la enseñanza (págs. 210-236). Siglo XXI Editores.
Coulson, C. (1955). The contributions of wave mechanics to chemistry. Journal of the Chemical Society, 2069-2084.
Dhindsa, H. S., y Treagust, D. F. (2014). Prospective pedagogy for teaching chemical bonding for smart and sustainable learning. Chemistry Education Research and Practice, 15(4), 435-446.
Erduran, S. y Mugaloglu, E. (2014). Philosophy of Chemistry in Chemical Education: Recent Trends and Future Directions. En M. Matthews, International Handbook of Research in History (págs. 287-315). Springer.
Erduran, S. y Scerri, E. (2002). The Nature of Chemical Knowledge and Chemical Education. En J. Gilbert (Ed), Chemical Education: Towards Research-based Practice (págs. 7-27). Kluwer Academic Publishers.
Fatokun, K. V. F. (2016). Instructional misconceptions of prospective chemistry teachers in chemical bonding. International Journal of Science and Technology Education Research, 7(2), 18-24.
García-Franco, A. y Garritz, A. (2006). Desarrollo de una unidad didáctica: El estudio del enlace químico en el bachillerato. Enseñanza de las Ciencias, 24(1), 111-124.
Gavroglu, K. y Simões, A. (2012). Quantum Chemistry qua Programming: Computers and the Cultures of Quantum Chemistry. The MIT Press.
Gillespie, R. (1997). The Great Ideas of Chemistry. Journal of Chemical Education, 74(7), 862-864.
Gillespie, R. (2006). El enlace químico y la geometría molecular. Educación química, 17(4e), 264-273.
Gillespie, R. J., y Popelier, P. L. A. (2001). Chemical bonding and molecular geometry: From Lewis to electron densities. Oxford University Press.
Hendry, R. (2008). Two concepts of the chemical bond. Philosophy of Science, 75, 909-920.
Hunter, K. H., Rodriguez, J.-M. G., y Becker, N. M. (2022). A review of research on the teaching and learning of chemical bonding. Journal of Chemical Education, 99(7), 2451-2464.
Jensen, W. (1998). Logic, History, and the Chemistry Textbook I. Does Chemistry Have a Logical Structure? Journal of Chemical Education, 75(6), 679-687.
Joki, J., y Aksela, M. (2018). The challenges of learning and teaching chemical bonding at different school levels using electrostatic interactions instead of the octet rule as a teaching model. Chemistry Education Research and Practice, 19(3), 932-953.
Labarca, M. (2011). La Filosofía de la Química en la Filosofía de la Ciencia Contemporánea. Redes, 11(021), 155-171.
Leach, M. R. (2013). Concerning electronegativity as a basic elemental property and why the periodic table is usually represented in its medium form. Foundations of Chemistry, 15(1), 13-29.
Lee, R. y Cheng, M. (2014). The Relationship Between Teaching and Learning of Chemical Bonding and Structures. En C. T. Bruguière, Topics and Trends in Current Science Education: 9th ESERA Conference Selected Contributions (págs. 403-417). Springer.
Levy Nahum, T., Mamlok-Naaman, R., Hofstein, A., y Kronik, L. (2008). A new “bottom-up” framework for teaching chemical bonding. Journal of Chemical Education, 85(12), 1680-1685.
Levy Nahum, T., Mamlok-Naaman, R., Hofstein, A., y Taber, K. (2010). Teaching and learning the concept of chemical bonding. Studies in Science Education, 46(2), 179-207.
Levy Nahum, T., Mamlok-Naaman, y Hofstein, A. (2013). Teaching and Learning of the Chemical Bonding Concept: Problems and Some Pedagogical Issues and Recommendations. En G. T. Sevian, Concepts of Matter in Science Education (págs. 373-390). Springer Dordrecht.
Lombardi, O. y Labarca, M. (2005). The Ontological Autonomy Of The Chemical World. Foundations of Chemistry, 7, 125-148.
Lombardi, O. y Martínez, J. (2012). Entre mecánica cuántica y estructuras químicas: ¿a qué refiere la química cuántica? Scientiæ studia, 10(4), 649-670.
Matus, L., Benarroch, A., y Nappa, N. (2011). La modelización del enlace químico en libros de texto de distintos niveles educativos. Revista Electrónica de Enseñanza de las Ciencias, 10(1), 178-201.
Needham, P. (2014). The source of chemical bonding. Studies in History and Philosophy of Science, 45, 1-13.
Newman, M. (2013). Emergence, supervenience, and introductory chemical education. Science & Education, 22(7), 1655-1667.
Ochiai, H. (2020). Understanding molecular structure requires constructive realism. Foundations of Chemistry, 22, 457-465.
Ochiai, H. (2025). Why do chemists take the chemical bond as real? Foundations of Chemistry, 27, 173-181.
Pauling, L. (1928). The Application of the Quantum Mechanics to the Structure of the Hydrogen Molecule and Hydrogen Molecule-Ion and to Related Problems. Chemical Reviews, (2), 173-213.
Piechota, E. J., y Meyer, G. J. (2019). Introduction to electron transfer: Theoretical foundations and pedagogical examples. Journal of Chemical Education, 96(11), 2450-2466.
Pizzochero, M. (2025). The Fuzzy Logic of the Chemical Bond. Journal for General Philosophy of Science, 56(2), 1-9.
Rubiano, D (2017) El estatuto ontológico de la concepción estructural del enlace químico: aportes a la didáctica de la química. [Tesis de Maestría, Universidad Pedagógica Nacional]. Repositorio Institucional – Universidad Pedagógica Nacional.
Ruedenberg, K. y Schmidt, M. (2007). Why does electron sharing lead to covalent bonding? A variational analysis. Journal of Computational Chemistry, 28(1), 391-410.
Ruthenberg, K. y Martínez-González, J. (2017). Electronegativity and its multiple faces: persistence and measurement. Foundations of Chemistry, 19, 61-75.
Ruthenberg, K. y Mets, A. (2020). Chemistry is pluralistic. Foundations of Chemistry, 22(3), 403-419.
Scerri, E. (2023). A commentary on Weisberg’s critique of the ‘structural conception’ of chemical bonding. Foundations of Chemistry, 25, 253-264.
Scerri, E. y McIntyre, L. (1997). The Case of the Philosophy of Chemistry. Synthese, 111, 213-232.
Seifert, V. (2023). The Chemical Bond is a Real Pattern. Philosophy of Science, 90(2), 269-287.
Shimajiri, T., Kawaguchi, S., Suzuki, T. y Y, I. (2024). Direct evidence for a carbon–carbon one-electron σ-bond. Nature, 634, 347-351.
Šima, J. (2016). Structure-related melting and boiling points of inorganic compounds. Foundations of Chemistry, 18, 67-79.
Sproul, G. (2001). Electronegativity and Bond Type: Predicting Bond Type. Journal of Chemical Education, 78(3), 387-390.
Taber, K. (1997). Student understanding of ionic bonding: molecular versus electrostatic thinking? School Science Review, 78(285), 85-95.
Taber, K. (2001). Building the Structural Concepts of Chemistry: Some Considerations From Educational Research. Chemistry Education: Research and Practice in Europe, 2(2), 123-158.
Taber, K. y Coll, R. (2002). Bonding. En J. Gilbert., Chemical Education: Towards Research-based Practice (págs. 213-234). Kluwer Academic Publishers.
Taber, K. S., Tsaparlis, G., y Nakiboğlu, C. (2012). Student Conceptions of Ionic Bonding: Patterns of thinking across three European contexts. International Journal of Science Education, 34(18), 2843-2873.
Talanquer, V. (2010). Pensamiento intuitivo en química: suposiciones implícitas y reglas heurísticas. Enseñanza de las Ciencias, 28(2), 165-174.
Tsaparlis, G., Pappa, E. T., y Byers, B. (2018). Teaching and learning chemical bonding: Research‑based evidence for misconceptions and conceptual difficulties experienced by students in upper secondary schools and the effect of an enriched text. Chemistry Education Research and Practice, 19(4), 1253-1269.
Vemulapalli, K. y Byerly, H. (1999). Remnants of Reductionism. Foundations of Chemistry, 1, 17-41.
Viswanathan, B., y Gulam Razul, M. S. (2022). Electronegativity provides the relationship between formal charge, oxidation state, and actual charge. Foundations of Chemistry, 25(1), 5-28.
Weisberg, M. (2008). Challenges to the structural conception of chemical bonding. Philosophy of Science, 75, 932-946.
Zohar, A. R., y Levy, S. T. (2019). Attraction vs. repulsion – learning about forces and energy in chemical bonding with the ELI‑Chem simulation. Chemistry Education Research and Practice, 20(4), 667-684.
Información adicional
Para citar este artículo: Aponte-Buitrago, R. y Garay, F. (2025). Concepciones epistemológicas sobre enlace químico en la práctica profesional de los profesores de química. Revista Eureka sobre Enseñanza y Divulgación de las Ciencias 22(3), 3602. https://doi.org/10.25267/Rev_Eureka_ensen_divulg_cienc.2025.v22.i3.3602
Declaración de autoría: Ricardo Aponte-Buitrago: conceptualización, investigación, metodología, análisis formal, visualización y redacción (revisión y edición). Fredy Garay Garay: conceptualización, validación, recursos y supervisión.
Información adicional
redalyc-journal-id: 920
