Síntesis y actividad antimicrobiana de derivados de pirimidinas análogas de uracilo
Síntesis y actividad antimicrobiana de derivados de pirimidinas análogas de uracilo
Avances en Química, vol. 11, núm. 1, pp. 17-24, 2016
Universidad de los Andes
Recepción: 18/09/2015
Revisado: 02/02/2016
Aprobación: 15/02/2016
Financiamiento
Fuente: Instituto de Investigaciones Farmacéuticas de la Facultad de Farmacia de la Universidad Central de Venezuela
Nº de contrato: (Proyecto IIF: 02/2014)
Financiamiento
Fuente: CDCH-UCV
Nº de contrato: PG-06-8827-2013/1 y 2013/2)
Resumen: Se reporta la síntesis de una serie de derivados de 6-amino-5-(arilmetilideno)-pirimidina-2,4-dionas 2a-l, análogas de uracilo. Esta involucra una reacción de ciclocondensación entre los derivados de (E)-2-ciano-3-fenil acrilato de etilo 1a-l y urea asistida por K2CO3. 1a-l fueron obtenidos por condensación de aldehídos aromáticos con cianoacetato de etilo en presencia de una cantidad catalítica de KOH. Todos los compuestos fueron caracterizados por el análisis de los datos espectroscópicos de IR, RMN 1H y RMN 13C. También se reportan los resultados de la actividad antimicrobiana in vitro de todos los compuestos sintetizados contra Staphylococcus aureus, Bacillus cereus, Escherichia coli, Pseudomonas aeruginosa y la levadura Candida tropicalis.
Palabras clave: pirimidina, actividad antimicrobiana: (E)-2-ciano-3-fenil acrilato de etilo.
Abstract: The synthesis of a series of 6-amino-5-(arylmethylideno)-pyrimidine-2,4-diones derivatives uracil analogues 2a-l is reported. This involves a cyclocondensation reaction between Ethyl-(E)-2-cyan-3-phenylacrylate derivatives 1a-l and urea assisted by K2CO3. 1a-l were obtained by condensation of aromatic aldehydes with ethyl cyanoacetate in the presence of a catalytic amount of KOH. All compounds were characterized by spectroscopic data analysis of IR, 1H and 13C NMR. The results of the in vitro antimicrobial activity against Staphylococcus aureus, Bacillus cereus, Escherichia coli, Pseudomonas aeruginosa and Candida tropicalis yeast of all the compounds synthesized are also reported.
Keywords: Pyrimidine, Antimicrobial activity, Ethyl-(E)-2-cyan-3-phenylacrylate.
Introducción
Químicamente, las pirimidinas son anillos de 6 miembros con dos átomos de nitrógeno en las posiciones 1 y 3. Existen tres derivados importantes que forman parte de los ácidos nucleicos, citosina, uracilo y timina (figura 1). La citosina posee un grupo carbonilo en el carbono 2 mientras que uracilo y timina lo poseen dos, en los carbonos 2 y 4. La timina y la citosina forman parte del ADN y el uracilo está presente en el ARN. Los derivados de pirimidinas ocupan un lugar importante en la química medicinal debido a la gran diversidad de propiedades farmacológicas que poseen, entre las que se incluyen, actividad antitumoral,2,3,4; antiviral5; anticancerígena6; antibacterial7; antiinflamatoria8; anticonvulsivante9,10, antifúngica11 y antimicrobiana12,13,14. Los derivados de pirimidinas con actividad antimicrobiana, están relacionados con la habilidad de inhibir enzimas involucradas en la biosíntesis del ADN tales como dihidrofolato reductasa (DHFR) del microorganismo invasor15.
Las enfermedades fúngicas y bacterianas originan la mayor morbilidad en cualquier especialidad médica y frecuentemente también la mortalidad en pacientes inmuno-suprimidos16. Un alto porcentaje de infecciones hospitalarias se debe a bacterias gram positivas resistentes, como por ejemplo Staphylococcus aureus17,18,19. En Venezuela, se han reportado cifras alarmantes de cepas resistentes a múltiples drogas de Staphylococcus aureus20.
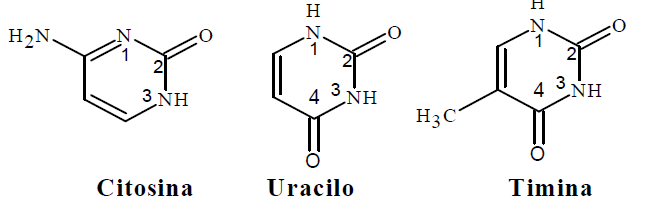
Fig. 1:
Derivados de pirimidinas presentes en los ácido nucleicos.
La resistencia a los antimicrobianos disponibles permite que las infecciones por microorganismos resistentes que no responden a los tratamientos habituales, prolonga la enfermedad y aumenta el riesgo de muerte, y pone en peligro el control de las enfermedades infecciosas. La resistencia reduce la eficacia del tratamiento, y los enfermos continúan infectados por más tiempo, hecho que a su vez propicia la propagación de los microorganismos resistentes a otras personas21. Entre los antimicrobianos derivados de pirimidinas inhibidores de DHFR se encuentran el trimetoprin; la pirimetamina; 5-fluoruracilo y epiroprim22 (figura 2).
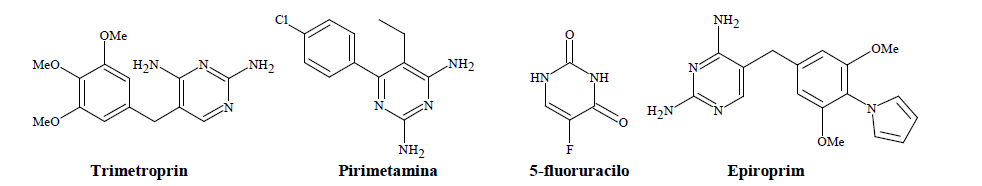
Fig. 2:
Derivados de pirimidinas inhibidoras de DHFR.
Como parte de un proyecto para la síntesis de compuestos heterociclos y evaluación de su actividad biológica, previamente hemos reportado la síntesis y actividad antimicrobiana de derivados de pirimidinas análogas de citosina23, 24. En este artículo presentamos los resultados de la síntesis y actividad antimicrobiana de una serie de derivados de pirimidinas análogas de uracilo 2a-l (figura 3). En estas nuevas estructuras, se introduce el grupo arilmetilideno en la posición 5 y un grupo amino en la posición 6 del uracilo.
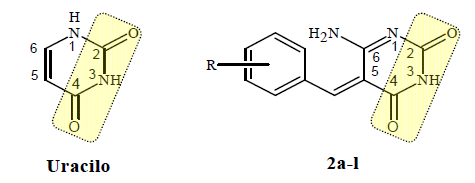
Fig. 3:
Cambios estructurales realizados en las posiciones C5 y C6 del uracilo.
Parte experimental
Caracterización general
Los puntos de fusión de los sólidos obtenidos fueron determinados en un aparato Fisher Johns y están sin corregir. Los espectros de infrarrojo (IR) se registraron usando pastillas de KBr, en un espectrofotómetro Shimadzu 470, las absorciones más importantes son señaladas y designadas en cm-1. Los espectros de RMN 1H y 13C fueron obtenidos en un espectrómetro JEOL 270 MHz. El desplazamiento químico ( δ ) está reportado en ppm con relación al CHCl3 o DMSO residual interno y las señales se representan como singlete (s), singlete ancho (sa), doblete (d), doblete de dobletes (dd), triplete (t), cuarteto (c), multiplete (m), constante de acoplamiento (J) y valor de la constante de acoplamiento en Hertz (Hz). Los reactivos cianoacetato de etilo y los diferentes aldehídos aromáticos fueron adquiridos de Aldrich Chemical Co. El carbonato de potasio, la urea y el alcohol absoluto fueron obtenidos de Riedel-de Haën.
Síntesis de los derivados (E)-2-ciano-3-fenilacrilato de etilo(1a-l)
A una solución de cianoacetato de etilo (10 mmoles) y el benzaldehído correspondiente (10 mmoles), en etanol anhidro (25 mL), se le añadió una cantidad catalítica de hidróxido de potasio. La mezcla de reacción se dejó agitando a temperatura ambiente hasta la aparición de un sólido, que indicó la formación del producto (30 m-24 h). El sólido formado se filtró y lavó con agua destilada, se dejó secar al aire y luego se recristalizó en etanol. Los cristales formados se filtraron y secaron en una estufa al vacío. El análisis de los datos espectroscópicos de RMN 1H y 13C fueron consistentes con las estructuras esperadas para los productos 1a-l (figura 4).
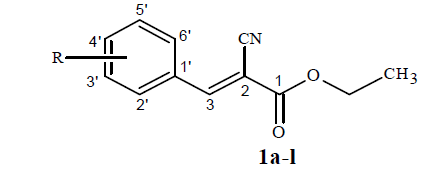
Fig. 4:
Estructura y esquema de asignación de los datos de RMN 1H y RMN 13C de los intermediarios 1a-l.
(E)-2-ciano-4-nitrocinamato de etilo1a. Cristales anaranjadas. Rto: 55 %; P.f: 172 ºC, reportado: 170-171 °C27. IR (KBr, cm-1): 2988 (CH2CH3); 2220 (C≡N); 1715 (C═O); 1594 (CH-Ar); RMN 1H (CDCl3, 270 MHz) δ: 1,41 (t, 3H, CH2CH3); 4,39 (c, 2H, CH2CH3); 8,13 (dd, 2H, J=8,1 y 1,9 Hz, H2’, H6’ ); 8,17 (s, 1H, H3); 8,29 (dd, 2H, J=8,1 y 1,98 Hz, H3’, H5’);. RMN 13C (CDCl3, 69 MHz) δ: 14,1(CH3); 63,3 (CH2); 107,6 (C2); 114,5 (CN); 124,2 (C2’, C6’); 131,5 (C3’, C5’); 137,01 (C1’), 149,9 (C4’); 151,6 (C3); 161,4 (C=O).
(E)-2-ciano-4-fluorcinamato de etilo1b. Cristales blancos Rto: 91 %. P.f: 78-80 ºC. IR (KBr, cm-1): 2996 (CH2CH3); 2220 (C≡N); 1717 (OC═O); 1600 (CH-Ar). RMN-1H (CDCl3, 270 MHz) δ: 1,38 (t, 3H, CH2CH3); 4,35 (c, 2H, CH2CH3); 7,18 (td, 2H, J=8,8; 8,3 y 1,8 Hz, F, H3’, H5’); 8,01 (td, 2H, J=8,8; 6,2 y 1,8 Hz, F, H2’, H6’); 8,19 (s, 1H, H3). RMN-13C (CDCl3, 69 MHz) δ: 14,1 (CH3); 62,7 (CH2); 102,9 (C2); 115,3 (CN); 116,9 (C3’, C5’); 128,0 (C1’); 133,5 (C2’, C6’); 153,3 (C3); 163,5 (C4’); 167,5 (C=O).
(E)-2-ciano-4-clorocinamato de etilo1c. Sólido verde. Rto: 96 %. P.f: 88 ºC, reportado: 89-90 °C27. IR (KBr, cm-1): 2996 (CH2CH3); 2216 (C≡N); 1715 (C═O); 1600 (CHAr). RMN-1H (CDCl3, 270 MHz) δ:1,36 (t, 3H, CH2CH3); 4,36 (c, 2H, CH2CH3); 7,48 (dd, 2H, J=8,42y 2,2Hz, H3’, H5’); 7,94 (dd, 2H, J=8,4 y 2,2 Hz, H2’, H6’); 8,19 (s, 1H, H3). RMN-13C (CDCl3, 69 MHz), δ: 14,1 (CH3); 62,8 (CH2); 103,7 (C2); 115,2 (CN); 129,7 (C3’, C5’); 130,0 (C1’); 132,2 (C2’, C6’); 139,5 (C4’); 153,3(C3); 162,2 (C=O).
(E)-2-ciano-3,4-diclorocinamato de etilo1d. Cristales verdes. Rto: 97 %. P.f: 120-122 ºC. IR (KBr, cm-1): 2980 (CH2CH3); 2216 (C≡N); 1715 (OC═O); 1606 (CH-Ar). RMN-1H (CDCl3, 270 MHz) δ: 1,38 (t, 3H, CH2CH3); 4,39 (c, 2H, CH2CH3); 7,58 (d, 1H, J=8,4 Hz, H5’); 7,98 (dd, 1H, J=10,1 y 2,2 Hz, H6’); 7,9 (d, 1H, J=1,9 Hz, H2’); 8,13 (s, 1H, H3). RMN-13C (CDCl3, 69 MHz), δ: 14,1 (CH3); 63,3 (CH2); 107,6 (C2); 114,4 (CN); 123,0 (C5’); 125,9 (C6’); 128,0 (C2’); 129,9 (C1’); 132,0 (C3’); 137,0 (C4’); 152,0 (C3); 161,7 (C=O).
(E)-2-ciano-4-bromocinamato de etilo1e. Cristales amarillos. Rto: 95 %. P.f: 86-88 ºC. IR (KBr, cm-1): 2984 (CH2CH3); 2208 (C≡N); 1715 (OC═O); 1608 (Ar). RMN-1H (CDCl3, 270 MHz) δ: 1,38 (t, 3H, CH2CH3); 4,36 (c, 2H, CH2CH3); 7,65 (dd, 2H, J=8,3 y 1,7 Hz, H3’, H5’), 7,84 (dd, 2H, J=8,4 y 1,7 Hz, H2’, H6’); 8,17 (s, 1H, H3). RMN-13C (CDCl3, 69 MHz), δ: 14,2 (CH3); 62,4 (CH2); 99,6 (C2); 112,1 (CN); 124,8 (C1’); 127,7 (C3’, C5’); 132,7 (C2’, C6’); 149,5 (C4’); 154,5 (C3); 163,1 (C=O).
(E)-2-ciano-cinamato de etilo1f. Cristales verdes. Rto: 98 %. P.f: 51 ºC, reportado: 49-50 °C27. IR (KBr, cm-1): 2992 (CH2CH3); 2208 (C≡N); 1715 (OC═O); 1606 (Ar). RMN-1H (CDCl3, 270 MHz) δ: 1,38 (t, 3H, CH2CH3); 4,36 (c, 2H, CH2CH3); 7,52 (m, 3H, H-Ar); 7,97 (dd, 2H, J=7,6 y 1,9 Hz, H-Ar); 8,24 (s, 1H, H3). RMN-13C (CDCl3, 69 MHz), δ: 14,2 (CH3); 62,7 (CH2); 103,4 (C2); 115,4 (CN); 131,1 (C-Ar); 131,1 (C-Ar); 131,7 (C-Ar); 133,2 (C-Ar); 154,9 (C3); 162,5 (C=O).
(E)-2-ciano-4-metilcinamato de etilo1g. Cristales verdes. Rto: 99 %. P.f: 92 ºC, reportado: 90-92 °C27. IR (KBr, cm-1): 3000 (CH2CH3); 2208 (C≡N); 1718 (OC═O); 1594 (CH-Ar). RMN-1H (CDCl3, 270 MHz) δ:1,38 (t, 3H, CH2CH3); 2,42 (s, 3H, CH3); 4,38 (c, 2H, CH2CH3); 7,29 (dd, 2H, J=8,2 y 2,7 Hz, H3’, H5’) 7,89 (dd, 2H, J=8,2 y 2,7 Hz, H2, H6’); 8,20 (s, 1H, =CH, H3). RMN-13C (CDCl3, 69 MHz), δ: 14,2 (CH3); 21,8 (Ar-CH3); 62,6 (CH2); 101,7 (C2); 115,7 (C≡N); 129,1(C1’); 130,1 (C3’, C5’); 131,3 (C2’, C6’); 144,6 (C4’); 155,0 (C3); 162,3 (C═O).
(E)-2-ciano-4-metoxicinamato de etilo1h. Sólido blanco. Rto: 94 %. P.f: 80ºC, reportado: 79-81 °C27. IR (KBr, cm-1): 2988 (CH2CH3); 2208 (C≡N); 1712 (OC═O); 1584 (CH-Ar). RMN-1H (CDCl3, 270 MHz) δ : 1,38 (t, 3H, CH2CH3); 3,88 (s, 3H, OCH3); 4,37 (c, 2H, CH2CH3); 6,98 (dd, 2H, J=8,91 y 2,00 Hz, H3’, H5’); 7,99 (dd, 2H, J=8,64 y 1,73 Hz, H2’, H6’); 8,16(s, 1H, H3). RMN-13C (CDCl3, 69 MHz), δ : 14,21 (CH3); 55,63 (OCH3); 62,42 (CH2); 99,75(C2); 114,85 (C3’, C5’); 116,17 (C≡N); 124,54 (C1’); 133,63 (C2’, C6’); 154,30 (C3); 163,14 (C=O); 163,87 (C4’).
(E)-2-ciano-3,4-dimetoxicinamato de etilo1i. Sólido beige. Rto: 93 %. P.f: 150-152 ºC. IR (KBr, cm-1): 2976 (CH2CH3); 2216 (C≡N); 1710 (C═O); 1600 (Ar). RMN-1H (CDCl3, 270 MHz) δ : 1,38 (t, 3H, , CH2CH3); 3,95 (s, 6H, 2OCH3); 4,37 (c, 2H, CH2CH3); 6,93 (d, 1H, J=8,6 Hz, H5’); 7,46 (dd, 1H, J=10,6 y 2,2 Hz, H6’); 7,78 (d, 1H, J=2,2 Hz, H2’); 8,14 (s, 1H, H, H3). RMN-13C (CDCl3, 69 MHz), δ: 14,17 (CH3); 56,0 (CH2); 62,9 (2OCH3); 103,9 (C2); 115,3 (CN); 128,3 (C1’); 130,4 (C5’); 132,2 (C6’); 132,7 (C2’); 147,0 (C3’); 151,0 (C3); 153,4 (C4’); 162,2 (C═O).
(E)-2-ciano-3,4,5-trimetoxicinamato de etilo 1j. Cristales amarillos. Rto: 85 %. P.f: 48 ºC, reportado: 46-48 °C27. IR (KBr, cm-1): 2976 (CH2CH3); 2208 (C≡N); 1731 (C═O); 1600 (CHAr). RMN-1H (CDCl3, 270 MHz) δ: 1, 38 (t, 3H, CH2CH3); 3,90 (s, 6H, 2OCH3); 3,94 (s, 3H, OCH3); 4, 38 (c, 2H, CH2CH3); 7, 28 (s, 2H, H2’, H6’); 8,13 (s, 1H, H3). RMN-13C (CDCl3, 69 MHz), δ: 14,2 (CH3); 56,4 (CH2); 61,1 (OCH3); 62,7 (2OCH3); 101,5 (C2); 108,8 (C2’, C6’); 115,9 (CN); 126,6 (C1’); 143,0 (C3’, C5’); 153,4 (C3); 154,8 (C4’); 162,8 (C═O).
(E)-2-ciano-4-metilaminocinamato de etilo1k. Cristales anaranjados. Rto: 96 % P.f: 140-142 ºC. IR (KBr, cm-1): 2984 (CH2CH3); 2208 (C≡N); 1727 (OC═O); 1600 (CH-Ar). RMN-1H (CDCl3, 270 MHz) δ: 1,38 (t, 3H, CH2CH3); 3,09 (s, 6H, N(CH3)2); 4,31(c, 2H, CH2CH3); 6,72 (dd, 2H, J=8,9 y 2,7 Hz, H3’, H5’); 7,93 (dd, 2H, J=8,7 y 2,7 Hz, H2’, H6’); 8,06 (s, 1H, H3). RMN-13C (CDCl3, 69 MHz), δ:14,3 (CH3); 39,6 (N(CH3)2); 56,4 (CH3); 101,5 (C2); 112,2 (C3’, C5’); 116,0 (CN); 126,6 (C1’); 143,0 (C2’, C6’); 154,4 (C3); 155,0 (C4’); 162,8 (C=O).
(E)-2-ciano-4-hidroxicinamato de etilo 1l. Sólido marrón. Rto: 90 %. P.f: 170 ºC, reportado: 169-171 °C27. IR (KBr, cm-1): 3640 (OH); 2992 (CH2CH3); 2224 (C≡N); 1729 (C═O); 1600 (CH-Ar). RMN-1H (CDCl3, 270 MHz) δ: 1,38 (t, 3H, CH2CH3); 4,35 (c, 2H, CH2CH3); 6,25 (ba, 1H, OH); 6,96 (dd, 2H, J=8,9 y 2,2 Hz, H3’, H5’); 7,96(dd, 2H, J=8,9 y 2,2 Hz, H2’, H6’); 8,18 (s, 1H, H3). RMN-13C (CDCl3, 69 MHz), δ: 14,2 (CH3); 62,6 (CH2); 99,4 (C2); 116,2 (CN); 116,5 (C3’, C5’); 124,5 (C1’); 133,9 (C2’, C6’); 154,8 (C3); 160,8 (C4’); 163,1(C=O).
Síntesis de los derivados de 6-amino-5-arilmetilidenopirimidina- 2,4-dionas análogas de uracilo2a-l.
Una solución de urea (78 mg, 1,20 mmoles), carbonato de potasio (170 mg, 1,20 mmoles) en etanol anhidro (10 mL) fue calentada a la temperatura de reflujo hasta la formación de una solución traslúcida. Luego se agregó cuidadosamente el respectivo derivado 1a-l (0,6 mmoles) disuelto en etanol (5mL). La mezcla de reacción se dejó agitando bajo reflujo hasta la formación de una sal. El solvente se eliminó a presión reducida. Al residuo resultante se le agregó agua (5 mL). Cualquier sobrenadante se eliminó filtrando a gravedad. Al filtrado se le añadió HCl al 10 % gota a gota hasta pH neutro. El sólido formado se filtró y recristalizó en DMF/etanol caliente. El análisis de los datos espectroscópicos de IR, RMN de 1H y 13C fueron consistentes con las estructuras de las pirimidinas esperadas 2a-l (figura 5).
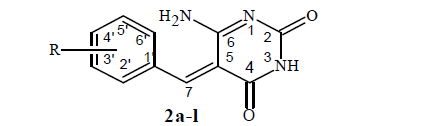
Fig. 5:
Estructura y esquema de asignación de los datos de RMN 1H y RMN 13C de las pirimidinas 2a-l.
6-amino-5-[(4’-nitrofenil)metilideno]pirimidina-2,4-diona(2a): Cristales rojos. Rto: 90 %. P.f: 130-134 ºC. IR (KBr, cm-1): 3750, 3675 (NH2); 3265 (NH); 1715 (C=O, C2); 1680 (C=O, C4); 1600 (CH-Ar), 1504 (C═C). RMN-1H (DMSOd6, 270 MHz) δ: 5,39 (s, 2H NH2, intercambio con D2O); 6,92 (dd, 2H, J=8,1 y 1,9 Hz, H2’, H6’); 7,35 (dd, 2H, J=8,0 y 1,9 Hz, H3’, H5’); 8,30 (s, 1H, H7); 10,12 (sa, 1H, NH, intercambio con D2O). RMN-13C (DMSOd6, 69 MHz) δ: 116,3 (C5); 126,6 (C2’, C6’); 129,0 (C3’, C5’); 139,0 (C1’); 148,8 (C4’); 150,9 (C7); 161,0 (C=O); 162,0 (C=O); 166,0 (C6).
6-amino-5-[(4’-fluorfenil)metilideno]pirimidina-2,4-diona (2b): Solido amarillo. Rto: 88 %. Pf: 258 ºC desc. IR (KBr, cm-1): 3536, 3461 (NH2); 3265 (NH); 1721 (C=O, C2); 1680 (C=O, C4); 1593 (CH-Ar); 1510 (C═C). RMN-1H, (DMSOd6 270 MHz) δ: 5,77 (s, 2H, NH2, intercambio con D2O); 7,41 (ddd, 2H, J=8,8 y 6,2, 1,9 Hz, 1F, H3’,H5’); 7,60 (ddd, 2H, J=8,8, 8,3 y 1,9 Hz, 1F, H2’,H6’); 7,61 (s, 1H, H7); 7,89-8,07 (ba, 1H, NH, intercambio con D2O. RMN-13C, (69 MHz, DMSOd6), δ: 115,9 (C5); 116,5 (C3’, C5’); 131,5 (C2’, C6’); 131,6 (C1’); 145,2 (C7); 160,3 (C=O, C2); 161,7 (C4’); 164,9 (C=O, C4); 166,2 (C6).
6–amino–5-[(4’-clorofenil)metilideno]pirimidin-2,4-diona(2c): Sólido blanco. Rto: 87 %. Pf: 240 ºC desc. IR (KBr, cm-1): 3536, 3461 (NH2); 3265 (NH), 1792 (C=O, C2); 1685 (C=O, C4) 1600(CH-Ar); 1510 (C=C). RMN-1H, (DMSOd6 270 MHz) δ: 5,77 (s, 2H, NH2 intercambio con D2O); 7,35 (dd, 2H, J=8,1 y 2,0 Hz, H3’, H5’); 8,08 (dd, 2H, J=8,1 Hz y 2,0 Hz, H2’, H6’); 8,34 (s, 1H, H7); 8,99 (ba, 1H, NH, intercambio con D2O). RMN-13C, (69 MHz, DMSOd6) δ: 117,0 (C5); 125,3 (C1’); 130,0 (C3’, C5’); 132,0 (C2’, C6’); 134,0 (C4’); 145,0 (C7); 160,4 (C=O); 162,0 (C=O); 166,4 (C6).
6-amino-5-[(3’,4’-diclorofenil)metilideno]pirimidina-2,4- diona(2d): Solido blanco. Rto: 85 %. Pf: 172-174 ºC. IR (KBr, cm-1): 3744, 3644 (NH2); 3287 (NH); 1715 (C=O, C2); 1680 (C=O, C4); 1575 (CH-Ar); 1510 (C=C). RMN-1H, (DMSOd6 270 MHz) δ : 5,22 (s, 2H, NH2, intercambio con D2O); 7,55 (dd, 1H, J=8,1 y 2,0 Hz, H6’); 7,77 (d, 1H, J=2,0 Hz, H2’); 7,98 (d, 1H, J=8,4 Hz, H5’); 8,04 (s, 1H, H7); 9,89 (sa, 1H, NH, intercambio con D2O). RMN-13C, (69 MHz, DMSOd6) δ: 116,2 (C5); 124,00 (C1’); 131,0 (C6’); 131,5 (C2’); 131,6 (C5’); 135,0 (C3’); 135,50 (C4’); 146,0 (C7); 160,0 (C=O); 164,9 (C=O); 166,3 (C6).
6-amino-5-[(4’-bromofenil)metilideno]pirimidina-2,4-diona(2e): Sólido amarillo. Rto: 87 %. P.f: 206-210 ºC. IR (KBr, cm-1): 3744, 3638 (NH2); 3265 (NH); 1715 (C=O, C2); 1680 (C=O, C4); 1578 (CH-Ar); 1510 (C=C). RMN-1H, (DMSOd6 270 MHz) δ : 5,75 (s, 2H, NH2, intercambio con D2O); 7,57 (dd, 2H, J=8,10 y 2,2 Hz, H3’, H5’); 7,98 (dd, 2H, J=8,1 y 2,2 Hz, H2’, H6’); 8,57 (s, 1H, H7); 9,72 (ba, 1H, NH, intercambio con D2O). RMN-13C, (69 MHz, DMSOd6) δ : 117,0 (C5); 125,0 (C1’); 128,0 (C3’, C5’); 129,0 (C4’); 130,0 (C2’, C6’); 150,0 (C7); 158,0 (C=O); 162,1 (C=O); 166,0 (C6).
6-amino-5-(bencilideno)pirimidina-2,4-diona(2f): Sólido beige. Rto: 80 %. P.f: 162-164 ºC. IR (KBr, cm-1): 3800, 3750 (NH2); 3265 (NH); 1715 (C=O, C2); 1682 (C=O, C4) 1600 (CH-Ar); 1510 (C=C). RMN-1H, (DMSOd6 270 MHz) δ: 4,72 (s, 2H, NH2, intercambio con D2O); 7,55 (m, 3H, H-Ar); 7,93 (m, 2H, H-Ar); 8,22 (s, 1H, H7); 13,00 (s, 1H, NH, intercambio con D2O). RMN-13C, (69 MHz, DMSOd6) δ: 117,0 (C5); 128,0 (C3’, C5’); 129,2 (C2’, C6’); 131,1 (C1’); 133,2 (C4’); 145,2 (C7); 159,0 (C=O); 163,1 (C=O); 165,2 (C6).
6-amino-5-[(4’-metilfenil)metilideno]pirimidina-2,4-diona(2g): Cristales verdes. Rto. 90 %. P.f: 202-204 ºC. IR (KBr, cm-1): 3530, 3445 (NH2) 3294 (NH); 1715 (C=O, C2); 1680 (C=O, C4); 1586 (CH-Ar); 1510 (C=C). RMN-1H, (DMSOd6 270 MHz) δ: 2,42 (s, 3H, CH3), 5,71 (s, 2H, NH2, intercambio con D2O); 7,20 (dd, 2H, J=10,5 y 1,98 Hz, H3’, H5’); 8,13 (dd, 2H, J=10,5 y 1,9 Hz, H2’, H6’); 8,57 (s, 1H, H7); 9,88 (s, 1H, NH, intercambio con D2O). RMN-13C, (69 MHz, DMSOd6) δ: 21,8 (CH3); 117,0 (C5); 127,7 (C3’, C5’); 129,0 (C1’), 130,7 (C2’, C6’); 142,0 (C4’); 149,5 (C7); 158,0 (C=O, C2); 162,1 (C=O, C4); 165,9 (C6).
6-amino-5-[(4’-metoxifenl)metilideno]pirimidina-2,4-diona(2h): Sólido beige. Rto. 85 %. P.f: 160 ºC desc. IR (KBr, cm-1): 3880, 3780 (NH2) 3264 (NH); 1715 (C=O, C2); 1688 (C=O, C4); 1584 (CH-Ar); 1510 (C=C). RMN-1H, (DMSOd6 270 MHz) δ : 3,84 (s, 3H, OCH3); 5,43 (s, 2H, NH2); 6,60 (dd, 2H, J=8,4 y 1,9 Hz, H3’, H5’); 7,70 (dd, 2H, J=8,4 y 1,9 Hz, H2’, H6’); 7,79 (s, 1H, H7); 9,89 (sa, 1H, NH). RMN-13C, (69 MHz, DMSOd6) δ : 55,6 (OCH3); 114,9 (C3’,5’); 116,2 (C5); 124,5 (C1’); 133,6 (C2’, C6’); 139,9 (C4’); 148,0 (CH=); 163,1 (C=O, C2); 163,8 (C=O, C4); 165,0 (C6).
6-amino-5-[(3’,4’-dimetoxifenil)metilideno]pirimidina-2,4- diona(2i): Sólido amarillo. Rto. 60 %. P.f: 170-172 ºC. IR (KBr, cm-1): 3680, 3581 (NH2) 3270 (NH); 1715 (C=O, C2); 1682 (C=O, C4); 1584 (CH-Ar); 1510 (C=C). RMN-1H, (DMSOd6 270 MHz) δ: 3,79 (s, 3H, OCH3); 3,83 (s, 3H, OCH3); 5,78 (s, 2H, NH2 intercambia con D2O); 7,08 (dd, 1H, J=7,4 y 1,2 Hz, H6’); 7,11 (s, 1H, H7); 7,13-7,15 (m, 2H, HAr); 7,94 (s, 1H, NH intercambia con D2O). RMN-13C, (69 MHz, DMSOd6) δ: 56,1 (OCH3); 56,2 (OCH3); 116,2 (C5); 126,5 (C1’); 128,2 (C6’); 133,6 (C2’); 146,7 (C7); 148,8 (C3’); 150,9 (C4’); 160,99 (C=O, C2); 161,81(C=O, C4); 166,43 (C6).
6-amino-5-[(3’,4',5’-trimetoxifenil)metilideno]pirimidina-2,4- diona(2j): Sólido Blanco. Rto. 50 %. P.f: 166 ºC desc. IR (KBr, cm-1): 3562, 3462 (NH2); 3265 (NH); 1715 (C=O, C2); 1680 C=O, C4); 1588 (CH-Ar); 1510 (C=C). RMN-1H, (DMSOd6 270 MHz) δ: 3,94 (s, 6H, 2OCH3); 3,96 (s, 3H, OCH3); 5,78 (s, 2H, NH2); 6,64 (s, 2H, H2’, H6’); 8,39 (s, 1H, H7); 9,88 (s, 1H, NH). RMN-13C, (69 MHz, DMSOd6) δ: 61,1; (2OCH3); 62,6 (OCH3); 108,8 (C2’, C6’); 117,1 (C5); 132,0 (C1’); 145,1 (C7); 153,0 (C-Ar); 154,8 (C-Ar); 158,0 (C4’); 160,0 (C=O, C2) 162,7 (C=O, C4); 166,0 (C6).
6-amino-5-[(4’-dimetilaminofenil)metilideno]pirimidin-2,4- diona(2k): Cristales anaranjados. Rto: 90 %. P.f: 216-218 ºC. IR (KBr, cm-1): 3565,3465 (NH2); 3294 (NH); 1715 (C=O, C2); 1688 (C=O, C4); 1606 (CH-Ar); 1510 (C=C). RMN-1H, (DMSOd6 270 MHz) δ: 3,06 (s, 6H, N(CH3)2); 5,65 (s, 3H, NH2, intercambio con D2O); 7,00 (dd, 2H, J=8,6 y 1,7 Hz, H3’, H5); 7,55 (dd, 2H, J=8,9 y 1,9 Hz, H2’, H6); 8,46 (s, 1H, H7); 9,60 (ba, 1H, NH, intercambio con D2O). RMN-13C, (69 MHz, DMSOd6) δ: 40,2 N(CH3)2; 111,8 (C3’,C5’); 116,01 (C5); 120,0 (C1’); 133,9 (C2’, C6); 145,0 (CH=); 152,0 (C4’); 158,0 (C=O C2); 165,0 (C=O, C4); 168,0 (C6).
6-amino-5-[(4’-hidroxifenil)metilideno]pirimidin-2,4-diona (2l): Cristales marrones Rto: 89 %. P.f: 250-254 ºC. IR (KBr, cm-1): 3780-3400 (OH, NH2, NH); 1715 (C=O, C2); 1670 (C=O, C4); 1590 (CH-Ar); 1510 (C=C). RMN-1H, (DMSOd6 270 MHz) δ: 5,25 (s, 3H, OH, NH2, intercambio con D2O); 6,91 (dd, 2H, J=8,6 y 2,2 Hz, H3’, H5); 7,35 (dd, 2H, J=8,9 y 2,2 Hz, H2’, H6); 8,29 (s, 1H, H7); 10,12 (ba, 1H, NH, intercambio con D2O). RMN-13C, (69 MHz, DMSOd6) δ: 112,0 (C3’, C5); 116,9 (C5); 120,0 (C1’); 134,0 (C2’, C6); 145,0 (C7); 158,0 (C=O, C2); 160,0 (C4’); 162,9 (C=O, C4); 165,9 (C6).
Actividad antimicrobiana
Todos los compuestos sintetizados 2a-l fueron evaluados para determinar su actividad antimicrobiana utilizando el método de difusión sobre placas de agar25. Los ensayos in vitro se realizaron contra los microorganismos Gram-positivos: Staphylococcus aureus (American Type Culture Colletion) [ATCC] 25923) y Bacillus cereus, (ATCC 14579) y los microorganismos Gram- negativos: Escherichia coli (ATCC 35218) y Pseudomonas aeruginosa (ATCC 27853) y la levadura Candida tropicalis (Micoteca Lorenzo De Montemayor (USB [MLDM] 372).
Pseudomonas aeruginosa, Bacillus cereus y Candida tropicalis fueron incubados a 30 ºC, mientras que Escherichia coli y Staphylococcus aureus fueron incubados a 37 ºC. Como controles positivos se utilizaron los antibióticos comerciales amikacina (AN) (30mcg); ampicilina/sulbactam (SAM) (20 mcg); ofloxacina (O) (5 mcg); tilmicosina (TIL) (15 mcg); (300 UI) y como control negativo se empleó la mezcla de solventes (S) utilizada para solubilizar las muestras (DMSO/Me2O/H2O 25:25:50). Se preparó una suspensión de cada compuesto en la mezcla de solventes (C=2-3 mg/mL, 5 µL). 0,1 mL de los cultivos microbianos crecidos en placas LB preparado en el laboratorio26 y ajustados en solución salina (0,85% v/v) a la concentración correspondiente al Standard de McFarland Nº 0.5, fueron sembrados en superficie en agar Mueller-Hinton (Merck 1.05437). En el caso de Candida tropicalis se utilizó una placa de YPD para la evaluación, ya que las levaduras crecen mejor en este medio. Sobre el césped microbiano se colocaron los discos de papel de filtro con las diferentes muestras y los controles. Las suspensiones fueron colocadas en discos de papel absorbente (Ø = 5 mm). Como controles positivos se emplearon antibióticos comerciales, 0,1 mL de los cultivos microbianos crecidos en placas LB preparado en el laboratorio26 , y ajustados en solución salina (0,85% v/v) a la concentración correspondiente al Standard de McFarland Nº 1, fueron sembrados en superficie en agar Mueller-Hinton (Merck 1.05437). Sobre el césped bacteriano se colocaron los discos de papel de filtro con las diferentes muestras. La zona de inhibición de cada compuesto evaluado se midió en mm.
Discusión de resultados
Química
La estrategia de síntesis para la obtención de los derivados de pirimidinas análogos de uracilo 2a-l, se fundamentó en un proceso de síntesis lineal de dos pasos. Dicha estrategia permitió la preparación de 12 derivados y el procedimiento es clave para la síntesis de heterociclos nuevos. En el primer paso, para preparar los intermediarios (E)-2-ciano fenilacrilatos de etilo 1a-l, existe varios procedimientos reportados en la literatura mediante el uso de catalizadores costosos, piridina o piperidina27,28,29,30. Ahora bien, los derivados 1a-l se obtuvieron en altos rendimientos mediante la reacción de condensación Knoevenagel entre cianoacetato de etilo con diferentes benzaldehídos en cantidades equimolares utilizando etanol como solvente y una cantidad catalítica de KOH a temperatura ambiente (esquema 1). Los datos espectrales de IR, RMN 1H y 13C de 1a-l fueron suficientes para confirmar su estructura. El IR muestra bandas se absorción entre 2988-3000 cm-1 atribuidas al grupo -CH2-CH3; a 2224 cm-1 que es característica del grupo -C≡N; entre 1717-1715 cm-1 indica la presencia del grupo C=O de éster y entre 1600-1594 cm-1 corresponde a las vibraciones C-H de anillo aromático. En el RMN-1H además de mostrar todas las señales correspondientes a los patrones de sustitución en el anillo aromático, mostraron un singlete común para todos los derivados que integró para un protón con un desplazamiento químico alrededor de 8,24-8,06 ppm asignado al protón H3. Entre 1,41-1,38 y 4,38-4,31 ppm aparecen el triplete y el cuarteto de los grupos metilo y metileno, respectivamente, característicos del grupo etoxi (–OCH2CH3) común en todos los derivados. En RMN 13C, se detectan el grupo metilo entre 14,8-14,1 ppm; el metileno entre 62,9-56,4; el carbono del nitrilo entre 116,1-112,1 ppm; el C2 a 99 ,6-107,6 ppm; C3 entre 151,0-155,0 ppm y el grupo C=O entre 167,5-161,5 ppm.
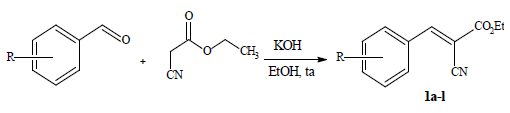
Esquema 1.
Síntesis de derivados de (E)-2-cianocinnamatos (1a-l)
La segunda etapa de la síntesis consistió en hacer reaccionar los derivados 1a-l con urea utilizando K2CO3 como base en etanol a reflujo para obtener los derivados de pirimidinas 2a-l (Esquema 2). Las evidencias espectroscópicas confirman la estructura esperada en cada caso. En el IR se observan las dos bandas de absorción del enlace H–N característico del grupo NH2 en la posición C6 (la primera aparecen entre 3880-3530 cm-1 y la segunda entre 3750-3461 cm-1). La banda correspondiente al grupo –N–H– en la posición N3 del núcleo de pirimidina aparece entre 3294-3256 cm-1. Dos bandas que aparecen entre 1792-1715 cm-1 y 1688-1670 cm-1 son atribuídas al grupo C=O en las posiciones C2 y C4 respectivamente. Es importante resaltar que las bandas del grupo C≡N y -CH2CH3 desaparecieron. En los espectros de RMN-1H desaparecen tanto el cuarteto como el triplete característicos de los grupos metilo y metileno del éster de partida, indicando que efectivamente se llevó a cabo el ataque nucleofílico al carbonilo acílico induciendo la salida del grupo –OCH2CH3 y adición al carbono del grupo nitrilo. Se observa un singlete ancho que integra para dos protones a 5,27-5,78 ppm que son asignados al grupo NH2 y una banda ancha que integra para un protón a 13,00-7,94 ppm es asignado al grupo NH. El intercambio de los protones en los grupos –NH2 y -HN– con D2O, causó que sus señales desaparecieran como era de esperar. Por otra parte, el protón olefínico H7 del grupo arilmetilideno aparece como singlete a 7,11-8,46 ppm. El espectro de RMN-13C normal en conjunto con los espectros bidimensionales como HETCOR y DEPT-135º, permitieron asignar de forma positiva el desplazamiento químico de C5 a 112,1-117,1 ppm; C6 a 165,0-168,0 ppm de la pirimidina. Los picos a 158,0-163,1 ppm y a 161,1-165,0 ppm, corresponden a los grupos carbonilo en C2 y C4, respectivamente. El mecanismo de reacción propuesto para la formación de los derivados 2a-l es análogo al propuesto en el trabajo previamente publicado23.
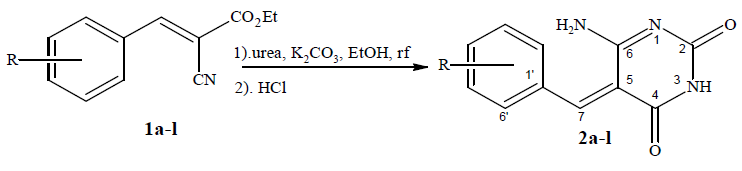
Esquema 2.
Síntesis de derivados de pirimidinas análogas de uracilo (2a-l).
Actividad antimicrobiana
Los resultados de la actividad antimicrobiana de los compuestos 2a-l son presentados en la tabla 1. Contra la bacteria E. coli, mostraron actividad los compuestos 2c-d,2f, 2i y 2k y de estos el más activo fue el compuesto 2f. Contra P. aeruginosa, mostraron actividad los compuestos 2c-f, 2h y 2l, siendo los más activos 2c y 2econ actividades superiores a todos los antibióticos utilizados como controles positivos (figura 6).
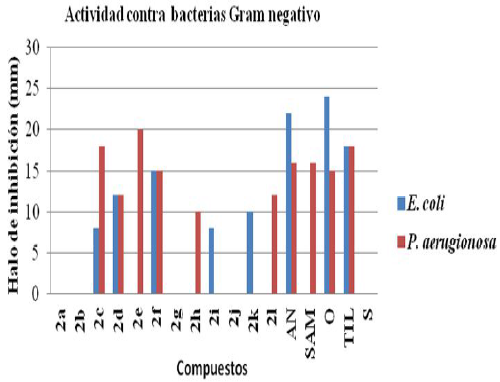
Fig. 6:
Actividad Antibacterial contra Gram negativo de 2a-l
(-) = No inhibición, AN: amikacina, SAM: ampicilina/sulbactam. O: ofloxacina. TIL: tilmicosina. S: mezcla de solvente.
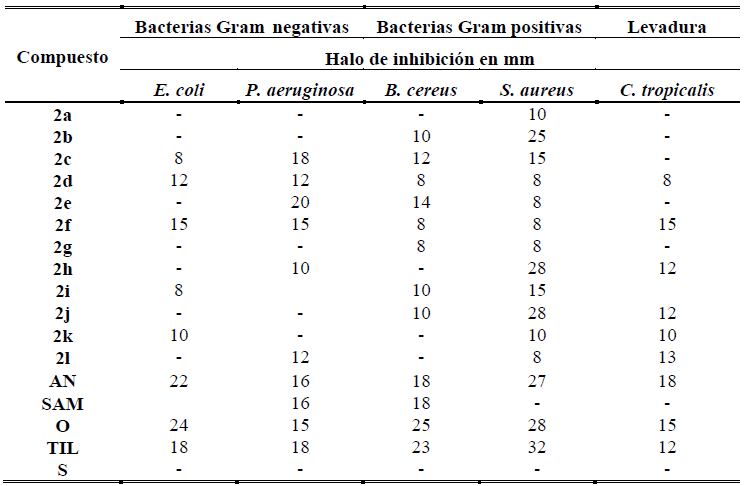
Contra las bacterias B. cereus, mostraron actividad los compuestos 2b-g2i y 2j mientras que todos los compuestos sintetizados fueron activos, contra S. aureus, de estos los más activos fueron 2b, 2h y 2j presentando valores de actividad comparables a la amikacina y la ofloxacina (figura 7).
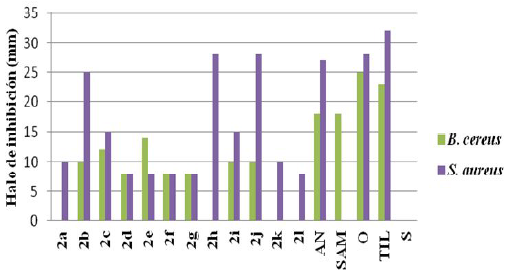
Fig. 7:
Actividad Antibacterial contra Gram positivo de 2a-l.
Seis compuestos fueron activos contra C. tropicalis y de estos 2f mostró valor de actividad exhibido por ofloxacina, 2h, 2j y 2l valores comparables a tilmicosina (figura 8).
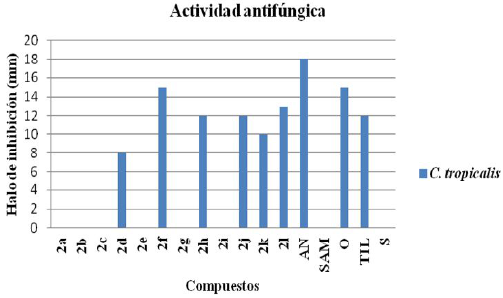
Fig. 8:
Actividad antifúngica 2a-l.
Conclusiones
Se lograron sintetizar 12 derivados nuevos de pirimidinas en dos pasos de reacción. El método de síntesis representa un gran potencial de aplicación para la síntesis de una gran variedad de pirimidinas con potencial actividad biológica. Se obtuvieron compuestos cuya actividad contra la bacteria oportunista Gram negativa P. aeruginosa resistente a la mayoría de los antibióticos comerciales es importante. Todos los compuestos obtenidos fueron activos contra S. aureus, este hecho es bien interesante ya que se trata de un microorganismo Gram positivo responsable de un alto porcentaje de infecciones hospitalarias, además de ser resistente a diversos antibióticos.
Agradecimientos
Se agradece el Instituto de Investigaciones Farmacéuticas de la Facultad de Farmacia de la Universidad Central de Venezuela (Proyecto IIF: 02/2014). Al CDCH-UCV (Proyecto PG-06-8827-2013/1 y 2013/2).
Referencias
1. N Zhang, S Ayral-Kaloustian, T Nguyen, R Hernandez, C Beyerb. 2-Cyanoaminopyrimidines as a class of antitumor agents that promote tubulin polymerization. Bioorg. Med. Chem. Lett., 17(11), 3003-3005 (2007).
2. N Mohamed, M Talaat El-Saidi, Y Ali, M Elnagdi. Utility of 6- amino-2-thiouracil as a precursor for the synthesis of bioactive pyrimidine derivatives. Bioorg. Med. Chem., 15, 6227-6235 (2007).
3. E Rakib, S Abourichaa, A Hanniouia, N Benchat, L Ait M’barekc and A Zyadc. Synthesis and in vitro Cytotoxicity Studies of Novel Triazolo[4,3 b]pyridazinones. J. Iranian Chem. Soc., 3(3), 272-276 (2006).
4. P Baraldi, M Pavani, M Nuñez, P Brigidi, B Vitali, R Gambari, R Romagnoli. Antimicrobial and Antitumor Activity of NHeteroimmine- 1,2,3- dithiazoles and Their Transformation in Triazolo-, Imidazo-, and Pyrazolo-pirimidines. Bioorg Med. Chem., 10 449–456 (2002).
5. A Kamel, B Munson. Collisionally-Induced Dissociation of Substituted Pyrimidine Antiviral Agents: Mechanisms of Ion Formation Using Gas Phase Hydrogen/Deuterium Exchange and Electrospray Ionization Tandem Mass Spectrometry. J. Am. Soc Mass Spectr., 18, 1477-1492 (2007).
6. N Hang, S Ayral-Kaloustian, T Nguyen, J Afragola, R Hernandez, J Lucas, J Gibbons, C Beyer. Synthesis and SAR of [1,2,4]Triazolo[1,5-a]pyrimidines, a Class of Anticancer Agents with a Unique Mechanism of Tubulin Inhibition. J. Med. Chem., 50, 319-327 (2007).
7. O Prakash, R Kumar, R Kumar, P Tyagi, R Kuhad. Organoiodine( III) mediated synthesis of 3,9-diaryl- and 3,9-difuryl-bis- 1,2,4-triazolo[4,3-a][4,3-c]pyrimidines as antibacterial agents. Euro. J. Med. Chem. ,42, 868-872 (2007).
8. S Sondhi, S Jain, M Dinodia, R Shuklab, R Raghubir. S Sondhi, S Jain, M Dinodia, R Shuklab, R Raghubir. Bioorg. Med. Chem., 15, 3334-3344 (2007).
9. M Shaquiquzzaman, S Khan, M Amir, M Alam. Synthesis, anticonvulsant and neurotoxicity evaluation of some new pyrimidine-5-carbonitrile derivatives. Saudi Pharm. J., 20(2), 149-164 (2012).
10. D Premnath, M Indiraleka. Design and synthesis, antiepileptic evaluation of 5-substituted pyrimidine derivatives. Asian J. Med. and Anal. Chem., 1(1), 27-32 (2014).
11. J McChesney, M Gonzales-Sierra. Antifungal Activity of Some Substituted Pyrimidines. Pharm. Res., 2(3), 146-147 (1985). DOI: 10.1023/A:1016323702665.
12. I Mangalagiu, M Ungureanu M, G Mangalagiu, G Grosu, M Petrovanu. Antimicrobial activity of some derivatives of pyrimidine. Ann. Pharm Fr., 56(4), 181-183 (1998).
13. L Cordies, L Machado, M Hamilton. Principios generales de la terapéutica antimicrobiana. Acta Médica, 8(1), 13-27 (1998).
14. A Eid, A El-Wahab, G Ali, M Khafagy. Synthesis and antimicrobial evaluation of naphtho[2,1-b]pyrano[2,3-d] pyrimidine and pyrano[3,2-e][1,2,4]triazolo[1,5-c] pyrimidine derivatives. Acta Pharm., 54 13–26 (2004).
15. J Paulsen, J Liu, D Bolstad, A Smith, N priestley, D Wright, A Anderson. In vitro biological activity and structural analysis of 2,4-diamino-5-(2’-arylpropargyl)pyrimidine inhibitors of Candida albicans. Bioorg. Med. Chem., 17(14), 4866-4862 (2009).
16. OMS. El primer informe mundial de la OMS sobre la resistencia a los antibióticos pone de manifiesto una grave amenaza para la salud pública en todo el mundo. Disponible en: http://www.who.int/mediacentre/news/releases/2014/amrreport/es/
17. D Chu, J Plattner, L Chu, J Plattner and L Katz. 1996. New Directions in Antibacterial Research. J. Med. Chem., 39, 3853- 3874 (1996).
18. A Vallano, D Rodríguez, M Barcelo, A López, A Cano, B Viñado. Sensibilidad antimicrobiana de los uropatógenos y los resultados del tratamiento antibiótico de las infecciones urinarias en atención primaria. Enferm. Infecc. Microbiol. Clin., 24, 418-425 (2006).
19. A Pulido, O Baniandrés, M Ceballos, M Mendoza, M Campo. Infecciones cutáneas causadas por Staphylococcus aureus resistente a meticilina de adquisición comunitaria: características clínico-microbiológicas en 11 pacientes. Actas Dermosifiliogr., 105(2), 150-158 (2013). DOI: 10.1016/j.ad.2013.09.002.
20. L Toledo, E Piña, A Paz Montes, E Torres. Determinación de la resistencia a meticilina y eritromicina de cepas de Staphylococcus aureus aisladas en un hospital del estado Zulia. Rev. Soc. Ven. Microbiol., 32(2), 88-94 (2012).
21. OMS. Resistencia a los antimicrobianos. Nota descriptiva N° 194. Mayo 2013. Disponible en: http://www.who.int/mediacentre/factsheets/fs194/es/
22. W Brumfitt, J Hamilton-Miller. Reassessment of the rationale for the combinations of sulphonamides with diaminopyrimidines. J. Chemother., 5, 465-469, (1993).
23. G Lobo, J Charris, A Taddei, M Monasterios, M Valderrama, J Romero, K Chávez. Síntesis y Actividad Antimicrobiana de Derivados de 4,6-aminopirimidinas análogos de citosina. Avances en Química, 7(2), 119-128 (2012).
24. G Lobo et al. 4,6-Diamino-5-(3,4-dochloro-benzylidene) pyrimidin- 2(5H)-one. Molbank M693, 2010. Doi: 10.3390/M693.
25. A Janssen, J Scheffer, A Baerheim. Antimicrobial Activity of Essential Oils: A 1976-1986 Review. Aspects of Tests Methods. Planta Medica, 53, 395-398 (1987).
26. J Sambrook, E Fritsch, T Maniatis. Molecular Cloning: A Laboratory Manual, Vol. 3, Appendix A, pp A.1. Cold Spring Harbor Laboratory Press, 2nd. Edition, New York (1989).
27. J Yadav, B Reddy, A Basak, B Visali, A Narsaiah, K Nagaiah. Phosphane-Catalyzed Knoevenagel Condensation: A Facile Synthesis of α-Cyanoacrylates and α-Cyanoacrylonitriles. Eur. J. Org. Chem., 546-551 (2004).
28. K Ebitani, K Motokura, K Mori, T Mizugaki, K Kaneda. Reconstructed Hydrotalcite as a Highly Active Heterogeneous Base Catalyst for Carbon-Carbon Bond Formations in the Presence of Water. J. Org. Chem., 71, 5440-5447 (2006).
29. C Su, Z Chen, Q Zhen. The ionic liquid 1-butyl-3-methylimidazonium tetrafluoroborate [bmim]BF4 was used for ethylene-diammonium diacetate (EDDA)-catalyzed Knoevenagel condensation between aldehydes or ketones with active methylene compounds. Catalyst and solvent can be recycled. Synthesis, 555-559 (2003).
30. J Augustine, Y Naik, A Mandal, N Chowdappa, V Praveen. gem-Dibromomethylarenes: A Convenient Substitute for Noncommercial Aldehydes in the Knoevenagel-Doebner Reaction for the Synthesis of α,β-Unsaturated Carboxylic Acids. J. Org. Chem., 72, 9854-9856 (2007).
Notas