Actividad intrínseca en la hidrogenación de ciclohexeno de catalizadores metálicos de Ni, Co, Pt y Pd soportados sobre tamices moleculares del tipo MCM-41
Actividad intrínseca en la hidrogenación de ciclohexeno de catalizadores metálicos de Ni, Co, Pt y Pd soportados sobre tamices moleculares del tipo MCM-41
Avances en Química, vol. 11, núm. 2, pp. 69-75, 2016
Universidad de los Andes
Recepción: 26/04/2016
Corregido: 12/07/2016
Aprobación: 28/08/2016
Financiamiento
Fuente: Oscar Zorrilla
Beneficiario: Ernesto Bastardo-González, Mariangela Patiño, Franklin J. Méndez, y Joaquín L. Brito
Fuente: Pablo Quiroz (DRX)
Fuente: Alberto Albornoz (XPS)
Fuente: José Luis Prin (MET)
Financiamiento
Fuente: EBG
Nº de contrato: 2011001359
Beneficiario: FONACIT
Resumen: Se sintetizó un material mesoporoso del tipo MCM-41 y se utilizó como soporte para la preparación de cuatro catalizadores que contenían como precursores catalíticos metálicos Ni, Co, Pd y Pt. El patrón de DRX del soporte presentó las cuatros reflexiones características de este tipo de material, con una contracción de la estructura después de extraído el agente director mediante calcinación. Los catalizadores Ni/MCM-41, Co/MCM-41, Pt/MCM-41 y Pd/MCM-41 presentaron las reflexiones del material de partida a bajos ángulos, pero con un mayor desorden estructural. Se apreció una retención de la estructura mesoporosa del material de partida y altas áreas específicas. Adicionalmente, se pudo observar e identificar a ángulos mayores de difracción (30-45°/2θ) los metales en fase óxido presentes de algunos de los catalizadores. Por espectroscopia foto-electrónica de rayos X se obtuvieron los estados de oxidación de los metales incorporados y los posibles óxidos en que se encuentran alguno de éstos, corroborándose con esta técnica la presencia de los metales a nivel de superficie. Por microscopía electrónica de transmisión se observó la morfología de la superficie de los sólidos en estudio. La conversión de ciclohexeno y su selectividad hacia la formación de ciclohexano indicaron que los catalizadores frescos presentan actividad intrínseca, que depende del carácter metálico de los sólidos estudiados.
Palabras clave: catalizadores, MCM-41, mesoporos.
Abstract: Synthesis and characterization of metallic catalysts of Ni, Co, Pt and Pd supported on molecular sieves MCM-41 type. A mesoporous material MCM-41 was prepared and used as support for four catalysts containing the metallic catalytic precursors of Ni, Co, Pd and Pt. The XRD pattern of the support showed the four typical reflections of this type of material, with a structure contraction after surfactant removal by calcination. The catalysts Ni/MCM-41, Co/MCM-41, Pt/MCM-41 and Pd/MCM-41 presented the reflections at low angle, but with much higher structural disorder. It was appreciated a retention of the mesoporous structure of the starting material and high surface areas. Additionally, it was possible to observe and identified the oxide phases in the diffraction range (30-45°/2θ) presented in all solids. Oxidation states of incorporated metal, and possible oxides in which are found some of them, were obtained by X-ray photoelectron spectroscopy, corroborating by this technique the presence of metals at surface level. Surface morphology of the solids under study was observed by transmission electron microscopy. The conversion of cyclohexen and the selectivity towards cyclohexane indicated that fresh catalysts show certain degree of intrinsic activity, which depends on the metallic character of the studied solids.
Keywords: Catalysts, MCM-41, Mesoporous.
Introducción
En las últimas décadas, la obtención de materiales mesoporosos mediante el empleo de moléculas tensoactivas como agentes estructurantes ha experimentado un gran desarrollo. Esto se debe, sin duda, a las magníficas propiedades que muestran estos materiales, que los hacen aplicables en el campo de la catálisis heterogénea y adsorción.
La atención de muchos investigadores ha sido atraída hacia el estudio de los materiales mesoporosos de la familia M41S, sintetizados en 1992 por investigadores de la Mobil Research and Development Corporation, los cuales poseen excelentes propiedades estructurales, texturales y superficiales, destacándose altas áreas específicas cercanas a 1000 m2/g, diámetro de poros entre 20 y 100 Å y alta capacidad de adsorción1,2.
El material con arreglo hexagonal, conocido como MCM-41, es el miembro más estudiado e importante de esta familia. Éste es formado en presencia de un surfactante catiónico en solución acuosa y la adición de una fuente de silicio en medio básico2. En la síntesis se forman micelas del surfactante, cargadas positivamente, que se usan como agentes directores de la estructura, alrededor de las cuales se organizan las especies inorgánicas con cargas negativas, presentes en la mezcla reaccionante. Al extraer el surfactante mediante calcinación queda el sólido inorgánico con un arreglo hexagonal de poros. Éste mecanismo de formación es conocido como Cristal Liquido Templante (CLT)1-3.
El material MCM-41 puro de óxido de silicio es inerte químicamente, lo que limita su aplicación como catalizador por sí solo. Por lo tanto, surge la necesidad de generar sitios activos, incorporando o impregnando elementos en su estructura porosa, con la finalidad de conferirle una actividad catalítica específica4.
Con este tipo de sólidos sintetizados se han encontrado múltiples aplicaciones. Entre las de mayor relevancia destaca: el estudio de oligomerización de etileno5 e hidrogenación de tolueno6 y benceno7, utilizando el catalizador Ni/MCM-41; formación de nanotubos de carbono8, oxidación de 2,4,6- triclorofenol en agua9 y oxidación de etilbenceno10, utilizando el catalizador Co/MCM-41; reducción catalítica selectiva de NOX11,12, isomerización de n-butano13, hidrogenación de ciclohexeno, 1-penteno y 1-hexeno14, utilizando el catalizador de Pt/MCM-41; síntesis de metanol15, hidrogenación de benzofenona16 y craqueo catalítico de polipropileno17, utilizando un catalizador Pd/MCM-41; entre muchas otras aplicaciones. El interés principal de este trabajo de investigación consistió en estudiar la capacidad intrínseca de transformar catalíticamente el ciclohexeno a través de reacciones de hidrogenación, de cuatro catalizadores de metales de transición soportados en el tamiz molecular mesoporoso MCM-41.
Metodología
La preparación de los catalizadores se realizó en dos fases: la primera correspondió a la preparación del soporte y la segunda a la impregnación de los metales.
Síntesis del soporte MCM-41
Para la síntesis del material MCM-41 se utilizó el procedimiento descrito por Méndez y col.18. Se preparó una solución de NaOH/SiO2 (Sigma-Aldrich) con una relación en mol igual a 2,0. La suspensión inicial se mantuvo en agitación a una temperatura aproximada de 70 ºC hasta obtener una solución completamente homogénea. En ese instante se detuvo el calentamiento y se mantuvo en agitación magnética hasta alcanzar la temperatura ambiente. Paralelamente, se preparó una solución surfactante disolviendo 0,048 moles de hidróxido de tetrametilamonio al 25 % v/v (Sigma-Aldrich) en 150 ml de agua desionizada, seguida de la adición 0,05 moles de bromuro de hexadecil-trimetilamonio (Sigma- Aldrich), hasta lograr la disolución completa del mismo. Posteriormente, se agregó la solución de NaOH/SiO2 preparada a la solución surfactante. Se ajustó el pH a 9 con la adición de H2SO4 (Fluka) al 10 % m/m y se dejó en agitación por un periodo de 2 horas. La mezcla resultante se dejó en añejamiento por 24 horas y el gel formado se filtró al vacío. El sólido obtenido se secó, pulverizó y se calcinó a 550 ºC por 8 horas.
Síntesis de los catalizadores M/MCM-41 (M = Ni, Co, Pt y Pd)
Para la preparación de los catalizadores Ni/MCM-41, Co/MCM-41, Pd/MCM-41, Pt/MCM-41 con un 1 % en peso del componente metálico se utilizó el método de impregnación incipiente, descrito por Méndez y col.18 y Vívenes y col.19. Para ello, se disolvieron cantidades adecuadas de las sales precursoras: Ni(NO3)2·6H2O, Co(CH3COO)2·4H2O, H2(PtCl6)·6H2O y PdCl2, todos suministrados por Merck, como fuentes de los metales, en 50 ml de agua desionizada. Cada solución se añadió, en forma dispersiva, sobre el material mesoporoso MCM-41 preparado. La suspensión obtenida se calentó a aproximadamente 70 ºC y, con continua agitación, se eliminó lentamente el agua por evaporación. El sólido obtenido se secó a 60 °C, pulverizó y calcinó a 500 ºC por 5 horas para así obtener los catalizadores deseados.
Caracterización fisicoquímica
Los patrones de difracción de rayos X (DRX) fueron obtenidos utilizando un difractómetro Phillips PW 710 con radiación de Cu Kα (1,5418 Å) y filtro de níquel, una velocidad de paso de 0,02º/segundo en el rango 1-10º/2Ɵ y 30- 45º/2Ɵ. La identificación de las diferentes fases fue realizada utilizando la librería JCPDS para polvos cristalinos20. Las propiedades texturales del soporte y los catalizadores oxídicos fueron determinadas con un analizador automático Micromeritics ASAP 2010 a la temperatura del N2 líquido. Las áreas específicas fueron calculadas por el método de Brunauer-Emmett-Teller (SBET), el volumen de poro (Vp) se determinó a una presión relativa de 0,99 y el diámetro promedio de poros (DBJH) fue estimado por medio de la aplicación del método de Barrett-Joyner-Halenda en la isoterma de desorción. Para este análisis, las muestras fueron previamente desgasificadas a 150 ºC por 4 h y una presión de 10-2 Torr. Para la obtención de las micrografías por microscopia electrónica de transmisión (MET) se empleó un microscopio electrónico marca Hitachi, modelo H-600 de 100 kV, mientras que el estado de oxidación de los precursores fue determinado por medio de espectroscopia fotoelectrónica de rayos X (XPS), utilizando un equipo VG-Escalab, modelo 220-XL, empleando radiación Kα1 de magnesio y una señal C1s a 284,6 eV como señal de referencia.
Comportamiento catalítico en la hidrogenación de ciclohexeno
Para medir la actividad intrínseca de los catalizadores metálicos, se utilizó la hidrogenación de ciclohexeno como reacción modelo. Este sistema de reacción consta de un matraz balón de 2 bocas con 30 ml del sustrato (ciclohexeno) a presión atmosférica a 25 °C y, posteriormente, se adicionaron 300 mg del catalizador fresco. La suspensión sustrato-catalizador se burbujea con un flujo de H2 de 100 ml/min durante 6 horas. Las muestras hidrogenadas fueron filtradas y medidas utilizando un cromatógrafo de gases Agilent Technologies modelo GC 6890 equipado con un detector de ionización a la llama y columna capilar GSGaspro de 60 m de longitud y 0,32 mm de diámetro interno.
Resultados
En la figura 1(a) se presentan los patrones de difracción de rayos X a bajo ángulo del tamiz mesoporoso MCM-41 antes y después de calcinar. Como se puede observar, el material antes de calcinar presenta una reflexión basal en el plano (100) a 2,84°/2θ y tres de menor intensidad en los planos (110), (200) y (210) a 4,36; 4,92 y 6,26°/2θ, respectivamente, las cuales son atribuidas a una estructura hexagonal previamente reportada1. Así mismo, la muestra después de calcinar presenta las mismas reflexiones mostradas anteriormente, más intensas y angostas, lo indica la retención de la estructura hexagonal y un mayor ordenamiento en la estructura porosa, producto de la deshidroxilación y condensación entre las diferentes fuentes inorgánicas que rodean a las micelas. Además, se puede apreciar el desplazamiento de dichas reflexiones hacia valores mayores de 2θ, lo que indica una contracción de la estructura, producto principalmente de la remoción de la parte orgánica de las micelas y a la mayor condensación entre los grupos silanol (Si-OH), como resultado de la calcinación, produciendo un mayor orden estructural, asociado a que la proporción de especies de silicio totalmente condensados, Si(OSi)4 es alta1,2,3.
En la figura 1(b) se muestran los patrones de difracción de rayos X de los materiales Ni/MCM-41, Pd/MCM-41, Co/MCM-41 y Pt/MCM-41 a bajos ángulos. En esta se demuestra la retención de la estructura hexagonal del material de partida, con presencia de la reflexión característica en el plano (100) a 2,58; 2,60; 2,62 y 2,80°/2θ para los catalizadores Co/MCM-41, Pd/MCM-41, Ni/MCM-41 y Pt/MCM-41 respectivamente, pero de menor intensidad relativa a las observadas en la figura 1(a). Igualmente, se puede observar que la intensidad de las reflexiones en los planos (110), (200) y (210) disminuye marcadamente para los catalizadores Co/MCM-41, Pd/MCM-41 y Ni/MCM-41, pero desaparece totalmente para catalizador Pt/MCM-41. Esta disminución de las reflexiones se puede atribuir a un colapso parcial de la estructura por la presencia de los metales, que a su vez causan una expansión en la estructura, desplazando la reflexión basal hacia valores de ángulos menores, en comparación al material de partida. Además, dicha destrucción parcial puede ser asociada al carácter hidrofóbico que presenta este tipo de materiales y al tratamiento térmico al cual se sometió, puesto que las paredes del material pudieron debilitarse debido a los diferentes tratamientos. Este efecto era esperado, puesto que las paredes del material MCM-41 presentan espesores entre 3-5 nm, lo cual lo hace hidrotérmicamente menos estable que otros materiales mesoestructurados. De acuerdo a esto, se puede decir que los catalizadores obtenidos son materiales más desordenados y colapsados estructuralmente.
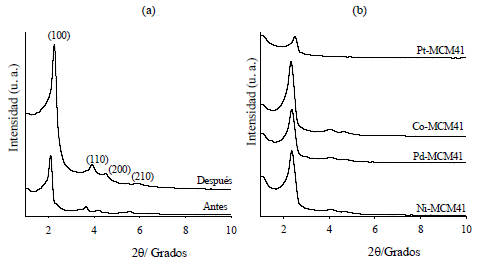
Fig. 1:
Patrones de difracción de rayos X de los materiales (a) MCM-41 antes y después de calcinar y (b) catalizadores M/MCM- 41 preparados (M = Ni, Co, Pd o Pt).
A ángulos de difracción mayores (figura 2) se pueden apreciar las reflexiones características para las fases oxídicas encontradas para algunos de los catalizadores. Para el catalizador Ni/MCM-41 se observan dos reflexiones bien definidas en los planos (101) y (012) a 37,74 y 43,26º/2θ atribuidas a cristales de NiO hexagonal (JCPDS 44-1159)20. Por otro lado, para el catalizador Co/MCM-41 aparece una reflexión intensa a 36,92º/2θ en el plano (311) y una de menor intensidad a 31,60º/2θ en el plano (220) características, que confirma la existencia del metal en forma de Co3O4 cúbico (JCPDS 74-1656)20. Para el catalizador Pt/MCM-41 no se pudo identificar claramente las reflexiones esperadas que indican una alta dispersión de la fase óxido del metal sobre el soporte, mientras que para el catalizador Pd/MCM-41, se aprecia una reflexión característica en el plano (101) a 34,14º/2θ y una en el plano (110) a 42,18º/2θ, que indica la presencia del PdO tetragonal (JCPDS 85-0713)20.
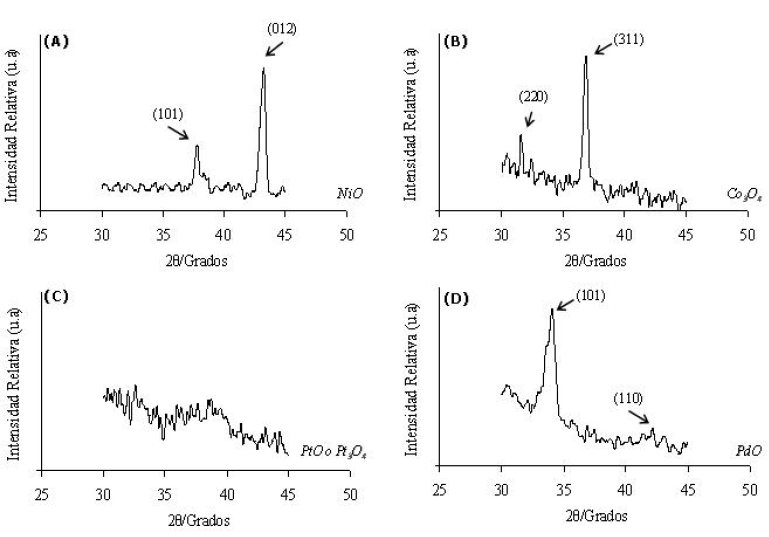
Fig. 2:
Patrones de difracción de rayos X de los catalizadores identificando los óxidos metálicos presentes. (A) Ni/MCM-41, (B) Co/MCM-41, (C) Pt/MCM-41 y (D) Pd/MCM-41.
En la figura 3 se pueden apreciar las isotermas de adsorcióndesorción de N2 del material MCM-41 usado como soporte y de los catalizadores preparados. En esta se observa que la isoterma del material MCM-41 de partida (figura 3a) es del tipo IV, característica de materiales mesoporosos, y de este tipo de sólidos de la familia M41S, donde existe un punto de inflexión a presiones relativas intermedias, que es característico de la condensación capilar en mesoporos uniformes. De igual manera, a presiones relativas bajas se observa el llenado de poros de menor tamaño (microporosidad) que participan significativamente en el área específica, y que es producto del uso de un cosurfactante. También, claramente se aprecia que todos los catalizadores presentan el mismo tipo de isoterma, lo que comprueba de que todos ellos retienen la naturaleza mesoporosa del soporte, en correlación al resultado obtenido por DRX a bajo ángulo (figura 1b). La tabla 1 resume las propiedades de textura de todos los sólidos preparados.
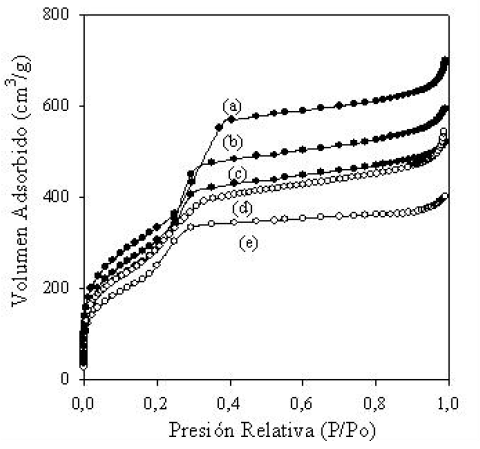
Fig. 3:
Isotermas de adsorción-desorción de N2 de los materiales: (a) MCM-41, (b) Ni/MCM-41, (c) Co/MCM-41, (d) Pd/MCM-41 y (e) Pt/MCM-41.
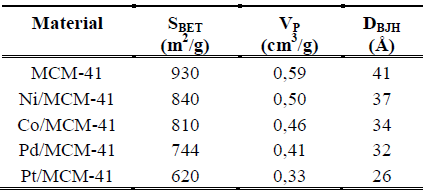
SBET = Área específica determinada por el método de Brunauer- Emmett-Teller; Vp = Volumen de poro determinado a una presión relativa de 0,99; DBJH = Diámetro promedio de poros determinada por el método de Barrett-Joyner–Halenda.
De la tabla 1 se observa la elevada área específica (> 900 m2/g) del material MCM-41, tal como se ha reportado en otros trabajos1,2,18,21. Se aprecia una reducción de este valor en los catalizadores preparados, lo que se puede atribuir a varios factores, entre ellos la destrucción parcial de la estructura porosa debido a la sorción de H2O, al aumento de masa por unidad de área producido por las impregnaciones y posterior tratamiento térmico y a la naturaleza hidrofóbica del soporte. Se descarta como posible efecto un bloqueo de los poros por la migración de algunas de las fases metálicas, debido al bajo porcentaje de impregnación de los mismos, y todos estos factores claramente están también relacionados con las disminuciones de los valores de Vp y DBJH (tabla 1).
En las figuras 4 y 5 se presentan los espectros obtenidos por espectroscopía fotoelectrónica de rayos X, correspondientes a los niveles de fotoemisión para el Ni2p, Co2p, Pt4f y Pd3d para los catalizadores soportados. Estas permitieron la determinación de los estados de oxidación de los metales y posibles óxidos y elementos depositados en la superficie.
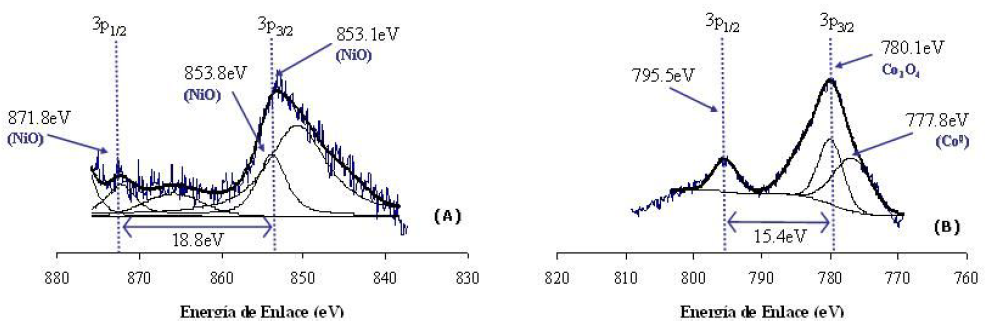
Fig. 4:
Espectro XPS de los catalizadores. (A) Ni/MCM-41; (B) Co/MCM-41.
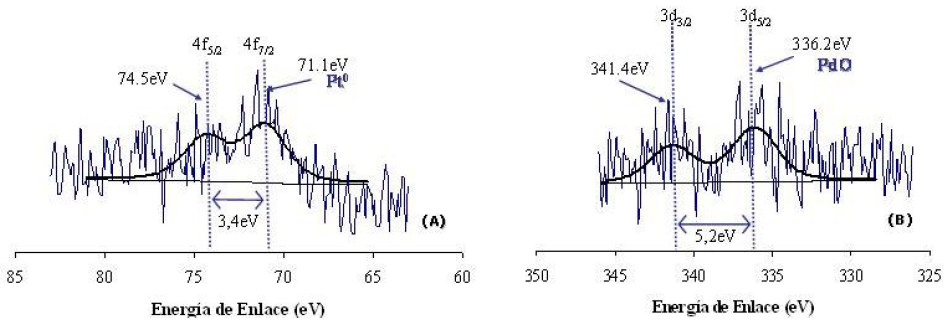
Fig. 5:
Espectro XPS de los catalizadores. (A) Pt/MCM41; (B) Pd/MCM-41.
En la figura 4A se aprecian dos señales, una de mayor intensidad a una energía de enlace de 853,1 eV y una de menor intensidad a 871,8 eV correspondiente al nivel de fotoemisión para el Ni3p3/2 y Ni3p1/2, y separadas por 18,7 eV.
Estas señales son atribuidas al níquel en su estado de oxidación más estable (2+) proveniente del NiO. De igual manera, en la figura 4B se aprecia un doblete, con una separación de 15,4 eV. La primera señal de este espectro a una energía de enlace de 780,1 eV y la segunda a 795,5 eV son atribuidas a los niveles de fotoemisión para el Co3p3/2 y Co3p1/2 respectivamente, los cuales muestran que el cobalto se encuentra en mayor proporción en su forma de Co3O4. Además, de una señal de menor intensidad a 777,8 eV, producto de este elemento en su estado elemental, disperso en la superficie en menor proporción.
En las figuras 5A y 5B, correspondientes a los catalizadores Pt/MCM-41 y Pd/MCM-41, respectivamente, se aprecian dobletes separados por 3,4 eV y 3,5 eV respectivamente. Para el catalizador de platino se observan señales a energías de enlace de 71,1 eV y 74,5 eV, correspondiente al nivel de fotoemisión para el Pt3p7/2 y Pt3p5/2, atribuida al platino elemental disperso en la superficie del catalizador. Así, para el catalizador de paladio el doblete característico se encontró a energías de enlace de 336,2 y 341,1 eV, correspondiente al nivel de fotoemisión para el Pd3p5/2 y Pd3p3/2, atribuida al este elemento en la forma de PdO (estados de oxidación 2+). Cada una de estas señales fue identificada por la cercanía de estas a los niveles de fotoemisión de cada elemento en estudio con los valores encontrados en la bibliografía22. Adicionalmente, se puede decir que las señales no identificadas se deben, posiblemente, a señales satélites de otros componentes presentes en la muestra.
En la figura 6 se observa la morfología interna de los materiales mediante micrografías en campo claro con una potencia de 100 kV. En cada una de las micrografías mostrada se pueden identificar las fases metálicas encontradas. Para el catalizador Ni/MCM-41 (figura 6A) se observan zonas oscuras en forma circular o de puntos, atribuidas al NiO presente en la superficie. Por otro lado, para el catalizador Co/MCM-41 se puede observar la cristalización del Co3O4 en forma de hilos o laminillas (figura 6B). Así mismo, se observa la fase de platino elemental sobre la superficie del catalizador Pt/MCM-41 (figura 6C), la cual tienen forma de pequeños puntos negros, de menor tamaño que las zonas oscuras observadas en las micrografías de los demás catalizadores, y que están distribuidos al azar. También, se verificó la existencia del paladio en la superficie del catalizador Pd/MCM-41 como zonas oscuras con forma de cuadrados o cubos (figura 6D).

Fig. 6:
Micrografías de los catalizadores soportados.
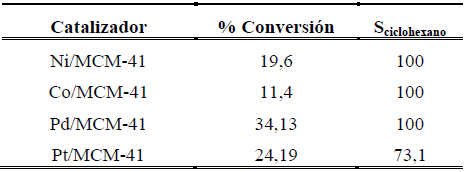
Los resultados del comportamiento catalítico intrínseco de los catalizadores (muestras sin reducir) en la hidrogenación de ciclohexeno se muestran en la tabla 3. En esta se puede apreciar que todos los catalizadores frescos presentan un grado de reactividad para la reacción en estudio a pesar de poseer su superficie fresca, indicando que estos metales de transición soportados en el material mesoporoso MCM-41 presentan la capacidad intrínseca de disociar hidrógeno en su superficie, mostrando la siguiente tendencias en correlación con el carácter metálico elemental del catalizador en su superficie (resultados observados por XPS): Co/MCM-41 < Ni/MCM-41 < Pt/MCM-41 < Pd/MCM-41. Por otro lado, todas las muestras presentaron una alta selectividad hacia la formación del producto hidrogenado (ciclohexeno → ciclohexano), sin embargo, el catalizador con mayor carácter reducido presentó dos productos de reacción, con formación adicional de pequeñas cantidades de metilciclopentano, lo que indica que el catalizador Pt/MCM-41 isomeriza el sustrato ciclohexeno a metil-ciclopenteno y posteriormente lo hidrogena formando así el metil-ciclopentano.
Conclusiones
Los catalizadores frescos basados en Ni, Co, Pt y Pd soportados en MCM-41 presentan una actividad de hidrogenación intrínseca, es decir, que no necesitan ser reducidos para transformar selectivamente el ciclohexeno a ciclohexano, sin embargo, el catalizador con mayor carácter metálico (Pt/MCM-41) presentó un producto adicional debido a la hidrogenación del isómero, formando así metilciclopentano.
Agradecimientos
Los autores agradecen el apoyo de Oscar Zorrilla y Pablo Quiroz (DRX), Alberto Albornoz (XPS) y de José Luis Prin (MET) por la ayuda técnica prestada en la caracterización de los sólidos sintetizados. Adicionalmente, EBG agradece el financiamiento económico del FONACIT a través del Proyecto 2011001359.
Referencias
1. J Beck, J Vartuli,W Roth, M Leonowicz, C Kresge, K Schmitt, C Chu, D Olson, E Sheppard, S McCullen, J Higgins, J Schlenker. A new family of mesoporous molecular sieves prepared with liquid crystal template. J. Am. Chem. Soc., 114, 10834-10843 (1992).
2. C Kresge, M Leonowicz, W Roth, J Vartuli, J Beck. Ordered mesoporous molecular sieves synthesized by a liquid crystal template mechanism. Nature, 359, 710-712 (1992).
3. R Mokaya. Mesoporous materials, synthesis and properties. Encyclopedia of Physical Science and Technology. Pags. 371- 375. Academic Press, Orlando (2002).
4. A Corma, D Kumar. Materiales mesoporosos en catálisis. Actas del XVI Memorias Simposio Iberoamericano de Catálisis. Cartagena-Colombia, Vol. I, 16-18 (1998).
5. M Lallemand, A Finiels, F Fajula, V Hulea. Ethylene oligomerization over Ni-containing mesostructured catalysts with MCM-41, MCM-48 and SBA-15 topologies. Studies in Surface Science and Catalysis, 170(2), 1863-1869 (2007).
6. A Szegedi, M Popova, V Mavrodinova, M Urbán, I Kiricsi, C Minchev. Synthesis and characterization of Ni-MCM-41 materials with spherical morphology and their catalytic activity in toluene hydrogenation. Microporous and Mesoporous Materials, 99, 149–158 (2007).
7. R Wojcieszak, S Monteverdi, M Mercy, I Nowak, M Ziolek, M Bettahar. Nickel containing MCM-41 and AlMCM-41 mesoporous molecular sieves: Characteristics and activity in the hydrogenation of benzene. Applied Catalysis A: General, 268, 241-253 (2004).
8. T Somanathan, A Pandurangan, D Sathiyamoorthy. Catalytic influence of mesoporous Co-MCM-41 molecular sieves for the synthesis of SWNTs via CVD method. J. Molecular Catalysis A: Chemical, 256, 193-199 (2006).
9. S Chaliha, K Gopal, K Bhattacharyya. Wet oxidative method for removal of 2,4,6-trichlorophenol in water using Fe(III), Co(II), Ni(II) supported MCM-41 catalysts. J. Hazardous Materials, 150, 728-736 (2008).
10. S Shrikant, A Bhoware, P Singh. Characterization and catalytic activity of cobalt containing MCM-41 prepared by direct hydrothermal, grafting and immobilization methods. J. Molecular Catalysis A: Chemical, 266, 118-130 (2007).
11. J Jang, S Lee, D Kim, M Kang, S Choung. Characterization of Pt-impregnated MCM-41 and MCM-48 and their catalytic performances in selective catalytic reduction for NOx. Applied Catalysis A: General, 286, 36-43 (2005.
12. J Park, J Yun, K Jeong, S Ihm. Platinum catalysts supported on macrostructured MCM-41 for the selective catalytic reduction of lean NOX with hydrocarbons. Studies in Surface Science and Catalysis, 170(2), 1362-1367 (2007).
13. V Nieminen, N Kumar, T Salmi, D Murzin. n-Butane isomerization over Pt-H-MCM-41. Catalysis Communications, 5, 15-19 (2004).
14. A Mastalir, B Rác, Z Király, G Tasi, A Molnár. Preparation of monodispersed Pt nanoparticles in MCM-41, catalytic applications. Catalysis Communications, 9, 762-768 (2008).
15. D Lee, G Jung, H Lee, J Lee. Methanol synthesis over Pd/SiO2 with narrow Pd size distribution prepared by using MCM-41 as a support precursor. Catalysis Today, 111, 373–378 (2006).
16. M Bejblová, P Zámostný, L Červený, J Čejka. Hydrodeoxygenation of benzophenone on Pd catalysts. Applied Catalysis A: General, 296, 169-175 (2005).
17. R Van Grieken, D Serrano, J Aguado, R García, C Rojo. Thermal and catalytic cracking of polyethylene under mild conditions. J. Analytical and Applied Pyrolysis, 58-59, 127- 142 (2001).
18. FJ Méndez, E Bastardo-González, P Betancourt, L Paiva, JL Brito. NiMo/MCM.41 catalysts for the hydrotreatment of polychlorinated biphenyls. Catalysis Letter, 143, 93-100 (2013).
19. A Vívenes, FJ Méndez, E Bastardo-González, JL Brito. Catalizadores M-Mo/HMS (M = Fe, Co o Ni) en sus formas sulfuradas y nitruradas como potenciales sistemas catalíticos de hidrogenación. Avances en Química, 10(1), 55-65 (2015).
20. JCPDS International Center for Diffraction Data. Power Difracction File (PDF). 1999. PCPDFWIN v.2.02. Newtown Square, PA, USA. 19073 (1999).
21. ZA Alothman. A review: fundamental aspects of silicate mesoporous materials. Materials, 5, 2874-2902 (2012).
22. C D Wagner, GE Muilenberg. Handbook of X-ray photoelectron spectroscopy: A reference book of standard data for use in X-ray photoelectron spectroscopy. Eden Prairie, Minn.: Physical Electronics Division, Perkin-Elmer Corp. (1979).
Notas de autor
ernieluis@hotmail.com