Desarrollo de un prototipo de biosensor basado en peroxidasa de palma real (Roystonea regia) y nanotubos de péptidos inmovilizados sobre electrodos de oro para detección de peróxido de hidrógeno
Development of a prototype biosensor based on real palm peroxidase (Roystonea regia) and nanotubes of peptides immobilized on gold electrodes for detection of hydrogen peroxide.
Desarrollo de un prototipo de biosensor basado en peroxidasa de palma real (Roystonea regia) y nanotubos de péptidos inmovilizados sobre electrodos de oro para detección de peróxido de hidrógeno
Avances en Química, vol. 11, núm. 3, pp. 105-111, 2016
Universidad de los Andes
Recepción: 04 Julio 2016
Aprobación: 17 Noviembre 2016
Resumen: En este trabajo se desarrolló un novedoso prototipo de biosensor enzimático para detección de peróxido de hidrógeno (H2O2) mediante la co-inmovilización de la peroxidasa de palma real (Roystonea regia) (PPR) y nanotubos de péptidos (NTPs) mediante el uso de glutaraldehído (GA) como agente entrecruzante sobre electrodos serigrafiados de oro. El desarrollo del electrodo enzimático comprendió primero la extracción y purificación de la peroxidasa de las hojas de la palma real. Posteriormente, la superficie de electrodos de oro fue modificada mediante la adsorción del conjugado PPRNTP y su caracterización se llevó a cabo mediante voltamperometría cíclica (VC) y cronoamperometría. Los estudios de VC mostraron un potencial redox de trabajo de la PPR de -0.4 V contra un electrodo de referencia Ag/AgCl. El biosensor enzimático presentó una respuesta en corriente a diferentes concentraciones de peróxido de hidrógeno. El estudio de los parámetros analíticos mostró un rango lineal en un intervalo de 500-6000 mM, una sensibilidad de calibrado de 0,022 mA.L/mol y un límite de detección de 432 mM. El proceso de transferencia de electrones enzima-electrodo estuvo controlado superficialmente y dependió del pH de la solución. El prototipo de biosensor enzimático desarrollado en éste estudio se convierte en una potencial herramienta bio-analítica para la detección de H2O2 en muestras reales de interés biomédico y ambiental.
Palabras clave: biosensor, peroxidasa de palma real, nanotubos de péptido.
Abstract: In this work we developed a novel H2O2 enzymatic biosensor through the co-immobilization of royal palm tree peroxidase (RPTP) (Roystonea regia) with peptide nanotubes (PNTs) on screen-printed gold electrodes employing glutaraldehyde as a cross-linking agent. The biosensor development begins with the isolation and purification of peroxidase from the leaves of palm tree. Then the surface of the electrode was modified by adsorption of the conjugate RPTP-PNT and the electrochemical characterization was made by cyclic voltammetry (CV) and chronoamperometry techniques. The CVs exhibited a redox potential around -0.4 V using an Ag/AgCl reference electrode. The enzymatic biosensor shows a catalytic response towards different hydrogen peroxide concentrations. Analytical parameters such as: linear range, sensibility and detection limit exhibited values of 500-6000 mM, 0.022 mA L/mol and 432 mM, respectively. A surface-controlled process electron transfer was observed and the biosensor exhibited a pH dependence. The novel biosensor presented in this work could be a potential bioanalytical tool for the detection of hydrogen peroxide in real samples of biomedical and environmental importance.
Keywords: Biosensor, Royal palm tree peroxidase, Peptide nanotubes.
Introducción
La determinación de H2O2 ha despertado considerable atención en los últimos años debido a su importancia en procesos relacionados con el cáncer y a sus efectos contaminantes en el medio ambiente1. Los enormes avances en la instrumentación analítica moderna han dado lugar a una mejora en la selectividad, inclusive para análisis de trazas, mediante técnicas como: cromatografía de gases, espectrometría de masas, cromatografía líquida de alta resolución, etc. Sin embargo, la gran mayoría de estas técnicas implican un elevado costo y consumo de tiempo, dada la necesidad de realizar pre-tratamientos a las muestras2.
Como alternativa a estos inconvenientes surge el desarrollo de los denominados biosensores, dispositivos en los que se emplean sustancias de origen biológico para el reconocimiento de especies particulares y que representan sistemas altamente sensibles y específicos3. Los biosensores juegan un rol determinante para abordar de modo rápido y confiable el análisis de un amplio espectro de especies: patógenos, compuestos asociados a procesos industriales, contaminantes ambientales, entre otros4.
La mayoría de biosensores utilizan la peroxidasa de rábano picante (PRP) (Armoracia rusticana) para la detección de peróxido de hidrógeno5,6,7; sin embargo, existen algunas limitaciones relacionadas con la estabilidad de ésta enzima como: desnaturalización de la peroxidasa en altas concentraciones de H2O2, altas temperaturas y pHs. De esta forma, surge la necesidad de encontrar nuevas enzimas con mejores propiedades catalíticas para el desarrollo de biosensores mejorados y más eficientes. Colombia es un país con excelentes recursos naturales prospectos a nuevas fuentes enzimáticas que pueden ser usadas para el desarrollo biotecnológico del país9. Esta biodiversidad da grandes ventajas competitivas que al ser basadas en el uso sostenible puede y debe convertirse en desarrollo científico para el país. Existe una gran motivación para encontrar nuevas fuentes potenciales de la peroxidasa (POD) con posibles aplicaciones para la construcción de biosensores amperométricos. En 2005, Alpeeva y cols.10 realizaron un estudio comparativo utilizando PRP, peroxidasa de batata dulce (PBD) (Ipomea batatas) y peroxidasa de palma real (PPR) (Roystonea regia). En este estudio se evaluaron parámetros analíticos tales como: nivel mínimo de detección, rango lineal de trabajo, estabilidad operacional y de almacenamiento. Los resultados obtenidos mostraron un comportamiento diferente para cada uno de los biosensores destacando la superioridad del biosensor de PPR.
El uso de la nanotecnología es, sin duda, una herramienta potente a la hora de diseñar biosensores11, ya que estos nanomateriales (nanotubos de carbono, nanotubos de péptidos o cualquier estructura con al menos una dimensión menor a 100 nm) presentan propiedades únicas como buena conductividad y biocompatibilidad por lo que mejoran la transferencia de carga desde las enzimas hacia los electrodos12,13. Los nanotubos de péptidos surgen como una alternativa hacia los ya usados nanotubos de carbono, además, presentan otras ventajas en comparación a estos últimos como facilidad a la hora de su síntesis y mayor reactividad14.
En este trabajo se utilizó la peroxidasa de palma real (Roystonea regia) adsorbida sobre electrodos de oro modificados con NTPs y GA para la construcción de un novedoso biosensor sensible a la presencia de H2O2.
Materiales y métodos
Extracción y semi-purificación de la peroxidasa de palma real
La extracción y semi-purificación de la PPR se llevó a cabo por medio de la metodología utilizada por Sakharov15. El extracto fue semi-purificado mediante un sistema de reparto bifásico compuesto por sulfato de amonio (10 % p/v) y polietilenglicol (14 % p/v). Posteriormente el extracto fue sometido a diferentes etapas cromatográficas. Finalmente se midió la actividad enzimática utilizando como sustrato el guayacol y se determinó la reacción de aparición del producto, el tetraguayacol, a 470 nm, con un coeficiente de extinción molar del producto de 5200 M-1.cm-1. La determinación de la concentración de proteínas en la solución enzimática de POD se hizo utilizando el método de Bradford15.
Síntesis de los nanotubos de péptido
La metodología para la formación de los NTPs ha sido descrita anteriormente14. Se añadieron 100 mg de difenil-alanina a 1 mL de 1,1,1,3,3,3-hexafluoro-2-propanol (HFP). De esta solución se tomaron 20 μL y se diluyeron a 1 mL, usando agua ultrapura. La concentración final fue de 2 mg/mL. Detalles adicionales de la obtención de los NTPs puede ser encontrada en la información de soporte (Fig. S1)
Modificación de los electrodos serigrafiados de oro
Se utilizaron electrodos serigrafiados de oro (DRP-220 AT, Dropsense) adquiridos comercialmente. Para la modificación de los electrodos se preparó una solución que contenía NTPs y POD en relación 1:1 v/v, luego se añadió GA en concentración 0,25 % p/v y se agitó durante 1 minuto a 50 rpm. La solución de PPR/GA/NTP se conservó a una temperatura de 4°C durante 2 h antes de su uso. 10 μL de solución de la solución preparada anteriormente se depositaron sobre la superficie del electrodo de trabajo y se almacenó a 4 °C durante 12 h. Posteriormente la superficie del electrodo fue lavada suavemente con buffer fosfato pH 7,0 para eliminar el exceso de enzima, GA y NPTs que no se adsorbieron sobre el electrodo. En la figura S2 (información de soporte) se puede apreciar el efecto de la presencia de la POD en el electrodo modificado comparado con el electrodo sin modificar en el proceso redox del ferrocianuro de potasio. Todas las mediciones fueron realizadas utilizando un Potenciostato/Galvanosotato Autolab y los datos fueron procesados mediante el software NOVA 1.10.1.9.
Reducción bioelectroquímica del peróxido de hidrógeno.
La caracterización cualitativa de la reducción bioelectroquímica del peróxido de hidrógeno se hizo por VC. Para ello se tomaron VCs de electrodos previamente modificados con 10 mL de la enzima, los cuales se pusieron en contacto dentro de una celda de acrílico de 7 mL de capacidad conteniendo una solución tampón de fosfatos 10 mM, pH 7,0; KCl 0,1 M y H2O2 5 mM. Todas las soluciones fueron desgasificadas usando nitrógeno para evitar interferencias con el oxígeno molecular.
Estudio del efecto de la velocidad de barrido
Se tomaron VCs de una solución tampón de fosfatos 10 mM pH 7,0; H2O2 1 mM a velocidades de barrido comprendidas entre 25 y 500 mV/s.
Estudio del efecto del pH
Se midió el VC de las siguientes soluciones tampón: 10 mM ácido cítrico/citrato trisodio (pH 3,0), 10 mM ácido acético/ acetato de sodio (pH 5.0), 10 mM fosfato de potasio dibásico/fosfato de potasio monobásico (pH 6,0; 7,0 y 8,0) y 10 mM carbonato de sodio/bicarbonato de sodio (pH 10). Cada solución contenía H2O2 5 mM y la velocidad de barrido lineal fue de 100 mV/s.
Estudio de los parámetros analíticos
Mediante la construcción de curvas de calibración a diferentes concentraciones de peróxido de hidrógeno se determinaron los siguientes parámetros analíticos: rango lineal del método, límite de detección y sensibilidad del método, para ello se utilizó cronoamperometría. Se utilizó un potencial fijo de -0.4 V y se usaron concentraciones de peróxido de hidrógeno en un rango de 1 a 5000 μM durante un tiempo de aproximadamente 12 min. Todas las mediciones fueron realizadas utilizando triplicados mediante la fabricación de electrodos preparados bajo las mismas condiciones.
Resultados
Purificación parcial de la peroxidasa de palma real
En la tabla 1, conocida como tabla de rendimiento, se puede observar la efectividad de cada una de las etapas usadas durante la purificación proteica de la peroxidasa. Como es normal, a medida que transcurre el proceso, el rendimiento se reduce y la muestra se va enriqueciendo en el compuesto de interés.
Finalmente las fracciones recogidas conteniendo la POD fueron incubadas a 4 °C para la modificación de los electrodos de oro y el diseño del biosensor.
Modificación física de los electrodos de oro para la determinación de peróxido de hidrógeno.
Para el desarrollo del biosensor, los electrodos de oro se modificaron depositando una solución que contenía NTP, PPR en una relación 1:1 y GA en concentración 0,25 % p/v para la determinación de H2O2. Este proceso no es posible con un electrodo de oro, grafeno o carbono vítreo que no cuente con la presencia de una enzima o de otra sustancia que pueda reducir el H2O2.
En esta conformación del biosensor, cada elemento juega un rol importante. Por un lado, los nanotubos de péptidos ofrecen una alternativa hacia los ya usados nanotubos de carbono (NTC), en cuanto a sus propiedades eléctricas, biocompatibilidad y, lo más importante, al proceso de transferencia de carga desde las proteínas hacía el electrodo12, además, químicamente los NTP son más reactivos en contraste con los NTC, por lo que no requiere su funcionalización14.
En segundo lugar, el GA sirve como un agente entrecruzante entre la enzima y los nanotubos. El grupo aldehído del GA puede reaccionar con los grupos aminos de los aminoácidos tanto de los nanotubos como de la enzima para formar bases de Schiff17. El uso del GA ha sido reportado anteriormente tanto para hacer uniones NTC-enzima18, como para NTPenzima19.
Finalmente la peroxidasa de palma real transfiere los electrones desde el grupo hemo hacia el H2O2 para su reducción. La peroxidasa de palma real es el componente biológico en nuestro biosensor.
Reducción bioelectroquímica del peróxido de hidrógeno.
La reducción bioelectrocatalítica del peróxido de hidrógeno fue estudiada mediante VC en ausencia/presencia de peróxido de hidrógeno a una velocidad de barrido lineal de 100 mV/s.
La figura 1 muestra los VCs obtenidos en una solución tampón fosfato 10 mM pH 7 con H2O2 5 mM. El VC del electrodo sin modificar no muestra ningún tipo de señal como respuesta luego de la adición de peróxido de hidrógeno a la solución, esto demuestra que la PPR es un componente esencial para la construcción del biosensor. Por otro lado el VC del electrodo modificado muestra un pico bien definido debido a la reducción bio-electrocatalítica del H2O2 alrededor de los -0,4 V. Este hecho demuestra la transferencia directa de electrones desde la enzima hacia el electrodo, gracias al puente de comunicación formado por los nanotubos y el GA como agente entrecruzante. Además el método de unión entre los componentes no involucra el sitio catalítico de la enzima. En la figura S3 (información de soporte) se compara la respuesta bioelectrocatalítica de los electrodos sin modificar, modificado con PPR, modificado con NTP y el electrodo PPR/GA/NTP.
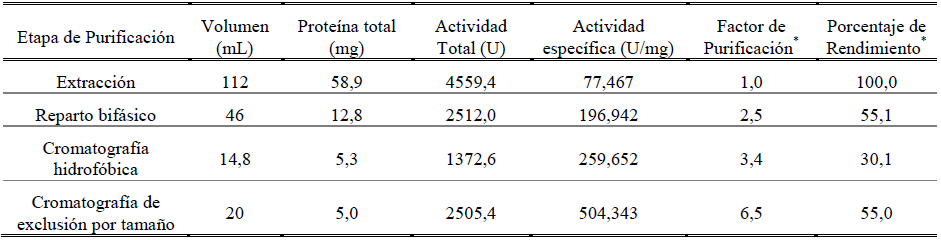
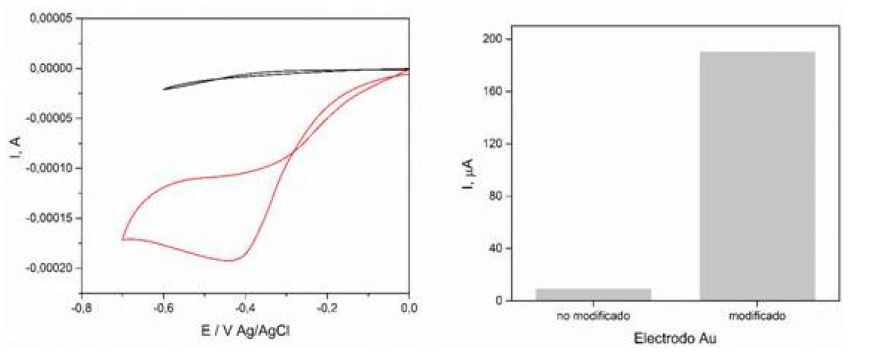
Fig. 1
VC de electrodos serigrafiados de oro sin modificar (-) y modificados (-) en presencia de H2O2 5 mM. Comparación de la corriente bioelectrocatalítica de los electrodos modificados y sin modificar. Velocidad de barrido 100 mV/s.
El mecanismo de detección del peróxido por parte de la POD engloba una oxidación de dos electrones del grupo ferrihemoprostético de la peroxidasa nativa por el H2O2. Esta reacción da lugar a un producto intermedio, compuesto I (estado de oxidación +5), que consiste en un ion oxiferrilo (Fe4+ = O) y un radical catiónico porfirínico π. El compuesto I tiene actividad catalítica y su radical porfirínico capta un electrón del electrodo originando el compuesto II el cual toma de nuevo otro electrón del electrodo para volver a su estado inicial de ferroperoxidasa. Además el compuesto II muestra una mayor estabilidad que el compuesto I, y el proceso de reducción del compuesto II hacia la PPR nativa es lento20. Se concluye entonces que el proceso de reducción del compuesto II es el detectado en este experimento21.
Estudio de la velocidad de barrido en la reducción biolectrocatalítica del peróxido de hidrógeno.
La figura 2A muestra los VCs obtenidos en solución tampón 10 mM pH 7 con H2O2 1 mM a diferentes velocidades de barrido lineal. Con el incremento de la velocidad de barrido de 50 a 500 mV/s, la corriente del pico de reducción del H2O2 incrementa de manera proporcional en este rango. Así la reacción en el electrodo es típica de un proceso reversible controlado difusionalmente en la superficie22.
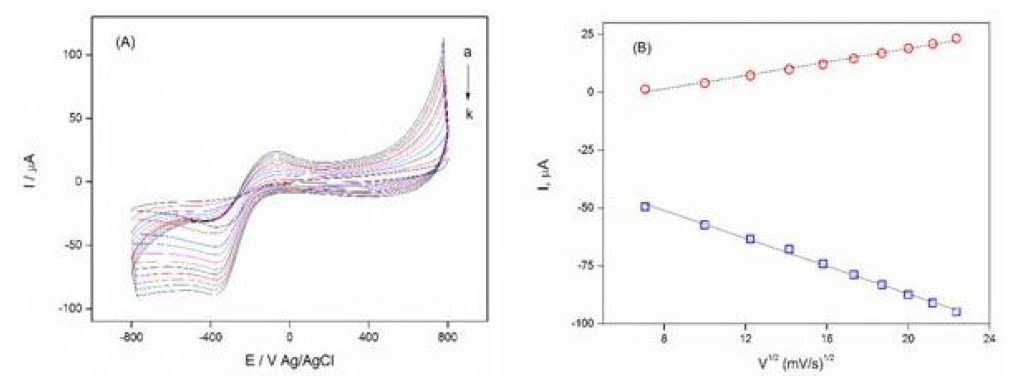
Fig. 2
A) VCs del electrodo modificado con PPR/GA/NTP en una solución tampón 10 mM pH 7 KCl 0,1 M, H2O2 1 mM a diferentes velocidades de barrido de la (a) a la (k): (a) 25, (b) 50, (c) 100, (d) 150, (e) 200, (f) 250, (g) 300, (h) 350, (i) 400, (j) 450, (k) 500 mV/s. B) Corriente del pico catódico y anódico vs raíz cuadrada de la velocidad del barrido lineal.
Los picos anódico y catódico incrementan linealmente con la raíz cuadra de la velocidad de barrido desde 50 hasta 500 mV.s-1.
Ipa (μA) = 1,45ν (mV/s-1) – 10,19 (r2=0,997)
Ipc (μA) = -2,99ν (mV/s-1) – 27,12 (r2=0,990)
Anteriores autores tales como Luet al., 20097 reportaron procesos reversibles para electrodos de oro modificados con HRP en el rango de 50-700 mVs-1.
Es bien sabido que el pH influye en la conformación de la enzima y sus propiedades biocatalíticas22. Como se observa en la figura 3 entre pH 5,0 y pH 7,0, la enzima mantiene hasta un 93 % de su actividad catalítica, a medida que el pH se desplaza hacia valores ácidos no hay respuesta por parte del biosensor, pero, en cambio hay respuesta significativa a pH básico (pH 10). Cabe resaltar que la POD de palma exhibe un mayor rango de trabajo que la HRP cuyo rango de pH está limitado únicamente a valores entre 6,0 y 8,022.
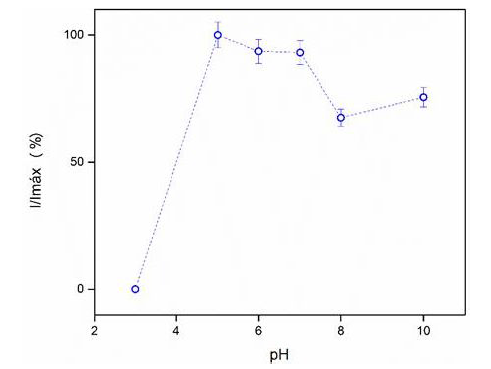
Fig. 3
Dependencia de la respuesta del biosensor en función del pH. Todas las mediciones de pH fueron realizadas por triplicado.
Respuesta del biosensor a adiciones sucesivas de peróxido de hidrógeno por cronoamperometría.
Se usó cronoamperometría para evaluar el cambio de corriente en el tiempo cuando se variaba la concentración de H2O2 en una solución tampón y así hallar la sensibilidad y la linealidad de la respuesta del electrodo PPR/GA/NTP mediante la construcción de curvas de calibración. El voltaje aplicado fue de -0,4 V vs Ag/AgCl, resultado que se dedujo de la señal obtenida en los VCs (Fig. 1).
La figura 4A muestra el cronoamperograma del electrodo PPR/GA/NTP luego de sucesivas adiciones de alícuotas de 100 mL de H2O2 en un rango de concentraciones desde 500 hasta 6000 mM. Como experimento control se realizaron las mismas adiciones de H2O2 a un electrodo sin modificar (Fig. 4A). Lo anterior confirma que la detección de H2O2 es debido a la presencia de la PPR inmovilizada sobre los electrodos de oro. En la figura 4B se aprecia la curva de calibración obtenida con los valores de la corriente a diferentes concentraciones de H2O2.
Como se observa en la figura 4A hay una relación lineal entre la corriente y la concentración de peróxido en el rango de 500 μM hasta 6000 μM. La ecuación que se ajusta por regresión lineal de los datos está dada a continuación:
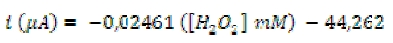
Esta ecuación presenta un coeficiente de correlación r2 de 0,9853. Este valor indica cuanto se ajusta la ecuación de la recta a los datos obtenidos. A partir de 400 s el valor de la corriente presenta cierto nivel de ruido debido probablemente a una desorción de la enzima lo cual dificultó la lectura del valor de la corriente. La sensibilidad del método se define entonces como el valor absoluto de la pendiente, es decir, 0,02461 para un electrodo modificado PPR/GA/NTP en un rango de 500-6000 μM.
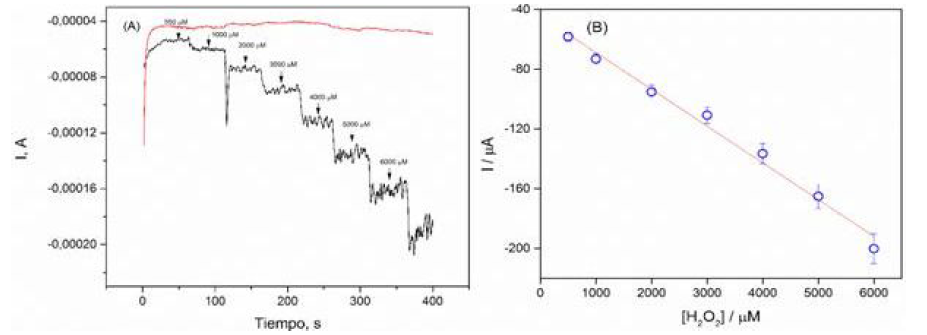
Fig. 4
Respuesta corriente vs tiempo para la adición de H2O2 a una diferencia de potencial de -0,4 V vs Ag. A) Electrodo sin modificar (-) y electrodo modificado con PPR/GA/NTP (-) y B) Curva de calibración obtenida de los datos de la cronoamperometría a diferentes concentraciones de peróxido (500-6000 mM). Todas las mediciones fueron realizadas por triplicado.
El límite de detección (LD) entonces sería la menor concentración de peróxido cuya señal puede ser distinguida de la del ruido. Para esta técnica analítica el límite de detección fue de 432 mM.
El LD fue calculado mediante la siguiente fórmula:
LD=(k*s_b)/m (1)
donde k es el llamado factor de confianza (K=3.), s_b corresponde a la desviación estándar de la determinación del blanco y m es la sensibilidad de calibrado.
En el desarrollo del presente trabajo se exploran nuevas fuentes de obtención de enzimas con aplicaciones analíticas. La PPR es una alternativa con mejores características (rango de trabajo según el pH, estabilidad térmica) a la ya estudiada HRP8,16. Los resultados obtenidos en este trabajo podrían abrir interesantes perspectivas para el desarrollo de biosensores novedosos usando fuentes naturales propias como elementos de reconocimiento biológico y para el diseño e investigación en la fabricación de novedosos sistemas de detección y así solucionar los problemas que la sociedad demanda hoy en día.
Conclusiones
En este trabajo se desarrolló un novedoso sistema de detección de peróxido de hidrógeno basado en un biosensor amperométrico de peroxidasa de palma real y nanotubos de péptido. El análisis electroquímico indicó que el sistema PPR/GA/NTP exhibió un potencial de trabajo alrededor de -0,4 V vs Ag/AgCl en presencia de soluciones de H2O2. La cronoamperometría permitió la obtención de curvas de calibración para la determinación de figuras de mérito como: rango lineal, sensibilidad de calibrado y límite de detección, las cuales arrojaron valores de 500-6000 mM, 0,02461 mAL/mol y 432 mM, respectivamente. El desarrollo del biosensor amperométrico abre así nuevas posibilidades de construcción de novedosos sistemas de detección de analitos de importancia biomédica y ambiental.
Agradecimientos
Los autores expresan su agradecimiento a la Universidad Industrial de Santander por el apoyo recibido mediante el proyecto de Convocatoria Interna número 1782 y al programa Capital Semilla número 1735.
Referencias
1. S Xu, X Zhang, T Wan, C Zhang. A third generation hydrogen peroxide biosensor based on horseradish peroxidase cross-linked to multi-walled carbon nanotubes. Microchimica Acta, 172, 199-205 (2011).
2. JJ Castillo, WE Svendsen, N Rozlosnik, P Escobar, F Martínez, J Castillo-León. Detection of cancer cells using a peptide nanotube-folic acid modified graphene electrode. Analyst, 138, 1026-1031 (2013).
3. J Castillo-León, S Gaspar, S Leth, M Niculescu, A Mortari, I Bontidean, V Soukharev, S Domeanu, A Ryabov, E Csöregi. Biosensors for life quality: Design, development and applications. Sensors and Actuators B: Chemical, 102, 179-194 (2004).
4. M Lei, J Feng, L Wu, J Zhou, J Chen, A Wang. Novel phenol biosensor based on laccase immobilized on reduced graphene oxide supported palladium-copper alloyed nanocages. Biosensors and Bioelectronics, 74, 347-352 (2015).
5. S Xu, J Li, Z Zhou, C Zhang. A third-generation hydrogen peroxide biosensor based on horseradish peroxidase immobilized by sol-gel thin film on a multi-walled carbón nanotube modified electrode. Analytical Methods, 6, 6310-6315 (2014).
6. G Lai, H Zhang, D Han. Amperometric hydrogen peroxide biosensor based on the immobilization of horseradish peroxidase by carbon-coated iron nanoparticles in combination with chitosan and cross-linking of glutaraldehyde. Microchimica Acta, 165, 159-165 (2009).
7. X Xu, S Li, H Ju. A novel hydrogen peroxide sensor via the direct electrochemistry of horseradish peroxidase immobilized on colloidal gold modified screen-printed electrode. Sensors, 3, 350-360 (2003).
8. I Sakharov, A Vorobiev, J Castillo. Synthesis of polyelectrolyte complexes of polyaniline and sulfonated polystyrene by palm tree peroxidase. Enzyme and Microbial Technology, 33, 661-667 (2003).
9. I Sakharov, G Bautista, I Sakharova. Peroxidasas de plantas tropicales. Revista Colombiana de Química, 28, 97-106 (1999).
10. I Alpeeva, M Niculescu, J Castillo-León, E Csöregi, I Sakharov. Palm tree peroxidase-based biosensor with unique properties characteristics for hydrogen peroxide monitoring. Biosensors and Bioelectronics, 21, 742-748 (2005).
11. Y Wang, H Chang, H Wu, H Liu. Bioinspired prospects of graphene: from biosensing to energy. Journal of Materials Chemistry B, 1, 3521-3524 (2013).
12. B Park, R Zheng, K Ko, B Cameron, D Yoon, D Kim. A novel glucose biosensor using bi-enzyme incorporated with peptide nanotubes. Biosensors and Bioelectronics, 38, 295-301 (2012).
13. B Park, D Yoon, D Kim. Encapsulation of enzymes inside peptide nanotubes for hydrogen peroxide detection. Electrochemical Society Transactions, 33, 25-29 (2010).
14. J Castillo, T Rindzevicius, K Wu, M Schmidt, K Janik, A Boisen, W Svendsen, J Castillo-León. Synthesis and characterrization of covalent diphenylalanine nanotube-folic acid conjugates. Journal of Nanoparticle Research, 16, 1-8 (2014).
15. M Bradford. A rapid and sensitive method for quantitation of microgram quantities of protein utilizing the principle of proteindye binding. Analytical Biochemistry, 72, 248-254 (1976).
16. I Sakharov, M Vesga, I Galaev, I Sakharova, O Pletjushkina. Peroxidase from leaves of royal palm tree Roystonea regia: purification and some properties. Plant Science, 161, 853-860 (2001).
17. R Pauliukaite, E Ghica, O Filho-Fatibello, C Brett. Comparative study of different cross-linking agents for the immobilization of functionalized carbon nanotubes with a chitosan film supported on a graphite-epoxy composite electrode. Analytical Chemistry, 81, 5364-5372 (2009).
18. M Yemini, M Reches, E Gazit, J Rishpon. Peptide nanotubemodified electrodes for enzyme-biosensor applications. Analytical Chemistry, 77, 5155-5159 (2005).
19. J Castillo, E Ferapontova, D Hushpulian, F Tasca, V Tishkov, T Chubar, I Gazaryan, L Gorton. Direct electrochemistry and bioelectrocatalysis of H2O2 reduction of recombinant tobacco peroxidase on graphite. Effect of peroxidase single-point mutation on Ca2+- modulated catalytic activity. Journal of Electroanalytical Chemistry, 588, 112-121 (2006).
20. E. Ferapontova, L. Gorton. (2001). Effect of proton donors on direct electron transfer in the system gold electrode-horseradish peroxidase. Electrochemistry Communications, 3, 767-774.
21. T Tangkuaraman, C Ponchio, T Kangkasomboon, P. Katikawong, W Veerasai. Design and development of a highly stable hydrogen peroxide biosensor on screen printed carbon electrode based on horseradish peroxidase bound with gold nanoparticles in the matrix of chitosan. Biosensors and Bioelectronics, 22, 2071-2078 (2007).
22. L Gary, J Long. Limit of detection a closer Look at the IUPAC definition. Analytical Chemistry, 55, 712A-724A (1983).
Información de soporte
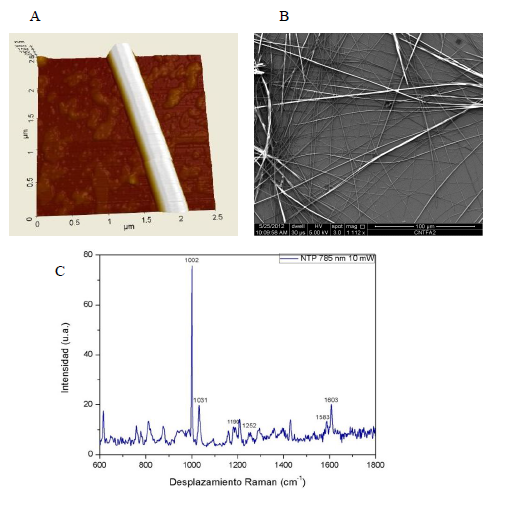
Fig. S1:
(A) Microscopia de fuerza atómica (AFM), por sus siglas en inglés) de NTP; (B) Imagen SEM de una muestra de NTPs y (C) Espectro Raman de las principales vibraciones de los NTPs.
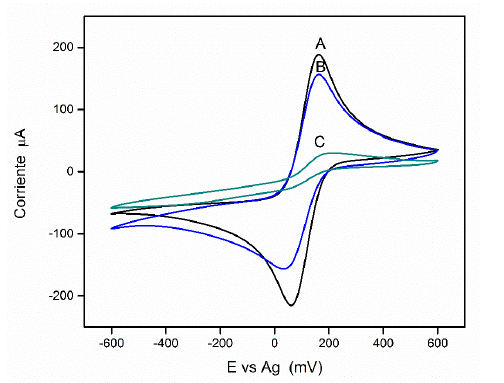
Fig. S2:
VCs de (A) electrodo de oro, (B) electrodo modificado con PPR y (C) electrodo modificado con NTPs-PPR. Ferrocianuro de potasio 10 mM, velocidad de barrido 100 mV/s.
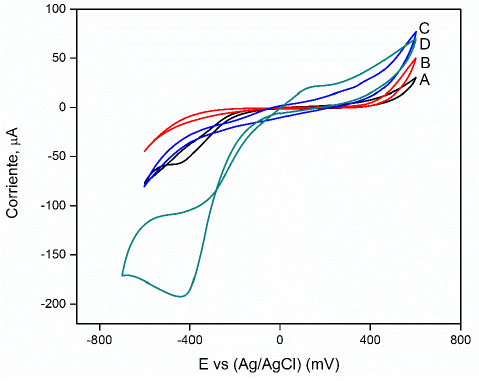
Fig. S3:
VCs de (A) electrodo de oro, (B) electrodo modificado con PPR y (C) electrodo modificado con NTPs-PPR. Solución tampón 10 mM pH 7,0 KCl 0,1 M, H2O2 1 mM; velocidad de barrido 100 mV/s.