Uso de la cáscara de mamón (Melicoccus bijugatus) para el teñido de telas
Using the shell of mammon fruit (Melicoccus bijugatus) for fabric dyeing.
Uso de la cáscara de mamón (Melicoccus bijugatus) para el teñido de telas
Avances en Química, vol. 11, núm. 3, pp. 123-128, 2016
Universidad de los Andes
Recepción: 20 Octubre 2016
Aprobación: 30 Diciembre 2016
Resumen: Este trabajo tiene como objetivo mostrar que la cáscara de Melicoccus bijugatus puede ser utilizada para obtener un colorante para telas. Por el método de reflujo, con NaOH 0,25 N como solvente de extracción, se obtuvo un extracto coloreado café oscuro. Un segundo reflujo con etanol, permitió identificar los metabolitos de la cáscara, causantes de la tinción de los tejidos. El colorante fue aplicado en diferentes tipos de tejidos utilizando diferentes sustancias fijadoras de color (mordientes), para verificar su capacidad de coloración. Los tejidos con mayor absorción del colorante fueron aquellos con mayor contenido de algodón, utilizando Fe2(SO4)3 como mordiente.
Palabras clave: colorante natural, mordientes, textiles.
Abstract: This paper aims to show that Melicoccus bijugatus peel can be used to obtain a dye that can be used in the textile industry. By the reflux method, with 0.25 N NaOH as an extraction solvent, a dark brown colored extract was obtained. A second reflux with ethanol was performed to identify metabolites of peel, that causing staining of tissues. The dye was applied in different tissue types using different binding substances color (mordants), to verify its dyeability. Tissues with higher dye uptake were those with higher content of cotton, using Fe2(SO4)3 as a mordant.
Keywords: natural coloring, mordant, textile industry.
Introducción
Desde la antigüedad la obtención de colorantes a partir de productos naturales ha sido una práctica común en diferentes culturas. Pero la importancia de los colorantes naturales en la industria textil bajó con el uso, ahora extendido, de los colorantes sintéticos empleados en distintas fibras. Sin embargo, durante los últimos 10 años, el uso de los colorantes naturales ha tenido un gran incremento a nivel mundial, debido a la exigencia de su uso en las industrias alimenticias, farmacéuticas y cosméticas establecidas por las legislaciones de los diferentes países; recientemente el uso de colorantes naturales en las industrias de cuero y textil ha iniciado su aplicación. El creciente uso de estos colorantes, ha dado como resultado el incremento de la demanda; generando en algunos casos problemas de abastecimiento en el mercado mundial. Los colorantes naturales han tenido mucho auge debido a su biodegradablilidad y a su baja toxicidad, dichos colorantes se emplean tanto para el teñido de fibras naturales o sintéticas, especialmente en Latinoamérica1.
Se han realizado trabajos basados en el aprovechamiento de los desechos generados por diferentes especies vegetales, para la obtención de colorantes naturales, principalmente para uso en textiles, tales como el realizado a partir de la semilla de aguacate (Persea americana)2, de cáscara de plátano verde (Musa paradisiaca)3, de la pulpa seca del café (Coffea arabica)4, de cáscara de cebolla blanca y morada (Allium cepa) y raíz de remolacha (Beta vulgaris)5, de la semilla del achiote (Bixa orellana)6 y del extracto de la cáscara de almendras7, entre otros.
El mamón (Melicoccus bijugatus), también conocido como mamoncillo, quenepa, genip y lime spanish, entre otros, es un frutal perteneciente a la familia Sapindaceae, género Melicoccus. Es originario de América Tropical y se ha cultivado y naturalizado a través de Centro y Sur América así como en las Antillas. En Venezuela este frutal crece hasta los mil metros sobre el nivel del mar. Es abundante en la zona cálida y su cultivo se hace de manera semi-silvestre se propaga por semillas las cuales crecen rápidamente al caer al suelo8.
En esta investigación se obtuvo un colorante para aplicación en la industria textil, partiendo de la cáscara de mamón, de la cual no se ha encontrado registro alguno de su aprovechamiento en la industria; por tanto, se constituye en un desecho orgánico, cuyas características fisicoquímicas le dan cierto potencial para ser aprovechado como la materia prima principal para la obtención de un colorante para la industria textil.
Parte experimental
Preparación de la muestra
Después de recolectar 6 kilogramos del fruto en diferentes zonas del área metropolitana de San José Cúcuta, Norte de Santander, Colombia, se separó la cáscara del fruto del mamón, de la cual se obtuvo una muestra con una masa aproximada de 1 kilogramo. La cáscara fue sometida a un proceso de secado por 24 horas a 55 °C, obteniendo 690 gramos de muestra seca, que luego fue molida y utilizada para realizar las extracciones. La extracción alcohólica, para la identificación fitoquímica, se realizó con etanol al 96 % (v/v) (Merck) y la alcalina, para la obtención del colorante, con soluciones de diferente concentración de hidróxido de sodio (Merck).
Obtención del extracto etanólico y determinación de la composición metabólica.
Según Lock, 2001, las plantas producen una diversidad de sustancias, producto del metabolismo secundario, algunas responsables de la coloración y aromas de flores y frutos; en el caso del mamón los metabolitos secundarios son los causantes de la tinción que se produce en la fibra textil al entrar en contacto con el fruto9. Con base en esta información, se realizó la obtención del extracto etanólico mediante reflujo, a una muestra de cáscara de mamón seca, luego se realizaron diferentes pruebas fitoquímicas en el extracto, con el fin de determinar cuál o cuáles son los metabolitos responsables de la tinción. En la figura 1 se muestra el procedimiento utilizado para obtener el extracto alcohólico y se mencionan las pruebas fitoquímicas realizadas al extracto.
Extracción del colorante
La extracción del colorante de la cáscara de mamón procesada, se realizó mediante el método de reflujo con solución de hidróxido de sodio (NaOH), para obtener el colorante en medio acuoso. Se realizaron seis pruebas variando la concentración de la solución de NaOH (2,00 N; 1,00 N; 0,50 N; 0,25 N; 0,125 N y 0,0625 N), se mantuvieron las condiciones de temperatura en 80 °C, tiempo de extracción una hora, volumen de solvente 200 mL y cantidad de muestra 20 g. Estas condiciones fueron seleccionadas teniendo en cuenta el trabajo de Devia10.
Aplicación del colorante
Mediante la técnica de tinción directa (sin uso de mordiente), se aplicaron los extractos coloreados obtenidos con las diferentes concentraciones de NaOH a diferentes pedazos de tela de 10 x 10 cm, luego se llevaron a calentamiento durante media hora con el fin de que el colorante entrara en contacto con la fibra. Se dejaron en reposo durante 24 horas, se lavaron y secaron. La tela seleccionada para la tinción directa se escogió teniendo en cuenta que tuviera un contenido intermedio de algodón, una tela que cumple este requisito es el velino, la técnica directa se realizó con un sólo tipo de tela con el fin de facilitar la selección del extracto coloreado que ocasionara mejor tinción en la fibra (intensidad del color perceptible visualmente) y que tuviese la menor concentración de NaOH.
Para realizar el método indirecto se utilizaron siete muestras textiles de diferente composición, unas con contenido de algodón (franela, chalis, punto roma y drill) y otras de origen sintético (dacrón, escuba y creepe). Se realizó con la presencia de diferentes soluciones mordientes (entre ellos, NaCl, Na2SO4, FeCl3, Fe2(SO4)3 y Al2(SO4)3 al 10 y 20 % p/v). En cada solución mordiente se introdujo una tira por cada tipo de tela seleccionada, se dejaron reposar por 30 minutos con el fin de que la fibra textil entrara en contacto con el mordiente, para ayudar a la posterior fijación del colorante. Pasado el tiempo de reposo, se retiró el exceso de la solución de mordiente y se adicionó a cada tela el extracto del colorante que causó mayor tinción por el método directo, luego fueron sometidas a calentamiento durante 30 minutos, se dejaron enfriar a temperatura ambiente, al final se retiraron las muestras textiles del colorante, se escurrieron y se secaron al ambiente. Se lavaron con agua y jabón en forma repetida para comprobar el grado de fijación del colorante en las mismas.
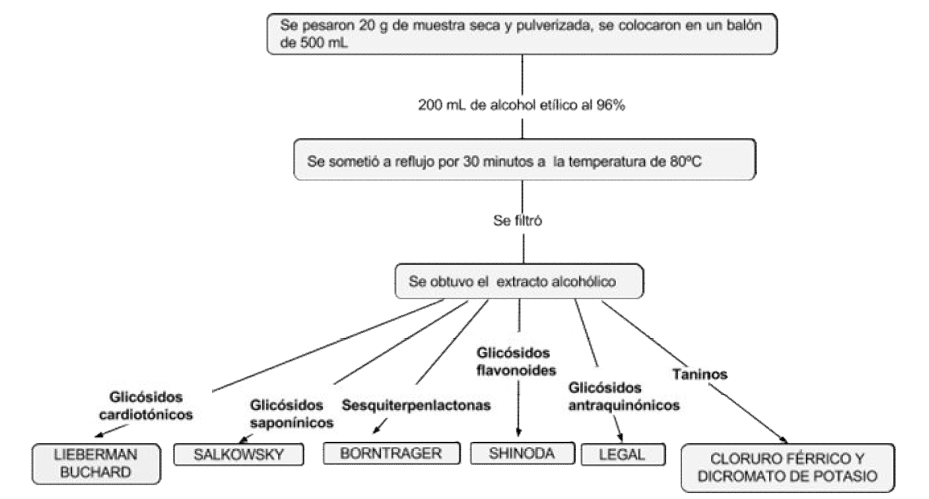
Fig. 1:
Esquema de extracción con alcohol etílico y pruebas fitoquímicas.
Pruebas de resistencia del color
Después de realizar el proceso de tinción indirecta, se seleccionaron tres mordientes (Al2(SO4)3, FeCl3 y Fe2(SO4)3 al 20 % p/v) y la tela que mejor intensidad de color presentó con dichos mordientes. Con estos dos factores (mordiente – tela) se realizaron las pruebas de resistencia del color: solidez del color a la exposición solar, solidez del color al lavado, solidez del color al planchado en tela lavada y sin lavar y solidez del color al frote. Para esto, se obtuvieron tres extractos coloreados de la cáscara del mamón por el método de reflujo con NaOH. Luego se tuvo en cuenta el factor mordiente-tela para teñir 45 trozos de tela por cada extracto, es decir 15 por cada mordiente, con el fin de evaluar su color con las pruebas de resistencia (figura 2).
Para las pruebas de resistencia del color se tomó como referencia el trabajo realizado por Paredes11, debido a que en este evaluó la obtención y aplicación de un colorante natural (Baccharis latifolia (chilca)), al igual que el presente trabajo. Las pruebas de resistencia del color se realizaron por triplicado.
Análisis del extracto coloreado y alcohólico por espectroscopia UV-Vis.
Se realizó el análisis UV-Vis en un espectrofotómetro UV 2300II (DINKO), tanto al extracto coloreado obtenido en NaOH 0,25 N, como al extracto etanólico en el que se extrajeron los componentes fitoquímicos de la cáscara del mamón, haciendo un barrido entre 200 y 700 nm.
Resultados y discusión
Obtención del extracto etanólico y determinación de la composición metabólica.
En el extracto alcohólico obtenido se realizaron pruebas fitoquímicas, con el fin de hacer la identificación de los metabolitos secundarios, estos fueron (tabla 1): glicósidos cardiotónicos (Lieberman Buchard), glicósidos saponínicos (Salkowsky), glicósidos flavonoides (Shinoda), glicósidos antraquinónicos (Borntrager), taninos (tricloruro de hierro y dicromato de potasio) y sesquiterpenlactonas (Legal).
Extracción y aplicación del colorante
En la extracción inicial del colorante se obtuvieron seis extractos en soluciones de NaOH (2,00 N; 1,00 N; 0,50 N; 0,25 N; 0,125 N y 0,0625 N), que fueron aplicados mediante la técnica de tinción directa a varias tiras de velino, el cual tiene un contenido intermedio de algodón. Esta se realizó con un solo tipo de tela, con el fin de facilitar la selección del extracto coloreado, el cual tuviese la menor concentración de NaOH y que ocasionara mejor tinción en la fibra, es decir, que la intensidad del color fuese perceptible visualmente. Después del proceso de tinción, reposo, lavado y secado de las tiras de tela, se observó que el extracto obtenido en la solución de NaOH 0,25 N, cumplía dichos requisitos (figura 3).
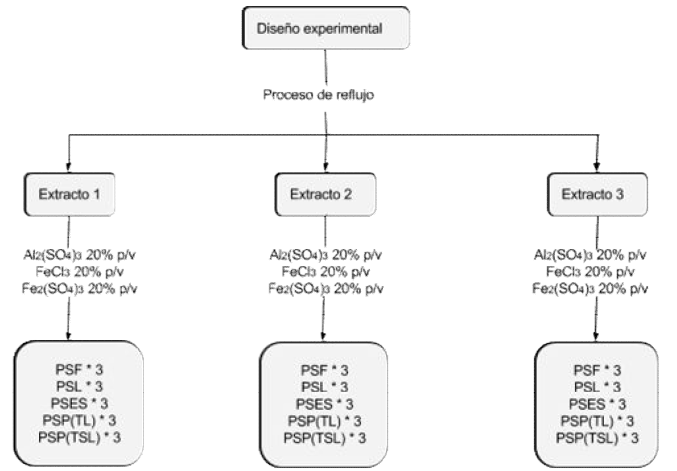
Fig. 2:
Diseño para evaluar la resistencia del color
PSF*3: prueba de solidez al frote por triplicado, PSL*3: prueba de solidez al lavado por triplicado, PSES*3: prueba de solidez a la exposición solar por triplicado, PSP (TL)*3: prueba de solidez al planchado en tela lavada por triplicado, PSP (TSL)*3: prueba de solidez al planchado en tela sin lavar por triplicado.

Fig. 3:
Resultados de la prueba de tinción directa en el velino con cada extracto obtenido en el reflujo con NaOH
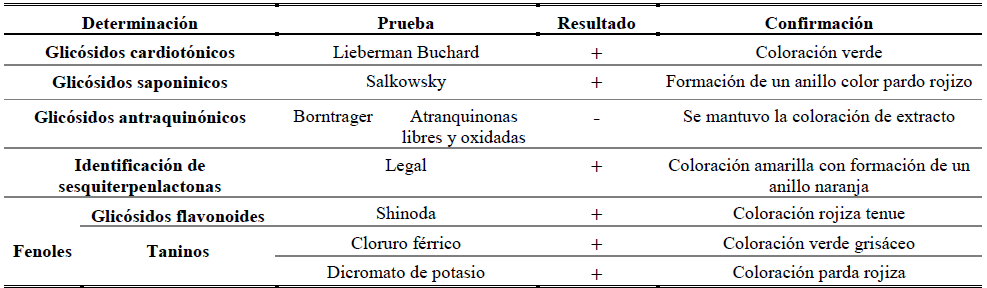
(+): Resultado Positivo de la prueba (-): Resultado Negativo de la prueba.
Una vez seleccionado el colorante que presentó la mayor intensidad de color mediante la tinción directa (0,25 N), se realizó la tinción indirecta de siete muestras textiles de diferente composición, unas con contenido de algodón (franela, chalis, punto roma y drill) y otras de origen sintético (dacrón, escuba y creepe). La tinción indirecta se realizó utilizando diferentes soluciones mordientes al 10 y 20 % p/v. Se seleccionaron los tres mordientes que mejor tinción produjeron (Al2(SO4)3, FeCl3 y Fe2(SO4)3al 20% p/v) y la tela que mayor intensidad de color presentó con dichos mordientes (chalis).
Pruebas de resistencia del color
Después de seleccionar la tela y los mordientes, se obtuvieron tres extractos coloreados de la cáscara del mamón, por el método de reflujo con NaOH 0,2500 N. Se tuvo en cuenta el factor mordiente-tela para teñir 45 trozos de tela por cada extracto, es decir 15 por cada mordiente, con el fin de evaluar su color con las pruebas de resistencia. Los valores que se tuvieron en cuenta para calificar la resistencia del color en las diferentes pruebas11, se observan en la tabla 2. Los resultados obtenidos se muestran en la tabla 3.

Paredes, 2002
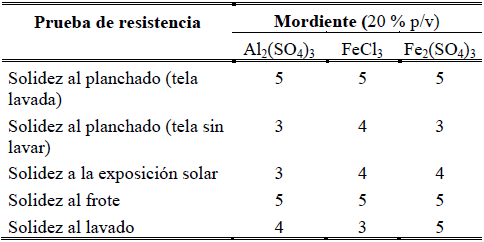
De los resultados de la tabla 3, respecto a la evaluación de las pruebas de resistencia del color con el índice reportado por Paredes, se encuentra que se tienen mejores resultados en cuanto a la solidez del color al planchado, cuando este se realiza en la tela lavada después de la aplicación del colorante, con valores del índice de 5 para los tres mordientes utilizados (Al2(SO4)3, FeCl3 y Fe2(SO4)3, respectivamente), lo que indica que la tela no destiñe, mientras que al realizar el planchado en la tela sin lavar, la tela destiñe sensiblemente, con respectivos valores del índice de 3, 4 y 3.
Con la prueba de resistencia del color a la exposición al sol, se observa que al utilizar Al2(SO4)3 como mordiente, la tela destiñe sensiblemente (3), mientras que con FeCl3 y con Fe2(SO4)3, la tela destiñe un poco, con valores del índice de 4, para los dos mordientes.
Los ensayos realizados en la prueba de solidez al frote, para las telas mordentadas con Al2(SO4)3, FeCl3 y Fe2(SO4)3, dieron como resultado valores del índice de 5, indicando que la tela no destiñe.
Respecto a la solidez del color al lavado de la tela con agua y detergente, se observó que al utilizar Al2(SO4)3 y FeCl3 como mordientes, la tela destiñe sensiblemente, mientras que con Fe2(SO4)3, el valor fue 5, lo que indica que en las pruebas repetidas la tela no destiñe.
Al observar los valores reportados por Paredes asignados en las pruebas de resistencia del color, con respecto a los mordientes, se evidencia que el que presentó mejores resultados fue el Fe2(SO4)3 al 20% p/v, seguido del FeCl3 al 20% p/v. Esto permite confirmar que el metal (en este caso el hierro), es el que predomina en el mordentado disociándose como catión (Fe+3), uniéndose a la fibra textil formando un complejo con las moléculas del colorante, siendo el metal el que determina la tonalidad final de la fibra11.
Análisis de los extractos coloreado y alcohólico por espectroscopia UV-Vis
Los espectros UV-Vis de los extractos, el coloreado obtenido en el proceso de reflujo con NaOH 0,25 N y del extracto alcohólico, en el que se extrajeron los componentes fitoquímicos de la cáscara del mamón, se muestran en las figuras 4a y 4b, respectivamente. Se puede observar la presencia de componentes que absorben tanto en la región visible como en la ultravioleta, sin embargo, por la apariencia de los dos espectros las sustancias “no son similares”, debido a que cada extracto está disuelto en un solvente diferente, el coloreado en solución acuosa de NaOH 0,25 N y el fitoquímico en etanol.
Según los resultados de las pruebas fitoquímicas, los metabolitos presentes en el extracto alcohólico fueron glicósidos cardiotónicos, glicósidos saponínicos, glicósidos flavonoides, taninos y sesquiterpenlactonas. Los rangos de absorbancia de los metabolitos presentes en el extracto alcohólico van desde 205 hasta 550 nm, los glicósidos cardiotónicos absorben entre 215-220 nm12, los glicósidos flavonoides entre 240-284 nm banda I y 300-550 banda II13, los glicósidos saponínicos en 231 nm14, los taninos entre 270-290 nm15 y las sesquiterpenlactonas entre 205-230 nm16; sin embargo, en las figuras 4a y 4b se evidencia la absorción de radiación hasta los 700 nm.
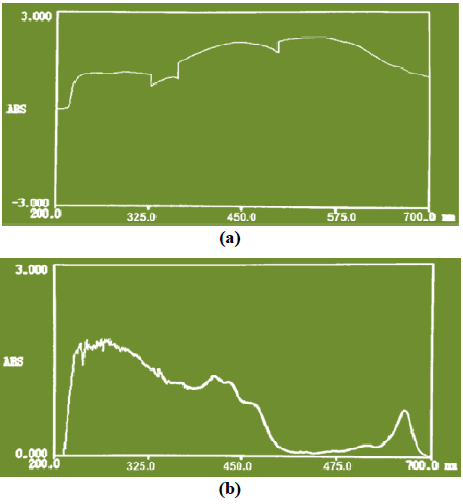
Fig. 4:
(a) Espectro ultravioleta visible del extracto coloreado. (b) Espectro ultravioleta visible del extracto alcohólico.
Es importante considerar que los compuestos orgánicos que contienen electrones p y no enlazantes (n), presentan las transiciones de estos electrones al estado excitado p*, que producen picos de absorción dentro de la región espectral de 200 a 700 nm17. Por lo tanto, la absorción por encima de los 550 nm, presente en los espectros (figuras 4a y 4b) es debida a que las estructuras de los metabolitos presentes contienen pares libres de electrones e insaturaciones.
Los glicósidos flavonoides son compuestos fenólicos que contribuyen a la pigmentación de muchas partes de la planta, por ejemplo, las antocianinas son las responsables del color rojo, naranja, azul, púrpura o violeta que se encuentra en las cáscaras de las frutas y hortalizas. Por otro lado, cuando los fenoles son oxidados, dan lugar a las quinonas responsables del color pardo que muchas veces es indeseable18.
Conclusiones
La tinción generada por la cáscara del Melicoccus bijugatus podría deberse a la presencia de pigmentos producidos por los flavonoides, estos pigmentos podrían representar un potencial para el reemplazo competitivo de colorantes sintéticos en la industria textil.
Entre las diferentes telas utilizadas (dacrón, franela, chalis, escuba, creepe, punto roma y drill), las que presentaron mayor absorción de color fueron aquellas con mayor contenido de algodón como el chalis y el drill, ya que las telas con bajo contenido o sin algodón como el dacrón, conservaban su color o se mantenían en tonalidades muy claras en comparación con las primeras.
Las pruebas de tinción indirecta con los diferentes mordientes utilizados, permitieron obtener en las tela una gama de tonos café, siendo el Fe2(SO4)3 el mordiente que presentó tonalidades más intensas y resistentes en las pruebas realizadas.
La obtención de un colorante para telas a partir de la cáscara de mamón, es una nueva alternativa para el aprovechamiento de este desecho orgánico, que a la vez permite fomentar el uso de colorantes naturales en la industria textil ante el uso excesivo de colorantes de origen sintético.
Referencias
1. A Rojas, F Maldonado, OA Pérez. Cinética y extracción de colorantes naturales. Memorias del XVI Congreso Latino-Americano de Química Textil. Quito-Ecuador (2001).
2. JE Devia, D F Saldarriaga. Proceso para Obtener Colorante a Partir de la Semilla del Aguacate. Revista Universidad EAFIT, 41(137), 36-43 (2005).
3. D Vásquez, CE Fuentes. Obtención de un colorante a partir de Musa paradisiaca (plátano verde) con aplicación en la industria textil. Universidad de El Salvador, El Salvador (2008).
4. MY Díaz, GN Elias. Propuesta para la obtención de un colorante natural a partir de la pulpa seca del Coffea arabica (Café). Universidad de El Salvador, El Salvador (2009).
5. SJ Trujillo, WM López. Obtención de colorantes naturales a partir de cáscara Allium cepa (cebolla blanca y morada) y raíz de Beta vulgaris (Remolacha) para su aplicación en la industria textil. Universidad de El Salvador, El Salvador (2010).
6. JE Devia, L Saldarriga. Planta piloto para obtener colorante de la semilla del achiote (Bixa orellana). Revista Universidad EAFIT, 39(131), 8-22 (2012).
7. İ Özlenen, L Yıldırım, E Özdoğan. Use of almond shell extracts plus biomordants as effective textile dye. Journal of Cleaner Production, 70, 61-67 (2014).
8. HC Pérez, M Gómez, J Vila. Evaluación de los parámetros de calidad en frutos de mamoncillo (Melicoccus bijuga L.). Características químicas. Revista Iberoamericana de Tecnología Postcosecha, 9(1), 7-15 (2008).
9. O Lock. Análisis Fitoquímico y Metabolitos Secundarios. In: M López y O Vargas. Manual de Fitoterapia. Lima: Es Salud. p. 41-64 (2001).
10. JE Devia. Pulverización de colorantes naturales por secado por atomización. Universidad EAFIT. Cuadernos de Investigación, (33), (2005).
11. B Paredes. Análisis y obtención de colorante natural a partir de la Baccharis latifolia (chilca). Universidad Técnica del Norte. Ibarra-Ecuador (2002)
12. A Martínez. Esteroides cardiotónicos (2002). Recuperado de: http://farmacia.udea.edu.co/~ff/cardiotonicos.pdf
13. O Lock. Colorantes naturales. Fondo editorial Pontificia Universidad Católica del Perú. Lima, Perú, 274 p. (1997).
14. A Martínez. Saponinas Esteroides (2001). Recuperado de: http://farmacia.udea.edu.co/~ff/saponinas2001.pdf
K Fernández. Caracterización de taninos (2007). Recuperado de: http://www.feng.pucrs.br/laboratorios/taninos/restrito/caracterizacion-taninos.pdf
16. A Martínez. Sesquiterpenlactonas (2001). Recuperado de: http://farmacia.udea.edu.co/~ff/slactonas2001.pdf
17. E Gimeno Creus. Compuestos fenólicos un análisis de sus beneficios para la salud. Offarm, 23(6), (2004)
18. D Skoog, J Holler, T Nieman. Principios de Análisis Instrumental. Mc Graw Hill. Madrid (2001).