Artículos científicos
Efecto de los tratamientos alcalino y de oscuridad-salinidad en agar de Gracilaria domingensis
Effect of the alcalino and dark-salinity treatments in agar of Gracilaria domingensis
Efecto de los tratamientos alcalino y de oscuridad-salinidad en agar de Gracilaria domingensis
Avances en Química, vol. 15, núm. 2, pp. 35-40, 2020
Universidad de los Andes

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial 4.0 Internacional.
Recepción: 31 Mayo 2020
Aprobación: 21 Agosto 2020
Resumen: Para la extracción del agar de Gracilaria domingensis, el alga fue dividida en dos partes, a una parte se le aplicó tratamiento alcalino con NaOH, mientras que a la otra se le aplicó tratamiento de oscuridad-salinidad. La evaluación de la temperatura de gelificación, temperatura de fusión y fuerza de gel de los agares extraídos mediante tratamiento alcalino indican que son de mejor calidad que los extraídos con tratamiento de oscuridad-salinidad. El análisis estadís- tico muestra que con tratamiento alcalino la concentración de 0,04 M de NaOH fue la que reportó el mayor rendimiento, mientras que a 0,06 M se extrajo el de mejor calidad.
Palabras clave: agar, fuerza de gel, Gracilaria, oscuridad-salinidad, tratamiento alcalino.
Abstract: For the extraction of Gracilaria domingensis agar, the alga was divided into two parts, a specific alkaline treatment with NaOH, while the other was applied a dark-salinity treatment. The evaluation of the gelation point, melting point and gel strength of the agar extracted by alkaline treatment indicates that they are of better quality than those extracted with dark-salinity treatment. Statistical analysis shows that with alkaline treatment the concentration of 0.04 M NaOH was the one that reported the highest yield, while the best quality was extracted at 0.06 M NaOH.
Keywords: Agar, Gel strength, Gracilaria, Treatment alkaline, Darkness-salinity.
Introducción
El agar es una mezcla de polisacáridos, la agarosa que es el polisacárido con propiedades gelificantes y posee una estructura alternante de 3,6 anhidro-L-galactosa (3,6-AG) y D- galactosa, y la agaropectina que es un polisacárido sulfatado con baja fuerza de gel1-2. Las unidades repetitivas pueden estar sustituidas en mayor o menor grado por grupos sulfatos, metilos y piruvatos., los grupos sustituyentes interfieren en la formación de la estructura en hélice durante el proceso de gelificación, por ejemplo agares con un alto contenido de grupos sulfato están asociados con geles de poca dureza3, la cantidad y localización de estos grupos sustituyentes en la molécula, además de factores medioambientales y diferentes procedimientos de extracción, pueden influir en la calidad del agar obtenido1,4. El rendimiento y las propiedades físicas del agar son función de la fuente del agarofito, los factores ambientales y fisiológicos, así como los procedimientos de extracción y recuperación.. La calidad del agar se refleja en sus características físicas, por ejemplo, sinéresis de gel, temperaturas de fusión y gelificación y fuerza de gel, este último es el principal indicador de la calidad del agar6.
El agar se extrae de las paredes de las algas Rhodophyta de los géneros Gelidium, Gracilaria, Pterocladia, Gelidiella . Ahnfeltia7,8, siendo Gelidium y Gracilaria los géneros que constituyen la mayor parte de la materia prima utilizada para la extracción de agar9. Gelidium es el género de preferencia en la extracción de agar, esto debido a la facilidad en el proceso de extracción10, pero las poblaciones naturales de este género han disminuido debido a que es un alga pequeña, posee una tasa de crecimiento baja y los intentos de cultivo no han demostrado ser comercialmente viables, en contra parte las especies de Gracilaria son algas más grandes y se han cultivado con éxito11, estas son grupo de algas de aguas tanto frías como templadas., según la FAO hay más de ciento cincuenta especies
en el mundo, algunas de las cuales tienen un valor económico muy importante12. El uso industrial que se le da a las especies del género Gracilaria, es principalmente como materia prima para la producción de agar12,1314, por lo que ahora son la principal fuente (alrededor del 65 por ciento) de agar11.
Especies del género Gracilaria producen agares débiles debido a que contienen grandes cantidades de sulfatos en comparación con agares obtenidos de especies de Gelidium., es por ello que a través de los años se han realizado diversos estudios con la finalidad de disminuir la gran cantidad de grupos sulfatos que contienen los agares de este género.. Una manera de solucionar la alta concentración de grupos sulfatos y la baja cantidad de agarosa del agar de especies de Gracilaria es por medio de un tratamiento alcalino con hidróxido de sodio. El tratamiento de especies de Gracilaria con NaOH reduce el alto contenido de sulfatos en el agar de estas especies, al convertir la L-galactosa-6-sulfato en 3-6 anhidro-L-galactosa1,2,8,10,15, como consecuencia de este tratamiento se ha observado la reducción del rendimiento en el agar y un incremento en la fuerza de gel, así como aumento de su temperatura de gelificación y fusión5,16. Debido a que las diferentes especies de Gracilaria poseen agar con diferentes concentraciones de sulfatos, el rendimiento y las características del agar de una especie en particular dependerán de la concentración de álcali utilizado..
Existe otro método alternativo para inducir la conversión del sulfato inestable a 3,6-AG para incrementar el rendimiento del agar, este método involucra el manejo de algunos procesos enzimáticos en el alga, a través de un tratamiento bajo condiciones de hiper e hiposalinidad y de oscuridad. Bajo estas condiciones se produce la activación de enzimas sulfohidrolasas y sulfotransferasas que provocan la desulfatación de la molécula aumentando los niveles de 3,6-AG y por lo tanto, la fuerza del agar17,18,19,20. Ekman et al. sugieren que el carbono resultante de la degradación del almidón florideano y del florodósido durante estas condiciones de oscuridad y choque osmótico puede movilizarse hacia la síntesis de agar17.
Se ha reportado varios estudios de extracción de agar en G. domingensis, Lahaye et al., extrajeron agar con etanol y agua caliente, y empleando espectroscopía de I3C-NMR determinaron que una fracción de agar estaba compuesta de 6-O- metilado agarobiosa, 6-sulfato-agarobiosa, agarobiosa y una unidad repetitiva con 4-O-metil-α-L-galactosa21. Duckworth et al., demostraron que la fuerza del gel del agar de G dominguensis, mejoró muy poco, de 14 a 22 g al aplicar tratamiento alcalino15. Durairatnam et al., evaluaron durante un año la influencia sobre el rendimiento y la fuerza de gel del agar de G. domingensis, extraído con ácido clorhídrico al 1%, blanqueado y tratado con una solución alcalina al 1% con calcio, los autores observaron que a pesar de mejorar el rendimiento del agar este mostró baja fuerza de gel22. Valiente et al. empleando espectroscopia RMN 1H y 13C, confirmaron que los polisacaridos de G. domingensis pertenecen al grupo de agar con un patrón de sustitución en C-6- de D-galactopiranosa con residuos de grupos O-metil y éster sulfato23.
Países como Argentina, Brasil, México y Venezuela ofrecen las mejores perspectivas para el desarrollo de las industrias de algas11,24. La naturaleza de la estructura química de los agares de especies de Gracilaria permite que sean ampliamente usados como agente espesante y gelificante en la industria alimentaria y en numerosas aplicaciones biotecnológicas, médicas y farmacéuticas4,12. Por lo que el propósito de este estudio fue observar el efecto que tienen los tratamientos de álcalinidad y oscuridad-salinidad sobre el rendimiento y las propiedades fisicoquímicas de agar de Gracilaria domingensis presente en las playas de la Península de Paraguaná, Venezuela.
Parte experimental
Área de estudio
La recolección de la especie G. domingensis (Kützing) Sonder ex Dickie 1874 se realizó en las costas de la Península de Paraguaná, específicamente en Puerto Escondido (69º41’- 70º17’ O y 12º11’ N). Rodríguez et al.25señalan que en dicha zona intermareal predominan las especies del género Gracilaria, debido a las condiciones ambientales adecuadas para su crecimiento, como es el movimiento moderado del agua. Las algas fueron lavadas en agua de mar para eliminar sedimentos y epifitas y fueron transportadas al laboratorio en bolsas de polietileno. A su llegada se dividió en dos partes para aplicar- les los respectivos tratamientos de extracción.
Tratamiento alcalino
Para el tratamiento alcalino las algas fueron lavadas con agua dulce, secadas sobre una superficie lisa expuestas al sol y pesadas, luego se siguió la metodología con modificaciones descrita por Meena et al.26, remojando 25 g de cada alga seca en un 1 L de agua por 12 h, seguidamente se realizaron extracciones por triplicado a una temperatura de 90 ºC por 2 h empleando concentraciones de hidróxido de sodio entre 0,02 y 0,10 M. Bechara y Betancourt27trabajaron esta especie a concentraciones entre 0,10 y 1,0 M de NaOH, reportando el mayor rendimiento a 0,10 M, por lo que recomendaron extraer el agar a concentraciones inferiores a esta. Luego se filtraron las soluciones con la ayuda de un trozo de tela, los extractos obtenidos, se dejaron en reposo a temperatura ambiente hasta que gelificaron, mientras que a los residuos se les aplicó una segunda extracción con 1 L de agua por 90 min por 1 h. Transcurrido este tiempo las soluciones se filtraron, lo extractos se dejaron en reposo a temperatura ambiente hasta que gelificaron. Después se congelaron a una temperatura menor de 10 ºC y se descongelaron para filtrarlos en frio. Una vez descongeladas las muestras se procedió a filtrarlas con una tela y con la ayuda de una espátula se retiraron los agares, y se llevaron a calentamiento con 250 mL de agua hasta ebullición por 15 min. Después se filtraron al vacío, secaron, pesaron y se calculó el rendimiento.
Tratamiento de oscuridad-salinidad
Para el tratamiento de oscuridad-salinidad se siguió la metodología descrita por Freile et al.18, las algas de G. do mingensis fueron almacenadas en tobos plásticos pintados de negro, con aireación y en oscuridad con soluciones al 50% de salinidad por 4 días, pasado estos, se les aplicó oscuridad en soluciones al 25% de salinidad por 4 días, al final de este tratamiento fueron pesadas, lavadas con agua dulce, secadas sobre una superficie lisa expuestas al sol y pesadas. Luego se remojaron por separado 25 g de algas secas de cada especie en 1 L de agua por 24 h. Transcurrido este tiempo las algas fueron sumergidas en 1 L de agua destilada a un pH de 6,3–6,4 y lleva-das a ebullición a una temperatura de 100–105 °C durante 1,5 h. Una vez culminada la extracción se procedió a filtrar las soluciones con la ayuda de una tela para separar los extractos de los residuos y se dejaron en reposo a temperatura ambiente hasta que gelificaron. A los residuos obtenidos de cada especie se les realizó una segunda extracción con 500 mL de agua por 30 min. Después de este paso se siguió la metodología descrita a partir de la segunda extracción de agar del tratamiento alcalino. Una vez pesados los agares se procedió a calcular el rendimiento.
Determinación de las propiedades fisicoquímicas
El porcentaje de humedad se determinó de acuerdo con el protocolo de la Association of Official Agricultural (AOAC 14.004)28. Las temperaturas de gelificación y fusión se determinaron siguiendo la metodología descrita por Freile-Pelegrin y Robledo16, utilizando soluciones de agar al 1,5% (p/v). Mientras que para la fuerza de gel se preparó una solución de agar al 1,5% (p/v) y se determinó utilizando un analizador de textura (TA-TX Plus, Stable Micro Systems Ltd.) equipado con un émbolo cilíndrico de 10 mm de diámetro, operado con una velocidad de penetración de 1 mm s−1. La fuerza del gel se calculó y expresó en g cm−2. Todas las determinaciones se realizaron por triplicado.
Análisis estadístico
Mediante el paquete estadístico STATPOINT TECHNOLOGIES. STARGRAPHICS Centurion XV1.0.2.1. 2012, primero se aplicó un diseño completamente al azar (ANOVA) de un factor a los valores de rendimiento y de las propiedades físicas con tratamiento alcalino para demostrar que las concentraciones de NaOH utilizadas en el tratamiento alcalino tuvieron un efecto sobre el rendimiento y las propiedades físicas del agar extraído, seguido de la prueba LSD para demostrar cuales concentraciones provocaron la diferencia. Luego mediante un ANOVA de un factor se realizó una comparación de los valores de rendimiento y propiedades físicas entre los mejores resultados bajo tratamiento alcalino con respecto a los obtenidos en el tratamiento de oscuridad-salinidad. Por último se realizó una regresión polinomial para explicar el comportamiento de alguna de las tres propiedades físicas.
Resultados y discusión
Los resultados de los rendimientos y propiedades fisicoquímicas del agar empleando el tratamiento alcalino a concentraciones de 0,02 y 0,10 NaOH y el de oscuridad-salinidad, se muestran en la tabla 1. Se encontró que con el tratamiento alcalino el rendimiento osciló entre 6,8 y 13,2%, obteniéndose el menor rendimiento a 0,10 M y el mayor a 0,04 M. A excepción del agar obtenidos con 0,08 M de NaOH los rendimientos obtenidos para todos los demás agares fueron superiores a los requeridos por la industria (>8%)10. El rendimiento obtenido a la concentración de 0,04 M de NaOH (13,2%) fue mayor que los reportados con el mismo tratamiento para G. longissima (5,8%) y G. vermiculophylla (9%)29, similares a los reportados para agares de G. gracilis (Turkey), G. chilensis (Chile), G. tenuistipitata (China), G. edulis (Indonesia), G. gracilis (Argentina) y G. gracilis (Brazil), con rendimientos entre 13,37% y 39,5%.; al agar de G. gracilis de Suráfrica (20,1%)30, a los de G. crassissima (13,1%) y G. blodgettii (26,2%). y a los obtenidos de de G corticata (17,47%) y G verrucosa de la costa de Kerala (23,77%)31. El rendimiento con el tratamiento de oscuridad-salinidad fue de 4,8±0,1%, esta disminución puede ser atribuible a la alta salinidad de exposición, lo que conlleva a la pérdida de carbono por respiración o degradación, ocasionando una disminución en la cantidad de agar extraído22. Por otra parte, Wikibia et al.30señalan que los rendimientos obtenidos con este método deben ser interpretados con cautela porque el método de extracción puede llevar a la inclusión de almidón florideano en el agar.
Para el agar extraído de G. domingensis empleando el tratamiento alcalino el contenido de humedad varió entre 12,8 y 16,7%, reportando el menor porcentaje de humedad a la concentración de 0,10 M y el mayor a 0,04 M; mientras que el porcentaje de humedad del agar del tratamiento de oscuridad- salinidad fue de 12,6±0,1%. En general los valores obtenidos de humedad indican altos contenidos de agua en el agar, sin embargo, se consideran aceptables, ya que se encuentran por debajo de lo establecido por la farmacopea de los Estados Unidos (USP) estándares10.
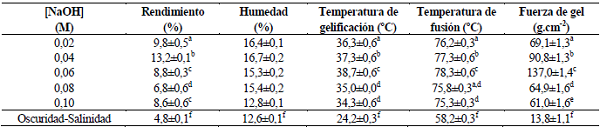
Las letras representan agrupamientos de acuerdo a la prueba LSD; medias con la misma letra no son significativamente distintas (α = 0,05)
En cuanto a la temperatura de gelificación de los agares aplicando el tratamiento alcalino, varió entre 34,3 y 38,7 ºC, mostrando la menor temperatura a la concentración de 0,10 M, observándose un máximo a la concentración de 0,06 M, el cual fue disminuyendo sustancialmente a medida que se disminuyó la concentración de NaOH, mientras que la temperatura de gelificación del agar del tratamiento de oscuridad- salinidad fue de 24,2±0,3 ºC. La diferencia en las temperaturas de gelificación observadas en los diferentes tratamientos se atribuye al grado de metoxilación de la agarobiosa que contiene el agar, a una mayor metoxilación en C. corresponde una mayor temperatura de gelificación, mientras que la metoxilación del resto de los carbonos reduce la temperatura de gelificación.. Las temperaturas de gelificación empleando tratamiento alcalino se encuentran dentro del rango de 29 y 42 ºC que reportan la UNDP/FAO para otras especies del genero Gracilaria12, lo que indica que puede formar geles firmes antes de llegar a la temperatura ambiente, mientras que la temperatura del agar mediante tratamiento de oscuridad- salinidad se encuentra por debajo del rango reportado por FAO. Según Duckworth et al. la presencia de 6-0-metil-D- galactosa afecta la temperatura de gelificación15.
La temperatura de fusión de los agares empleando tratamiento alcalino osciló entre 75,3 y 78,3 ºC, reportando la menor temperatura a la concentración de 0,10 M y la mayor a 0,06 M, también se observa que la temperatura de fusión incrementa a medida que aumenta la concentración NaOH hasta 0,06 M, pero disminuye a valores mayores a 0,06 M. Para las concentraciones mayores de 0,06 M bajo tratamiento alcalino las temperaturas de fusión se encuentra fuera del rango de 76 y 92 ºC que reporta la UNDP/FAO12 para temperaturas de fusión de otras especies. La temperatura de fusión del agar mediante tratamiento de oscuridad-salinidad fue de 58,2±0,3 ºC, indicando que es un agar muy soluble ya que dicho valor se encuentra muy por debajo de los límites establecidos.
La fuerza de gel de los agares empleando el tratamiento alcalino osciló entre 61,0 y 137,0 g/cm., obteniendo la menor fuerza de gel a la concentración de 0,10 M y la mayor a 0,06 M, observándose que la fuerza incrementa a medida que se aumenta la concentración NaOH, hasta llegar a 0,06 M NaOH pero decrece sustancialmente a partir de este valor; mientras que para el agar obtenido aplicando el tratamiento de oscuridad-salinidad la fuerza de gel fue de 13,8±1,1 g/cm.. El aumento en la fuerza del gel después del tratamiento alcalino está relacionado con la presencia de un ester sulfato en el oxígeno del C. de la unidad de la galactosa enlazada en C., y estos residuos con este tipo de sustitución son precursores de 3,6 A-G. De esta manera, la concentración de 3,6-AG se incrementó con la aplicación del tratamiento alcalino, este alto contenido de 3,6-AG produce geles fuertes, mientras que los geles de baja fuerza como el obtenido con el tratamiento de oscuridad-salinidad (13,8±1,1 g/cm.) son asociados a altas concentraciones de sulfatos y baja cantidad de 3,6-AG10,15. La fuerza de gel de G. domingensis con tratamiento alcalino con NaOH al 0,06 M se acerca a los valores reportados con tratamiento para agares de G. longissima (280 g cm–2) y G. vermiculophylla (177,5 g cm–2)29y de G corticata (116,77 g cm–2) y G verrucosa (276,53 g cm–2)31 pero es muy inferior a los reportados para agares de G. tikvahiae (309-485 g cm–2) y G. blodgettii (1059-1293 g cm–2)32, de G. gracilis de Turquia (335 g cm–2)5, de G. cornea (974–1758 g cm–2)16, de G. gracilis de Suráfrica (612 g cm–2)30, de G. cornea (1020 g cm–2) y G. crassissima (1266 g cm–2)33.
En el ANOVA de un factor realizado a los valores de rendimiento y de las propiedades físicas obtenidos en el tratamiento alcalino para G. domingensis, se observó que el valor-P calculado fue de 0,000 (tabla 2) lo que indica que las concentraciones empleadas en dicho tratamiento tuvieron un efecto sobre el rendimiento y las propiedades físicas de los agares extraídos.

De igual forma en la prueba LSD se evidenció que para las concentraciones 0,06 y 0,10 M no presentaron diferencias significativas entre ellas con respecto al rendimiento. Respecto a los valores de temperatura de gelificación se observa que las medias que no reportaron diferencias significativas fueron a 0,08 y 0,10 M, mientras que para la temperatura de fusión las concentraciones 0,02 y 0,08 M y las concentraciones 0,08 y 0,10 M no presentaron diferencias significativas entre ellas. Por su parte con respecto a la fuerza de gel todas las medias tuvieron diferencias significativas (tabla 1).
En el ANOVA de un factor con los valores de rendimiento y propiedades físicas de la concentración con tratamiento alcalino donde se obtuvieron los mejores resultados (0,06 M de NaOH) y los obtenidos en el tratamiento de oscuridad- salinidad, se observó que el valor-P calculado fue de 0,000 (tabla 3); lo que indica que la metodologías de extracción utilizadas si tuvieron un efecto sobre el rendimiento y las propiedades físicas de los agares extraídos.
Con los valores obtenidos de la fuerza de gel de los agares se realizó una regresión polinomial (figura 1), esto debido a que
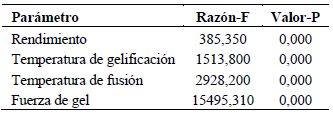
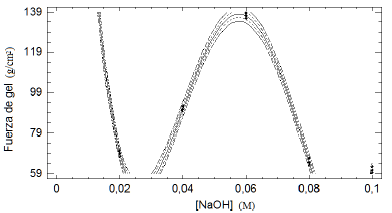
Fig. 1
Regresión polinomial de la fuerza de gel del agar
es la propiedad más importante, ya que también tiene una relación directa con el contenido de 3,6-AG y entre más alta es la concentración 3,6-AG, mayor será la fuerza de gel10,15,34. En dicha regresión se observó que los valores se ajustaron a una ecuación de grado 4 (Ec. 1) con R. igual a 0,9983 en el rango de concentraciones estudiados.
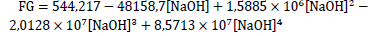 (Ec. 1)
(Ec. 1)Conclusiones
El rendimiento con el tratamiento alcalino fue mayor al obtenido en el tratamiento de oscuridad-salinidad. El agar extraído empleando el tratamiento de alcalinidad fue el que reportó los resultados aceptables de temperatura de gelificación, temperatura de fusión y fuerza de gel. Si se desea el mayor rendimiento de agar se debe realizar la extracción a la concentración de 0,04 M de NaOH, mientras que si lo que se desea es un agar de mejor calidad se debe emplear la concentración de 0,06 M.
Se comprobó que tanto la concentración empleada en el tratamiento alcalino, como la metodología de extracción utiliza-das generaron diferencias significativas en el rendimiento y las propiedades físicas del agar extraído; y que los valores de fuerza de gel se ajustaron a un polinomio de grado 4.
A pesar de que el agar obtenido mostró baja fuerza de gel en comparación a otros agares, la calidad de los geles de agar en la industria, suele ser evaluado en términos de sus aplicaciones prácticas.
Agradecimientos
Los autores desean expresar su agradecimiento a la Dra. Aura Coba del Laboratorio de Alimentos de la Universidad Simón Bolívar por el apoyo en la determinación de la fuerza de los geles, y al Centro de Investigaciones Tecnológicas de la UNEFM por la subvención otorgada al proyecto.
Referencias
1. E Murano. Chemical structure and quality of agars from Gracilaria. J. Appl. Phycol., 7(3), 245–254 (1995).
2. Y Freile-Pelegrín, E Murano. Agars from three species of Gracilaria (Rhodophyta) from Yucatan Peninsula. Bioresour. Technol., 96(3), 295-302 (2005).
3. M Lahaye, C Rochas. Chemical structures and physicochemical properties of agar. Hydrobiologia, 221(1), 137–148 (1991).
4. R Armisén, F Galatas. Agar. En: Handbook of Hydrocolloids. Eds. G Phillips y P Williams. Woodhead Publishing. England (2000).
5. J Rebello, M Ohno, H Ukeda, M Sawamura. Agar quality of commercial agarophytes from different geographical origins. 1. Physical and rheological properties. J. Appl. Phycol., ., 517– 521 (1997).
6. WK Lee, YY Lim, A Leow, P Namasivayam, J Ong, Ch Ho. Factors affecting yield and gelling properties of agar. J. Appl. Phycol., 29(.), 1527-1540 (2017).
7. R Armisen, F Galatas. Production, properties and uses of agar. En: Production and Utilization of Products from Commercial Seaweeds. Ed. McHugh (pp. 1–44). FAO Fish Tech, 288 (1987).
8. DJ McHugh. A guide to the seaweed industry. Food and Agriculture Organization of the United Nations. (pp. 105) FAO Fisheries Technical Paper, 441 (2003). Disponible en: http://www.fao.org/ 3/a-y4765e.pdf
9. DJ McHugh. Alcance de la industria de las algas marinas. En: El estado mundial de la pesca y la acuicultura. Eds. U. Wijkström, A. Gumy y R. Grainger. Food and Agriculture Organization of the United Nations. FAO (2004). Disponible en: http://www.fao. org/3/ y5600s/y5600s07.htm#P5_1117
10. R Armisén. Worldwide use and importance of Gracilaria. J. Appl. Phycol., ., 231-243 (1995).
11. DJ McHugh. Prospects for seaweed production in developing countries. (pp. 968). FAO Fish. Circ., 968 (2002). Disponible en: http://www.fao.org/3/Y3550E/Y3550E00.htm
12. UNDP/FAO (1990) Training Manual on Gracilaria Culture and Seaweed Processing in China. Training Manual 6. Regional Seafarming Development and Demonstration Project (RAS/90/ 002) – UNDP/FAO, People’s Republic of China (1990). Disponible en: http://www.fao.org/3/AB730E/AB730 E00.htm
13. P Torres, J Pires, F Chow, D dos Santos. A comprehensive review of traditional uses, bioactivity potential, and chemical diversity of the genus Gracilaria (Gracilariales, Rhodophyta). Algal Research, 37, 288–306 (2019).
14. A Espi, D Robledo, L Hayashi. Development of seaweed cultivation in Latin America: current trends and future prospects, Phycologia, 58.5), 462-471 (2019).
15. M Duckworth, K Hong, W Yaphe. The agar polysaccharides of Gracilaria species. Carbohydr. Res., 18(1), 1-9 (1971).
16. Y Freile-Pelegrín, D Robledo. Influence of alkali treatment on agar from Gracilaria cornea from Yucatán, México. J. Appl. Phycol., 9(6), 533-539 (1997).
17. P. Ekman, S Yu, M Pedersén. Effect of altered salinity, darkness and algal nutrient status on florodósido and starch content, α- galactosidase activity and agar yield of cultivated Gracilaria sordida. Br. Phycol. J., 26(2), 123–131 (1991).
18. Y Freile-Pelegrín, D Robledo, M Pedersén, E Bruno, J Rönnqvist. Efecto del tratamiento de oscuridad y salinidad en el rendimiento de calidad del agar de Gracilaria cornea (Rhodop- hyceae). Cienc. Mar., 28(3), 289-296 (2002).
19. R Rincones, S Yu, M. Pedersén. Effect of dark treatment on the starch degradation and the agar quality of cultivated Gracilaria lemaneiformis (Rhodophyta, Gracilariales) from Venezuela. Hy- drobiologia, 260/261, 633–640 (1993).
20. P Ekman, M Pedersén. The influence of photon irradiance, day length, dark treatment, temperature, and growth rate on the agar composition of Gracilaria sordida and Gracilaria verrucosa (Hudson) Papenfuss (Gigartinales, Rhodophyta). Bot. Mar., 33(6), 483–495 (1990).
21. M Lahaye, W Yaphe. The chemical structure of agar from Gracilaria compressa (C. Agardh) Greville, G. cervicornis (Turner) J. Agardh, G. damaecornis J. Ag and G. domingensis Sonder ex K€utzing (Gigartinales, Rhodophyta). Bot. Mar. 32(4), 369–377 (1989).
22. M Durairatnam, T de Brito, A de Sena, Studies on the yield and gel strength of agar from Gracilaria domingensis Sonder ex Kuetzing (Gracilariales, Rhodophyta) following the addition of calcium. Hydrobiologia, 204/205, 551-553 (1990).
23. O Valiente, LE Fernandez, RM Perez, G Marquina, H Velez. Agar polysaccharides from the red Seaweeds Gracilaria domingensis Sonder ex Kützing and Gracilaria mammillaris (Montagne) Howe. Bot. Mar., 35(.), 77-81 (1992).
24. L Hayashi, C Bulboa, P Kradolfer, G Soriano, D Robledo. Cultivation of red seaweeds: a Latin American perspective. J. Appl. Phycol., 26(2), 719–727 (2013).
25. J Rodríguez, C Rodríguez, L Molins, M Nuñez, M Colmenares. Comunidad bentónica asociada a una plataforma rocosa en el Cabo San Román Edo. Falcón. IV Congreso de investigación so- bre la Investigación en el siglo XXI: Oportunidades y retos (2007). Disponible en: http://facyt.uc.edu.ve/sites/default/ fi- les/Paraguana%20Gregorio_0.pdf
26. R. Meena, K Prasad, M Ganesan, AK Siddhanta. Superior quality agar from Gracilaria species (Gracilariales, Rhodophyta) collected from the Gulf of Mannar, India. J. Appl. Phycol., 20(4), 397–402 (2008).
27. N Bechara, R Betancourt. Efecto del tratamiento alcalino en el proceso de extracción solido-liquido del agar-agar de algas agarofitas. Trabajo de grado no publicado. Universidad Nacional Experimental “Francisco de Miranda”. Coro-Falcón, Venezuela (2001).
28. Association of Official Agricultural Chemists [AOAC]. Official methods of analysis (18th Ed.). Arlington,Virginia: AOAC (2005).
29. J Orduña-Rojas, R Suárez-Castro, E López-Álvarez, R Riosmena-Rodríguez, I Pacheco-Ruiz, J Zertuche-González, A Meling- López. Influence of alkali treatment on agar from Gracilariopsis longissima and Gracilaria vermiculophylla from the Gulf of California, México. Cienc. Mar. 34(4), 503-511 (2008).
30. JG Wakibia, RJ Anderson, DW Keats. Growth rates and agar properties of three Gracilarioids in suspended open-water cultivation in St. Helena Bay, South Africa. J. Appl. Phycol., 13(3), 195–207 (2001).
31. J Lekshmi. Difference in agar content of major agarophytes from coast of Kerala. Trends in Biosciences, 11(.), 1507-1510 (2018).
32. KT Bird, TK Hinson. Seasonal variations in agar yields and quality from North Carolina agarophytes. Bot. Mar., 35(4), 291– 295 (1992).
33. J Espinoza-Avalos, E Hernández-Garibay, JA Zertuche- González, ME Meave. Agar from two coexisting species of Gracilaria (Gracilariaceae) from the Mexican Caribbean. Cienc. Mar., 29(2), 211–228 (2003).
34. N Montaño, R Villanueva, J Romero. Chemical characteristics and gelling properties of agar from tow Philippine Gracilaria spp. (Gracilariales, Rhodophyta). J. Appl. Phycol., 11, 27-34 (1999).
Notas de autor
mquintero05@gmail.com
Información adicional
Citar como:: M Quintero, JR Martínez, C Maldonado, J Leañez, D Duno. Efecto de los tratamientos alcalino y de oscuridad-salinidad en agar de Gracilaria domingensis. Avances en Química, 15(2), 35-40 (2020).