Artículos científicos
Preparación del compuesto Beta/MCM-41: un material con una isoterma de adsorción-desorción poco convencional (†)
Preparación del compuesto Beta/MCM-41: un material con una isoterma de adsorción-desorción poco convencional (†)
Avances en Química, vol. 15, núm. 2, pp. 41-47, 2020
Universidad de los Andes

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial 4.0 Internacional.
Recepción: 30 Abril 2020
Aprobación: 29 Julio 2020
Resumen: Se reporta la preparación de un material micro/mesoporoso Beta/MCM-41 mediante la recristalización de zeolita Beta en medio alcalino. El material es caracterizado por Difracción de Rayos X en polvo (DRX), espectroscopia infrarroja con transformada de Fourier (IR-TF), Microscopía Electrónica de Barrido (MEB) y fisisorción de nitrógeno. Los resultados de DRX corroboran la presencia de la zeolita Beta y del material MCM-41. La isoterma de adsorción-desorción de N2 del material muestra un comportamiento no convencional que hace sugerir la presencia de un sistema estructurado y jerarquizado en el que coexisten las fases, micro y mesoporosa.
Palabras clave: Beta, MCM-41, isoterma de adsorción-desorción, método de recristalización.
Abstract: The preparation of a micro/mesoporous Beta/MCM-41 material by recrystallization of Beta zeolite in an alkaline medium is reported. The material is characterized by X-Ray Powder Diffraction (XRPD), Fourier Transformed Infrared spectroscopy (FT-IR), Scanning Electron Microscopy (SEM) and nitrogen physisorption. XRPD results corroborate the presence of the Beta zeolite and the MCM-41 material. Nitrogen adsorption-desorption isotherm showed a non-conventional behavior suggesting the presence of a structured and hierarchical system in which the micro- and mesoporous phase coexist.
Keywords: Beta, MCM-41, adsorption-desorption isotherm, recrystallization method.
Introducción
Durante los últimos años, el enfoque de diversos grupos de investigación en el diseño y la preparación de materiales con múltiples niveles de porosidad se ha incrementado debido a sus potenciales aplicaciones1,2,3,4,5,6,7. Uno de estos sistemas, que incluye la participación de fragmentos zeolíticos y de materiales mesoporosos ordenados ha dado lugar a los compuestos micro/mesoporosos, los cuales han demostrado una mayor eficiencia en transformaciones catalíticas de moléculas voluminosas al compararse con los materiales microporosos individuales de partida8,9,10,11,12,13,14.
Es bien conocido que los materiales porosos pueden ser descritos de acuerdo a sus propiedades de adsorción15,16. La relación entre la porosidad y la adsorción de un material viene dada por el tamaño del poro y la clasificación de la isoterma obtenida, de acuerdo a las convenciones de la IU- PAC de 198517. En este contexto, el comportamiento del mecanismo de adsorción y desorción asociado a los materiales microporosos y mesoporosos es característico de isotermas tipo I y tipo IV, respectivamente18. Por lo tanto, es de esperar que el análisis por fisisorción de N. en materiales compuestos micro/mesoporosos adquiera comportamientos de ambos tipos de materiales.
Dentro de estos compuestos micro/mesoporosos se han reportado diversos trabajos de síntesis con contribución variable de zeolita Beta, uno de los catalizadores heterogéneos más importantes a nivel industrial19y de MCM-41, un material cuya estructura forma poros hexagonales y unidireccionales siendo el más representativo de la familia M41S20. Consecuente con ello, se exponen algunos reportes sobre la preparación de compuestos del tipo Beta/MCM-41, haciendo énfasis en sus análisis texturales. En 2001, Guo y col.21prepararon materiales Beta/MCM-41 a través de un proceso de cristalización en dos etapas. Los autores indicaron que los datos de porosidad sugieren que los compuestos contienen sistemas bimodales de estructuras mesoporosas y microporosas de zeolita beta. Años más tarde, Ooi y col.22usaron el método de cristalización en dos etapas para la preparación de materiales Beta/MCM-41 y lo compararon con el método de siembra. Los autores informaron que los materiales obtenidos por el método de siembra muestran un mayor aumento en el proceso de adsorción para valores de P/P. = 0,3-0,4, asociándolo con la presencia de un tamiz molecular mesoporoso. Además, indicaron un sistema de poros no uniforme, porque la isoterma mostró una histéresis de tipo B23. Otra metodología, que implicó la disolución de la zeolita Beta en medio alcalino seguida de su recristalización, para sintetizar compuestos micro/mesoporosos fue aplicada por Ordonsky y col.24Una de las muestras recristalizadas mostró una isoterma con un aumento agudo a un valor de presión relativa de 0,35, relacionado con la presencia de me-oporos uniformes. El ciclo de histéresis (P/P. = 0,45) sugiere la existencia de mesoporos texturales secundarios. Posteriormente, Xu y col.25sintetizaron materiales compuestos Beta/MCM-41 a través del ensamble de nano-agregados de zeolita Beta y su posterior hidrólisis en presencia del surfactante correspondiente, en condiciones estáticas y de agitación. Todos los materiales compuestos mostraron isotermas de tipo IV con una etapa aguda de condensación de nitrógeno a una presión relativa entre 0,3 a 0,4. Por último, Scherban y col.26obtuvieron unos materiales micro/mesoporosos parcialmente zeolitizados, usando una plantilla micelar con precursores de zeolita Beta. Estos autores informaron que un grupo de mues- tras presentaban isotermas de adsorción con un aumento entre 0,40 y 0,45 de P/P., lo cual indica presencia de poros más grandes que los característicos para el material MCM-41.
En este trabajo se presenta la preparación de un material compuesto micro/mesoporoso (Beta/MCM-41) empleando zeolita Beta como material de partida a través del método de recristalización en medio alcalino, seguido de un tratamiento en presencia de bromuro de cetiltrimetilamonio (CTAB) como Agente Director de Estructura (ADE). El material preparado y modificado se caracteriza por un conjunto de técnicas dando especial atención al análisis textural, debido a su comporta- miento no convencional.
Metodología
Síntesis de la zeolita Beta
La síntesis de la zeolita Beta se llevó a cabo de acuerdo a la metodología encontrada en un trabajo previamente reportado por nuestro grupo de investigación27. Luego, la zeolita sintetizada, denominada Beta, se calcinó en modo estático desde temperatura ambiente con una rampa de calentamiento de 2°C/min hasta 500 °C por 18 h. Posteriormente, se realizó un proceso de calcinación adicional, con flujo de O. (60 mL/min), desde temperatura ambiente con un aumento gradual 2 °C/min hasta 500 °C por 8 h y se enfrió a temperatura ambiente. El sólido obtenido se intercambió con una solución acuosa de NH.NO. 1,5 M por 6 h, se filtró, se lavó con agua y se secó a 80 °C. El proceso de intercambio se repitió. Por último, el sólido se calcinó en modo dinámico (flujo de N.=60 mL/min) desde temperatura ambiente con una rampa de calentamiento de 2 °C/min hasta 500 °C por 10 h y se enfrió a temperatura ambiente. Este proceso de calcinación final modificó el sólido a su forma ácida, el cual se denotó como H-Beta.
Síntesis del compuesto Beta/MCM-41
El compuesto Beta/MCM-41 se preparó por tratamiento alcalino de la zeolita H-Beta en presencia de una solución acuosa de bromuro de cetiltrimetilamonio (CTAB, Merck, 98%), de acuerdo a la metodología propuesta por Ivanova y Knyaseva28. Se suspendió la zeolita H-Beta en una solución acuosa de hidróxido de sodio (NaOH, Baker, 99%) y se agitó lentamente por 3 h. Luego, se añadió CTAB y se continuó la agitación por 1,5 h. La suspensión resultante, que poseía las siguientes relaciones másicas: H-Beta/NaOH = 2,5000, H-Beta/H2O = 0,0600 y H-Beta/CTAB = 0,5377, fue introducida en un reactor de teflón con camisa de acero inoxidable y se mantuvo isotérmicamente a 110 °C por 24 h. El reactor se enfrío hasta temperatura ambiente y se añadieron 12 g de agua a la suspensión, además se reguló el pH a 10,3 con adición gota a gota de H2SO4 (Erba, 98 % m/m). Finalmente, la mezcla resultante se trató hidrotermalmente a 110 °C por 48 h en el mismo reactor, limpio y seco. El sólido se filtró, se lavó con agua hasta que los lavados alcanzaron un pH neutro y se secó a 80 °C durante la noche, obteniéndose el material sintetizado que se denominó Beta/MCM-41. Los procedimientos para la transformación del producto sintetizado a su forma ácida son los mismos que los descritos en el apartado anterior. En este caso, el material final obtenido se denotó como H-Beta/MCM-41. Adicionalmente, se preparó una mezcla mecánica, denotada como MM, con iguales proporciones másicas de H-Beta y de MCM-41. El material MCM-41 fue preparado de acuerdo al protocolo seguido por Rodríguez y col.29
Caracterización
Los patrones de Difracción de Rayos X en polvo de los materiales sintetizados fueron registrados en un difractometro Siemens D5005 con geometría Bragg-Brentano, equipado con radiación CuKα (λ=1,5418 Å) operando a 40 kV y 30 mA. Los espectros infrarrojo se registraron en un espectrofotómetro Perkin Elmer con transformada de Fourier, modelo Frontier, en un rango de número de onda de 4000-400 cm-1. Las micrografias de los materiales sintetizados fueron registradas en un microscopio electrónico de barrido Hitachi modelo S2500. Las muestras fueron recubiertas con una capa delgada de oro a fin de hacerlas conductoras y mejorar su brillo y contraste. El voltage de aceleración empleado fue de 10 kV. La adsorción-desorción de N2a -196 °C se realizó en un sortómetro Micromeritics TriStar II Series. Las muestras fueron pre-tratadas a 350 °C por 3 h bajo un vacío de 10-3 torr. Los modelos BET30 y t-plot31 fueron aplicados para calcular los parámetros texturales y el modelo BJH32 para determinar la distribución del tamaño de poros.
Discusión de resultados
En la figura 1 se muestran los patrones de difracción de las muestras Beta y Beta/MCM-41. Se observa una disminución en la intensidad del conjunto de picos de difracción a ángulos convencionales para el compuesto Beta/MCM-41, lo cual se puede asociar con la disolución parcial de fragmentos zeolíticos en el tratamiento alcalino e hidrotermal durante su preparación. Además, se observan cuatro líneas de difracción en Beta/MCM-41 que están ausentes en la zeolita Beta, lo cual sugiere la formación de un material meso-estructurado. Estos picos de difracción están relacionados con los del reporte PDF 00-049-1712 del material MCM-41, a través de los planos de difracción y de las distancias interplanares siguientes: (100) = 42,2 Å, (110) = 24,5 Å, (200) = 21,3 Å y (210) = 16,1 Å20,33.
Por otro lado, existe una correlación en la posición de los picos de difracción de la muestra Beta con el reporte PDF 00- 056-0467, relacionado con la preparación de la zeolita Beta desarrollada por Caullet y col.34De acuerdo a la intensidad de las líneas de difracción, se puede inferir una proporción mesoporosa predominante en la muestra Beta/MCM-41.
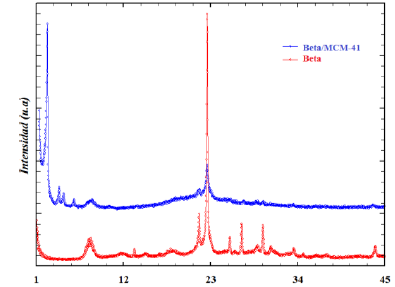
Fig. 1
Patrones de difracción de las muestras sintetizadas Beta y Beta/MCM-41.
En la tabla 1 se muestra la asignación de las vibraciones de las muestras H-Beta y H-Beta/MCM-41 que se encuentran en el espectro infrarrojo (Fig. 2). Se hace evidente la similitud para la mayoría de las bandas en ambas muestras. La presencia de agua adsorbida en los materiales se corrobora por los modos vibracionales de tensión (A) y de deformación (B) del enlace O-H, respectivamente. La principal diferencia entre los espectros IR-TF es la banda de deformación del enlace T-O de los tetraedros internos, es decir, la banda H. Se propone que el tratamiento alcalino modifica dicha banda por disolución de las unidades de construcción primarias del entramado zeolítico. Ambas muestras exhiben el modo de tensión asimétrica T- O-T (C), lo cual confirma la presencia de unidades de construcción tetraédricas, las cuales conforman a materiales zeolíticos y/o meso-estructurados. Esta misma banda (señal C) se encuentra desplazada hacia un valor más bajo de número de onda en la muestra H-Beta/MCM-41, lo cual podría indicar la desilicación de la zeolita Beta durante el tratamiento de síntesis para la formación del material compuesto35,36.
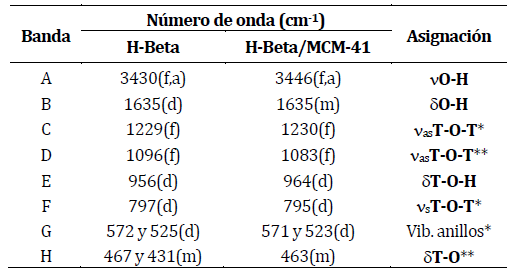
n = tensión, d = deformación, as = asimétrica, s = simétrica, T = Si o Al, f = fuerte, d = débil, m = mediana, a =a ncha.
(*) Enlaces externos entre tetraedros TO4(**) Vibraciones internas entre tetraedros TO4.
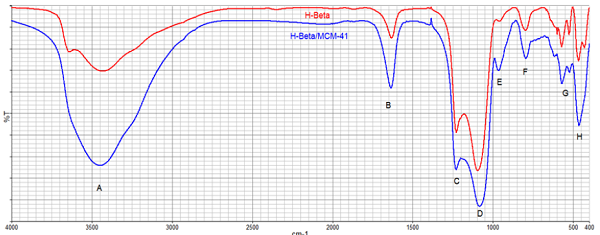
Fig. 2
Espectros IR-TF de las muestras acídicas H-Beta y H-Beta/MCM-41.
Las micrografías electrónicas de barrido del compuesto H- Beta/MCM-41 se muestran en la figura 3(a-d). Las micrografías se tomaron a diferentes escalas con la intención de conocer los diferentes tamaños y morfologías de las partículas correspondientes al material compuesto. En estas se puede apreciar una serie de agregados en forma de corales [Fig. 3(a-b)], compuestos por otras partículas más pequeñas [Fig. 3(c-d)], cuyo tamaño promedio es de 0,5 µm. La morfología de dichas partículas da cuenta de cubos y también se pueden apreciar partículas con forma de esferas ovaladas, tal como se encuentra reportado en la literatura para la zeolita Beta37,38. En la figura 3(e) se muestra la micrografía del material sintético de partida (H-Beta), corroborando la morfología descrita anteriormente. En este caso, las partículas de H-Beta presentan un tamaño promedio de 0,4 µm. La micrografía mostrada en la figura 3(f) corresponde al material mesoporoso cristalino (MCM-41), sintetizado en el laboratorio, y se puede observar que la morfología de este material consiste de partículas esféricas con tamaños promedios de 2,0 µm. La comparación morfológica de H-BEA/MCM-41 con los materiales BEA y MCM-41, podría sugerir que el material hibrido tiene características morfológicas que pueden coincidir con las halladas para los materiales en su forma separada.
En la figura 4(a-c) se muestran las isotermas de adsorcióndesorción de las muestras H-Beta, H-Beta/MCM-41 y de la mezcla mecánica MM. La isoterma de la muestra H-Beta es de tipo IV con un ciclo de histéresis H439. El ciclo de histéresis hace sugerir la presencia de mesoporosidad intercristalina, la cual se confirma por la distribución del tamaño de poros (Fig. 4d). García40reporta que algunos materiales zeolíticos presentan ciclo de histéresis en su isoterma, mientras que Camblor y col.41indican que la presencia de histéresis está directamente relacionada con la desaluminación generada por tratamientos de calcinación oxidantes. El proceso de adsorción del material H-Beta/MCM-41 (Fig. 4b) está caracterizado por la presencia de tres cambios de pendientes a 0,05, a 0,23 y a 0,83 en el eje de P/Po. El primer cambio está asociado con el llenado de los microporos y los cambios posteriores, a meso- poros de diferentes tamaños. Esto se respalda por los resultados obtenidos de la distribución del tamaño de poros, lo cual indica una repartición de mesoporos con tamaños desde 100 hasta 200 Å, pudiéndose asociar a fracciones minoritarias de óxido de silicio y de aluminio, de tipo aluminosilicatos amorfos, obtenidos como producto del tratamiento alcalino al que se somete la zeolita Beta.
Las otras contribuciones para las distribuciones más estrechas se observan con tamaños aproximados a 25 y a 40 Å, los cuales se pudieran asociar con mesoporos intercristalinos formados por la interacción de fragmentos zeolíticos y/o mesoporos propios del material MCM-41. Por otra parte, la isoterma de la muestra MM presenta un comportamiento tipo IV, característico de un rango estrecho de mesoporos uniformes (P/P. = 0,35)

Fig. 3
Micrografías electrónicas de barrido (a-d) del compuesto H- Beta/MCM-41, (e) de H-Beta y (f) de MCM-41. El voltaje de acele- ración de la micrografía 3(f) corresponde a 20 kV.
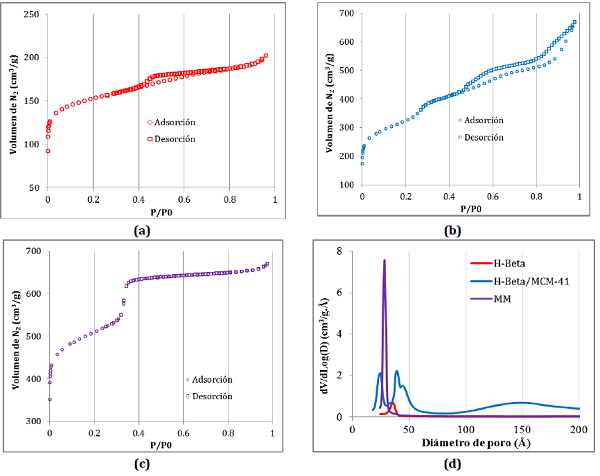
fig. 4
Isotermas de adsorción-desorción de N2 de las muestras (a) H-Beta, (b) H-Beta/MCM-4, (c) MM, y (d) la distribución de los tamaños de poros de las muestras H-Beta, H-Beta/MCM-41 y MM.
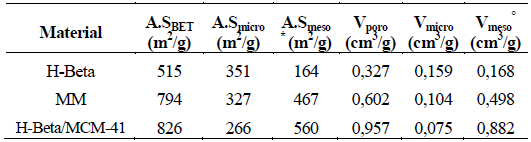
A.S = Área superficial específica, V= volumen,
* Smeso = SBET-Smicro, Vmeso° = Vporo-VmicroEs muy evidente la diferenciación entre las isotermas y la distribución del tamaño de poros del material compuesto y de la mezcla mecánica. De igual forma, en la tabla 2 se muestran los parámetros texturales de las muestras H-Beta, H-Beta/ MCM-41 y MM. Se observa que la muestra H-Beta/MCM- 41, cuyo patrón de DRX en polvo confirma la presencia de MCM-41, presenta los valores más altos de área superficial BET, de volumen de microporo y de mesoporo, así como también los valores más bajos de los parámetros microporosos. Esto puede explicarse a partir del hecho de que el tratamiento sintético disuelve una fracción importante del material zeolítico y lo transforma en fase mesoporosa.
Conclusiones
El método de recristalización en medio alcalino de la zeolita Beta permitió sintetizar un material compuesto Beta/MCM- 41, cuyas fases, micro y mesoporosa, fueron determinadas por DRX, IR-TF y MEB. El proceso de adsorción-desorción de N. del material compuesto en forma acídica genera una iso-terma con un comportamiento no convencional. El compuesto H-Beta/MCM-41 exhibió mayores valores en los parámetros texturales de área superficial y volumen de poro, así como una marcada diferencia en la distribución del tamaño de poros con respecto a las muestras H-Beta y MM.
Agradecimientos
Los autores agradecen el financiamiento por parte del CDCHT-ULA por el proyecto C-2005-18-08-C y al Laboratorio Nacional de Di- fracción de Rayos X de la Facultad de Ciencias de la Universidad de Los Andes por su proyecto N° LAB-97000821 que permitió el registro de los patrones de difracción. Además, J.C-Z expresa un agradecimiento especial, a su Padre Emmanuel Jesús, por todo el amor y las bendiciones recibidas en cada día de su vida.
Referencias
1. ME Davis. Ordered porous materials for emerging applications. Nature, 417, 813-821 (2002).
2. C Sanchez, G Soler-Illia, F Ribot, D Grosso. Design of functional nano-structured materials through the use of controlled hybrid organic–inorganic interfaces. Comptes Rendus Chimie, 6, 1131-1151 (2003).
3. F Fajula, A Galarneau, F Di Renzo. Advanced porous materials: New developments and emerging trends. Microporous Mesoporous Mater., 82, 227-239 (2005).
4. M Coppens, J Sun, T Maschmeyer. Synthesis of hierarchical porous silicas with a controlled pore size distribution at various length scales. Catal. Today, 69, 331-335 (2001).
5. Y Lee, JS Lee, YS Park, KB Yong. Synthesis of large monolithic zeolite foams with variable macropore architectures. Adv. Mater., 13, 1259-1263 (2001).
6. D Kuang, T Brezesinski, B Smarsly. Hierarchical porous silica materials with a trimodal pore system using surfactant templates. J. Am. Chem. Soc., 126, 10534-10535 (2004).
7. T Sen, GJT Tiddy, JL Casci, MW Anderson. Synthesis and characterization of hierarchically ordered porous silica materials. Chem. Mater., 16, 2044-2054 (2004).
8. JC Groen, LA Peffer, JA Moulijn, J Pérez-Ramírez. On the introduction of intracrystalline mesoporosity in zeolites upon desilication in alkaline medium. Microporous Mesoporous Mater., 69, 29–34 (2004).
9. J Čejka, S Mintova. Perspectives of Micro/Mesoporous Composites in Catalysis. Catal. Rev., 49, 457–509 (2007).
10. J Vernimmen, V Meynen, P Cool. Synthesis and catalytic applications of combined zeolitic/mesoporous materials. Beilstein J. Nanotechnol., 2, 785–801 (2011).
11. S López-Orozco, A Inayat, A Schwab, T Selvam, W Schwieger. Zeolitic materials with hierarchical porous structures. Adv. Ma- ter., 23, 2602–2615 (2011).
12. DP Serrano, JM Escola, P Pizarro. Synthesis strategies in the search for hierarchical zeolites. Chem. Soc. Rev., 42, 4004-4035 (2013).
13. K Li, J Valla, J García-Martínez. Realizing the commercial po- tential of hierarchical zeolites: New opportunities in catalytic cracking. ChemCatChem, 6, 46-66 (2013).
14. X Vu, U Armbruster, A Martin. Micro/mesoporous zeolitic composites: Recent developments in synthesis and catalytic applications. Catalysts, 6, 1-23 (2016).
15. Z Alothman. A review: Fundamental aspects of silicate meso- porous materials. Materials, 5, 2874-2902 (2012).
16. S Brunauer, L Deming, W Deming, E Teller. On a theory of the van der waals adsorption of gases. J. Am. Chem. Soc., 62, 1723- 1732 (1940).
17. K Sing, D Everett, R Haul, L Moscou, R. Pierotti, J Rouquerol, T Siemieniewska. Reporting physisorption data for gas/solid systems with special reference to the determination of surface area and porosity. Pure Appl. Chem., 57(4), 603-619 (1985).
18. S Lowell, J Shields, M Thomas, M Thommes. Characterization of porous solids and powders: Surface area, pore size and density. Springer, Países Bajos (2004).
19. R Martínez-Franco, C Paris, ME Martínez-Armero, C Martínez, M Moliner, A Corma. High-silica nanocrystalline Beta zeolites: Efficient synthesis and catalytic application. Chem. Sci., 7, 102- 108 (2016).
20. V Meynen, P Cool, EF Vansant. Verified syntheses of mesoporous materials. Microporous Mesoporous Mater., 125, 170-223 (2009).
21. W Guo, C Xiong, L Huang, Q Li. Synthesis and characterization of composite molecular sieves comprising zeolite Beta with MCM-41 structures. J. Mater. Chem., 11, 1886–1890 (2001).
22. Y Ooi, R Zakaria, A Mohamed, S Bhatia. Synthesis of composite material MCM-41/Beta and its catalytic performance in waste used palm oil cracking. Appl. Catal. A-Gen., 274, 15–23 (2004).
23. J Thomas, W Thomas. Principles and practice of heterogeneous catalysis. VCH, Alemania (1997).
24. V Ordomsky, V Murzin, Y Monakhova, Y Zubavichus, E Knyazeva, N Nesterenko, I Ivanova. Nature, strength and accessibility of acid sites in micro/mesoporous catalysts obtained by recrystallization of zeolite BEA. Microporous Mesoporous Mater., 105, 101–110 (2007).
25. H Xu, J Guan, S Wu, Q Kan. Synthesis of Beta/MCM-41 composite molecular sieve with high hydrothermal stability in static and stirred condition. J. Colloid Interf. Sci., 329, 346–350 (2009).
26. N Shcherban, R Barakov, P Yaremov, V Solomakha, S Gryn, O Khaynakova, V Ilyin. Template synthesis, structure, sorption properties and acidity of micro-mesoporous materials obtained from sol-precursor of zeolite BEA. J Porous Mater., 21, 355- 363 (2014).
27. J Colmenares-Zerpa, P Rodríguez-Sulbarán, G Márquez, A Dugarte, JM Delgado, J Contreras, C Lugo, M Villarroel, H Del Castillo, F Imbert. Caracterización estructural mediante difracción de rayos X de polvo de la zeolita Beta. Av. Quím., 13, 45- 48 (2018).
28. I Ivanova, E Knyazeva. Micro–mesoporous materials obtained by zeolite recrystallization: synthesis, characterization and catalytic applications. Chem. Soc. Rev., 42, 3671-3688 (2013).
29. P Rodríguez, F Aguirre, E Sosa, E García, M Villarroel, Á Uzcategui, H Del Castillo, E Bastardo, F Imbert. Síntesis y caracterización de catalizadores mesoporosos del tipo MCM-41 y SBA-15 modificados con ácido tungstofosfórico. Rev. Soc. Quim. Perú, 75, 464-472 (2009).
30. S Brunauer, P Emmett, E Teller. Adsorption of Gases in Multimolecular Layers. J. Am. Chem. Soc., 60, 309-319 (1938).
31. R Lippens, J De Boer. Studies on pore systems in catalysis V. the. plot method. J. Catal., 4, 319-323 (1965).
32. EP Barrett, LG Joyner, PP Halenda. The determination of pore volume and area distributions in porous substances. I. Computa- tions from nitrogen isotherms. J. Am. Chem. Soc., 73, 373-380 (1951).
33. CT Kresge, ME Leonowicz, WJ Roth, JC Vartuli, JS Beck. Ordered mesoporous molecular sieves synthesized by a liquid- crystal template mechanism. Nature, 359, 710-712 (1992).
34. P Caullet, J Hazm, J Guth, J Joly, J Lynch, R Raatz. Synthesis of zeolite Beta from nonalkaline fluoride aqueous aluminosilicate gels. Zeolites, 12, 240-250 (1992).
35. W Chester, EG Derouane. Zeolite Characterization and Catalysis. Springer, EUA (2001).
36. SM Auerbach, KA Carrado, PK Dutta. Handbook of zeolite science and technology. Marcel Dekker Inc, EUA (2003).
37. M Camblor, J Pérez-Pariente. Crystallization of zeolite beta: Effect of Na and K ions. Zeolites, 11, (1991) 202-210.
38. M Quintero, M Pérez, H Meléndez, J Rondón, F Imbert. Síntesis y caracterización de la zeolita Beta. Av. Quim., 7, 223-226 (2012).
39. M Thommes, K Kaneko, A Neimark, J Olivier, F Rodríguez- Reinoso, J Rouquerol, K Sing. Physisorption of gases with special reference to the evaluation of surface area and pore size distribution (IUPAC Technical Report). Pure. Appl. Chem., 87, 1051-1069 (2015).
40. J García-Martínez, J Pérez-Pariente. Materiales Zeolíticos: síntesis, propiedades y aplicaciones. Publicaciones de la Universidad de Alicante, España (2003).
41. M Camblor, A Corma, S Valencia. Characterization of nanocrystalline zeolite Beta. Microporous Mesoporous Mater., 25, 59-74 (1998).
Notas
Notas de autor
jccolzer@gmail.com
Información adicional
Citar como: : J Colmenares-Zerpa, JM Delgado, J Contreras, A Balza, D Dávila, C Valero, P Rodríguez-Sulbarán. Preparación del compuesto Beta/MCM-41: un material con una isoterma de adsorción-desorción poco convencional. Avances en Química, 15(2), 41-47 (2020)