Investigación
Evaluación del Rendimiento de Extractos en Hojas de Ricinus communis L.
Evaluation of the Yield of Extracts in Leaves of Ricinus communis L.
Evaluación del Rendimiento de Extractos en Hojas de Ricinus communis L.
Conciencia Tecnológica, núm. 52, pp. 12-18, 2016
Instituto Tecnológico de Aguascalientes
Recepción: 21 Enero 2016
Aprobación: 20 Junio 2016
Resumen:
Se presenta un estudio para la extracción de hojas de Ricinus communis L., con solventes orgánicos (metanol, diclorometano y acetona) determinando el contenido de sólidos, rendimiento total y su viabilidad como repelente de insectos. Se encontró que los tratamientos con metanol (TM) y metanol con hidróxido de potasio (TMK) presentaron el mayor contenido en sólidos. Esto también se puede observar en la prueba estadística de medias, mostrando que el mejor rendimiento se dá en el extracto con metanol (TM) y metanol con hidróxido de potasio (TMK). El análisis de varianza confirmó que el tipo de solvente y el hidróxido de potasio (KOH) influyen significativamente en el contenido y rendimiento del extracto. En el sitio paraíso con sebos de tortilla los tratamientos con mayor tiempo de aceptación (DTA) fueron TDTB (diclorometano) y TMKTB (metanol con hidróxido de potasio). Por otro lado los tratamientos con mayor repelencia (DTR) fueron; TDKTB (diclorometano con hidróxido de potasio), TATB (acetona), TAKTB (acetona con hidróxido de potasio), TMTB (metanol), MADTB (mezcla de solventes) y MADKTB (mezcla de solventes con hidróxido de potasio). Con sebos de bagazo de naranja el mayor tiempo de aceptación (DTA) lo presenta el tratamiento MADKPB mientras que el resto de tratamientos TDPB, TDKPB, TAPB, TAKPB, TMPB, TMKPB y MADPB tuvieron mayor repelencia (DTR). En el sitio capulín, con sebo de tortilla y bagazo de caña se observó que todos los tratamientos presentaron alta repelencia (DTR).
Palabras clave: extractos orgánicos, hojas de Ricinus communis L., repelente de insectos.
Abstract: Presents a study for the extraction from leaves of Ricinus communis L., solvent-based organic (methanol, dichloromethane and acetone) determining the content of solids, total yield and viability as a repellent of insects. We found that treatment with methanol (TM) and methanol (TMK) potassium hydroxide showed the highest content in solid. This can also be seen in the statistical test averages, showing that the best performance is given in the extract with methanol (TM) and methanol (TMK) potassium hydroxide. Variance analysis confirmed that the type of solvent and the potassium hydroxide (KOH) significantly influence the content and performance of the extract. In place paradise with tallow of tortilla nest treatments with greater time of acceptance (DTA) were TDTB (dichloromethane) and TMKTB (methanol with potassium hydroxide). On the other hand greater repellency (DTR) treatments were; TDKTB (dichloromethane with potassium hydroxide), TATB (acetone), TAKTB (acetone with potassium hydroxide), TMTB (methanol), MADTB (mixture of solvents) and MADKTB (mixture of solvents with potassium hydroxide). With orange bagasse tallow as long accepted treatment MADKPB presented (DTA) while the rest of TDPB, TDKPB, TAPB, TAKPB, TMPB, TMKPB and MADPB treatments had greater repellency (DTR). In place capulin, with tortilla and bagasse tallow was observed in all treatments showed high repellency (DTR).
Keywords: organic extracts, leaves of Ricinus communis L., repellent insect.
Introducción
La extracción de compuestos activos mediante solventes orgánicos, que alteran o modifican el funcionamiento en animales e insectos, son y seguirán siendo una alternativa de aplicación [1]. Muchas especies vegetales poseen propiedades insecticidas o de repelencia [2]; entre ellas la familia de Euphorbiaceas, las cuales poseen alcaloides y proteínas de origen tóxico, localizados en las semillas, hojas y frutos [3]. Dicha toxicidad ha permitido que estos componentes sean importantes para el tratamiento de tumores, repelentes de insectos e inhibidores de crecimiento en larvas y microorganismos [4]. Un ejemplo es la ricinina, alcaloide encontrado en semillas y hojas de la especie Ricinus communis L. la cual es una planta arbustiva distribuida por todas las regiones templadas del mundo [5]. Respecto al alcaloide (ricinina), este contiene un grupo ciano en su estructura, lo cual le confiere su toxicidad; propiedad que sugiere su utilización como insecticida y/o repelente natural [6].
El objetivo de este trabajo fue determinar el contenido y rendimiento en sólidos, extraídos con tres diferentes solventes orgánicos (diclorometano, acetona y metanol y su mezcla en 33 %), con lo que se pretendió proponer un método de extracción óptimo en función del rendimiento en extracto y su eficacia de repelencia en la hormiga a partir de bioensayos en campo.
Fundamentos Teóricos
En las plantas, la formación de alcaloides es considerado como un proceso de protección a través de la síntesis de proteínas capaces de proveer nitrógeno, necesario para conformar núcleos de coenzimas y hormonas con diferente funcionalidad [7]; muchos de ellos son insolubles o poco solubles en agua formando sales con ácidos vegetales y minerales, como el ácido acético, láctico, clorhídrico y nítrico con estructuras moleculares complejas que manifiestan actividad farmacológica intensa, en animales y humanos, y que se encuentran normalmente en toda la planta [8-9].
Estudios realizados en hojas y semillas de Ricinus communis L. muestran los siguientes compuestos reactivos; el ácido gálico, gentísico, glicósido, flavonoide y quercitina, además de los triterpenos como el beta-amirina y lupeol. Además de los anteriormente mencionados, contiene N-dimetil-ricinina y ricina; las semillas contienen un triglicérido denominado ácido ricinoleico en alto porcentaje (90 %) [10-11-12-13].
Se ha reportado que el alcaloide ricinina (Fig. 1) y la toxoalbúmina ricina, presentan toxicidad muy alta para humanos, mamíferos e insectos (debido al grupo “Ciano” en sus estructuras, por lo que en los vegetales funciona como mecanismo de repelencia [14].
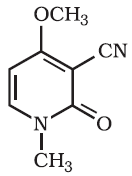
Figura 1
Estructura de la ricinina
Se ha reportado que en extracciones sometidas a percloración con etanol concentradas en rotavapor a 40°C y vacio; tienen una alta actividad tóxica a 860 ppm sobre larvas de Aedes Aegypti [15].
Por otro lado, se han extraído mediante maceración, semillas y hojas de Ricinus communis en agua (500 mL) y filtradas; encontraron que a una concentración del 15 % se produce actividad insecticida en gusano cogollero de maíz (Spodoptera frugiperda) [16]. También se ha obtenido repelencia con extracto acuoso de hojas de higuerilla con hojas de eucalipto, sobre hormiga obrera (Atta sexdens rubropilosa) [17, 18].
Por otro lado, extractos empleando hexano a temperatura ambiente (21°C) durante 48 h, acetona durante 24 h y metanol durante 48 h, a partir de plantas como Nicotiana rustica, Nicotiana tabacum, Solanum nigru y Calendula arvensis, reportan efectos significativos de toxicidad, inhibición y repelencia sobre larvas de coleópteras (Tribolium castaneum) [19].
En estudios realizados sobre hormiga negra común Acromyrmex lundi, y su respuesta a extractos cetónicos totales, obtenidos en Soxhlet y por cocimiento de hojas de Ricinus communis, Melia azedarach y Trichillia glauca, muestran que los extractos de Ricinus y Melia generaron mayor efecto repelente, independientemente del solvente de extracción utilizado; la Trichillia presentó la mayor toxicidad por que se sugiere como insecticida [20].
Es importante señalar que, con base en lo referenciado anteriormente, se adaptaron y aplicaron en este trabajo las condiciones del solvente, tiempo de maceración y gramos de muestra, dadas en los diferentes métodos de extracción, con lo cual pudiéramos lograr un procedimiento de extracción específico para este tipo de vegetal [21-22-23-24].
Materiales y Métodos
La colecta de hojas se realizó en el Campo Experimental Bosque Escuela ubicado en Cuxpala Jalisco. El corte de la hoja se realizó con tijeras de jardinería dejando 10 cm de tallo. Las hojas se dejaron secar durante 72 h a la sombra y temperatura ambiente.
Las hojas secas se molieron en un molino de martillos Retsch GmbH 5657 Type Skiwest Germany con criba # 1 (Fig. 2), determinando la humedad en el material molido de acuerdo al método Tappi 258 om-89, y se guardó en bolsas de polietileno para mantener la humedad.

Figura 2
Molienda de hojas secas
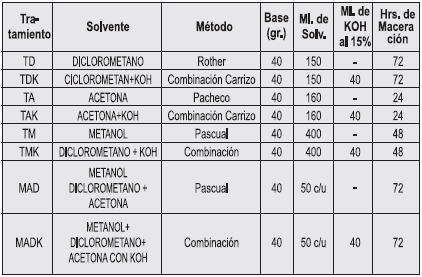
Posteriormente, se prepararon las muestras de hoja molida de acuerdo a cada tratamiento, con referencia a las condiciones de maceración dadas en la tabla de condiciones experimentales elaborada a partir de las referencias bibliográficas (Tabla 1).
Durante la maceración se aplicó agitación mecánica (Fig. 3); los tratamientos con 400 mL de solvente en placa de agitación magnética Thermoline nuova II a 60 rpm y los tratamientos con 50 a 160 mL con un agitador de propela Barnant Mixer S-20 a 150 rpm.

Figura 3
Maceración y extracción de la hoja
La filtración y separación de la fase sólida (Fig. 4) se realizó en un equipo Millipore modelo QTI 1 EA con papel Whatman No. 1. La fase líquida se filtró en membrana (0.45 micras) con bomba de vacío. Los filtrados de cada tratamiento se etiquetaron y colocaron en envases de vidrio color ámbar llevándose a refrigeración.

Figura 4
Filtración de extractos
La determinación cualitativa de alcaloides se realizó mediante cromatografía en columna, en 5 g de harina de hoja (desgrasada con hexano) con 7.5 mL de KOH al 25% y reposo de 3 h. Se molió en mortero junto con 4.5 g de tierra de diatomeas hasta obtener un polvo seco blanquecino. Se transfirió a una columna de 2cm de diámetro y 35cm de altura previamente empacada con 2cm de arena purificada y 5cm de tierra de diatomeas alcalinizada con KOH. Los alcaloides fueron eluidos de la columna con cantidades que fluctúan entre 150 - 200 mL de diclorometano, tomando una gota del filtrado sobre papel filtro. La presencia de alcaloides se puede confirmar al adicionar 4 gotas de reactivo Dragendorf (yoduro-potásico-bismútico), hasta cambio de café a rojizo.
De acuerdo a la bibliografía, los bioensayos se llevaron a cabo durante marzo y julio en el bosque La Primavera en el Estado de Jalisco; nido paraíso, cercano a un árbol de paraíso (Melía azedarach) [(20°34’54.75’’N) (103°37’57.98’’O)] elevación 1540 m.s.n.m., y nido capulín cercano a un árbol de capulín (Prunus serotina) [(20°46’23.99’’N) (103°36’25.22’’O)] elevación 1559 m.s.n.m. Se seleccionaron dos cebos distintos: bagazo de naranja exprimida de 0.7-0.9g y disco de tortilla de maíz cortada con sacabocado de 4.5mm de diámetro y 0.8–0.9 g, ambos se secaron a temperatura ambiente, con un contenido de humedad entre 25 a 30% [25].
Los sebos se remojaron durante 15 min en cada extracto de cada tratamiento, colocado el bastidor metálico de 56.5cm de diámetro sobre el orifico de entrada del hormiguero; los sebos se ubicaron de acuerdo al cuadrante del bastidor (Fig. 5) y se monitorearon en un horario de 7:00 a 10:00 am en el nido paraíso y de 11:00 a 14:30 pm en el nido capulín [26].

Figura 5
Bastidor para la ubicación de los sebos
Resultados y Discusión
En la Tabla 2 se puede observar que los tratamientos con metanol TM (18.45 %) y metanol e hidróxido de potasio TMK (22.82 %), presentaron el mayor contenido en sólidos y rendimiento en %.

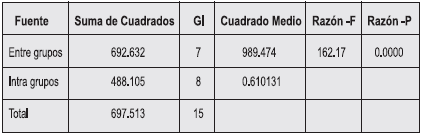
El análisis de varianza (Anova) de acuerdo a una hipótesis nula (P>0.5) nos indicaría que no existen diferencias significativas en el rendimiento de los extractos, por otro lado, para una hipótesis alternativa (P<0.5) como es en este caso (Tabla 3) nos indica que al menos uno de los grupos tiene diferencias significativas (medias diferentes), por lo tanto, la influencia del KOH en el rendimiento (%) es significativa.
La prueba de medias (Fig. 6), muestran que el rendimiento más alto se da en el extracto con metanol (18.45%) y metanol con hidróxido de potasio (22.82%).
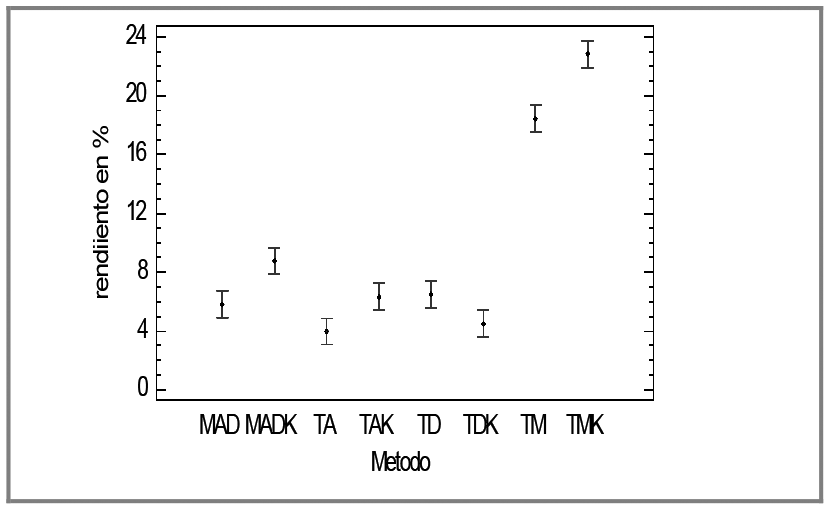
Figura 6
Prueba de Medias
La evaluación de los bioensayos con respecto a las variables DTA (tiempo de aceptación) y DTR (tiempo de repelencia), se pueden observar en las Figuras 7 al 10. Para nido paraíso las claves de los extractos con sebos de tortilla de maíz, fueron; TDTB, TDKTB, TATB, TAKTB, TMTB, TMKTB, MADTB, MADKTB y TESTB. Para el sebo de bagazo de naranja se sustituyó TB por PB. Para nido capulín las claves de los extractos con tortilla de maíz, se cambiaron las dos últimas letras TB por TC, y para el bagazo de naranja se cambio PB por PC.
En el nido paraíso con sebos de tortilla (Figura 7) se muestra que los tratamientos con mayor tiempo de aceptación fueron TDTB y TMKTB, es decir, las hormigas lo transportaron, lo metieron a su nido y al término de 25 a 28 min lo sacaron. El sebo con agua (TESTA) lo aceptaron durante más tiempo (90 a 105 min), aumentando el tiempo de aceptación hasta en 350 % con respecto a los tratamientos TDTB y TMKTB. Contrariamente al efecto de aceptación, los tratamientos con mayor repelencia (DTR) fueron; TDKTB, TATB, TAKTB, TMTB, MADTB y MADKTB (0 a 2 minutos).

Figura 7
Efecto del tiempo de aceptación y repelencia para cada tratamiento.
Para el caso del nido paraíso con sebos de bagazo de naranja (Figura 8) se muestra que el mayor tiempo de aceptación lo presenta el tratamiento MADKPB (28 minutos) y el resto de tratamientos TDPB, TDKPB, TAPB, TAKPB, TMPB, TMKPB y MADPB tuvieron menor tiempo de aceptación (0 a 2 min) es decir, al contacto con el sebo se presentó el rechazo o repelencia.
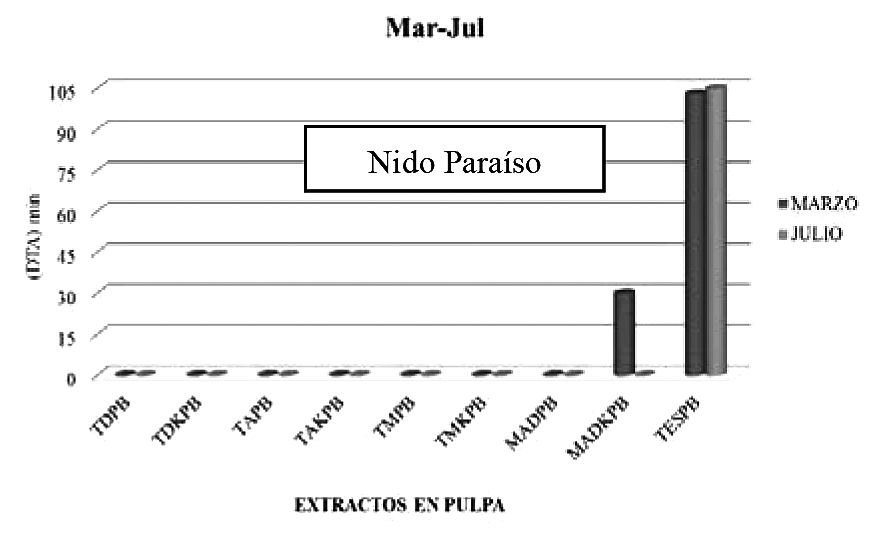
Figura 8
Efecto del tiempo de aceptación y repelencia para cada tratamiento.
Respecto al nido capulín con sebo de tortilla y bagazo de caña presentados en las Figuras 9 y 10, se observó que ningún extracto fue aceptado, es decir presentaron mayor repelencia (menor aceptación).
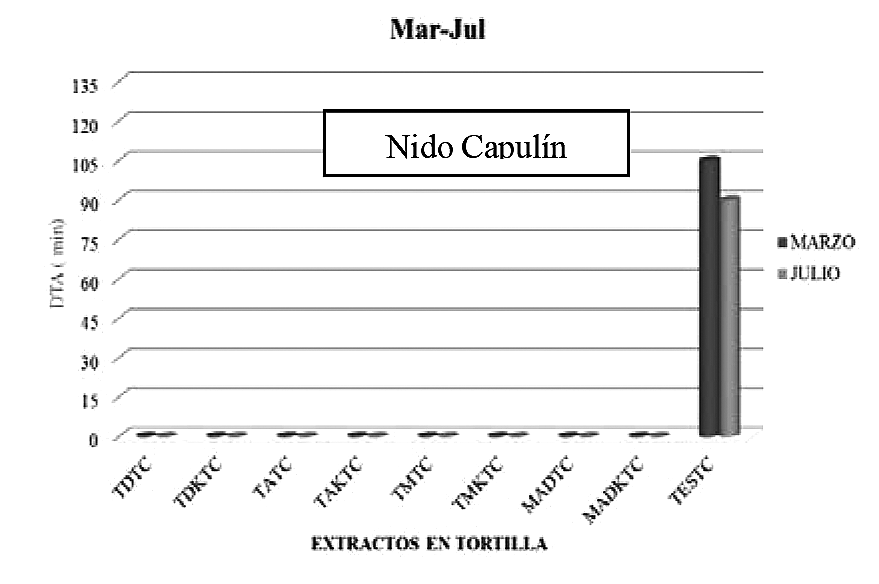
Figura 9
Efecto del tiempo de aceptación y repelencia para cada tratamiento.
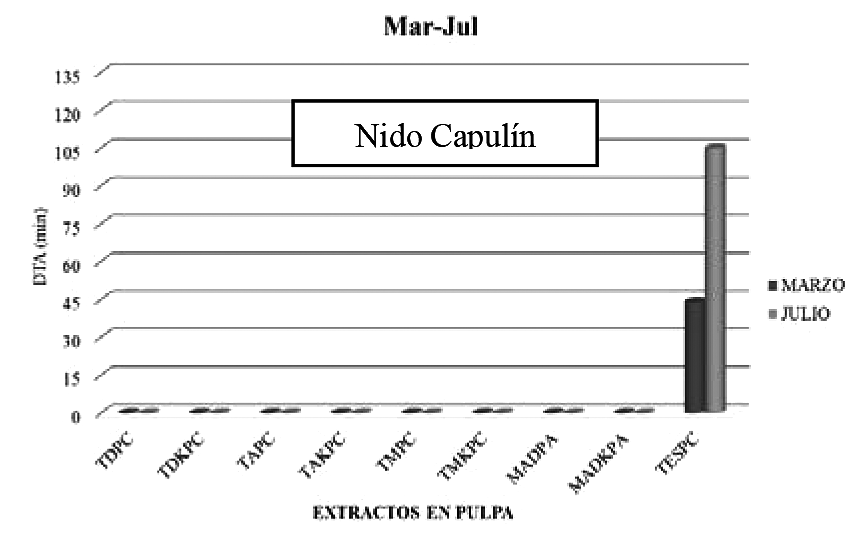
Figura 10
Efecto del tiempo de aceptación y repelencia para cada tratamiento.
Conclusiones
De acuerdo a lo expuesto anteriormente, se concluye que el mayor rendimiento en sólidos se encontró en los tratamientos con metanol y metanol con KOH, además, presentaron menos pérdidas por evaporación durante la operación de maceración y filtrado, aunque también fueron los que tuvieron mayor volumen de solvente (400 ml) y un tiempo de maceración (48 horas). El KOH influyó significativamente en el rendimiento del extracto con metanol. Se recomienda su uso en función de la afinidad de los compuestos a extraer y en un rango de aplicación del 5 al 10 % en peso.
Los tratamientos TAK y presentaron mayores tiempos de filtración (30 a 90%) con respecto a los otros tratamientos.
Respecto a DTA en nido paraíso y nido capulín, los extractos con mayor tiempo de aceptación (25 a 28 min) fueron; TDTB, TMKTB y MADKPB.
Los extractos que presentaron mayor repelencia fueron: TDKTB, TATB, TAKTB, TMTB (metanol en sebo de tortilla), MADTB y MADKTB (mezcla de solventes sin y con hidróxido de potasio en sebo de tortilla). En el nido capulín ningún tratamiento presentó aceptación, es decir, todos presentaron alta repelencia.
Comparativamente con los extractos, los testigos con agua destilada en ambos sebos y nidos incrementaron hasta en un 350 % su aceptación.
Se sugiere estudiar los extractos con metanol con vista al aislamiento de los compuestos polares que tiene la hoja como son; clorofila, azúcares, flavonoides, terpenos, etcétera. Por otro lado, si se requiere un extracto con menor contenido de sólidos, la acetona o diclorometano son los indicados, pudiendo analizar y/o aislar azúcares, aminoácidos o glucósidos. Para la caracterización y concentración de la ricinina en hojas, se sugiere la cromatografía en contracorriente.
Referencias
[1] Celis B. C. (2006). Evaluación del efecto del extracto de alcaloides de Dendrobates truncatus (Anura: dendrobatidae) sobre unión neuromoscular de mamífero. Director: Gabriel Pascual Amaya. Pontificia Universidad Javeriana, Bogotá D. C., Departamento de Ciencias Fisiológicas.
[2] Jermy, T. (1990). Prospects of antifeedant approach to pest control”. A critical review. Journal of Chemical Ecology. 16(11), p. 3151-3166.
[3] Rivera, D. y Obon de Castro, C. (1991). La guía de incafo de las plantas útiles y venenosas de la península ibérica y baleares. Ed. Incafo (Instituto de la Caza Fotográfica y Ciencias de la Naturaleza). Vol. 7. Incafo, Madrid, p. 100.
[4] Jiménez, J. (1990). Una nueva sección y una especie nueva de Manihot (Euphorbiaceae) del estado de Guerrero. Acta Botánica. 60, p. 49-53.
[5] Arribere, María Cecilia y Caffini, N. Oscar. (1988). Enzimas Lipolíticas de Plantas Superiores. Lipasas de Semillas de Ricino. Acta Farmacéutica Bonaerense. 7(3), p. 215-223.
[6] Ramawat, KG., Rachnana, Sharma Suri, SS., Merillon, J.M. (2007). Secondary metabolites. Ed. Medicinal Plants in Biotechnology-Oxford and IBH, India, p. 66-367. ISBN 9781578084289
[7] Arango, A. G.J. (2002). Alcaloides y compuestos nitrogenados. Ed. Universidad de Antioquia, p. 88.
[8] Saxena, P.B. (2007) Chemistry of alkaloids. 1er. Edition, Discovery Publishing House, p. 338. ISBN 818356163
[9] American Chemical Society (1989). Chemical Abstracts. Ed. Universidad de Michigan, vol. 111, p. 350.
[10] Upasani, S.M., Kothar, H.M., Menki, P.S., Maheshwari, V. L. (2003). Partial characterization and insecticidal properties of Ricinus communis L foliageflavonoids. Pest Manag Sci. 59 (12), p. 1349-1354.
[11] Ferraz, A.C., Angelucci, M. E. M., Da costa, M. L., Batista, I. R., De oliveira, B. H. y Da cunha, C, (1999). Pharmacological Evaluation of Ricinine, a Central Nervous System Stimulant Isolated from Ricinus communis. Pharmacology Biochemistry and Behavior. 63(3), p. 367–375.
[12] Singh, P.P., Ambika, Chauhan S.M.S, (2009). Activity guided isolation of antioxidants from the leaves of Ricinus communis L. Food chemistry. 114(3), p. 1069 – 1072.
[13] Manpreet, Rana., Hitech, Dhamija., Bhajat, Prahar y Shivani, Sharma (2012). Ricinus communis L. A Review. International Journal of PharrmTech Research USA. 4, p. 1706-1711.
[14] Mazid, M.; Khan, T. A., Mohamad, F. (2001). Role of secondary metabolites in defense mechanisms of plants. Review Article Biology and Medicine. 3 (2), p. 232-249.
[15] Parra, G. J., García, P. M. C., Cotes, T.J.M, (2007). Actividad insecticida de extractos vegetales sobre Aedes aegypti (Diptera: Culicidae) vector del dengue en Colombia. Revista Médica. 21(1), p. 47-52.
[16] Ramos, L. M.A., Perez, G.S., Zavala, S. M. A., Rodríguez, H.. C. y Mahucu, G. (2007). Actividad de extractos acuosos de Ricinus communis y de Azadirachta indica contra Spodoptera frugiperda. Plantas Insecticidas. Memorias del XXV Congreso de Entomología y II Simposio Nacional sobre Sustancias Vegetales y Minerales en el Combate de Plagas. Oaxaca, México, p.112-119
[17] Woodruff, R. E. (1972). The coffee bean pest (Coleoptera: Anthribidae) . Florida Department of Agriculture and Consumer Services, Division of Plant Industry, Entomology. (3), p. 7-15.
[18] Silveira, C., Hebling, M. J. A., Rocha, W. C., Fernandes, J. R,. Pagnocca, F. C., Bueno, O. C., Racci, J.R, Vieira, P. y Silva, M. J. (2003). Toxicidade de duas especies do género ricinine para operarias de Atta sexdens ruprilosa (Hymenoptera: Formicidae). Anais do XVI Simposio de Mirmecología. Florianopolis. Sc. p. 118-121.
[19] Pelicano, A., Caffarini, P. Carrizo, P y Ferro, M. (2002). Eficiencia de sustancias de origen vegetal sobre hormigas cortadoras. XV Jornadas Fitosanitarias Argentinas. Rio Cuarto, Córdoba. p. 59-64.
[20] Pascual, M. J. (1998). Repelencia, inhibición del crecimiento y toxicidad de extractos vegetales, en larvas de Tribolium castaneum Herbst. (Coleoptera: Tenebrionidae). Boletín de Sanidad Vegetal. (24), p. 143-154.
[21] Bruneton, J. (2001). Farmacognosia, Fitoquímica. Plantas Medicinales. 2da Ed. Zaragoza: Acriba S.A. p. 1100.
[22] Caffarini, P., Carrizo, P., Pelicano, A., Roggero, P., Pacheco J. (2008). Efectos de extractos cetónicos y acuosos de Ricinus communis (ricino), Melia azedarach (paraíso) y Trichillia glauca (Trichillia), sobre la Hormiga Negra común (Acromyrmex lundi). Idesia, 26(1), p. 59-64.
[23] Pacheco, P. Rafael., Rodriguez H. Cesáreo., Lara, R. Joel., Montes B. Roberto., Ramirez, V. Gustavo. (2004). Toxicidad de aceites, esencias y extractos vegetales en larvas de mosquito culex Quinquefasciatus say (Diptera: Culicidae). Acta Zoologica Mexicana. 20(1), p. 141-152.
[24] Caffarini, P., Carrizo, P. y Pelicano, A. (2006). “Extractos cítricos como atrayentes para cebos hormiguicidas con sustancias naturales”. Revista Facultad de Ciencias Agrícolas UNCuyo., 38(1):19-26.
[25] Boaretto, M. A., Forti, L.C. (1997). “Perspectivas no controle de formigas cortadeiras”. Departamento de Defensa Fitosanitária de FCA/UNESP. Série técnica IPEF. 11(30), p. 31-46
[26] Fernández, F. E. D. (2003). Introducción a las hormigas de la región neotropical. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt, Bogotá, CO. XXVI. p. 398.
Notas
Notas de autor