Artículos
Recepción: 28 Noviembre 2020
Aprobación: 30 Mayo 2021
Resumen:
Una gran cantidad de reacciones que se llevan a cabo en la industria química, son exotérmicas, donde el control de la temperatura se logra por medio de la remoción de calor usando chaquetas o serpentines de enfriamiento internos. Sin embargo, puede ocurrir el descontrol térmico como consecuencia de la incapacidad para remover suficiente cantidad de calor en el sistema de reacción causando la explosión y liberación de grandes cantidades de gases tóxicos y/o inflamables en la atmósfera con consecuencias negativas para trabajadores o incluso habitantes cercanos en la zona. En este trabajo se aplicó un análisis cuantitativo de riesgos para cuantificar el riesgo del proceso bajo los diferentes escenarios generados. El análisis de riesgo está basado en modelos matemáticos que describen el proceso químico.
Se analiza el caso de estudio que consiste en un reactor semi-continuo en donde se produce la oxidación en ácido nítrico de 2-octanol para producir 2-octanona. El análisis de consecuencias tiene el objetivo de estimar el número de daños y fatalidades que ocurren en una población expuesta a sustancias tóxicas. La metodología aplicada en este trabajo permitió investigar el efecto de la desviación de una variable de proceso en el reactor sobre el riesgo de fatalidad, analizando tres diferentes escenarios.
Palabras clave: reactor, riesgo, descontrol térmico, simulación de procesos.
Abstract:
A large number of reactions carried out in the chemical industry are exothermic, where temperature control is achieved by means of the removal of heat using jackets or internal cooling coils. However, thermal runaway can occur as a result of the inability to remove sufficient amount of heat in the reaction system causing the explosion and release of large quantities of toxic and/or flammable gases in the atmosphere with negative consequences for workers or populations in the nearby area. In this work, a quantitative risk analysis was applied to quantify the risk of the process under the different scenarios generated. The risk analysis is based on mathematical models that describe the chemical process.
We analyze the case study that consists of a semi-continuous reactor where oxidation occurs in nitric acid of 2-octanol to produce 2-octanone. The analysis of consequences has the objective of estimating the number of damages and fatalities that occur in a population exposed to toxic substances. The methodology applied in this work made it possible to investigate the effect of the deviation of a process variable in the reactor over the risk of fatality, analyzing three different scenarios.
Keywords: reactor, risk, thermal runaway, process simulation.
Introducción
Una gran cantidad de reacciones en la industria de química fina, farmacéutica y síntesis orgánicas son exotérmicas, donde el control de la temperatura se logra por medio de la remoción de calor usando chaquetas o serpentines de enfriamiento internos. Sin embargo, puede ocurrir el descontrol térmico como consecuencia de la incapacidad para remover suficiente cantidad de calor en el sistema de reacción, lo cual puede suscitarse por diferentes fallas, entre ellas la del sistema de enfriamiento. Esta falla puede ocasionarse por: impurezas en los reactivos, disminución en el flujo del fluido refrigerante, disminución del área de intercambio de calor, temperatura de refrigeración demasiado alta o pérdida de agitación. Una falla en el sistema de refrigeración conduce a un aumento en la velocidad de reacción y un aumento en reacciones de descomposición no deseadas y por consecuente un aumento en la presión, debido a la formación de gases. Si la presión se eleva por encima de un valor crítico, el reactor puede explotar y liberar grandes cantidades de gases tóxicos y/o inflamables en la atmósfera con consecuencias negativas para trabajadores o incluso habitantes cercanos en la zona. La explosión del reactor puede generar además ondas de choque y proyección de fragmentos que pueden ocasionar a su vez daño en equipos aledaños y causar un efecto dominó.
El descontrol térmico en reactores ha sido estudiado desde hace tiempo. Existen varios trabajos donde se han realizado modelos dinámicos del descontrol térmico de reactores [1,2,3,4,5]. Los objetivos de estos modelos han sido validar datos experimentales de cinéticas de reacción o bien evaluar el funcionamiento de las medidas de seguridad al generar diferentes escenarios de riesgo que pueden ocurrir.
En este trabajo se cuantifica el riesgo de un reactor semi-continuo cuando existe una desviación en el valor normal de la temperatura de entrada del flujo de refrigerante en el sistema de enfriamiento y al presentarse un descontrol térmico en el reactor se considera que se libera un compuesto tóxico por la ruptura del equipo.
El reactor sobre el que se hizo el caso de estudio fue modelado por Eizenberg et al [6]. En ese estudio, los autores realizan un análisis HAZOP (hazard and operability) al proceso, midiendo cuantitativamente las desviaciones hechas a diferentes variables del proceso. En este trabajo se eligió la desviación de una de las variables (flujo del refrigerante) y se aplicó un análisis de riesgo para las posibles consecuencias de esta desviación en la variable de operación. Para calcular el riesgo se considera que el reactor está cerca de una población. El número de daños y fatalidades que ocurren en una población expuesta a un compuesto tóxico se representa por una función probit [7].
Fundamentos teóricos
El término “Loss prevention” recientemente ha reemplazado el concepto de seguridad, pues incluye la identificación de amenazas o peligros, su evaluación técnica y el re-diseño de ingeniería de los procesos para prevenir las pérdidas humanas y materiales. Así, este campo de estudio se refiere a la prevención de accidentes a través del uso de tecnologías apropiadas para identificar las amenazas de una planta química y eliminarlas antes de que ocurra un accidente, todo ello a través del análisis de riesgos. Con respecto a los peligros, estos pueden ser cualquier sustancia química o condición física que tiene el potencial de causar daño a las personas, propiedades o al medio ambiente. Por otra parte, un riesgo es una medida del daño hacia una persona, el medio ambiente o pérdida económica en términos de tanto la probabilidad de que ocurra el incidente y la magnitud de la pérdida o daño [8].
En este trabajo se aplicará el análisis de riesgos a un reactor químico. Este equipo se considera en muchos casos el corazón de un proceso químico. Esto se debe a que en el reactor ocurren las transformaciones de la materia prima a los productos deseados a través de una o varias reacciones químicas. Para ciertos tipos de reactores industriales, como batch o semi-batch, existe la posibilidad de presentarse un descontrol térmico. Esta situación se refiere a la pérdida del control de la temperatura y ocurre a menudo por reacciones altamente exotérmicas y debido a limitaciones o fallas en el sistema de enfriamiento del reactor. El descontrol térmico significa que por algunas razones el calor generado es mayor que el calor removido del equipo y entonces la temperatura del proceso se incrementa. La velocidad del calor generado se incrementa exponencialmente con respecto a la temperatura, contrariamente al calor removido que aumenta linealmente con la temperatura. Estas condiciones de aumento de la temperatura, y por consecuencia de presión, han ocasionado severos accidentes industriales en distintas partes del mundo [4, 8].
Materiales y métodos
Se analiza el caso de estudio que consiste en un reactor semi-continuo en donde se produce la oxidación en ácido nítrico de 2 octanol para producir 2-octanona y ácidos carboxílicos [9]. En el reactor se tienen dos fases presentes, al inicio se tiene una fase acuosa de ácido nítrico, donde ocurrirán las reacciones, y la fase líquida orgánica que contiene al 2-octanol se adiciona a una velocidad constante hasta que se alcanza la relación molar deseada de reactivos. La dosificación controlada de un reactante en el reactor tiene la ventaja de minimizar la cantidad de energía disponible para impedir un descontrol térmico. De esta manera se debe evitar acumular el reactivo a dosificarse sin reaccionar en el reactor. Las reacciones que ocurren en el reactor son:
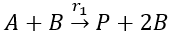 (1)
(1)
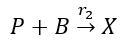 (2)
(2)Donde A es el 2-octanol, P es la 2-octanona, B es el ión nitrosonio y X son los productos de la oxidación, que pueden ser ácido fórmico, ácido acético, ácido hexanoico y ácido heptanoico. Si no se controla adecuadamente la temperatura se puede presentar una reacción indeseable que consume la 2-octanona y la convierte en ácidos carboxílicos. En este caso por simplicidad se considerará que el principal producto de la oxidación será el ácido fórmico. El ácido fórmico se considera tóxico. Los peligros para las personas son: por contacto líquido con la piel y ojos provoca quemaduras; por contacto con los vapores se produce irritación de las vías respiratorias altas y ojos. Los peligros para el medio ambiente es un producto tóxico para animales y peces.
El calor de reacción se remueve del reactor usando una chaqueta externa por donde circula un refrigerante. Durante la operación normal del reactor la temperatura no debe exceder el límite de los 0°C y solamente alrededor del 7.5% de la 2-octanona se descompone en ácidos carboxílicos. Sin embargo, si la temperatura excede los 5°C comienza el descontrol térmico y se alcanzan temperaturas por encima de los 200°C y se convierte toda la 2-octanona en ácido fórmico.
El modelo matemático del proceso de reacción y la chaqueta de enfriamiento fue desarrollado por van Woezik et al [9] y Eizenberg et al [6]:
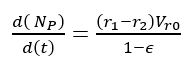 (3)
(3)
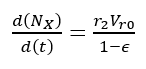 (4)
(4)
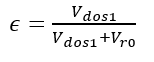 (5)
(5)
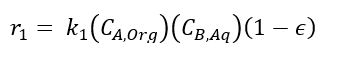 (6)
(6)
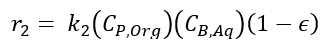 (7)
(7)
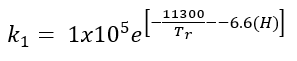 (8)
(8)
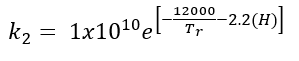 (9)
(9)
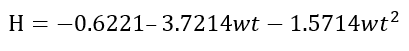 (10)
(10)
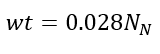 (11)
(11)
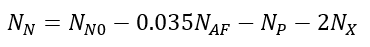 (12)
(12)
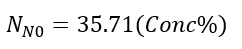 (13)
(13)
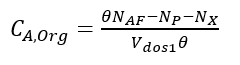 (14)
(14)
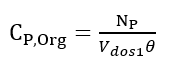 (15)
(15)
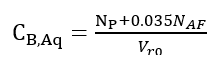 (16)
(16)
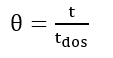 (17)
(17)
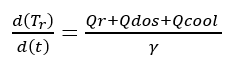 (18)
(18)
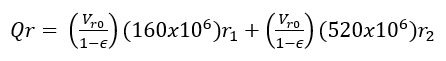 (19)
(19)
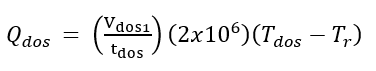 (20)
(20)
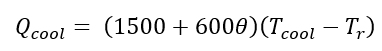 (21)
(21)
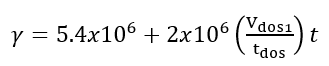 (22)
(22)
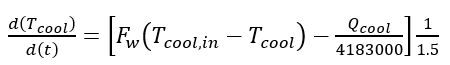 (23)
(23)Donde t es el tiempo de reacción (s) con un valor inicial de 0 s; Np es el número de moles de la 2-octanona (kmol); Nx es el número de moles de ácidos carboxílicos (kmol); Vr0 es el volumen inicial en el reactor (1.5 m3); E es la fracción volumétrica de la fase dispersa; Vdos1 es el volumen final de los reactivos que se alimentan (0.6 m3); r1 y r2 son las velocidades de reacción (kmol/m3 s); k1 y k2 son las constantes cinéticas (m3/kmol s); CA,Org, CP,Org y CB,Aq son las concentraciones de A, P y B en la fase orgánica y acuosa, respectivamente (kmol/m3); Tr es la temperatura en el reactor (K) y su valor inicial es de 260 K; H es la función de acidez de Hammett’s; wt es la concentración en peso del ácido nítrico; NN es el número de moles de HNO3 (kmol); NN0 es el número inicial de moles de HNO3 (kmol); Conc% es la concentración másica inicial de la solución de HNO3 (60%); NAF es el total de moles alimentados de 2-octanol (3.78 kmol);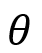 es un tiempo adimensional; tdos es el tiempo que dura la adición de reactivos (36000 s); Qr es la suma del calor de las dos reacciones (W); Qdos es la entrada de calor por la adición de reactivos (W); Qcool es el calor removido por la chaqueta de enfriamiento (W); Tdos es la temperatura a la que se adicionan los reactivos (293.15 K);
es un tiempo adimensional; tdos es el tiempo que dura la adición de reactivos (36000 s); Qr es la suma del calor de las dos reacciones (W); Qdos es la entrada de calor por la adición de reactivos (W); Qcool es el calor removido por la chaqueta de enfriamiento (W); Tdos es la temperatura a la que se adicionan los reactivos (293.15 K); 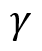 es la capacidad calorífica total del sistema (J/K); Tcool es la temperatura del fluido de enfriamiento en la chaqueta (K) con una temperatura de entrada Tcool,in de 260 K y Fw es el flujo de refrigerante en la chaqueta (100 l/min). Los valores en el tiempo inicial para las variables que se integraran a lo largo de un tiempo de 20 h son NP = 0, NX = 0, Tr = 260 K y Tcool = 273.15 K. El modelo del reactor se resolvió usando Polymath [10].
es la capacidad calorífica total del sistema (J/K); Tcool es la temperatura del fluido de enfriamiento en la chaqueta (K) con una temperatura de entrada Tcool,in de 260 K y Fw es el flujo de refrigerante en la chaqueta (100 l/min). Los valores en el tiempo inicial para las variables que se integraran a lo largo de un tiempo de 20 h son NP = 0, NX = 0, Tr = 260 K y Tcool = 273.15 K. El modelo del reactor se resolvió usando Polymath [10].
En este trabajo se retoma el análisis que hicieron Eizenberg et al. [6] a este reactor. Los autores del mencionado trabajo realizan un análisis HAZOP cuantitativo al proceso, midiendo cuantitativamente las desviaciones hechas a algunas variables del proceso y que pueden ocasionar el descontrol térmico del reactor. Las variables que analizaron Eizenberg et al. [6] fueron: Tcool,in, Fw, tdos, Vdos1 y Conc%.
En caso de descontrol térmico se comenzará a elevar la temperatura ocasionando una sobrepresión en el reactor que causaría una ruptura catastrófica del equipo y la consecuente liberación de material tóxico (ácido fórmico). Este accidente puede afectar a poblaciones ubicadas cerca del reactor. En este trabajo el análisis de consecuencias tiene el objetivo de estimar el riesgo individual para una población cercana, ocasionado por una desviación en el flujo de refrigerante Fw. El número de daños y fatalidades que ocurren en una población expuesta a sustancias tóxicas se representa por una función Probit [7]:
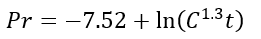 (25)
(25)Donde t es el tiempo de exposición y C es la concentración en mg/m3 de la sustancia tóxica. Para causar un 1% y 50% de fatalidad se requieren 431 y 2159 ppm, respectivamente. Para los parámetros de la función Probit del ácido fórmico, de acuerdo con dDomenico et al. [7], se recomienda usar el valor de la sustancia acrilonitrilo. Esta recomendación, se debe a la falta de una función Probit para el ácido fórmico y datos de toxicidad en humanos en el momento del estudio.
Resultados y discusión
Se plantearon tres escenarios posibles cuando sucede el descontrol térmico del reactor. En el incidente A se consideró una fuga instantánea por la ruptura completa del equipo, en los incidentes B y C el escenario se plantea con la posibilidad de fugas continuas por un sistema de venteo o por un orificio en alguna tubería del equipo, respectivamente. Para los tres escenarios analizados se aplicó el modelo gaussiano para modelar la dispersión del material tóxico [8]. Las condiciones atmosféricas son clasificadas de acuerdo con seis clases de estabilidad (A-F). La clase de estabilidad depende de la velocidad del viento y la cantidad de luz solar. Durante el día, mientras el sol brilla, comúnmente se tienen estabilidades de la A a la C, la clase D es neutral y las clases E y F ocurren conforme se acerca la noche con poco viento [8]. En nuestro caso, se decidió arbitrariamente elegir la clase F que representa condiciones atmosféricas moderadamente estables con una velocidad del viento de 1.5 m/s, pues estas condiciones darían lugar al peor escenario con una baja dispersión del material tóxico. Posteriormente, se aplicó la función Probit con un tiempo de exposición de 30 minutos para encontrar la concentración que causaría un 50% de fatalidades. Se considera que el viento sopla predominantemente en la dirección Este y que se ubica una población a menos de 1000 m de la ubicación del reactor.
Para el primer escenario (incidente A), el modelo del reactor se resolvió usando Polymath, luego se genera la desviación en la variable Fw, flujo del refrigerante, lo cual ocasionó el descontrol térmico del reactor. Se analizaron también las desviaciones en las variables de Tcool,in, tdos, Vdos1 y Conc% en el modelo del reactor. En cualquiera de los casos analizados se obtuvo una cantidad similar de formación de ácidos carboxílicos. Por esta razón se consideró sólo analizar el efecto de la desviación en la variable Fw. El valor de 100 l/min para Fw, sirvió como base y a partir de este valor se hicieron los cambios que se observan en las Figuras 1 y 2, hasta obtener el descontrol térmico. Esto sucede para un valor de Fw de 50 l/min.
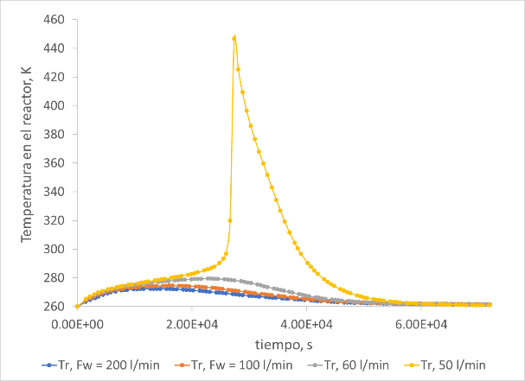
Fig. 1:
Variación en Tr
Del modelo resuelto en Polymath indicado por las ecuaciones anteriores se obtiene la cantidad de ácido fórmico (3.5 kmol o 173.88 kg) que se produce en el reactor y suponiendo que el reactor no cuenta con sistemas de seguridad, se liberará esta cantidad de material tóxico causando daños a la población cercana. Después de 10 minutos de la liberación del material tóxico se encontró que el centro de la isopleta se encuentra a 900 m con una altura de 25.4 m.
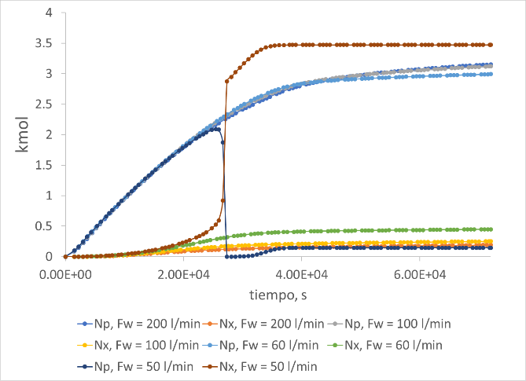
Fig. 2:
Variación en Np y Nx
En la Figura 3, el origen considera que es la ubicación de la planta, donde se encuentra el reactor y a 900 m en la dirección Este, que es hacia donde soplan los vientos predominantemente, se encuentra una población.
Para el segundo escenario (incidente B) se supuso una fuga continua de ácido fórmico de 6 kg/s. Esta situación genera una isopleta con un centro en los 992.8 m (en dirección Este) y 50.9 m de altura. En el tercer escenario posible (incidente C) se supone la fuga de ácido fórmico a través de un orificio de 1.5 cm, generando un flujo de 3.9 kg/s de ácido fórmico. Este incidente ocasiona una isopleta con centro a 768.7 m (en dirección Este) y altura de 40.2 m. En la Figura 3 se muestran las zonas de afectación de los tres incidentes superpuestas.
La frecuencia de cada uno de los eventos iniciales que originan la liberación de material se supone de 6.5x10-6, 4.5x10-5, 5x10-6/año, respectivamente para los tres incidentes. Los valores de estas frecuencias se toman de valores típicos reportados históricamente para eventos iniciales de accidentes ocurridos en la industria química [11].
Para estimar el riesgo individual se sobreponen las áreas de afectación de las consecuencias de las fugas. El cálculo del riesgo individual en cualquier punto considera que todas las contribuciones de los incidentes son aditivas. En teoría, cada una de estas zonas deberían afectarse por la probabilidad con que sopla el viento en las diferentes direcciones, sin embargo, como la población solamente se ubica al este, solo se calcula el riesgo en esa dirección.
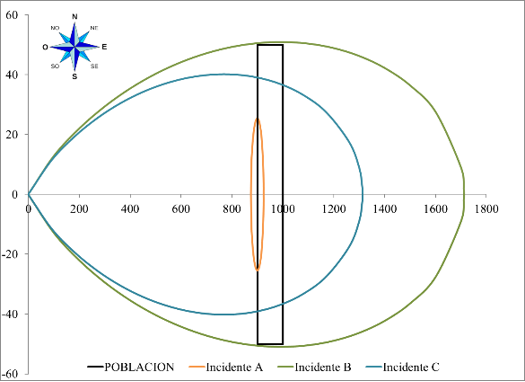
Fig. 3:
Mapa de vulnerabilidad
En este caso, el riesgo de fatalidad para todos los posibles eventos es de 2.8x10-5/año para una cierta parte de la población que se ubica a una distancia menor a 925 m. Más allá de esta distancia el riesgo es solo por los incidentes B y C, siendo el riesgo de fatalidad de 2.5 x10-6/año.
Aunque en este trabajo se supusieron los flujos de venteo en los incidentes de las fugas continuas de material tóxico, se podría modificar el modelo existente del proceso para incluir las ecuaciones del sistema de venteo. Así mismo se podría incluir en el modelo algún sistema de seguridad que permita investigar su efecto en la disminución del riesgo de fatalidad.
En este trabajo se amplían los resultados obtenidos por Eizenberg et al [6], quienes realizan un análisis HAZOP (hazard and operability) del descontrol térmico de la reacción de oxidación del ácido nítrico y 2 octanol para producir 2-octanona. Los accidentes que se simulan ofrecen un panorama hipotético de las posibles consecuencias y se podría aplicar esta metodología a otros procesos o cambiar las situaciones de los escenarios. De esta forma, la principal contribución del estudio es combinar en una misma metodología el análisis cuantitativo HAZOP y la metodología QRA.
Conclusiones
En este trabajo se estableció una metodología que permitió cuantificar el efecto de la desviación de una variable de proceso sobre el riesgo de fatalidad. La metodología se aplicó a la operación de un reactor discontinuo y esta misma metodología se podría aplicar a otros procesos químicos. El uso de simuladores para generar situaciones de riesgo en equipos o procesos permite proponer sistemas de seguridad a las variables que muestren mayor riesgo. El análisis de riesgos mostró que, en el caso del descontrol térmico del reactor, las áreas de afectación son mayores en los casos de los incidentes B y C, donde se plantea la posibilidad de fugas continuas por un sistema de venteo o por un orificio en alguna tubería del equipo, respectivamente, con respecto al escenario A de una ruptura completa del equipo. Esto señala la importancia de mantener un programa de revisión continua de fugas en los equipos.
Agradecimientos
El co-autor Florianne Castillo-Borja agradece el apoyo de TecNM a través del proyecto 5841.19-P.
Referencias
1 Luyben, W.L., (2012), “Use of dynamic simulation for reactor safety analysis”, Comp. Chem. Eng., volumen 40, p. 97-109
2 Copelli, S., M. Derudi, C. Cattaneo, G. Nano, M. Raboni, V. Torretta y R. Rota, (2014), “Synthesis of 4-Chloro-3-nitrobenzotrifluoride: Industrial thermal runaway simulation due to cooling system failure”, Proc. Safety Env. Prot., volumen 92, p. 659-668.
3 Ni, L., A. Mebarki, J. Jiang, M. Zhang, V. Pensee y Z. Dou, (2016), “Thermal risk in batch reactors: Theoretical framework for runaway and accident”, J. Loss Prev. Proc. Ind., volumen 43, p. 75-82.
4 Kummer, A., Varga, T., Nagy, L. (2020), “Semi-batch reactor control with NMPC avoiding thermal runaway”, Comp. Chem. Eng., volumen 134, p. 106694-10.
5 Dakkoune, A., Vernières-Hassimi, L., Lefebvre, D., Estel, L., (2020), “Early detection and diagnosis of thermal runaway reactions using model-based approaches in batch reactors”, Comp. Chem. Eng., volumen 140, p. 106908-16.
6 Eizenberg, S., M. Shacham y N. Brauner, (2006), “Combining HAZOP with dynamic simulation. Applications for safety education”, J. Loss Prev. Proc. Ind., volumen 19, p. 754-761.
7 di Domenico, J., C. André Vaz Jr. y M. Bezerra de Souza Jr., (2014), “Quantitative risk assessment integrated with process simulator for a new technology of methanol production using recycled CO.”, J. Hazardous Mat., 274, p. 164-172.
8 Crowl, D.A. y J.F. Louvar, (2002), Chemical Process Safety. Fundamentals with Applications, Prentice Hall (USA).
9 Van Woezik, B.A.A. y K.R. Westerterp, (2001), “Runaway behavior and thermally safe operation of multiple liquid-liquid reactions in the semi-batch reactor. The nitric acid oxidation of 2-octanol”, Chem. Eng. Proc., volumen 41, p. 59-77.
10 Shacham, M., Cutlip, M., Elly, M., “Polymath software”, https://www.polymath-software.com/, visitado el 1 de noviembre de 2020.
11 CCPS (Center for Chemical Process Safety), (1999), Guidelines for Chemical Process Quantitative Risk Analysis, 2nd Edition, Wiley (USA).
Notas de autor
Contacto: florianne.cb@aguascalientes.tecnm.mx
