Artículos
Caracterización de la Super-acidez del Carbón Sulfatado por Espectroscopia
Characterization of Super-acidity of Sulfated Char by Spectroscopy Analysis
Caracterización de la Super-acidez del Carbón Sulfatado por Espectroscopia
Conciencia Tecnológica, núm. 62, 2021
Instituto Tecnológico de Aguascalientes
Recepción: 03 Agosto 2021
Aprobación: 30 Noviembre 2021
Resumen: En este trabajo se caracteriza un nuevo material basado en un sólido carbonoso que fue funcionalizado como catalizador super-ácido al usar ácido sulfúrico como fuente de iones sulfonilo –SO.H. Este material carbonoso que se preparó por el proceso de pirólisis aplicado a hule de llanta, puede ser usado como catalizador directamente o bien, como soporte catalítico. El proceso de pirólisis fue realizado con flujo de N. a temperaturas relativamente altas y así obtener un material mesoporoso en base al carbono y que fue sulfonado de forma efectiva. El método de sulfonación del carbón obtenido de hule de llanta fue mediante inmersión en ácido sulfúrico concentrado y a reflujo. Dos muestras de carbón, el original y el sulfonado, fueron caracterizados por medio de diferentes técnicas analíticas, principalmente por las espectroscopías Raman y Fotón-electrónica de rayos-X. Las diversas señales resultantes de estos análisis sugieren super-acidez protónica del carbón sulfonado, siendo tal propiedad relacionada a la estructura de grupos o iones relativos al ácido sulfónico en la superficie del material.
Palabras clave: Carbón sulfonado, Análisis espectroscópico, Sitios protónicos, Sólido super-ácido.
Abstract: A new acid catalyst based in a carbonaceous solid was functionalized using sulfuric acid as source of –SO.H species. This carbon-based material prepared by the pyrolysis of waste tire rubber was used either as catalyst or as catalytic support. The pyrolysis process was performed with a flow of N. at relatively high temperature to obtain a mesoporous material and after, achieve an effective sulfonation. The sulfonation of char obtained from tire rubber was through direct immersion into concentrated H.SO. under reflux. Chars, original and sulfated, were characterized by several analytic techniques including an elemental analysis. Mainly by Raman and X-ray Photon-electronic spectroscopies. Resultant signals are suggestive of protonic superacidity on sulfonated char, this property being related to the structure of surface sulfonic species.
Keywords: Sulfoned char, Spectroscopy analysis, Protonic sites, Super-acid solid.
Fundamentos teóricos
Se puede señalar que los ácidos fuertes más importantes son; clorhídrico, sulfúrico, nítrico y fosfórico y si los iones positivos que se generan en la disociación pudieran anclarse en un sólido se tendría un catalizador ácido o muy ácido lo que posibilitaría la transformación de un proceso químico homogéneo en uno heterogéneo y así evitar el uso de ácidos líquidos que dañan los equipos en un proceso químico y preservar el producto valioso que se busca obtener.
Los alumino-silicatos cristalinos del tipo zeolitas son el ejemplo más importante de materiales sólidos con sitios ácidos. Los centros activos mencionados atrás se desarrollan al hacer un intercambio iónico de los cationes positivos de sodio o potasio inherentes al sólido por iones amonio (NH4+) y que con la calcinación a 450 ºC se elimina el amoniaco (NH3) para formar sitios protónicos (H+) en la superficie del sólido, de acuerdo con el esquema siguiente:
![Esquema de un sitio ácido Bronsted en la superficie de un alumino-silicato cristalino [1].](../94469878003_gf8.png)
Figura 1
Esquema de un sitio ácido Bronsted en la superficie de un alumino-silicato cristalino [1].
El esquema de la Figura 1 es en realidad la conjugación de dos sitios ácidos; Bronsted y Lewis porque al romperse el enlace Al-O, en el aluminio se forma la vacancia electónica activándose un sitio ácido Lewis.
La super-acidez se presenta en ácidos que tienen la fuerza ácida mayor al ácido sulfúrico el cual presenta un factor Ho de -12 de acuerdo con el método del indicador Hammett. Algunos sólidos como el Nafión-H y óxidos metálicos como; zirconia, titania o las mismas zeolitas cuando han sido sulfonados pueden presentar factores Ho menores a -12. Por ejemplo, el material Zr6O5(OH)3(BTC)2-(SO4)2.5(H2O)2.5 presenta un factor Ho de -14.5, mucho menor al detectado para ácidos minerales [2].
En el proceso de sulfonación del óxido metálico que suele hacerse mediante la mezcla ácido/sólido a temperatura relativamente alta y con agitación, lo que se fija en la superficie del sólido es la molécula incompleta de ácido sulfúrico o se fija completa en dos partes y su anclaje puede ser en diferentes orientaciones. En la fijación de los grupos ácidos en los átomos de metal, un ión hidrógeno queda en posición perpendicular a la superficie del sólido para formar un sitio ácido, es decir, un protón (H+) disponible para entrar en acción como un centro super-ácido tipo Bronsted y combinarse con electrones de la molécula orgánica.
De acuerdo con la Figura 2, adaptada de Huang y colaboradores. [3], la porción oxigenada del ácido sulfúrico está anclada al metal en esta estructura propuesta y los átomos de hidrógeno están enlazados directamente a un átomo de oxígeno y a su vez, esté oxígeno es parte del óxido metálico. Debido a que en ese grupo de átomos hay un desequilibrio de cargas, uno de los átomos de hidrógeno presenta la vacancia electrónica que se traduce en una carga positiva; el protón que se requiere para formar el sitio super-ácido.
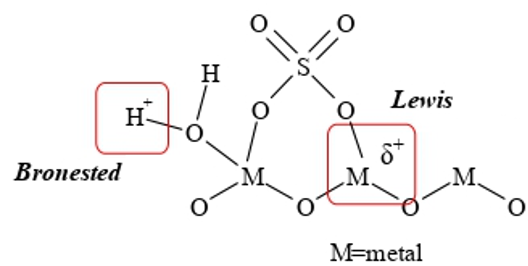
Figura 2
Representación de los sitios super-ácidos Bronsted y Lewis en un óxido metálico sulfonado.
Debido a la configuración de las partes ancladas de la molécula original de ácido sulfúrico y su orientación, de forma simultánea se puede formar un sitio super-ácido tipo Lewis donde en lugar de actuar un protón ávido de electrones, está la vacancia electrónica (ión positivo) en un átomo del metal sobre la superficie del sólido y dispuesto a aceptar electrones con la misma intensidad mostrada por el protón (ver Figura 1). Esta vacancia en el átomo de metal se forma al compartir sus electrones por la alta demanda de tres átomos de oxígeno alrededor del átomo metálico. Por cierto, aún existen procesos en la industria química realizados en fase líquida, que utilizan sales o complejos de metales de transición como catalizadores ácidos de Lewis homogéneos debido la capacidad de coordinación de los metales en disolución. Sin embargo, estos sistemas se han visto desplazados por el uso de catalizadores sólidos que son ácidos de Lewis potencialmente más activos, selectivos y fáciles de separar del sistema heterogéneo ya sea en reacciones ácido-base típicas o en reacciones de reformación de hidrocarburos. Tales sitios ácidos se forman, como ya vimos anteriormente, debido a la incorporación de especies metálicas con vacantes en un entorno de coordinación.
En algunos procesos se requieren catalizadores super-ácidos con sitios preferentemente del tipo Bronstead debido en parte, a que presentan un acceso más fácil a las moléculas orgánicas que actúan como reactivos. Por fortuna, es posible interconvertir los sitios ácidos Lewis en Bronstead por medio de la hidratación del óxido metálico a temperaturas moderadas donde la transformación principal se esquematiza en la Figura 3 que ha sido adaptada del trabajo de Brown y Hargreaves [4].
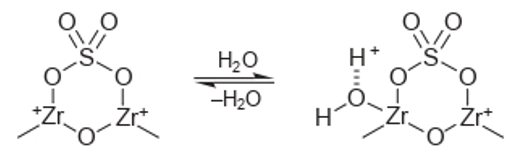
Figura 3
Transformación propuesta de un sitio ácido Lewis a un sitio ácido Bronsted y biceversa en zirconia sulfatada, SO4-2/ZrO2.
Las orientaciones de la molécula incompleta del ácido sulfúrico sobre la superficie sólida y que se presentan aquí, probablemente no son las únicas posibles, y con seguridad son las más consistentes y estables. Por esa razón son las configuraciones más estudiadas, aunque algunos químicos y sobre todos aquellos que se dedican al estudio de la catálisis, suelen visualizar pequeñas variaciones sin llegar a proponer diferentes estructuras químicas.
De la gran cantidad de resultados referenciados se conoce que la inusual fuerza ácida de los óxidos metálicos y materiales compuestos (composites) sulfatados está asociada a varios factores, entre otros: i) la alta estabilidad en el grafitado de los iones sulfónico y sulfato (SO42-) sobre la superficie del sólido, ii) la electronegatividad presentada por el metal del óxido, iii) el metal o complejo orgánico incorporado al óxido metálico [5]. Esto último también promueve la super-acidez debido en gran parte a que los metales tienen diferentes electronegatividades. Por ejemplo, los cationes del elemento estroncio (Sr2-) presentan una electronegatividad baja y en forma de óxido sulfonado tiene un factor de Hammett, Ho de -12.70, apenas menor al del H2SO4 [6]. En contraste, la zirconia dopada con tricarboxilato bencénico y posteriormente sulfatada, puede presentar un factor de casi -15.0 [2].
En este trabajo se aplicó un análisis espectroscópico para demostrar la presencia de la super-acidez del tipo Bronsted en un sólido carbonoso obtenido del pirólisis de hule de llanta a temperaturas moderadas. El objetivo principal fue correlacionar esa importante propiedad en el material con la estructura de las especies sulfato ancladas en la superficie del carbón.
Materiales y métodos
Aunque el método Hammett se sigue usando para la definir la fuerza o intensidad en los sitios super-ácidos, este no da indicación de la estructura, densidad o tipo de sitio ácido y para ello, hay técnicas más sofisiticadas y que son complementarias a otras técnicas de caracterización como las espectroscopias del infra-rojo (IR), Raman y fotón-electronica de rayos-X (XPS). La primera técnica se basa en la interacción de moléculas con la radiación electromagnética dentro del rango del infra-rojo. Al hacer un barrido de longitudes de onda de la radiación y por lo tanto de energías, los enlaces de las moléculas absorben energía en una cantidad de acuerdo con el enlace y a su modo de vibración inducida, de tal manera que se obtiene un espectro característico de la molécula o moléculas presentes donde cada banda o pico de absorbancia identifica un enlace o un grupo molecular.
En un análisis Raman las moléculas se irradian con un haz láser de cierta frecuencia. La interacción de las moléculas con la energía asociada en el rayo láser da como resultado la distorsión momentánea de los electrones distribuidos alrededor de los enlaces moleculares generando un fenómeno muy peculiar que es el esparcimiento de radiación con diferentes longitudes de onda (λe), mayores y menores a la longitud de onda del haz incidente (λo). Por lo común, se obtiene el espectro Stokes con bandas de mayores longitudes de onda y cada una de estas bandas o picos identifica un grupo molecular presente en la muestra.
La espectroscopia fotón-electrónica de rayos-X se ha referenciado ser útil para discriminar la estructura de grupos moleculares, para correlacionar la fuerza ácida de sitios en la superficie sólida y para definir el espacio vecino o alrededor de un un átomo en específico. En el caso de un material grafitado con algún grupo del ácido sulfúrico u otro ácido similar, interesa conocer el espacio alrededor del oxígeno analizado de acuerdo con sus electrones liberados y sobre todo del subnivel electrónico a que pertenecen En el análisis XPS se usa la radiación con más energía que la Ultravioleta como lo es la proporcionada por los rayos X. Cuando un fotón interacciona con un electrón, le transfiere toda su energía parte de la cual se usa para liberar el electrón de la atracción que le infringe el núcleo (energía potencial) y una parte menor para sacarlo del átomo a alta velocidad (energía cinética). Obviamente que la energía que adquiera el electrón debe ser suficiente para vencer la atracción del núcleo positivo y vencer la barrera energética definida como Nivel de Fermi y pasar a la banda de conducción electrónica y finalmente escapar del átomo. Por medio de un analizador de electrones se detectan y separan los electrones por su energía de enlace (EB) que es característica de cada elemento y del subnivel donde fueron liberados.
Los materiales analizados son dos sólidos compuestos de carbono que se obtuvieron del pirólisis de hule de llanta a 500-550 ºC y en flujo de N2. El primer material analizado fue el sóilido tal como se obtiene del proceso de pirólisis y el segundo se obtuvo mediante la inmersión en ácido sulfúrico concentrado y a reflujo de la mezcla. Ambos carbones resultaron ser del tipo mesoporoso de tal manera que pueden usarse en un proceso de transformación química como catalizadores heterogéneos ácidos o bien como soportes catalíticos.
Los espectros Raman de los carbones fueron registrados con un espectrofotómetro dispersivo JASCO NRS-5100 bajo la resolución de 5 cm-1 y la línea de excitación de 532 nm, usando la potencia del láser de 30 mW sobre la muestra. Del análisis de estas muestras se espera detectar en principio los dos picos característicos del carbón; D1 y G en las posiciones 1350 y 1580 cm−1, respectivamente [5]. El siguiente análisis espectroscópico fotón-electrónico de rayos-X fue realizado con equipo Kratos Axis Ultra-DLD XP el cual se ha reportado para correlacionar con la fuerza ácida de grupos superficiales –OH de acuerdo con varios investigadores como Perazzolo y colaboradores en 2015 [6].
En este proceso, las muestras fueron pre-tratadas a 673 K al vacío y las mediciones realizadas bajo atmósfera de N2. Los valores de energía de enlace proporcionadas por el espectrofotómetro XPS fueron corregidos a la señal O1s en la posición de 531 eV como un blanco o estándar interno.
Resultados y discusión
Las técnicas de caracterización mencionadas en la sección de Materiales y métodos pueden detectar grupos funcionales en las moléculas ancladas sobre un sólido como carbón o un óxido metálico y determinar los enlaces alrededor de un átomo sin poder definir orientaciones de los átomos en esos grupos moleculares. En el caso de los materiales sulfonados pueden identificar los grupos O=S=O, S=O y S-O y otros similares o derivados.
Como ejemplo de un análisis Raman en dos muestras de carbón; original y sulfatado (Figura 4), se presentan los espectros en la zona donde aparecen los grupos funcionales característicos del ácido sulfúrico, y que se detectan solamente en el sólido sulfonado, el carbón original solo presenta aquellos picos que son propios de las láminas de carbón [7].
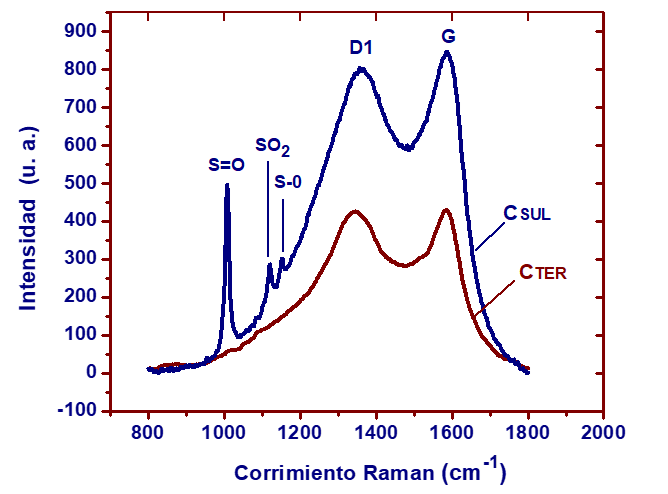
Figura 4
Espectros Raman para el carbón original (CTER) y para el carbón sulfonado (CSUL).
En un estudio adicional usando transmitancia de radiación en el infra-rojo con transformada de Fourier (FT-IR), se pudo observar la banda de vibración O-H en 3462 cm-1 para el material CSUL, la cual no se observó en el espectro IR del carbón original, CTER [8]. Se asume que este enlace está ligado al grupo sulfónilo O=S-OH que resultó de la leve descomposición del ácido sulfúrico. Un esquema simplificado de tales especies sobre la superficie del carbón se propone en la Figura 5.
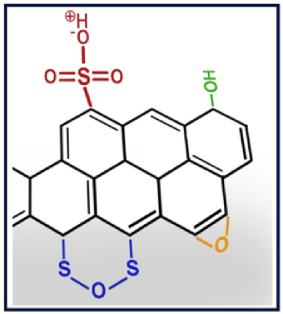
Figura 5
Especies sulfonilo propuestas y ancladas sobre la superficie del carbón sulfonado.
Se hace uso del mismo procedimiento para obtener y presentar resultados de la interesante técnica de caracterización definida como espectroscopía XPS (Figura 6). Un escaneo en la región propia del oxígeno y para el subnivel electrónico O1s, muestra la señal principal en 532.8 eV y una señal débil en 531 eV, que son picos del carbón original y que corresponden a las especies químicas C-O-C and –C=O. En contraste, el espectro XPS del carbón sulfonado es dominado por la banda simple en 534.2 eV y de esto se nota que, debido al tratamiento de sulfonación, la mayoría de los grupos –C=O que estaban presentes en el carbón original, ya se transformaron en sitios ácidos tipo Bronstead identificados como especies -SO3H y detectados en 534.2 eV. Estos grupos ya han sido detectados de forma similar por Bullock y colegas [9] y Aldana-Pérez y colaboradores [10].
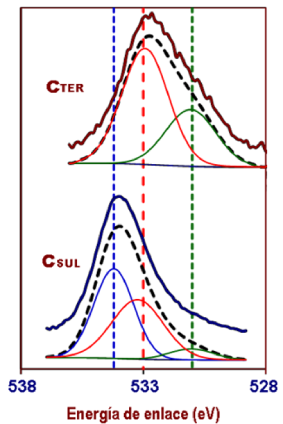
Figura 6
Espectros XPS para las dos muestras de carbón en la región específica para el oxígeno; O1s.
El valor absoluto de la energía de enlace para la muestra sulfatada es significativamente más alto que la reportada por Bullock y sus colegas [9] para la sílice sulfonada, y esto podría ser un indicio de la super-acidez protónica en la superficie del carbón. Aunque este tipo de comparaciones deben de hacerse con sumo cuidado y corroborar los resultados con técnicas analíticas adicionales.
Conclusiones
El carbón obtenido de la pirólisis, así como el carbón sulfonado y analizados en este estudio pueden ser usados ya sea como un soporte catalítico antes de ser sulfonado o como un catalizador super-ácido.
Las técnicas de caracterización aplicadas para sondear la superficie de estos materiales de carbón han confirmado propiedades especiales que son sugestivas de un carácter super-ácido con sitios sulfónicos tipo Bronsted enlazados o anclados en la superficie.
La proporción relativa de los sitios super-ácidos depende del material de origen, de las condiciones en la obtención del carbón y de las condiciones aplicadas en el proceso de sulfonación.
En contraste, y a partir de datos reportados en otro escrito [11], el material de carbón original resultó ser activo en la esterificación de aceite vegetal para producir biodiesel de alta calidad, aunque la actividad del carbón sulfonado fue mucho mayor y en proporción a los sitios ácidos detectados en el material.
Referencias
[1] Jin, F., Li, Y., (2009), Catal. Today, Vol. 145, Issues 1–2, 101-107.
[2] Jiang, J., Gándara, F., Zhang, Y. B., Na, K., Yaghi, O. M., Klemperer, W. G., (2014), J. Am. Chem. Soc., 136, 12844−12847.
[3] Huang, Ch. Ch., Yang, Ch. J., Gao, P. J., Chang, J. Sh., (2015), Green Chemistry 17(6), 3609-3620.
[4] Brown, A. S. C., Hargreaves, J. S. J., (1999), Green Chemistry, 17-20.
[5] Riemer, T., Spielbauer, D., Hunger, M., Mekhemer, G. A. H., Knozingera, H., (1994), J. Chem. Soc., Chem. Commun., 10, 1181-1182.
[6] Perazzolo, V., Durante, C., Pilot, R., Paduano, A., Gian, J. Z., Rizzi, A., Martuccic, A., Granozzi, G., Gennaro, A., (2015), Carbon,Vol. 95, 949-963.
[7] Medina-Valtierra, J., Sánchez-Olmos, L. A., Carrasco-Marin, F., Sánchez-Cárdenas, M., (2017), Intern. J. Chem. React. Eng., 72, 1-15.
[8] Sánchez-Olmos, L. A., Sánchez-Cárdenas, M., Sathish-Kumar, K., Tirado-González, D. N., Maldonado-Ruelas, V. A., Ortiz-Medina, R. A., (2020), Revista Mexicana de Ingeniería Química, 19, 2.
[9] Bullock, J., Kiriya, D., Grant, N., Azcatl, A., Hettick, M., Kho, T., Phang, P., Sio, H. C., Yan, D., Macdonald, D., Quevedo-Lopez, M. A., Wallace, R. M., Cuevas, A., Javey, A., (2016), ACS Appl. Mater. Interfaces, 8 (36), 24205-24211.
[10] Aldana-Pérez, A., Lartundo-Rojas, L., Gómez, R., Niño-Gómez, M. E., (2012), Fuel 100, 128–138.
[11] Sánchez-Olmos, L. A., Medina-Valtierra, J., Sathish-Kumar, K., Sánchez-Cárdenas, M., (2017) EPSE Journal, Vol.36, No.2, 620-626.
Notas de autor