Recepción: 23/11/15
Aprobación: 04/03/16
Resumen: La mastitis subclínica es un grave problema en las unidades de producción de leche caprina a nivel mundial, reportándose una prevalencia superior al 30%, estando implicados diversos agentes bacterianos. Se presenta un caso de mastitis subclínica en una cabra criada bajo un sistema intensivo en la comunidad El Recreo, municipio Miranda del estado Falcón, Venezuela, en el cual se realizó el aislamiento e identificación de Morganella morganii morganii mediante técnicas bacteriológicas convencionales en el laboratorio de Microbiología Veterinaria del Programa de Ciencias Veterinarias de la Universidad Nacional Experimental Francisco de Miranda. Se trató de un cocobacilo Gram negativo, que formó colonias pequeñas, elevadas y translucidas en agar Mac Conkey, fermentador de glucosa, productor de gas, móvil, lactosa, maltosa y trehalosa negativo, el cual mostró resistencia a varios antibióticos de uso frecuente a nivel de campo. Este es el primer reporte de Morganella morganii morganii aislada a partir de leche de cabra en el estado Falcón.
Palabras clave: Morganella morganii morganii, mastitis subclínica, leche de cabra.
Abstract: Subclinical mastitis is a serious problem in goat milk farms on the world, it had been reported prevalence higher than 30%, being implicated several bacterial genus. A case of subclinical mastitis is presented in a goat farm operated under an intensive system in the community El Recreo, Miranda County of Falcon State, Venezuela, where isolation and identification of Morganella morganii morganii was carrying out, using conventional bacteriological techniques at the Veterinary Microbiology Lab from Programa de Ciencias Veterinarias of the Universidad Nacional Experimental Francisco de Miranda. It was a Gram negative coccobacillus, which grow forming small, high and translucent colonies in agar Mac Conkey; glucose fermenter, gas producer and mobile, lactose, maltose and trehalose negative, and shows resistance to antibiotics commonly used in veterinary medicine. This is the first report of Morganella morganii morganii isolated from goat milk in the Falcon State.
Keywords: Morganella morganii morganii, subclinic mastitis, goat milk.
INTRODUCCIÓN
La infección intramamaria en cabras (Capra hircus) constituye un grave problema de salud animal, dado que altera la composición de la leche, disminuye su calidad bacteriológica, desmejora las condiciones para su procesamiento y causa grandes pérdidas económicas en la industria lechera [37, 39].
La mastitis subclínica no suele causar signos evidentes en el animal o en la leche [3], por lo tanto, no puede ser diagnosticada mediante examen físico o evaluación directa, por ello es necesario realizar el contaje de células somáticas o cultivo de la leche a fin detectar la presencia de agentes patógenos intramamarios [42]. En este orden de ideas, una de las pruebas cualitativas más utilizadas para determinar la presencia de células somáticas en leche de cabra es el California Mastitis Test (CMT) [17]; según Stuhr y Aulrich [37], esta prueba permite estimar el número aproximado de células inflamatorias y epiteliales en una muestra de leche con un alto nivel de correlación con los valores del contaje de células somáticas en leche de cabra, por lo cual juega un papel crucial en la detección de infección intramamaria subclínica en caprinos. Igualmente, los resultados obtenidos al comparar el CMT con los cultivos bacteriológicos de leche de cabra avalan la importancia de esta prueba a nivel de campo en el diagnóstico de mastitis subclínica en caprinos [25].
La incidencia de mastitis clínica o subclínica en cabras varía en función de diversos factores como las condiciones nutricionales, sanitarias y de manejo de cada unidad de producción (UP); esta patología, además de su impacto económico puede tener efectos negativos sobre la salud pública [22].
Al respecto, Najeeb y col. [27] refieren que, los principales microorganismos involucrados en la etiología de mastitis clínica o subclínica en cabras lecheras son Staphylococcus aureus (S. aureus), Escherichia coli, Streptococcus spp. y especies de los géneros Corynebacterium, Brucella, Bacillus y Pseudomonas. Entre estas especies, S. aureus es el principal causante de mastitis en cabras lecheras, sin embargo, la prevalencia y la importancia de los diferentes agentes etiológicos pueden variar en función de las regiones geográficas. Esta situación se ve acentuada en UP, donde la suma de factores, entre ellos, la baja productividad por animal, el sistema de ordeño, las condiciones de explotación, factores climáticos adversos y la dispersión de las actividades productivas en grandes áreas geográficas, dificulta el monitoreo de la calidad sanitaria de la leche [18].
La tasa de incidencia de mastitis subclínica en cabras frecuentemente supera el 30%, siendo los estafilococos coagulasa negativo, S. aureus y estreptococos, los principales microorganismos identificados [3]. Se han reportado datos similares en varias regiones a nivel mundial, tal como lo demuestran investigaciones realizadas en Estados Unidos, Gran Bretaña, Francia y España donde se han identificado cifras de 36; 36; 33 y 18%, respectivamente [42].
En el estado Falcón, en un estudio llevado a cabo por Clavijo y col. [6] se encontraron seis agentes etiológicos bacterianos implicados en los casos de mastitis subclínica en cabras, a saber: S. aureus (62%), E. coli (10,3%), Streptococcus dysgalactiae (10,3%), Streptococcus uberis (6,8%), Enterobacter aerogenes (6,8%) y Mycoplasma spp. (3,4%), con un porcentaje de positividad de 69% de las cabras muestreadas en su estudio.
En otro orden de ideas, Klinger y Roshenthal [18], al evaluar la presencia de enterobacterias en el proceso de elaboración y maduración de queso duro de cabra revelaron alteraciones de la flora microbiana a lo largo de la línea de producción. Se identificaron abundantes especies bacterianas en leche cruda de cabra, tales como Serratia liquefaciens, Morganella morganii, Hafnia alvei, Klebsiella oxytoca y Yersinia enterocolitica.
Entre estas especies, M. morganii es frecuentemente aislada de heces, particularmente de seres humanos con diarrea y algunas cepas pueden ser causantes de esta condición [36]. Aunque este microorganismo está ampliamente distribuido entre varias especies, raramente causa enfermedad en individuos sanos, sin embargo, los casos clínicos descritos cursan con cifras importantes de severidad y mortalidad, quizás por la multiresistencia a antimicrobianos, sobre todo hacia cefalosporinas de primera generación y ampicilina-clavulanato [21], tal como ha sido reportado tras el aislamiento de esta especie bacteriana en pollos, donde la cepa identificada mostró una alta tasa de resistencia a los antibióticos de uso frecuente, entre ellos: ampicilina, cefalosporinas de primera generación (cefalexina, cefalotina y cefadrina) y eritromicina, así como claritromicina, kanamicina y vancomicina; no obstante, se encontró sensibilidad a cefotaxima, cefoperazona, neomicina y norfloxacina [43].
M. morganii es una enterobacteria, inicialmente catalogada como la única especie del género, la cual consta de dos subespecies: morganii y sibonii. La diferenciación entre ambas se basa en la fermentación de la trehalosa, siendo M. morganii sibonii, trehalosa positivo [30]. Sin embargo, más recientemente, Baylis y col. [2] refieren que ha sido identificada una nueva especie, Morganella psychrotolerans, con dos subespecies morganii y sibonii, en vista de los hallazgos que demuestran su capacidad de tolerar y crecer a temperaturas de 0 a 2 ºC, encontrándose un 98,6% de similitud en las secuencias del gen 16S rRNA con los aislados mesófilos [9].
En este reporte, se presentó un caso de mastitis subclínica en una cabra lechera, en cuya muestra se realizó aislamiento e identificación de M. morganii morganii mediante técnicas bacteriológicas convencionales y evaluación de la susceptibilidad a los antimicrobianos, siendo el primer caso descrito en el estado Falcón, Venezuela.
MATERIALES Y MÉTODOS
Luego de establecido el diagnóstico de mastitis subclínica por parte del Médico Veterinario encargado de la UP mediante la prueba cualitativa CMT y solicitado el apoyo diagnóstico al laboratorio de Microbiología Veterinaria de la Universidad Nacional Experimental Francisco de Miranda (UNEFM), bajo condiciones de asepsia, con previo lavado y secado de la ubre y luego de descartar los tres primeros chorros, se tomaron muestras de leche de los medios afectados de las ubres de las cabras [24], las cuales son criadas en un sistema intensivo en una UP caprina ubicada en la comunidad El Recreo, municipio Miranda del estado Falcón, región caracterizada por un clima muy cálido y escasamente lluvioso, con temperatura promedio superior a 26,0ºC y 300 a 699 mm3 de pluviosidad al año [20].
Las muestras se trasladaron inmediatamente y bajo refrigeración al laboratorio donde se procedió a su análisis bacteriológico.
Una de las muestras de leche, proveniente de una cabra mestiza Nubian - Alpino francés, de dos partos, fue procesada considerando el protocolo diagnóstico del laboratorio de la UNEFM; se realizó cultivo para aislamiento primario mediante la técnica de siembra por diseminación y estrías en placas de agar sangre (BBL™, EUA), agar MacConckey (BBL™, EUA) y agar manitol salado (BBL™, EUA), fueron incubadas a 37ºC en condiciones de aerobiosis y microaerofilia (solo para agar sangre). Se realizaron lecturas a las 24 y 48 horas (h) de incubación para la caracterización macroscópica de las colonias, verificando la pureza mediante realización de frotis y coloración de Gram [19]. Las colonias aisladas fueron resembradas en agar inclinado Brain Heart Infusion (BHI) (BBL™, EUA) e incubadas a 37ºC durante 24 h, a fin de obtener cultivos puros [19, 23] para su posterior identificación bioquímica.
Luego, se efectuaron las pruebas de catalasa y oxidasa, rojo de metilo, Voges-Proskaüer, producción de indol, reducción de nitratos, uso del citrato como fuente de carbono, desaminación de la fenilalanina, motilidad, hidrólisis de la gelatina y la úrea, utilización del malonato, fermentación de carbohidratos (glucosa, lactosa, sacarosa, maltosa y trehalosa), producción de gas y H2S, las cuales son recomendadas para la identificación de enterobacterias [4, 16, 19, 23, 40] siendo claves para la caracterización de aislados de M. morganii [13, 15, 43], y en virtud de que estos microorganismos presentan poca variabilidad fenotípica [13, 15], no se estila realizar comparaciones con cepas de referencia [13, 15, 43].
Una vez identificado el espécimen bacteriano, se procedió a realizar el montaje del ensayo de susceptibilidad a antimicrobianos según la técnica de Difusión en Disco [1, 7], aunque este método no es el más confiable, ha sido aprobado por el Grupo Ad hoc de expertos en resistencia a antimicrobianos de la OIE [41] realizando la selección de los antibióticos y la lectura e interpretación de los halos de susceptibilidad de acuerdo a los estándares del CLSI [8], tal y como se ha efectuado para M. morganii en otras investigaciones [15, 17, 43], tratando de evaluar en la medida de las disponibilidades, antibióticos de uso clínico, tanto en el campo de la medicina humana como en veterinaria [10, 29], por lo cual, se incluyeron fármacos como: ampicilina 10 μg (Himedia®, India), amoxicilina-ácido clavulánico 30 μg (BBL™, EUA), amikacina 30 μg (BBL™, EUA), ciprofloxacina 5 μg (Liofilchem®, Italia) [8, 28].
RESULTADOS Y DISCUSIÓN
En agar MacConckey se evidenciaron colonias redondas, de bordes lisos, elevadas, traslúcidas y de aproximadamente 1 mm de diámetro a las 24 y 48 h de incubación en las zonas de inoculación, descartando la posibilidad de contaminantes ambientales. La observación microscópica de los frotis teñidos mediante la tinción de Gram reveló cocobacilos Gram negativos, los cuales resultaron ser positivos a la prueba de catalasa y negativos a la reacción de oxidasa [9], de manera semejante a otras enterobacterias (Ej.: Proteus spp. y Providencia spp.), la cepa aislada no fermentó la lactosa, mostró motilidad y se evidenció la producción de fenilalanindesaminasa [33], además del resultado positivo a las pruebas de Rojo de Metilo y Ureasa [13, 15], siendo que la mayoría de los especímenes descritos de M. morganii son móviles [36].
Estos datos fenotípicos preliminares permitieron ubicar la bacteria aislada en el género Morganella, que al conjugarse con la información obtenida del resto de las pruebas bioquímicas (TABLA I), permitió finalmente identificarle como M. morganii subespecie morganii, especialmente por el resultado negativo a la fermentación de la trehalosa [10, 13, 15, 30], teniendo en especial consideración que los aislamientos de M. morganii presentan poca variabilidad fenotípica en los ensayos bioquímicos [13, 15].
COMPARACIÓN ENTRE LAS CARACTERISTICAS BIOQUIMICAS DE LA CEPA AISLADA Y LAS SUBESPECIES DE Morganella morganii
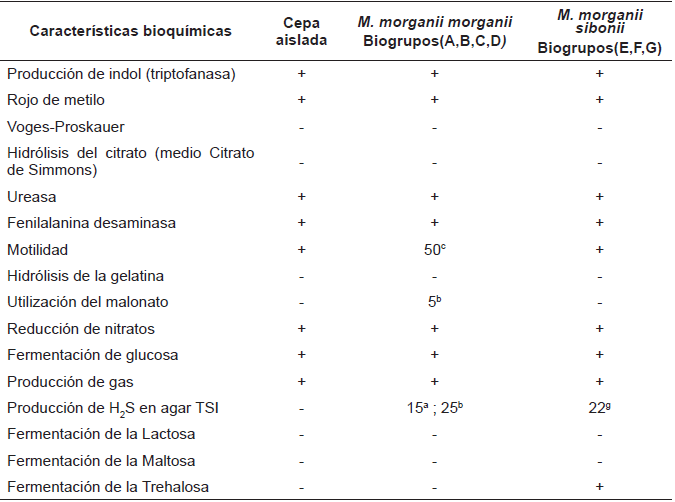
a,b,c,d,e,f,g Solo en el % de los aislamientos del biogrupo correspondiente. [13, 30].
El aislamiento resultó sensible a la amikacina y resistente a la ampicilina, la amoxicilina/ácido clavulánico y ciprofloxacina [35], coincidiendo con otros reportes de aislamiento de M. morganii en leche caprina [17], en casos clínicos humanos [5] y ensayos in vitro [28], mientras que otras fuentes describen la multiresistencia a varias familias de antimicrobianos [21, 43]. El perfil de resistencia observado en la cepa aislada en esta ocasión, permite inferir que probablemente se deba a la presencia de una β lactamasa de la familia AmpC codificada cromosómicamente [21], de manera semejante a lo descrito para Providencia spp. [30]. Todo esto deja claro la existencia de altos niveles de resistencia bacteriana a los antibióticos, lo cual podría atribuirse al uso indiscriminado que se ha dado a estos fármacos [5].
La presencia de microorganismos potencialmente patógenos en la leche de cabra, ya sea por mastitis subclínica o por contaminación secundaria durante su procesamiento, es un elemento de riesgo para la salud pública y animal, además de las conocidas implicaciones negativas en la producción de leche [26] y el impacto económico asociado [39], ya que genera cambios significativos en su composición y en el rendimiento de la producción láctea [34].
Adicionalmente, M. morganii ha sido aislada en insectos comunes en lecherías, considerando a los artrópodos como posibles vectores mecánicos que facilitarían la contaminación de los productos lácteos con importantes patógenos [12], sin embargo, esta bacteria ha sido reportada como causante de infecciones intramamarias subclínicas en cabras con una baja frecuencia [17]; ahora bien, su potencial riesgo a la salud humana queda en evidencia al relacionarse con casos de sepsis neonatal [5] y otros cuadros clínicos severos [21], recordando la idiosincrásica costumbre en ciertos hogares de usar la leche de cabra sin pasteurizar, como reemplazo de la lactancia materna [14,31] hecho tangible en las comunidades rurales falconianas y en otras zonas donde la cría caprina está ampliamente difundida.
Por otra parte, M. morganii está asociada a la generación de histamina en alimentos ricos en histidina que no han sido preservados adecuadamente, con la consecuente intoxicación alimentaria; este fenómeno ha sido relacionado principalmente con el consumo de ciertas especies de pescado [9,11,32] y en quesos de cabra [31], ya que este aminoácido es el octavo más abundante en la leche de cabra y alcanza concentraciones de hasta 0,45 mg/dL, más elevadas que las detectadas para la de ovinos (Ovis aries) [38].
CONCLUSIONES
Este es el primer reporte de M. morganii subespecie morganii aislada a partir de una muestra de leche de cabra criada bajo condiciones intensivas en el estado Falcón, por lo que se requiere profundizar en la identificación de los agentes etiológicos de los casos de mastitis clínica y subclínica en la región.
Las condiciones de la toma de muestra sugieren que M. morganii es el causante de la infección intramamaria subclínica, no obstante, esta bacteria ha sido implicada en la contaminación secundaria de la leche y subproductos lácteos.
El patrón de resistencia a los antibióticos observado en la cepa evaluada, guarda relación con los hallazgos de estudios previos, no obstante, es necesaria la evaluación constante de los patrones de resistencia a los antimicrobianos en las diferentes cepas bacterianas aisladas a nivel de campo en diversos procesos infecciosos.
Agradecimientos
Especial agradecimiento al personal obrero que labora en el laboratorio de Microbiología Veterinaria del Programa de Ciencias Veterinarias de la Universidad Nacional Experimental “Francisco de Miranda”, por la colaboración prestada en la ejecución de esta investigación.
Referencias
[1] BARRY, A.L.; THORNSBERRY, C. Susceptibily tests: diffusion test procedures. En: Leanette, E.H.; Balows, A.; Hausler, W.J.; Shadomy, H.J. (Eds.). Manual of Clinical Microbiology. 4th Ed. American Society for Microbiology. Washington D.C. EUA. Pp 978-987. 1985.
[2] BAYLIS, C.; UYTTENDAELE, M.; JOOSTEN, H.; DAVIES, A. The enterobacteriaceae and their significance to the food industry. International Life Sciences Institute, Europe. Belgium. 48 pp. 2011.
[3] BAZAN, R.; CERVANTES, E.; SALAS, G.; SEGURACORREA, J. Prevalencia de mastitis subclínica en cabras lecheras en Michoacán, México. Rev.Cientif. FCV-LUZ XIX (4): 334 -338. 2009.
[4] CARTER, M.E.; CHENGAPPA, M.M. Enterobacteria. En: Carter, G.R.; Cole, J.R. (Eds.) Diagnostic Procedures in Veterinarian Bacteriology and Micology. 5th Ed. Academic Press. Pp 107 – 128. 1990.
[5] CHANG, H.Y.; WANG, S.M.; CHIU, N.C.; CHUNG, H.Y.; WANG, H.K. Neonatal Morganella morganii sepsis: a case report and review of the literature. Ped. Internat. 53:121- 123. 2011.
[6] CLAVIJO, A.; MELENDEZ, B.; CLAVIJO, M.; GODOY, A.; SANTANDER, J. Efecto del sistema de explotación sobre la aparición de mastitis caprina en dos fincas del estado Falcón, sus agentes etiológicos y la resistencia a antimicrobianos. Zoot. Trop. 20 (3): 383-395. 2003.
[7] CLINICAL AND LABORATORY STANDARDS INSTITUTE (CLSI). Performance Standards for Antimicrobial Susceptibility Testing: Sixteenth Informational Supplement. CLSI document M100-S16. 26 (3). Clinical and Laboratory Standards Institute, Wayne, Pennsylvania. 182 pp. 2006.
[8] CLINICAL AND LABORATORY STANDARDS INSTITUTE (CLSI). Performance Standards for Antimicrobial Disk Susceptibility Tests Approved Standard. CLSI document M100-S21. 31 (1). Clinical and Laboratory Standards Institute, Wayne, Pennsylvania. 165 pp. 2011.
[9] EMBORG, J.; DALGAARD, P.; AHRENS, P. Morganella psychrotolerans sp. nov., a histamine producing bacterium isolated from various seafoods. Internat. J. of Systemat. and Evolut. Microbiol. 56: 2473–2479. 2006.
[10] FRANKLIN, A.; ACAR, J.; ANTHONY, F.; GUPTA, R.; NICHOLLS, T.; TAMURA, Y.; THOMPSON, S.; THRELFALL, E.J.; VOSE, D.; VAN VUUREN, M.; WHITE, D.G.; WEGENER, H.C.; COSTARRICA, M.L. Antimicrobial resistence: harmonisation of national antimicrobial resistance monitoring and surveillance programmes in animals and in animal derived food. Rev. Sci. Tech. Off Int. Epiz. 20: 859 - 870. 2001.
[11] GARCÍA-TAPIA, G.; BARBA-QUINTERO, G.; GALLEGOSINFANTE, J.A.; PACHECO A., R.; RUÍZ-CORTÉS, J.A.; RAMÍREZ, J.A. Influence of physical damage and freezing on histamine concentration and microbiological quality of yellowfin tuna during processing. Food Sci. and Tech. 33:463-467. 2013.
[12] IPINZA-REGLA, J.; GONZALEZ, D.; FIGUEROA, G. Hormiga argentina Linepithema humile Mayr, 1868 (Hymenoptera: Formicidae) y su rol como posible vector de contaminación microbiana en una lechería de cabras Capra hircus Linnaeus, 1758 (Artiodactyla: Bovidae) Arch. Med. Vet. 47: 317-323. 2015.
[13] JANDA, J.M.; ABBOTT, S.L.; KHASHE, S.; ROBIN, T. Biochemical Investigations of Biogrups and Subspecies of Morganella morganii. J. of Clin. Microbiol. 34:108-113. 1996.
[14] JANDAL, J.M. Comparative aspects of goat and sheep milk. Small Rum. Res. 22:177-185. 1996.
[15] JENSEN, K.T.; FREDERIKSEN, W.; HICKMAN-BRENNER, F.W.; STEIGERWALT, A.G.; RIDDLE, C.F.; BRENNER, D.J. Recognition of Morganella Subspecies, with Proposal of Morganella morganii subsp. morganii subsp. nov. and Morganella morganii subsp. sibonii subsp. nov. Internat. J. of Systemat. Bacteriol.. 42:613-620. 1992.
[16] KELLY, M.T.; BRENNER, D.J.; FARMER III, J.J. Enterobacteriaceae. En: Leanette, E.H.; Balows, A.; Hausler, W.J.; Shadomy, H.J. (Eds.) Manual of clinical Microbiology, 4th Ed. American Society for Microbiology. Washington. Pp 263-277. 1985.
[17] KIM, H.; JUNG, J.; KIM, S.; PARK, J.; CHO, I.; SHIN, S.; SON, C.; OK, K.; HUR, T.; JUNG, Y.; CHOI, C.; SUH, G. Isolation and antimicrobial susceptibility of microorganisms from milk samples of dairy goat. Kor. J. of Vet. Serv. 35:295-305. 2012.
[18] KLINGER, I.; ROSENTHAL, I. Public health and the safety of milk and milk products from sheep and goats. Rev. Sci. Tech. Off. Int. Epiz. 16 (2): 482-488.1997.
[19] KONEMAN, E.W.; ALLEN, S.D.; JANDA, W.M.; SCHRECKENBERGER, P.C. WINN, W.C. Diagnóstico microbiológico Texto y Atlas a Color. Médica Panamericana, Argentina, 900 pp. 1999.
[20] LEON-SILVA, G.A. Tipos y subtipos climáticos de Venezuela. Universidad de Los Andes, Facultad de Ciencias Forestales y Ambientales, Escuela de Geografía. Trabajo de ascenso. 41pp. 2010.
[21] LIN, T.Y.; CHAN, M.C.; YANG, Y.S.; LEE, Y.; YEH, K.M.; LIN, J.C.; CHANG, F.Y. Clinical manifestations and prognostic factors of Morganella morganii bacteremia. Eur. J. Clin. Microbiol. Infect. Dis. 34:231-236. 2015.
[22] LITTERIO, N.J. Estudio farmacocinético-farmacodinámico de la cefquinoma en cabras en función de la edad, la gestación y la lactancia. Universidad Complutense de Madrid, Facultad de Veterinaria, Departamento de Toxicología y Farmacología. Tesis Doctoral. 210 pp. 2013.
[23] MAC FADDIN, J. Pruebas bioquímicas para la identificación de bacterias de importancia clínica. 3era edic. Editorial Medica Panamericana, Mexico, 850 pp. 2003.
[24] MARTINEZ-HERRERA, D.I.; ABELEDO, M.A.; LARAGUTIERREZ, A.; PENICHE-CARDEÑA, A.; ROBLEDOSALINAS, M.L.; PULIDO-CAMARILLO, E.; ROSASSASTRE, J.; FLORES-CASTRO, R. Evaluación de métodos de cultivo para el aislamiento Primario de Brucella melitensis a partir de leche de cabras. Rev. Salud Anim. 31 (3): 164-169. 2009.
[25] MBINDYO, C.M.; CITAO, C.G.; BEBORA, L. A crosssectional study on the prevalence of subclinical mastitis and antimicrobial susceptibility patterns of the bacterial isolates in milk samples of smallholder dairy goats in Kenya. Amer. J. of Res. Commun. 2(8): 30-51. 2014.
[26] MICHELOUD, J.F.; NEDER, V.; NUOVO, F.; SUAREZ, V.H., CALVINHO, L. Brote de mastitis clínica por Corynebacterium spp. y Streptococcus dysgalactiae en cabras en Salta, Argentina. Rev. Inv. Agrop. 40 (1): 34- 37. 2014.
[27] NAJEEB, M.F.; ANJUM, A.A.; AHMAD, M.U.D.; KHAN, H.M.; ALI, M.A.; SATTAR, M.M.K. Bacterial etiology of subclinical mastitis in dairy goats and multiple drug resistance of the isolates. J. Anim. Plant. Sci. 23(6): 1541 – 1544. 2013.
[28] NAVARRO-RISUEÑO, F.; MIRÓ-CARDONA, E.; MIRELISOTERO, B. Lectura interpretada del antibiograma de enterobacterias. Enferm. Infecc. Microbiol. Clin. 20 (5): 225-234. 2002.
[29] OFICINA INTERNACIONAL DE EPIZOOTIAS (OIE). Armonización de los Programas de vigilancia y Seguimiento de la Resistencia a los Antimicrobianos. 2011 En: Código Sanitario para los Animales Terrestres. 20ma Ed. En: http: www.oie.int/es.normas-internacionales/codigo-terrestre/ 19-08-2015.
[30] O´HARA,C.; BRENNER, F.; MILLER, M. Classification, Identification, and Clinical Significance of Proteus, Providencia, and Morganella. Clin. Microbiol. Rev. 23: (4): 234 – 546. 2000.
[31] PARK, Y.W.; HAENLEIN, G.F.W. Therapeutic and Hypoallergenic Values of Goat Milk and Implication of Food Allergy, En: Park, Y.W.; Haenlein, G.F.W (Eds.) Handbook of Milk of Non-Bovine Mammals. Blackwell Publishing Company, Iowa. Pp 121-135. 2006.
[32] PODEUR, G.; DALGAARD, P.; LEROI, F.; PRÉVOST, H.; EMBORG, J.; MARTINUSSEN, J.; HANSEN, L.H.; PILET, M. Development of a real-time PCR method coupled with a selective pre-enrichment step for quantification of Morganella morganii and Morganella psychrotolerans in fish products. Internat. J. of Food Microbiol.. 203:55-62. 2015.
[33] PUERTA-GARCIA, A.; MATEOS-RODRIGUEZ, F. Enterobacterias. Medicine 10(51): 3426 - 3431. 2010.
[34] ROBERTSON, N.H.; MULLER, C.J.C. Somatic cell count in goat’s milk as an indication of mastitis. SA. Anim. Sci. 6: 1-6. 2005.
[35] ROJAS, L.; VINUESA, T.; TUBAU, F.; TRUCHERO, C.; BENZ, R.; VIÑAS, M. Integron presence in a multiresistant Morganella morganii isolate. Int. J. Antimicrob. Agents. 27(6): 505-512. 2006.
[36] SENIOR, B.W.; VOROS, S. Protein profile typing-a new method of typing Morganella morganii strains, J. Med. Microbiol. 33: 259-264.1990.
[37] STUHR, T.; AULRICH, K. Intramammary infections in dairy goats: recent knowledge and indicators for detection of subclinical mastitis. Agricult. and Forestry Res. 4 (60): 267-280. 2010.
[38] TAMINE, A.Y.; DEETH, H.C. Amino acid composition in milk and yogurt of different species. J. Food Prot. 43:939- 943.1980.
[39] TOMITA, G.M.; HART, S.P. The mastitis problem. Proc. 16th Ann. Goat Field Day. Langston University, Langston, Oklahoma. Pp 6-9. 2001.
[40] VALENZUELA, M.; ASTORGA, J. Tablas TLM para identificación de Enterobacterias. Departamento de Laboratorio de Salud, Instituto de Salud Pública de Chile. Santiago de Chile. 28 pp. 1991.
[41] WHITE, D.G.; ACAR, J.; ANTHONY, F.; FRANKLIN, A.; GUPTA, R.; NICHOLSS, T.; TAMURA, Y.; THOMPSON, S.; THRELFALL, E.J.; BOSE, V.; VAN VUUREN, N.; WEGENER, H.C.; COSTARRICA, M.L. Antimicrobial resistence: Standardization and harmonization of laboratory methodologies for the detection and quantification of antimicrobial resistance. Rev. Sci. Tech. Off. Int. Epiz. 20: 849-858. 2001.
[42] WHITE, E. The prevalence of mastitis in small ruminants and the effect of mastitis on small ruminant production. NMC 46th Annual Meeting Proceedings. San Antonio, 01/ 21-24. Texas, EUA. Pp 119 - 127. 2007.
[43] ZHAO, C.; TANG, N.; WU, Y.; ZHANG, Y.; WU, Z.; LI, W.; QIN, X.; ZHAO, J.; ZHANG, G. First reported fatal Morganella morganii infections in chickens. Vet. Microbiol. 156: 452–455. 2012.
Notas de autor
veco1982@hotmail.com
