Recepción: 13/10/16
Aprobación: 21/01/17
Resumen: Para determinar el efecto de incluir semillas de Linaza (Linum usitatissimum L.) y Chía (Salvia hispanica L.) como fuente de Ácidos Grasos Esenciales (AGEs [omega n3, n6]) en dietas para codorniz japonesa (Coturnix coturnix japonica) sobre el desempeño productivo, reproductivo y perfil de AG en yema de huevo, se utilizaron 120 aves (100 hembras; 20 machos) de siete semanas de edad, alojadas en 10 jaulas durante once semanas. Las codornices de cinco jaulas se asignaron al azar a los tratamientos: Grupo I) Dieta a base de maíz y harina de soja, con 20% de PC y 2,9 Mcal kg-1 de EM (Testigo). Grupo II) Dieta testigo más 1,86% de semillas de linaza y 0,10% de chía, con 21% de PC y 3,096 Mcal kg-1 de EM. Se registró el consumo de alimento por codorniz, porcentaje de postura, alimento consumido por pollito nacido viable, incubabilidad, fertilidad, mortalidad embrionaria y AG en yema. Los resultados no mostraron diferencia significativa (P≥ 0,05) en consumo de alimento (34,56 g por codorniz), postura (80,73%) y huevo para incubar (65,48%). Las codornices del grupo II consumieron menos alimento (16 g) por pollito nacido, tuvieron 5,52% más huevos fértiles, de los que nacieron 3,48% más pollitos, con 3,61% menor mortalidad embrionaria (P≤ 0,01). La inclusión de semillas de linaza y chía, aumentó en la yema 2,96% los AG Poliinsaturados (AGP), y redujo a 7,39:1 la relación n6/n3, y a 0,5:1 la relación de AG Saturados (AGS)/AGP (P≤ 0,05). Se concluye que la inclusión de semillas de linaza y chía como fuente de AGEs disminuye el consumo de alimento por pollito nacido, la relación de omegas n6/n3 y AGS/AGP en yema de huevo, y mejora la incubabilidad, fertilidad y mortalidad embrionaria en huevos de codorniz japonesa.
Palabras clave: Linum usitatissimum L, Salvia hispanica L, AGEs, incubabilidad, fertilidad.
Abstract: To determine the effect of including flax (Linum usitatissimum L.) and chia (Salvia hispanica L.) seed as a source of Essential Fatty Acids (EFAs [omega n3, n6]) in Japanese quail (Coturnix coturnix japonica) diets on productive, reproductive performance and FA profile in egg yolk, 100 females and 20 males seven-week of age were used and housed in 10 cages for eleven weeks. The quails were randomized one of two treatments: Group I) Received a diet based on corn and soybean meal, with 20% CP and 2.9 Mcal kg-1 ME (control). Group II) Received control diet plus 1.86% flax and chia 0.10% seed, with 21% CP and 3.096 Mcal kg-1 ME. Feed intake, egg laying rate, feed consumed per viable chick born, hatchability, fertility, embryo mortality and FA in yolk was measured. The results showed no significant differences (P≥ 0.05) in feed intake (34.56 g quail), egg laying (80.73%) and hatching eggs (65.48%). Quails in Group II consumed less feed (16 g) per chick born, had 5.52% more fertile eggs, from which 3.48% more chicks were born, with 3.61% lower embryonic mortality (P≤ 0.01). The inclusion of flax and chia seeds, increased 2.96% polyunsaturated FAs (PUFA) in yolk, and reduced to 7.39:1 the n6/n3 ratio, and to 0.5:1 the ratio of saturated fatty acids (SFA)/PUFA) (P≤ 0.05). It is concluded that the inclusion flax and chia seed as a source of EFAs decreases feed intake per chick born, the ratio of omegas n6/n3 and SFA/PUFA in egg yolk, and improves hatchability, fertility and embryo mortality in Japanese quail eggs.
Keywords: Linum usitatissimum L, Salvia hispanica L, EFAs, hatchability, fertility.
INTRODUCCIÓN
Las fuentes de lípidos en las dietas para gallinas (Gallus gallus domesticus) productoras de huevo para plato modifican el perfil de ácidos grasos (AG) en la yema de huevo [18]. Los AG son precursores de los ácidos grasos esenciales (AGEs), el omega-3 (n3) y el omega-6 (n6); éstos a su vez, regulan genes que codifican las proteínas implicadas en el metabolismo lipídico, energético e inmunidad innata y adquirida [13], ya que son precursores para la síntesis de eicosanoides, compuestos similares a hormonas que regulan la inflamación. La cantidad y proporción de AGEs presente en las membranas es determinante para el tipo de eicosanoide que se generará. La reducción de ácido araquidónico (AA) en relación con el ácido docosapentaenoico (DPA un n3) es importante, porque DPA promueve la producción de resolvinas que compite con la eicosanoide pro inflamatorio prostaglandina E2 (PGE2) por la actividad de la enzima ciclooxigenasa, la cual inhibe la apoptosis e induce la proliferación celular y la angiogénesis [25]. El AA es el de mayor disponibilidad en una dieta típica, fuente de eicosanoides, con efectos pro inflamatorios, además liberan radicales libres causantes de daños a la membrana celular [27]. Los AG de la yema representan más del 90% del total de los requerimientos energéticos para el desarrollo y síntesis estructural de membranas del embrión de las aves [14]; sin embargo, los AGEs contenidos en el huevo afectan la composición de las membranas celulares embrionarias durante su crecimiento y desarrollo [27]. Los vasos sanguíneos extraembrionarios o vitelinos se desarrollan en las membranas extraembrionarias sobre el vitelo, que transportan nutrientes entre el saco vitelino y el embrión, necesarios para su desarrollo, también son afectados por éstos [13]. Un factor que interviene en la dinámica de crecimiento vascular son los AGE y sus derivados, de los cuales no hay suficiente información. El pescado es la fuente más importante de AGE n3 en la dieta humana, rico en ácido eicosapentaenoico (EPA) y docosahexaenoico (DHA); otra fuente de AGEs son las semillas de oleaginosas, especialmente linaza (Linum usitatissimum L.), que contiene un alto nivel (50 a 55%) de ácido linolénico (ALA) [8]. Además, las dietas elaboradas con aceite de linaza, disminuyen significativamente el contenido de AG n6 y con esto la proporción n6/n3 [18]. Otra fuente es la semilla de chía (Salvia hispanica L.) [6], que se caracteriza por un alto contenido de nutrientes, como: 23,60% de proteínas, carbohidratos 18,6%, lípidos 29,8% [5], dentro de ellos el contenido de ácido linoleico n6 (AL) es de 19% y de ALA en 63,8, clasificado éste último como n3; la semilla de chía, lo contiene más que otras fuentes, como algas (Cryptheconium spp., Mortierella spp., Schizochytrim spp.), arenque (Clupea spp.) y salmón (Salmo spp.) [6]; los aceites de uso común como oliva (Olea europea), cártamo (Carthamus tinctorius), soja (Glycine max), maíz (Zea mays) y canola (Brassica napus), no destacan por su contenido de n3, ya que ninguno supera el 9% [24]. El aceite de linaza tiene 57,5% de ALA; además es una fuente de Ca, P, Mg, Fe, K, Zn y Cu. La fracción fibrosa de la semilla de chía tiene capacidad antioxidante comparable con el vino, té (Camellia sinensis), café (Coffea spp.) y jugo de naranja (Citrus sinensis) [5]. Se ha observado que la adición de aceites ricos en AGEs n3, provenientes de linaza y de pescado (Hypophthalmichthys molitrix) en la dieta de machos de codorniz (Coturnix coturnix japonica), mejoraron el volumen de eyaculado, concentración espermática, espermatozoides vivos totales, espermatozoides vivos normales, en comparación con aceite de girasol (Helianthus annuus) o maíz, sugiriendo que la inclusión de aceite de pescado y linaza en las dietas mejora el rendimiento reproductivo de machos de codorniz [2].
Al alimentar gallinas de postura con maíz y soja, los ácidos grasos saturados (AGS) encontrados en la yema de huevo, fueron el palmítico y el esteárico [24]. En estudios llevados a cabo en ratones de laboratorio (Mus musculus) y en humanos, en los que se evaluó el desarrollo del sistema nervioso, aprendizaje, sueño y niveles de colesterol, los resultados muestran que la alimentación correcta debe proporcionar n6/n3 en una relación 4:1 hasta 1:1 [26]. De tal manera que los n3 y n6 son fundamentales para el organismo humano ya que se absorben siguiendo una proporción de equilibrio. Con base en lo anterior, el objetivo del presente estudio fue determinar el efecto de incluir semillas de Linaza (Linum usitatissimum L.) y Chía (Salvia hispanica L.) como fuente de AGEs sobre el desempeño productivo, reproductivo y perfil de AG en yema de huevo de codorniz japonesa.
MATERIALES Y MÉTODOS
Lugar de trabajo
El experimento se realizó en la Unidad Avícola de la Facultad de Medicina Veterinaria y Zootecnia de la Universidad Autónoma de Sinaloa, en Culiacán, Sinaloa, México (24o 46’ 13’’ LN y 107o 21’ 14’’ LO). La región se caracteriza por tener un clima BS1 (h’) w(w)(e), el cual se define como clima semiseco, muy cálido, con lluvias en verano, según la clasificación de Köppen y modificada por García [16]; con temperatura promedio anual de 25,9ºC, máxima de 30,4ºC en junio y julio, y mínima de 20,6ºC en enero; la humedad relativa promedio es de 68%, con máxima de 81% en septiembre y mínima de 51% en abril; la precipitación anual promedio es de 688,5 mm [7].
Animales y manejo
Se utilizaron 100 hembras y 20 machos de codorniz japonesa de siete semanas de edad; las aves se alojaron en 10 jaulas (60x50x20 cm) en batería dentro de una caseta convencional; durante el experimento, la temperatura ambiental promedio de la caseta fue de 22±2ºC, y se manejó un programa de luz (14 L:10 O). Las codornices de cinco jaulas (250 cm2/codorniz) se asignaron al azar a uno de dos tratamientos (TABLA I): Grupo I. Dieta testigo a base de maíz y harina de soja, (20,06% de proteína cruda (PC) y 2,935 Mcal kg-1). Grupo II. Dieta similar a la testigo adicionada con 1,86% semilla de Linaza más 0,10% semilla de Chía, (21% PC y 3,096 Mcal Kg-1), formulada según las recomendaciones de National Research Council [22], con valores para Proteína Cruda y Extracto Etéreo obtenidos del Análisis Químico Proximal [19], y energía calculada con la ecuación propuesta por Moir y col. [21]. La TABLA II presenta los contenidos calculados de AGEs en alimento en función de la composición química de las materias primas mostradas en investigaciones anteriores [1, 5, 10, 17]. El alimento se proporcionó ad libitum en forma de harina, al finalizar cada semana (sem) se calculó el consumo de alimento por ave, el número y peso del huevo se registraron diariamente; con esta información se calculó el porcentaje de postura y el consumo de alimento por codorniz.
La colección de huevo para incubar se inició a partir de que las codornices alcanzaron las nueve sem de edad; la incubación se realizó una vez por sem durante nueve sem (Huacuja®; Modelo 1020; Guadalajara, Jalisco, México). Los criterios para seleccionar el huevo para incubar se basaron en el peso (12 a 16 g), de forma ovoide, buena consistencia y color del cascarón. Éste se almacenó de 12 a 18°C durante 7 días (d) (Refrigerador Nieto®; Modelo Critotec CFX-8; Guadalajara, Jalisco, México), y antes de cada incubación el huevo se atemperó 3 horas (h); a 22±1,05°C, y se desinfectó con peroximonosulfato de potasio 21,41%, cloruro de sodio 1,50%, otros ingredientes 77,09% (Virkon®), a una dosis 1:50.
COMPOSICIÓN Y APORTE NUTRIMENTAL CALCULADO DE LAS DIETAS EXPERIMENTALES
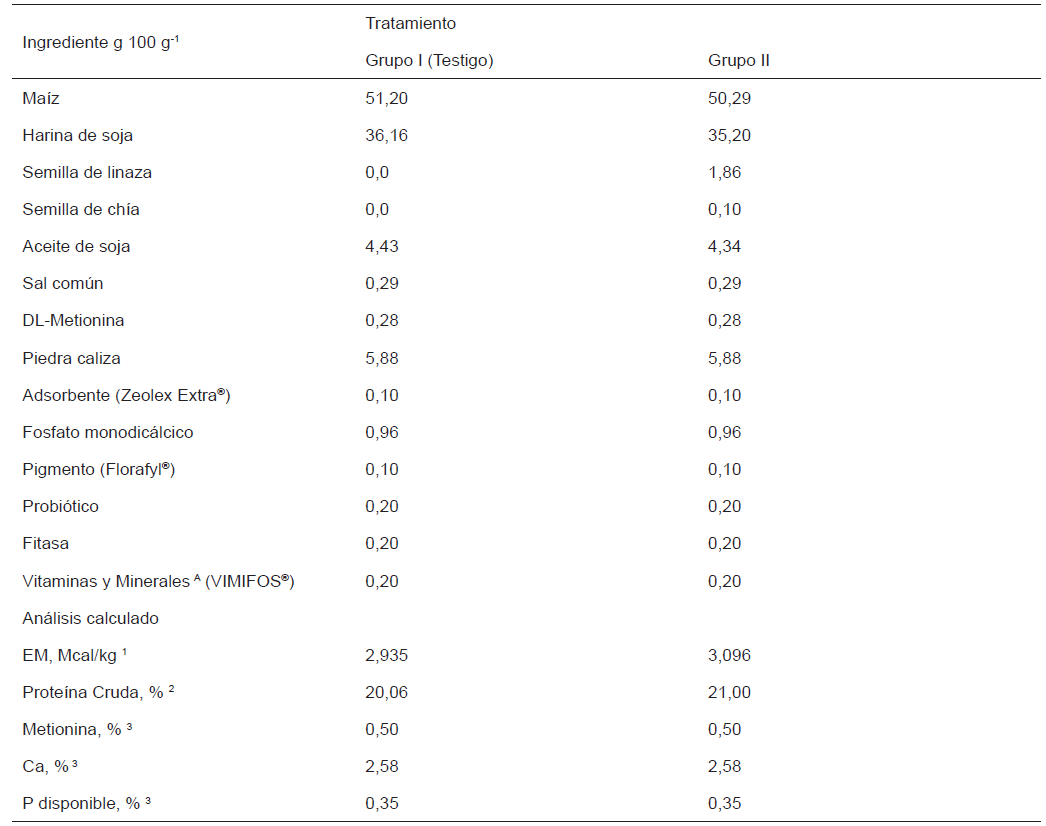
A Premezcla de vitaminas y minerales proporciona por kg de dieta: 3,75 mg de retinol; 112 μg colecalciferol; 30 mg acetato tocoferol; 3 mg bisulfuro sódico; 1,5 mg tiamina; 3 mg piridoxina; 15 μg cianocobalamina; 1,5 mg ácido fólico; 55 mg Ca pantotenato; 180 μg biotina; 600 mg de colina; 75 mg Mn; 75 mg de Zn; 75 mg de Fe; 900 μg Mo; 750 μg Co; 1,6 mg de Cu; 105 μg Se; 120 mg Banox (BTA+BHT). 1 Valores calculados por ecuación. 2Análisis Químico Proximal. 3 Valores calculados de tablas.
PERFIL DE ÁCIDOS GRASOS DE LAS DIETAS EXPERIMENTALES (COMO % DEL TOTAL DE LÍPIDOS)
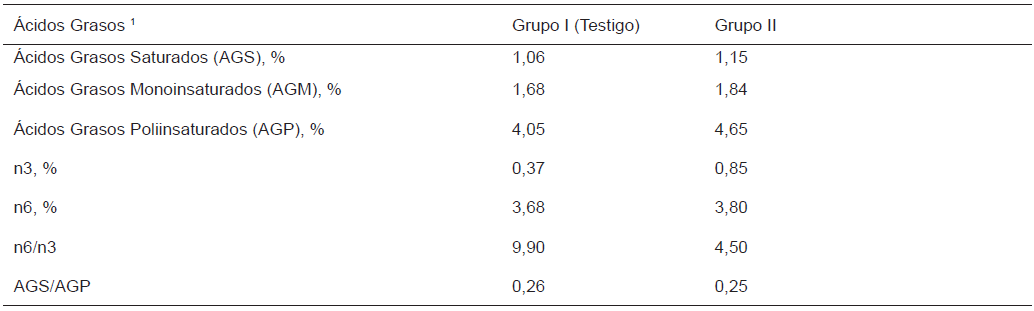
1Valores calculados en función de la composición química teórica de las materias primas. La incubación se llevó a cabo en un equipo automático, con volteo cada 2 h, calibrada a 37,7±1°C y 50 a 60% de humedad relativa. A los 14 d, los huevos se transfirieron a nacedora (Huacuja®; Modelo 1200; Guadalajara, Jalisco, México).
La incubabilidad se determinó como la razón de pollitos de codorniz nacidos del total de huevos fértiles, los pollitos se retiraron de la nacedora a partir de 12 h de iniciada la eclosión y se registró el peso individual. Los huevos no eclosionados al d 18 de la incubación fueron abiertos, y la fertilidad y mortalidad embrionaria se determinó bajo los siguientes criterios: Muerte embrionaria temprana: Embriones que mostraron primeros signos de desarrollo caracterizado por el desarrollo del ojo, con ausencia de yemas en las extremidades; Muerte embrionaria intermedia: Embriones que mostraron las extremidades desarrolladas; Muerte embrionaria tardía: Embriones que mostraron presencia de plumas; pollos que picaron y no nacieron: Huevos que mostraron signos de ruptura por fuerza interna al d 18, independientemente de si el pollito este vivo o muerto [11]. Se consideró huevo no fértil tomando como referencia macroscópica la presencia de una zona transparente y zona opaca en la yema [11]. La fertilidad se calculó como la razón de los pollitos nacidos más los que desarrollaron embrión no viable hasta los 18 d de incubación, y el total de huevos incubados. A los d 28; 56 y 62 del experimento se colectaron huevos por tratamiento, los que se mantuvieron en congelación (Congelador Polar®; Modelo CH- 7; Guadalupe Nuevo León, México) hasta la determinación del perfil de AG, en el laboratorio los lípidos totales se extrajeron con una mezcla de cloroformo, metanol y agua de acuerdo con la técnica de Folch [15], bajo atmósfera de nitrógeno. Cada muestra fue procesada por triplicado y la conversión de los AG en metil ésteres se llevó a cabo con NaOH y BF3 metanólico al 14%, según el método 969,33 de la Association International of Oficial Analytical Chemists Methods of Análisis (AOAC) [3]. Los metil ésteres disueltos en hexano se analizaron con un cromatógrafo de gases (Agilent®; Modelo 7820; EUA), equipado con una columna capilar de 30 m de largo, 0,32 mm de diámetro interno (Omegawax 320) y un detector de ionización de llama. Para la cuantificación se utilizaron estándares de metil ésteres de AG de 99% de pureza (Supelco®; Lipid Standard C4-C24; EUA).
Análisis estadístico
El análisis de los resultados de respuesta productiva se realizó bajo el modelo para un diseño experimental totalmente al azar con un factor nido (dieta) y un factor cruzado (semana), donde la unidad experimental fue la jaula con 10 codornices, con cinco réplicas por tratamiento, para ello se utilizó el procedimiento para modelos mixtos (Proc MIXED) de SAS [28], donde la jaula se declaró como efecto aleatorio y se consideraron varianzas heterogéneas, la comparación de medias se hizo con la prueba de Tukey-Cramer. Los resultados de AG se analizaron con la prueba t de Student para muestras independientes, previa prueba de Fisher del análisis de la razón de las varianzas [29], donde la unidad experimental fue cada yema de huevo, con tres réplicas por tratamiento. Las proporciones de incubabilidad, fertilidad y mortalidad embrionaria se analizaron con la prueba de Ji cuadrado [29]. El nivel de alfa máximo para aceptar diferencia estadística fue 0,05.
RESULTADOS Y DISCUSIÓN
Respuesta productiva
Los resultados de respuesta productiva se presentan en la TABLA III. La inclusión de semilla de linaza y chía no afectó el alimento consumido (34,56 g), postura (80,73%) y huevo para incubar (65,48%). El consumo de alimento es similar al observado por Al-Daraji [1] al alimentar codornices con 3% de alguno de los aceites de girasol, linaza maíz y pescado (34,71 g). Así mismo, el consumo estimado de energía y proteína diario por ave solo difirió 4,87 cal y 0,38 g, respectivamente (TABLA III). El porcentaje de postura fue similar al reportado por Ayerza y col. [6] al incluir semilla de linaza (3 a 5%) y de chía (7 a 14%) en la dieta de gallinas, con un 74%. El grupo II consumió menos alimento (16 g) por pollito nacido. El efecto significativo (P≤ 0,03) para porcentaje de postura, o cercano a la significancia (P= 0,07) en alimento consumido por huevo para incubar, para la fuente de variación de sem, en ambos casos, es el resultado lógico a esperar, ya que la producción de huevos aumenta en el tiempo, independientemente de las dietas y el alimento consumido por huevo incubado.
RESPUESTA PRODUCTIVA DE CODORNIZ JAPONESA CON INCLUSIÓN DE SEMILLA DE LINAZA Y CHÍA EN EL ALIMENTO
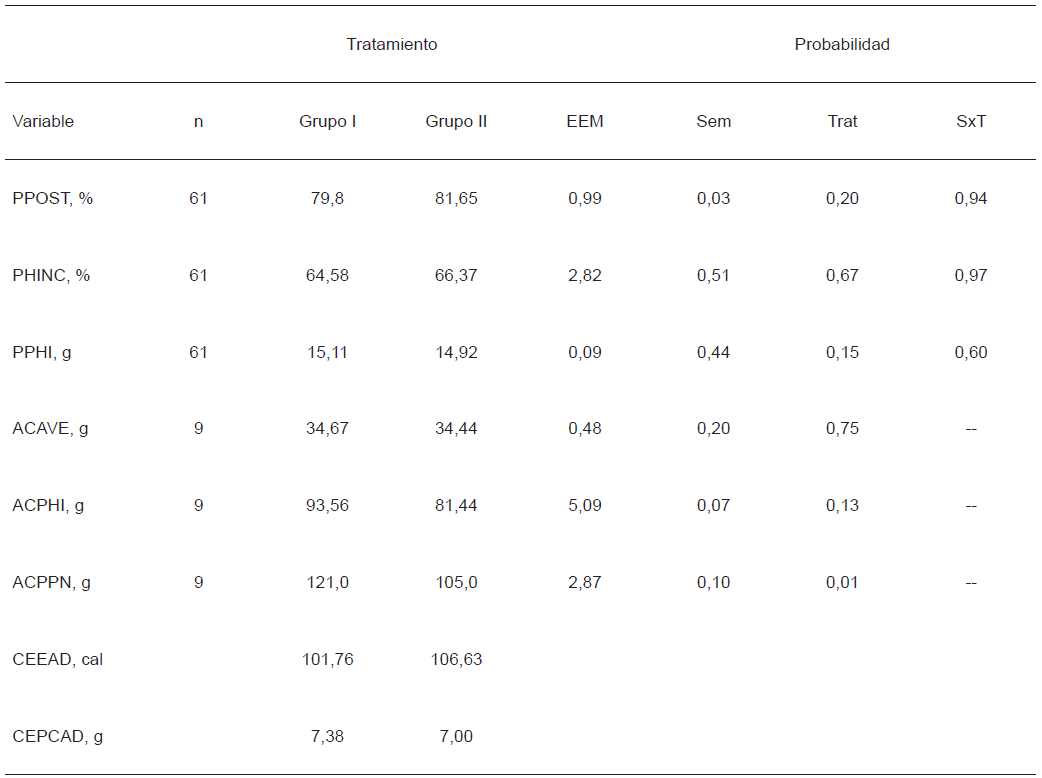
PPOST: Porcentaje de postura, PHINC: Porcentaje de huevo incubable, PPHI: Peso promedio de huevo para incubar, ACAVE: Alimento consumido por ave, ACPHI: Alimento consumido por huevo para incubar, ACPPN: Alimento consumido por pollito nacido, CEEAD: Consumo estimado de energía por ave por día, CEPCAD: Consumo estimado de proteína cruda por ave por día, EEM: Error estándar de la media, Sem: Semana, Trat: Tratamiento, SxT: Interacción semana por tratamiento.
Perfil de ácidos grasos
Los resultados del perfil de AG en la yema de huevo se muestran en la TABLA IV. En el grupo de semillas de Linaza y Chía, para algunos AG el equipo no detectó elevaciones en el cromatograma. Los AG Cis-8,11,14-eicosatrienoico (C20:5 n3), Cis-13,16-docosadienoico (C22:2), Cis-4,7,10,13,16,19- docosahexaenoico (C22:6 n3), aumentaron su concentración (P≤ 0,01), en 7,88; 70 y 3,55%, respectivamente, esto contribuyó a un 15,85% más (P≤ 0,01) de AGP; así mismo, la proporción de AGS fue menor (P≤ 0,01) en 11,26%, por lo tanto la relación AGS/AGP fue menor en 1,43, y la proporción de n3 y n6 fue mayor (P≤ 0,01) en 2,96 y 13,00%, respectivamente; y la relación n6/n3 fue en 9,51 más estrecha (P≤ 0,01). Estos resultados concuerdan con los observados por Cherian [9] en huevo de gallinas reproductoras alimentadas con AGP n3, donde el ácido docosahexaenoico (DHA) se incrementó, y la relación n6/n3 fue más estrecha.
PERFIL DE ÁCIDOS GRASOS EN YEMA DE HUEVO CRUDO DE CODORNIZ JAPONESA CON INCLUSIÓN DE SEMILLA DE LINAZA Y CHÍA EN EL ALIMENTO (COMO % DEL TOTAL DE LÍPIDOS)
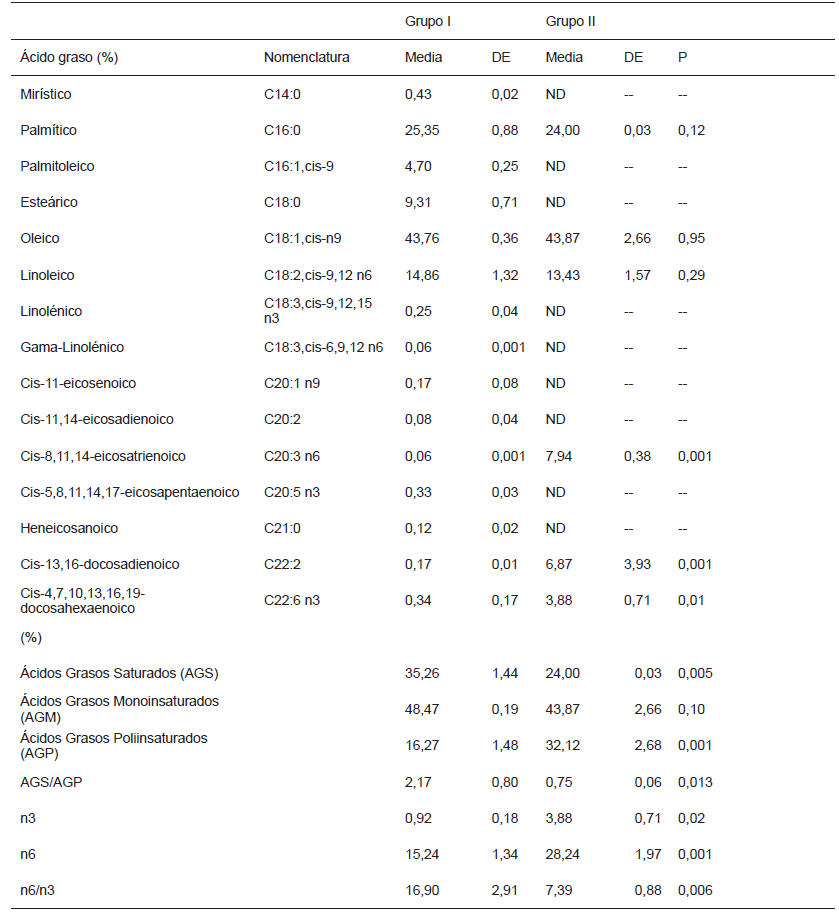
ND: Niveles no detectables, AGS: Ácidos grasos saturados, AGP: Ácidos grasos poliinsaturados, DE: Desviación estándar de 3 muestras, P: Probabilidad.
Respuesta reproductiva
Los resultados para respuesta reproductiva se presentan en la TABLA V. Incluir semilla de linaza y chía mejoró (P≤ 0,01) la incubabilidad en 3,48% más pollitos nacidos viables y 5,52% más huevos fértiles con respecto al total de huevos transferidos. Resultados similares se obtuvieron al utilizar aceite de linaza o maíz, logrando 3,19 y 4,4% más en fertilidad e incubabilidad, respectivamente [1], esto se puede deber al beneficio que aportan los AGE, ya que estudios realizados con machos de codornices que consumieron dietas que contenían 3% de aceite de pescado mostraron mejora en el volumen y motilidad espermática [2], además éstos mejoran la flexibilidad de látigo del espermatozoide [30]. Los resultados de mortalidad embrionaria se muestran en la TABLA VI. La inclusión de semilla disminuyó (P≤ 0,01) la mortalidad embrionaria total en 3,61%, y esta se atribuye a la menor mortalidad (P≤ 0,01) en la etapa tardía (2,68%). La mejor respuesta en incubabilidad, fertilidad y mortalidad embrionaria se puede atribuir al efecto de la relación de AGS/AGP de 1,42 y AGEs n6/n3 de 39,51, más amplia para el grupo I. Dietas donde la proporción de AGS es alta, incrementa la mortalidad embrionaria [23]; se ha demostrado que la adición de 0,5% de ácido linoleico conjugado a la dieta de codornices, aumentó los AGS y la mortalidad embrionaria registró 36% más, con una relación AGS/AGP de 1,18 más amplio respecto al testigo [4].
RESPUESTA REPRODUCTIVA DE CODORNIZ JAPONESA CON INCLUSIÓN DE SEMILLA DE LINAZA Y CHÍA EN EL ALIMENTO
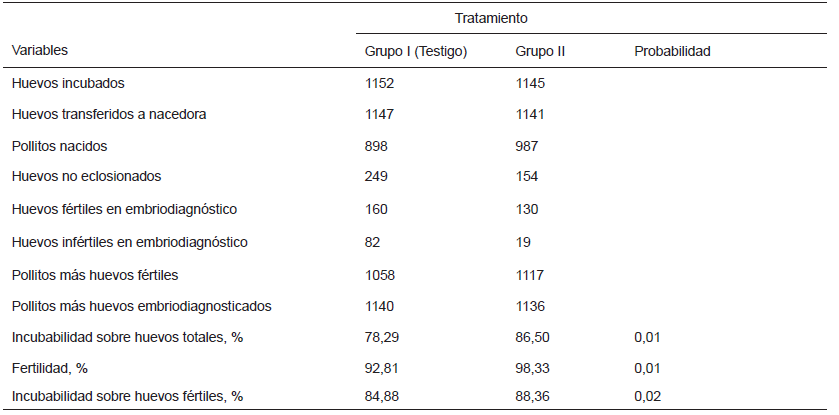
EMBRIODIAGNÓSTICO DE HUEVO NO ECLOSIONADO DE CODORNIZ JAPONESA CON INCLUSIÓN DE SEMILLA DE LINAZA Y CHÍA EN EL ALIMENTO
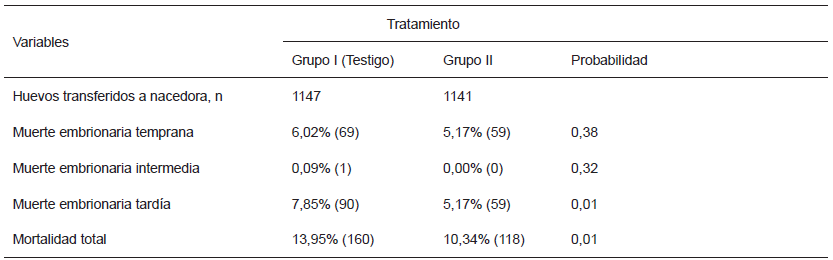
En otro estudio [12], al incluir semilla de linaza al 4 y 7% en el alimento de codornices, refieren valores de incubabilidad sobre huevo fértil de 86,96 y 89,91%, respectivamente, estos valores son mayores a los obtenidos con dietas a base de maíz y trigo (81,21%) pero sin reportar mortalidad embrionaria, sin embargo, es posible inferir que fue menor al mostrar mayor incubabilidad sobre huevo fértil. Al-Daraji y col. [1], al incluir aceite y semilla de ajonjolí (Sesamum indicum) en 0,5, 1 y 2% obtuvieron mejores resultados de fertilidad, incubabilidad y disminución de mortalidad embrionaria a favor de la semilla sobre el aceite; estos resultados pueden indicar que el manejo de los aceites puede ser más importante que su contenido de AG, y que la oxidación de los AGP sea la causa de las variaciones en los resultados en gallinas de postura, utilizando aceite de pescado o concentrados de DHA y EPA [20]. Para gallinas reproductoras pesadas donde los parámetros reproductivos se ven afectados por el sobrepeso y obesidad, y que son alimentadas con dietas típicas a base de harina de soja, harina de maíz y aceites de éstos, el empleo de semillas de linaza y chía, constituyen una buena combinación a fin de promover el incremento del consumo de ácidos grasos insaturados, lo cual puede mejorar los indicadores reproductivos.
A pesar de la evidencia y el uso actual en productos para alimentación humana, todavía hay necesidad de más estudios, que determinarán el requerimiento, relación n6/n3, y qué importancia pueden tener en la reproducción de las aves al incluirlos en su alimentación, sin efectos adversos.
CONCLUSIONES
Se concluye que, para las condiciones en las que se realizó este trabajo, la inclusión de semillas de linaza y chía como fuente de consumo de AGP durante 63 d en codorniz japonesa reproductora, incrementó la incubabilidad, fertilidad y redujo la mortalidad embrionaria, asociado a mayor proporción de los AGEs n3 y una relación n6/n3 más estrecha en la yema de los huevos para incubar.
Agradecimientos
Al Centro de Investigación en Alimentación y Desarrollo A.C. Unidad Culiacán, por permitir el uso del equipo de Cromatografía para el perfil de ácidos grasos. Al CONACyT por la beca de estudio para CBCT.
Referencias
[1] AL-DARAJI, H.J.; AL-MASHADANI, H.A.; AL-HAYANI, W.K.; MIRZA, H.A.; AL-HASSANI, A.S. Effect of dietary supplementation with different oils on productive and reproductive performance of quail. Int. J. Poultr. Sci. 9 (5):429-435. 2010.
[2] AL-DARAJI, H.J.; AL-MASHADANI, H.A.; AL-HAYANI, W.K.; AL-HASSANI, A.S.; MIRZA, H.A. Effect of n-3 and fatty acids supplemented diets on semen quality in japanese quail (Coturnix coturnix japonica). Int. J. of Poult. Sci. 9 (7):656-663. 2010.
[3] ASSOCIATION OF OFFICIAL ANALYTICAL CHEMISTS (AOAC). Method 969.33. Oils and Fat. Determination of fatty acids in oils and fats In: Official Methods of Analysis of AOAC International. Oils and Fat. Horwitz W. (Ed.) Virginia, USA. Pp 19-20. 2000.
[4] AYDIN, R.; COOK M.E. The effect of dietary conjugated linoleic acid on egg yolk fatty acids and hatchability in japanese quail. Poult. Sci. 83:2016–2022. 2004.
[5] AYERZA, R.; COATES, W. Chia and Other Sources of Omega-3 Fatty Acids. Chia: rediscovering a forgotten crop of the Aztec. The University Arizona Press, Tucson, Arizona, USA. Pp 109-112. 2005.
[6] AYERZA, R.; COATES, W. Influence of environment on growing period and yield, protein, oil and alfa-linolenic content of three chia (Salvia hispanica L.) selections. Ind. Crops and Prod. 30:321-324. 2009.
[7] CIAPAN. Guía para la asistencia técnica del Valle de Culiacán. Instituto Nacional de Investigaciones Agrícolas, Forestales y Pecuarias. Culiacán, Sinaloa, México. 92 pp. 2002.
[8] CHEN, Z.Y.; RATNAYAKE, W.M.N.; CUNNANE, S.C. Oxidative stability of linseed lipids during baking. J. Am. Oil Chem. Soc. 71 (6):629-632. 1994.
[9] CHERIAN, G. Egg quality and yolk polyunsaturated fatty acid status in relation to broiler breeder hen age and dietary n-3 oils. Poult. Sci. 87:1131-1137. 2008.
[10] CORTÉS, C.A.; CELIS, G.A.; ÁVILA, G.E.; MORALES, B.E. Valor nutrimental de cuatro pastas de soya procesadas en diferentes estados de la República Mexicana. Vet. Méx. 33(3):209-217. 2002.
[11] DALTON, M.N. Effects of Dietary Fats on Reproductive Performance, Egg Quality, Fatty Acid Composition of Tissue and Yolk and Prostaglandin Levels of Embryonic Tissues in Japanese Quail (Coturnix coturnix japonica). Faculty of the Virginia Polytechnic Institute and State University. Thesis of Grade. Pp 60. 2000.
[12] DANUTA, S.; TARASEWICZ, Z.; SULIK, M.; KOPCZYŃSKA, E.; PYKA, B. Effect of the diet with common flax (Linum usitatissimum) and black cumin seeds (Nigella sativa) on quail performance and reproduction. Anim. Sci. Pap. Rep. 30 (3):261-269. 2012.
[13] DECKELBAUM, R.; WORGALL, T.S.; SEO, T. n-3 fatty acids and gene expression. Am. J. Clin. Nutr. 83(6):1520S-1525S. 2006.
[14] DING, S.T.; LILBURN, M.S. Inclusion of coconut oil in diets for turkey breeders and its effects on embryonic yolk and liver fatty acids. Poult. Sci. 76:1714-1721. 1997.
[15] FOLCH, J.; LEES, M.; STANLEY, G.H. A simple method for the isolation and purification of total lipids from animal tissues. J. Biol. Chem. 226:497-509. 1957.
[16] GARCÍA, E. Modificaciones al sistema de clasificación climática de Köppen (para adaptarla a las condiciones climáticas de la República Mexicana). Instituto de Geografía. Universidad Nacional Autónoma de México.144 pp. 1988.
[17] GÜÇLÜ, B.K.; UYANIK, F.; ISCAN, K.M. Effects of dietary oil sources on egg quality, fatty acid composition of eggs and blood lipids in laying quail. S. Afr. J. Anim. Sci., 38 (2):91-100 2008.
[18] HARGIS, P.S.; VAN ELSWYK, M.V.; HARGIS, B.M. Dietary modification of yolk lipid with menhaden oil. Poult. Sci. 70:874-883. 1991.
[19] KJELDAHL, J. Neue Methode zur Bestimmung des Stickstoffs in organischen Körpern. Z. Anal. Chem. 22:366-382.1883.
[20] KOPPENOL, A.; DELEZIE, E.; WANG, Y.; FRANSSENS, L.; WILLEMS, E.; AMPE, B.; BUYSE, J.; EVERAERT, N. Effects of maternal dietary EPA and DHA supplementation and breeder age on embryonic and post-hatch performance of broiler offspring: age and n-3 pufa affect embryonic and post-hatch performance. J. Anim. Physiol. Anim. Nutr. 99:36-47. 2015.
21] MOIR, K.W.; YULE W.J.; CONOR, J.K. Energy losses in the excreta of poultry: a model for predicting dietary metabolizable energy. Aust. J. Exp. Agric. Anim. Husb. 20:151-155. 1980.
[22] NATIONAL RESEARCH COUNCIL (NRC). Nutriment Requirements of Poultry: 9th.Ed. Rev. National Academy Press, Washington, D. C. 145pp. 1994.
[23] NOBLE, R.C.; COCCHI, M. Lipid metabolism and the neonatal chicken. Proc. Lipid Res. 29:107–140. 1990.
[24] O´BRIEN, R.D. Fats and oils analysis. In: O´Brien R.D. (Ed). Fat and oil, formulating and processing for application. Techonomic publishing Co, Inc. Lancaster PA; Pp 181–249. 1998.
[25] PAI, W.Y.; HSU, C.C.; LAI, C.Y.; CHANG, T.Z.; TSAI, Y.L.; HER, G.M. Cannabinoid receptor 1 promotes hepatic lipid accumulation and lipotoxicity through the induction of SREBP-1c expression in zebrafish. Transgenic Res. 22(4):823-838. 2013.
[26] SIMOPOULOS, A.P.; CLELAND, L.G. Omega–6/Omega–3 essential fatty acid ratio: The scientific evidence. World Rev. Nutr. Diet. Basel: Karger, 92:37–56. 2003.
[27] SPEAKE, B.K.; NOBLE, R.C.; MURRAY A.M.B. The utilization of yolk lipids by the chick embryo. Poult. Sci. 54:319-334. 1998.
[28] STATISTICAL ANALYSIS SYSTEM INSTITUTE (SAS). User’s Guide Statistics. Version 8,1. USA. 2001.
[29] STEEL, R.; TORRIE, J. Comparaciones múltiples. Homogeneidad de la varianza. Estadística no paramétrica. Bioestadística: Principios y Procedimientos. 2da. Ed. Editorial McGraw-Hill. México, D.F. Pp 179-180, 460-461 y 522-528. 1988.
[30] TAVILANI, H.; DOOSTI, M.; ABDI, K.; VAISIRAYGANI, A.; JOSHAGHANI. H.R. Decreased polyunsaturated and increased saturated fatty acid concentration in spermatozoa from asthenozoospermic males as compared with normozoospermic males. Androl. 38:173–8. 2006.
Notas
