Resumen: En los anteriores artículos, se revisaron las patologías hepáticas más frecuentes desde el punto de vista morfológico y la importancia de una adecuada correlación, para lograr un mejor entendimiento entre clínicos y patólogos. El ejercicio que se hará a continuación, se basa en establecer una aproximación al diagnóstico histopatológico de algunas de las patologías hepáticas a las que se les realiza biopsias con mayor frecuencia, teniendo en cuenta algoritmos basados en patrones de daño hepático.
Palabras clave:Biopsia hepáticaBiopsia hepática,algoritmosalgoritmos,patronespatrones,infiltrados portalesinfiltrados portales,granulomasgranulomas,reacción ductularreacción ductular,proliferación colangiolarproliferación colangiolar,injuria lobulillarinjuria lobulillar,pigmentospigmentos,fibrosisfibrosis,cirrosiscirrosis,esteatosisesteatosis,masa hepáticamasa hepática.
Abstract: Previous articles have reviewed the most frequent liver pathologies from the morphological point of view and looked at the importance of adequate correlation for obtaining better understanding between clinicians and pathologists. The next exercise is directed toward histopathological diagnosis of some of the liver diseases for which biopsies are performed most frequently. It takes into account algorithms based on patterns of liver damage.
Keywords: Liver biopsy, algorithms, patterns, portal infiltrates, granulomas, duct reaction, cholangiolar proliferation, lobular injury, pigments, fibrosis, cirrhosis, steatosis, hepatic mass.
Educación médica continuada
Algoritmos útiles para el diagnóstico histopatológico de la enfermedad hepática con base en los patrones de daño hepático
Useful Algorithms for Histopathological Diagnosis of Liver Disease Based on Patterns of Liver Damage
Asociación Colombiana de Gastroenterologia
Recepción: 01 Noviembre 2016
Aprobación: 15 Noviembre 2016
El estudio de una biopsia hepática realizado con la simple descripción de lo que se observa en una lámina histológica, tiene un muy limitado valor diagnóstico. El patólogo debe asegurarse del óptimo manejo de la biopsia, de la adecuada fijación, procesamiento, conocer y utilizar los estudios adicionales de histoquímica, inmunohistoquímica o moleculares que pueden aportar valor al estudio, para finalmente identificar y analizar el tipo de injuria que presenta el hígado, concluyendo finalmente en un diagnóstico. Es aquí donde encajar los hallazgos morfológicos de lesión dentro de uno de los patrones de daño hepático, puede lograr una aproximación al diagnóstico, siempre en correlación con la información clínica.
La respuesta hepática a la injuria es limitada, sin importar cuál es la causa desencadenante. Se debe recordar que los cambios morfológicos se resumen en la presencia de edema celular o balonización, esteatosis, colestasis, necrosis y/o apoptosis, inflamación, cambios regenerativos y alteración de la arquitectura con o sin fibrosis. Estas características, presentándose en forma aislada o simultáneamente varias de ellas, dan lugar a patrones de daño hepático; son netamente morfológicas y cada una de ellas engloba varios diagnósticos diferenciales. Analizadas en forma algorítmica, orientan el diagnóstico; el análisis conjunto con la historia clínica puede lograr una aproximación diagnóstica muy acertada.
Los patrones más importantes son:
-
Patrón I, infiltrados celulares
-
Patrón II, reacción ductular
-
Patrón III, cambios mínimos o casi normal
-
Patrón IV, injuria o lesión lobulillar
-
Patrón V, esteatosis
-
Patrón VI, fibrosis
-
Patrón VII, presencia de masas
El primer paso consiste en identificar si existe o no alteración de la arquitectura lobulillar normal. Determinar la existencia de espacios porta con presencia de estructuras normales de la triada portal, vena central y trabéculas hepatocelulares uniformemente distribuidas (figura 1).
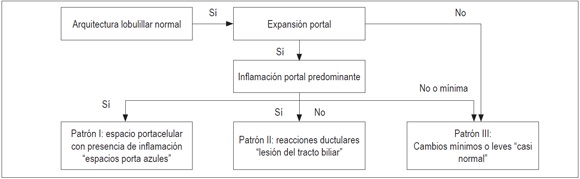
Figura 1.
Algoritmo de arquitectura lobulillar normal. Es útil cuando la arquitectura del lobulillo hepático es normal.
Uno de los hallazgos más frecuentes en la patología hepática, es la presencia de infiltrados inflamatorios portales, estos se observan en una amplia variedad de enfermedades hepáticas que incluyen, principalmente, enfermedades necroinflamatorias, como las hepatitis virales, hepatitis autoinmune y las inducidas por medicamentos, también en enfermedades colestásicas crónicas, como colangitis biliar primaria o la colangitis esclerosante primaria, enfermedades metabólicas de tipo enfermedad de Wilson, deficiencia de α 1 antitripsina o condiciones neoplásicas, como infiltración por linfoma, leucemias o síndrome linfoproliferativo postrasplante (figura 2A).
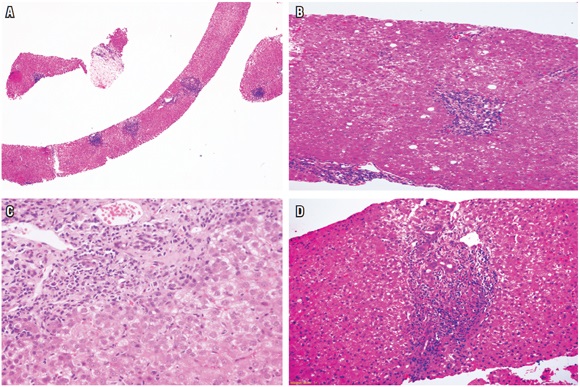
Figura 2.
Patrón I, inflación portal. A. H&E 4x. Inflamación portal de aspecto nodular. B. H&E 10x. VHC, inflamación portal con linfocitos. En el lobulillo se observan algunas vacuolas grasas. C. H&E 40x. Inflamación portal y periportal con plasmocitos en una hepatitis autoinmune. D. H&E 20x. Inflamación portal con infiltrado heterogéneo con linfocitos, neutrófilos y eosinófilos frecuentes en un rechazo agudo celular.
Luego de identificar este patrón de expansión portal celular por inflamación, es importante tener en cuenta otras claves para el diagnóstico histopatológico, como son el tipo de infiltrado, el patrón de compromiso inflamatorio de la placa limitante o del lobulillo, asociación con necrosis y la presencia de fibrosis. Algunas de estas características se trataron anteriormente y se resumirán a continuación:
Esta característica se observa principalmente en las hepatitis crónicas B y C, hepatitis aguda causada por la infección por virus hepatotropos, virus no hepatotropos y toxicidad por medicamentos (figura 2B) (1, 2).
-
Inflamación portal linfocitaria con agregados o folículos linfoides con centros germinales
-
Hepatitis de interfase
-
Hepatitis lobulillar con linfocitos en filas indias
-
Necrosis y/o apoptosis hepatocelular
-
Esteatosis macrovesicular
-
Fibrosis según el estadioFibrosis según el estadio
-
Inflamación portal linfocitaria
-
Hepatitis de interfase
-
Hepatitis lobulillar
-
Necrosis y/o apoptosis hepatocelular
-
Células en vidrio esmerilado
Son entidades con predominio de plasmocitos. En primer lugar se encuentra la hepatitis autoinmune y otras como colangitis biliar primaria, anteriormente llamada cirrosis biliar primaria, colangitis esclerosante primaria, enfermedad por IgG4, patología del trasplante, enfermedades recurrentes, como la hepatitis autoinmune o colangitis biliar y el rechazo celular tardío rico en plasmocitos (figura 2C) (3-6).
-
Infiltrado portal con predominio de plasmocitos muy denso
-
Hepatitis de interfase
-
Formaciones de rosetoides hepatocelulares
-
Hepatitis lobulillar
-
Glóbulos hialinos en células de Kupffer
Son numerosas las enfermedades hepáticas que tienen eosinófilos, pero cuando son predominantes, no necesariamente implican toxicidad o hipersensibilidad medicamentosa, también condiciones sistémicas con eosinofilia, gastroenteritis eosinofílica o enfermedades parasitarias infrecuentes, como la esquistosomiasis del sistema portal, puede producir abscesos de eosinófilos. El diagnóstico diferencial también incluye algunos tumores y lesiones seudotumorales que comprometen el hígado, como histiocitosis de células de Langerhans, seudotumor inflamatorio o tumor miofibroblástico, y en el postrasplante, el rechazo agudo celular (figura 2D) (7, 8).
Característico del rechazo agudo celular, enfermedad de Hodgkin, hepatitis viral y hepatitis inducida por medicamentos.
La prevalencia de los granulomas se encuentra en un rango que oscila entre 2,4% y 15%, de los cuales, más de 60% es secundario a procesos sistémicos, una tercera parte a condiciones primarias hepáticas y entre 6% a 10% son idiopáticos (7, 9, 10).
Los granulomas, pueden localizarse a nivel portal, en el parénquima o ambos. La localización y las características de los granulomas pueden orientar el diagnóstico. En la tabla 1 se resumen algunas de estas características.
Caracterización de los granulomas hepáticos
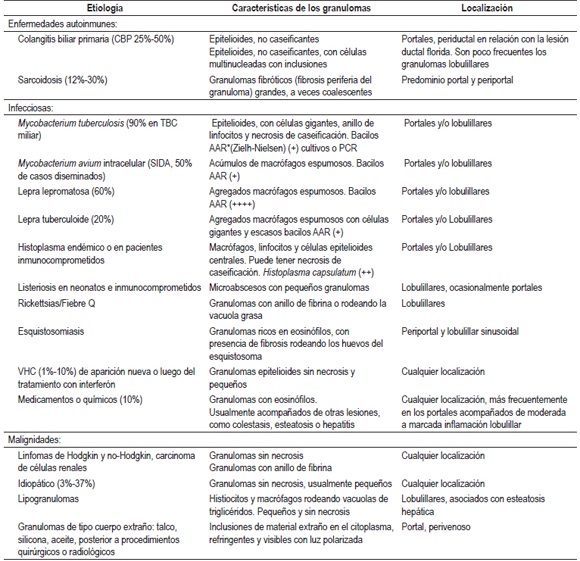
*AAR: ácido alcohol resistentes
Anteriormente, se utilizaba el término proliferación ductular o colangiolar refiriéndose a la proliferación de pequeños conductos biliares en la periferia de los tractos portales; sin embargo, este patrón no solo incluye la proliferación de colangiolos, sino adicionalmente cambios en el estroma portal, en la interfase y en el parénquima. La combinación de estos elementos ayuda a definir las enfermedades que se caracterizan por una prominente reacción ductular. Se debe recordar que las células del epitelio hepatobiliar responden a la lesión del conducto biliar o de los hepatocitos, que se consideran las células madre progenitoras, también la metaplasia biliar de los hepatocitos de la interfase representa procesos de tipo regenerativo. Cuando existe reacción ductular importante se relaciona, en primera instancia, con enfermedades del tracto biliar agudas o crónicas (11, 12).
Una obstrucción de la vía biliar aguda o crónica por cálculos, parásitos, fibrosis o masas, usualmente no requieren biopsia por tratarse de un diagnóstico claramente clínico y/o de imágenes. Constantemente se encuentran en las biopsias postrasplante o como hallazgo durante una autopsia. Otras causas de RD son la colangitis ascendente, colangitis lenta, hepatitis aguda con necrosis submasiva o masiva y en enfermedades colestásicas crónicas, como colangitis biliar primaria y colangitis esclerosante primaria. La reacción ductular biliar se define como la proliferación de conductos biliares acompañada de neutrófilos y, a su vez, se divide en 3 tipos: tipo I, asociado con obstrucción biliar, tipo II relacionado con hepatitis activa y tipo III asociado con necrosis hepática masiva, esta terminología solo es útil para orientar las posibles etiologías (figura 3) (13-15).
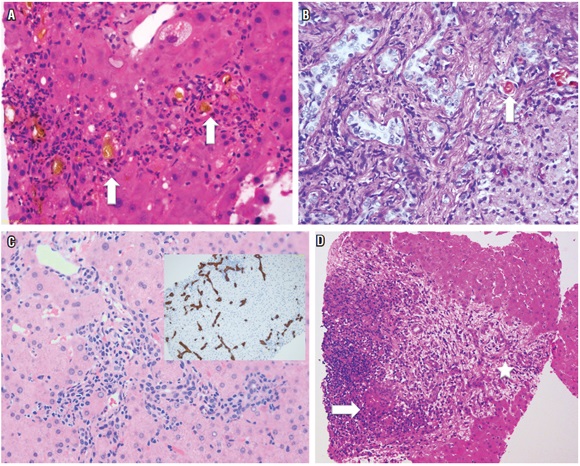
Figura 3.
Patrón II, reacciones ductulares A. H&E 40x. Reacción ductular prominente en colestasis aguda. H&E 20x. Se puede observar la inflamación con neutrófilos en el espacio porta y tapones biliares. B. PAS 40x. Se hace más evidente la proliferación de colangiolo. Con las flechas blancas se identifican algunos de los tapones biliares presentes en las microfotografías. C. H&E 20x. Reacción ductular prominente en una colestasis crónica. Espacio porta con marcada proliferación de colangiolo, ausencia de pimento biliar. En el recuadro, el estudio de inmunohistoquímica para citoqueratina 7 lo corrobora (proliferación ductular de color café) (izquierda). D. H&E 20x. Reacción ductular prominente en una enfermedad colestásica crónica de tipo colangitis biliar primaria. Obsérvese la derecha de la imagen, la proliferación ductular (asterisco) y la inflamación con lesión ductal. a la izquierda (flecha).
-
Proliferación de conductos que parecen anastomosarse con pequeñas luces
-
Marcado edema del estroma circundante
-
Infiltrado de neutrófilos variable
-
Colestasis canalicular y hepatocelular variable
-
Infartos biliares cuando la obstrucción es importante
-
Proliferación de colangiocitos con presencia de neutrófilos intraluminales
-
Inflamación aguda del epitelio del conducto
-
Dilatación del conducto con atenuación del epitelio
-
Colestasis hepatocanalicular variable
-
Los infartos biliares periportales son comunes
-
Se presenta en pacientes con sepsis o sepsis inminente, obstrucción de la vía biliar o por endotoxinas. Se considera una urgencia médica. Presenta proliferación ductular con conductos dilatados llenos de bilis (colestasis ductular), concreciones biliares en el espacio portal o zona de interfase y mínima inflamación.
-
Reacción ductular prominente por activación de las células madre al tratar de regenerar el parénquima y restaurar su función
-
Mínimo edema
-
Inflamación leve, usualmente por neutrófilos
-
Macrófagos con material PAS diastasa positivo
-
Proliferación colangiolar
-
Mínimo edema
-
Leve inflamación de linfocitos
-
Efecto de halo claro en región periportal o periseptal
-
Cambio xantomatoso hepatocitario (colestasis)
-
Depósito de cobre periportal
-
Fibrosis periductal
En cerca de 5% de las biopsias se encuentra cambios inespecíficos, infiltrados inflamatorios mínimos portales o lobulillares, o están ausentes, no hay evidencia de fibrosis ni cambios estructurales. En 80% de estos pacientes, existe anomalías persistentes en las pruebas de función hepática y en 20% ascitis inexplicada, que obliga a realizar una biopsia.
Aproximadamente en la mitad de estos pacientes que llevan una adecuada historia clínica y estudios paraclínicos, es posible definir una etiología, como el compromiso hepático en condiciones autoinmunes sistémicas (lupus eritematoso sistémico y artritis reumatoidea) (15%), hepatitis autoinmune, colangitis biliar primaria o sarcoidosis (10%), síndrome metabólico (10%), condiciones inflamatorias crónicas del tracto gastrointestinal (5%), isquemia hepática (1%-5%) e hipertensión portal no cirrótica (1%). Muchas de estas patologías tienen un compromiso heterogéneo y focal, como por ejemplo, las enfermedades colestásicas crónicas y la enfermedad hepática grasa; otras durante su curso clínico tienen períodos de latencia e inactividad.
En algunos casos, especialmente en entidades que causan hipertensión portal no cirrótica, los cambios vasculares son sutiles y focales. La dilatación sinusoidal o vasos portales dilatados o con fibrosis pueden pasar fácilmente desapercibidos. En 25% de los casos, durante el curso clínico, las anomalías de las pruebas de función se normalizarán y el otro 25% persistirá por muchos años. La tabla 2 resume los diagnósticos probables y se describen los cambios morfológicos que deben buscarse cuando en la biopsia no se identifican lesiones específicas y luce normal o casi normal la biopsia hepática (figura 4) (7).
Características del Patrón III, donde se observan cambios mínimos o es una biopsia que parece normal
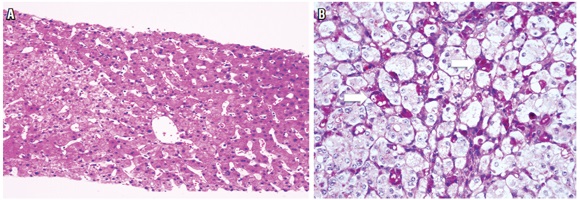
Figura 4.
Patrón III, cambios sinusoidales. A. H&E 10x. Muestra dilatación sinusoidal en zonas 2 y 3 sin evidencia de inflamación encontrada en un paciente con hipertensión portal no cirrótica, obliga a estudiar una obstrucción al flujo venoso. B. PAS diastasa 40x. Presencia de material PAS positivo resistente a la digestión con diastasa en células de Kupffer. En casos de hepatitis reactiva, en ocasiones es el único hallazgo observado.
En la figura 5 se muestra un algoritmo con arquitectura lobulillar normal y expansión portal. Se debe buscar la presencia de injuria lobulillar o esteatosis.
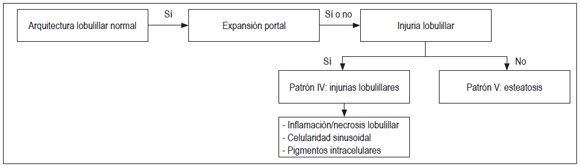
Figura 5.
Algoritmo de muestra de arquitectura lobulillar normal y expansión portal, con presencia de injuria lobulillar o esteatosis. Es útil para el análisis de una biopsia sin cambios arquitecturales pero con inflamación portal y alteraciones lobulillares.
Cuando se observa con poco aumento, el lobulillo luce intranquilo, sea porque está ocupado por células inflamatorias o porque hay evidencia de necrosis, significa que existe una lesión o daño lobulillar. Son múltiples las posibilidades y requiere un estudio minucioso con mayor aumento para buscar claves adicionales que orienten el diagnóstico, para el posterior análisis conjunto con la historia clínica.
Algunos ejemplos de este patrón son la hepatitis aguda o subaguda, hepatitis por virus no hepatotrópicos, como citomegalovirus, herpes virus, adenovirus, Epstein-Barr o hepatitis E; compromiso por enfermedades sistémicas, como la enfermedad celiaca, linfomas o leucemia, hipervitaminosis A o por presencia de pigmentos de lipofuscina, cobre o hierro (16-20).
Usualmente no es indicación de biopsia. En raras ocasiones se indica, por ejemplo cuando existe duda o error en el diagnóstico clínico, o cuando, a pesar de estar bien establecido el diagnóstico, el clínico necesita información más certera del estadio o gravedad de la enfermedad, y por último, en el postrasplante. Muestra prominente inflamación lobulillar, inflamación portal linfocitaria leve, edema o balonización hepatocelular, necrosis o apoptosis aislada, dispersa en el lobulillo, cuerpos acidofílicos, acúmulos de macrófagos con material PAS diastasa positivo y colestasis hepatocanalicular, en casos moderados y graves (figura 6).
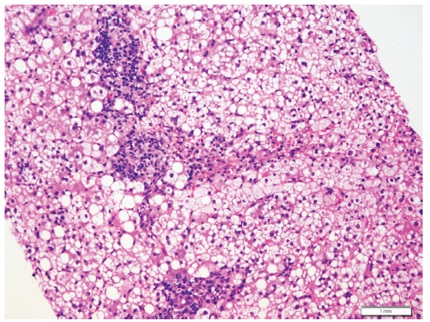
Figura 6.
Patrón IV, inflamación e injuria lobulillar. En una hepatitis aguda se observa importante edema celular, inflamación lobulillar y portal, con ocasionales cuerpos acidofílicos.
Ocurre en pacientes inmunosuprimidos. Se presenta con inflamación portal y lobulillar con linfocitos y neutrófilos, microabscesos de polimorfonucleares neutrófilos localizados en el lobulillo, inclusiones virales de CMV y no hay distribución zonal.
Semejante a la hepatitis por CMV, es rara y se observa en pacientes inmunosuprimidos. Produce inflamación y necrosis dispersa en parches en el lobulillo e inclusiones virales o nucleares amfofílicas o eosinofílicas con anillo periférico por marginación cromatínica.
Infección rara, usualmente mortal y en pacientes inmunosuprimidos, semejante al herpes virus. Presenta grandes áreas de compromiso parenquimatoso con necrosis sin distribución zonal, inflamación linfocítica en los extremos de las zonas de necrosis y presencia de inclusiones del adenovirus.
Un aumento de las células a nivel del espacio sinusoidal, puede ser un hallazgo sutil, requiriendo análisis con gran aumento; si es muy notoria la celularidad a nivel sinusoidal, se debe pensar en una infección grave o neoplasias.
Se enumeran las condiciones que con más frecuencia producen aumento de la celularidad sinusoidal:
Compromiso hepático hasta en 30% de los pacientes al momento del diagnóstico. Amplio espectro de hallazgos desde una apariencia normal, hepatitis lobulillar, cambios sugestivos de enfermedad autoinmune, como hepatitis autoinmune, cirrosis biliar o colangitis esclerosante primaria asociados o no con fibrosis (19). Presenta células inflamatorias linfoides sinusoidales, escasas células apoptóticas dispersas, leve inflamación portal de linfocitos, cambio graso e hiperplasia nodular regenerativa.
En pacientes inmunosuprimidos es más frecuente, pero también puede presentarse en individuos jóvenes aparentemente sanos (20, 21). Presenta numerosas células inflamatorias linfoides sinusoidales, simulando un síndrome parecido a la mononucleosis o patrón predominantemente lobulillar, así como pequeños granulomas epitelioides con anillo de fibrina, ausencia de células apoptóticas o muy ocasionales y dispersas, leve inflamación portal de linfocitos e hibridación localizada (EBER) positiva.
La mayoría son de compromiso secundario. Presentan células linfoides atípicas sinusoidales y/o portal. Es indispensable realizar estudios de inmunohistoquímica y/o citometría de flujo para establecer el fenotipo.
Es un mecanismo compensatorio por el cual se producen células sanguíneas fuera de la médula ósea cuando la producción de médula ósea es incapaz de mantener las necesidades del organismo. La HEM puede observarse en una variedad de trastornos hematológicos, como enfermedades mieloproliferativas, anemia crónica en neonatos y niños con hepatitis gigantocelular o con otras patologías (22, 23). Presenta normoblastos y megacariocitos, evidencia de mielopoyesis y eritropoyesis, en el espacio sinusoidal (figura 7).
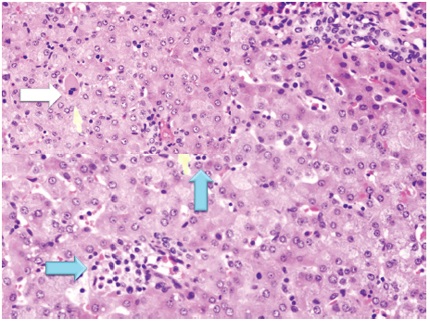
Figura 7.
Patrón IV, celularidad sinusoidal. H&E 40x. Se observa aumento de la celularidad en las sinusoides con normoblastos (flechas azules) y megacariocitos (flecha blanca). El ejemplo corresponde a un paciente con síndrome mieloproliferativo.
En el hígado normal, la vitamina A se almacena en células estrelladas hepáticas, que se activan y adquieren un fenotipo similar a los miofibroblastos, lo que produce matriz extracelular; por lo cual, la toxicidad o hipervitaminosis puede ser grave e incluso llegar a cirrosis (24, 25).
Presenta prominencia de células esteladas en sinusoides en espacio de Dissé, células de núcleos oscuros en forma de media luna por expansión de vacuolas lipídicas dando la imagen de cielo estrellado y proliferación de miofibroblastos, con fibrosis subsinusoidal.
Presencia en células hepáticas, más frecuente en el citoplasma de los hepatocitos, de agregados granulares finos o gruesos que adquieren una coloración variable y que pueden requerir estudios especiales de histoquímica para determinar su etiología. Los más frecuentes corresponden a depósitos de lipofuscina, hierro, cobre o bilis (figura 8).
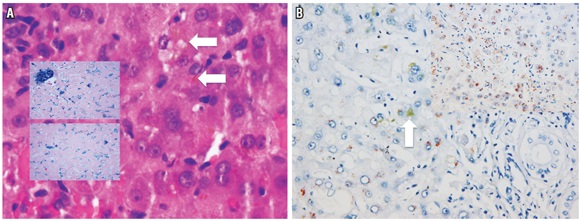
Figura 8.
Pigmentos celulares. A. H&E 20x. En recuadros coloración de azul de Prusia para hierro 40x. Presencia de pigmento pardo, en ocasiones evidente, como el señalado por la flecha blanca, pero no evidente en las demás células. En azul se demuestra la siderosis grave, no solo identificado en la célula marcada con la flecha, sino en las células de Kupffer y citoplasma de hepatocitos. B. Estudio de histoquímica para orceína. 40x. Muestra los depósitos de cobre, de color amarillo, en una enfermedad colestásica crónica. Adicionalmente, se observa pigmento biliar de color verdoso (flecha blanca).
Es un constituyente normal del hígado adulto, especialmente por envejecimiento (entre la quinta y sexta décadas de la vida ) , se deposita también en enfermedades hepáticas crónicas como VHC o cirrosis biliar primaria (7). Presenta un aumento del depósito de pigmento granular color oro o café. Se distribuye en las zonas 3 perivenular y 2, o midzonal. En citoplasma de hepatocitos, ocurre cerca de los canalículos biliares o pericanalicular.
Se observa en condiciones primarias, como la hemocromatosis hereditarias y no hereditarias, como siderosis por transfusiones, hemodiálisis, dieta por aumento de la ingesta de hierro; y enfermedades hepáticas, como la esteatohepatitis alcohólica y no alcohólica y la hepatitis C (7, 26). Tiene un depósito de pigmento granular color oro o café, refráctil, de distribución periportal. En la hemocromatosis hereditaria se identifican además en todo el lobulillo. Localizado en el hepatocito a nivel pericanalicular, en formas hereditarias también se deposita en las células de Kupffer, endotelios, células del estroma y del epitelio del conducto. En las siderosis por transfusiones o dieta se localiza en las células de Kupffer. Reactividad con estudio de histoquímica de azul de Prusia.
Se refleja en enfermedades colestásicas crónicas por interferencia con la excreción o en condiciones hereditarias por defectos en la excreción, como la enfermedad de Wilson (7, 27). Tiene depósitos de pigmento grisáceo en el citoplasma. El cobre se muestra con gránulos de color amarillo ladrillo con los estudios de histoquímica de rodamina, orceína o azul Victoria, o en forma indirecta con depósito de su proteína fijadora con la tinción de aldehído fuscina. Frecuentemente, son PAS diastasa (+). En las enfermedades colestásicas crónicas, se localizan en la zona periportal o en la interfase.
La esteatosis es la acumulación de grasa, hallazgo comúnmente observado en las biopsias. Un algoritmo útil para orientar el diagnóstico, es observar la presencia o no de células balonizadas y cuerpos de Mallory-Denk (figura 9). Este tema se trató extensamente en un artículo anterior (28).
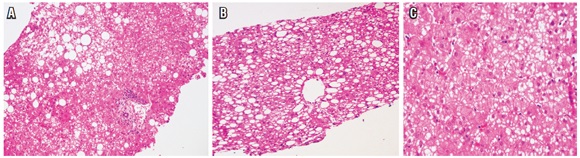
Figura 9.
Patrón V, esteatosis. A. H&E 20x. Esteatosis con balonización, puede observarse en esteatohepatitis alcohólica o no alcohólica (NASH). B. H&E 20x. Esteatosis de macrovacuola sin balonización. C. H&E 40x. Esteatosis de microvacuola sin balonización.
En la figura 10 se presenta el algoritmo utilizado para este patrón.
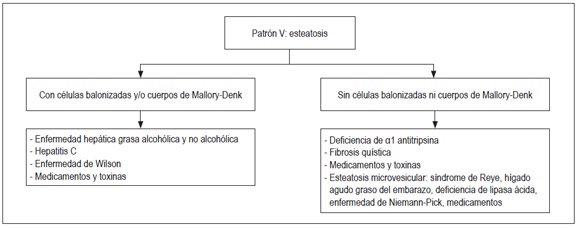
Figura 10.
Algoritmo de análisis de esteatosis
La fibrosis es el resultado final de la gran mayoría de las enfermedades hepáticas, no es un patrón de lesión temprana. Determinar el estadio, la cantidad y el tipo de fibrosis es un componente muy importante e indispensable en el análisis de una biopsia. Siempre debe evaluarse utilizando estudios de histoquímica como el tricrómico de Masson, que es el más usado, o con menos frecuencia el rojo Sirius. El patrón de la fibrosis otorga las claves para el diagnóstico y la subclasificación, ayuda a establecer la gravedad de la enfermedad y se correlaciona directamente con la gravedad de la hipertensión portal (figura 11) (7, 29).
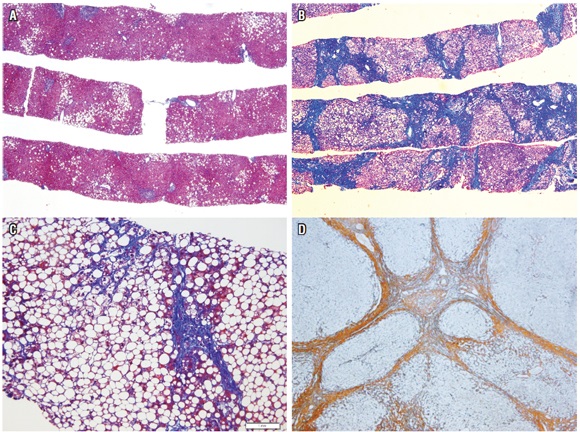
Figura 11.
Patrón VI, fibrosis. Es indispensable utilizar coloraciones especiales para establecer la fibrosis; la más usada es el tricrómico de Masson (TM). A. TM 4x. Esteatohepatitis sin fibrosis. Estadío 0. B. TM 4x. Esteatohepatitis con marcada fibrosis, formación de nódulos Estadío 4. C. TM 20x. Esteatohepatitis con esteatosis grave, fibrosis subsinusoidal y fibrosis portal. Estadio 2. D. La coloración de retículo también es útil para establecer la fibrosis. En esta imagen se presenta una cirrosis establecida.
La figura 12 muestra el algoritmo utilizado cuando encontramos alteración de la arquitectura lobulillar.
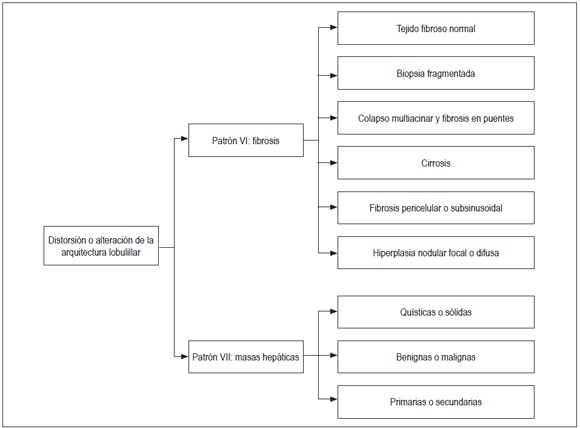
Figura 12.
Algoritmo de alteración arquitectural. Es útil cuando existe alteración de la arquitectura sea por fibrosis o por la presencia de una masa.
Frecuentemente, las biopsias subcapsulares hacen que se sobreestime la fibrosis en una biopsia. Se considera normal un espesor de hasta 5 mm en la cápsula, observándose mayor cantidad de tejido fibroso en los espacios porta y alrededor de las venas centrales, inclusive la presencia de algunos tabiques fibrosos. Adicionalmente, la cantidad de tejido fibroso también depende del tamaño de los espacios porta y está directamente en proporción al tamaño de las estructuras de la triada portal. Asimismo, los cortes longitudinales que atraviesan la longitud de la biopsia hacen pensar que se trata de tabiques fibrosos o puentes que en realidad no existen.
La fragmentación de las biopsias hepáticas percutáneas es común y aumenta con la progresión de la fibrosis de temprana a avanzada. Los especímenes con importante fibrosis o con cirrosis, se fragmentan más a menudo y de forma más extensa. No siempre es fácil identificar esta posibilidad si no se cuenta con los bordes fibrosos. Una apariencia redondeada, la arquitectura lobulillar alterada (ausencia de vena central o de estructuras de la triada portal) o la trama reticular fragmentada, ayudan a sugerir que se trata de una posible cirrosis, a pesar de no observarse la formación de verdaderos nódulos (30).
Especialmente cuando existe una hepatitis aguda con necrosis del parénquima reciente, hay depósito de colágeno joven (azul claro, con el tricrómico de Masson) que se puede sobreinterpretar y llevar a errores de diagnóstico. El colapso de la trama reticular, ayuda a establecer la verdadera naturaleza de la lesión. Determinar si la fibrosis corresponde al depósito de colágeno maduro, con pérdida de la trama reticular y presencia de proliferación colangiolar en zonas de necrosis y parénquima con ausencia de sus normales estructuras, indica que realmente se trata de fibrosis en puentes con tabiques incompletos o completos (cirrosis).
La fibrosis pericelular o subsinusoidal se observa característicamente en la zona 3 en la esteatohepatitis no alcohólica y alcohólica; en esta última puede progresar, ocluyendo la vena central. También se presenta en enfermedades que causan obstrucción al flujo venoso en forma crónica, como la enfermedad venooclusiva sinusoidal y el síndrome de Budd Chiari; en enfermedades metabólicas, como la enfermedad de Wilson, tirosinemia, galactosemia, entre otras; y en enfermedades infecciosas, como leishmaniosis o sífilis congénita. La fibrosis centrada en el espacio porta ocurre en la enfermedad hepática crónica de cualquier etiología, especialmente hepatitis virales B, C y autoinmune. Inicia en forma irregular en el espacio porta, con extensión periportal, posteriormente desarrolla tabiques porta-porta y, finalmente, portacentrales, hasta conformar nódulos cirróticos regenerativos. El término de cirrosis incompleta o temprana se utiliza cuando la nodularidad no es completa (29).
El algoritmo utilizado para el estudio de las masas (figura 13), consiste en determinar si se trata de una masa quística o sólida, observar el tipo de revestimiento epitelial o la célula de origen de la proliferación tumoral (figura 14). Estudios adicionales de histoquímica e inmunohistoquímica pueden ser de utilidad. Adicionalmente, se debe establecer si se trata de una masa primaria o secundaria donde la correlación clínica y de imágenes es fundamental (30, 31).
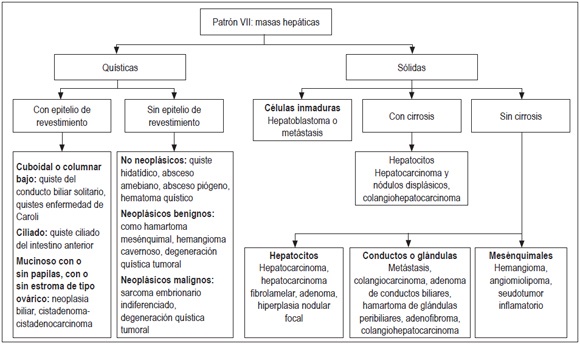
Figura 13.
Algoritmo de análisis de la presencia de masas. Se utiliza ante la presencia de masas hepáticas.
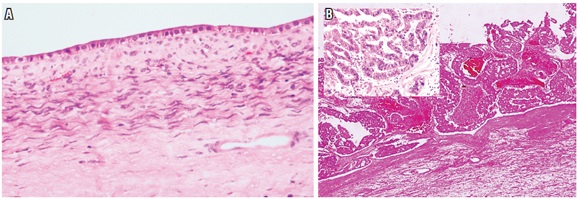
Figura 14.
Patrón VII, masas. A. H&E 20x. Masa quística con revestimiento epitelial. Cistoadenoma biliar. Pared revestida por una monocapa de células cúbicas bajas sin atipia. B. Masa quística maligna con revestimiento epitelial. El ejemplo corresponde a una cistoadenocarcinoma. Pared quística revestida por epitelio complejo, con múltiples capas de células epiteliales que forman estructuras glandulares, seudopapilas irregulares con pleomorfismo nuclear, hipercromasia y mitosis.
La patología hepática es extensa y compleja; cuando se debe hacer frente al estudio de una biopsia hepática y se analizan los hallazgos morfológicos, resulta de mucha ayuda apoyarse en algoritmos que, de una manera más simple, permite una aproximación al diagnóstico; sin embargo, solo una adecuada correlación entre la histopatología y la historia clínica completa puede lograr óptimos resultados .

Figura 1.
Algoritmo de arquitectura lobulillar normal. Es útil cuando la arquitectura del lobulillo hepático es normal.

Figura 2.
Patrón I, inflación portal. A. H&E 4x. Inflamación portal de aspecto nodular. B. H&E 10x. VHC, inflamación portal con linfocitos. En el lobulillo se observan algunas vacuolas grasas. C. H&E 40x. Inflamación portal y periportal con plasmocitos en una hepatitis autoinmune. D. H&E 20x. Inflamación portal con infiltrado heterogéneo con linfocitos, neutrófilos y eosinófilos frecuentes en un rechazo agudo celular.
Caracterización de los granulomas hepáticos

*AAR: ácido alcohol resistentes

Figura 3.
Patrón II, reacciones ductulares A. H&E 40x. Reacción ductular prominente en colestasis aguda. H&E 20x. Se puede observar la inflamación con neutrófilos en el espacio porta y tapones biliares. B. PAS 40x. Se hace más evidente la proliferación de colangiolo. Con las flechas blancas se identifican algunos de los tapones biliares presentes en las microfotografías. C. H&E 20x. Reacción ductular prominente en una colestasis crónica. Espacio porta con marcada proliferación de colangiolo, ausencia de pimento biliar. En el recuadro, el estudio de inmunohistoquímica para citoqueratina 7 lo corrobora (proliferación ductular de color café) (izquierda). D. H&E 20x. Reacción ductular prominente en una enfermedad colestásica crónica de tipo colangitis biliar primaria. Obsérvese la derecha de la imagen, la proliferación ductular (asterisco) y la inflamación con lesión ductal. a la izquierda (flecha).
Características del Patrón III, donde se observan cambios mínimos o es una biopsia que parece normal


Figura 4.
Patrón III, cambios sinusoidales. A. H&E 10x. Muestra dilatación sinusoidal en zonas 2 y 3 sin evidencia de inflamación encontrada en un paciente con hipertensión portal no cirrótica, obliga a estudiar una obstrucción al flujo venoso. B. PAS diastasa 40x. Presencia de material PAS positivo resistente a la digestión con diastasa en células de Kupffer. En casos de hepatitis reactiva, en ocasiones es el único hallazgo observado.

Figura 5.
Algoritmo de muestra de arquitectura lobulillar normal y expansión portal, con presencia de injuria lobulillar o esteatosis. Es útil para el análisis de una biopsia sin cambios arquitecturales pero con inflamación portal y alteraciones lobulillares.

Figura 6.
Patrón IV, inflamación e injuria lobulillar. En una hepatitis aguda se observa importante edema celular, inflamación lobulillar y portal, con ocasionales cuerpos acidofílicos.

Figura 7.
Patrón IV, celularidad sinusoidal. H&E 40x. Se observa aumento de la celularidad en las sinusoides con normoblastos (flechas azules) y megacariocitos (flecha blanca). El ejemplo corresponde a un paciente con síndrome mieloproliferativo.

Figura 8.
Pigmentos celulares. A. H&E 20x. En recuadros coloración de azul de Prusia para hierro 40x. Presencia de pigmento pardo, en ocasiones evidente, como el señalado por la flecha blanca, pero no evidente en las demás células. En azul se demuestra la siderosis grave, no solo identificado en la célula marcada con la flecha, sino en las células de Kupffer y citoplasma de hepatocitos. B. Estudio de histoquímica para orceína. 40x. Muestra los depósitos de cobre, de color amarillo, en una enfermedad colestásica crónica. Adicionalmente, se observa pigmento biliar de color verdoso (flecha blanca).

Figura 9.
Patrón V, esteatosis. A. H&E 20x. Esteatosis con balonización, puede observarse en esteatohepatitis alcohólica o no alcohólica (NASH). B. H&E 20x. Esteatosis de macrovacuola sin balonización. C. H&E 40x. Esteatosis de microvacuola sin balonización.

Figura 10.
Algoritmo de análisis de esteatosis

Figura 11.
Patrón VI, fibrosis. Es indispensable utilizar coloraciones especiales para establecer la fibrosis; la más usada es el tricrómico de Masson (TM). A. TM 4x. Esteatohepatitis sin fibrosis. Estadío 0. B. TM 4x. Esteatohepatitis con marcada fibrosis, formación de nódulos Estadío 4. C. TM 20x. Esteatohepatitis con esteatosis grave, fibrosis subsinusoidal y fibrosis portal. Estadio 2. D. La coloración de retículo también es útil para establecer la fibrosis. En esta imagen se presenta una cirrosis establecida.

Figura 12.
Algoritmo de alteración arquitectural. Es útil cuando existe alteración de la arquitectura sea por fibrosis o por la presencia de una masa.

Figura 13.
Algoritmo de análisis de la presencia de masas. Se utiliza ante la presencia de masas hepáticas.

Figura 14.
Patrón VII, masas. A. H&E 20x. Masa quística con revestimiento epitelial. Cistoadenoma biliar. Pared revestida por una monocapa de células cúbicas bajas sin atipia. B. Masa quística maligna con revestimiento epitelial. El ejemplo corresponde a una cistoadenocarcinoma. Pared quística revestida por epitelio complejo, con múltiples capas de células epiteliales que forman estructuras glandulares, seudopapilas irregulares con pleomorfismo nuclear, hipercromasia y mitosis.
