ARTÍCULO
Recepción: 13 Noviembre 2020
Aprobación: 22 Abril 2021
Resumen: El puma se encuentra actualmente entre los carnívoros más conflictivos de Argentina debido a la depredación de animales domésticos. Su dieta ha sido estudiada en Patagonia, encontrándose un consumo, principalmente, de especies exóticas y nativas. El objetivo de este trabajo fue caracterizar la dieta del puma en el Parque Nacional Los Glaciares (PNLG), provincia de Santa Cruz. Se realizaron recorridas por los principales senderos del PNLG, durante los años 2004-2006, donde se colectaron 68 heces de puma. Para determinar los ítem-presa, se utilizaron pelos, mandíbulas, maxilares, dientes y plumas encontrados en las heces y se calculó la frecuencia de ocurrencia (FOi) y la biomasa consumida (BC). Se identificaron 19 especies de mamíferos: 14 nativos, cuatro domésticos y uno exótico. Los valores más altos de FOi fueron para la liebre (95.58%) y el piche (57.37%), seguido por el caballo (33.82%). Las especies que más aportaron a la BC fueron la liebre (valores entre 23.68% y 22.79%), el caballo (valores entre 21.65% y 17.97%) y la oveja (valores entre 16.08% y 17.12%). Estos resultados para el PNLG indicarían una tendencia al consumo de especies exóticas y domésticas, por sobre las especies nativas. Las especies domésticas serían consumidas por este felino fuera del parque. Futuros estudios deberían orientarse a aumentar el conocimiento sobre la dieta del puma dentro y fuera del PNLG, y a estudiar la disponibilidad de presas nativas para generar información que favorezca la coexistencia entre los productores y los carnívoros.
Palabras clave: Área protegida, especies domésticas, Lepus europaeus, puma.
Abstract: The cougar is currently among the most conflictive carnivores in Argentina due to the predation of domestic animals. Their diet has been studied in Patagonia, finding a consumption mainly of exotic and native species. The objective of this work was to characterize the cougar’s diet in Los Glaciares National Park (LGNP), Santa Cruz province. Tours of the main trails of the LGNP were carried out during the years 2004-2006, where 68 cougar feces were collected. To determine the prey items, hairs, mandible, jaws, teeth and feathers found in the feces were used and the frequency of occurrence (FOi) and the biomass consumed (BC) were calculated. Nineteen mammal species were identified: 14 native, 4 domestic and 1 exotic. The highest FOi values were for the hare (95.58%) and the piche (57.37%), followed by the horse (33.82%). The species that contributed the most to the BC were the hare (values between 23.68% and 22.79%), the horse (values between 21.65% and 17.97%) and the sheep (values between 16.08% and 17.12%). These results for LGNP show a trend towards the consumption of exotic and domestic species, over native species. The domestic species would be consumed by this feline outside the park. Future studies should focus on increasing the knowledge of the diet of the puma inside and outside of PNLG and in the study of native prey availability, to generate information to promote coexistence between ranchers and carnivores.
Keywords: Domestic species, Lepus europaeus, protected area, puma.
INTRODUCCIÓN
Según la Unión Internacional para la Conservación de la Naturaleza (IUCN en inglés), las áreas protegidas (AP) representan “un espacio geográfico claramente definido, reconocido, dedicado y gestionado, mediante medios legales u otros tipos de medios eficaces para conseguir la conservación a largo plazo de la naturaleza y de sus servicios ecosistémicos y sus valores culturales asociados” (Dudley 2008). Dentro de las AP, encontramos los Parques Nacionales (PP. NN.) que, en la República Argentina, pueden variar en el manejo, la superficie y la administración del territorio. En algunos PP. NN. determinadas actividades antrópicas no son permitidas (e.g., la ganadería extensiva) y se realiza un manejo estricto de especies exóticas dentro de sus límites; en otros, sí se permite una determinada carga ganadera y no se realizan manejos específicos de fauna exótica (Sistema de Información de Biodiversidad-SIB). Los PP. NN. en Argentina cubren, aproximadamente, el 1.31% del total del territorio, con un mínimo de superficie de 8 ha a un máximo de 731000 ha (SIB). La mayoría de estos territorios se ubican en matrices agro-ganaderas, representando así “islas” ecológicas, particularmente para especies de gran tamaño (e.g., mayores de 15 kg).
Actualmente, los grandes carnívoros son protagonistas del conflicto entre humanos y vida silvestre a raíz de los ataques ocasionados a distintas especies domésticas, especialmente el ganado (Treves 2004; Inskip & Zimmermann 2009; Castaño-Uribe et al. 2016). Numerosos estudios han demostrado cómo los PP. NN., en otras partes del mundo, tienden a exacerbar el conflicto entre carnívoros y ganadería en áreas próximas a PP. NN. (Mishra 1997; Conforti & Azevedo 2003; Pacheco et al. 2004; Kolowski & Holekamp 2006; Holmern et al. 2007; Gallardo et al. 2009; Sogbohossou et al. 2010; Mwakatobe et al. 2013; R Core Team 2013). El estudio de la dieta de carnívoros conflictivos es una herramienta útil para entender qué especies están consumiendo y, de forma indirecta, cuáles son las más disponibles en el territorio. Además, permite conocer de manera indirecta el potencial impacto que generan los carnívoros sobre especies de interés económico para los humanos (e.g., caprinos, ovinos; Novaro et al. 2000; Fernández & Baldi 2014; Gelin et al. 2017; Llanos & Travaini 2020), en casos donde pueda documentarse una depredación en lugar de consumo como carroña.
Dentro de los carnívoros que generan un impacto significativo sobre el ganado a lo largo de todo el continente americano, encontramos al puma Puma concolor (Inskip & Zimmermann 2009; Guerisoli et al. 2020). A lo largo de su distribución, el puma se alimenta de un amplio espectro de especies, incluyendo principalmente mamíferos y aves. En la parte norte del continente americano se alimenta, principalmente, de artiodáctilos con pesos mayores a 6.1 kg (Monroy-Vilchis et al. 2009); en América Central, preda sobre especies de tamaño mediano (Moreno et al. 2006), que en promedio pesan menos de 6.1 kg (Monroy-Vilchis et al. 2009); mientras que en América del Sur se alimenta, principalmente, de presas de tamaño mediano (1 a 15 kg) a pequeño (<1 kg) (López-González & González-Romero 1998). Trabajos recientes han identificado a esta especie como un carnívoro generalista, que está diversificando el uso de recursos, expandiendo su nicho e interactuando con nuevas presas (e.g., mesocarnívoros sinantrópicos y especies domésticas) en ecosistemas altamente modificados (Moss et al. 2016). Una revisión actual en América del Sur identificó al puma como depredador de especies exóticas silvestres, principalmente liebre Lepus europaeus y jabalí Sus scrofa (Buenavista & Palomares 2017), mientras que las especies domésticas representan la menor contribución a su amplia dieta (e.g., entre 0.30% y 14.60% de la frecuencia de ocurrencia, Pacheco et al. 2004; Villalobos 2008; Fernández & Baldi 2014).
En Argentina, el puma está presente en 63 áreas protegidas, de las cuales 37 son de jurisdicción nacional, manejadas por la Administración de Parques Nacionales (APN) (SIB). En el sur de Argentina, donde los PP. NN. poseen las mayores extensiones dentro del sistema de áreas protegidas (SIB), el puma es protagonista de intensos conflictos con los productores ganaderos (Pia & Novaro 2005). Los estudios sobre su dieta en el sur de Argentina y Chile se concentran principalmente en áreas protegidas y alrededores, e incluyen como ítems predominantes al guanaco Lama guanicoe (Rau et al. 1991a,b; Fernández & Baldi 2014), la mara Dolichotis patagonum (Zanón-Martínez et al. 2012), el piche Zaedyus pichiy (Fernández & Baldi 2014), el ciervo colorado Cervus elaphus (Novaro et al. 2000), el jabalí (Bank et al. 2002; Skewes et al. 2012), la liebre (Novaro et al. 2000; Rau & Jiménez 2002) y mamíferos domésticos (e.g., ovinos, Fernández & Baldi 2014).
El objetivo de este trabajo fue caracterizar la dieta del puma en un área del Parque Nacional Los Glaciares, provincia de Santa Cruz (República Argentina), cuantificando la importancia de las especies exóticas silvestres y domésticas como recurso dietario dentro del parque.
MATERIALES Y MÉTODOS
Área de estudio
El Parque Nacional Los Glaciares (PNLG; Fig. 1) cubre una extensión de 726927 ha. Se encuentra dentro de la ecorregión de los Bosques Patagónicos (Burkart et al. 1999), inmerso en una matriz de establecimientos ganaderos que están orientados, principalmente, a la cría de vacas Bos taurus, caballos Equus caballus y ovejas Ovis aries (Martín 1997). La vegetación corresponde a la Provincia Fitogeográfica Subantártica, distrito de los Bosques Caducifolios y a la Provincia Fitogeográfica Altoandina (Cabrera 1976). Los bosques de lenga Nothofagus pumilio y ñire Nothofagus antartica ocupan valles, quebradas y laderas desde los 425 a los 1200 m s. n. m. (Quintana et al. 2003). Según datos de la estación meteorológica de la seccional Lago Viedma que se encuentra ubicada en la zona norte del PNLG, la precipitación media anual es de 439 mm, uniformemente repartida durante todo el año, y la temperatura media es de 7ºC.
Recolección de muestras y procesamiento
Las heces de puma fueron identificadas por su forma y tamaño siguiendo a Chame (2003). Las heces fueron colectadas en el sector norte del PNLG (Fig. 1), que corresponde a una zona del parque destinada a un uso recreativo extensivo, abarcando el sector de senderos de trekking. Las heces se recolectaron entre los meses de octubre y abril de 2004, 2005 y 2006, de manera oportunista, en senderos de trekking que fueron recorridos al menos tres veces por semana, y en zonas alejadas de los mismos. Cada sitio de colecta fue identificado con un número, fecha de recolección y datos de altitud, latitud y longitud (Apéndice 1).
Las heces se esterilizaron en estufa a 90°C por 48 h. Posteriormente, se colocaron en remojo con agua tibia para facilitar su disgregación y se utilizó un tamiz de malla de 0.2 mm para eliminar residuos no incorporados en los análisis. Cada hez fue luego colocada en una bandeja para separar pelos de plumas o material óseo, los cuales fueron analizados en su totalidad.
Para el análisis de los pelos se extrajo de cada hez una submuestra de 30 ítems. Siguiendo la metodología propuesta por Chehébar & Martín (1989), se comparó cada pelo macroscópica y microscópicamente (i.e., por color, largo, presencia/ausencia de bandas, patrones medulares y cuticulares) con pelos de referencia de todas las especies de mamíferos presentes en el PNLG y sus alrededores, y guías de identificación (Day 1966; Chehébar & Martín 1989; Vanstreels et al. 2010; Bonzano & Dellafiore 2018).
Para la identificación de los fragmentos de huesos, mandíbulas, maxilas y dientes también se utilizaron claves (e.g., Reise 1973; Pearson 1995) y material de referencia perteneciente a la colección mastozoológica del Laboratorio de Investigaciones en Evolución y Biodiversidad (LIEB, Facultad de Ciencias Naturales y Ciencias de la Salud, Universidad Nacional de la Patagonia “San Juan Bosco”, Esquel, Chubut).
Análisis
Para estimar el número mínimo de heces necesarias para describir la dieta del puma en el PNLG, se empleó una curva de acumulación de presas (Foster et al. 2010; Hernández- Guzmán et al. 2011), sumándose aleatoriamente todas las muestras y estimándose el promedio y el desvío estándar de 1 000 permutaciones, para eliminar la influencia del orden en que se agregó cada hez (Gotelli & Colwell 2001). El análisis se realizó utilizando la función specaccum del paquete Vegan (Oksanen 2007) en R Studio 3.3.3 (R Core Team 2013). Además, se elaboró una lista con las especies presentes en el Parque Nacional (PN) que pudieran ser potenciales presas del puma (Apéndice 2) (Foster et al. 2010).
Los distintos ítem-presa de mamíferos presentes en las heces fueron identificados a nivel específico, excepto para el género Lycalopex y algunos miembros de la familia Cricetidae, mientras que para las aves la identificación específica no fue posible. Se estimó la frecuencia de ocurrencia de todos los ítem-presa (Foi) como el número de heces con el ítem “i” dividido por el número total de las heces. El porcentaje de ocurrencia (Poi) se calculó como el número de heces con el ítem “i” dividido por el número total de ítems multiplicado por 100 (Ackerman et al. 1984). Para caracterizar el aporte de cada presa sobre el total de ítems ingeridos, se calculó la biomasa consumida relativa (BC) de cada presa identificada. Para esto se utilizaron dos estimaciones de BC:
1) se aplicó la ecuación de Ackerman et al. (1984), que se expresa como Bra= Foi*(0.035*Pp+1.98) (para presas >2 kg) y Bra=Foi*Pp (para presas <2 kg), donde Bra=biomasa-presa (kg)/hez; Pp= peso (promedio) de las presas (ítem “i”) en kg;
2) debido a que el consumo de especies grandes (>de 15 kg, Scognamillo et al. 2003) puede sobrestimarse (Khorozyan et al. 2017), se utilizó la ecuación no lineal de Chakrabarti et al. (2016), Brc=Foi*(0.033–0.025*e-4.284*BMi/C), donde Brc = biomasa de presa (kg)/heces por kg de peso del felino y C = peso (medio) de la especie felina, en kg (para Puma concolor se usó el peso corporal promedio de 53.9 kg tomado de PanTHERIA, Jones 2009).
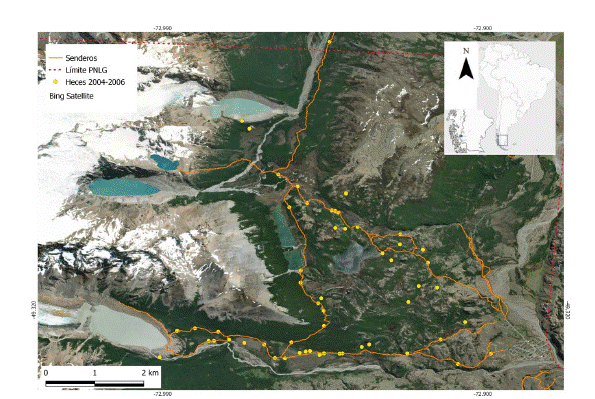
Fig. 1
Área de estudio del Parque Nacional Los Glaciares (provincia de Santa Cruz, República Argentina), donde fueron colectadas las muestras.
El peso de las diferentes especies consumidas fue tomado de diferentes fuentes, a saber: para Bos taurus y Equus caballus se utilizó el peso promedio de los terneros y potros de menos de 12 meses de edad (Guerisoli et al. 2017); para Cricetidae, los pesos se tomaron de Chébez et al. (2014); para Ovis aries se utilizó la base de datos PanTHERIA (Jones 2009); para el resto de las especies se utilizó la base de datos de Animal Diversity Web (Myers et al. 2019).
La amplitud trófica (Feinsinger et al. 1981) fue calculada por el índice de Levins estandarizado (Bst) (Colwell & Futuyma 1971), cuyo valor varía entre 0 y 1, usando la siguiente ecuación: Bst = (B-1)/(n-1), siendo B el Índice de Levins, donde B = 1/Sumatoria (pi)2, donde pi = ni/N (proporción del ítem “i” respecto al total de la muestra N) y n = Nº total de ítems consumidos. Los valores menores a corresponden a un consumo de pocas presas, indicando un depredador especialista, mientras que valores mayores a 0.6 corresponden a dietas de depredadores generalistas (Krebs 1989; Labropoulou & Eleftheriou 1997).
Posteriormente se agrupó a las presas identificadas en tres categorías de análisis: nativas, exóticas silvestres (de aquí en adelante “exóticas”) y domésticas, para determinar cuál es la contribución de cada una y si existe una prevalencia en el consumo de alguna de estas categorías en la dieta del puma.
Por último, las presas fueron agrupadas de acuerdo a su tamaño corporal en presas pequeñas (<1 kg), presas medianas (1-15 kg) y presas grandes (>15 kg) (Scognamillo et al. 2003) para evaluar el rango de tamaño de presas más consumido por puma. Para dichas categorías se calculó el promedio y el desvío estándar (DS), y biomasa consumida (BC) kg/heces.
RESULTADOS
Se colectó un total de 68 heces (11 en 2004, 56 en 2005 y 1 en 2006) y de su análisis se obtuvo una curva de acumulación de presas, indicando una alta riqueza de presas en la dieta del puma en esta área de estudio (Fig. 2). Se identificaron 24 ítems como parte de la dieta del puma en el PNLG, que incluyó mamíferos (su principal ítem con un peso corporal promedio de 24.86 kg), aves indeterminadas, restos indeterminados y basura, con un promedio de ítems por hez de 4.57 kg (Tabla 1). Se determinaron 19 especies de mamíferos (Tabla 1): 14 nativos, cuatro domésticos y uno exótico; las aves se determinaron hasta clase. En cuanto a la amplitud del nicho trófico, el valor obtenido para el índice de Levins estandarizado fue de Bst=0.99, indicando que el puma se comportaría como un depredador generalista en el PNLG.
Los ítems consumidos de mamíferos se identificaron a nivel familia en un 83.56%, y a nivel de especie en un 70.54%. La clase “Aves” se encontró en 11 heces, contribuyendo a la Foi con el 16.17%, mientras que “Mammalia” se encontró en todas las heces (Foi=100%, nheces=68) (Tabla 1). El orden Lagomorpha (con una única especie exótica silvestre registrada en las muestras, la liebre) presentó el mayor aporte, tanto en términos de frecuencia de ocurrencia como de porcentaje de ocurrencia (Foi=95.58%, nheces=65, Poi=22.26%), seguido por Rodentia (Foi=92.64%, nheces=63, Poi=24.80%). El orden Cingulata, representado por una sola especie, el piche, presentó una frecuencia de ocurrencia importante del 57.35% (nheces=39) y un porcentaje de ocurrencia menor (13.35%). Los Artiodactyla y Perissodactyla (estos últimos con una única especie, el caballo) siguieron en importancia en cuanto a frecuencia de ocurrencia en las heces (54.41%, nheces=37 y 33.82%, nheces= 23; respectivamente), con un porcentaje de ocurrencia del 14.56% y 7.87% respectivamente (Tabla 1). De los artiodáctilos nativos presentes en el parque solo se registró al guanaco (nheces=3) y en una sola muestra se detectó la presencia de llama Lama glama (no nativo, Tabla 1 ). Llamativamente, en el 4.41% de las heces (nheces=3) se encontraron restos de basura (e.g., fragmentos de plástico, fósforos, hilo).
Composición de la dieta de Puma concolor en el Parque Nacional Los Glaciares (provincia de Santa Cruz, República Argentina) entre los años 2004 y 2006. Se detalla, en función de las heces analizadas, la frecuencia de ocurrencia del ítem i (Foi), el porcentaje de ocurrencia del ítem i (Poi), los pesos de las presas y el peso promedio obtenido en los diferentes órdenes, y la biomasa consumida calculada siguiendo Ackerman et al. (1984) (Bra) y Chakrabarti et al. (2016) (Brc). Las especies exóticas, domésticas y de valor especial se indican por uno (*), dos (**) o tres (***) asteriscos, respectivamente.
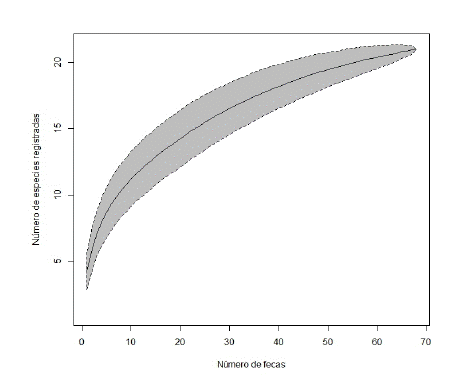
Fig. 2
Curva de acumulación de especies que ilustra el número de heces utilizado para describir la dieta del puma en el Parque Nacional Los Glaciares (provincia de Santa Cruz, República Argentina) entre los años 2004 y 2006. El sombreado gris indica un intervalo de confianza del 95%.
De las 12 especies de vertebrados consideradas de valor especial para el PNLG por la APN (SIB), tres se registraron en la dieta del puma: guanaco, piche y hurón menor Galictis cuja. Además, se encontraron restos indeterminados de zorros que podrían ser asignados a una o a las dos especies de zorro que son comunes en la zona, Lycalopex culpaeus y L. gymnocercus, ambos de valor especial para APN (Tabla 1).
En referencia al aporte de biomasa consumida, los mayores valores se obtuvieron para Artiodactyla (Bra=33.11% y Brc=28.17%), seguido de Lagomorpha (Bra=22.68% y Brc=22.21%) y Perissodactyla (Bra=20.74% y Brc=17.51%; Tabla 1). Consecuentemente, las especies que más aportaron a la BC en la dieta del puma fueron la liebre (Bra=23.66% y Brc=22.79%), el caballo (Bra=21.64% y Brc= 17.97%) y la oveja (Bra=16.08% y Brc=17.12%), seguidas por la vaca (Bra=10.35% y Brc=8.59%) y el piche (Bra=10.04% y Brc=9.98%; Tabla 1).
Cuando se agruparon las presas consumidas fueran nativas, exóticas o domésticas, las especies nativas fueron llamativamente las que menos contribuyeron en la dieta del puma, con un promedio de Foi= 11.21±17.84% (nespecies=16; Tabla 2). Las especies domésticas estuvieron representadas por cuatro especies con un promedio de Foi= 20.96±15.30%, mientras que la liebre fue la única especie exótica encontrada en las heces y la que más contribuyó a la dieta del puma en el PNLG, habiéndose encontrado en el 95.59% de la heces analizadas. También la liebre presentó el mayor aporte en la biomasa consumida por el felino (Bra=39.54%; Brc=38.38%; Tabla 2). Para las especies domésticas, la Bra fue de 35.01%, mientras que para Brc resultó ser de un 30.25%; Tabla 2. En cuanto a las especies nativas, la BC presentó valores más bajos de biomasa consumida (Bra=25.44%) y Brc (31.36%; Tabla 2).
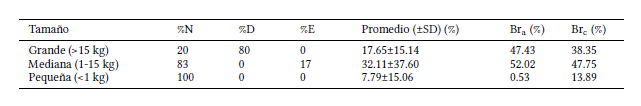
Las especies medianas predominaron en la dieta del puma con un promedio de Foi= 32.11±37.60%, seguidas por las grandes con un promedio de Foi= 17.65±15.14%; Tabla 3. Las presas medianas y pequeñas fueron, a excepción de la liebre (17%, nespecies=1), todas nativas (83%, nespecies=15). Tanto los resultados de Bra como los de Brc coinciden en que las especies medianas, seguidas de las especies grandes, son las que más aportaron a la biomasa (medianas: Bra=52.02% y Brc=47.75%; grandes: Bra=47.43% y Brc=38.35%; Tabla 3). Las especies medianas (nespecies =6) presentaron una media de la Foi mayor que las especies de tamaño grande (nespecies=5) y las especies pequeñas (nespecies=10 Tabla 3).
DISCUSIÓN
Este trabajo aporta nueva información sobre los hábitos alimentarios del puma en el PNLG, único depredador tope en el sur de su distribución considerado especie paraguas e, indirectamente, como un indicador del estado de “salud” de los ecosistemas.
El tamaño de muestra utilizado se acerca a lo recomendado por Foster et al. (2010), quienes sugieren recolectar entre 70 y 100 heces para describir adecuadamente la dieta de este felino en regiones tropicales, indicando que con la mitad de las muestras se estarían detectando, probablemente, las presas principales. También recomiendan que, para la interpretación de los resultados de estudios con bajo número de heces, se elabore una lista de especies presas potenciales del área o una curva de acumulación de especies (Foster et al. 2010). En este trabajo combinamos el uso de una lista con las potenciales presas del área muestreada, que detectó 19 de las 29 especies de mamíferos presentes en el PNLG (representando a todos los órdenes) y una curva de acumulación de especies que se aproximó a una meseta, indicando que, para el PNLG, el número de muestras (n=68) fue adecuado para detectar las potenciales especies presa del área. Los análisis aquí realizados muestran que el puma en el PNLG se alimenta principalmente de la liebre, una especie exótica de tamaño mediano, mientras que las especies nativas están poco representadas en la dieta de este felino. Se destaca, además, el consumo de especies domésticas, y la presencia de restos de basura de origen antrópico (Bartolucci et al. 2020).
La liebre resultó ser la presa con mayor contribución en la dieta del puma, en coincidencia con otros estudios realizados en la Patagonia argentina y chilena (Yáñez et al. 1986; Franklin et al. 1999; Novaro et al. 2000; Rau & Jiménez 2002; Ferreyra et al. 2010). Según Novaro et al. (2004), la liebre es probablemente el ítem-presa más aprovechable, comparándolo con la mayoría de las presas nativas, debido a su cantidad, tamaño y vulnerabilidad. Si bien no hay datos para PNLG, Amaya et al. (1983) indican una densidad de entre 8 y 12 liebres por hectárea de mallín para los alrededores de El Calafate (provincia de Santa Cruz, Argentina), a 120 km al sur de la zona estudiada.
Históricamente, las presas naturales del puma en el área de estudio podrían haber sido ungulados (e.g., huemul Hippocamelus bisulcus, guanaco), armadillos (e.g., peludo Chaetophractus villosus y piche) y roedores (e.g., mara, cricétidos), como así también otros carnívoros (e.g., zorro, zorrino Conepatus chinga, gato montés Leopardus geoffroyi) y aves (e.g., choique Rhea pennata, cauquén Chloephaga spp.). Sin embargo, en nuestro estudio, las especies nativas fueron, en promedio, las que menos contribuyeron en la dieta del puma en esta área protegida. El consumo aquí documentado de especies no nativas podría deberse a una baja disponibilidad de especies nativas, o que estas resulten insucientes para la población de pumas en el PNLG. Algunas de las potenciales presas nativas (e.g., huemul, guanaco) se han visto afectadas por incendios, caza y transmisión de enfermedades por parte del ganado doméstico, dando como resultado una disminución en sus poblaciones naturales (Serret 2001). Además, otras especies registradas como presas en otras zonas de Patagonia, como el choique y en especial el guanaco, sufren la caza furtiva dentro y fuera del área protegida (C. Bartolucci obs. pers.). Coincidente con el bajo consumo de guanaco por parte del puma en el área protegida.
En este estudio se encontró un porcentaje importante de heces que contenían restos de ganado (vacuno, equino y ovino), además de que la mayoría de las heces tenía restos de liebre, similar a lo reportado por Ferreyra et al. (2010). En otras áreas templadas de Argentina, el consumo de vacunos por pumas fue reportado para la Reserva La Payunia, Mendoza (Gelin et al. 2017) con valores de Foi (7.1%); los ovinos, por otra parte, representaron el 0.6% de Foi en la Reserva Natural Parque Luro, La Pampa (Zanón-Martínez et al. 2016). En Patagonia, las vacas y caballos representaron el 0.4% de Foi en el noroeste del Neuquén (Novaro et al. 2000) y los ovinos representaron el 11% de Foi en el noreste del Chubut (Fernández & Baldi 2014). En comparación, los valores obtenidos en nuestro estudio para Foi por consumo de ganado por puma fueron más altos, con 16.17% para vacunos, 32.82% para equinos y 32.35% para ovinos. La introducción en territorio argentino de especies exóticas (domésticas), como la vaca y el caballo, ocurrió entre los años 1536-1550 (Navas 1987), y la ovina se inició en Patagonia entre 1880-1885 (Coronato 2010). La liebre, especie exótica silvestre, fue introducida en Santa Cruz en el año 1930 (Carman 1976; Bonino et al. 2010). Este grupo de especies alteró la dinámica de las relaciones entre depredadores y presas en la Patagonia afectando a carnívoros como el puma (Lambertucci et al. 2014). En un contexto de deterioro de los ambientes naturales y su reemplazo por pasturas o ambientes con diferente antropización, las especies exóticas domésticas y silvestres pueden ser consideradas presas “alternativas o amortiguadoras”, que pueden reemplazar, en la dieta de los depredadores, a las principales presas cuando estas disminuyen (e.g., Hamlin et al. 1984). El consumo de estas especies por parte del felino podría deberse a la escasez de especies de porte similar (e.g., guanaco) dentro del área estudiada. Ferreyra et al. (2010), en un estudio realizado en un área que incluye la porción norte del PNLG, la Reserva Provincial Lago del Desierto y propiedades privadas, reportaron el consumo de vaca, caballo y oveja como componentes de la dieta del puma. Sin embargo, las especies más frecuentes fueron, en orden de importancia, la liebre, los cricétidos y el caballo (Ferreyra et al. 2010). En el noreste del Chubut, Fernández & Baldi (2014) registraron, en términos de biomasa, al guanaco (Foi=18.9%) y la oveja (Foi=11%) como componentes principales de la dieta del puma, lo que podría estar indicando que, en esa zona de la Patagonia, el guanaco sigue siendo funcional como presa. Esto es diferente de lo que ocurre en algunas zonas en el noroeste de la Patagonia, particularmente en las provincias de Río Negro y Neuquén, donde algunas especies nativas incluyendo el guanaco, se encuentran ecológicamente extintas como presas, y tanto puma como otros carnívoros modificaron sus relaciones funcionales alimentándose, mayormente, de especies domésticas y exóticas (Novaro et al. 2000). Si bien el puma puede depredar especies domésticas y exóticas, en áreas donde las presas naturales se encuentran en mayor abundancia, el consumo se inclina hacia presas nativas como el guanaco. Estudios en el sur de Chile documentaron que los pumas consumieron más liebres cuando las densidades de guanaco fueron bajas, disminuyendo su consumo cuando el guanaco aumentó su proporción (Yáñez et al. 1986; Iriarte et al. 1990). Como ocurre en otras áreas protegidas donde otras especies parecieran estar más disponibles, el guanaco deja de ser la primera opción (e.g., Parque Nacional Torres del Paine, Chile; Parque Nacional Monte León, Parque Nacional Perito Moreno Monumento Natural Bosques Petrificados, Argentina) donde la principal especie consumida fue la liebre seguida del guanaco (Yáñez et al. 1986; Zanón-Martínez et al. 2012).
Composición de la dieta del puma en el Parque Nacional Los Glaciares (provincia de Santa Cruz, República Argentina) entre los años 2004 y 2006, según el tipo de especie-presa de mamífero consumida, agrupadas por categorías (exótica, doméstica y nativa). Se detalla el promedio por categoría y biomasa consumida en kg/heces, calculada siguiendo Ackerman et al. (1984) (Bra) y Chakrabarti et al. (2016) (Brc); DS=desvío estándar.

Composición de la dieta del puma en el Parque Nacional Los Glaciares (provincia de Santa Cruz, República Argentina) entre los años 2004 y 2006, indicando el tipo de especie-presa de mamífero consumida según su tamaño corporal: presas pequeñas (<1 kg), presas medianas (1-15 kg) y presas grandes (>15 kg). Se detalla el promedio, porcentaje de especies nativas (%N), domésticas (%D) y exóticas (%E) y biomasa consumida en kg/heces, calculada siguiendo Ackerman et al. (1984) (Bra) y Chakrabarti et al. (2016) (Brc) por tamaño. Foi = frecuencia de ocurrencia por especie; DS=desvío estándar.
La presencia de carnívoros en las heces analizadas podría indicar que el puma cumpliría un rol importante regulando las poblaciones de mesocarnívoros o carnívoros menores del área de estudio. Este tipo de interacción, denominada “depredación intragremio” (Polis & Holt 1992), se da cuando dos especies simpátricas utilizan recursos similares y una de ellas interfiere con la otra, resultando, generalmente, en la muerte y consumo de la especie de menor tamaño (Polis & Holt 1992; Castillo Sánchez et al. 2021). Aunque no hay información directa sobre esta interacción en el PNLG, el consumo de liebres por parte del puma y el zorro colorado, aunque en distintas proporciones, fue documentado en la zona de estudio por Ferreyra et al. (2010), generando una alta probabilidad de competencia por este recurso y, quizás, el desplazamiento de la especie más pequeña por exclusión (Polis & Holt 1992).
Conocer el aporte de los distintos ítems a la dieta de los carnívoros potencialmente conflictivos, como el puma, en términos de especies y biomasa consumida, permite contar con estimaciones más robustas y de esta forma evitar sobrestimar la “utilización” de las especies domésticas por parte de este carnívoro, lo cual puede ser útil a la hora de tomar decisiones de manejo. Los resultados de los dos modelos utilizados para cuantificar el aporte de las presas, en términos de biomasa consumida, coinciden con que las especies que más aportaron fueron la liebre y el caballo, observándose una tendencia a la subestimación de las presas pequeñas y sobrestimación de las presas grandes por parte del modelo lineal (Ackerman et al. 1984). Los estimadores tróficos pueden maximizar la incidencia de las presas de tamaño grande (i.e., cuando el depredador regresa a alimentarse de una presa grande; Wilson 1984; Yáñez et al. 1986), pudiendo sobrestimar la ocurrencia numérica de estas en la dieta (Chakrabarti et al. 2016). El uso de la metodología propuesta por Chakrabarti et al. (2016), al ajustarse al carnívoro estudiado (i.e., incorporando el peso del carnívoro depredador en la ecuación), podría brindar informacion más precisa. Estas estimaciones pueden resultar relevantes para el puma, siendo un carnívoro que frecuentemente se ve involucrado en conflictos de depredación de ganado doméstico en la región (Fernández 2007; Fernández & Baldi 2014; Llanos et al. 2014, 2019). Estos ataques generan represalias por parte de los productores, como por ejemplo la caza (Llanos et al. 2014; Guerisoli et al. 2017). Si bien en el PNLG no hay reportes oficiales de depredación, sí hay registros en forma verbal (S. Queiro, com. pers.) sumado a que fuera del PN el puma es perseguido y cazado (obs. pers.).
Si bien los resultados aquí descriptos son preliminares y encuadrados en una época del año, es necesario continuar analizando la dieta del puma en la zona, incorporando la de otros carnívoros presentes en el PNLG y estudiar la disponibilidad de presas nativas. Los datos generados permitirán incrementar el conocimiento sobre la dieta de base del ensamble de carnívoros del PNLG, incorporando muestreos anuales o estacionales para evaluar si existen cambios en sus hábitos alimentarios, si se incrementa el consumo de especies exóticas, y anticipar la generación de posibles conflictos por la depredación de especies domésticas favoreciendo la coexistencia entre productores y carnívoros. Creemos que esta información de base aportará una mirada integral a las estrategias de manejo en el área protegida.
Agradecimientos
A la Administración de Parques Nacionales y al Parque Nacional Los Glaciares, especialmente al personal de la Seccional Lago Viedma. Al personal de la Dirección Regional Patagonia Austral por el asesoramiento brindado y la obtención de permisos de investigación. Al Centro de Investigación Esquel de Montaña y Estepa Patagónica por el uso de sus instalaciones para el procesamiento de las muestras, especialmente a Cecilia Brand. A la Universidad Nacional de la Patagonia San Juan Bosco, sede Esquel. Especialmente a Sergio Vincon y Adriana Kutschker. A todos los revisores que con sus aportes mejoraron este trabajo.
REFERENCIAS
Ackerman, B., F. Lindzey, & T. Hemker. 1984. Cougar food habits in southern Utah. Journal of Wildlife Management 48:147-155. https://doi.org/10.2307/3808462
Amaya, J. N., N. Bonino, R. Clarke, & M. Díaz. 1983. Informe preliminar sobre la situación actual de la liebre europea Lepus europaeus en la provincia de Santa Cruz. INTA EEA Bariloche, Informe Técnico. https://doi.org/10.1163/2210-7975hrd-0382-0068
Bank, M., R. Sarno., N. Campbell, & W. Franklin. 2002. Predation of guanacos (Lama guanicoe) by southernmost mountain lions (Puma concolor) during a historically severe winter in Torres del Paine National Park, Chile. Journal of Zoology 258:215-222. https://doi.org/10.1017/s0952836902001334
Bartolucci, C., M. Guerisoli, & G. Martin. 2020. Primer registro de basura en heces de puma (Puma concolor) en el Parque Nacional Los Glaciares, provincia de Santa Cruz, República Argentina. Notas sobre mamíferos sudamericanos, https://doi.org/10.31687/saremNMS.20.0.29
Bonino, N., D. Cossíos, & J. Menegheti. 2010. Dispersal of the European hare, Lepus europaeus in South America. Folia Zoologica 59:9-15. https://doi.org/10.25225/fozo.v59.i1.a3.2010
Bonzano, M., & C. Dellafiore. 2018. Atlas para la identificación de pelos de mamíferos de Argentina. 1era edición. Fundación BIORED. Río Cuarto, Argentina. Libro digital.
Buenavista, S., & F. Palomares. 2017. The role of exotic mammals in the diet of native carnivores from South America. Mammal Review 4:37-47. https://doi.org/10.1111/mam.12111
Burkart, R., N. Bárbaro, R. Sánchez, & D. Gómez. 1999. Eco-regiones de la Argentina. Programa de desarrollo institucional, componente de política ambiental, Administración de Parques Nacionales.
Cabrera, A. 1976. Regiones Fitogeográficas Argentinas. Enciclopedia Argentina de Agricultura y Ganadería 2:1-85.
Carman, R. 1976. About the hare and its introduction in Argentina. Diario La Prensa, agosto 15, Buenos Aires.
Castaño-Uribe, C., R. Hoogesteijn, A. Diaz-Pulido, & E. Payán (ed.). 2016. II. Conflictos entre felinos y humanos en América Latina. Serie Editorial Fauna Silvestre Neotropical. Instituto de Investigación de Recursos Biológicos Alexander von Humboldt (IAvH), Bogotá, D. C., Colombia. https://doi.org/10.47603/manovol4n2.46-53
Castillo Sánchez, L. et al. 2021. ¿Potencial depredación intragremio? Puma concolor y Lycalopex gymnocercus en el ecotono Chaco-Monte, San Luis, República Argentina. Notas sobre Mamíferos Sudamericanos 3:2-9. https://doi.org/10.31687/saremNMS.21.3.3
Chakrabarti, S., Y. Jhala, S. Dutta, Q. Qureshi, R. Kadivar, & V. Rana. 2016. Adding constraints to predation through allometric relation of scats to consumption. Journal of Animal Ecology 85:660-670. https:/doi.org/10.1111/1365-2656.12508
Chame, M. 2003. Terrestrial mammal feces: a morphometric summary and description. Memorias do Instituto Oswaldo Cruz 98:71-94. https://doi.org/10.1590/s0074-02762003000900014
Chébez, J., U. Pardiñas, & P. Teta. 2014. Mamíferos terrestres de la Patagonia sur de Argentina y Chile. 1ª Ed. Vázquez Mazzini.
Chehébar, C., & S. Martín. 1989. Guía para el reconocimiento microscópico de los pelos de los mamíferos de la Patagonia. Doñana Acta Vertebrata 16:247-291.
Colwell, R., & D. Futuyma. 1971. On the Measurement of Niche Breadth and Overlap. Ecological Society of America 52:567-576. https://doi.org/10.2307/1934144
Conforti, V., & F. De Azevedo. 2003. Local perceptions of jaguars (Panthera onca) and pumas (Puma concolor) in the Iguaçu National Park area, south Brazil. Biological Conservation, 111:215-221. https://doi.org/10.1016/s0006-3207(02)00277-x
Coronato, F. 2010. El rol de la ganadería ovina en la construcción del territorio de la Patagonia. Tesis doctoral. Institut des Sciences et Industries du Vivant et de l’Environnement (Agro Paris Tech). https://doi.org/10.35537/10915/53806
Day, M. 1966. Identification of hair and feather remains in the gut and faeces of stoats and weasels. Journal of Zoology 148:201-217. https://doi.org/10.1111/j.1469-998.1966.tb02948.x
Dudley, N. 2008. Directrices para la aplicación de las categorías de gestión de áreas protegidas. Gland, Suiza. IUCN. https://doi.org/10.2305/iucn.ch.2008.paps.2.es
Feinsinger, P., E. Spears, & R. Poole. 1981. A Simple Measure of Niche Breadth. Ecological Society of America 62:27-32. https://doi.org/10.2307/1936664
Fernández, C. 2007. Hábitos alimentarios del Puma (Puma concolor) en la Patagonia Árida. Tesis de grado. Universidad Nacional de la Patagonia San Juan Bosco, Puerto Madryn. https://doi.org/10.22201/fi.25940732e.2012.13n1.011
Fernández, C., & R. Baldi. 2014. Hábitos alimentarios del puma (Puma concolor) e incidencia de la depredación en la mortandad de guanacos (Lama guanicoe) en el noreste de la Patagonia. Mastozoología Neotropical 21:331-338. https://doi.org/10.22201/ie.20074484e.2014.4.2.196
Ferreyra, N., G. Aprile, & A. Vila. 2010. Dieta de Puma y Zorro Colorado en el Valle del Río de las Vueltas, Provincia de Santa Cruz. Informe preliminar. https://doi.org/10.4067/s0718-686x2011000100011
Foster, R., B. Harmsen, & C. Doncaster. 2010. Sample-size effects on diet analysis from scats of jaguars and pumas. Mammalia 74:317-321. https://doi.org/10.1515/mamm.2010.006
Franklin, W., W. Johnson, R. Sarno, & J. Iriarte. 1999. Ecology of the Patagonia puma Felis concolor patagonica in southern Chile. Biological Conservation 90:33-40. https://doi.org/10.1016/s0006-320700008-7
Gallardo, G., A., Nuñez, L., Pacheco, & M. Ruiz-García. 2009. Conservación del puma en el Parque Nacional Sajama (Bolivia): estado poblacional y alternativas de manejo. Mastozoología Neotropical 16:59-67.
Gelin, M., L. Branch, D. Thornton, A. Novaro, M. Gould, & Caragiulo. 2017. Response of pumas (Puma concolor) to migration of their primary prey in Patagonia. PLoS ONE 12, 12: e0188877. https://doi.org/10.1371/journal.pone.0188877
Gotelli, N., & R. Colwell.2001. Quantifying biodiversity: procedures and pitfalls in the measurement and comparison of species richness. Ecology Letters 4:379-391. https://doi.org/10.1046/j.1461-0248.2001.00230.x
Guerisoli, M., E. Luengos Vidal, M. Franchini, N. Caruso, E. Casanave, & M. Lucherini. 2017. Characterization of puma-livestock conflicts in rangelands of central Argentina. Royal Society Open Science 4:170852. https://doi.org/10.1098/rsos.170852
Guerisoli, M., E. Luengos Vidal, N. Caruso, A. Giordano, & M. Lucherini. 2020. Puma–livestock conflicts in the Americas: a review of the evidence. Mammal Review 5:228-246. https://doi.org/10.1111/mam.12224
Hamlin, K., S. Riley, D. Pyrah, A. Dodd, & R. Mackie. 1984. Relationships among mule deer fawn mortality, coyotes, and alternate prey species during the summer. Journal of Wildlife Management 48:489-499. https://doi.org/10.2307/3801181
Hernández-Guzmán, A., E. Payán, & O. Monroy-Vilchis. 2011. Hábitos alimentarios del Puma concolor (Carnivora: Felidae) en el Parque Nacional Natural Puracé, Colombia. Revista de Biología Tropical 59:1285-1294. https://doi.org/10.15517/rbt.v0i0.3399
Holmern, T., J., Nyahongo, & E., Roskaft. 2007. Livestock loss caused by predators outside the Serengeti National Park, Tanzania. Biological Conservation 135:518-526. https://doi.org/10.1016/j.biocon.2006.10.049
Inskip, C., & A. Zimmermann. 2009. Human-felid conflict: a review of patterns and priorities worldwide. Oryx 43:18-34. https://doi.org/10.1017/s003060530899030x
Iriarte, A., W. Franklin, W. Johnson, & K. Redford. 1990. Biogeographic variation of food habits and body size of the America puma. Oecologia 85:185-190. https://doi.org/10.1007/bf00319400
Jones, K. et al. 2009. PanTHERIA: a species-level database of life history, ecology, and geography of extant and recently extinct mammals. Ecology 90:2648-2648. https://doi.org/10.1890/08-1494.1
Khorozyan, I., T. Lumetsberger, A. Ghoddousi, M. Soofi, & M. Waltert. 2017. Global patterns in biomass models describing prey consumption by big cats. Mammal Review 47:124-132. https://doi.org/10.1111/mam.12084
Kolowski, J., & K. Holekamp. 2006. Spatial, temporal, and physical characteristics of livestock depredations by large carnivores along a Kenyan reserve border. Biological Conservation 128:529-541. https://doi.org/10.1016/j.biocon.2005.10.021
Krebs, C.1989. Ecological methodology. Harper and Row Publishers Inc., New York, EEUU.
Labropoulou, M., & A. Eleftheriou. 1997. The foraging ecology of two pairs of congeneric demersal fish species: importance of morphological characteristics in prey selection. Journal of Fish Biology 50:324-340. https://doi.org/10.1111/j.1095-8649.1997.tb01361.x
Lambertucci, S., S. Walker, & A. Novaro. 2014. Carnívoros y carroñeros renovaron la dieta (Capítulo 8, Recuadro 1): Ecología e historia natural de la Patagonia Andina: un cuarto de siglo de investigación en biogeografía, ecología y conservación (E. Raffaele, M. de Torres Curth, C. L. Morales & T. Kitzberger, eds.). Fundación de Historia Natural Félix de Azara. Ciudad Autónoma de Buenos Aires, Argentina. https://doi.org/10.35537/10915/52662
Llanos, R., A. Travaini, S. Montanelli, & E. Crespo. 2014. Estructura de edades de pumas (Puma concolor) cazados bajo el sistema de remoción por recompensas en Patagonia. ¿Selectividad u oportunismo en la captura? Ecología Austral 24:311-319. https://doi.org/10.25260/ea.14.24.3.0.8
Llanos, R., A. Andrade, & A. Travaini. 2019. Puma and livestock in central Patagonia (Argentina): from ranchers’ perceptions to predator management. Human Dimensions of Wildlife 2:1-16. https://doi.org/10.1080/10871209.2019.1668987
Llanos, R., & A. Travaini. 2020. Diet of puma (Puma concolor) in sheep ranches of central Patagonia (Argentina). Journal of Arid Environments 177:104-145. https://doi.org/10.1016/j.jaridenv.2020.104145
López-González, C., & A. González-Romero. 1998. A synthesis of current literature and knowledge about ecology of the puma (Puma concolor Linnaeus). Acta Zoológica Mexicana 75:171-190.
Martín, C. 1997. Plan preliminar de manejo Parque Nacional Los Glaciares. Administración de Parques Nacionales, Bariloche, Argentina.
Mishra, C. 1997. Livestock depredation by large carnivores in the Indian trans-Himalaya: conflict perceptions and conservation prospects. Environmental Conservation 24:338-343. https://doi.org/10.1017/s0376892997000441
Monroy-Vilchis, O., Y. Gómez-Ortiz, M. Janczur, & V. Urios. 2009. Food Niche of Puma concolor in Central Mexico. Wild Life Biology 15:97-105. https://doi.org/10.2981/07-054
Moreno, R., R. Kays, & R. Samudio, Jr. 2006. Competitive release in diets of ocelot (Leopardus pardalis) and puma (Puma concolor) after jaguar (Panthera onca) decline. Journal of Mammalogy 87:808-816. https://doi.org/10.1644/05-mamm-a-360r2.1
Moss, W., M. Alldredge, K. Logan, & J. Pauli. 2016. Human expansion precipitates niche expansion for an opportunistic apex predator (Puma concolor). Scientific Reports 6:39639. https://doi.org/10.1038/srep39639
Mwakatobe, A., J., Nyahongo, & E., Røskaft. 2013. Livestock depredation by carnivores in the Serengeti Ecosystem, Tanzania. Environment and Natural Resources Research 4:46-57. https://doi.org/10.5539/enrr.v3n4p46
Myers, P., R. Espinosa, C. Parr, T. Jones, G. Hammond, & T. Dewey. 2019. The Animal Diversity Web (online). Accessed at https://animaldiversity.org.
Navas, J. 1987. Los vertebrados exóticos introducidos en la Argentina. Revista del Museo Argentino de Ciencias Naturales Bernardino Rivadavia 2:8-38. https://doi.org/10.22179/revmacn.13.214
Novaro, A., M. Funes, & R. Walker. 2000. Ecological extinction of native prey of a carnivore assemblage in Argentine Patagonia. Biological Conservation 92:25-33. https://doi.org/10.1016/s0006-320700065-8
Novaro, A., M. Funes, & J. Jiménez. 2004. Patagonian foxes. Biology and Conservation of Wild Canids (D. Macdonald & C. Sillero-Zubiri, eds.). Oxford University Press, UK. https://doi.org/10.1093/acprof:oso/9780198515562.003.0015
Oksanen, J. et al.2007. Vegan: Community ecology package 10:631-637.
Pacheco, L., A. Lucero, & M. Villca. 2004. Dieta del puma (Puma concolor) en el Parque Nacional Sajama, Bolivia y su conflicto con la ganadería. Ecología en Bolivia 39:75-83. https://doi.org/10.4067/s0716-078x2009000100007
Pearson, O. 1995. Annotated keys for identifying small mammals living in or near Nahuel Huapi National Park, Southern Argentina. Mastozoología Neotropical 2:99-148.
Pia, M., & A. Novaro. 2005. Monitoreo de poblaciones de carnívoros y análisis de alternativas para reducir conflictos con la ganadería en el área circundante al Parque Nacional Monte León. Fundación Patagonia Natural. Informe final de consultoría. https://doi.org/10.4067/s0718-22442012000200010
Polis, G., & R. Holt 1992. Holt intraguild predation: The dynamics of complex trophic interactions.Trends in Ecology and Evolution 7:151-154. https://doi.org/10.1016/0169-5347(92)90208-s
Quintana, R., N. Madanes, P. Vuillermoz, & P. Otero. 2003. Relevamiento ambiental del campo “Los Huemules”, Provincia de Santa Cruz. Sistema de Relevamientos Ecológicos Rápidos. Fundación Vida Silvestre Argentina. Buenos Aires, Argentina. https://doi.org/10.35537/10915/44361
R Core Team. 2013. R: A language and environment for statistical computing. R Foundation for Statistical Computing, Vienna, Austria. URL http://www.R-project.org/
Rau, J., M. Tillería, D. Martínez, & A. Muñoz. 1991a. Dieta de Felis concolor (Carnivora: Felidae) en áreas silvestres protegidas del sur de Chile. Revista Chilena de Historia Natural 64:139-144.
Rau, J. et al. 1991b. Predación de pumas (Felis concolor) sobre pudúes (Pudu pudu): rol de las liebres (Lepus europaeus) como presas alternativas. Gestión en Recursos Naturales. Un enfoque integrado para el desarrollo (J. Oltremari, ed.). Sociedad de Vida Silvestre, Universidad Austral de Chile, UNESCO. https://doi.org/10.18846/renaysoc.2017.03.03.01.0001
Rau, J., & J. Jiménez. 2002. Diet of Puma (Puma concolor, Carnivora: Felidae) in Coastal and Andean Ranges of Southern Chile. Studies on Neotropical Fauna and Environment 37:201-205. https://doi.org/10.1076/snfe.37.3.201.8567
Reise, D. 1973. Clave para la determinación de los cráneos de marsupiales y roedores chilenos. Gayana: Zoología 27:3-20.
Scognamillo, D., I. Maxit, & J. Polisar. 2003. Coexistence of jaguar (Panthera onca) and puma (Puma concolor) in a mosaic landscape in the Venezuelan llanos. The Zoological Society of London 259:269-279. https://doi.org/10.1017/s0952836902003230
Serret, A. 2001. El Huemul: Fantasma de la Patagonia. Zagier & Urruty Publications, Buenos Aires, Argentina.
Skewes, O., C. Moraga, P. Arriagada, & J. Rau. 2012. El jabalí europeo (Sus scrofa): Un invasor biológico como presa reciente del puma (Puma concolor) en el sur de Chile. Sociedad de Biología de Chile. Revista Chilena de Historia Natural 85:227-232. https://doi.org/10.4067/s0716-078x2012000200009
Sogbohossou, E., H., De Iongh, B., Sinsin, G., De Snoo, & P. Funston. 2010. Human–carnivore conflict around Pendjari Biosphere Reserve, northern Benin. Oryx 45:569-578. https://doi.org/10.1017/s0030605310001109
Treves, A. et al. 2004. Predicting human-carnivore conflict: a spatial model derived from 25 years of data on wolf predation on livestock. Conservation Biology 18:114-125. https:/doi.org//10.1111/j.1523-1739.2004.00189.x
Vanstreels, R., F. Ramalho, & C. Adania. 2010. Microestrutura de pelos-guarda de felídeos brasileiros: considerações para a identificação de espécies. Biota Neotropical 10:333-337. https://doi.org/10.1590/s1676-06032010000100029
Villalobos, R. 2008. Hábitos predatorios del puma (Puma concolor) y su impacto en la ganadería de la provincia de Parinacota, región de Arica y Parinacota, Chile. Tesis de grado. Universidad de Chile. Santiago, Chile. https://doi.org/10.4206/rev.austral.cienc.soc.2013.n25-03
Wilson, P. 1984. Puma predation on guanacos in Torres del Paine National Park, Chile. Mammalia 45:515-522. https://doi.org/10.1515/mamm.1984.48.4.515
Yáñez, J., J. Cárdenas, P. Gezelle, & F. Jaksic. 1986. Food habits of the Southermost mountain lions (Felis concolor) in South America: natural versus livestocked ranges. Journal of Mammalogy 67:604-606. https://doi.org/10.2307/1381301
Zanón-Martínez, J., A. Travaini, S. Zapata, D. Procopio, & M. Santillan. 2012. The ecological role of native and introduced species in the diet of the puma (Puma concolor) in southern Patagonia. Oryx 46:106-111. https://doi.org/10.1017/s0030605310001821
Zanón-Martínez, J., M. Santillan, J. Sarasola, & A. Travaini. 2016. A native top predator relies on exotic prey inside a protected area: The puma and the introduced ungulates in Central Argentina. Journal of Arid Environments 134:17-20. https://doi.org/10.1016/j.jaridenv.2016.06.015
Apéndice 1
Número de identificación (ID), fecha de recolección, altitud, latitud al sur (S) y longitud al oeste (O) de los sitios de colecta de heces de Puma concolor en el Parque Nacional Los Glaciares (provincia de Santa Cruz, República Argentina) entre los años 2004 y 2006.

Apéndice 2
Lista de especies presentes en el Parque Nacional Los Glaciares (provincia de Santa Cruz, República Argentina) que pudieran ser potenciales presas de Puma concolor. Se indican las especies exóticas, domésticas y de valor especial por uno (*), dos (**) o tres (***) asteriscos, respectivamente. Fuente Sistema de información de Biodiversidad de la Administración de Parques Nacionales, actualizado en noviembre 2019.

Información adicional
Editor asociado: Dra. Sonia C. Zapata
Citar como: Bartolucci, C, S., M. M. Guerisoli & G.M. Martin. 2021. Nativas versus exóticas: ¿Cuánto contribuyen en la dieta del puma, Puma concolor, en el Parque Nacional Los Glaciares, Patagonia, Argentina? Mastozoología Neotropical, 28(2):e0572. https://doi.org/10.31687/saremMN.21.28.2.0.06.e0572
