Casos clínicos

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.
Recepción: 10 Junio 2022
Aprobación: 01 Agosto 2022
Resumen:
Introducción: los teratomas maduros pertenecen al grupo de los tumores de ovario de estirpe germinal; por lo general, tienen un comportamiento benigno. La transformación maligna ocurre en un rango de 0.2 a 1% de los tumores. El objetivo es mostrar los resultados de peritonectomía con HIPEC en el tratamiento de un teratoma maduro con diferenciación maligna con células en anillo de sello.
Caso clínico: mujer de 43 años de edad, con diagnóstico de teratoma maduro maligno con células en anillo de sello. Se realizó cirugía de citorreducción primaria optima; histerectomía total, salpingooforectomía bilateral, peritonectomía, apendicectomía, colecistectomía y esplenectomía, además de quimioterapia hipertérmica intraoperatoria (HIPEC).
Conclusiones: la transformación maligna de un teratoma maduro del ovario es un evento raro, pero no excepcional. Se utilizó HIPEC posterior a la citorredución óptima y hubo buenos resultados, ya que la paciente lleva un periodo libre de enfermedad de 36 meses. Es necesario el reporte de casos a fin de comparar diversos tipos de tratamiento para mejorar resultados oncológicos.
Palabras clave: Teratoma Maduro, Carcinoma, Células en Anillo de Sello, Quimioterapia Intraperitoneal Hipertérmica.
Abstract:
Background: Mature teratomas belong to the group of germ line ovarian tumors; they generally have benign behavior. Malignant transformation occurs in 0.2% to 1% of tumors. The objective is to show the results of peritonectomy with HIPEC in the treatment of a mature teratoma with malignant differentiation with signet ring cells.
Clinical case: 43-year-old woman diagnosed with mature malignant teratoma with signet ring cells. It was performed optimal primary cytoreduction surgery, total hysterectomy, bilateral salpingo-oophorectomy, peritonectomy, appendectomy, cholecystectomy and splenectomy adding intraoperative hyperthermic chemotherapy (HIPEC).
Conclusions: Malignant transformation of a mature teratoma of the ovary is a rare event, but not exceptional. HIPEC was used after optimal cytoreduction, with good results, since the patient is in a disease-free period of 36 months. It is necessary to report cases in order to compare different types of treatment to improve oncological results.
Keywords: Teratoma, Mature, Carcinoma, Signet Ring Cell, Hyperthermic Intraperitoneal Chemotherapy.
Introducción
El teratoma maduro es el tumor de ovario de mayor incidencia, pues constituye 10-20% de todos los tumores de ovario. Es de estirpe germinal y por lo general tiene un comportamiento benigno.1,2 Se compone de tejido maduro de ectodermo, mesodermo y endodermo.3
La transformación maligna ocurre en un rango que va del 0.2 al 1% de los teratomas maduros.4,5,6,7 Se diagnostican entre los 30 y los 70 años, con un pico de incidencia entre los 40 y los 60 años. La mayoría de las pacientes son posmenopáusicas, con una mediana de 50.6 años.8,9El carcinoma de células escamosas (SCC por sus siglas en inglés) representa más del 80% de los casos,4,6 seguido del adenocarcinoma derivado del epitelio ciliado respiratorio, el melanoma, el tumor carcinoide, el carcinoma de tiroides, el oligodendroglioma y el sarcoma.2 El SCC derivado de la transformación maligna del teratoma maduro se ha revisado en informes anteriores y se ha analizado su perfil clínico. En 2008 se publicó una revisión sistemática de 277 casos por Akazawa et al., quienes informaron las características clínicas del SCC. Sin embargo, en histologías no escamosas, el tratamiento y el pronóstico no es claro, por lo que es de especial interés hacer una revisión de la literatura disponible. El objetivo de esta publicación es mostrar el tratamiento y los resultados obtenidos en teratoma maduro con diferenciación maligna en células en anillo de sello, tratado con pertinectomía con quimioterapia hipertérmica intraoperatoria (HIPEC por sus siglas en inglés), del cual hasta el momento solo se tiene un reporte de caso.4
La transformación maligna es difícil de dignosticar en la etapa preoperatoria, ya que se asemeja a un teratoma quístico maduro.3,8 Algunos de los cambios que la sugieren son la adherencia a las estructuras pélvicas circundantes, los nódulos, las placas o el engrosamiento en la pared del quiste.5,10
La utilidad clínica de los marcadores tumorales no está clara.7 Sin embargo, en algunas series el nivel de CA-125 fue significativamente más alto en no SCC que en SCC.4,6
El tratamiento quirúrgico ha constituido el pilar del manejo. En la serie más grande reportada por Akazawa et al., se hizo histerectomía abdominal con salpingooforectomía bilateral en el 80% de las pacientes con SCC y no SCC. Otros autores publicaron tratamientos preservadores de la fertilidad, incluida la salpingooforectomía unilateral o la cistectomía. Aproximadamente la mitad de los pacientes de ambos grupos se sometieron a omentectomía y linfadenectomía, sin diferencias significativas en la tasa de cada abordaje quirúrgico, y se reportó que la linfadenectomía mejoró las tasas de supervivencia en estadios avanzados, pero no la omentectomía.4,11,12 Tseng et al. sugirieron ooforectomía unilateral conservadora sin necesidad de tratamiento postoperatorio, en etapa clínica IA, en pacientes jóvenes y nulíparas.5,7
Adyuvancia
La quimioterapia adyuvante de primera línea para los cánceres de ovario epiteliales es el régimen más utilizado en SCC y no SCC. El carboplatino/paclitaxel es el esquema utilizado con más frecuencia, aunque parece ser menos eficaz en comparación con los cánceres epiteliales comunes de ovario.11,13 Se debate el papel de la radioterapia y la quimiorradioterapia.2
Sobrevida global
La sobrevida global en pacientes con tratamiento quirúrgico y adyuvancia con quimioterapia reportada en la literatura no difirió significativamente y mostró mejor pronóstico en el estadio I, en comparación en los estadios II, III y IV.
Se ha reportado un tiempo medio de sobrevida global de 51.8 meses (rango de 12-140 meses). De un total de 15 series de casos con 155 pacientes, solo un caso presentó células en anillo de sello y se trató con carboplatino/paclitaxel, por lo que no existe información suficiente que permita comparar esquemas de tratamiento.2,4
Pronóstico
El pronóstico de los pacientes con transformación maligna en teratoma es adverso8,9 y la mayoría mueren en el plazo de un año.11 Sin embargo, el pronóstico es mejor si el tumor se limita a un ovario con cápsula intacta y con un grosor uniforme de la pared del quiste.5 Stamp et al. informaron otros factores asociados a mal pronóstico: diseminación tumoral, ascitis, adherencia y tipo de tumor distinto del SCC.11,14,15
Caso clínico
Se describe el caso de una mujer de 43 años de edad, con antecedente de ser madre con cáncer de mama, diagnosticado antes de la menopausia. La paciente comenzó con síntomas gastrointestinales inespecíficos, como plenitud postprandial, aumento del perímetro abdominal, dolor abdominal intermitente con predominio en el mesogastrio de 12 meses de evolución. Posteriormente, se agregó disnea de medianos esfuerzos. La paciente acudió con un médico de primer contacto, quien estableció el protocolo de estudio y le solicitó ultrasonido de abdomen y pelvis, el cual evidenció un tumor que abarcaba la totalidad de la cavidad abdominal, y complementó el estudio con tomografía computarizada contrastada de tórax, abdomen y pelvis, la cual mostró un tumor de 27.5 x 12.7 x 28.2 cm, heterogéneo, de predominio líquido, con presencia de septos (figuras 1 y 2).
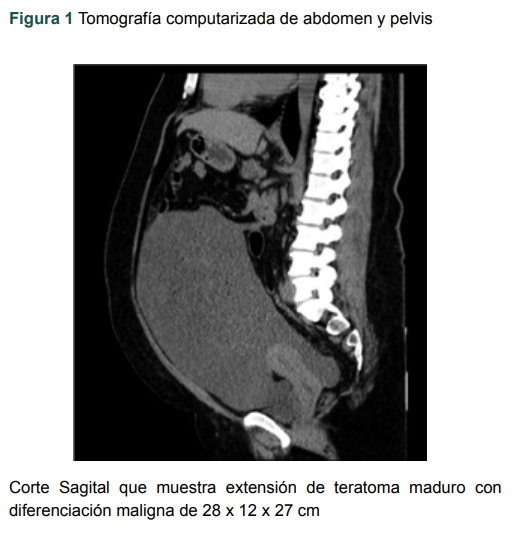
Figura 1
Tomografía computarizada de abdomen y pelvis
Corte Sagital que muestra extensión de teratoma maduro con diferenciación maligna de 28 x 12 x 27 cm
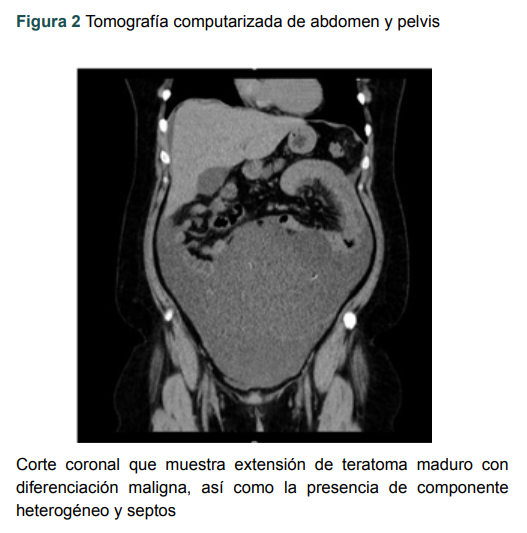
Figura 2
Tomografía computarizada de abdomen y pelvis
Corte coronal que muestra extensión de teratoma maduro con diferenciación maligna, así como la presencia de componente heterogéneo y septos
Los marcadores tumorales presentaron Ca 125 en 84.16, ACE 10.07, AFP 1.83, B-HGC 0.1. La biometría hemática mostró pruebas de función hepática y tiempos de coagulación dentro de parámetros normales. La paciente fue enviada al Servicio de Tumores Ginecológicos del Hospital de Oncología del Centro Médico Nacional Siglo XXI, donde propusimos laparotomía con estudio transoperatorio. Se procedió a intervención quirúrgica en la que se llevó a cabo salpingooforectomía izquierda, la cual fue enviada a estudio transoperatorio.
En el evento quirúrgico se encontró mucinosis, con un índice de carcinomatosis de 16 puntos, con implantes de mucina en toda la extensión del peritoneo parietal, cápsula de Gleason y bazo, además de tumor de ovario izquierdo roto (figura 3).
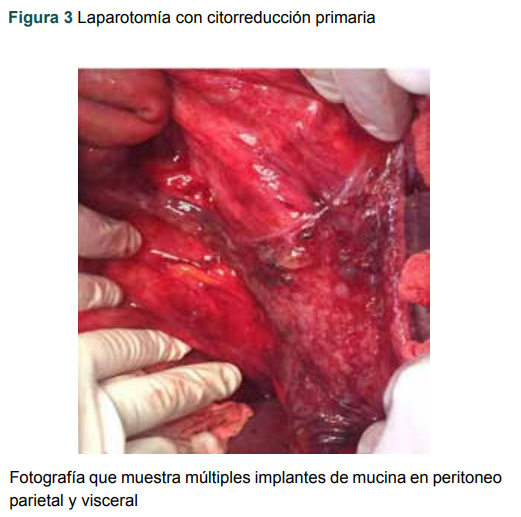
Figura 3
Laparotomía con citorreducción primaria
Fotografía que muestra múltiples implantes de mucina en peritoneo parietal y visceral
Se recibió en estudio transoperatorio el ovario izquierdo de 3450 g, que midió 28 x 27 x 14 cm, con cápsula rota, superficie interna multiloculada con contenido mucinoso y se identificó un área quística de 7 x 6.5 cm, con contenido sebáceo y pelos. A los cortes histológicos, se observó tejido de ectodermo compuesto por epitelio escamoso y folículos pilosos, así como tejido de endodermo compuesto por epitelio de tipo intestinal, el cual en diversos cortes presentó atipia marcada con disposición arquitectural compleja hasta llegar a encontrar células en anillo de sello, correspondiente a adenocarcinoma. No se identificaron elementos inmaduros en el muestreo del tumor (figuras 4 y 5).
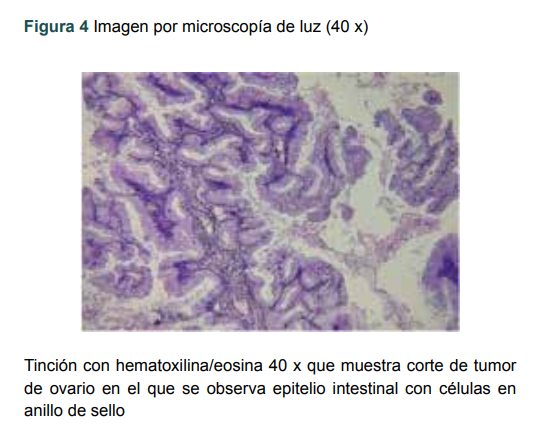
Figura 4
Imagen por microscopía de luz (40 x)
Tinción con hematoxilina/eosina 40 x que muestra corte de tumor de ovario en el que se observa epitelio intestinal con células en anillo de sello
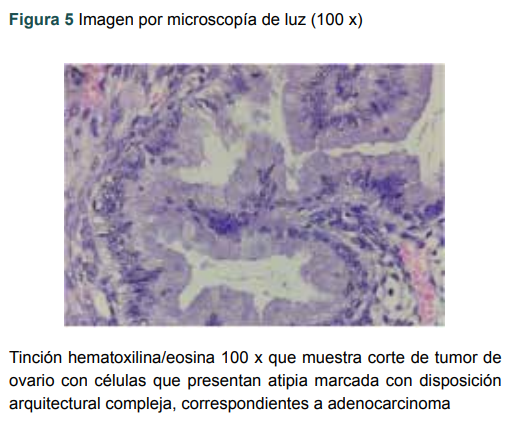
Figura 5
Imagen por microscopía de luz (100 x)
Tinción hematoxilina/eosina 100 x que muestra corte de tumor de ovario con células que presentan atipia marcada con disposición arquitectural compleja, correspondientes a adenocarcinoma
Se continuó con la cirugía etapificadora y citorreductora de ovario, que consistió en histerectomía total + salpingooforectomía bilateral + peritonectomía + apendicectomía. Ante hallazgos de actividad tumoral se decidió realizar colecistectomía y esplenectomía y se adicionó quimioterapia hipertérmica intraoperatoria con 45 mg de cisplatino en 1000 mL de solución salina fisiológica al 0.9% a 40 grados centígrados, y se logró una citorreducción óptima, que se clasificó como etapa IIIC. Asimismo, se observaron implantes del tumor (adenocarcinoma) en el omento, la cápsula hepática y la cápsula esplénica en el reporte histopatológico.
La paciente fue enviada al Servicio de Oncología Médica y se le consideró candidata a recibir adyuvancia con carboplatino y paclitaxel en seis ciclos, los cuales finalizaron sin eventualidades. Por el momento, tiene buenos resultados oncológicos, con periodo libre de enfermedad de siete meses; se encuentra en seguimiento en el Servicio de Tumores Ginecológicos.
Discusión
Los teratomas maduros son tumores benignos comunes y representan del 10 al 20% de todos los tumores de ovario; sin embargo, la diferenciación maligna es bastante infrecuente y su incidencia ronda entre el 0.2 y 2%. Hay series como la de Wei et al. que reportan un 7.6% de transformación maligna. La incidencia en grupo de pacientes posmenopáusicas fue de 75%16 y en 80% de los casos en carcinoma de células escamosas. La diferenciación maligna en células en anillo de sello solo se encontró en 0.6% de los casos en la serie más grande publicada, con un total de un caso, por lo que hay poca evidencia científica acerca del pronóstico y el tratamiento.17,18 Existen otras series de casos reportados en la literatura, las cuales pueden servir de preámbulo para el tratamiento en los casos con diferenciación maligna en anillo de sello. En el cuadro I se incluyen las series más relevantes, ya que al ser un caso excepcional no contamos con antecedentes.
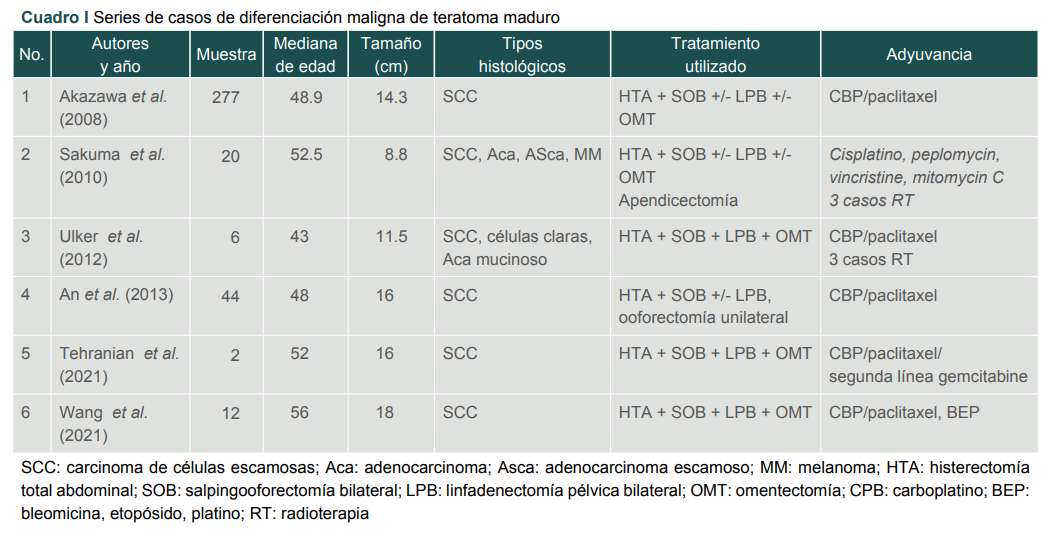
Cuadro I
Series de casos de diferenciación maligna de teratoma maduro
SCC: carcinoma de células escamosas; Aca: adenocarcinoma; Asca: adenocarcinoma escamoso; MM: melanoma; HTA: histerectomía total abdominal; SOB: salpingooforectomía bilateral; LPB: linfadenectomía pélvica bilateral; OMT: omentectomía; CPB: carboplatino; BEP: bleomicina, etopósido, platino; RT: radioterapia
Se debe considerar la posibilidad de transformación maligna, especialmente en mujeres posmenopáusicas y cuando hay tumores de gran tamaño.19 Los marcadores tumorales prequirúrgicos no han jugado un papel relevante en la diferenciación de los teratomas benignos y malignos, especialmente en los diferentes a los de células escamosas; por lo tanto, se requiere un mayor esfuerzo para desarrollar nuevos biomarcadores para el diagnóstico temprano, junto con la evaluación y el seguimiento de los tratamientos. El examen de la sección congelada juega un papel activo en la identificación tanto del método de tratamiento quirúrgico como del pronóstico del paciente.5,20 Dada la rareza de estas neoplasias es muy probable que en el estudio transoperatorio no se llegue a identificar la zona de transformación maligna del teratoma, ya que el muestreo extenso del tumor se hace en el estudio definitivo.19 La transformación maligna puede presentarse en cualquiera de las tres capas de células germinales (ectodermo, mesodermo y endodermo) y la más común es la originada del ectodermo, que es el carcinoma epidermoide que corresponde a un 80% de los casos reportados.21 Otras neoplasias que pueden presentarse son adenocarcinomas, carcinoma adenoescamoso, carcinoma tiroideo, carcinoma sebáceo, melanoma, sarcomas y neoplasias neuroendócrinas que representan del 0.2 al 1.4%.8,14,22
En nuestro caso tuvimos la fortuna de que se identificó un área multiloculada compacta sospechosa, a la que se le realizó corte congelado y mostró múltiples glándulas con arquitectura compleja y atipia nuclear que ayudó con el diagnóstico transoperatorio. Respecto a la inmunohistoquímica Yan et al. encontraron que p62 y la caspasa 8 pueden convertirse en nuevos biomarcadores de pronóstico para el tratamiento del cáncer de ovario.16,23
Respecto al tratamiento, al igual que los tumores epiteliales, la mayoría recibe quimitoterapia adyuvante a base de platinos, más comúnmente asociado a taxanos o bien en combinación con bleomicina y etopósido.24 En la serie de 14 casos publicada por Qin et al., 12 pacientes obtuvieron remisión completa de la enfermedad; sin embargo, se presentó progresión en dos casos cuya sobrevida fue de 26.3 meses, lo cual sugiere que la mayoría puede responder bien a la quimioterapia. Las tasas estimadas de sobrevida global y supervivencia libre de enfermedad a cinco años fueron 31.2 y 31.6%, respectivamente.17
La paciente presentada fue tratada con quimioterapia hipertérmica asociada a peritonectomía, debido a que según estudios publicados por Van Driel et al. entre las pacientes con cáncer de ovario epitelial en estadio III, la adición de HIPEC a la cirugía citorreductora resultó en mayor periodo libre de progresión y aumento en la sobrevida global, comparada con la cirugía sola y no dio lugar a tasas mayores de efectos secundarios. Si bien todo ello se ha demostrado en el contexto de cirugías de intervalo, en el caso de nuestra paciente fue otorgada en cirugía citorreductora primaria con buenos resultados oncológicos; sin embargo, se requieren más estudios para sugerirlo como tratamiento estándar, pues este caso es el primero reportado con este tratamiento y características.25
Conclusiones
La transformación maligna de un teratoma maduro del ovario es un evento raro, pero no excepcional que suele presentarse como un hallazgo patológico incidental. Representa un reto para el ginecólogo oncólogo. No se pueden planificar ensayos prospectivos aleatorizados sobre el tratamiento quirúrgico y postoperatorio debido a la rareza de estas neoplasias malignas. Sin embargo, una gran base de datos centralizada internacional podría maximizar el conocimiento de los médicos para definir mejor las pautas de tratamiento, por lo que este trabajo es una aportación sumamente valiosa para una base de datos futura, especialmente en esta histología y tratamiento.2
Referencias
1. Mathew MR, Ramdas A, Kurian SS, Kuruvilla L, Singh N. A rare malignant transformation of an ovarian cystic teratoma: A case report. Case Rep Pathol. 2018;2018:1-4. doi: 10.1155/2018/6892783
2. Gadducci A, Pistolesi S, Guerrieri M, Cosio S, Carbone F, Naccarato A. Malignant Transformation in Mature Cystic Teratomas of the Ovary: Case Reports and Review of the Literature. Anticancer Res. 2021(6):3669-75. doi: 10.21873/anticanres.12644
3. Black JD, Roque DM, Pasternak MC, Buza N, Rutherford TJ, Schwartz PE, et al. A Series of Malignant Ovarian Cancers Arising From Within a Mature Cystic Teratoma A Single Institution Experience Int J Gynecol Cancer. 2015;25(5):792-7. doi: 10.1097/IGC.0000000000000431
4. Akazawa M, Onjo S. Malignant Transformation of Mature Cystic Teratoma Is Squamous Cell Carcinoma Different From the Other Types of Neoplasm? Int J Gynecol Cancer. 2018;28(9):1650-6. doi: 10.1097/IGC.0000000000001375
5. Sayhan S, Ayaz D, Demir Keçeci S, Dicle N, Kiliçalp A, Hanhan M. Malign Transformation in the Mature Cystic Teratoma of the Ovary: Presentation of 9 Case Studies. Turkiye Klinikleri J Gynecol Obst. 2015;25(1):1-6.
6. Shimada T, Higashijima A, Fukushima A, Komatsu N, Noguchi M, Ohashi K, et al. Malignant transformation from mature cystic teratoma of the ovary: Malignant transformation from teratoma. J Obstet Gynaecol Res. 2019;45(9):1957-60. doi:10.1111/jog.14043
7. Rim SY, Kim SM, Choi HS. Malignant transformation of ovarian mature cystic teratoma. Int J Gynecol Cancer. 2006;16:140-4. doi: 10.1111/j.1525-1438.2006.00285.x
8. Mandal S, Badhe BA. Malignant transformation in a mature teratoma with metastatic deposits in the omentum: a case report. Case Rep Pathol. 2012;2012:568062. doi:10.1155/2012/568062
9. Rathore R, Sharma S, Agarwal S. Malignant transformation in mature cystic teratoma of the ovary: a retrospective study of eight cases and review of literature. Prz Menopauzalny. 2018;17(2):63-8. doi:10.5114/pm.2018.77304
10. Kelly RR, Scully RE. Cancer developing in dermoid cyst of the ovary. A report of 8 cases, including carcinoid and a leiomyo- sarcoma. Cancer. 1961;14:989-1000.
11. Tehranian A, Ghahghaei-Nezamabadi A, Seifollahi A, Kasraei S, Dehghani-Nejad H, Maleki-Hajiagha A. Ovarian mature cystic teratoma with malignant transformation: two case reports. J Med Case Rep. 2021;15(1):23. doi:10.1186/s13256-020-02594-4
12. Toba N, Takahashi T, Ota K, Takanashi A, Iizawa Y, Endo Y, et al. Malignant transformation arising from mature cystic teratoma of the ovary presenting as ovarian torsion: a case report and literature review. Fukushima J Med Sci. 2020;66(1):44-52. doi:10.5387/fms.2019-31
13. Vang R, Gown AM, Zhao C, Barry TS, Isacson C, Richardson MS, et al. Ovarian mucinous tumors associated with mature cystic teratomas: morphologic and immunohistochemical analysis identifies a subset of potential teratomatous origin that shares features of lower gastrointestinal tract mucinous tumors more commonly encountered as secondary tumors in the ovary. Am J Surg Pathol. 2007;31(6):854-69. doi:10.1097/pas.0b013e31802efb4
14. Sakuma M, Otsuki T, Yoshinaga K, Utsunomiya H, Nagase S, Takano T, et al. Malignant transformation arising from mature cystic teratoma of the ovary: a retrospective study of 20 cases. Int J Gynecol Cancer. 2010;20:766-71.
15. Mandal S, Badhe BA. Malignant Transformation in a Mature Teratoma with Metastatic Deposits in the Omentum: A Case Report. Case Reports in pathology. 2012. Article ID 568062. doi: 10.1155/2012/568062
16. Wei F, Jiang Z, Yan C. Analysis of 20 mature ovarian cystic teratoma cases in postmenopausal women. Chin Med J (Engl). 2001;114:137-8.
17. Qin L, Zhao T, Liu X, Wang H, Gu X, Chen D, et al. Malignant transformation arising from mature ovarian cystic teratoma: A case series. Medicine. 2021;100:13(e24726). doi: 10.1097/MD.0000000000024726
18. Vang R, Gown AM, Zhao C, Barry TS, Isacson C, Richardson MS, et al. Ovarian mucinous tumors associated with mature cystic teratomas: morphologic and immunohistochemical analysis identifies a subset of potential teratomatous origin that shares features of lower gastrointestinal tract mucinous tumors more commonly encountered as secondary tumors in the ovary. Am J Surg Pathol. 2007;31(6):854-69. doi:10.1097/pas.0b013e31802efb45
19. Belaid I, Khechine W, Ben Abdelkader A, Bedioui A, Ezzairi F, Chabchoub I, et al. Adenocarcinoma of intestinal type arising in mature cystic teratoma of ovary: A diagnostic dilemma. Clin Case Rep. 2020;8:644-7. doi: 10.1002/ccr3.2718
20. Vernea F, Volodarsky-Perel A. Mature Cystic Teratoma of Ovary With Mucinous Epithelial Neoplasm and Malignant Mural Nodule. A Case Report and Review of the Literature. International Journal of Gynecological Pathology. 2015;34(1):25-9. doi: 10.1097/pgp.0000000000000110
21. Bonnett BM, Seidman JD. Mucinous tumors arising in ovarian mature cystic teratomas. Relationship to the clinical syndrome of pseudomyxoma peritonei. Am J Surg Pathol. 2003;27:650-7.
22. An JS, Wu LY, Li XG, Zhang R, Song Y, Ma SK, et al. [Clinical analysis of 44 cases with malignant transformation of ovarian mature cystic teratoma.] [Article in Chinese] Zhonghua Fu Chan Ke Za Zhi. 2013;48:123-8.
23. Jamor J, Conte AB, Alaoui FZF, Jayi S, Chaara H, Melhouf MA. Malignant transformation of ovarian mature teratoma: 04 cases report, review of the literature. Int J Reprod Contracept Obstet Gynecol. 2020;9:819-24.
24. Wang X, Li W, Kong Y, Liu X, Cui Z. Clinical analysis of 12 cases of ovarian cystic mature teratoma with malignant transformation into squamous cell carcinoma. J Int Med Res. 2021;49(2):300060520981549. doi: 10.1177/0300060520981549
25. Van Driel WJ, Koole SN, Sikorska K, Schagen van Leeuwen JH, Schreuder, HWR, Hermans RHM, et al. Hyperthermic Intraperitoneal Chemotherapy. N Engl J Med. 2018;378:230-40. doi: 10.1056/NEJMoa1708618
Notas de autor
Comunicación con: Magaly Denise Peña Arriaga Teléfono: 81 8010 6591
Información adicional
Declaración de conflicto de interés:: los autores han completado y enviado la forma traducida al español de la declaración de conflictos potenciales de interés del Comité Internacional de Editores de Revistas Médicas, y no fue reportado alguno relacionado con este artículo.
Enlace alternativo
http://revistamedica.imss.gob.mx/editorial/index.php/revista_medica/article/view/4682/4492 (pdf)
