Artículo original
Recepción: 08 Julio 2019
Aprobación: 24 Octubre 2019
DOI: https://doi.org/10.29262/ram.v66i4.643
Resumen : El impacto sanitario y económico de las enfermedades alérgicas está aumentando rápidamente y se necesitan cambios en las estrategias para su manejo. Su influencia reduce al menos en un tercio la capacidad de desempeño laboral y escolar. Los ICP (Vías Integradas de Atención) de las enfermedades de las vías respiratorias son planes de atención estructurados y multidisciplinarios, que promueven las recomendaciones de las guías en protocolos locales y su aplicación a la práctica clínica. En este documento se presenta un resumen ejecutivo para Argentina, México y España. Se desarrollan las guías ARIA de próxima generación para el tratamiento farmacológico de la rinitis alérgica (RA) utilizando las pautas basadas en GRADE para RA, probadas con evidencia de la vida real proporcionada por tecnología móvil basada en escalas visuales analógicas. Se concluye que en el tratamiento de la RA, los antihistamínicos anti-H1 son menos efectivos que los corticoides intranasales (CINS), que en la rinitis grave los CINS representan la primera línea de tratamiento, y que la combinación intranasal de CINS + anti-H1 es más eficaz que la monoterapia. Sin embargo, según el estudio MASK observacional en vida real, los pacientes tienen pobre adherencia al tratamiento y frecuentemente se automedican de acuerdo con sus necesidades.
Palabras clave: ARIA, Rinitis alérgica, Vías integradas de atención, Estudios en vida real, Adherencia, Automedicación.
Abstract: The health and economic impact of allergic diseases are increasing rapidly, and changes in management strategies are required. Its influence reduces the capacity of work and school performance by at least a third. The ICPs of the airways (integrated care pathways for respiratory diseases) are structured multidisciplinary healthcare plans, promoting the recommendations of the guidelines in local protocols and their application to clinical practice. This document presents an executive summary for Argentina, Mexico, and Spain. Next-generation ARIA guidelines are being developed for the pharmacological treatment of allergic rhinitis (AR), using the GRADE-based guidelines for AR, tested with real-life evidence provided by mobile technology with visual analogue scales. It is concluded that in the AR treatment, H1-antihistamines are less effective than intranasal corticosteroids (INCS), in severe AR the INCS represent the first line of treatment, and intranasal combination INCS + anti-H1 is more effective than monotherapy. However, according to the MASK real-life observational study, patients have poor adherence to treatment and often self-medicate, according to their needs.
Keywords: ARIA, Allergic rhinitis, Integrated care pathways, Real life, Adherence, Self medication.
Antecedentes
En todas las sociedades, la carga y el costo de las enfermedades alérgicas están aumentando rápidamente y se necesitan cambios de estrategias de gestión para sustentar la transformación del sistema de atención de la salud para su atención integrada.1
Hasta el momento existen tres países hispanoparlantes (Argentina, España y México) en los que se ha implementado la app MASK-Air (actualización de Diario de Alergia) para la atención integrada de la rinitis alérgica (RA).
Argentina
Los estudios epidemiológicos evidencian que la RA es la enfermedad respiratoria crónica más frecuente. Para que dichos estudios puedan ser comparables y confiables requieren metodologías validadas, como The International Study of Asthma and Allergies in Childhood (ISAAC), del que participaron diversas ciudades argentinas (Buenos Aires, Rosario, Córdoba, Neuquén y Salta) en sus fases I y III,2,3 incluyendo los grupos etarios de seis y siete años y 13 y 14 años. Específicamente en 2002, los resultados del ISAAC fase III en el grupo de 13 y 14 años mostraron una prevalencia de síntomas de rinitis entre 22.8 y 40 %, aunque tomando síntomas asociados de rinitis y conjuntivitis, los cuales son más indicativos de RA, el rango de frecuencia varió entre 11.3 y 20.9 %. El promedio de síntomas de rinitis a nivel nacional fue de 34.9 % y de rinoconjuntivitis de 16 %, mientras que solo 12.7 % recibió diagnóstico alguna vez.3,4
Más recientemente, en 2014, se realizó una encuesta nacional (Prevalencia en Argentina de Rinitis Alérgica, PARA) utilizando una metodología diferente a ISAAC, que incluyó pacientes de cinco a 44 años entrevistados telefónicamente. La prevalencia global de síntomas de RA fue de 20.5 %. No hubo diferencias estadísticamente significativas entre los tres grupos etarios, dado que los porcentajes de prevalencia fueron de 21.1 % para el grupo de cinco a 11 años, 23.1 % para el de 12 a 19 años y 19.4 % para el de 20 a 44 años.5
En este contexto, el subdiagnóstico es posible. Además de los datos mencionados, el estudio AILA,6 que incluyó pacientes de cuatro a 60 años con diagnóstico médico de rinitis, mostró una prevalencia en Argentina de 3.6 % y, finalmente, el estudio PARA mostró que 63.8 % de los pacientes con síntomas de rinitis no tenía diagnóstico médico.5
El impacto de la rinitis en la capacidad del desempeño laboral y escolar evidenció una disminución de 33 % en los días con mayor sintomatología, similar a lo que evidencia el estudio AIM en asma bronquial.7 Además, el estudio AILA describió que la utilización de productos de venta libre en el tratamiento de la rinitis es de 42 % en adultos y de 25 % en niños.
Los datos precedentes avalan el concepto de que la rinitis es una enfermedad subestimada por los pacientes, infradiagnosticada por los médicos y, consecuentemente, subtratada.
España
Se han realizado diferentes estudios epidemiológicos para evaluar la prevalencia de la rinitis. En el estudio ISAAC, desarrollado en 1994 en 56 países, se estableció una prevalencia media de 14.9 % en niños entre seis y siete años y de 39.7 % en niños entre 13 y 14 años. En España, la prevalencia en la población pediátrica se estableció en 21.8 %.8 En una fase posterior, realizada en 2001-2004, la prevalencia de rinitis pediátrica en cualquier momento fue de 39.2 %.9 Se observó incremento de la prevalencia de la presencia de síntomas de alergia, especialmente de rinoconjuntivitis en los últimos 12 meses (RM = 1.61, IC 95 % = 1.48-1.76) al comparar ambas fases, después de ajustar por sexo, centro y variación estacional. La prevalencia de síntomas de RA fue mayor en los niños que en las niñas. Se apreciaron amplias variaciones entre centros con elevadas prevalencias en Asturias, Madrid, Cartagena y Bilbao. Las menores se observaron en Barcelona, Castellón y Pamplona.10
En 2004 se realizó un estudio en diversos países europeos (Bélgica, Francia, Alemania, Italia, España y Reino Unido), mediante 9646 encuestas telefónicas y un estudio médico en un subgrupo de 725 personas, con lo que se registró una prevalencia de rinitis de 22.7 % en la población europea general adulta y 21.5 % en España.11 En un estudio realizado en 2014 entre 2603 trabajadores españoles, la prevalencia de rinitis fue de 16.9 %.12
Alergológica 2015 es un estudio epidemiológico efectuado en los servicios de alergia españoles. La muestra fue de 2914 pacientes atendidos en centros públicos y privados de toda España. Se invitó a participar a 500 alergólogos. Los datos se compararon con los de los estudios de 1992 y 2005. La rinoconjuntivitis fue el principal motivo de consulta, que afectó a 52.5 % de pacientes adultos13 y 53.8 % de pacientes pediátricos,14 ligeramente inferior a los estudios previos. La etiología fue alérgica en 79.3 % de los casos. La causa más frecuente fue la alergia a pólenes (70.8 %), seguida de ácaros, epitelios de mascotas y hongos. Según la clasificación ARIA (Allergic Rhinitis and its Impact on Asthma) modificada,15 la rinitis fue persistente en 66 % de los casos y la intensidad fue leve en 29.9 %, moderada en 59.7 % y grave en 8.7 %. Mediante el cuestionario ESPRINT16 se evaluó la afectación de la calidad de vida: la dimensión más afectada fue la de los síntomas seguida por el sueño, por encima de las actividades diarias o aspectos psicológicos.
En la población general, según los datos del European Community Health Survey, la prevalencia de asma en España es baja, con una notable variabilidad regional (Albacete, 10 %; Barcelona, 5 %; Galdácano, 14.5 %; y Oviedo, 9.4 %).17 En Alergológica 2015, 21.2 % de los pacientes que acudían a consultas de alergia presentaba asma bronquial;13,14 fue intermitente en 38.3 % y persistente en 57.5 %. El control, según GINA, fue bueno en 35 %, parcial en 31 % y malo en 10 %. La mayoría de los pacientes con asma fueron alérgicos (82.2 %), mientras que en 16.8 % la RA fue intrínseca. Hubo predominio en mujeres.
México
Este país también participó en los estudios ISAAC. En la tercera fase de ISAAC se reportó 11.6 % de niños entre seis y siete años de edad con síntomas de rinitis y 8.4 % con síntomas de asma. Para adolescentes entre 12 y 13 años, la prevalencia fue de 15.4 y 15.6 %, respectivamente.3
En 2013, un grupo de investigadores mexicanos se dio a la tarea de diseñar un cuestionario diagnóstico para RA para estudios epidemiológicos en México, el cual fue validado18 antes de aplicarlo en diferentes estados de la república. Posteriormente se reportaron los resultados de la aplicación del cuestionario en escuelas. Fue llenado por alumnos de 12 años o mayores y por los padres en los niños menores a esa edad. En cuatro ciudades de cuatro estados diferentes del centro y sur de México se obtuvieron 8159 cuestionarios contestados. Se encontró una prevalencia promedio de rinitis alérgica de 15 % en mayores de 13 años y de 13 % en niños de 12 años o menos.19 Aproximadamente tres años después se aplicó el mismo cuestionario en 3446 niños escolares en Puebla, ciudad cerca de la Ciudad de México, encontrando una prevalencia de RA de 12 %.20
Otro grupo de investigadores aplicó recientemente el cuestionario de ISAAC acerca de síntomas de asma y de rinitis a casi 15 000 niños en cinco ciudades en el centro del país (el Bajío). La prevalencia de RA fue de 5.4 % (IC 95 % = 5.1-5.8), de rinitis más conjuntivitis de 19.2 % (IC 95 % = 18.6-19.8). Las prevalencias de asma, asma con el ejercicio y asma actual fueron de 6.1 % (IC 95 % = 5.7-6.5), 2.1 % (IC 95 % = 1.9-2.3) y 11.6 % (IC 95 % = 11.1-12.1), respectivamente.21
En este momento se está llevando a cabo el estudio GAN, que dará una visión mejor y más actualizada acerca de la prevalencia de patologías alérgicas en México.
Desde el verano de 2017, un grupo de alergólogos mexicanos se incorporó en las iniciativas de diseminación de ARIA y la aplicación móvil para pacientes con RA, lo que ayudará a mejorar el control de la enfermedad. Los médicos invitan a sus pacientes a usar la app y los ayudan a cargarla en su celular y llenar los datos iniciales. Esta estrategia ha sido exitosa. Hasta el momento, la app fue descargada por más de 1800 pacientes y más de 1500 completaron por lo menos un dato. En el futuro se espera ligar los datos obtenidos con la aplicación con referencias acerca de contaminación ambiental, especialmente en la Ciudad de México.
Vías Integradas de Atención en RA
Durante una reunión celebrada en París el 3 de diciembre de 2018, relativa al tratamiento de enfermedades crónicas, MASK (Red Celular Centinela de las Vías Aéreas) y POLLAR (Impacto de la Contaminación del Aire en el Asma y la Rinitis, del Instituto Europeo para la Innovación y Tecnología),22 profesionales y organizaciones de pacientes en el campo de las alergias y las enfermedades de las vías respiratorias recomendaron la evaluación de los ICP (Integrated Care Pathways) para la atención integral y en la vida real, con uso de medios digitales, de la rinitis y el asma con sus multimorbilidades, centrados en la persona, incluyendo la exposición ambiental.1,23
Los ICP son planes de atención multidisciplinarios estructurados que detallan los pasos clave de la atención al paciente,23,24,25 promueven la traducción de las recomendaciones de las guías en protocolos locales y su aplicación a la práctica clínica.25,26,27 Los ICP generalmente mejoran las recomendaciones combinando intervenciones reiteradas, integran el aseguramiento de la calidad y promueven la coordinación de la atención. Los ICP de las vías respiratorias26 fueron los primeros pasos para desarrollar los ICP para la multimorbilidad de la rinitis y el asma. En la RA existe una necesidad urgente de desarrollar pautas de próxima generación para la farmacoterapia y los ICP para la inmunoterapia específica con alérgenos (ITE). En este documento se presenta un resumen ejecutivo (figura 1). Lo anterior se modifica en los diferentes países o regiones para adaptar las conclusiones de los documentos al uso local y los sistemas de salud.
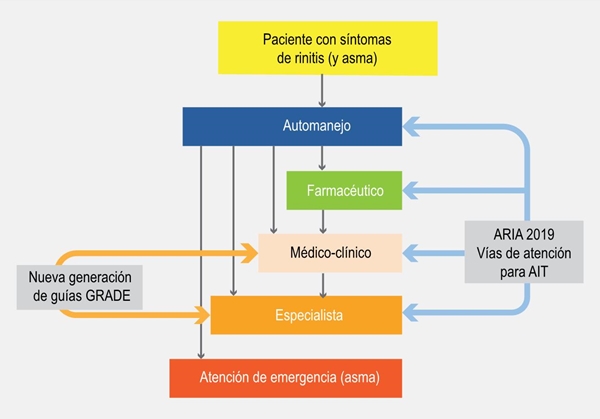
Figura 1
Vías de tratamiento de ARIA de nueva generación.
Guías ARIA-GRADE de nueva generación
La selección de la farmacoterapia para los pacientes con RA está destinada a controlar la enfermedad y depende de los siguientes aspectos:
-
Empoderamiento y preferencias del paciente.
-
Síntomas prominentes, su gravedad y multimorbilidad.
-
Eficacia y seguridad del tratamiento.28
-
Velocidad de inicio de acción del tratamiento.
-
Tratamiento actual.
-
Respuesta histórica al tratamiento.
-
Estrategias de autocontrol.
-
Uso de recursos.
Se diseñó un algoritmo31 y se digitalizó32 para proponer un tratamiento ascendente o descendente de la RA, pero se debe contextualizar según la disponibilidad de medicamentos y recursos en los diferentes países. Además, los algoritmos requieren pruebas utilizando ensayos controlados aleatorios (ECA) y una investigación observacional llamada “evidencia del mundo real” (RWE, real world evidence)19,20,21,22,23,24,33,34,35
La metodología GRADE (Grading of Recommendations Assessment, Development and Evaluation) considera explícitamente todos los tipos de diseños de estudios, desde ECA a informes de casos, aunque los desarrolladores de guías a menudo prefieren restringir las directrices a los ECA.36,37,38 Además de la evidencia, GRADE también considera valores y preferencias, aceptabilidad y viabilidad o transparencia de los hallazgos. Hay una tendencia creciente a utilizar RWE para informar la práctica clínica, especialmente porque los ECA a menudo están limitados por la aplicabilidad de los resultados.39
Durante la reunión de París se desarrollaron guías de próxima generación para el tratamiento farmacológico de la RA utilizando pautas basadas en GRADE para RA,30,39,40,41,42 probadas con RWE proporcionada por tecnología móvil22,41,43 y estudios de cámara de exposición a alérgenos. Estas recomendaciones se utilizaron para refinar el algoritmo MASK para el tratamiento de la RA propuesto por un grupo de consenso.31
Evidencia considerada para el desarrollo de las ICP de ARIA
-
Algoritmo MASK para el tratamiento farmacológico de la RA. El algoritmo MASK basado en una escala visual analógica (EVA)44 ha sido creado por el grupo de expertos de ARIA para la selección de farmacoterapia para los pacientes con RA y su escalamiento o decrecimiento dependiendo del control (figura 2a y 2b).31
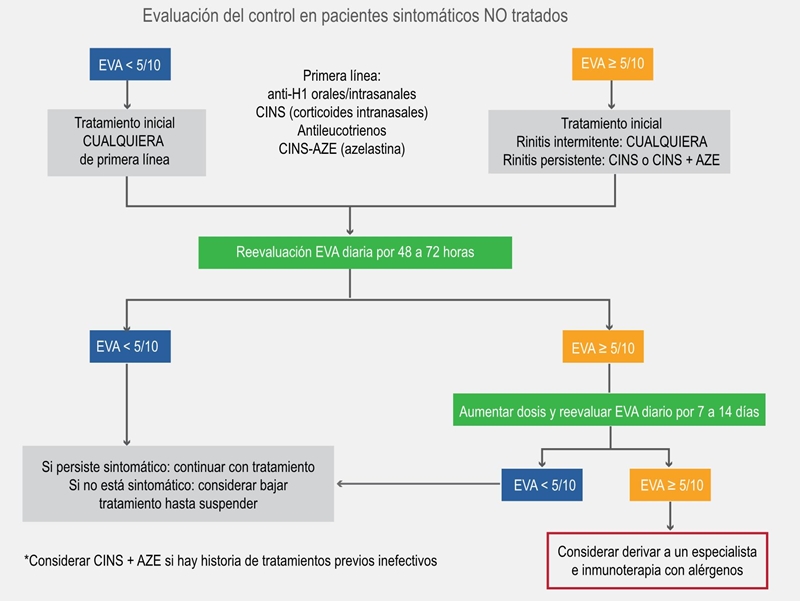
Figura 2a
Algoritmo ascendente para adolescentes y adultos sin tratamiento, utilizando una escala visual análoga (EVA).32 El algoritmo propuesto considera los pasos del tratamiento y la preferencia del paciente. Niveles de escala visual análoga en proporciones. Si persisten síntomas oculares, una vez que se ha iniciado el tratamiento, incluir tratamiento tópico ocular.
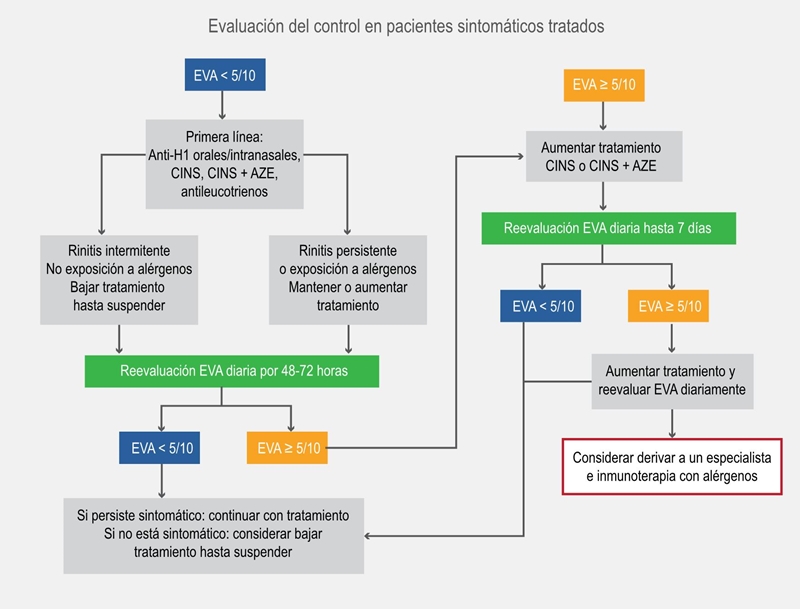
Figura 2b
Algoritmo ascendente, para pacientes tratados utilizando la escala visual analógica (EVA) en adolescentes y adultos.32 El algoritmo propuesto considera los pasos del algoritmo y la preferencia el paciente. Niveles de escala visual análoga en proporciones. Si persisten síntomas oculares, incluir tratamiento tópico ocular. AZE =
-
ARIA 2010, revisión 2016 y Parámetros de Práctica Clínica de Rinitis Estacional 2017 de Estados Unidos. A pesar de que hay unas pocas comparaciones disponibles de los medicamentos usando ensayos aleatorizados controlados,45,46,47 la comparación de medicaciones para la RA ha sido propuesto por varias revisiones35 y guías.28,40,41,42 Una evaluación de Health Technology Assessment concluyó que la mayoría de los medicamentos para la RA tenían un efecto similar.47 De todas formas, dicho análisis utilizó un método demasiado estricto, que no permitió diferenciar entre las medicaciones. Pero en general, las guías de RA están de acuerdo con los puntos importantes (cuadro 1).28,40,41,42 La revisión ARIA 201641 y los Parámetros de Práctica Clínica de Rinitis Estacional de Estados Unidos 2017,42 desarrollados en forma independiente, usaron el mismo método de abordaje GRADE.37,38,39 Interesantemente se analizaron las mismas preguntas. Se consideraron dos objetivos principales en el tratamiento de la rinitis moderada y grave: eficacia y rapidez de acción (cuadros 2 y 3).
Recomendaciones para la farmacoterapia en rinitis alérgica

CINS = corticoides intranasales, MP-AzeFlu = combinación intranasal de propionato de fluticasona y azelastina, RA = rinitis alérgica.
Recomendaciones generales de ARIA41

RA = rinitis alérgica, CINS = corticoides intranasales, MP-AzeFlu = combinación intranasal de propionato de fluticasona y azelastina, Para todas estas recomendaciones el nivel de evidencia fue bajo22,23 o muy bajo.1
Consejos clínicos importantes de los Parámetros Prácticos de Rinitis Estacional de los Estados Unidos sobre el tratamiento de la rinitis alérgica estacional en su actualización 2017.42

ARIA revisión 201642 y Parámetros Prácticos de los Estados Unidos sobre el Tratamiento de la Rinitis Alérgica Estacional en su actualización 2017,42 mayormente basados en estudios controlados y aleatorizados, aprueban el algoritmo MASK.28 RA = rinitis alérgica, CINS = corticoides intranasales
-
Rapidez de acción de los medicamentos. La Food and Drugs Administration ha propuesto tres tipos de estudio para medir el comienzo de la acción de los medicamentos para la RA:61,62 estudios estándar de fase 3, doble ciego controlados y aleatorizados con placebo, estudios de exposición natural en parques y estudios en cámaras de exposición a alérgenos.63 Los estudios aleatorizados y controlados son informativos, pero no proveen suficiente precisión para evaluar el inicio de la eficacia. Los estudios en cámaras con alérgenos ofrecen algunas ventajas para evaluar el inicio de la eficacia en minutos.63 Estos últimos son más consistentes que los estudios en parques.64
-
Varias medicaciones intranasales fueron evaluadas en las cámaras de exposición a alérgenos de Ontario58,65,66,67 y Viena.68,69,70 Los estudios en la cámara de Ontario muestran la rapidez de inicio de acción para azelastina y sus combinaciones, incluyendo MP-AzeFlu. Otros antihistamínicos intranasales tienen un inicio de acción más lento. Los corticoides intranasales (CINS) en monoterapia o con antihistaminicos orales no son efectivos antes de las dos horas. Los estudios en la cámara de exposición a alérgenos de Viena mostraron que la azelastina y la levocabastina + furoato de fluticasona son las medicaciones que actúan más rápido en comparación con los antihistamínicos orales o los CINS.
-
Evidencia en vida real utilizando tecnología móvil. Las guías ARIA de próxima generación evaluaron las recomendaciones basadas en GRADE frente a la evidencia de vida real, utilizando datos obtenidos por herramientas móviles de salud (mHealth) para confirmar o refinarlas y el algoritmo MASK. Si bien hay muchas herramientas móviles de salud disponibles para la RA,71 solo MASK ha proporcionado datos acerca de los medicamentos que pueden ser usados en RWE.22,72
-
Estudio piloto de tratamiento MASK 2017. Con un diseño transversal observacional de vida real en 2871 usuarios (17 091 días de EVA), aportó percepciones sobre el tratamiento de la RA en vida real utilizando la EVA para los síntomas alérgicos en general (EVA global) en 15 países (cuadro 4).4
Resultados de evidencias en vida real sobre el tratamiento de la RA.

RA = rinitis alérgica, MP-AzeFlu = combinación intranasal de propionato de fluticasona y azelastina, CINS = corticoides intranasales
-
Estudio de tratamiento MASK 2017.73 Se llevó a cabo en forma observacional transversal en el escenario de la vida real en 22 países, como complemento del estudio piloto del año 2017;43 9122 usuarios completaron 112 054 días de EVA entre 2016 y 2017. Los mismos resultados se obtuvieron en EVA global (cuadro 4). Por otra parte, se encontró la misma tendencia en la EVA para los síntomas nasales, asma, síntomas oculares y productividad laboral.
-
Estudio de adherencia al tratamiento MASK 2018.74 De tipo observacional transversal, se llevó a cabo con 12 143 usuarios. La adherencia fue imposible de probar directamente, ya que los usuarios no proporcionaron los datos todos los días y pudieron no informar sobre todos los medicamentos utilizados. La adherencia secundaria se evaluó usando una relación de posesión de medicación modificada y la proporción de días cubiertos. La adherencia fue inferior a 5 %.
Limitaciones de MASK
Como todos los estudios que utilizan datos de participación, los sesgos potenciales incluyen la probabilidad de sesgo en la muestra y una clasificación errónea que no puede ser evaluada, así como la disponibilidad de poca información sobre las características del paciente o días de tratamiento debido a problemas éticos. Además, los usuarios de la aplicación no son representativos de todos los pacientes con RA.
MASK utilizó los días en un análisis transversal43,75 porque no existe un patrón claro de tratamiento y no fue posible un estudio longitudinal, ya que la mayoría de los usuarios utilizó la aplicación en forma intermitente.
El diagnóstico de RA no fue confirmado por un profesional médico, pero es probable que la mayoría de los usuarios sufriera rinitis (alérgica o no).43 La caracterización precisa del paciente usando una aplicación es imposible debido a razones de privacidad. No obstante, la tecnología móvil se está convirtiendo en una herramienta importante para entender mejor y gestionar la RA y añade información que no estaba disponible con otros métodos.75,76,77,78,79,80,81 No existen otros estudios de salud con tecnología móvil que hayan evaluado la eficacia de diferentes medicamentos a gran escala.
Existe una completa desconexión entre la prescripción médica y el comportamiento del paciente frente al tratamiento de la RA inducida por polen. La mayoría de los alergólogos prescribe medicamentos para toda la temporada, recomendando al paciente su uso regular aún en los días con poca sintomatología. Algunos alergólogos prescriben un tratamiento preestacional, sin clara evidencia de su eficacia. Por otra parte, la mayoría de los pacientes utiliza su medicación a demanda cuando su RA no está bien controlada y no sigue las recomendaciones de las guías.43,82,83,84 Cuando los médicos son pacientes, se comportan como pacientes cuando tratan su propia RA y no siguen las prescripciones que ellos mismos recomiendan.
Próxima generación de guías ARIA-GRADE
El algoritmo propone un enfoque gradual para la selección de medicamentos en la RA basada en recomendaciones GRADE refinadas con RWE y estudios de provocación en cámara (cuadro 5).
Nueva generación de guías ARIA-GRADE
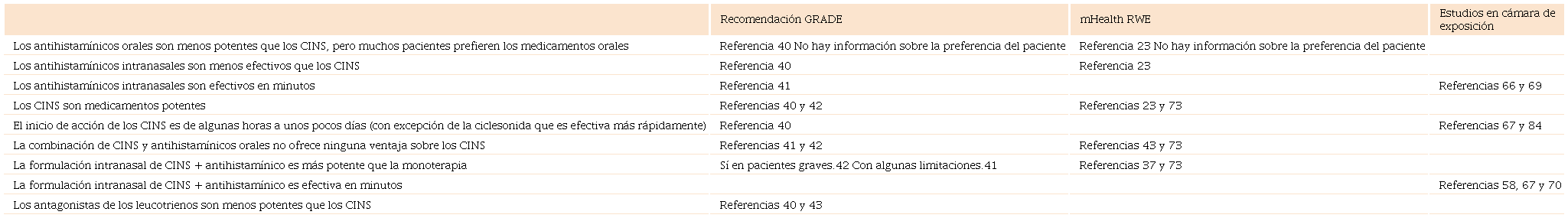
CINS = corticoides intranasales
El enfoque propuesto confirma la validez de la mayoría de las recomendaciones de GRADE para la RA,85 permite alguna evidencia condicional para ser apoyada por RWE y proporciona algunas nuevas ideas:
-
Al inicio del tratamiento, la combinación de antihistamínicos orales y corticoides nasales no demostró ser más efectiva que los corticoides nasales en monoterapia.
-
La formulación intranasal de corticoides + antihistamínico demostró ser más efectiva que los corticoides nasales en monoterapia.
-
Los medicamentos que contienen antihistamínicos intranasales son efectivos en pocos minutos.
El algoritmo de ARIA para la RA fue probado con ensayos aleatorizados y ECA, investigación observacional RWE y estudios de campo. El algoritmo en general fue apropiado y no fue necesario ningún cambio.
Conclusiones
Este enfoque, la primera guía GRADE (para cualquier enfermedad crónica) integrando RWE y estudios adicionales (estudios en cámaras de exposición a alérgenos) podría ser un modelo para las enfermedades crónicas.
Estas guías informarán las IPC y se incluirán en el Directorate-General for Health and Food Safety (DG SANTE) habilitado digitalmente, de manera integrada y centrándose en el cuidado de los pacientes, y representa la estrategia de cambio en la fase 4 del manejo de ARIA.1,67
Referencias
Bousquet J, Hellings PW, Agache I, Amat F, Annesi-Maesano I, Ansotegui IJ, 4. ARIA Phase 4 (2018): change management in allergic rhinitis and asthma multimorbidity using mobile technology. J Allergy Clin Immunol. 2019;143(3):864-879. DOI: 10.1016/j.jaci.2018.08.049
Asher MI, Keil U, Anderson HR, Beasley R, Crane J, Martinez F, et al. International Study of Asthma and Allergies in Childhood (ISAAC): rationale and methods. Eur Respir J. 1995;8(3):483-491. DOI: 10.1183/09031936.95.08030483
Aït-Khaled N, Pearce N, Anderson HR, Ellwood P, Montefort S, Shah J, et al. Global map of the prevalence of symptoms of rhinoconjunctivitis in children: The International Study of Asthma and Allergies in Childhood (ISAAC) Phase Three. Allergy. 2009;64(1):123-148. DOI: 10.1111/j.1398-9995.2008.01884.x
Chong-Neto HJ, Rosário NA, Solé D, Latin American ISAAC Group. Asthma and rhinitis in South America: how different they are from other parts of the world. Allergy Asthma Immunol Res. 2012;4(2):62-67. DOI: 10.4168/aair.2012.4.2.62
Vázquez D, Medina I, Logusso G, Gattolin G, Arias S, Parisi C. Cross-sectional prevalence survey of allergic rhinitis in Argentina: Study PARA. Rev Alerg Mex. 2019;66(1):55-64. DOI: 10.29262/ram.v66i1.543
Neffen H, Mello JF, SoléD , Naspitz CK, Dodero AE, Garza HL, et al. Nasal allergies in the Latin American population: results from the Allergies in Latin America survey. Allergy Asthma Proc. 2010;31(Suppl 1):S9-S27. DOI: 10.2500/aap.2010.31.3347
Maspero JF, Jardim JR, Aranda A, Tassinari CP, González-Díaz SN, Sansores RH, et al. Insights, attitudes, and perceptions about asthma and its treatment: findings from a multinational survey of patients from Latin America. World Allergy Organ J. 2013;6(1):19. DOI: 10.1186/1939-4551-6-19
Strachan D, Sibbald B, Weiland S, Aït-Khaled N, Anabwani G, Anderson HR, et al. Worldwide variations in prevalence of symptoms of allergic rhinoconjunctivitis in children: the International Study of Asthma and Allergies in Childhood (ISAAC). Pediatr Allergy Immunol. 1997;8(4):161-176. DOI: 10.1111/j.1399-3038.1997.tb00156.x
Björkstén B, Clayton T, Ellwood P, Stewart A, Strachan D, ISAAC Phase III Study Group. Worldwide time trends for symptoms of rhinitis and conjunctivitis: Phase III of the International Study of Asthma and Allergies in Childhood. Pediatr Allergy Immunol. 2008;19(2):110-124. DOI: 10.1111/j.1399-3038.2007.00601.x
Arnedo-Pena A, García-Marcos L, García-Hernández G, Aguinagua-Ontoso I, González-Díaz C, Morales-Suárez-Varela M, et al. Time trends and geographical variations in the prevalence of symptoms of allergic rhinitis in 6-7-year-old children from eight areas of Spain according to the ISAAC. An Pediatr (Barc). 2005;62(3):229-236. DOI: 10.1157/13071837
Bauchau V, Durham SR. Prevalence and rate of diagnosis of allergic rhinitis in Europe. Eur Respir J. 2004;24(5):758-764. DOI: 10.1183/09031936.04.00013904
Vicente-Herrero MT, Prieto-Andrés L, López-González AA, Pérez-Francés C, Ramírez-Íñiguez de la Torre MV, Santamaría-Navarro C, et al. Prevalence of rhinitis and asthma respiratory symptoms in Spanish working population. Rev Med Inst Mex Seguro Soc. 2014;52(1):50-59.
Ojeda P, Sastre J, Olaguibel JM, Chivato T. Alergológica 2015: a national survey on allergic diseases in the adult Spanish population. J Investig Allergol Clin Immunol. 2018;28(3):151-164. DOI: 10.18176/jiaci.0264
Ojeda P, Ibáñez MD, Olaguibel JM, Sastre J, Chivato T. Alergológica 2015: a national survey on allergic diseases in the Spanish pediatric population. J Investig Allergol Clin Immunol. 2018;28(5):321-329. DOI: 10.18176/jiaci.0308
Valero A, Ferrer M, Sastre J, Navarro AM, Monclús L, Martí-Guadaño E, et al. A new criterion by which to discriminate between patients with moderate allergic rhinitis and patients with severe allergic rhinitis based on the Allergic Rhinitis and its Impact on Asthma severity items. J Allergy Clin Immunol. 2007;120(2):359-365. DOI: 10.1016/j.jaci.2007.04.006
ESPRINT Study Group and Investigators, Valero A , Alonso J, Antepara I, et al. Development and validation of a new Spanish instrument to measure health-related quality of life in patients with allergic rhinitis: the ESPRINT questionnaire. Value Health. 2007;10(6):466- 77. DOI: 10.1111/j.1524-4733.2007.00202.x
Janson C, Antó J, Burney P, Chinn S, de Marco R, Heinrich J, et al. The European Community Respiratory Health Survey: what are the main results so far? European Community Respiratory Health Survey II. Eur Respir J. 2001;18(3):598-611. DOI: 10.1183/09031936.01.00205801
Mancilla-Hernández E, Barnica-Alvarado RH, Morfín-Maciel B, Larenas-Linnemann D. Validation of a diagnostic questionnaire on asthma in children and adults for epidemiological studies. Rev Alerg Mex. 2014;61(2):73-80. DOI: 10.29262/ram.v61i2.29
Mancilla-Hernandez E, Medina-Ávalos MA, Barnica-Alvarado RH, Soto-Candia D, Guerrero-Venegas R, Zecua-Nájera Y. Prevalence of rhinitis allergic in populations of several states of Mexico. Rev Alerg Mex. 2015;62(3):196-201. DOI: 10.29262/ram.v62i3.107
Mancilla-Hernández E, González-Solórzano E. Prevalence of allergic rhinitis, and symptoms as indicators of risk in schoolchildren of the Puebla Northern Mountain Range. Rev Alerg Mex. 2018;65(2):140-147. DOI: 10.29262/ram.v65i2.330
Ramírez-Soto M, Bedolla-Barajas M, González-Mendoza T. Prevalence of asthma, allergic rhinitis and atopic dermatitis in school children of the Mexican Bajío region. Rev Alerg Mex. 2018;65(4):372-378. DOI: 10.29262/ram.v65i4.527
Bousquet J, Anto JM, Annesi-Maesano I, Dedeu T, Dupas E, Pepin JL, et al. POLLAR: impact of air POLLution on asthma and rhinitis; a European Institute of Innovation and Technology Health (EIT Health) project. Clin Transl Allergy. 2018;8:36. Disponible en: https://ctajournal.biomedcentral.com/articles/10.1186/s13601-018-0221-z
Bousquet J, Arnavielhe S, Bedbrook A, Bewick M, Laune D, Mathieu-Dupas E, et al. MASK 2017: ARIA digitally-enabled, integrated, person-centred care for rhinitis and asthma multimorbidity using real-world-evidence. Clin Transl Allergy. 2018;8:45. DOI: 10.1186/s13601-018-0227-6
Campbell H, Hotchkiss R, Bradshaw N, Porteous M. Integrated care pathways. BMJ. 1998;316(7125):133-137. DOI: 10.1136/bmj.316.7125.133
Hujala A, Taskinen H, Rissanen S. How to support integration to promote care for people with multimorbidity in Europe? Alemania: European Observatory Policy Briefs; 2017.
Palmer K, Marengoni A, Forjaz MJ, Jureviciene E, Laatikainen T, Mammarella F, et al. Multimorbidity care model: recommendations from the consensus meeting of the Joint Action on Chronic Diseases and Promoting Healthy Ageing across the Life Cycle (JA-CHRODIS). Health Policy. 2018;122(1):4-11. DOI: 10.1016/j.healthpol.2017.09.006
Bousquet J, Addis A, Adcock I, Agache I, Agusti A, Alonso A, et al. Integrated care pathways for airway diseases (AIRWAYS-ICPs). Eur Respir J. 2014;44(2):304-323. DOI: 10.1183/09031936.00014614
Meltzer EO, Wallace D, Dykewicz M, Shneyer L. Minimal Clinically Important Difference (MCID) in allergic rhinitis: agency for healthcare research and quality or anchor-based thresholds? J Allergy Clin Immunol Pract. 2016;4(4):682-688. DOI: 10.1016/j.jaip.2016.02.006
Muñoz-Cano R, Ribó P, Araujo G, Giralt E, Sánchez-López J, Valero A . Severity of allergic rhinitis impacts sleep and anxiety: results from a large Spanish cohort. Clin Transl Allergy. 2018;8:23. Disponible en: https://ctajournal.biomedcentral.com/articles/10.1186/s13601-018-0212-0
Vandenplas O, Vinnikov D, Blanc PD, Agache I, Bachert C, Bewick M, et al. Impact of rhinitis on work productivity: a systematic review. J Allergy Clin Immunol Pract. 2018;6(4):1274-1286. DOI: 10.1016/j.jaip.2017.09.002
Bousquet J, Schunemann HJ, Hellings PW, Arnavielhe S, Bachert C, Bedbrook A, et al. MACVIA clinical decision algorithm in adolescents and adults with allergic rhinitis. J Allergy Clin Immunol. 2016;138(2):367-374. DOI: 10.1016/j.jaci.2016.03.025
Courbis AL, Murray RB, Arnavielhe S, Caimmi D, Bedbrook A, van Eerd M, et al. Electronic clinical decision support system for allergic rhinitis management: MASK e-CDSS. Clin Exp Allergy. 2018;48(12):1640-1653. DOI: 10.1111/cea.13230
Use of real-world evidence to support regulatory decision-making for medical devices. EE.UU.: Guidance for Industry and Food and Drug Administration Staff; 2017.
Sherman RE, Anderson SA, Dal Pan GJ, Gray GW, Gross T, Hunter NL, et al. Real-world evidence. What is it and what can it tell us? N Engl J Med. 2016;375(23):2293-2297. DOI: 10.1056/NEJMsb1609216
Briere JB, Bowrin K, Taieb V, Millier A, Toumi M, Coleman C. Meta-analyses using real-world data to generate clinical and epidemiological evidence: a systematic literature review of existing recommendations. Curr Med Res Opin. 2018;34(12):2125-2130. DOI: 10.1080/03007995.2018.1524751
Brozek JL, Akl EA, Alonso-Coello P, Lang D, Jaeschke R, Williams JW, et al. Grading quality of evidence and strength of recommendations in clinical practice guidelines. Part 1 of 3. An overview of the GRADE approach and grading quality of evidence about interventions. Allergy. 2009;64(5):669-677. DOI: 10.1111/j.1398-9995.2009.01973.x
Brozek JL, Akl EA, Compalati E, Kreis J, Terracciano L, Fiocchi A, et al. Grading quality of evidence and strength of recommendations in clinical practice guidelines part 3 of 3. The GRADE approach to developing recommendations. Allergy. 2011;66(5):588-595. DOI: 10.1111/j.1398-9995.2010.02530.x
Brozek JL, Akl EA, Jaeschke R, Lang DM, Bossuyt P, Glasziou P, et al. Grading quality of evidence and strength of recommendations in clinical practice guidelines: part 2 of 3. The GRADE approach to grading quality of evidence about diagnostic tests and strategies. Allergy. 2009;64(8):1109-1116. DOI: 10.1111/j.1398-9995.2009.02083.x
Oyinlola JO, Campbell J, Kousoulis AA. Is real world evidence influencing practice? A systematic review of CPRD research in NICE guidances. BMC Health Serv Res. 2016;16:299. DOI: 10.1186/s12913-016-1562-8
Brozek JL, Bousquet J, Baena-Cagnani CE, Bonini S, Canonica GW, Casale TB, et al. Allergic Rhinitis and its Impact on Asthma (ARIA) guidelines: 2010 revision. J Allergy Clin Immunol. 2010;126(3):466-476. DOI: 10.1016/j.jaci.2010.06.047
Brozek JL, Bousquet J, Agache I, Agarwal A, Bachert C, Bosnic-Anticevich S, et al. Allergic Rhinitis and its Impact on Asthma (ARIA) guidelines-2016 revision. J Allergy Clin Immunol. 2017;140(4):950-958. DOI: 10.1016/j.jaci.2017.03.050
Dykewicz MS, Wallace DV, Baroody F, Bernstein J, Craig T, Finegold I, et al. Treatment of seasonal allergic rhinitis: an evidence-based focused 2017 guideline update. Ann Allergy Asthma Immunol. 2017;119(6):489-511. DOI: 10.1016/j.anai.2017.08.012
Bousquet J, Arnavielhe S, Bedbrook A, Alexis-Alexandre G, van Eerd M, Murray R, et al. Treatment of allergic rhinitis using mobile technology with real world data: The MASK observational pilot study. Allergy. 2018;73(9):1763-1774. DOI: 10.1111/all.13406
Klimek L, Bergmann KC, Biedermann T, Bousquet J, Hellings P, Jung K, et al. Visual analogue scales (VAS): measuring instruments for the documentation of symptoms and therapy monitoring in cases of allergic rhinitis in everyday health care: position paper of the German Society of Allergology (AeDA) and the German Society of Allergy and Clinical Immunology (DGAKI), ENT Section, in collaboration with the working group on Clinical Immunology, Allergology and Environmental Medicine of the German Society of Otorhinolaryngology, Head and Neck Surgery (DGHNOKHC). Allergo J Int. 2017;26(1):16-24. DOI: 10.1007/s40629-016-0006-7
Horak F, Bruttmann G, Pedrali P, Weeke B, Frolund L, Wolff HH, et al. A multicentric study of loratadine, terfenadine and placebo in patients with seasonal allergic rhinitis. Arzneimittelforschung. 1988;38(1):124-128.
Hampel FC, Ratner PH, van Bavel J, Amar NJ, Daftary P, Wheeler W, et al. Double-blind, placebo-controlled study of azelastine and fluticasone in a single nasal spray delivery device. Ann Allergy Asthma Immunol. 2010;105(2):168-173. DOI: 10.1016/j.anai.2010.06.008
Carr W, Bernstein J, Lieberman P, Meltzer E, Bachert C, Price D, et al. A novel intranasal therapy of azelastine with fluticasone for the treatment of allergic rhinitis. J Allergy Clin Immunol. 2012;129(5):1282-1289. DOI: 10.1016/j.jaci.2012.01.077
Kaszuba SM, Baroody FM, de Tineo M, Haney L, Blair C, Naclerio RM. Superiority of an intranasal corticosteroid compared with an oral antihistamine in the as-needed treatment of seasonal allergic rhinitis. Arch Intern Med. 2001;161(21):2581-2587. DOI: 10.1001/archinte.161.21.2581
Glacy J, Putnam K, Godfrey S, Falzon L, Mauger B, Samson D, et al. Treatments for seasonal allergic rhinitis. EE.UU.: Agency for Healthcare Research and Quality; 2013.
Scadding GK, Durham SR, Mirakian R, Jones NS, Leech SC, Farooque S, et al. BSACI guidelines for the management of allergic and non-allergic rhinitis. Clin Exp Allergy. 2008;38(1):19-42. DOI: 10.1111/j.1365-2222.2007.02888.x
Wallace DV, Dykewicz MS, Bernstein DI, Blessing-Moore J, Cox L, Khan DA, et al. The diagnosis and management of rhinitis: an updated practice parameter. J Allergy Clin Immunol. 2008;122(Suppl 2):S1-S84. DOI: 10.1016/j.jaci.2008.06.003
Roberts G, Xatzipsalti M, Borrego LM, Custovic A, Halken S, Hellings PW, et al. Paediatric rhinitis: position paper of the European Academy of Allergy and Clinical Immunology. Allergy. 2013;68(9):1102-1116. DOI: 10.1111/all.12235.
Scadding GK. Optimal management of allergic rhinitis. Arch Dis Child. 2015;100(6):576-582. DOI: 10.1136/archdischild-2014-306300
Larenas-Linnemann D, Mayorga-Butron JL, Sánchez-González A, Ramírez-García A, Medina-Ávalos M, Figueroa-Morales MA, et al. ARIA Mexico 2014. Adaptation of the clinical practice guide ARIA 2010 for Mexico. Methodology ADAPTE. Rev Alerg Mex. 2014;61(Suppl 1):S3-S116. Disponible en: http://revistaalergia.mx/ojs/index.php/ram/article/view/52/69
Meltzer EO. Pharmacotherapeutic strategies for allergic rhinitis: matching treatment to symptoms, disease progression, and associated conditions. Allergy Asthma Proc. 2013;34(4):301-311.
Seidman MD, Gurgel RK, Lin SY, Schwartz SR, Baroody FM, Bonner JR, et al. Clinical practice guideline: allergic rhinitis executive summary. Otolaryngol Head Neck Surg. 2015;152(2):197-206. DOI: 10.2500/aap.2013.34.3676
Seidman MD, Gurgel RK, Lin SY, Schwartz SR, Baroody FM, Bonner JR, et al. Clinical practice guideline: allergic rhinitis. Otolaryngol Head Neck Surg. 2015;152(Suppl 1):S1-S43. DOI: 10.1177/0194599814561600
Bousquet J, Meltzer EO, Couroux P, Koltun A, Kopietz F, Munzel U, et al. Onset of action of the fixed combination intranasal azelastine-fluticasone propionate in an allergen exposure chamber. J Allergy Clin Immunol Pract. 2018;6(5):1726-1732. DOI: 10.1016/j.jaip.2018.01.031
Bachert C, Bousquet J, Hellings P. Rapid onset of action and reduced nasal hyperreactivity: new targets in allergic rhinitis management. Clin Transl Allergy. 2018;8:25. Disponible en: https://ctajournal.biomedcentral.com/articles/10.1186/s13601-018-0210-2
Church MK, Maurer M, Simons FE, Bindslev-Jensen C, van Cauwenberge P, Bousquet J, et al. Risk of first-generation H(1)-antihistamines: a GA(2)LEN position paper. Allergy. 2010;65(4):459-466. DOI: 10.1111/j.1398-9995.2009.02325.x
Allergic rhinitis: developing drug products for treatment. Guidance for industry. EE.UU.: U.S. Department of Health and Human Services/Food and Drug Administration/Center for Drug Evaluation and Research; 2000.
Allergic rhinitis: developing drug products for treatment. Guidance for industry. EE.UU.: U.S. Department of Health and Human Services/Food and Drug Administration/Center for Drug Evaluation and Research; 2016.
Katial RK, Salapatek AM, Patel P. Establishing the onset of action of intranasal corticosteroids: is there an ideal study design? Allergy Asthma Proc. 2009;30(6):595-604. DOI: 10.2500/aap.2009.30.3291
Pfaar O, Calderon MA, Andrews CP, Angjeli E, Bergmann KC, Bonlokke JH, et al. Allergen exposure chambers: harmonizing current concepts and projecting the needs for the future-an EAACI position paper. Allergy. 2017;72(7):1035-1042. DOI: 10.1111/all.13133
Patel P, D’Andrea C, Sacks HJ. Onset of action of azelastine nasal spray compared with mometasone nasal spray and placebo in subjects with seasonal allergic rhinitis evaluated in an environmental exposure chamber. Am J Rhinol. 2007;21(4):499-503. DOI: 10.2500/ajr.2007.21.3058
Patel P, Roland PS, Marple BF, Benninger PJ, Margalias H, Brubaker M, et al. An assessment of the onset and duration of action of olopatadine nasal spray. Otolaryngol Head Neck Surg. 2007;137(6):918-924. DOI: 10.1016/j.otohns.2007.08.005
Salapatek AM, Lee J, Patel D, D’Angelo P, Liu J, Zimmerer RO, et al. Solubilized nasal steroid (CDX-947) when combined in the same solution nasal spray with an antihistamine (CDX-313) provides improved, fast-acting symptom relief in patients with allergic rhinitis. Allergy Asthma Proc. 2011;32(3):221-229. DOI: 10.2500/aap.2011.32.3444
Horak F, Zieglmayer UP, Zieglmayer R, Kavina A, Marschall K, Munzel U, et al. Azelastine nasal spray and desloratadine tablets in pollen-induced seasonal allergic rhinitis: a pharmacodynamic study of onset of action and efficacy. Curr Med Res Opin. 2006;22(1):151-157. DOI: 10.1185/030079906X80305
Zieglmayer P, Zieglmayer R, Bareille P, Rousell V, Salmon E, Horak F. Fluticasone furoate versus placebo in symptoms of grass-pollen allergic rhinitis induced by exposure in the Vienna Challenge Chamber. Curr Med Res Opin. 2008;24(6):1833-1840. DOI: 10.1185/03007990802155792
Murdoch RD, Bareille P, Ignar D, Miller SR, Gupta A, Boardley R, et al. The improved efficacy of a fixed-dose combination of fluticasone furoate and levocabastine relative to the individual components in the treatment of allergic rhinitis. Clin Exp Allergy. 2015;45(8):1346-1355. DOI: 10.1111/cea.12556
Sleurs K, Seys S, Bousquet J, Fokkens W, Gorris S, Pugin B, et al. Mobile health tools for the management of chronic respiratory diseases. Allergy. 2019;74(7):1292-1306. DOI: 10.1111/all.13720
Bousquet J, Hellings PW, Agache I, Bedbrook A, Bachert C, Bergmann KC, et al. ARIA 2016: care pathways implementing emerging technologies for predictive medicine in rhinitis and asthma across the life cycle. Clin Transl Allergy. 2016;6:47. Disponible en : https://ctajournal.biomedcentral.com/articles/10.1186/s13601-016-0137-4
Bédard A, Basagaña X, Anto JM, Garcia-Aymerich J, Devillier P, Arnavielhe S, et al. Mobile technology offers novel insights into the control and treatment of allergic rhinitis: The MASK study. J Allergy Clin Immunol. 2019;144(1):135-143. DOI: 10.1016/j.jaci.2019.01.053
Menditto E, Guerriero F, Orlando V, Crola C, Di Somma C, Illario M, et al. Self-assessment of adherence to medication: a case study in Campania region community-dwelling population. J Aging Res. 2015;2015:682503. DOI: 10.1155/2015/682503
Caimmi D, Baiz N, Tanno LK, Demoly P, Arnavielhe S, Murray R, et al. Validation of the MASK-rhinitis visual analogue scale on smartphone screens to assess allergic rhinitis control. Clin Exp Allergy. 2017;47(12):1526-1533. DOI: 10.1111/cea.13025
Bonini M. Electronic health (e-Health): emerging role in asthma. Curr Opin Pulm Med. 2017;23(1):21-26. DOI: 10.1097/MCP.0000000000000336
Pizzulli A, Perna S, Florack J, Pizzulli A, Giordani P, Tripodi S, et al. The impact of telemonitoring on adherence to nasal corticosteroid treatment in children with seasonal allergic rhinoconjunctivitis. Clin Exp Allergy. 2014;44(10):1246-1254. DOI: 10.1111/cea.12386
Bousquet J, Caimmi DP, Bedbrook A, Bewick M, Hellings PW, Devillier P, et al. Pilot study of mobile phone technology in allergic rhinitis in European countries: the MASK-rhinitis study. Allergy. 2017;72(6):857-865. DOI: 10.1111/all.13125
Bousquet J, Arnavielhe S, Bedbrook A, Fonseca J, Morais-Almeida M, Todo-Bom A, et al. The Allergic Rhinitis and its Impact on Asthma (ARIA) score of allergic rhinitis using mobile technology correlates with quality of life: The MASK study. Allergy. 2018;73(2):505-510. DOI: 10.1111/all.13307
Bousquet J, Devillier P, Anto JM, Bewick M, Haahtela T, Arnavielhe S, et al. Daily allergic multimorbidity in rhinitis using mobile technology: a novel concept of the MASK study. Allergy. 2018;73(9):1763-1774. DOI: 10.1111/all.13448
Bousquet J, VandenPlas O, Bewick M, Arnavielhe S, Bedbrook A, Murray R, et al. The Work Productivity and Activity Impairment Allergic Specific (WPAI-AS) questionnaire using mobile technology: The MASK Study. J Investig Allergol Clin Immunol. 2018;28(1):42-44. DOI: 10.18176/jiaci.0197
Price D, Scadding G, Ryan D, Bachert C, Canonica GW, Mullol J, et al. The hidden burden of adult allergic rhinitis: UK healthcare resource utilisation survey. Clin Transl Allergy. 2015;5:39. Disponible en: https://ctajournal.biomedcentral.com/articles/10.1186/s13601-015-0083-6
Bousquet J, Murray R, Price D, Somekh D, Münter L, Phillips J, et al. The allergic allergist behaves like a patient. Ann Allergy Asthma Immunol. 2018;121(6):741-742. DOI: 10.1016/j.anai.2018.07.034
Couroux P, Kunjibettu S, Kunjibettu S, Hall N, Wingertzahn MA. Onset of action of ciclesonide once daily in the treatment of seasonal allergic rhinitis. Ann Allergy Asthma Immunol. 2009;102(1):62-68. DOI: 10.1016/S1081-1206(10)60110-X
Bousquet J, Schünemann H, Togias A, Bachert C, Erhola M, Hellings P, et al . Next-generation Allergic Rhinitis and Its Impact on Asthma (ARIA) guidelines for allergic rhinitis based on Grading of Recommendations Assessment, Development and Evaluation (GRADE) and real-world evidence. J Allergy Clin Immunol. 2020;145(1):70-80. DOI: 10.1016/j.jaci.2019.06.049
Glosario
ARIA: Allergic Rhinitis and its Impact on Asthma
ECA: ensayo controlado y aleatorizado
EVA: escala visual analógica
GRADE: Grading of Recommendations Assessment, Development and Evaluation
ICP: Integrated Care Pathways
ISAAC: The International Study of Asthma and Allergies in Childhood
MASK: Red Celular Centinela de las Vías Aéreas
MASK-Air: actualización de Diario de Alergia
mHealth: herramientas móviles de salud
POLLAR: Impacto de la Contaminación del Aire en el Asma y la Rinitis, del Instituto Europeo para la Innovación y Tecnología
RA: rinitis alérgica
RWE: real word evidence
Notas
Notas de autor
*Correspondencia: Juan Carlos Ivancevich. ivancev@gmail.com
