Artículos científicos
Recepción: 16 Agosto 2023
Aprobación: 10 Enero 2024
Publicación: 20 Junio 2024
DOI: https://doi.org/10.21829/myb.2024.3042627
Resumen: La invasión de especies no autóctonas es una de las principales amenazas para la conservación de la biodiversidad y para la provisión de servicios ecosistémicos. Uno de los ecosistemas más vulnerables a escala mundial por la presencia de especies exóticas invasoras (EEI) es el bosque de manglar, ya que estas pueden desestabilizar la estructura y función de las redes tróficas y reducir su productividad, principalmente por competencia y depredación de especies nativas. En este estudio se realizó un análisis en los sistemas de información de biodiversidad y la literatura científica especializada para determinar la presencia de EEI en los bosques de manglar de las reservas de la biosfera Ría Celestún y Ría Lagartos ubicadas en la península de Yucatán, México; se identificó el nivel de riesgo de las EEI de acuerdo con el método de evaluación rápida de invasividad, y se generó información sobre las implicaciones de las EEI en los bosques de manglar. Entre las dos áreas naturales protegidas (ANP), se encontró la presencia de 16 EEI, de las cuales, 56.25% tienen valor de riesgo de invasividad “muy alto” y 43.75% riesgo de invasividad “alto”, lo que significa una alerta de peligro para los bosques de manglar de las ANP. La información generada en este estudio servirá de base para el planteamiento de estrategias de gestión para la atención de EEI y sobre la conservación de los bosques de manglar en las ANP.
Palabras clave: Área natural protegida, conservación, manejo forestal, prevención, riesgo de invasividad, servicios ecosistémicos.
Abstract: The invasion of non-native species is one of the main threats to biodiversity conservation and the provision of ecosystem services. Mangroves are one of the most vulnerable ecosystems worldwide due to invasive alien species (IAS), as they can destabilize the structure and function of trophic webs and reduce their primary productivity, mainly through competition and predation of native species. In this paper, an analysis of biodiversity information systems and scientific literature were used to determine the presence of IAS within the mangrove forests of the Ria Celestún and Ría Lagartos biosphere reserves in the Yucatan Peninsula, Mexico; the level of risk of IAS was identified according to the rapid invasiveness assessment method, and information was generated on the implications of IAS in mangrove forests. In both natural protected areas (NPAs), 16 IAS were found, of which 56.25% had a "very high" invasiveness risk value, and 43.75% had a “high” invasiveness risk, which implies a danger alert for mangrove forests in the NPAs. The information generated in this study can be used to identify strategies for managing IAS and the conservation of mangrove forests in NPAs.
Keywords: Natural protected area, conservation, forest management, prevention, risk of invasiveness, ecosystem services.
INTRODUCCIÓN
Las especies exóticas son aquellas cuya presencia en una región es atribuible a acciones humanas, deliberadas o involuntarias, que les permitieron superar barreras biogeográficas (Pyšek et al., 2020; Unión Internacional para la Conservación de la Naturaleza [IUCN, por sus siglas en inglés], 2000). Una vez que las especies exóticas logran establecerse, reproducirse y dispersarse en los ecosistemas receptores, inician un proceso de invasión con repercusiones ecológicas, económicas y sociales considerables lo que las convierte en especies exóticas invasoras (EEI) (Cuthbert et al., 2021; Hulme; 2003, 2006; Wittenberg y Cock, 2001; Pimentel et al., 2001). Muchos de estos impactos pueden alterar el funcionamiento de los ecosistemas y sus servicios, lo que tiene un efecto adverso en los medios de vida humanos, generalmente irreversibles (Kumschick et al., 2014; Simberloff et al., 2013; IUCN, 2000).
Se ha demostrado que las EEI incrementan las probabilidades de extinción de las especies nativas; afectan la composición genética de las poblaciones; modifican el comportamiento, la riqueza y la abundancia de las especies; alteran la diversidad filogenética entre las comunidades y, modifican las redes tróficas, la estructura y productividad de los ecosistemas, los ciclos de los nutrientes y los procesos hidrológicos (Pyšek et al., 2020; Blackburn et al., 2014; Wittenberg y Cock, 2001; Vitousek, 1990). En términos económicos, las EEI provocan pérdidas significativas en sectores como agricultura, silvicultura, pesca y salud pública (Haubrock et al., 2021; Pimentel et al., 2001; 2005). Entre los estudios sobre pérdidas económicas asociadas con invasiones biológicas, se encuentran los realizados por Haubrock et al. (2021), quienes mencionan la pérdida de 116 610 millones de euros (EUR) para 39 países europeos entre 1960 y 2020; la Oficina de Evaluación Tecnológica del Congreso de los Estados Unidos [OTA, por sus siglas en inglés] (1993) estimó una pérdida de 97 billones de dólares en daños por 79 especies exóticas de 1906 a 1991, principalmente causados por insectos y plantas; mientras que Pimentel et al. (2005) revelan que los costos por daños económicos asociados a EEI y su control en Estados Unidos asciende a 120 000 millones de dólares (USD) al año.
En un estudio realizado por Moodley et al. (2022), se demuestra que diversas EEI han causado daños en áreas naturales protegidas (ANP) de todos los continentes, con costos significativos en la gestión para controlarlas y/o erradicarlas, mientras que la resiliencia de las ANP a invasiones biológicas sigue siendo en gran parte desconocida (Hulme, 2018; Ziller et al., 2020). El impacto de las invasiones biológicas puede ser más significativo en las ANP que en los paisajes desprotegidos, ya que a menudo preservan una mayor proporción de especies nativas, endémicas y/o amenazadas que están menos adaptadas a las perturbaciones antropogénicas (Moodley et al., 2022).
Dentro de los ecosistemas más amenazados por la presencia de EEI a escala mundial, se encuentran los manglares (Ordinola-Zapata et al., 2019; Biswas et al., 2018; Valiela et al., 2001). Estos ecosistemas complejos y dinámicos se ubican en ecotonos costeros en constante fluctuación entre la tierra y el mar, localizados dentro de las latitudes 25° N y 30° S, y están considerados dentro de los ecosistemas más importantes y productivos del planeta debido a su capacidad para capturar y almacenar carbono, brindar protección costera ante fenómenos hidrometeorológicos y otros servicios ecosistémicos de sustento, aprovisionamiento, regulación y culturales (Leal y Spalding, 2022; Gorman, 2018; Donato et al., 2011; Zaldívar et al., 2004; Valiela et al., 2001). Sin embargo, algunas especies invasoras, principalmente plantas, modifican la estructura y composición de la vegetación nativa, impiden la regeneración natural de los mangles, reducen la productividad y la comunidad faunística (Biswas et al., 2018). La invasión de plantas en los bosques de manglar es mucho más generalizada y problemática de lo que comúnmente se percibe, lo que indica la necesidad de integrar estrategias de manejo en cada área particular (Biswas et al., 2018).
Por ejemplo, en la zona costera de Campeche, Yucatán y Quintana Roo, México, se encuentran dos ANP que conservan importantes bosques de manglar, las reservas de la biosfera Ría Celestún (RBRC) y Ría Lagartos (RBRL) las cuales, por su importancia biológica y ecológica a escala mundial, están listadas en la Red de Humedales de Importancia Internacional (The Secretariat of the Convention on Wetlands, 2023) y pertenecen al Programa Sobre el Hombre y la Biosfera (Organización de las Naciones Unidas para la Educación, la Ciencia y la Cultura [Unesco, por sus siglas en inglés], 2023), debido a esta importancia para la región, es fundamental contribuir al conocimiento para su conservación. La distribución e implicaciones de las EEI sobre los bosques de manglar en la RBRC y RBRL se desconoce, por lo que, este estudio brinda información importante para desarrollar estrategias de atención a EEI que permitan la conservación y restauración de los ecosistemas de las ANP.
OBJETIVOS
Los objetivos de este estudio fueron: 1) determinar la presencia de EEI en los bosques de manglar de la RBRC y RBRL ubicadas en la península de Yucatán, México; 2) identificar el nivel de riesgo de las EEI, y 3) aportar información de las implicaciones de las EEI en los bosques de manglar, con la finalidad de que se implementen estrategias de conservación y restauración en las ANP.
MATERIALES Y MÉTODOS
Área de estudio
La RBRC y RBRL (Fig. 1) se encuentran en la provincia biogeográfica Yucatán (Comisión Nacional para el Conocimiento y Uso de la Biodiversidad [Conabio], 1997), dentro de la región hidrológica prioritaria 102 “Anillo de cenotes” (Arriaga et al., 2002); en las regiones marinas prioritarias 60 “Champotón - El Palmar” y 62 “Dzilam-Contoy” (Arriaga et al., 1998); y en las regiones terrestres prioritarias 145 “Petenes-Ría Celestún” y 146 “Dzilam - Ría Lagartos - Yum Balam” (Arriaga et al., 2000).
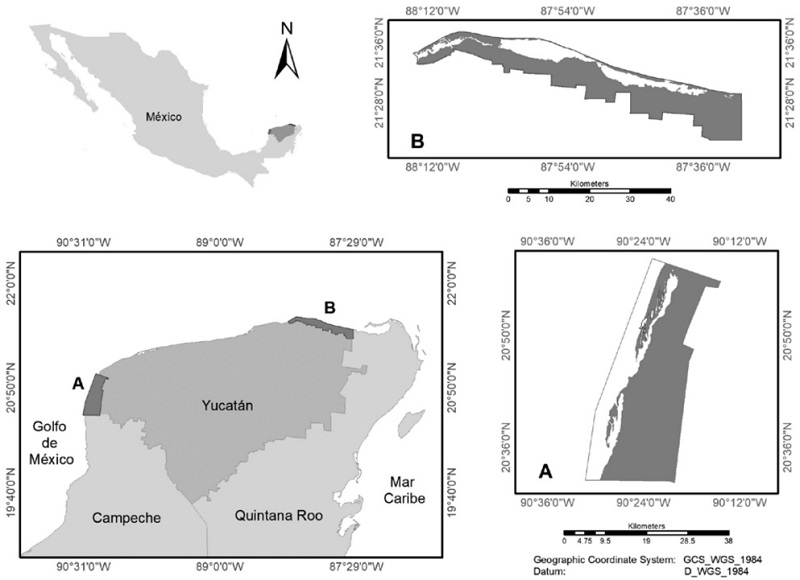
Figura 1
Ubicación geográfica de las reservas de la biosfera Ría Celestún (A) y Ría Lagartos (B).
La RBRC se localiza en la porción noroccidental de la península de Yucatán, en la franja costera que comprende los límites de los estados de Campeche y Yucatán, en las coordenadas extremas 20° 59’ 33.72" N, 90° 14’ 23.10" E, 20° 31’ 37.74" S y 90° 31’ 13.14" W; forma parte de la planicie continental de la costa norte de la península de Yucatán y tiene una altura promedio de 3 m s.n.m. (Comisión Nacional de Áreas Naturales Protegidas [Conanp] 2000; 2023). Tiene una superficie de 81 482.33 ha y como límites destaca, el corredor biológico que conforma al norte con la reserva estatal “El Palmar” y al sur con la reserva de la biosfera “Los Petenes” (Conanp, 2000); limita al este con los municipios de Celestún, Maxcanú, Halachó y Hunucmá en Yucatán, y Calkiní en Campeche, y al oeste con el Golfo de México (Instituto Nacional de Estadística y Geografía [Inegi], 2023). El tipo de vegetación más representativo es el manglar (Rhizophora mangle, Laguncularia racemosa y Avicennia germinans) que se encuentra en un buen estado de conservación, y desempeña una función determinante en la productividad biológica, tanto terrestre como marina (Tapia et al., 2008; Arriaga et al., 2000; Conanp, 2000).
La RBRL se localiza en el extremo oriental de la franja litoral de Yucatán, en las coordenadas extremas 21° 37’ 29.56’’ y 21° 23’ 00.96’’ latitud norte; 88° 14’ 33.35’’ y 87° 30’ 50.67’’ longitud oeste. Limita al norte con el Golfo de México, al sur con los municipios de Tizimín, Ría Lagartos y San Felipe, al este mantiene un corredor biológico con el área de protección de flora y fauna Yum Balam y al oeste con la reserva estatal de Dzilam (Conanp, 2007; Inegi, 2023). Constituye un complejo de ecosistemas terrestres, dulceacuícolas y marinos limitados por 90 vértices de la poligonal con una superficie de 60 347.82 ha (Conanp, 2007). No existen corrientes superficiales y el agua se filtra formando un manto freático de poca profundidad compuesta por grutas, corrientes subterráneas, cenotes y aguadas. En la porción sur, se localizan los únicos lomeríos que alcanzan los 10 m s.n.m, estas pequeñas variaciones topográficas son de gran importancia para la hidrodinámica superficial. El principal tipo de vegetación es el manglar (Rhizophora mangle, Avicennia germinans, Conocarpus erectus y en menor abundancia Laguncularia racemosa) que tiene un elevado valor biogeográfico y ecosistémico, el cual ocupa 24.31% de la superficie del polígono del ANP (Arriaga et al., 2000; Conanp 2007; 2023).
Análisis de información
Para determinar la presencia de las EEI en la RBRC y RBRL, se realizó un análisis con base en el Sistema Nacional de Información sobre Biodiversidad (SNIB) de la Comisión Nacional para el Conocimiento y Uso de la Biodiversidad (Conabio, 2023); el Sistema Global de Información sobre Biodiversidad [GBIF, por sus siglas en inglés] (2023); los listados taxonómicos del programa de manejo de la RBRC (Conanp, 2000) y del programa de conservación y manejo de la RBRL (Conanp, 2007); y se realizó una búsqueda de la literatura científica especializada en los siguientes recursos electrónicos: Google académico, PubMED, Redalyc, Scielo y Springer Link. Para la validación biogeográfica de las EEI dentro de los polígonos de la RBRC y RBRL, se utilizó el atlas de las áreas naturales protegidas de México y el GBIF (Conanp, 2023; GBIF, 2023), mientras que para la distribución en los bosques de manglar se utilizó la capa de información “distribución de los manglares de México en 2020” del portal de geoinformación del SNIB (Conabio, 2023).
Para validar la nomenclatura taxonómica de las EEI identificadas, se utilizaron las siguientes referencias de información especializada: Mammal Species of the World (Wilson y Reader, 2005), International Ornithological Commitee (Gill et al., 2023), Fishbase (Froese y Pauly, 2023), Reptile-database (Uetz et al., 2023), World Register of Marine Species (WoRMS Editorial Board, 2023), Tropicos.org. Missouri Botanical Garden (Tropicos, 2023), Algaebase (Guiry y Guiry, 2023) y del Centro de Biociencia Agrícola Internacional [CABI, por sus siglas en inglés] (2023).
El criterio para catalogar una especie como exótica invasora dependió de dos elementos: 1) las características de la definición de la Ley General de Vida Silvestre, que menciona a aquella especie o población que no es nativa, que se encuentra fuera de su ámbito de distribución natural, que es capaz de sobrevivir, reproducirse y establecerse en hábitats y ecosistemas naturales y que amenaza la diversidad biológica nativa, la economía o la salud pública (Congreso General de los Estados Unidos Mexicanos, 2010), y 2) que la especie estuviera evaluada a través del Método de Evaluación Rápida de Invasividad (MERI). El MERI es una herramienta basada en el método jerárquico analítico para la evaluación rápida del riesgo potencial de una especie como invasora (Conabio, 2015). Adicionalmente, se identificó si las EEI se encuentran en el acuerdo por el que se determina la lista de especies exóticas invasoras para México (Secretaría de Medio Ambiente y Recursos Naturales [Semarnat], 2016) y en la lista de las 100 EEI más invasivas del mundo (Lowe et al., 2004).
Derivado de que la RBRC y la RBRL comparten características de forma, extensión, ecosistemas y problemática, se elaboró un dendrograma con los datos de presencia-ausencia del total de las EEI identificadas en ambas ANP para determinar su similitud, para lo cual se utilizó el programa estadístico Past v4.13 aplicando el índice de Jaccard, el cual tiene el siguiente fundamento:

El resultado del índice de Jaccard varía entre 0 y 1. Un valor de 0 indica que no hay especies en común, mientras que un valor de 1 indica que los sitios tienen máxima similitud en composición de especies.
RESULTADOS Y DISCUSIÓN
Derivado del análisis de la información, se determinó la presencia de 35 EEI en ambas ANP (Tabla 1), de las cuales, 30 corresponden a la RBRC y 29 a la RBRL, estas se ordenaron en siete grupos taxonómicos: mamíferos (4 especies); aves (7); reptiles (3); peces (1); invertebrados (4); plantas (14) y macroalgas (2) (Fig. 2).
Listado taxonómico de especies exóticas invasoras en las reservas de la biosfera Ría Celestún (RBRC) y Ría Lagartos (RBRL).
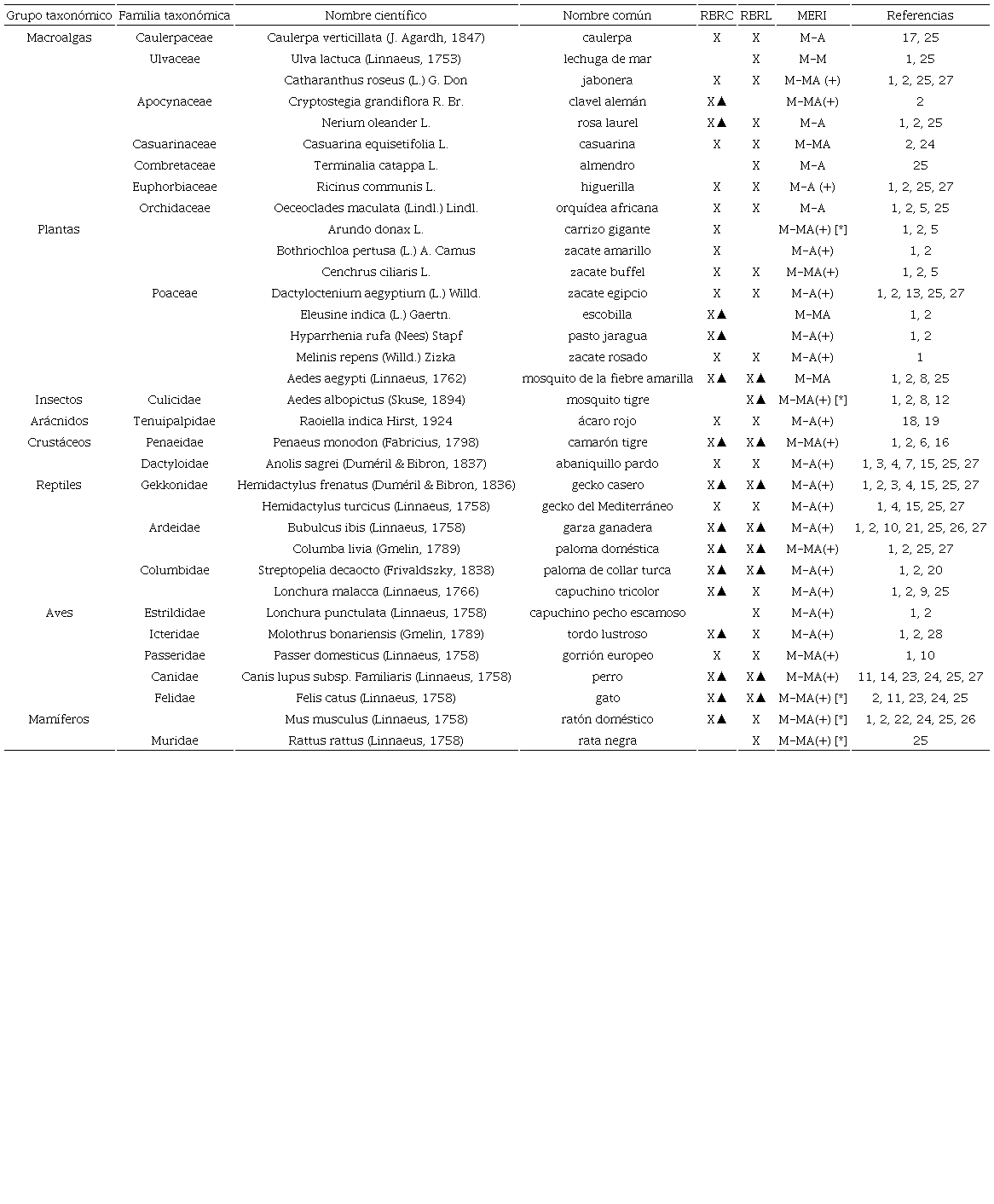
▲ = Especie en áreas de distribución de bosque de manglar; M-MA = MERI - Muy Alto; M-A = MERI - Alto; M-M = MERI - Medio; (+) = Especie dentro del Acuerdo por el que se determina la lista de las especies exóticas invasoras para México; [*] = Lista de las 100 especies exóticas invasoras más dañinas del mundo. Referencias de la tabla: Conabio, 2023 (1); GBIF, 2023 (2); Ortiz-Medina et al., 2022 (3); González-Sánchez et al., 2021 (4); Martínez et al., 2021 (5); Wakida-Kusunoki et al., 2021 (6); Vásquez-Cruz et al., 2020 (7); Bond et al., 2019 (8); Degante-González et al., 2018 (9); Flota-Bañuelos et al., 2018 (10); Fundación Pedro y Elena Hernández, 2018 (11); Ortega-Morales et al., 2018 (12); Parra-Tabla et al., 2018 (13); Pronatura Península de Yucatán, 2018 (14); González-Sánchez et al., 2017 (15); Wakida-Kusunoki et al., 2016 (16); Espinoza-Avalos et al., 2015 (17); Ramírez, 2014 (18); Villa et al., 2013 (19); Chablé-Santos et al., 2012 (20); Cepeda-González et al., 2011 (21); Chablé-Santos y Sosa-Escalante, 2010 (22); De la Gala y Plata, 2008 (23); Kantún, 2008 (24); Conanp, 2007 (25); Cimé et al., 2006 (26); Conanp, 2000 (27); Kluza, 1998 (28).
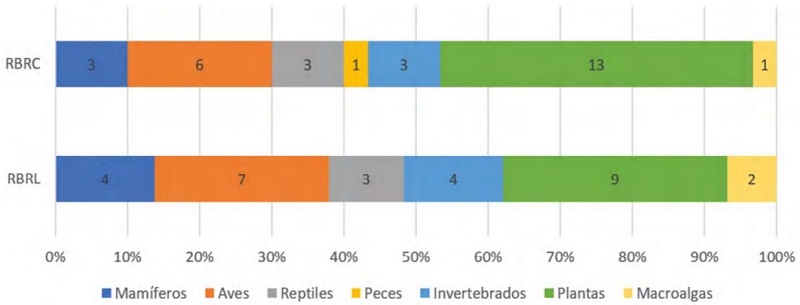
Figura 2
Número de especies exóticas invasoras identificadas por grupo taxonómico en las reservas de la biosfera Ría Celestún y Ría Lagartos y su proporción en porcentaje.
Por el número de EEI, los grupos taxonómicos más representativos fueron las plantas y las aves. Para el caso de las plantas se identificaron seis familias taxonómicas: Poaceae (7 especies); Apocynaceae (3); Casuarinaceae (1), Combretaceae (1); Euphorbiaceae (1) y Orchidaceae (1), mientras que para las aves se identificaron cinco familias taxonómicas: Columbidae (2 especies); Estrildidae (2); Ardeidae (1); Icteridae (1) y Passeridae (1).
De acuerdo con el análisis sobre la presencia de EEI en los bosques de manglar, se encontró el registro de 16 especies (Tabla 1), lo que representa 45.71% del total de las EEI identificadas en el polígono de las áreas de estudio. Las especies fueron: mamíferos (Canis lupus subsp. familiaris, Felis catus y Mus musculus); aves (Bubulcus ibis, Columba livia, Lonchura malacca, Molothrus bonariensis y Streptopelia decaocto); reptiles (Hemidactylus frenatus); invertebrados (Aedes aegypti, Aedes albopictus y Penaeus monodon) y plantas (Cryptostegia grandiflora, Eleusine indica; Hyparrhenia rufa y Nerium oleander).
De las 16 EEI identificadas en los bosques de manglar, destacan las especies ferales como el perro (Canis lupus subsp. familiaris) y el gato (Felis catus), que son consideradas de alto impacto a los ecosistemas, los cuales tienen como punto de partida los centros rurales o urbanos situados en las zonas de influencia de las ANP (Lessa et al., 2016). Los gatos son cazadores oportunistas y su comportamiento depredador es innato, por lo que son una seria amenaza para muchas especies de vida silvestre (Mella-Méndez et al., 2022), de igual forma, se ha demostrado que el mayor impacto de los perros sobre la biodiversidad nativa es la depredación (Hughes y Macdonald, 2013). El caso más emblemático registrado es la aniquilación de 50% de una población del kiwi marrón (Apteryx mantelli) por un solo perro en la isla norte de Nueva Zelanda (Taborsky, 1988).
Es importante evaluar la abundancia de perros y los patrones de movimiento en los bosques de manglar de la RBRC y RBRL para evidenciar las afectaciones a la biodiversidad en general, ya que solo se tiene registro del impacto sobre las poblaciones de flamenco rosado (Phoenicopterus ruber) y las tortugas marinas (Eretmochelys imbricata y Chelonya midas) en la RBRL (Pronatura, 2018; Fundación Pedro y Elena Hernández, 2018). Además, la presencia de perros ferales en áreas naturales aumenta el riesgo de trasmisión de enfermedades para la vida silvestre (Young et al., 2011).
Referente al nivel de riesgo de las EEI identificadas en la RBRC y la RBRL, utilizando los parámetros del MERI, se encontraron 16 EEI con riesgo muy alto, lo que representa 45.71%; 18 EEI con riesgo alto (51.42%) y una EEI con riesgo medio (2.85%) (Tabla 1). Particularmente, para las 16 EEI identificadas en los bosques de manglar, nueve tienen un nivel de riesgo de invasividad “muy alto” y siete “alto”, lo que representa 56.25% y 43.75% respectivamente (Tabla 1).
De manera complementaria, para la RBRC y la RBRL se identificó que 74% de las EEI presentes se encuentran dentro del acuerdo por el que se determina la lista de las especies exóticas invasoras para México (Tabla 1), lo que deja a 26% de las especies sin normatividad pese a que cuentan con un MERI que les da el carácter de EEI. Preocupa el caso particular de las especies forestales como la casuarina (Casuarina equisetifolia) que afecta las zonas costeras y erosiona el suelo; la altamente invasiva orquídea africana (Oeceoclades maculata) y el mosquito de la fiebre amarilla (Aedes aegypti).
Respecto a la lista de las 100 especies exóticas invasoras más dañinas del mundo, se identificaron las siguientes: carrizo gigante (Arundo donax), mosquito tigre (Aedes albopictus); gato (Felis catus); ratón doméstico (Mus musculus) y rata negra (Rattus rattus) (Tabla 1), todas con riesgo de invasividad muy alto de acuerdo con el MERI y todas en el acuerdo por el que se determina la lista de las especies exóticas invasoras para México.
En lo que respecta a las implicaciones de las EEI en los bosques de manglar, de acuerdo con información de la Base de Datos Mundial sobre Especies Invasoras [GISD, por sus siglas en inglés] (2023), el compendio de especies invasoras de CABI (CABI, 2023) y del MERI (Conabio, 2015) se identificaron los siguientes impactos: Mus musculus (compite con especies de roedores nativos, se adapta rápidamente a todo tipo de ambientes y ha sido asociado a extinción de especies); Bubulcus ibis (compite con otras garzas por alimento, sitios de anidación y material para la construcción de nidos); Columba livia y Streptopelia decaocto (asociadas a comunidades humanas compiten con aves nativas por alimento y sitios de anidación); Lonchura malacca (compite por alimento con otras aves); Molothrus bonariensis (destruye huevos de otras especies de aves); Aedes albopictus (ataca a aves, reptiles y anfibios y puede transmitir enfermedades); Penaeus monodon (compite por alimento con otros camarones ya que es un depredador agresivo que consume pequeños crustáceos y moluscos); Cryptostegia grandiflora (desplaza vegetación nativa e incrementa el riesgo de erosión del suelo); Eleusine indica (invade hábitats perturbados en márgenes de vegetación natural y zonas costeras; Hyparrhenia rufa y Nerium oleander (desplazan plantas nativas).
El establecimiento de EEI impacta significativamente a las especies de mangle y a la comunidad faunística asociada, lo que afecta la estructura de las cadenas tróficas y los beneficios sociales derivados de los bosques de manglar. Asimismo, otros problemas como la tala, la contaminación del agua y suelo, y la urbanización son presiones que conducen a la degradación, permitiendo la invasión de especies exóticas y posterior colonización del bosque (Programa de las Naciones Unidas para el medio ambiente [UNEP, por sus siglas en inglés], 2023).
Las vías de introducción de las EEI, por lo tanto, derivan de presiones antropogénicas recurrentes. Para el caso de la RBRC, la construcción de carreteras e infraestructura para el turismo no solo fragmenta ecosistemas naturales y abre espacios para la invasión de especies exóticas, sino que ha impactado en la pérdida de bosques de manglar y la modificación de los flujos de agua dulce tan necesarios para ese ecosistema (Conanp, 2000). Para el caso de la RBRL, el cambio de uso de suelo para actividades productivas - como la ganadería - ha causado la reducción de áreas de bosque de manglar (Conanp, 2007), aunado a que la ganadería no sostenible es considerada una vía de introducción de pastos exóticos invasores.
Pese a que la RBRC y la RBRL se encuentran en litorales opuestos en el estado de Yucatán, se identificó una similitud de 0.68 de acuerdo con el índice de Jaccard (Fig. 3). La similitud por grupo taxonómico correspondió a: 0.75 mamíferos; 0.85 aves; 1.0 reptiles; 0 peces; 0.75 invertebrados; 0.57 plantas y 0.5 macroalgas. Por lo que se sugiere una distribución generalizada en la mayoría de los grupos en la región costera del estado de Yucatán y/o vías de introducción similares.
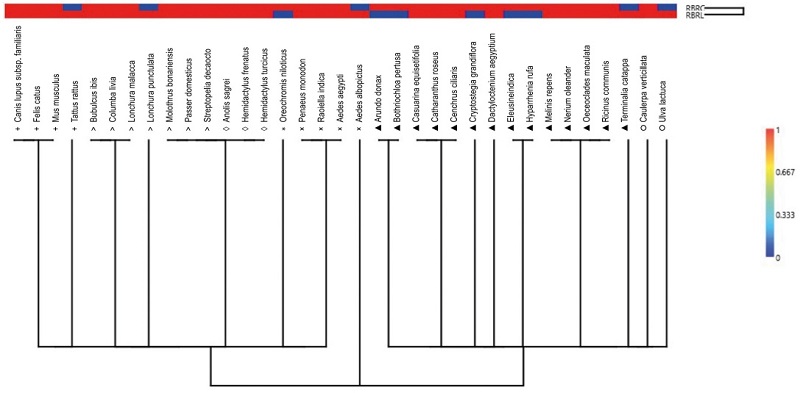
Figura 3
Similitud entre las especies exóticas invasoras en las reservas de la biosfera Ría Celestún y Ría Lagartos.
(+) mamíferos; (>) aves; (◊) reptiles; (*) peces; (×) invertebrados; (▲) plantas; (○) macroalgas.
La premisa de que las invasiones biológicas perjudican el desempeño de las ANP para conservar bosques de manglar (Ren et al., 2021) tiene una gran implicación en este estudio, ya que la contribución al conocimiento de este tema, debe incentivar a fortalecer las estrategias de prevención, erradicación y control de EEI en los bosques de manglar de la RBRC y de la RBRL, las cuales deberían ser implementadas en función de la presencia temprana o distribución restringida de las EEI, y de la disponibilidad de recursos humanos, técnicos y financieros. Se deben invertir los mayores esfuerzos en estrategias que ofrezcan los mejores resultados a gran escala con el menor costo posible, con la finalidad de tener mejores oportunidades para la conservación de los bosques de manglar, mantener la biodiversidad y los servicios ecosistémicos.
CONCLUSIONES
Se encontró la presencia de 16 especies exóticas invasoras en áreas de distribución de bosques de manglar de las reservas de la biosfera Ría Celestún y Ría Lagartos, las cuales se clasificaron en los siguientes grupos taxonómicos: plantas (cuatro especies), invertebrados (3), reptiles (1), aves (5) y mamíferos (3). De las 16 especies, nueve tienen un nivel de riesgo de invasividad “muy alto” y siete de “alto”, lo que representa 56.25% y 43.75% respectivamente. Las implicaciones de las especies exóticas invasoras sobre los bosques de manglar se centran en la desestabilización de su estructura y funcionamiento, ya que compiten, depredan y trasmiten enfermedades a las poblaciones de especies nativas afectando a mayor escala los servicios ecosistémicos, por lo que se deben fortalecer estrategias de prevención, erradicación y control de EEI en los bosques de manglar de las reservas de la biosfera Ría Celestún y Ría Lagartos. La aplicabilidad del presente estudio puede extrapolarse hacia las áreas naturales protegidas con las cuales los sitios de estudio forman corredores biológicos y plantear estrategias regionales para evitar la dispersión de especies exóticas invasoras o prevenir el ingreso de nuevas especies.
RECONOCIMIENTOS
El primer autor agradece al Consejo Nacional de Humanidades, Ciencias y Tecnologías por la beca para realizar los estudios de doctorado. El segundo autor agradece a la UAM-Xochimilco por el financiamiento del proyecto: “Modelos de ecología y dinámica poblacional de peces en sistemas costeros estuarinos tropicales”, y la participación de la Dra. Brenda Iliana Vega Rodríguez.
REFERENCIAS
Arriaga, L., Aguilar, V., & Alcocer, J. (2002). Aguas continentales y diversidad biológica de México. Conabio. http://www.conabio.gob.mx/conocimiento/regionalizacion/doctos/hidrologicas.html
Arriaga, L., Espinoza, J. M., Aguilar, C., Martínez, E., Gómez, L., & Loa, E. (2000). Regiones terrestres prioritarias de México. Conabio. http://www.conabio.gob.mx/conocimiento/regionalizacion/doctos/terrestres.html
Arriaga, L., Vázquez, E., González, J., Jiménez, R., Muñoz, E., & Aguilar, V. (1998). Regiones marinas prioritarias de México. Conabio. http://www.conabio.gob.mx/conocimiento/regionalizacion/doctos/marinas.html
Base de Datos Mundial sobre Especies Invasoras [GISD] (2023). Invasive Species Specialist Group. GISD. http://www.iucngisd.org/gisd/
Biswas, S. R., Biswas, P. L., Limon, S. H., Yan, E., Xu, M., & Khan, M. S. I. (2018). Plant invasion in mangrove forests worldwide. Forest Ecology and Management, 429, 480-492. https://doi.org/10.1016/j.foreco.2018.07.046
Blackburn, T. M., Essl, F., Evans, T., Hulme, P. E., Jeschke, J. M., Kühn, I., Kumschick, S., Marková, Z., Mrugała, A., Nentwig, W., Pergl, J., Pyšek, P., Rabitsch, W., Ricciardi, A., Richardson, D. M., Sendek, A., Vilà, M., Wilson, J. R., Winter, M., Bacher, S. (2014). A unified classification of alien species based on the magnitude of their environmental impacts. PLOS Biology, 12(5), e1001850. https://doi.org/10.1371/journal.pbio.1001850
Bond, J. G., Casas, M., Moo, D. A., Marina, C. F., Danis, R., Ulloa, A., Elizondo, A. E., Ortega, A., & Núñez, C. (2019). Diagnóstico del estado actual de la invasión biológica por Aedes (Stegomyia) albopictus (Skuse) (Díptera: Culícidae) en las principales áreas naturales protegidas de la Península de Yucatán, México. Conabio. http://www.conabio.gob.mx/institucion/proyectos/resultados/InfLI040.pdf
Centro de Biociencia Agrícola Internacional [CABI] (2023). Compendium Invasive Species. CABI. https://www.cabidigitallibrary.org/product/qi
Cepeda-González, M. F., Escalona-Segura, G., Montero-Muñoz, J. L., Méndez-González, M. E., Pozo-de la Tijera, C., & Hernández-Betancourt, S. (2011). Composición de especies de aves en potreros de matrices de origen antropogénico y mixto en la Reserva de la Biosfera Ría Lagartos, Yucatán, México. Brenesia, 2011(75-73), 37-48.
Chablé-Santos, J., Gómez-Uc, E., & Hernández-Betancourt, S. (2012). Registros reproductivos de la paloma de collar (Streptopelia decaocto) en Yucatán, México. Huitzil Revista Mexicana de Ornitología, 13(1), 1-5. https://doi.org/10.28947/hrmo.2012.13.1.140
Chablé-Santos, J., & Sosa-Escalante, J. (2010). Valoración y medición de la biodiversidad de aves y mamíferos terrestres de la Reserva de la Biosfera Ría Celestún, Yucatán, México. En E. Acosta-Lugo, D. Alonzo-Parra, M. Andrade-Hernández, D. Castillo-Tzab, J. Chablé-Santos, R. Durán, C. Espadas-Manrique, I. Fernández-Stohanzlova, J. Fraga, E. Galicia, J.A. González-Iturbe, J. Herrera-Silveira, J. Sosa-Escalante, G.J. Villalobos-Zapata, & F. Tun-Dzul (Eds.), Plan de Conservación de la Eco-región: Petenes-Celestún-Palmar (pp. 97-125). Universidad Autónoma de Campeche Pronatura Península de Yucatán A. C. http://etzna.uacam.mx/epomex/pdf/Eco-region.pdf
Cimé, J. A., Chablé-Santos, J. B., Sosa-Escalante, J. E., & Hernández-Betancourt, S. F. (2006). Quirópteros y pequeños roedores de la reserva de la biosfera Ría Celestún, Yucatán, México. Acta Zoológica Mexicana, 22(1), 127-131. https://doi.org/10.21829/azm.2006.2211967
Comisión Nacional de Áreas Naturales Protegidas [Conanp] (2000). Programa de Manejo de la Reserva de la Biosfera Ría Celestún. Conanp. https://www.conanp.gob.mx/que_hacemos/pdf/programas_manejo/celestun.pdf
Comisión Nacional de Áreas Naturales Protegidas [Conanp] (2007). Programa de Conservación y Manejo de la Reserva de la Biosfera Ría Lagartos. Conanp. https://iefectividad.conanp.gob.mx/iefectividad/PYyCM/RB%20Ria%20Lagartos/2.COMPONENTE%20CON-TEXTO%20PLANEACION/10.-Recursos%20Culturales/PCM_RiaLagartos%20final-2007.pdf
Comisión Nacional de Áreas Naturales Protegidas [Conanp] (2023). Información espacial de las áreas naturales protegidas. Conanp. http://sig.conanp.gob.mx/website/pagsig/info_shape.htm
Comisión Nacional para el Conocimiento y Uso de la Biodiversidad [Conabio] (1997). Provincias biogeográficas de México. Conabio. http://geoportal.conabio.gob.mx/metadatos/doc/html/rbiog4mgw.html
Comisión Nacional para el Conocimiento y Uso de la Biodiversidad [Conabio] (2015). Método de Evaluación Rápida de Invasividad (MERI) para especies exóticas en México. Conabio. https://www.biodiversidad.gob.mx/media/1/especies/Invasoras/files/Instrutivo_MERI_2020.pdf
Comisión Nacional para el Conocimiento y Uso de la Biodiversidad [Conabio] (2023). Sistema Nacional de Información sobre Biodiversidad. Conabio. https://www.snib.mx/
Ley General de Vida Silvestre. Diario Oficial de la Federación. https://www.diputados.gob.mx/LeyesBiblio/pdf/146_200521.pdf
Cuthbert, R. N., Diagne, C., Haubrock, P. J., Turbelin, A., & Courchamp, F. (2021). Are the “100 of the world’s worst” invasive species also the costliest? Biological Invasions, 24(7), 1895-1904. https://doi.org/10.1007/s10530-021-02568-7
Degante-González, A. P., Tepatlán-Vargas, R., Ramírez-Utrera, A. L., Mora-Heredia, E., & Villegas-Patraca, R. (2018). Registro del capuchino tricolor (Lonchura malacca) en el istmo de Tehuantepec, Oaxaca, México. Revista Mexicana de Biodiversidad, 89(2), 582-586. https://doi.org/10.22201/ib.20078706e.2018.2.2036
De la Gala, J. R., & Plata, M. A. (2008). Ría Celestún. En E. Schüttler, & C.S. Karez (Eds.), Especies exóticas invasoras en las Reservas de Biosfera de América Latina y el Caribe. Un informe técnico para fomentar el intercambio de experiencias entre las Reservas de Biosfera y promover el manejo efectivo de las invasiones biológicas (pp. 235-237). Unesco. https://unesdoc.unesco.org/ark:/48223/pf0000182768
Donato, D. C., Boone, J., Murdiyarso, D., Kurnianto, S., Stidham, M., & Kanninen, M. (2011). Mangroves among the most carbon-rich forests in the tropics. Nature Geoscience, 4(5), 293-297. https://doi.org/10.1038/ngeo1123
Espinoza-Avalos, J., Aguilar-Rosas, L. E., Aguilar-Rosas, R., Gómez-Poot, J. M., & Raigoza-Figueras, R. (2015). Presencia de Caulerpaceae (Chlorophyta) en la Península de Yucatán, México. Botanical Sciences, 93(4), 845-854. https://doi.org/10.17129/botsci.160
Flota-Bañuelos, C., Candelaria-Martínez, B., Mejénes-López, S. M. A., Vázquez-May, L. A., Castillo-Sánchez, L., & López-Coba, E. (2018). Avifauna de áreas agropecuarias y de regeneración en Tizimín, Yucatán, México. Agroproductividad, 11(6), 24-30. https://www.revista-agroproductividad.org/index.php/agroproductividad/article/view/422
Froese, R., & Pauly, D. (2023). FishBase. https://www.fishbase.org
Fundación Pedro y Elena Hernández (2018). Monitoreo y conservación del flamenco del Caribe y su hábitat en cuatro áreas naturales protegidas de la península de Yucatán. Conanp.
Gill, F., Donsker, D., & Rasmussen, P. (2023). IOC World Bird List (v13.1). https://doi.org/10.14344/IOC.ML.13.1
González-Sánchez, V. H., Johnson, J. D., García-Padilla, E., Mata-Silva, V., DeSantis, D. L., & Wilson, L. D. (2017). The Herpetofauna of the Mexican Yucatan Peninsula: composition, distribution, and conservation status. Mesoamerican herpetology, 4(2), 264-380.
González-Sánchez, V. H., Johnson, J. D., González-Solís, D., Fucsko, L. A., & Wilson, L. D. (2021). A review of the introduced herpetofauna of Mexico and Central America, with comments on the effects of invasive species and biosecurity methodology. ZooKeys, 1022, 79-154. https://doi.org/10.3897/zookeys.1022.51422
Gorman, D. (2018). Historical Losses of Mangrove Systems in South America from Human-Induced and Natural Impacts. In C. Makowski, & C.W. Finkl (Eds.), Threats to Mangrove Forests (pp. 155-171). Springer. https://doi.org/10.1007/978-3-319-73016-5_8
Guiry, M.D., & Guiry, G.M. (2023). AlgaeBase. National University of Galway. https://www.algaebase.org
Haubrock, P. J., Turbelin, A., Cuthbert, R. N., Novoa, A., Taylor, N. G., Angulo, E., Ballesteros-Mejia, L., Bodey, T. W., Capinha, C., Diagne, C., Essl, F., Golivets, M., Kirichenko, N., Kourantidou, M., Leroy, B., Renault, D., Verbrugge, L., & Courchamp, F. (2021). Economic costs of invasive alien species across Europe. NeoBiota, 67, 153-190. https://doi.org/10.3897/neobiota.67.58196
Hughes, J., & Macdonald, D. W. (2013). A review of the interactions between free-roaming domestic dogs and wildlife. Biological Conservation, 157, 341-351. https://doi.org/10.1016/j.biocon.2012.07.005
Hulme, P. E. (2003). Biological invasions: winning the science battles but losing the conservation war? Oryx, 37(2), 178-193. https://doi.org/10.1017/s003060530300036x
Hulme, P. E. (2006). Beyond control: wider implications for the management of biological invasions. Journal of Applied Ecology, 43(5), 835-847. https://doi.org/10.1111/j.1365-2664.2006.01227.x
Hulme, P. E. (2018). Protected land: Threat of invasive species. Science, 361(6402), 561-562. https://doi.org/10.1126/science.aau3784
Instituto Nacional de Estadística y Geografía [Inegi] (2023). Mapa digital de México. Inegi. https://www.inegi.org.mx/app/mapa/espacioydatos/
Kantún, R. (2008). Ría Lagartos. En E. Schüttler, & C. S. Karez (Eds.), Especies exóticas invasoras en las Reservas de Biosfera de América Latina y el Caribe. Un informe técnico para fomentar el intercambio de experiencias entre las Reservas de Biosfera y promover el manejo efectivo de las invasiones biológicas (pp. 238-240). Unesco. https://unesdoc.unesco.org/ark:/48223/pf0000182768
Kluza, D. A. (1998). First Record of Shiny Cowbird (Molothrus bonariensis) in Yucatán, Mexico. The Wilson Bulletin, 110(3), 129-130. https://sora.unm.edu/sites/default/files/journals/wilson/v110n03/p0429-p0430.pdf
Kumschick, S., Gaertner, M., Vilà, M., Essl, F., Jeschke, J. M., Pyšek, P., Ricciardi, A., Bacher, S. , Blackburn, T. M., Dick, J. T. A., Evans, T., Hulme, P. E., Kühn, I., Mrugała, A., Pergl, J., Rabitsch, W., Richardson, D. M., Sendek, A., & Winter, M. (2014). Ecological Impacts of Alien Species: Quantification, scope, caveats, and recommendations. BioScience, 65(1), 55-63. https://doi.org/10.1093/ biosci/biu193
Leal, M., & Spalding, M. (2022). The State of the World’s Mangroves 2022. Global Mangrove Alliance. https://www.mangrovealliance.org/wp-content/uploads/2022/09/The-State-of-the-Worlds-Mangroves-Report_2022.pdf
Lessa, I., Guimarães, T. C. S., Bergallo, H. G., Cunha, A., & Vieira, E. M. (2016). Domestic dogs in protected areas: a threat to Brazilian mammals? Natureza & Conservacao, 14(2), 46-56. https://doi.org/10.1016/j.ncon.2016.05.001
Lowe, S., Browne, M., Boudjelas, S. & De-Poorter, M. (2004). 100 de las Especies Exóticas Invasoras más dañinas del mundo. Una selección del Global Invasive Species Database. Grupo Especialista de Especies Invasoras de la Unión Mundial para la Naturaleza. https://portals.iucn.org/library/sites/library/files/documents/2000-126-Es. pdf
Martínez, M. L., Castillo-Campos, G., García-Franco, J. G., Pérez-Maqueo, O., Mendoza-González, G., & Pale-Pale, J. (2021). Mexican Coastal dunes: recipients and donors of alien flora. Diversity, 13(11), 530. https://doi.org/10.3390/d13110530
Moodley, D., Angulo, E., Cuthbert, R. N., Leung, B., Turbelin, A., Novoa, A., Kourantidou, M., Heringer, G., Haubrock, P. J., Renault, D., Robuchon, M., Fantle-Lepczyk, J., Courchamp, F., & Diagne, C. (2022). Surprisingly high economic costs of biological invasions in protected areas. Biological Invasions, 24(7), 1995-2016. https://doi.org/10.1007/s10530-022-02732-7
Mella-Méndez, I. M., Flores-Peredo, R., Amaya-Espinel, J. D., Bolívar-Cimé, B., MacSwiney, M. C., & Martínez, A. J. (2022). Predation of wildlife by domestic cats in a neotropical city: a multi-factor issue. Biological Invasions, 24(5), 1539-1551. https://doi.org/10.1007/s10530-022-02734-5
Oficina de Evaluación Tecnológica del Congreso de Estados Unidos [OTA] (1993). Harmful Non-Indigenous Species in the United States. Oficina de Evaluación Tecnológica del Congreso de Estados Unidos. https://ota.fas.org/reports/9325.pdf
Ordinola-Zapata, A., Siccha, Z. R., Castillo-Carrillo, P. S., & Luque, C. (2019). Identification by DNA barcode of invading fish in the mangrove of Tumbes (Peru). Manglar, 16(2), 91-97. https://doi.org/10.17268/manglar.2019.013
Organización de las Naciones Unidas para la Educación, la Ciencia y la Cultura [Unesco] (2023). World Network of Biosphere Reserves. Unesco. https://en.unesco.org/biosphere/lac#Mexico
Ortega-Morales, A. I., Bond, G., Méndez‐López, R., Garza-Hernández, J. A., Hernández-Triana, L. M., & Casas-Martínez, M. (2018). First record of invasive mosquito Aedes albopictus in Tabasco and Yucatan, Mexico. Journal of The American Mosquito Control Association, 34(2), 120-123. https://doi.org/10.2987/18-6736.1
Ortiz-Medina, J. A., Peña-Peniche, A., & Chablé-Santos, J. (2022). Diversidad de anfibios y reptiles en cuatro tipos de vegetación de la Reserva de la Biosfera Ría Lagartos, México. Revista Latinoamericana de Herpetología, 5(4), 16-32. https://doi.org/10.22201/fc.25942158e.2022.4.435
Parra-Tabla, V., Albor-Pinto, C., Tun-Garrido, J., Angulo, D. F., Barajas, C., Silveira, R., Ortiz-Díaz, J. J., & Arceo-Gómez, G. (2018). Spatial patterns of species diversity in sand dune plant communities in Yucatan, Mexico: Importance of invasive species for species dominance patterns. Plant Ecology & Diversity, 11(2), 157-172. https://doi.org/10.1080/17550874.2018.1455232
Pimentel, D., McNair, S., Janecka, J. E., Wightman, J. A., Simmonds, C., O’Connell, C., Wong, E., Russel, L., Zern, J., Aquino, T., & Tsomondo, T. (2001). Economic and environmental threats of alien plant, animal, and microbe invasions. Agriculture, Ecosystems and Environment, 84(1), 1-20. https://doi.org/10.1016/s01678809(00)00178-x
Pimentel, D., Zuniga, R., & Morrison, D. (2005). Update on the environmental and economic costs associated with alien-invasive species in the United States. Ecological Economics, 52(3), 273-288. https://doi.org/10.1016/j.ecolecon.2004.10.002
Programa de las Naciones Unidas para el Medio Ambiente [UNEP] (2023). Decades of mangrove forest change: what does it mean for nature, people and the climate? UNEP. https://www.unep.org/resources/report/decadesmangrove-forest-change-what-does-it-mean-nature-people-and-climate
Pronatura (2018). Conservación de las Tortugas Marinas en la Playa Río Lagartos. Pronatura Península de Yucatán Conanp.
Pyšek, P., Hulme, P. E., Simberloff, D., Bacher, S. , Blackburn, T. M., Carlton, J. T., Dawson, W., Essl, F., Foxcroft, L. C., Genovesi, P., Jeschke, J. M., Kühn, I., Liebhold, A. M., Mandrak, N. E., Meyerson, L. A., Pauchard, A., Pergl, J., Roy, H. E., Seebens, H., Richardson, D. J. (2020). Scientists’ warning on invasive alien species. Biological Reviews, 95(6), 1511-1534. https://doi.org/10.1111/brv.12627
Ramírez, J. (2014). Mecanismos de dispersión y resistencia al ayuno en Raoiella indica Hirst (Acari: Tenuipalpidae) [Tesis de maestría, Colegio de Postgraduados]. http://colposdigital.colpos.mx:8080/jspui/bit-stream/10521/2239/1/Ramirez_Lopez_J_MC_Entomologia_Acarologia_2014. pdf
Ren, J., Chen, J., Xu, C., Van De Koppel, J., Thomsen, M. S., Qiu, S., Cheng, F., Song, W., Liu, Q., Xu, C., Bai, J., Zhang, Y., Cui, B., Bertness, M. D., Silliman, B. R., Li, B., & He, Q. (2021). An invasive species erodes the performance of coastal wetland protected areas. Science Advances, 7(42). https://doi.org/10.1126/sciadv.abi8943
Secretaría de Medio Ambiente y Recursos Naturales [Semarnat] (2016). Acuerdo por el que se determina la lista de especies exóticas invasoras para México. Diario Oficial de la Federación. https://www.dof.gob.mx/nota_detalle.php?codigo=5464456&fecha=07/12/2016#gsc.tab=0
Simberloff, D., Martin, J., Genovesi, P., Maris, V., Wardle, D. A., Aronson, J., Courchamp, F., Galil, B. S., García-Berthou, E., Pascal, M., Pyšek, P., Beja, P., Tabacchi, E., & Vilà, M. (2013). Impacts of biological invasions: what’s what and the way forward. Trends in Ecology and Evolution, 28(1), 58-66. https://doi.org/10.1016/j.tree.2012.07.013
Sistema Global de Información sobre Biodiversidad [GBIF] (2023). GBIF Global Biodiversity Information Facility. GBIF. https://www.gbif.org/
Taborsky, M. (1988). Kiwis and dog predation: observations at Waitangi state forest. Notornis, 35(3), 197-202. https://www.behav.iee.unibe.ch/unibe/portal/fak_naturwis/d_dbio/b_ioekev/abt_be/content/e1010340/e1010392/e1012437/e1044378/e1210996/files1224848/Dog_predation_on_Kiwis_eng.pdf
Tapia, F. U., Herrera-Silveira, J. A., & Aguirre-Macedo, M. L. (2008). Water quality variability and eutrophic trends in karstic tropical coastal lagoons of the Yucatán Peninsula. Estuarine Coastal and Shelf Science, 76(2), 418-430. https://doi.org/10.1016/j.ecss.2007.07.025
Tropicos (2023). Tropicos v3.4.2. Missouri Botanical Garden. https://tropicos.org
The Secretariat of the Convention on Wetlands (2023). The List of Wetlands of International Importance. The Secretariat of the Convention on Wetlands. https://www.ramsar.org/sites/default/files/documents/library/sitelist.pdf
Uetz, P., Freed, P., Aguilar, R., Reyes, F., & Hošek, J. (Eds.). (2023). The Reptile Database. http://www.reptile-database.org
Unión Internacional para la Conservación de la Naturaleza [IUCN] (2000). Guidelines for the prevention of biodiversity loss caused by alien invasive species. IUCNucn. https://portals.iucn.org/library/sites/library/files/documents/Rep-2000-051.pdf
Valiela, I., Bowen, J. L., & York, J. K. (2001). Mangrove Forests: One of the World's Threatened Major Tropical Environments: At least 35% of the area of mangrove forests has been lost in the past two decades, losses that exceed those for tropical rain forests and coral reefs, two other well-known threatened environments, BioScience, 51(10), 807-815. https://doi.org/10.1641/0006-3568(2001)051[0807:MFOOTW]2.0.CO;2
Vásquez-Cruz, V., Reynoso-Martínez, A., Fuentes-Moreno, A., & Canseco-Márquez, L. (2020). The distribution of Cuban brown anoles, Anolis sagrei (Squamata: dactyloidae), in Mexico, with new records and comments on ecological interactions. Reptiles & Amphibians, 27(1), 29-35. https://doi.org/10.17161/randa.v27i1.14442
Villa, J., Valdez, M. M., Novelo, L. M., & Cocom, C. E. (2013). Diagnóstico fitosanitario de Raoiella indica en los estados de Quintana Roo y Yucatán. Comisión Nacional Forestal. http://sivicoff.cnf.gob.mx/ContenidoPublico/10%20Material%20de%20Consulta/Literatura/Especies%20ex%C3%B3ticas%20invasoras/Diagn%C3%B3stico%20Raoiella%20indica%20marzo%202013.pdf
Vitousek, P. M. (1990). Biological Invasions and Ecosystem Processes: Towards an integration of population biology and ecosystem studies. Oikos, 57(1), 7. https://doi.org/10.2307/3565731
Wakida-Kusunoki, A. T., Cruz-Sánchez, J. L., & López-Téllez, N. A. (2021). A review of recent sightings and reports of the giant tiger shrimp Penaeus monodon (Decapoda: Penaeidae) on the Mexican coast of the Gulf of Mexico (2012-2019). Revista de Biología Marina y Oceanografía, 56(1), 83. https://doi.org/10.22370/rbmo.2021.56.1.2802
Wakida-Kusunoki, A. T., De Anda-Fuentes, D., & López-Téllez, N. A. (2016). Presence of giant tiger shrimp Penaeus monodon (Fabricius, 1798) in eastern peninsula of Yucatan Coast, Mexico. Latin American Journal of Aquatic Research, 44(1), 155-158. https://doi.org/10.3856/vol44-issue1-fulltext-16
Wilson, D. E., & Reeder, D. M. (2005). Mammal Species of the World. A Taxonomic and Geographic Reference (3a ed.). Johns Hopkins University Press. https://www.departments.bucknell.edu/biology/resources/msw3/
Wittenberg, R., & Cock, M. J. W. (2001). Invasive Alien Species: A Toolkit of Best Prevention and Management Practices. CAB International. https://www.cbd.int/doc/pa/tools/Invasive%20Alien%20Species%20Toolkit.pdf
WoRMS Editorial Board (2023). World Register of Marine Species. WoRMS Editorial Board. https://www.marinespecies.org
Young, J. K., Olson, K. A., Reading, R. P., Amgalanbaatar, S., & Berger, J. (2011). Is wildlife going to the dogs? Impacts of feral and free-roaming dogs on wildlife populations. BioScience, 61(2), 125-132. https://doi.org/10.1525/bio.2011.61.2.7
Zaldívar, A., Herrera, J., Coronado, C., & Alonso, D. (2004). Estructura y productividad de los manglares en la Reserva de Biosfera Ría Celestún, Yucatán, México. Madera y Bosques, 10(3), 25-35. https://doi.org/10.21829/ myb.2004.1031264
Ziller, S. R., De Sá, M., Duarte, R. A., Marquez, H., Souza, M., Da Silva, L. F., Mello, B. C., & Zenni, R. D. (2020). A priority-setting scheme for the management of invasive non-native species in protected areas. NeoBiota, 62, 591-606. https://doi.org/10.3897/neobiota.62.52633
Notas
Notas de autor
*Autor de correspondencia: occelott@gmail.com
